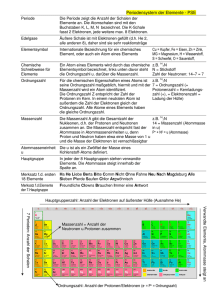
Probeprüfung 5: Periodensystem der Elemente
Werbung

Name: Datum: Unterschrift keine nötig Probeprüfung 5: Periodensystem der Elemente Maximal mögliche Punktzahl: Punktzahl für Note 6: 53 Erwartete 50 Punktzahl: Note: Erreichte Punktzahl: Die Verwendung des Periodensystems ist erlaubt! Aufgabe 1 (Lernziel A): Kreuze alle richtigen Antworten an. Mehrfachauswahl und Leerwahl sind möglich! a) Warum sind Wasserstoff, Lithium, Natrium, Kalium alle untereinander geschrieben? Sie haben gleiche Eigenschaften. Sie haben alle die gleiche Anzahl Elektronen. Sie haben alle die gleiche Anzahl Elektronen in der äussersten Schale. Sie sind alle Metalle. Sie sind alle fest. b) Warum hat Natrium die Ordnungszahl 11 und Magnesium die Ordnungszahl 12? Natrium wurde 1811 entdeckt, Magnesium um 1912. Natrium wiegt 11 g pro cm3, Magnesium 12 g pro cm3. Natrium hat 11 Protonen, Magnesium hat 12 Protonen. Natrium hat 11 Neutronen, Magnesium hat 12 Neutronen. Natrium hat 11 Elektronen, Magnesium hat 12 Elektronen. (____ / 3 + 3 Pkt.) Aufgabe 2 (Lernziel B): Beantworte die Fragen: a) Wie heisst das Element mit der Ordnungszahl 43? _______________ b) Welche Abkürzung hat das Element mit Ordnungszahl 22? _______________ c) Welche Ordnungszahl hat das Element mit Abkürzung Hg? _______________ d) Welche Ordnungszahl hat das Element Silber? _______________ e) Welchen Siedepunkt hat das Element Magnesium? _______________ f) Welchen Schmelzpunkt hat das Element O? _______________ g) Welche Atommasse hat das Element Wolfram? _______________ h) Welches Element hat Atommasse 32,06 u? _______________ i) Welche Dichte hat das Element Aluminium? _______________ j) Welche Dichte hat das Element Chlor? _______________ (____ / 10 Pkt.) Aufgabe 3 (Lernziel C): Nenne die drei Bestandteile der Atome und ihre Ladung: ____________________________________________________________________________ ____________________________________________________________________________ ____________________________________________________________________________ (____ / 6 Pkt.) Aufgabe 4 (Lernziel D+E): Gib für die folgenden beiden Elemente sowohl den Aufbau des Kerns wie auch den Aufbau ihrer Schalen an: a) Sauerstoff (O): b) c) Aluminium (Al): Selen (Se): (____ / 15 Pkt.) Aufgabe 5 (Lernziel F): Ergänze die folgenden chemischen Reaktionen: a) _____ K + _____ I _____ KI b) _____ Na + _____ S _____ Na2S c) _____ Al + _____ Br _____ AlBr3 d) _____ Ca + _____ P _____ Ca3P2 e) _____ Al + _____ C _____ Al4C3 f) _____ C + _____ H2 _____ CH4 g) _____ H2 + _____ F2 _____ HF h) _____ K + _____ O2 _____ K2O i) _____ H2 + _____ N2 _____ NH3 j) _____ S + _____ F2 _____ SF6 k) _____ Fe + _____ O2 _____ Fe3O4 (____ / 11 Pkt.) Aufgabe 6 (Lernziel G): a) Zeichne das vereinfachte Kugelmodell von NH3 (Ammoniak) b) Zeichne das vereinfachte Kugelmodell von C3H6 (Propen). (____ / 2 + 3 Pkt.) Viel Erfolg! Lerntipp: Spiele das Spiel „Wer gewinnt 1000?“ unter: http://www.seilnacht.com/spiele/spiel2/index.html Lösungen zur Probeprüfung N & T (R) – 5 Periodensystem der Elemente: 1) a) b) gleiche Eigenschaften / gleiche Anzahl Elektronen in der äussersten Schale (1. + 3.) 11 Protonen, 12 Protonen / 11 Elektronen, 12 Elektronen (3. und 5.) 2) a) b) c) d) e) f) g) h) i) j) Technetium Ti 80 47 1363 K (1090° C) 50 K (-223° C) 183,85 u Schwefel 2,70 g/cm3 3,17 g/l 3) Elektronen (negativ), Protonen (positiv), Neutronen (keine Ladung / neutral) 4) a) Sauerstoff: (2-6 = 8) b) Aluminium: (2-8-3 = 13) 8 p+ 8n 13 p+ 14 n c) Selen: (2-8-18-6 = 34) 34 p+ 45 n 5) a) c) e) g) i) k) 6) a) K + I KI Al + 3 Br AlBr3 4 Al + 3 C Al4C3 H2 + F2 2 HF 3 H2 + N2 2 NH3 3 Fe + 2 O2 Fe3O4 b) d) f) h) j) b) 2 Na + S Na2S 3 Ca + 2 P Ca3P2 C + 2 H2 CH4 4 K + O2 2 K2O S + 3 F2 SF6 oder: