Vimpat ® 10 mg/ml iv Infusionslösung 1
Werbung
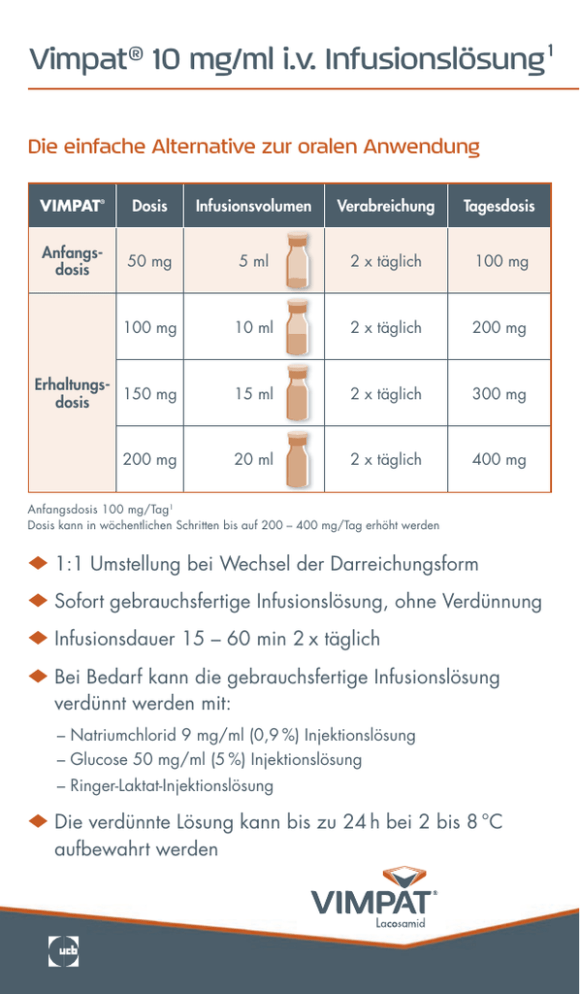
Vimpat ® 10 mg/ml i.v. Infusionslösung 1 Die einfache Alternative zur oralen Anwendung VIMPAT Dosis Infusionsvolumen Verabreichung Tagesdosis Anfangsdosis 50 mg 5 ml 2 x täglich 100 mg 100 mg 10 ml 2 x täglich 200 mg Erhaltungs150 mg dosis 15 ml 2 x täglich 300 mg 200 mg 20 ml 2 x täglich 400 mg ® Anfangsdosis 100 mg/Tag1 Dosis kann in wöchentlichen Schritten bis auf 200 – 400 mg/Tag erhöht werden u 1:1 Umstellung bei Wechsel der Darreichungsform u Sofort gebrauchsfertige Infusionslösung, ohne Verdünnung u Infusionsdauer 15 – 60 min 2 x täglich uB ei Bedarf kann die gebrauchsfertige Infusionslösung verdünnt werden mit: – Natriumchlorid 9 mg/ml (0,9 %) Injektionslösung – Glucose 50 mg/ml (5 %) Injektionslösung – Ringer-Laktat-Injektionslösung uD ie verdünnte Lösung kann bis zu 24 h bei 2 bis 8 °C aufbewahrt werden Immer in Kombination mit zugelassenem Indikationsgebiet! Vimpat ® u Signifikante zusätzliche Anfallskontrolle 2–4 u Direktes Dosieren – kein Verdünnen erforderlich u Bei Raumtemperatur lagerfähig u Gute Verträglichkeit i.v. Applikation wie orale Gabe 5 u Linerare Pharmakokinetik u Keine klinisch relevanten Interaktionen Referenz: 1. Vimpat® Fachinformation, November 2008. 2. Schmidt, D. et al.: Z Epileptol 21 (4), 180-199, 2008. 3. Ben-Menachem, E. et al.: Epilepsia 48 (7), 1308-1317, 2007. 4. Halász, P. et al.: Epilepsia, 50 (3), 443 – 453, 2009. 5. Biton, V. et al.: Epilepsia, 49 (3): 418 – 424, 2008. Vimpat® 10 mg/ml Infusionslösung. Wirkstoff: Lacosamid Zusammensetzung: 1 ml Inf.lsg. enth. 10 mg Lacosamid. Sonst. Bestandteile: 2,99 mg Natrium, Wasser für Injektionszwecke, Natriumchlorid, Salzsäure (zur pH-Wert-Einstellung). Anwendungsgebiete: Zusatzbehandlung fokaler Anfälle mit oder ohne sekundäre Generalisierung bei Epilepsiepatienten ab 16 Jahren. Alternative für Patienten, wenn orale Anwendung vorübergehend nicht möglich. Gegenanzeigen: Überempfindlichkeit gegen Lacosamid oder einen der sonst. Bestandteile. Bekannter AV-Block 2. oder 3. Grades. Nebenwirkungen: Sehr häufig (≥ 1/10): Schwindelgefühl, Kopfschmerzen, Diplopie, Nausea. Häufig (≥ 1/100, < 1/10): Depression, Gleichgewichts-, Koordinations-, Geh-, Gedächtnisstörungen, Kognitive Störungen, Somnolenz, Tremor, Nystagmus, Verschwommenes Sehen, Drehschwindel, Erbrechen, Obstipation, Flatulenz, Pruritus, Asthenie, Müdigkeit, Stürze, Hautwunden. Anwendung von Lacosamid wird mit dosisabhängiger Verlängerung des PR-Intervalls in Verbindung gebracht. Nebenwirkungen möglich, die mit Verlängerung des PR-Intervalls assoziiert sind (z.B. AV-Block, Synkope, Bradykardie). Gelegentlich (≥ 1/1.000, < 1/100): Synkopen, AV-Block 1. Grades; keine Fälle von AV-Block 2. oder höheren Grades beobachtet. Warnhinw.: Auftreten von Schwindelgefühl kann Häufigkeit von unbeabsichtigten Verletzungen und Stürzen erhöhen. Wegen Verlängerung des PR-Intervalls nur mit besonderer Vorsicht bei Patienten mit bekannter Störung der Erregungsleitung, schwerer Herzerkrankung (z. B. Herzinfarkt, -insuffizienz) in der Vorgeschichte. Daher Vorsicht besonders bei älteren Patienten oder Lacosamid in Kombination mit PR-verlängernden Arzneimitteln. Berichte über suizidale Gedanken u. suizidales Verhalten b. mit Antiepileptika behandelten Pat. liegen vor. Pat. sollten hinsichtl. Anzeichen überwacht u. geeignete Behandl. in Erwägung gezogen werden. Schwangerschaft: Strenge ärztl. Nutzen-Risiko-Abwägung. Stillzeit: Nicht empfohlen. Verkehrstüchtigkeit: Geringer bis mäßiger Einfluss auf Verkehrstüchtigkeit/Fähigkeit zum Bedienen von Maschinen möglich. Enthält Natrium, zu berücksichtigen bei Personen unter Na-kontrollierter Diät. Weitere Angaben siehe Fachinfo. Stand der Information: 11/2008. Verschreibungspflichtig. UCB Pharma SA, Allée de la Recherche 60, B-1070 Bruxelles, Belgien Immer in Kombination mit zugelassenem Indikationsgebiet!