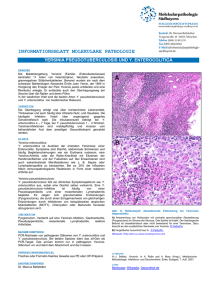
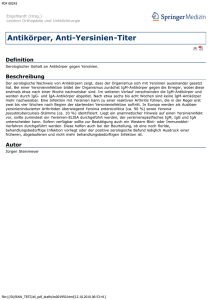
Biochemische und strukturelle Charakterisierung von YopM
Werbung

Biochemische und strukturelle Charakterisierung von YopM aus Yersinia enterocolitica WA-314 und dessen WirtsZielstrukturen Dissertation Zur Erlangung der Würde des Doktors der Naturwissenschaften des Fachbereichs Biologie, der Fakultät für Mathematik, Informatik und Naturwissenschaften, der Universität Hamburg vorgelegt von Dipl.-Biol. Andreas Rumm aus Speyer Hamburg, 2014 Die vorliegende Arbeit wurde von November 2009 bis Mai 2014 unter Anleitung von Prof. Dr. Martin Aepfelbacher am Institut für Medizinische Mikrobiologie, Virologie und Hygiene am Universitätsklinikum Hamburg-Eppendorf durchgeführt. Dissertation zur Erlangung des Doktorgrades im Fachbereich Biologie der Universität Hamburg vorgelegt von Diplom-Biologe Andreas Rumm aus Speyer Dissertationsgutachter: Prof. Dr. Martin Aepfelbacher Prof. Dr. Wolfgang Streit Tag der Disputation: 08. August 2014 I Inhaltsverzeichnis I Inhaltsverzeichnis I Inhaltsverzeichnis ................................................................................................... 3 II Einleitung................................................................................................................ 5 II.1 Die Gattung Yersinia..................................................................................... 5 II.2 Yersinia enterocolitica................................................................................... 6 II.2.1 Klassifizierung .................................................................................... 6 II.2.2 Pathogenese und Infektionsroute ...................................................... 7 II.3 Virulenzfaktoren ............................................................................................ 7 II.3.1 Chromosomal vermittelte Virulenz ..................................................... 7 II.3.2 Das Virulenzplasmid .......................................................................... 9 II.5 LRR-Proteine .............................................................................................. 16 II.5.1 YopM in der Familie der LRR-Proteine ............................................ 18 II.6 DDX3 .......................................................................................................... 19 II.6 Zielsetzung ................................................................................................. 22 III Material und Methoden ....................................................................................... 23 III.1 Material ...................................................................................................... 23 III.1.1 Geräte ............................................................................................. 23 III.1.2 Verbrauchsmittel ............................................................................. 24 III.1.3 Kits, Enzyme und Reagenzien ........................................................ 25 III.1.4 Puffer und Lösungen ....................................................................... 26 III.1.5 Protein und DNA Leitern ................................................................. 31 III.1.6 Bakterienstämme ............................................................................ 32 III.1.7 Plasmide ......................................................................................... 32 III.1.8 Oligonukleotide ............................................................................... 35 III.1.9 Elektronische Datenverarbeitung .................................................... 38 III.2 Methoden ................................................................................................... 39 III.2.1 Mikrobiologische Methoden ............................................................ 39 III.2.2 Molekularbiologische Methoden ...................................................... 40 III.2.3 Biochemische Methoden ................................................................. 44 III.2.4 Methoden zur Strukturaufklärung von Proteinen ............................. 51 3 I Inhaltsverzeichnis IV Ergebnisse .......................................................................................................... 54 IV.1 Strukturaufklärung von YopM .................................................................... 54 IV.1.1 Klonierung, Expression und Aufreinigung von YopM aus Y. enterocolitica WA-314........................................................................... 54 IV.1.2 Überprüfung des Translationsstarts von YopM aus Y. enterocolitica WA-314........................................................................... 56 IV.1.3 Analytische Größenbestimmung und Dispersitätskontrolle von YopM .................................................................................................................. 58 IV.1.4 Strukturanalyse von YopM .............................................................. 59 IV.2 Überprüfung des inhibitorischen Effekts von YopM auf Caspase-1 ......... 70 IV.3 Interaktion von YopM mit der DEAD-Box-Helikase DDX3 ......................... 72 IV.3.1 GST-Pulldown ................................................................................ 72 IV.3.2 Heterologe Expression und Aufreinigung von DDX3 ...................... 73 IV.3.3 Struktur von DDX3_51-418 in Lösung ............................................ 75 IV.3.4 Bestimmung der Bindungsaffinität von YopM und DDX3 ................ 77 IV.3.5 Darstellung des Komplexes aus YopM und DDX3 mittels Größenausschlusschromatographie ......................................................... 80 IV.4 Strukturanalyse des Komplexes aus YopM und DDX3 ............................. 84 IV.4.1 Kristallisation von YopM/DDX3 ....................................................... 84 IV.4.2 Struktur des Komplexes aus YopM und DDX3 in Lösung ............... 86 V Diskussion ........................................................................................................... 91 V.1 Struktur von YopM aus Y. enterocolitica WA-314 ............................... 91 V.2 YopM und Caspase-1 ......................................................................... 98 V.3 YopM und DDX3 ................................................................................. 99 VI Zusammenfassung ........................................................................................... 104 VIa Summary ......................................................................................................... 105 VII Literaturverzeichnis......................................................................................... 106 VIII Tabellenverzeichnis........................................................................................ 126 IX Abbildungsverzeichnis .................................................................................... 127 X Abkürzungsverzeichnis .................................................................................... 129 XI Danksagung ...................................................................................................... 132 XII Vorveröffentlichungen .................................................................................... 134 XIII Eidesstattliche Versicherung......................................................................... 135 4 II Einleitung II Einleitung Der menschliche Darm ist von einer Vielzahl an Bakterien besiedelt, die einen unterstützenden Einfluss auf die Verdauung oder das Immunsystem des Menschen haben können. Neben diesen Kommensalen gibt es jedoch auch eine Reihe potenziell pathogener Erreger, die in den Darm gelangen. Das Darmepithel bildet hier eine wirksame Barriere, um den Körper vor Infektionen durch Mikroorganismen zu schützen. Neben dem physikalischen Schutz ist dieses Gewebe mit einer Vielzahl von Zellen des angeborenen sowie des adaptiven Immunsystems besiedelt, die effektiv die Invasion durch Pathogene verhindern (Turner 2009). Diese Barriere ist jedoch nicht absolut und so haben einige Erreger Wege gefunden, die Mechanismen der Immunabwehr auszuhebeln und sich ihre Nische im menschlichen Körper zu suchen. Das Eindringen dieser Mikroorganismen in den Körper kann zu lebensbedrohlichen Infektionen führen. II.1 Die Gattung Yersinia Yersinien sind gram-negative, stäbchenförmige Bakterien aus der Familie der Enterobacteriaceae. Sie wachsen fakultativ anaerob, sind Katalase-positiv, Zytochromoxidase-negativ und bilden keine Sporen. Benannt ist die Gattung seit 1964 nach Alexandre J. Yersin, dem es während der Hong Kong-Epidemie 1894, zeitgleich mit Shibasaburo Kitasato, erstmals gelang Yersinia pestis aus menschlichem Gewebe zu isolieren und zu beschreiben (Drancourt & Raoult 2002; Treille & Yersin 1894). Unter den 11 bisher beschriebenen Arten sind lediglich drei humanpathogen: Yersinia enterocolitica, Yersinia pseudotuberculosis und Yersinia pestis. Die Krankheiten, die diese Erreger verursachen, reichen von einer harmlosen, selbstlimitierenden Gastroenteritis bis zur Pest, die unbehandelt in 70-90 % der Fälle tödlich ist. Y. pestis ist in der Lage bei Temperaturen von 4 bis 40°C zu wachsen, wobei das Temperaturoptimum bei 28 bis 30°C liegt. Das Bakterium hat einen komplexen Lebenszyklus: Der indische Rattenfloh (Xenopsylla cheopis), in dessen Magen sich die Bakterien vermehren, überträgt diese als natürlicher Vektor auf den Menschen. Nach dem Biss des Flohs wandern die Erreger von der subkutanen Eintrittsstelle in angrenzendes Lymphgewebe, wo sich nach 1-7 Tagen Inkubationszeit sogenannte Bubonen bilden. Von dort aus kann sich das Bakterium über die Blutbahn weiter ausbreiten und Organe wie Leber, Nieren oder die Lunge befallen (Perry & Fetherston 1997). Im Wesentlichen greift das Pathogen für diese parasitäre Lebensweise auf Faktoren zurück die auf drei Virulenzplasmiden liegen (Wren 2003). pYV, welches für ein Typ III-Sekretionssystem und eine Reihe von Effektorproteinen codiert, die die Wirts-Immunabwehr unterdrücken, kommt in allen drei humanpathogenen Spezies vor. Im Gegensatz dazu sind zwei weitere Plasmide ausschließlich in Y. pestis zu finden. Das Plasmid pPla codiert unter anderem für einen Plasminogen-Aktivator und eine Coagulase, welche für die subkutane Verbreitung innerhalb des Säugetier-Wirts notwendig sind (Sodeinde et al. 1988). pMT1 wiederum ermöglicht durch das sogenannte „murine Toxin“ und das „F1-capsule-like antigen“ das Überleben im Flohvektor (Hinnebusch et al. 1998; Hinnebusch et al. 2002). Durch die Aneignung und den Verlust dieser und anderer genetischer Faktoren hat sich Y. pestis vor 1500-20000 Jahren aus Y. pseudotuberculosis zu einem obligat parasitären Organismus entwickelt (Achtman et al. 1999). 5 II Einleitung Y. pseudotuberculosis, das eine Homologie in der chromosomalen DNA von bis zu 97 % im Vergleich mit Y. pestis besitzt, zeigt ein deutlich weniger dramatisches klinisches Bild. So befällt dieser Erreger, der natürlicherweise in der Umwelt vorkommt, überwiegend Tiere (Chain et al. 2004). Die Übertragung auf den Menschen findet ausschließlich durch den Verzehr kontaminierter Lebensmittel oder Wasser statt. Nach Aufnahme der Bakterien, gelangen diese in den Dünndarm, wo sie in der Lage sind über sogenannte M-Zellen in den Peyerschen Plaques durch das Darmepithel in anliegendes Lymphgewebe zu translozieren (Sansonetti 2004; Lian et al. 1987). Dort kommt es durch Entzündungserscheinungen zu den typischen Symptomen der Gastroenteritis, welche sich bis zu einer mesenteren Lymphadenitis entwickeln kann. Trotz der genetisch nicht so nahen Verwandtschaft, zeigt Y. enterocolitica, der dritte humanpathogene Erreger der Gattung, deutlich mehr Parallelen in Lebenszyklus und Pathogenität zu Y. pseudotuberculosis als Y. pestis (Perry & Fetherston 1997). So stellt Y. enterocolitica den zweiten Erreger der humanen Yersiniose dar (Vantrappen et al. 1977). Er wird ebenso über kontaminiertes Fleisch sowie über Milchprodukte übertragen (Black et al. 1978). Nach Salmonella und Campylobacter ist Y. enterocolitica der dritthäufigste bakterielle Durchfallerreger in Deutschland. Allen drei humanpathogenen Yersinia-Spezies ist ihre Vorliebe für lymphatisches Gewebe gemein. Durch ihre invasive Lebensweise bedingt sich eine gewisse Resistenz gegen die körpereigene Immunabwehr. Dies gilt im Besonderen der Verhinderung der Phagozytose durch Makrophagen und des Angriffs durch Leukozyten. Hierzu haben alle drei Pathogene, teilweise unabhängig voneinander, eine Reihe chromosomaler oder plasmidär lokalisierter Virulenzfaktoren erworben, die ihnen das Überleben im Organismus des Wirts ermöglichen (Bleves & Cornelis 2000; Reuter et al. 2014). In den von ihnen ausgelösten Krankheitsbildern unterscheiden sich die drei Spezies jedoch, wie dargestellt, enorm. II.2 Yersinia enterocolitica Erste Anzeichen auf Yersinia enterocolitica in der Literatur finden sich 1934 durch McIver und Pike. Fünf Jahre später greifen Schleiffstein und Coleman die Entdeckung des Erregers auf und geben ihm den Namen Bacterium enterocoliticum (Bottone 1997). Erst 1964 wurde die Art durch Frederiksen der neuen Gattung Yersinia zugeordnet (Frederiksen 1964). Die Spezies ist weit verbreitet und findet sich meist in aquatischen und tierischen Reservoiren, wobei das Schwein das Hauptreservoir für humane Infektionen darstellt. Interessanterweise sind die meisten Isolate, die nicht aus dem Hausschwein stammen apathogen (Bottone 1997). II.2.1 Klassifizierung Y. enterocolitica lässt sich auf Grundlage biochemischer Eigenschaften in 6 verschiedene Biovare (1B, 1A, 2, 3, 4, 5) (Wauters et al. 1987) und durch Charakterisierung der O (Lipopolysacharid)- und H (Geißel)-Antigene in über 60 Serovare einteilen. Unter den Serotypen sind geographische Besonderheiten zu verzeichnen. So stellen O:4, O:8, O:13, O:18, O:20 und O:21, die alle zu dem hoch pathogenen Biovar 1B gehören, die Hauptvertreter in den USA dar (Aleksic & Bockemühl 1990), während in Europa eher die Stämme O:3, O:5,27 und O:9 verbreitet sind (Kwaga et al. 1992). Diese gehören den weniger pathogenen Stämmen 2-5 an. Biovar 1A ist apathogen. Neben der klassischen biochemischen Charakterisierung findet heute vermehrt die Typisierung über Massenspektrometrie statt (Stephan et al. 2011). 6 II Einleitung II.2.2 Pathogenese und Infektionsroute Analog zu Y. pseudotuberculosis gelangt der Mikroorganismus hauptsächlich durch kontaminiertes Wasser oder durch den Genuss von befallenem Fleisch in den Gastrointestinaltrakt (Aleksic & Bockemühl 1990), wodurch es zu akuter Enteritis, Enterocolitis, mesenterischer Lymphadenitis oder terminaler Ileitis kommen kann (Bottone 1997). Angelangt im humanen Wirt, muss zunächst eine Anpassung der Oberflächenantigene an die erhöhte Temperatur von 37°C stattfinden. Ein Teil dieser neu exprimierten Antigene ist auf dem 64 bis 75 kb großen Virulenzplasmid pYV kodiert. Dieses Plasmid fehlt apathogenen Stämmen (Portnoy et al. 1981). Es kodiert darüber hinaus für eine Reihe weiterer Proteine, die dem Pathogen helfen zu invadieren und sich in seiner ökologischen Nische im Extrazellularraum zu etablieren (Portnoy & Falkow 1981). Weitere wichtige Faktoren in dieser Phase der Infektion sind chromosomal auf dem sogenannten „Attachment invasion locus“ Ail kodiert (Miller & Falkow 1988). Im terminalen Ileum durchqueren die Bakterien das Darmepithel durch sogenannte M-Zellen und besiedeln schließlich das darmassoziierte lymphatische Gewebe der Peyerschen Plaques. Hierbei spielt das Membranprotein Invasin eine große Rolle, indem es Kontakt mit zellulären β1-Integrinen vermittelt und nachgeschaltete Signalwege induziert, die die Internalisierung der Bakterien zur Folge haben (Grassl et al. 2003). Nach der Translokation in die Peyerschen Plaques proliferiert das Bakterium im Extrazellularraum und kann sich über abfließende lymphatische Gefäße bis in die mesenteralen Lymphknoten ausbreiten (Trülzsch et al. 2007). Um innerhalb des Wirts zu überleben und der angeborenen Immunabwehr zu entgehen, bedient sich Y. enterocolitica einer Reihe von Virulenzfaktoren. Ein sehr großer Teil dieser Faktoren liegt auf dem Virulenzplasmid pYV. Ebenso gibt es aber auch eine sehr große Anzahl chromosomal vermittelter Virulenzdeterminanten, ohne die die invasive Lebensweise des Pathogens nicht möglich wäre. II.3 Virulenzfaktoren II.3.1 Chromosomal vermittelte Virulenz Im Gegensatz zu dem obligat parasitären Y. pestis kommt Y. enterocolitica als Umweltkeim im Boden oder aquatischen Reservoiren vor und kann feuchte, natürliche Biotope sowie Lebensmittel besiedeln. Hierfür ist ein hochadaptives Repertoir an Stoffwechseleigenschaften von Nöten, wobei die Umgebungstemperatur eine wichtige Rolle bei deren Genexpression spielt. So werden zum Beispiel Flagellen, die für die Motilität außerhalb des Wirts von Bedeutung sind und das bakterielle Adhärenzprotein Invasin (Inv) bei gemäßigten Temperaturen sehr stark exprimiert, bei 37°C jedoch kaum. (Straley & Perry 1995) Yersinia spp. besitzen ein ca. 4,6 mb großes zirkuläres Genom mit einem durchschnittlichen GC-Gehalt von 47 %. Neben den üblichen Haushaltsgenen, kam es durch horizontalen Gentransfer zum Eintrag einer Reihe von Virulenzfaktoren, die zusammen mit plasmidär kodierten Determinanten, eine optimale Anpassung an den Wirt darstellen. Diese Regionen zeigen üblicherweise einen für die Spezies atypischen GC-Gehalt und sind als sogenannte GC-Spitzen im Genom gut erkennbar. 7 II Einleitung Abbildung 1: Genomvergleich von Y. enterocolitica WA-314 und 8081 (Garzetti et al. 2012). Zirkuläre Darstellung des Genomvergleichs zwischen den Y. enterocolitica Stämmen WA-314 und 8081. GCGehalt des Stammes 8081 sowie die Position der wichtigsten Virulenzgene sind angezeigt. Einer dieser Regionen ist die „High Pathogenicity Island“ (HPI). Dieser ca. 40 kb große Bereich kodiert für ein Eisenaufnahmesystem und kommt in allen drei humanpathogenen Spezies vor. Das System ermöglicht die Biosynthese und den Transport des Yersiniabactins (Ybt). Dieses Siderophor komplexiert Eisenionen in der Wirtszelle und wird über das Membranprotein FyuA („ferric yersiniabactin uptake“) von den Yersinien wieder aufgenommen. Die HPI ist für eine systemische Infektion essentiell und daher meist bei hochpathogenen Stämmen zu finden (Heesemann et al. 1993; Carniel et al. 1996; Brem et al. 2001). Ein weiterer wichtiger chromosomaler Virulenzfaktor ist das 17 kDa Membranprotein AIL („Attachment Invasion Locus“), welches eine Rolle bei der Anheftung der Bakterien an Epithelzellen spielt und die daraus resultierende Translokation in angrenzendes Gewebe vermittelt. Im Gegensatz zu Invasin, welches bei Temperaturen über 30°C nur sehr gering exprimiert wird, kommt AIL sowohl in der logarithmischen Wachstumsphase bei 30°C als auch in der stationären Phase bei 37°C vor (Pierson & Falkow 1993). Entdeckt wurde das Oberflächenantigen in einem E.coli-Screen auf genetisch übertragbare, invasionsvermittelnde Faktoren. E.coli-Stämme, die das ail-Gen trugen, waren in der Lage an CHO-und Hep-2 Zellen zu adhärieren und in diese einzudringen (Miller & Falkow 1988). Bei Untersuchungen zur Infektion im Maus-Modell spielte AIL, im Vergleich zu Invasin und dem weiter unten beschriebenen YadA, jedoch eine untergeordnete Rolle (Pepe et al. 1995). 8 II Einleitung Der wichtigste Internalisierungsfaktor der enteropathogenen Yersinia-Arten ist Invasin. Entdeckt wurde das 103 kDa Oberflächenprotein, welches strukturelle Homologien zur Familie der Intimine aufweist, zuerst in Y. pseudotuberculosis (Isberg et al. 1987) und später in Y. enterocolitica (Pepe & Miller 1990). Hier beträgt das Molekulargewicht nur 92 kDa, was an der Abwesenheit der Domäne D2 liegt (Grassl et al. 2003). Das Protein aus Y. pseudotuberculosis vermittelt eine hochaffine Bindung an β1-Integrine der M-Zellen, wodurch nachgeschaltet eine Reihe von Prozessen stattfindet, die zur Internalisierung der Bakterien führt (Pepe & Miller 1993a; Pepe & Miller 1993b; Wiedemann et al. 2001). Für die Bindung relevant sind hierbei die letzten 192 C-terminalen Aminosäuren (Leong et al. 1990). In diesem konservierten Bereich ist das Y. enterocolitica Invasin, welches lediglich eine molekulare Masse von 92 kDa besitzt, zu 79 % homolog. Die bevorzugte Expression bei niedrigeren Temperaturen (23°C) belegt die Rolle des Invasins als wichtiger Virulenzfaktor der frühen Phase der Infektion (Isberg & Leong 1988). Neben den beschriebenen und vielen weiteren chromosomal vermittelten Virulenzfaktoren, beherbergen alle pathogenen Yersinia-Arten ein ca. 70 kb großes Virulenzplasmid. Dieses, meist pYV genannt, kodiert unter anderem für ein Typ III-Sekretionssystem und eine Reihe von Effektorproteinen (Cornelis et al. 1998). II.3.2 Das Virulenzplasmid In den 1950er Jahren war bekannt, dass Y. pestis nicht in der Lage ist in Ca2+-defizientem Medium bei 37°C zu wachsen. Ebenso wusste man, dass dieser Phänotyp verloren gehen konnte und mit diesem Verlust eine Verringerung der Virulenz einherging (Cornelis et al. 1998). Wesentlich später entdeckte man, dass dieses als „low calcium response“ (lcr) benannte Phänomen durch ein ca. 70 kb großes Plasmid hervorgerufen wurde (Gemski et al. 1980; Zink et al. 1980), welches heute unter dem Namen pYV bekannt ist. Die Virulenzplasmide verschiedener Yersinia-Spezies sind sich alle äußerst ähnlich, doch sind im Laufe der Evolution verschiedene Insertionen durch transposable Elemente und Phagen aufgetreten. Der augenscheinlichste Unterschied zwischen den Plasmiden von Y. enterocolitica und Y. pseudotuberculosis ist jedoch eine Inversion, die nahezu das halbe Plasmid betrifft (Biot & Cornelis 1988). Neben einem weiteren wichtigen Oberflächenprotein, dem „Yersinia Adhesin A“ (YadA) und zahlreichen anderen Faktoren, kodiert das Plasmid für ein Typ III-Sekretionssystem (TTSS) und die dadurch in die Wirtszelle translozierten Effektorproteine, die „Yersinia outer proteins“ (Yops). Die genetische Organisation des Virulenzplasmids pYVWA-314 aus Y. enterocolitica WA-314 ist in Abbildung 2 dargestellt. 9 II Einleitung pYV-WA-314 66.845bp Abbildung 2: Karte des Y. enterocolitica WA-314 Virulenzplasmids (Oberhettinger et al. 2011). Dargestellt ist die genetische Organisation des 66.9 kb Virulenzplasmids pYVWA-314. Gene sind in blau gezeigt, der Replikationsursprung in gelb. ysc: Gene des Typ III-Sekretionssystems, yop: Gene der Yops. II.3.2.1 Typ III-Sekretionssystem (TTSS) Seit 1991 ist bekannt, dass der Yop-Sekretionsapparat ebenso wie die Effektoren auf dem Virulenzplasmid pYV kodiert ist (Michiels & Cornelis 1991). Die ysc-Gene kodieren für ein sogenanntes Typ III-Sekretionssystem, das in der Lage ist, Effektorproteine über drei Membranen zu translozieren. Dieser Multiproteinkomplex , der über ein Megadalton groß ist, ähnelt dabei einer molekularen Spritze und ist bei gram-negativen Pathogenen weit verbreitet (Gerlach & Hensel 2007). Strukturell und evolutionär ist der Apparat nahe verwandt mit bakteriellen Flagellen. Das Sekretionssystem in Yersinia ist aus mehr als 20 Proteinen aufgebaut, die durch die ysc („yersinia secretion proteins“)-Gene kodiert werden. YscC formt hierbei einen Ring in der äußeren (Koster et al. 1997), YscD und YscJ in der inneren Bakterienmembran (Yip et al. 2005). Diese Ringe bilden das Gerüst für die Nadel und den Basalkörper. Der Basalkörper, der die innere und äußere Bakterienmembran durchspannt, wird von den Proteinen YscD, YscR, YscS, YscT, YscU und YscV gebildet (Dewoody et al. 2013). Er enthält darüber hinaus eine ATPase (YscNKL), die strukturelle Ähnlichkeit zur Flagellen-Protonenpumpe FoF1 besitzt (Woestyn et al. 1994) und einem C-Ring (YscQ). Dem Basalkörper schließt sich die von nur einem Protein, YscF, gebildete, sogenannte Nadel an. Dieses Homomultimer kann in Y. enterocolitica eine Länge von bis zu 600 Å (60 nm) annehmen und bildet die Brücke zur 10 II Einleitung eukaryontischen Wirtszelle. Abgeschlossen wird der Apparat durch den aus YopBD und LcrV gebildeten Porenkomplex (Neyt & Cornelis 1999; Montagner et al. 2011). A B Porenkomplex Nadel Basalkörper Abbildung 3: Aufbau des Typ III-Sekretionssystems. A: Schematische Darstellung des Translokationsapparates in Y. enterocolitica (Dewoody et al. 2013). B: STEMAufnahme von LcrV (Mueller et al. 2005) und EM-Aufnahme des Translokationsapparates aus Shigella flexneri (Blocker et al. 2001). Mit diesem Apparat ist es den Yersinien möglich sechs Effektorproteine in die Wirtszelle einzuschleusen, die dort auf unterschiedliche Art die Phagozytose verhindern, eine Reorganisation des Zytoskeletts bewirken oder die Ausschüttung proinflammatorischer Zytokine verhindern. Dadurch wird das Persistieren der Bakterien im Interzellularraum ermöglicht (Cornelis & Wolf-Watz 1997). Die Proteine, die durch das TTSS in die Wirtszelle injiziert werden besitzen keine klassischen Signal-Sequenzen (Michiels et al. 1990) und so ist die Erkennung der Translokatoren durch den Injektionsapparat nicht vollends verstanden. Ebenso herrscht Unklarheit über den exakten Mechanismus der Translokation. Hierfür gibt es mehrere Modelle, bei denen die aus YopBD gebildete Pore entweder im Komplex mit den translozierten Effektoren von der Nadel wegdiffundiert oder als fester Bestandteil des Apparates an der Nadel verbleibt und lediglich als Öffnung der eukaryontischen Zellmembran fungiert (Dewoody et al. 2013). Die in vivo-Translokation der Effektoren erfolgt normalerweise nach Kontakt mit der Wirtszelle durch die Yersinia-Adhäsine (Rosqvist et al. 1994). In vitro jedoch kann durch Depletion von Ca2+ die Sekretion der Yops künstlich induziert werden (Heesemann et al. 1986). Bei einer Inkubation der Yersinien bei 37 °C in einem Ca2+-defizienten Medium kommt es zum Stillstand des bakteriellen Wachstums und die Sekretion der Effektoren in den Kulturüberstand erfolgt (Carter et al. 1980). Die sechs von Y. enterocolitica translozierten, immunmodulierenden Effektoren sind: YopT, YopE, YopO, YopH, YopP und YopM. Diese sollen im Folgenden näher beschrieben werden. 11 II Einleitung II.3.2.2 YopT: Eine Cystein-Transferase YopT aus Y. enterocolitica ist ein ca. 35 kDA großes Protein, welches zur Gruppe der CACysteinproteasen gehört. Es bindet bevorzugt die Rho-GTPasen RhoA, Rac1 und CDC42 (Shao et al. 2002). Dabei spaltet es den C-terminalen Geranylgeranyl-Cystein-Rest, der den GTPasen als Membrananker dient und bewirkt somit deren Translokation ins Zytosol (Shao et al. 2003). Dies führt zur Inaktivierung und Akkumulierung der Proteine im Zytoplasma (Zumbihl et al. 1999; Aepfelbacher et al. 2003). Über die Modifikation der Rho-GTPasen inhibiert YopT schlussendlich die Phagozytose von Yersinien durch Makrophagen und Neutrophile (Grosdent et al. 2002). Darüber hinaus wird die Reorganisation des AktinZytoskeletts an den sogenannten „phagocytic cups“ und an podosomalen Adhäsionsstrukturen durch YopT-exprimierende Yersinien inhibiert. Dies führt zu einer Störung der Chemotaxis der Makrophagen und erschwert somit das Auffinden der Pathogene (Aepfelbacher 2004). In dem Effekt auf Rho-GTPasen überschneidet sich die Funktion YopTs teilweise mit der von YopE. Somit kooperieren die beiden Proteine in der Modulation des Aktin-Zytoskeletts und der damit verbundenen Verhinderung der Phagozytose (Aepfelbacher et al. 2007). II.3.2.3 YopE: Ein GTPase aktivierendes Protein (GAP) YopE ist ein ca. 25 kDA großes GAP-Protein für Rho-GTP bindende Proteine (Black & Bliska 2000; Von Pawel-Rammingen et al. 2000; Andor et al. 2001). Obwohl YopE keine Sequenzhomologie zu eukaryontischen GAPs zeigt, ist es doch strukturell diesen sehr ähnlich (Scheffzek et al. 1998; Evdokimov et al. 2002). YopE inaktiviert die gebundenen GTPasen, indem es die Hydrolyse von GTP zu GDP katalysiert. Da Rho-GTPasen eine Rolle in der Organisation des Aktinzytoskeletts spielen, bewirkt deren Inaktivierung durch YopE eine Umstrukturierung der Aktinmikrofilamente. Dies unterstützt die Phagozytoseresistenz der Yersinien (Aepfelbacher & Heesemann 2001). Eine in vitro-GAP-Aktivität konnte für Rho, Rac und cdc42 gezeigt werden (Von Pawel-Rammingen et al. 2000; Black & Bliska 2000). Neben den Effekten auf die Aktinremodellierung, inhibiert YopE die Caspase-1 vermittelte Reifung und Sekretion von Interleukin-1β und somit die Rekrutierung von Immunzellen (Schotte et al. 2004). Somit ist YopE ein wichtiger Bestandteil der Pathogenität der Yersinien, indem es einerseits die Immunabwehr und andererseits die Phagozytose hemmt. II.3.2.4 YopO: Eine Serin-/Threoninkinase YopO (YpKA in Y. pseudotuberculosis) ist ein ca. 80 kDa großes Multidomänenprotein, welches eine N-terminale Serin/Threoninkinasedomäne besitzt (Galyov et al. 1993). Darüber hinaus ist der N-Terminus für die Sekretion durch das TTSS unabdingbar und zeigt eine Membranbindedomäne (Håkansson et al. 1996; Dukuzumuremyi et al. 2000). Die C-terminale Hälfte des Proteins besteht aus einer Rho-GTPase-Bindedomäne und die letzten 21 Aminosäuren interagieren mit Aktin (Dukuzumuremyi et al. 2000; Juris et al. 2000). HeLaZellen die mit einem YpKA überexprimierendem Stamm von Y. pseudotuberculosis infiziert wurden, zeigten Abrundung, Ausbildung von Retraktionsfasern sowie Ablösungen des AktinZytoskeletts. Die Abrundung der Zellen lässt sich auf die Kinaseaktivität, die Ablösung des Zytoskeletts auf die GDI-Domäne zurückführen (Prehna et al. 2006; Trasak et al. 2007). Die Kinase-Domäne inhibiert darüber hinaus Gαq-Signalwege. Gαq gehört zur Familie der GProteine die Phospholipase-C-β stimulieren (Navarro et al. 2007). Diese Interaktion könnte zu 12 II Einleitung dem „abnormalen Bluten“ von Pest-Patienten beitragen, da Gαq-Knockout-Mäuse zu erhöhter Blutungsdauer und Defizienz in der Thrombozytenaktivierung neigen (Laskowski-Arce & Orth 2007). II.3.2.5 YopH: Eine Tyrosin-Phosphatase YopH ist ein 50 kDa großes Protein mit einer Tyrosin-Phosphatase-Domäne, die C-terminal lokalisiert ist (Juris et al. 2002). YopH ist eine der potentesten bisher bekannten Tyrosinphosphatasen und es wird spekuliert, dass das yopH-Gen ursprünglich durch horizontalen Gentransfer aus eukaryonten Wirtszellen aufgenommen wurde (Guan & Dixon 1990). Unterstützt wird diese These durch die hohe strukturelle Ähnlichkeit des Enzyms zu eukaryontischen Pendants (Phan et al. 2003; Sun et al. 2003). Das Protein dephosphoryliert hauptsächlich Proteine des fokalen Adhäsionskomplexes, wie p130Cas, „focal adhesion kinase“ (Fak), Paxillin, „Fyn-binding protein“ (FyB) und das Gerüstprotein SKAP-HOM (Viboud & Bliska 2005; Cornelis 2002). Die Inaktivierung von p130Cas durch YopH-vermittelte Dephosphorylierung, führt zum Abriss von Aktinstrukturen inklusive der fokalen Adhäsionen und damit zu einer Inhibition der Phagozytose (Andersson et al. 1996). Neben den antiphagozytischen Effekten hemmt YopH die „Chemoattractant-protein-1“ Produktion in Makrophagen (Sauvonnet, Lambermont, et al. 2002) und die T-Zell-Aktivierung (Yao et al. 1999). II.3.2.6 YopP: Eine Acetyltransferase Das 33 kDa große Protein YopP (YopJ in Y. pestis und Y. pseudotuberculosis) interagiert mit dem NFκB (nuclear factor κ B) aktivierenden IKK-Komplex und mehreren Kinasen der MAPKKinase-Familie (MKK), den Aktivatoren der MAPK (mitogen activated protein kinase). Daraus resultiert eine Unterdrückung der Zytokinproduktion in Makrophagen (TNFa), Epithel- (IL-8) und Endothelzellen (IL-6, IL-8) (Mills et al. 1997; Monack et al. 1997; Ruckdeschel et al. 1997; Palmer et al. 1998; Schesser et al. 1998; Orth et al. 1999; Denecker et al. 2002). Lange Zeit wurde angenommen, dass YopP/J aufgrund seiner vorhergesagten strukturellen Homologie zu AVP und „ULP-1 like proteins“, die eine katalytische Triade besitzen, eine Cysteinprotease sei (Orth et al. 2000). Dies deckte sich mit frühen Beobachtungen in YopJ Überexpressionsstudien, dass das Vorhandensein von aktivem YopJ mit erhöhter DeUbiquitinierung und De-SUMOylierung einherging (Orth et al. 2000; Orth 2002; Viboud & Bliska 2005). Sechs Jahre nach der Entdeckung des potenziellen aktiven Zentrums von YopJ konnte dies jedoch, unabhängig voneinander, durch zwei Arbeitsgruppen widerlegt werden. Sie konnten zeigen, dass YopJ als Acetyltransferase fungiert. Sie acetyliert wichtige Serinund Threoninreste in den Aktivierungsloops von Signalkinasen (MKKs und IKKs) und verhindert damit deren aktivierende Phosphorylierung (Mittal et al. 2006; Mukherjee et al. 2006). Diese Ergebnisse konnten später glaubhaft belegt werden (Trosky et al. 2008). 13 II Einleitung II.3.2.7 YopM: Ein Gerüstprotein YopM ist ein ca. 50 kDa großes Protein und einer der wichtigsten Virulenzfaktoren von Yersinia spp. im Maus-Modell (Leung et al. 1990; Kerschen et al. 2004). Während die anderen Yops in Größe und Sequenz hochkonserviert sind (Sequenzhomologien von bis zu 97 %), ist bereits seit längerem bekannt, dass YopM durch alle drei Spezies in verschiedenen Isoformen vorliegt (Boland et al. 1998). Dies fiel auf als Boland und Kollegen das SDS-PAGE-Profil der sekretierten Yops eines neuen Y. enterocolitica O:8-Stammes (A127/90) überprüften. Im Vergleich zu ihrem Referenzstamm (E40) fehlte die 41 kDa YopM-Bande, während eine zusätzliche Bande bei 55 kDa auftauchte. Diese Bande zeigte positive Reaktion auf ein polyklonales anti-YopM Serum. Die unterschiedlichen Größen der Proteine verschiedener Yersinia-Stämme lassen sich durch YopMs strukturellen Aufbau erklären. Bereits bei seiner ersten Charakterisierung 1989 war durch Sequenzvergleiche aufgefallen, dass es sich um ein höchst repetitives Protein handelt, das aus einer definierten Anzahl an Leucin-reichen Wiederholungen besteht. Zusätzlich zeigten sich Ähnlichkeiten zu dem „human platelet surface protein“ GPIb (Leung & Straley 1989). Der Unterschied in der Größe der später von Boland und Kollegen untersuchten YopMIsoformen lag eben in diesem repetitiven Bereich, während die N- und C-Termini identisch waren (Boland et al. 1998). Die erwähnte Ähnlichkeit zwischen YopM und GPIb führte sogleich zu einem ersten Aufklärungsversuch der Rolle YopMs in der Yersinien-Infektion. So legten Leung und Straley 1990 kurz nach der Entdeckung des Effektors dar, dass YopM im Extrazellularraum mit Thrombin interagiert und dadurch antagonistisch die Thrombozytenaggregation verhindert (Leung et al. 1990; Reisner & Straley 1992; Skrzypek & Straley 1996; Hines et al. 2001). Eine spätere Studie ergab darüber hinaus, dass YopM in der Lage ist, extrazellulär α1-Antitrypsin zu binden. Diese Interaktion zeigte jedoch keinen Einfluss auf dessen Funktion (Heusipp et al. 2006). Die Relevanz dieser Funde für die Virulenz YopMs ist jedoch zumindest fraglich, da eindeutig bewiesen werden konnte, dass YopM, wie die anderen Yops nicht sezerniert wird, sondern über das TTSS in die Wirtszelle transloziert (Boland et al. 1996). Zudem konnte bei Versuchen YopM extrazellulär durch Antikörper zu neutralisieren, keine signifikante Verschlechterung der Virulenz erreicht werden (Nemeth & Straley 1997). In der Wirtszelle ist YopM in der Lage über einen Vesikel-assoziierten Prozess in den Nucleus zu gelangen, wobei jedoch auch ein Teil des Proteins, oft in der Nähe der Kernmembran, im Zytosol verbleibt (Skrzypek et al. 1998). Dieser Prozess scheint abhängig von Mikrotubuli zu sein. Durch Struktur- und Sequenzvergleiche konnte kein klassisches Kernlokalisationssignal (NLS) für YopM bestimmt werden. Jedoch konnten, mittels Deletionsmutanten in einem Saccharomyces-Modell, zwei strukturelle Bereiche von YopM für dessen Transport in den Nukleus verantwortlich gemacht werden. Diese Bereiche entsprechen den ersten drei LRRs und den letzten 32 C-terminalen Aminosäuren und sind in allen bisher bekannten YopMIsoformen hochkonserviert (Skrzypek et al. 2003; Benabdillah et al. 2004). Die Tatsache, dass ein klassisches NLS fehlt und stattdessen hochkonservierte Bereiche des YopM-Proteins für dessen Translokation verantwortlich sind, spricht dafür, dass YopM über einen bisher unbekannten Interaktionspartner in den Kern gelangen könnte. Diese neugewonnene Erkenntnis der Kernlokalisation legte die Vermutung nahe, dass YopM einen Einfluss auf transkriptionelle oder translationelle Prozesse der Wirtszelle nehmen könnte. Die Ergebnisse 14 II Einleitung zweier Arbeitsgruppen hierzu waren jedoch widersprüchlich. So berichteten Sauvonnet und Kollegen, dass YopM in der Lage war, in einem Infektionsmodell von J774-Zellen, die Expression Zellzyklus und Zellwachstum regulierender Gene zu induzieren. Hoffmann und Kollegen konnten unter sehr stringenten Bedingungen jedoch keine Regulation der Genexpression durch YopM beobachten (Sauvonnet, Pradet-Balade, et al. 2002; Hoffmann et al. 2004). In verschiedenen Infektionsmodellen konnten eine Reihe von Hinweisen darauf gesammelt werden, dass YopM eine entscheidende Rolle in der Unterdrückung der Immunantwort des Wirts auf die Infektion mit Yersinien spielt. Im Maus-Modell zeigte sich, dass YopM-defiziente Yersinia-Mutanten deutliche Wachstumsdefizite aufwiesen und bereits zwei Tage nach der Infektion („post infection“, p.i.) eine deutlich reduzierte Zellzahl zeigten. Dies ging einher mit einer sehr starken Aktivierung des Immunsystems. Am vierten Tag p.i. waren alle Bakterien abgetötet. Im Gegensatz dazu zeigte der Wildtyp uneingeschränkte Vermehrung, was zum Tod der Mäuse an Tag 6 p.i. führte (Kerschen et al. 2004). Dieser drastische Unterschied in der Überlebensfähigkeit der Mutante war auch bei SCID-Mäusen, denen B- und T-Zellen fehlen, zu beobachten. Weiter zeigten Leber und Milz der Mäuse stark erhöhte Werte für proinflammatorische Zytokine wie IL-12, IL-18, TNF-α, IL-1β und IL-15 (Kerschen et al. 2004; Ye et al. 2009). Ähnlich Effekte konnten durch Rüter und Kollegen bestätigt werden. Diese legten dar, dass extrazelluläres YopM in der Lage war autonom (vermittelt durch die beiden Nterminalen α-Helices) in Makrophagen einzudringen und dort die Expression der Zytokine zu unterdrücken (Rüter et al. 2010). Weiterhin konnte dieses YopM im Kern gefunden werden (Scharnert et al. 2013). Einen möglichen Erklärungsansatz für die Reduktion der Zytokinausschüttung durch YopMvermittelte Effekte lieferten LaRock und Kollegen. In einem Screen auf Yersinia-Effektoren, die mit Caspase-1 interagieren, entdeckten sie YopM. Aktivierung der Cystein-Protease Caspase-1 vermittelt eine Reihe von Prozessen, die zur Ausschüttung von Zytokinen wie IL1β und IL-18 führen und an deren Ende die Pyroptose steht. In einer Reihe von Experimenten wurde dargestellt, dass YopM durch direkte Interaktion in der Lage ist, Caspase-1 in vivo und in vitro zu hemmen. Dieser inhibitorische Effekt verhindert den durch Pyroptose vermittelten programmierten Zelltod von Makrophagen und die dadurch induzierte Rekrutierung des Inflammasoms (LaRock & Cookson 2012). Als weitere Bindungspartner von YopM konnten bereits 2003 die „protein kinase C-like 2“ (PRK2/PKN2) und die „ribosomal S6 protein kinase 1 (RSK1) identifiziert werden (McDonald et al. 2003). In einer direkten Interaktion bringt YopM hierbei die beiden Kinasen in einen zuvor unbekannten Komplex, indem hyperphosphoryliertes RSK1, PKN2 phosphoryliert und damit aktiviert. Die physiologischen Konsequenzen dieses neuen Signalwegs sind jedoch bis dato unbekannt. In darauf aufbauenden Arbeiten konnte gezeigt werden, dass die Interaktion mit YopM zu einer Blockade der Dephosphorylierung von RSK1 führt und diese somit daueraktiviert. In dieser Arbeit wurde weiterhin offengelegt, dass YopM alle Mitglieder der RSK-Familie (RSK1-4) sowie weitere Isoformen von PKN gleichermaßen bindet (Hentschke et al. 2010). Durch Experimente zweier Arbeitsgruppen konnten die YopM-Epitope, die für die Bindung der Kinasen verantwortlich sind, eingeengt werden. Die letzten sechs C-terminalen Aminosäuren von YopM scheinen für die Interaktion mit RSK1 unabdingbar zu sein (McCoy et al. 2010), während die Interaktion mit PKN2 über den Kernbereich LRR6-15 von YopM aus 15 II Einleitung Y. pseudotuberculosis YPIII vermittelt wird (McPhee et al. 2010). Bei Deletion der für die Interaktion verantwortlichen Molekülabschnitte zeigte sich eine verminderte, YopM-vermittelte Pathogenität. Hierbei ist anzumerken, dass unterschiedliche Stämme mit verschiedenen YopM-Isoformen für die Interaktionsstudien verwendet wurden, welche sich teilweise drastisch in ihrem LRR-Gehalt unterscheiden. In einer Studie, die die Ergebnisse von McDonald und Kollegen unter Infektionsbedingungen reproduzieren sollte, konnte von Moritz Hentschke, neben den Mitgliedern der RSK- und PKNFamilie (Hentschke et al. 2010), auch ein weiterer, bisher unbekannter Interaktionspartner identifiziert werden, die DEAD-Box-Helikase DDX3. Die gesammelten Ergebnisse der YopM-Forschung zeigen, dass das Protein über keine direkte katalytische Funktion verfügt, jedoch über eine Reihe von Interaktionen mit Wirtsproteinen sowie durch zahllose, noch unaufgeklärte Prozesse unabdingbar für die volle Entfaltung der Virulenz von Yersinia spp. ist. Die Strukturaufklärung von YopM aus Y. pestis 195/P (Evdokimov et al. 2000; Evdokimov et al. 2001) lieferte erste Eindrücke wie YopM diese Mannigfaltigkeit an Interaktionen vermitteln könnte. YopM gehört zur Familie der LRRProteine, die in einer Vielzahl von Organismen vorhanden sind und hauptsächlich ProteinProtein-Interaktionen vermitteln. II.5 LRR-Proteine Der „Leucine Rich Repeat“ (LRR) ist ein weit verbreitetes, 20-30 Aminosäuren langes Motiv aus zwei oder mehreren Leucin reichen Domänen. Es kommt in einer Vielzahl von Proteinen aus allen Bereichen des Lebens, von Viren und Bakterien über Pflanzen bis zum Menschen vor. Die Vertreter dieser Proteinfamilie stellen zum größten Teil sogenannte Gerüstproteine für Protein-Protein-Interaktionen dar (Bella et al. 2008). Jeder LRR besteht aus 20-30 Aminosäuren und hat einen ungewöhnlich hohen Anteil an hydrophoben Leucinen. Das die Klasse definierende Element stellt die Konsensus-Sequenz LxxLxLxxNxL (x, beliebige Aminosäure) dar (Kajava 1998), obwohl auch andere hydrophobe Aminosäuren, wie Isoleucin oder Valin, an die Stelle des Leucins treten können. Mitglieder der Familie können intrazelluläre, extrazelluläre oder Membranproteine mit weit gefächerten biologischen Wirkungsspektren sein (Kresse & Schönherr 2001; Matilla & Radrizzani 2005; Hohenester et al. 2006). Trotz der großen Spannbreite an unterschiedlichen Funktionen, besitzen sie eine gemeinsame strukturelle Architektur, die sie dazu prädestiniert Proteine zu binden. Die erste Kristallstruktur eines LRR-Proteins war der RibonucleaseInhibitor (RNI), welcher die Proteinfamilie prägte (Kobe & Deisenhofer 1993). Seit dessen Entdeckung gibt es eine Unmenge weiterer LRR-Proteinstrukturen, mit jährlichem Zuwachs in der PDB-Datenbank. Protein-Domänen mit einer LRR-Architektur nehmen eine sogenannte „magnetspulenartige“ Form ein, in der jeder Repeat eine Windung der Spule darstellt (Bella et al. 2008). Dieser Aufbau führt in der Konsequenz zu Proteinen, die je nach Länge ,Anzahl und Aufbau der Repeats, in der Form von flachen, „hufeisenartigen“ bis zu helikalen Strukturen variieren (Abbildung 4). 16 II Einleitung A B Abbildung 4: Vergleichende Sekundärstruktur von LRR-Proteinen. Vergleich zweier LRR-Proteine mit unterschiedlich starker Biegung A: Charakteristische, nahezu flache Hufeisenform des Toll Like Receptor 3 (PDB Nr. 2A0Z) B: Stark gebogene Form von Internalin A (PDB Nr. 1V0T). Ribbon-Repräsentation, dargestellt mit USCF Chimera (Pettersen et al. 2004). α-helikale Strukturen in orange, βFaltblätter in lila und verbindende Loops in grau gezeigt. Die konkave Seite aller LRR-Proteine besteht aus einer geordneten β-Faltblattstruktur, zu der jeder Repeat einen Strang beisteuert. Der Aufbau der konvexen Seite ist wiederum variabel und abhängig von der Aminosäureanzahl einer einzelnen Wiederholungseinheit. Hier findet man je nach Länge α-Helices, 310-Helices, Polyprolin II-Regionen, β-Turns oder sogar βFaltblattstrukturen. Der innere Kern der spulenartigen Struktur wird von den hydrophoben Aminosäuren gebildet. Hier sind die konservierten Leucine und andere aliphatische Aminosäuren dicht gepackt und die Seitenketten liegen isoliert von der Hydrathülle. Durch die strenge Sequenztreue bilden Van der Waals-Kräfte zwischen benachbarten Repeats ein äußerst stabiles hydrophobes Rückgrat (Bella et al. 2008). Dieser Aufbau bedingt auch das Vorhandensein eines an den letzten Repeat angrenzenden Capping-Motivs, um den hydrophoben Kern abzuschließen. Ebenso geht man davon aus, dass die Repeats für die korrekte Faltung auf eine vorgeschaltete, N-terminale Leitstruktur angewiesen sind. Diese Motive sind strukturell äußerst divers und können, neben der Initiation der Faltung der LRRs, weitere biologische Funktionen übernehmen (Kobe & Deisenhofer 1995). Die gebogene LRR-Architektur scheint besonders für Protein-Protein-Interaktionen geeignet zu sein und man geht generell davon aus, dass die konkave Seite der Proteine den Hauptanteil an der Ligandenbindung trägt. Hierfür gibt es viele Beispiele in der Literatur, auch bakterielle, wie der Komplex aus Internalin und E-Cadherin (Schubert et al. 2002). Die Stärke der Bindung wird dabei zu einem großen Teil durch die Interface-Fläche bestimmt, was bei großen Interaktionsbereichen zu Bindungen mit Dissoziationskonstanten (Kd) im bis zu femtomolaren Bereich führen kann (Lee et al. 1989). Am Beispiel von Internalin und ECadherin wird jedoch klar, dass auch die Interaktion der Seitenketten einen großen Einfluss auf die Bindungsstärke hat. So liegt die Kd in diesem Komplex im niedrigen mikromolaren Bereich, lässt sich jedoch durch Mutationen der an der Bindung beteiligten Aminosäure um das vierfache steigern (Schubert et al. 2002; Wollert et al. 2007) Der repetetive Aufbau der LRR-Proteine lässt schließlich eine sehr große Variabilität der internen Architektur zu. Durch Replikation, Deletion bzw. Neuorganisation einzelner LRRs können neue Epitope geschaffen werden, ohne die Stabilität bzw. den generellen Aufbau des Proteins drastisch zu verändern. Dieses Prinzip findet beispielsweise im Immunsystem vieler 17 II Einleitung Vertebraten Anwendung. Hier sind Immunrezeptoren in der Lage durch unterschiedliche Splicevarianten des selben Proteins, ein immer neues Set an Erkennungsdomänen zu kreieren, um auf unterschiedlichste Antigene reagieren zu können (Street et al. 2006). II.5.1 YopM in der Familie der LRR-Proteine Bereits 2001 waren Evdokimov und Kollegen in der Lage YopM aus Y. pestis 195/P zu kristallisieren und die Röntgenstruktur des Proteins mit einer Auflösung von 2,1 Å zu lösen (Evdokimov et al. 2000; Evdokimov et al. 2001). YopM ist ein typischer Vertreter der LRR-Proteine, der mit einer Repeat-Länge von 20 bzw. 22 Aminosäuren (LRR4, 6 und 8) eine sehr kurze Wiederholungseinheit besitzt. Die KonsensusSequenz der LRRs lautet: **L*A/V**N*L**LPD/EL..PP*L. Die 15 Repeats werden N-Terminal von zwei Alpha-Helices und C-Terminal von einem kurzen Capping-Motiv umschlossen. Dieses Motiv erinnert mit seiner Sequenz (EDLRMN) an einen unfertigen LRR. In der Kristallstruktur zeigten die ersten 33-N-terminalen und die letzten 24 Cterminalen Aminosäuren keine Elektronendichte. Wie bei allen Vertretern der LRR-Proteine wird die konkave Seite durch β-Faltblattstrukturen gebildet. Die konvexe Seite besteht als Konsequenz der Kürze der Repeats aus einem elongierten Bereich mit einer Polyprolin IIRegion, im Falle der 20-As Repeats, und einer kurzen 310-Helix, im Falle des 22-As Repeats. Abbildung 5: YopM_195/P Monomerstruktur. Struktur des YopM_195/P Monomers (1jl5) in Ribbon-Repräsentation. Dargestellt mit USCF Chimera (Pettersen et al. 2004). α-helikale Strukturen in orange, β-Faltblätter in lila und verbindende Loops in grau gezeigt. Die beiden N-terminalen α-Helices dienen wahrscheinlich der korrekten Faltung der nachfolgenden Repeat-Struktur und so konnte kürzlich gezeigt werden, dass eine Chimäre aus dem YopM-N-Terminus und der LRR-Einheit von InlB eine intakte Faltung aufweist. Dieses Konstrukt war in der Lage den bekannten Interaktionspartner von InlB, den METRezeptor, mit einer ähnlichen Affinität wie das native Protein zu binden. Die Generierung eines funktionalen Proteins, das lediglich aus dem LRR-Bereich bestand, war hingegen nicht möglich (Breitsprecher et al. 2014). Der kurze C-Terminus dient dem Schutz des hydrophoben Kerns des Proteins. Interessanterweise trat YopM in mehreren von Evdokimov beschriebenen Kristallformen als Tetramer in Erscheinung. In diesem kunstvollen Gebilde, sind zwei YopM-Monomere an ihren C-Termini miteinander verbunden. Das „Tail-to-Tail“-Dimer lagert sich an ein weiteres, gleich gebautes Dimer an und kreiert so eine Art Doppelhelix. Diese Helix bildet einen Tunnel mit 35 Å Durchmesser. Bei der Stabilisierung dieses Dimers spielen Ca2+-Ionen, die in hoher 18 II Einleitung Konzentration im Kristallisationsansatz vorhanden waren, eine tragende Rolle. Ein Nachweis des Tetramers in Lösung konnte jedoch nicht erbracht werden und so bleibt es zumindest fraglich, ob es eine biologische Relevanz besitzt oder ein Kristallisationsartefakt darstellt. A B Abbildung 6: YopM_195/P Kristall-Tetramer. A: Struktur des YopM_195P Tetramers in Ribbon-Repräsentation, erstellt mit PyMol (Schrödinger LLC, USA). B: Darstellung der an der Stabilisierung des Tetramers beteiligten Wechselwirkungen wichtiger Aminosäuren mit 2+ Ca (Evdokimov et al. 2001). Die Ergebnisse von Evdokimov und Kollegen lieferten einen ersten Einblick in den strukturellen Aufbau des YopM-Proteins. Wie unter III.3.2.7 erwähnt ist YopM jedoch äußerst heterogen und kommt in unterschiedlichen Yersinia spp. bzw. unterschiedlichen Serotypen ein und derselben Spezies in verschiedenen Isoformen vor. Aus Sequenzvergleichen geht hervor, dass allen Proteinen der α-helikale N-Terminus und die ersten drei Repeats sowie der letzte Repeat und der abschließende C-Terminus gemein sind. Durch Duplikationen bzw. Deletionen einzelner LRRs kommt es jedoch zu einem hohen Maße an Variabilität im LRRKernbereich der Proteine. So reicht die Anzahl an LRR in bisher bekannten YopM-Isoformen von 13 – 21, und auch die Zusammensetzung der Repeats ist deutlich heterogen (Boland et al. 1998; Vieux & Barrick 2011). II.6 DDX3 Wie unter II.3.2.7 beschrieben konnte durch Moritz Hentschke in einem J774-MakrophagenInfektionsmodell mit Y. enterocolitica WA-314, DDX3 als neuer Bindungspartner für YopM identifiziert werden. Für diesen Versuch wurde ein TAP („Tandem Affinity Purification“)getaggtes YopM-Konstrukt kreiert, welches N-Terminal einen SBP („Streptavidin Binding Peptide“) sowie einen CBP („Calmodulin Binding Peptide“)-Tag besitzt. Dieses Protein wurde über das native TTSS der Yersinien in die Makrophagen injiziert. Nach erfolgter Infektion wurden die Zellen lysiert und das TAP-YopM wurde sequentiell über Streptavidin- und Calmodulin-Affinitätschromatographie gereinigt. Die co-präzipitierten Proteine wurden anschließend mittels MALDI-TOF-Massenspektrometrie identifiziert. DDX3 ist eine ATP-abhängige Helikase, die zur Familie der DEAD-Box-Helikasen gehört. Die Mitglieder dieser Familie sind an verschiedenen Prozessen des mRNA-Metabolismus wie Transkription, Splicing, Translation und RNA-Export beteiligt (Rocak et al. 2005; Cordin et al. 2006; Lai et al. 2008; Lee et al. 2008). Namensgebend für die Familie ist ein, aus den Aminosäuren Asp-Glu-Ala-Asp (DEAD) gebildetes Motiv im Kern des Enzyms, welches in 19 II Einleitung allen Mitgliedern der Familie vorhanden ist. DEAD-Box Helikasen kommen in allen Eukaryoten und einigen Prokaryoten vor. Ihr molekularer Aufbau besteht aus einer hochkonservierten Helikase-Kernstruktur, die aus zwei Domänen gebildet wird. Diese beinhaltet die Bindestellen für ATP und RNA (Caruthers & McKay 2002; Singleton et al. 2007; Fairman-Williams et al. 2010). Der Kern ist wiederum umgeben von variablen Strukturen, die die Spezifität der einzelnen Proteine definieren. Abbildung 7: Strukturelle Komposition der DEAD-Box-Helikase DDX3 (Högbom et al. 2007). Aufbau von DDX3 mit den in allen DEAD-Box-Helikasen konservierten Motiven und gebundenem AMP. Details siehe Text. Der konservierte Kern besteht aus neun Konsensus-Sequenzen, die die funktionale Helikase bilden. Motiv Q, I (Walker A mit dem Phosphat bindenden P-Loop), II (Walker B, DEAD-Box), Ia, Ib und III liegen auf Domäne 1, während Motiv IV, V und VI auf Domäne II zu finden sind. Strukturelle und biochemische Analysen ergaben, dass die verschiedenen Motive an der Nukleotid-Bindung (Q, I und II), der RNA Bindung (Ia, Ib, IV und V) und an der ATP-Hydrolyse (III und IV) beteiligt sind (Cordin et al. 2006). Strukturell besitzen beide Domänen eine Faltung der RecA-Superfamilie mit fünf β-Faltblättern, die von fünf α-Helices umgeben sind. DDX3 wird eine Reihe zellulärer Funktionen in Zellzykluskontrolle, Zellwachstum und Proliferation zugeschrieben und so wurde herausgefunden, dass eine Dysregulation des Enzyms zur Bildung von Brustkrebs oder hepatozellulären Karzinomen führen kann (Botlagunta et al. 2008; Chang et al. 2006). Des Weiteren interagiert DDX3 mit dem Translations-Initiationsfaktor eIF3 und nimmt somit Einfluss auf die Translation. Neben diesen und zahlreichen weiteren zellulären Effekten scheint DDX3 eine wichtige Rolle in der antiviralen Immunantwort zu spielen, indem es in Signaltransduktions-Prozesse involviert ist, die bei der Erkennung von Viruspartikeln eine Rolle spielen und zur Freisetzung von Interferon beta (IFNβ) führen. So wurde beschrieben dass DDX3 mit der „Tank binding 20 II Einleitung kinase 1“ (TBK1) interagiert und dadurch die Ausschüttung von IFNβ beeinflusst. Hierbei bewirken beide Proteine einen positiven synergistischen Effekt auf den IFNβ-Promotor. Dieser Einfluss konnte gezeigt werden, da das K7 Protein von Pockenviren eben diesen Signalweg durch Hemmung von DDX3 unterbindet (Soulat et al. 2008; Schröder et al. 2008). Zahlreiche weitere Publikationen beschreiben DDX3 als Ziel viraler Manipulation. So ist DDX3 an der Replikation von HIV, HCV sowie Pockenviren beteiligt (Mamiya & Worman 1999; Owsianka & Patel 1999; Schröder 2011). Darüber hinaus ist DDX3 ein essentieller Wirtsfaktor für HIV. Das Rev-Protein interagiert mit DDX3 und dem nukleären Exportprotein CRM1 („chromosome maintenance 1“) und bewirkt somit den Export ungespliceter oder teilweise gespliceter RNA aus dem Kern (Schröder 2010). CRM1 bewerkstelligt den Export von Proteinen aus dem Zellkern ins Zytoplasma (Fukuda et al. 1997). Über die Interaktion mit CRM1 ist DDX3 schließlich in der Lage zwischen Zellkern und Zytoplasma zu pendeln (Yedavalli et al. 2004). Der Einfluss, den nun YopM als erster beschriebener bakterieller Effektor auf DDX3 hat, ist bislang unbekannt und wird unabhängig von der hier dargelegten Arbeit untersucht. Erste Resultate konnten jedoch bisher keine Auswirkungen der Interaktion auf die natürlichen Funktionen, wie die ATPase oder Helikase Aktivität von DDX3 belegen. Ebenso konnte bisher kein Einfluss auf die IFN-beta Produktion oder eine Auswirkung auf Transkriptionsfaktoren festgestellt werden (Hentschke et al. unveröffentlicht) 21 II Einleitung II.6 Zielsetzung Ziel der vorliegenden Arbeit war es das 20-LRR beinhaltende YopM aus Y. enterocolitica WA314 aufzureinigen und strukturell sowie biochemisch zu charakterisieren. YopM aus Y. pestis 195/P formte in der Kristallstruktur von Evdokimov ein kunstvoll designtes Tetramer, indem sich zwei Monomere in einer „Tail-toTail“-Konformation zusammenlagerten und einen Strang einer Doppelhelix bildeten (Evdokimov et al. 2001). Dass dieses Tetramer physiologisch ist, konnte jedoch nicht bewiesen werden. Neben der hochauflösenden Kristallstruktur von YopM_WA-314, sollte deshalb vor allem die Struktur des Proteins in Lösung Aufschluss über dessen Oligomerisierungsgrad geben. Weiterhin sollte untersucht werden, welchen Einfluss die fünf zusätzlichen LRRs auf die Grundarchitektur des Proteins nehmen. Hier sollte der Vergleich mit der vorhandenen Struktur aus Y. pestis 195/P Gemeinsamkeiten bzw. eventuelle Unterschiede offenlegen. In einer Vorarbeit konnte die DEAD-Box-Helikase DDX3 als neuer Bindungspartner für YopM in einem Infektionsmodell mit J774-Maus-Makrophagen identifiziert werden. Es sollte nun zunächst mit biochemischen Experimenten überprüft werden, ob es sich dabei um eine direkte Interaktion handelt. Hierzu mussten geeignete Expressionskonstrukte generiert werden, mit denen es möglich war, eine direkte Interaktion nachzuweisen und zu charakterisieren. Handelte es sich tatsächlich um eine direkte Bindung zwischen YopM und DDX3, so sollte die Art der Bindung auch mit strukturbiologischen Mitteln analysiert werden. Die Ergebnisse aus diesen Experimenten sollten Aufschluss darüber geben, wie YopM mit anderen Proteinen interagiert. Da mittlerweile eine Vielzahl verschiedener Interaktionspartner intra- wie extrazellulär beschrieben sind, sollte herausgefunden werden über welche Mechanismen YopM in der Lage ist, diese zum Teil gleichzeitigen Interaktionen zu vermitteln. Schließlich sollte der beschriebene inhibierende Einfluss auf Caspase-1 (LaRock & Cookson 2012) in einem in vitro-Experiment mit verschiedenen Isoformen von YopM überprüft werden. Der dargelegte Effekt und die Auswirkung der Interaktion auf die Rekrutierung des Inflammasoms könnten den ersten direkten Zusammenhang zwischen YopM und der Immunabwehr der Wirtszelle bestätigen. 22 III Material III Material und Methoden III.1 Material III.1.1 Geräte Tabelle 1: Geräte Gerät Typ, Hersteller DLS Gerät Elektrophorese SpectroSIZE 300 Nabitec (G) Agarose-Gel: Roth, Karlsruhe (G); SDS-PAGE: Mini-Protean II and Western Blot apparatus, BioRad, Munich (G) Curix 60, Agfa, Mortsel (B) Hartenstein, Würzburg (G) Äktapurifier; Äktaexplorer; Äktaprime plus, GE Healthcare (UK) -80°C: HERA freeze, Heraeus, Kendro Laboratory, Hanau (G); -20°C: comfort, Liebherr-International AG, Bulle (CH) Gel dryer 543, BioRad, München(G) Honeybee 961, Genomic Solutions ( USA) Infinite M200, TECAN, Männedorf (CH) Monolith NT.115, Nanotemper (G) Mikroskop SZX12 mit Kamera DP10 , Olympus (J) 900W, Panasonic, Kadoma/Osaka (J) PeqLab, Erlangen (G) Seven easy, Mettler-Toledo, Giessen (G) Ultrospec 3100 pro, Amersham/GE Healthcare Europe, Munich (G) 2, 10, 20, 100, 200, 1000 µl, Gilson, Den Haag (NL); 5000 µl Eppendorf, Hamburg (G); Accu-jet pro, Brand, Wertheim (G) CanoScan 4400F, Canon, Amsterdam (NL) Certomat BS-1, Sartorius, Göttingen (G) Digital Sonifier 250-D, Branson, Danbury (USA) Hera Safe, Thermo Scientific, Rockford (USA) Petra III, DESY, Hamburg, Deutschland Doris III, DESY, Hamburg, Deutschland Entwickler für Röntgenfilme Filmkassette FPLC Gefrierschränke Geltrockner Kristallisationsroboter Microplate reader Microscale Thermophoresis Mikroskop Mikrowelle NanoDrop® ND-1000 pH-Meter Photometer Pipetten Scanner Schüttelinkubator Sonifizierer Sterilbank Synchrotron 23 III Material Messplätze X33 SAXS beamline (DORIS) P12 EMBL BioSAXS Beamline (PETRA) Thermocycler Transilluminator UV-Transilluminator + Detektor Vortex Waage Wasserbad Western Blot-Apparatur Zentrifugen P14 EMBL Beamline Macromolecular Crystallography II - MX2 Beamline (PETRA) Primus-96, MWG-Biotech, Ebersberg (G); Mastercycler gradient, Eppendorf, Hamburg (G) Vilber Lourmat, ETX, Eberhardzell (G) ChemiDoc XRS, BioRad, Munich (G) REAX top, Heidolph Instruments, Schwabach (G) 440-47N, Kern, Balingen-Frommern (G) GFL Typ 1013, GFL, Burgwedel (G) OWL HEP-1, Thermo Scientific, Rockford (USA) Sorvall RC-5B und RC 28S, Thermo Scientific, Rockford (USA) 5417R and 5810R, Eppendorf, Hamburg (G) Sigma centrifuge 3-18K, Sigma, Osterode (G) III.1.2 Verbrauchsmittel Tabelle 2: Verbrauchsmittel Verbrauchsmittel Typ, Hersteller Chromatographiesäulen Anionenaustauscher UnoQ6, Biorad, Berkeley (USA) Gelfiltrationssäulen Superdex 75/200, GE Healthcare Europe, München (G) Glutathion Sepharose GSTrap FF, GE Healthcare Europe, München (G) Ni-NTA Sepharose HisTrapFF, GE Healthcare Europe, München (G) Slide-A-Lyzer G2 Dialysis Cassettes, Thermo Fisher Scientific (USA) GE Healthcare, Uppsala (S) Steritop™ Filter Units 0,22 µm, Merck Millipore, Darmstadt (G) 190 g/m2, Hartenstein, Würzburg (G) Dialysekassetten Glutathion-Sepharose 4B Flaschenfilter Filterpapiere für Western Blot Monolith™ NT.115 Hydrophilic Capillaries Monolith™ NT.115 Standard Treated Capillaries Multiwell-Platten NanoTemper Technologies GmbH, München (G) NanoTemper Technologies GmbH, München (G) 6- / 12-well Sarstedt, Nümbrecht (G); Nunclon 96-well flat 24 III Material Ni-NTA Agarose Polypropylensäulen 1 ml, 5ml Reaktionsgefäße Parafilm M Pasteurpipetten Pipettenspitzen PVDF-Membran Röntgenfilm RedSafe Nucleic Acid Staining Solution Serologische Pipetten Skalpell Spritzen Spritzenfilter Zentrifugenröhrchen Zentrifugenfilter bottom black polystyrol, Thermo Scientific/Nunc, Rockford (USA) Qiagen, Hilden, (G) Qiagen, Hilden, (G) 0.2 ml, Biozym Scientific, Hessisch Oldendorf (G); 0.5, 1.5, 2 ml Standard; 1.5 ml Protein LoBind, Eppendorf, Hamburg (G) Bemis®, Pechiney Plastic Packaging, Neenah (USA) 230 mm, Heinz Herenz Medizinalbedarf, Hamburg (G) Sterile Biosphere filter tips and non-sterile 10, 200, 1000 µl, Sarstedt, Nümbrecht (G); 5000 µl, Eppendorf, Hamburg (G) Immobilon-P Membrane, Merck Millipore, Darmstadt, (G) Super RX, Fuji medical X-ray film, Fujifilm, Tokyo (J) HiSS Diagnostics GmbH, Freiburg (G) Sterile 2, 5, 10, 25 ml, Sarstedt, Nümbrecht (G) Sterile, B. Braun, Melsungen (G) Sterile 5, 20 ml, B. Braun, Melsungen (G) SFCA 0.2 µm, Thermo Scientific/Nalgene, Rockford (USA) Sterile 15 ml/50 ml, Sarstedt, Nümbrecht (G) Vivaspin® 6,15,20 MWCOs from 3 000 to 10000, GE Healthcare Europe, München (G) Ultrafree-MC, VV 0.1 µm, Millipore, Billerica (USA) III.1.3 Kits, Enzyme und Reagenzien Tabelle 3: Kits, Enzyme und Reagenzien Kit, Enzym, Reagenz Hersteller BioRad Gel Filtration Standard BioRad Protein Assay EndoFree Plasmid Maxi Kit FastAPTM (Alkaline Phosphatase) FastDigest® restriction enzymes Gel Filtration Molecular Weight Markers Kit for Molecular Weights 6,500–66,000 Da GoTaq® Hot Start Polymerase HisProbe™-HRP Kristallisationsscreen AmSO4 Suite Kristallisationsscreen ClassicsSuite Kristallisationsscreen ComPAS Suite Kristallisationsscreen Cryos Suite BioRad, München (G) BioRad, München (G) Life Technologies, Carlsbad (USA) Thermo Scientific, Rockford (USA) Thermo Scientific, Rockford (USA) Sigma-Aldrich, St. Louis (USA) Promega, Madison (USA) Thermo Scientific, Rockford (USA) Qiagen, Hilden (G) Qiagen, Hilden (G) Qiagen, Hilden (G) Qiagen, Hilden (G) 25 III Material Kristallisationsscreen JCSG+ Suite Kristallisationsscreen PACT premier Kristallisationsscreen Protein Complex Suite Kristallisationsscreen The Stura FootPrint Kristallisationsscreen Morpheus® HT-96 Monolith™ NT.115 Protein Labeling Kit RED-NHS NucleoSpin Extract II Kit PCR Extender System SuperSignal West Femto/ Pico detection T4-DNA-Ligase Taq-DNA-Polymerase + Puffer Thrombin ZR Plasmid Miniprep Kit Qiagen, Hilden (G) Qiagen, Hilden (G) Qiagen, Hilden (G) Molecular Dimensions Limited, Suffolk (UK) Molecular Dimensions Limited, Suffolk (UK) NanoTemper Technologies GmbH, München (G) Macherey-Nagel, Düren (G) 5 Prime, Hamburg (G) Thermo Scientific, Rockford (USA) Roche, Mannheim (G) Peqlab, Erlangen (G) GE Healthcare Europe, München (G) Zymo Research, Irvine (USA) III.1.4 Puffer und Lösungen Chemikalien und Puffer wurden von folgenden Firmen bezogen: Amersham/GE Healthcare, München (G), BD Biosciences, Heidelberg (G), Invitrogen/Life Technologies, Roche, Mannheim (G), Biozyme, Oldendorf (G), Merck, Darmstadt (G), PAA, Pasching (A), PromoCell, Heidelberg (G), Roth, Karlsruhe (G), Sigma-Aldrich, St. Louis (USA) sowie Thermo Fisher Scientific, Waltham (USA). Die Medien wurden für 20 min bei 121 °C und 1.4 bar autoklaviert. Puffer wurden entweder ebenfalls autoklaviert oder bei hitzeempfindlichen Inhaltsstoffen mittels 0,22 µm Filtereinheiten sterilfiltriert. III.1.4.1 Wachstumsmedien Tabelle 4: Wachstumsmedien Medien Zusammensetzung, Hersteller LB-medium (Luria/Miller) 10 g/l Trypton 5 g/l Hefeextrakt 10 g/l Natriumchlorid pH 7,0 Carl Roth GmbH, Karlsruhe (G) 10 g/l Trypton 5 g/l Hefeextrakt 10 g/l Natriumchlorid 15 g/l Agar pH 7,0 Carl Roth GmbH, Karlsruhe (G) LB-Agar (Luria/Miller) 26 III Material Terrific-Broth 12 g/l Casein 24 g/l Hefeextrakt 9,4 g/l K2HPO4 2,2 g/l KH2PO4 Carl Roth GmbH, Karlsruhe (G) Tabelle 5: Antibiotika, Zusätze Antibiotika, Zusätze Stammkonzentration Ampicillin Chloramphenicol Isopropyl-β-Dthiogalactopyranosid (IPTG) Kanamycin L-Arabinose Tetrazyklin 100 mg/ml 20 mg/ml 1M 50 mg/ml 20 % (w/v) 20 mg/ml III.1.4.2 Chemisch-kompetente E. coli Tabelle 6: Chemisch-kompetente E.coli Puffer Zusammensetzung TFB1 100 mM RbCl 50 mM MnCl2 30 mM Kaliumacetat 10 mM CaCl2 15 % (v/v) Glycerol pH 5,8 mit Essigsäure 10 mM MOPS 10 mM RbCl 75 mM CaCl2 15 % (v/v) Glyverol pH 8,0 TFB2 III.1.4.3 Proteinaufreinigung Tabelle 7: Proteinaufreinigung Puffer Zusammensetzung Anionenaustauscher PufferA Anionenaustauscher PufferB 20 mM NaH2PO4 pH 6,0 20 mM NaH2PO4 1 M NaCl 27 III Material Gelfiltrationspuffer DDX3 Gelfiltrationspuffer TEV-Protease Gelfiltrationspuffer YopM GST-Elutionspuffer His-Lysepuffer His-Waschpuffer His-Elutionspuffer PBS (phosphate buffered saline) TEV-Reaktionspuffer pH 6,0 50 mM Hepes 250 mM NaCl 2 mM DTT 10 % (v/v) Glycerol pH7,5 25 mM NaH2PO4 100 mM NaCl 10 % (v/v) Glycerol pH 7,5 50 mM Hepes 250 mM NaCl 2 mM DTT pH 7,5 50 mM Tris-HCl 30 mM Glutathion 1 mM DTT pH 7,5 50 mM NaH2PO4 300 mM NaCl 10 mM Imidazol pH 7,4 50 mM NaH2PO4 300 mM NaCl 20 mM Imidazol pH 7,4 50 mM NaH2PO4 300mM NaCl 250 mM Imidazol 10 % v/v Glycerol pH 7,4 137 mM NaCl 2,65 mM KCl 10 mM Na2HPO4 1,76 mM KH2PO4 pH 7,5 50 mM Tris-HCl 0.5 mM EDTA 1 mM DTT pH 8,0 28 III Material Tabelle 8: Chemikalien und Zusätze Chemikalien, Zusätze Hersteller 1,4-Dithiothreitol (DTT) cOmplete, EDTA-free EDTA-Dinatriumsalz TCEP (tris(2carboxyethyl)phosphine) Sigma-Aldrich, St. Louis (USA) Roche, Basel (Ch) Merck-Millipore, Darmstadt (USA) Sigma-Aldrich, St. Louis (USA) III.1.4.4 Elektrophorese und Western Blot Tabelle 9: Elektrophorese und Western Blot Puffer Zusammensetzung Coomassie-Färbelösung 0,1 % (w/v) Coomassie Brilliant Blue R-250 40 % (v/v) Methanol 10 % (v/v) Essigsäure 40 % (v/v) Methanol 10 % (v/v) Essigsäure 30 % (v/v) Glycerol 0,25 % (w/v) Bromphenolblau 0,25 % (w/v) Xylenblau 1x TAE Puffer 1.37 M NaCl 26.5 mM KCl 0.1 MNa2HPO4 17.6 mM KH2PO4 pH 7.7 1x PBS 0,1% Tween20 1.5 M Tris Base 0.004 % (w/v) SDS pH 8,8 250 mM Tris/HCl pH 6,8 20 % (w/v) Glycerol 8 % (w/v) SDS 4 mg Bromphenolblau (4% (v/v) β-Mercaptoethanol) 0.025 M Tris Base 0.192 M Glycin 0.1 % (w/v) SDS 0,5M Tris Base 0,004% (w/v) SDS pH 6,8 Coomassie-Entfärbelösung DNA-Ladepuffer PBS 10x PBST Resolving Puffer (SDS-PAGE) SDS-PAGE Ladepuffer (reduzierend) SDS-PAGE Laufpuffer (10x) Stacking Puffer (SDS-PAGE) 29 III Material TAE (50x) TBS (10x) TBST Transfer-Puffer (Western Blot) 2 M Tris-Acetat pH 8,3 0,5 M EDTA pH 7.4 200 mM Tris-Base 1,5 M NaCl pH 7,4 1x TBS 0.3 % Tween20 150 m M Tris-Base 25 mM Glycin 20 % (v/v) Methanol III.1.4.4.1 SDS-Polyacrylamidgele Tabelle 10: SDS-Polyacrylamidgele Puffer/Bestandteil Sammelgel ddH2O Stacking buffer Resolving buffer 30 % Acrylamid 10 % APS TEMED 3,1 ml 1,25 ml -0,65 ml 50 µl 5 µl Trenngel 7,5% 4,86 ml 2,5 ml 2,5 ml 50 µl 10 µl III.1.4.5 GST-Pulldown Tabelle 11: GST-Pulldown Puffer Zusammensetzung MBP Column Buffer 20 mM Tris-HCl pH 7,5 200 mM NaCl 1 mM EDTA 10 mM β-Mercaptoethanol 1x protease inhibitors (cOmplete) 20 mM Tris-HCl pH 7,5 500 mM NaCl 0.5 % NP40 10 mM Tris-HCl pH 7.5 150 mM NaCl 0.1% NP40 PD-Bindepuffer PD-Waschpuffer 30 10% 4,18 ml -2,5 ml 3,34 ml 50 µl 10 µl 12,5% 3,2 ml 2,5 ml 4,16 ml 50 µl 10 µl III Material III.1.4.6 Microscale Thermophorese Tabelle 12: MST-Puffer Puffer Zusammensetzung Labeling-Puffer 50 mM Hepes 150 mM NaCl pH 7,5 50 mM Hepes 150 mM NaCl 0,05 % Tween20 0,5 mg/ml BSA 2 mM DTT pH 7,5 MST-Reaktionspuffer III.1.4.7 Caspase-1 Assay Tabelle 13: Caspase Assay Puffer Zusammensetzung Caspase-1 Assay Puffer 50 mM Hepes 100 mM NaCl 0,1 % Chaps 1 mM EDTA 10% (v/v) Glycerol 10 mM DTT pH 7,4 III.1.5 Protein und DNA-Leitern A B Abbildung 8: Protein und DNA-Leitern. A: PageRuler Prestained Protein Ladder (Thermo Scientific, Rockford, USA). B: GeneRuler 1 kb DNA Ladder (Thermo Scientific, Rockford, USA). 31 III Material III.1.6 Bakterienstämme III.1.6.1 Escherichia coli Tabelle 14: E. coli-Stämme Stamm Genotyp Referenz DH5α F- endA1 glnV44 thi-1 recA1 relA1 gyrA96 deoR nupG Φ80dlacZΔM15 Δ(lacZYA-argF)U169, hsdR17(rK- mK+), λ– F- mcrA Δ(mrr-hsdRMS-mcrBC) Φ80lacZΔM15ΔlacX74 nupG recA1 araD139 Δ(ara-leu)7697 galE15 galK16 rpsL(StrR) endA1 λF– ompT gal dcm lon hsdSB(rB- mB-) λ (Taylor et al. 1993) TOP10 BL21-AI™ BL21CodonPlus®RIL B F–ompT hsdS(rB–mB–) dcm+ Tetr gal λ(DE3) endA Hte [argU ileY leuW Camr (Grant et al. 1990) (Moffatt & Studier 1987) (Dunn 1988) III.1.6.2 Yersinia Tabelle 15: Yersinia-Stämme Stamm Charakteristik Referenz Y. enterocolitica WA-314 Serotyp O:8; klinisches Isolat, Träger des Virulenzplasmids pYV-WA-314 Serotyp 0:8; Biotyp 1B, klinisches Isolat, Träger des Virulenzplasmids pYV8081 Serotyp III; klinisches Isolat (Heesemann & Laufs 1983) (Thomson et al. 2006) Y. enterocolitica 8081 Y. pseudotuberculosis YpIII (Bolin et al. 1982; Gemski et al. 1980) III.1.7 Plasmide III.1.7.1 Prokaryotische Proteinexpression Tabelle 16: Plasmide zur prokaryotischen Proteinexpression Vektor/ Konstrukt Characteristik Referenz pGEX-4T2 Vektor zur prokaryotischen Expression eines GSTFusionsproteins; MCS downstream GST-Tag GE Healthcare, München (G) 32 III Material pET302 pET303 pQE30-TEV Vektor zur prokaryotischen Expression eines 6xHisFusionsproteins; MCS downstream His-Tag Vektor zur prokaryotischen Expression eines GSTFusionsproteins; MCS upstream His-Tag Vektor zur prokaryotischen Expression eines GSTFusionsproteins; MCS upstream His; einklonierte TEV-ProteaseSchnittstelle Thermo Fisher Scientific, Waltham (USA) Thermo Fisher Scientific, Waltham (USA) Qiagen, Hilden (G); verändert, Rumm III.1.7.2 Eukaryotische Proteinexpression Tabelle 17: Plasmide zur eukaryotischen Proteinexpression Vektor/ construct pEGFP-N1 Charakteristik Vektor zur eukaryotischen Expression eines GFP-Fusionsproteins; MCS upstream His-Tag Referenz Clontech, Heidelberg (G) III.1.7.3 Expressionskonstrukte Tabelle 18: Expressionskonstrukte Konstrukt YopM (Y.e. WA-314) 6x NT-His-TEV-YopM_Full 6x NT-His-TEVYopM_Core 6x CT-His-YopM_Full (Annotation) 6x CT-His-YopM_Full 6x CT-His-YopM_noC 6x CT-His-YopM_Core Vektor; insert Referenz pET302; YopM-Volllänge (AS 1 – 506), TEV-ProteaseErkennungssequenz pET302; YopM-Kerndomäne (AS 34 – 481), TEV-ProteaseErkennungssequenz pET303; YopM-Volllänge, laut Annotation (AS -21 – 506) pET303; YopM-Volllänge (AS 1 – 506) pET303; YopM ohne C-Terminus (AS 1 – 481) pET303; YopM-Kerndomäne (AS 34 – 481) Diese Arbeit 33 Diese Arbeit Wolters, unveröffentlicht Diese Arbeit Diese Arbeit Diese Arbeit III Material 6x CT-His-YopM_LRR CT-GFP-YopM_Full NT-GST-YopM_Full NT-FLAG-GPI_YopM_Full pET303; YopM LRR (AS-74-481) pEGFP-N1; YopM-Volllänge (AS 1-506) pGEX-4T2; YopM-Volllänge (AS 1-506), Thrombin-ProteaseErkennungssequenz pCMVSPORT6; YopM-Volllänge (AS 1-506), GPI-Membrananker Diese Arbeit Diese Arbeit pET302; YopM-Volllänge (AS 1 – 368), TEV-ProteaseErkennungssequenz pET302; YopM-Kerndomäne (AS 34 – 343), TEV-ProteaseErkennungssequenz Diese Arbeit pET302; YopM-Volllänge (AS 1 – 409), TEV-ProteaseErkennungssequenz pET302; YopM-Kerndomäne (AS 34 – 385), TEV-ProteaseErkennungssequenz Diese Arbeit pGEX-4T2; DDX3-Volllänge (AS 1-662), Thrombin-ProteaseErkennungssequenz pGEX-4T2; DDX3-ATPaseDomäne (AS 1-406), ThrombinProtease-Erkennungssequenz pGEX-4T2; DDX3-HelicaseDomäne (AS 411-662), ThrombinProtease-Erkennungssequenz pGEX-4T2; kristallisierte Domäne von DDX3 (AS 168-580), Thrombin-ProteaseErkennungssequenz pET303; DDX3-Volllänge (AS1-662) Diese Arbeit Diese Arbeit Diese Arbeit YopM (Y.e. 8081) 6x NT-His-TEV-YopM_Full 6x NT-His-TEVYopM_Core Diese Arbeit YopM (Y.p. YpIII) 6x NT-His-TEV-YopM_Full 6x NT-His-TEVYopM_Core Diese Arbeit DDX3 NT-GST-DDX3 NT-GST-DDX3-ATPase NT-GST-DDX3-Helicase NT-GST-DDX3-Crystal 6x CT-His-DDX3 34 Diese Arbeit Diese Arbeit Diese Arbeit Diese Arbeit III Material 6x CT-His-DDX3_Crystal 6x CT-His-DDX3_1-418 6x CT-His-DDX3_51-418 6x CT-His-DDX3_101-418 6x CT-His-DDX3_168-418 6x CT-His-DDX3_201-418 pET303; kristallisierte Domäne von DDX3 (AS 168-580) pET303; DDX3 (AS 1-418) pET303; DDX3 (AS 51-418) pET303; DDX3 (AS 101-418) pET303; DDX3 (AS 168-418) pET303; DDX3 (AS 201-418) Diese Arbeit Diese Arbeit Diese Arbeit Diese Arbeit Diese Arbeit Diese Arbeit III.1.8 Oligonukleotide Tabelle 19: Oligonukleotide Name Sequenz (5´3´) YopM (pET303) YopMpet303for AAATCTAGAATGTATGGTTTTGTTTG C YopMshortNpet303for AAATCTAGAATGTTTATAAATCCAAG A YopMpet303rev GTGCTCGAGCTCAAAAACATCATCT TC YopMpetnoC303rev GTGCTCGAGGTCCATCCGAAGATCT TC YopMLRR6pet303rev GTGCTCGAGTAAGAAGATTAAACTC TG YopMpET303_KSK AAATCTAGAATGAAATCTAAGACTGA ATA pET303_YopMLRR GAGGTCTAGAATGCATGAGCTAGAA _for CTAAAT Länge Besonderheit 27 XbaI 27 XbaI 27 XhoI 27 XhoI 27 XhoI 29 XbaI 31 XbaI 52 EcoRI; TEV 58 EcoRI; TEV 34 BamHI 34 BamHI YopM (pET302) 302TevYopMfor 302TevKSKYopMfor 302TevYopMrev 302TevYopMcorrev CGTGAATTCGGAGAATCTTTATTTTC AGGGCTTTATAAATCCAAGAAATGTA CGTGAATTCGGAGAATCTTTATTTTC AGGGCAAATCTAAGACTGAATATTAT AATGCA ATTCGGATCCCTACTCAAAAACATCA TCTTCAAG ATTCGGATCCTTAGTCCATCCGAAG ATCTTCCAC YopM (pGEX-4T2) 35 III Material pGEX_6P2_YopM_f CTGGGATCCTTTATAAATCCAAGA 24 BamHI pGEX_6P2_YopM_r GCCGAATTCCTACTCAAAAACATCAT C 27 EcoRI DDX3 (pET303) DDX3_for DDX3_51_for DDX3_101_for DDX3_151_for DDX3_168_for DDX3_201_for DDX3_248_for DDX3_303_for DDX3_356_for DDX3_411_for DDX3_419_for DDX3_167_rev DDX3_406_rev DDX3_418_rev DDX3_580_rev DDX3_rev GAGGTCTAGAATGAGTCATGTGGCA GTGG GAGGTCTAGAATGGGTTTCTACGAT AAAGAC GAGGTCTAGAATGCGGAGTGATTAC GATGGC AGGTCTAGAATGTTTTCTGGAGGCA ACACT GAGGTCTAGAATGGTTGAGGCAACA GGCAAC GAGGTCTAGAATGACTCGCCCAACT CCAGTG GAGGTCTAGAATGGGCGAGGCTTT GAGGGCC GAGGTCTAGAATGGCCGATATTGGT CAGCAG GAGGTCTAGAATGGGGTTTGAGCCT CAGATT GAGGTCTAGAATGACCTCTGAAAAC ATCACA GAGGTCTAGAATGGTAGTTTGGGTG GAAGAA TACCCTCGAGTGGAATGTCATCGTA TTT TACCCTCGAGTCCTACAGCCAAGAA GAT TACCCTCGAGTTTCTGTGTGATGTTT TC TACCCTCGAGGTAGTGGTGTTCATA AGC TACCCTCGAGGTTACCCCACCAGTC XbaI 29 XbaI 31 XbaI 31 XbaI 30 31 XbaI 31 XbaI 31 XbaI 31 XbaI 31 XbaI 31 XbaI 31 XbaI XhoI 28 XhoI 28 XhoI 28 28 XhoI 25 XhoI 25 27 EcoRI EcoRI DDX3 (pET302) pET302_DDX3_for pET302_DDX3_51_for GTGAATTCGAGTCATGTGGCAGTGG GTGAATTCGGGTTTCTACGATAAAG AC 36 III Material pET302_DDX3_101_f or pET302_DDX3_151_f or pET302_DDX3_for pET302_DDX3_167_r ev pET302_DDX3_406_r ev pET302_DDX3_418_r ev pET302_DDX3_rev GTGAATTCGCGGAGTGATTACGATG GC GTGAATTCGTTTTCTGGAGGCAACA CT GTGAATTCGAGTCATGTGGCAGTGG GCCGGATCCGATTATGGAATGTCAT CGTATTT GCCGGATCCGATTATCCTACAGCCA AGAAGAT GCCGGATCCGATTATTTCTGTGTGA TGTTTTC GCCGGATCCGATTAGTTACCCCACC AGTC 27 EcoRI 27 EcoRI 25 32 EcoRI BamHI 32 BamHI 32 BamHI CTGGGATCCCCAGGAATTCCCATGA GTCATGTGGCAGTG CTGGGATCCCCAGGAATTCCCGTTG AGGCAACAGGCAACAAC CTGGGATCCCCAGGAATTCCCACCT CTGAAAACATCACACAG GGCCGCTCGAGTTCAGTTACCCCAC CAGTCAAC GGCCGCTCGAGTTTATCCTACAGCC AAGAAGATATA GGCCGCTCGAGTTTAGTAGTGGTGT TCATAAGCCAT 39 BamHI; EcoRI 42 BamHI; EcoRI 42 BamHI; EcoRI 33 XhoI 36 XhoI 36 XhoI 29 DDX3 (pGEX_4T2/6P2) DDX3_for DDX3_168_for DDX3_411_for DDX3_rev DDX3_406_rev DDX3_580_rev 37 III Material III.1.9 Elektronische Datenverarbeitung Tabelle 20: Software Software Adobe Photoshop CS3 ATSAS Suite Biosaxs software CCP4 CLC-Main Workbench COOT GraphPad Prism 5 ImageJ iMOSFLM NTAnalysis Office software pymol UCSF Chymera Hersteller Adobe Systems GmbH, Munich (G) EMBL, Hamburg (G) (Winn et al. 2011) CLC bio, Aarhus (DK) (Emsley et al. 2010) La Jolla (USA) Bethesda (USA) (Battye et al. 2011; Leslie 2006) Nanotemper GmbH, München (G) Microsoft, Redmond, (USA) Schrödinger, Portland (USA) Resource for Biocomputing, Visualization, and Informatics at the University of California, San Francisco, (USA) 38 III Methoden III.2 Methoden Alle mikrobiologischen Arbeiten wurden in Laboren der gentechnischen Sicherheitsstufe 2 (S2) durchgeführt. III.2.1 Mikrobiologische Methoden III.2.1.1 Anzuchtbedingungen Zur Anzucht in Flüssigmedium wurden Y. enterocolitica oder Y. pseudotuberculosis-Stämme aus Glycerinkultur oder von LB-Agarplatte in LB-Medium überführt und bei 27°C schüttelnd inkubiert. Zum Wachstum auf Festmedium wurden die Yersinia-Stämme mit einer sterilen Impföse aus Flüssig- bzw. Glycerinkultur auf Agarplatten ausgestrichen. Alternativ wurden 100 μl einer Flüssigkultur mit einem Drigalski-Spatel ausplattiert. Die Inkubation erfolgte bei 27°C. Zur Anzucht von E. coli wurden 5 ml LB-Medium mit einer einzelnen Kolonie von Platte beimpft und bei 37°C unter Schütteln über Nacht inkubiert. III.2.1.2 Yop Release-Assay Bei Temperaturen von 37°C und unter Ca2+-Mangel können Y. enterocolitica Stämme dazu gebracht werden ihre Yops in den Kulturüberstand abzugeben ohne dass hierfür ein Zellkontakt nötig ist. (Heesemann et al. 1986) Anschließend können die sich im Kulturüberstand befindlichen Proteine isoliert und mittels Trichloressigsäure (TCA) gefällt werden. Eine 27°C Übernachtkultur des entsprechenden Stammes wurde 1:20 in frischem LBMedium verdünnt und bei 37°C für 1,5 h inkubiert. Die Stimulation der Yop-Sekretion erfolgte durch Zugabe von 5 mM EGTA, 0,2 % Glukose und 15 mM MgCl2. EGTA ist ein Chelatbildner für zweiwertige Kationen und sorgt damit für den erforderlichen Ca 2+-Mangel im Kulturmedium. Nach Inkubation für weitere 3 h bei 37°C wurden die Bakterien in 50 ml Zentrifugenröhrchen bei 10000 rpm und 4°C (Sigma 3-18K) pelletiert und der Überstand wurde in ein neues 50 ml Reaktionsgefäß überführt. Die Proteine wurden für eine Stunde auf Eis durch Zugabe von 10 % (v/v) TCA gefällt. Nach erneuter Zentrifugation für 30 min bei 10000 rpm und 4°C wurden die Proteine zweimal in eiskaltem Aceton gewaschen. Ein dritter Waschschritt erfolgte mit ddH2O. Das Pellet wurde anschließend in reduzierendem SDSPAGE Ladepuffer (Tabelle 9) aufgekocht und in einer SDS-PAGE aufgetrennt. III.2.1.3 Stammkonservierung Zur dauerhaften Konservierung der E. coli-Stämme wurden Glycerinkulturen angelegt. Hierzu wurden 0,8 ml LB-Medium mit 40 % (w/v) Glycerol in Cryoröhrchen (Nunc) vorgelegt und jeweils 0,8 ml einer exponentiell wachsenden Flüssigkultur (OD600 = 0,5-0,8) zugegeben. Diese Mischung wurde gevortext, sofort in flüssigem Stickstoff schockgefroren und bei -80°C gelagert. III.2.1.4 Transformation von E. coli Die Möglichkeit E. coli zu transformieren (Sambrook & Russell 2001) stellt die Grundlage für weiterführende Klonierungen dar. Vektorkonstrukte werden in geeigneten E. coli-Stämmen amplifiziert und zur weiteren Analyse in hoher Kopiezahl isoliert. Im Folgenden wurde eine 39 III Methoden abgewandelte Methode zur Transformation von E. coli durch Behandlung mit CaCl2 (Hanahan & Harbor 1983) verwendet. III.2.1.4.1 Herstellung chemisch kompetenter Bakterien 300 ml LB-Medium (in einem 1 l Erlenmeyer-Kolben) wurden mit einem gewünschten E. coli-Stamm beimpft und bis zu einer optischen Dichte von 0,5 bei 600 nm (OD600) schüttelnd inkubiert. Die Kultur wurde anschließend auf Eis gestellt. Nach Zentrifugation für 10 min bei 4°C und 3000 rpm (Sigma 3-18K) wurde das erhaltene Zellpellet in 20 ml kaltem TFB 1 Puffer (Tabelle 6) resuspendiert und für 90 min auf Eis gelagert. Der Ansatz wurde wie oben beschrieben erneut abzentrifugiert und das Pellet wurde in 1,5 ml eiskaltem TFB 2 Puffer (Tabelle 6) resuspendiert. Die Zellsuspensionen wurden zu 100 µl Portionen aliquotiert, in flüssigem N2 schockgefroren und bei -80°C gelagert. III.2.1.4.2 Transformation von E. coli Zur Transformation der kompetenten E. coli-Stämme wurde ein 100 µl Aliquot auf Eis langsam aufgetaut, mit 1-100 ng DNA gemischt und für weitere 10 min auf Eis gestellt. Danach folgte ein Hitzeschock (90 sec, 42°C) zur Aufnahme der DNA in die Zellen. Die Zellen wurden anschließend auf Eis überführt und zu 900 µl sterilem LB-Medium in einem Glasröhrchen pipettiert. Die phänotypische Expression der Resistenz erfolgte durch schüttelnde Inkubation der Kultur für 90 min bei 37°C. Nach der phänotypischen Expression wurden 100 µl der Suspension bzw. geeigneter Verdünnungen auf Selektivagar-Platten plattiert und über Nacht bei 37°C inkubiert. III.2.2 Molekularbiologische Methoden III.2.2.1 Agarose-Gelelektrophorese Zur Auftrennung und zum Sichtbarmachen von DNA-Fragmenten wurde die AgaroseGelelektrophorese verwendet. Die aufgrund der Phosphat-Gruppen negativ geladene DNA bewegt sich hierbei in einem Spannungsfeld von der Kathode zur Anode. Dabei werden DNA-Fragmente aufgrund ihres unterschiedlichen Laufverhaltens je nach Größe sowie Konformation im elektrischen Feld innerhalb einer Agarose-Matrix aufgetrennt. Die Wanderungsgeschwindigkeit ist weiterhin abhängig von der angelegten Spannung (8 V/cm) sowie der Konzentration der eingesetzten Agarose (0,8-2 %). Bei höherer Spannung sowie geringerer Agarosekonzentration bewegen sich Teilchen im Feld schneller. Zur Durchführung wurde die gewünschte Menge Agarose in adäquater Menge 1x TAE-Puffer gelöst und in der Mikrowelle bei 800 W erhitzt bis das Pulver vollständig gelöst war. Danach wurde die mit RedSAFE (HISS Diagnostics, Freiburg, G) Agarose in einen Gelschlitten gegossen, in den ein Kamm eingesetzt war, welcher nach Abkühlung des Gels die Taschen für die spätere Probenapplikation lieferte. Nach Aushärtung des Gels wurde der Schlitten in eine Elektrophorese-Kammer eingesetzt und das Gel mit 1x TAE-Laufpuffer vollständig überschichtet. DNA Proben wurden mit adäquater Menge 6x DNA-Probenpuffer versetzt und in die vorgesehenen Taschen pipettiert. Als Größenstandards diente ein 1 kb DNA-Ladder (GeneRulerTM 1 kb-DNA Ladder, Thermo Fisher, Waltham, USA). Die Elektrophorese wurde bei einer Spannung von 8 V/cm durchgeführt. Zur Sichtbarmachung der DNA wurde das Gel anschließend auf einem Transilluminator (ChemiDoc XRS, BioRad, München, G) gelegt. 40 III Methoden Hierbei macht man sich die Fluoreszenz-Eigenschaften (309nm/419nm) des an die DNA bindenden REDSafe-Farbstoffs zunutze. Die verwendeten Puffer sind Tabelle 9 zu entnehmen. III.2.2.1 Konzentrationsbestimmung von DNA Die Konzentrationsbestimmung von DNA basiert auf dem Absorptionsmaximum der Nucleinsäuren bei 260 nm. Für die Absorption sind dabei die aromatischen Ringe der Basen verantwortlich. Die Absorption eines 1 µl Tropfens wurde hierbei im NanoDrop (ND-1000 peqlab, Erlangen, G) photometrisch gemessen. Eine Lösung die 50 ng doppelsträngige DNA beinhaltet erhält hierbei den Absorptionswert 1. Die Konzentration eventuell noch vorhandener Proteine oder Phenol wird bei 280 nm Wellenlänge gemessen. Der Quotient der Absorption OD260/OD280 bestimmt hierbei die Reinheit der Lösung und sollte für DNA idealerweise zwischen 1,8 und 2 liegen. III.2.2.2 Isolierung von Plasmid-DNA Plasmid DNA wurde mithilfe des ZR Plasmid Miniprep-Classic Kits (Zymo Research, Irvine, USA) laut Anleitung aufgereinigt. III.2.2.3 Polymerase-Kettenreaktion (PCR) Die Polymerase-Kettenreaktion ist eine einfache Methode zur Amplifikation von kurzen DNAFragmenten (Saiki et al. 1988). Eine thermostabile DNA-Polymerase amplifiziert hierbei einen Teil einer DNA-Sequenz, der durch zwei Oligonukleotide (Primer) begrenzt wird. Eine PCR besteht typischerweise aus drei Schritten. Zunächst wird die doppelsträngige DNA durch hohe Temperaturen (95-98°C) aufgeschmolzen (Schritt 1: Denaturierung), bevor sich in einem zweiten Schritt durch Herabsetzen der Temperatur Primer an die komplementären Stellen der DNA anlagern können (Schritt 2: Annealing). Die sogenannte AnnealingTemperatur der Oligonukleotid-Primer ist dabei abhängig von GC-Gehalt sowie Länge der Primer. Anschließend erfolgt eine 5´ 3´ gerichtete Verlängerung der Oligonukleotide komplementär zu der als Matrize dienenden Template-DNA (Schritt 3: Elongation). Die Elongationstemperatur richtet sich nach dem thermodynamischen Wirkungsoptimum des verwendeten Enzyms und liegt bei den üblichen aus Thermus aquaticus isolierten Polymerasen bei 72°C. Durch 30-35 fache Wiederholung dieser Schritte erhält man somit eine hohe Anzahl an Kopien des ursprünglichen Templates. Die Länge des PCR-Produkts wird durch die Primer bestimmt, die an den gegenläufigen Enden der DNA lokalisiert sind. Die Auswahl der verwendeten Primerpaare folgte den von Newton und Graham (1994) aufgestellten Regeln, welche GC-Gehalt, Länge sowie Basenverteilung beinhalten. Die Schmelztemperatur der beiden Primer eines Paares sollte annähernd gleich sein. Für die in dieser Arbeit durchgeführten Reaktionen wurden je nach Zweck zwei verschiedene DNA-Polymerasen verwendet. Für rein analytische Ansätze, bei denen lediglich das Vorhandensein eines bestimmten DNABereichs nachgewiesen werden sollte, wurde die GoTaq® DNA-Polymerase (Promega, Fitchburg, USA) verwendet. Diese Polymerase besitzt keine Korrekturlesefunktion (3´ 5´ Exonuklease), wodurch es zu einer Fehlerhäufigkeit (statistische Fehlpaarung von Basen) von 8 x 10-6 kommt. Ein Standardansatz für diese Polymerase lautet wie folgt: 41 III Methoden Tabelle 21: PCR-Ansatz GoTaq® Komponente Konzentration Volumen DNA-Template oder Kolonie ® GoTaq -Reaktionspuffer forward primer reverse primer dNTPs Taq-Polymerase ddH2O 100 ng/µl 5x 10 pmol/µl 10 pmol/µl 10 mM 5 units/µl 1 µl 10 µl 1 µl 1 µl 2 µl 0,25 µl ad 50 µl Tabelle 22: PCR-Programm GoTaq® Schritt Temperatur Dauer Zyklen 1. Initiale Denaturierung (colony PCR) 95 °C 3 min (5 min) 1 2. 3. 4. 5. 95 °C Tm -5°C 72 °C 72 °C 30 s 30 s 1 kb DNA/min 5 min 4 °C ∞ Denaturierung Annealing Elongation Finale Elongation 6. Pause 30-35 1 1 Bei der Herstellung von PCR-Produkten für Klonierungen bzw. für gezielte Mutagenese war 33-37 eine möglichst niedrige Fehlerrate erforderlich. Aus diesem Grund wurde für präparative Zwecke die Phusion High-fidelity DNA Polymerase (Thermo Scientific, Waltham, USA) verwendet, welche eine Korrekturlesefunktion besitzt. Mit ihr ist eine etwa 50-fach höhere Genauigkeit (4,4* 10-7) beim Nukleotid Einbau zu erreichen. Zusätzlich hat sie eine höhere Amplifikationsrate pro Zeit und kann längere Produkte liefern. Sie bildet im Gegensatz zur Taq-Polymerase Blunt Ends. Ein Standardansatz für diese Polymerase lautet wie folgt: Tabelle 23: PCR-Ansatz Phusion-Polymerase Komponente Konzentration Volumen DNA-Template Phusion HF Reaktionspuffer forward primer reverse primer dNTPs Phusion-Polymerase ddH2O 100 ng/µl 5x 10 pmol/µl 10 pmol/µl 10 mM 5 units/µl 1 µl 10 µl 1 µl 1 µl 2 µl 0,25 µl ad 50 µl 42 III Methoden Tabelle 24: PCR-Programm Phusion Schritt Temperatur Dauer Zyklen 1. Initiale Denaturierung 98 °C 2 min 1 2. 3. 4. 5. 98 °C Tm +3°C 72 °C 72 °C 10 s 20 s 1 kb DNA/15 s 5 min 4 °C ∞ Denaturierung Annealing Elongation Finale Elongation 6. Pause 30-35 1 1 III.2.2.4 Aufreinigung von DNA 33-37 Die Aufreinigung von DNA, insbesondere von PCR-Produkten oder Plasmiden, ist wichtig um diese von restlichen Puffern, Lösungen oder Proteinverunreinigungen, die weitere Experimente behindern könnten, zu befreien. Zur direkten Aufreinigung von PCR-Produkten wurde das „Nucleo Spin Extract II“ Kit (Macherey-Nagel, Düren, G) nach Herstellerangaben verwendet. Zur Aufreinigung von PCR-Produkten aus Agarosegelen wurden Gele mit ausreichend großen Taschen hergestellt, die einen Gesamtansatz von 50-100 µl fassen. Auf das Agarosegel wurde eine geeignete DNA-Leiter und der gesamte Reaktionsansatz aufgetragen, wobei 1 µl von diesem in eine benachbarte Tasche pipettiert wurde. Die Elektrophorese erfolgte bei geringer Voltzahl um eine gute Auftrennung der DNA-Banden zu gewährleisten. Um die DNA der zu eluierenden Probe nicht durch UV-Einwirkung zu beschädigen wurde diese abgeschnitten. Nach Färbung des restlichen Gel-Fragmentes mit DNA-Leiter und Probenspur im RED Safe-Bad wurde unter UV-Licht der Bereich der gewünschten Bande mit dem Skalpell markiert. Nach Zusammenlegen der Teile wurde die entsprechende Laufhöhe aus der Probenspur ausgeschnitten und mit dem „Nucleo Spin Extract II“ Kit (Macherey-Nagel, Düren, G) gemäß Anleitung aufgereinigt. III.2.2.5 Restriktionsverdau von DNA Zur Subklonierung von PCR-Produkten in Expressionsvektoren wurden zunächst mittels PCR spezifische Schnittstellen in die zu klonierenden DNA-Fragmente eingeführt. Die korrespondierenden Schnittstellen fanden sich ebenso in dem gewählten Zielvektor. Die Restriktion erfolgte mittels FastDigest® Restriktionsendonukleasen (Thermo Fisher, Waltham, USA) nach Herstellerangaben in einem Wasserbad (GFL Typ 1013, GFL, Burgwedel, G)oder im Thermocycler (Primus-96, MWG-Biotech, Ebersberg, G). Die erhaltenen Produkte wurden mittels Agarosegelelektrophorese (2.2.1) aufgetrennt und aufgereinigt (2.2.4). III.2.2.6 Ligation Zur Ligation von DNA-Fragmenten wurde die T4-DNA-Ligase (1U/µl; Roche, Mannheim G) verwendet. Diese verknüpft freie 3´-OH Gruppen mit 5´-Phosphatgruppen unter Bildung einer Phosphodiesterbindung. Die verwendeten mit BamHI, EcoRI, XhoI, XbaI und HindI geschnittenen DNA-Fragmente und Vektoren verfügten über kohäsive Enden und wurden daher meist in äquimolaren Mengen eingesetzt (je ca. 0,09 pmol). Es wurde jeweils 1 µl der Ligase in dem mitgelieferten Puffer eingesetzt und bei 16-20°C über Nacht ligiert. Die bei der Ligation eingesetzten DNA-Mengen wurden mit nachfolgender Formel bestimmt: ng (Vector) x kb (Insert) ng (Insert) = kb (Vector) x molar ratio (Vector/Insert) 43 III Methoden III.2.2.7 Hersellung der in dieser Arbeit verwendeten Konstrukte Zur heterologen Expression von Y. enterocolitica WA-314 GST-YopM in E.coli BL21 RIL wurde das Zielgen aus dem aufgereinigten Virulenzplasmid pyV-WA314 (Accession number: FR687019) mittels PCR amplifiziert und über die Schnittstellen für BamHI und EcoRI in den Zielvektor pGEX-4T2 ligiert. YopM Konstrukte, die einen abspaltbaren 6x His-Tag tragen, wurden kreiiert, in dem das jeweilige Zielgen mittels PCR aus den Virulenzplasmiden pyVWA314 (Accession number: FR687019), pYPIII (nicht vollständig sequenziert) bzw. pYVe8081 (Accession number: NC_008791) amplifiziert wurde. Die verwendeten Primer trugen die für die Klonierung benötigten Schnittstellen EcoRI und BamHI. Zusätzlich wurde in den Vorwärts-Primer eine Sequenz „in frame“ eingebaut, die für die TEV-ProteaseErkennungssite ENLYFQG codiert. Das jeweilige PCR-Produkt wurde dann wie unter 2.2.42.2.6 beschrieben in den Zielvektor pET302 eingebracht. Zur Klonierung von YopM Konstrukten in pET303 wurden die Schnittstellen XhoI und XbaI mittels PCR aus pyVWA314 eingebracht und wie unter 2.2.4-2.2.6 beschrieben weitergeführt. DDX3-Konstrukte wurden durch Amplifikation aus humaner cDNA (Accession number: NM_001356) generiert. Die Klonierung in die Zielvektoren erfolgte äquivalent zu den beschriebenen YopM-Konstrukten. Eine vollständige Liste aller verwendeteten Konstrukte und der benutzten Oligonukleotide findet sich in Tabelle 18 und Tabelle 19. III.2.2.8 DNA-Sequenzierung DNA Sequenzierungen wurden von der Firma Seqlab (Göttingen, G) laut deren Standardprotokollen durchgeführt. Die Sequenzen wurden mit dem Programm CLC Workbench (CLC bio, Aarhus, DK) analysiert. III.2.3 Biochemische Methoden III.2.3.1 Heterologe Genexpression in E. coli Seit den Entdeckungen von Herbert Boyer und Stanley N. Cohen zur Klonierung und Expression fremder Gene in E. coli 1974 (Cohen et al. 1972; Cohen et al. 1973) und der erstmaligen Produktion eines humanen Proteins (Somatostatin) durch die Firma Genetech 1974 ist die heterologe Genexpression eine Standardprozedur zur Untersuchung der Funktion und biochemischen Eigenschaften eines Proteins. Sie stellen eine der Grundlagen moderner biochemischer Arbeiten dar. Für die Expression der in dieser Arbeit untersuchten Proteine wurden im Wesentlichen die Stämme E. coli BL21 AI und BL21 RIL benutzt (siehe Tabelle 14). Der grundlegende Ablauf wird im Folgenden beschrieben. Zunächst wurde eine Übernachtkultur des entsprechenden Stammes angesetzt. Hierzu wurden 25 ml LB-Medium mit Ampicillin (100 µg/ml) entweder aus einem Glycerolstock oder von einer Agarplatte mit einer Kolonie beimpft. Die Vorkultur wurde bei 200 rpm und 37°C über Nacht (ca. 16 h) inkubiert. Für die Expressionskultur wurde 1 l LB-Medium mit Ampicillin (100µg/ml) 1:40 aus der Übernachtkultur beimpft und schüttelnd (200 rpm 37°C) bis zu einer optischen Dichte bei 600 nm (OD600) von 0,5-0,8 inkubiert. Nach Induktion der Proteinexpression mit 0,5-1 mM IPTG (BL21 AI; BL21 RIL) und 0,2 % (w/v) L-Arabinose (BL21 AI) wurde entweder für weitere 4 h bei 37°C inkubiert oder die Kultur wurde auf 16°C heruntergekühlt und über Nacht weiterinkubiert. Der Temperaturshift sollte der Verhinderung der Bildung von “Inclusion Bodies” dienen und damit die Löslichkeit des Zielproteins 44 III Methoden erhöhen. Zur Zellernte wurde die Bakteriensuspension für 10 min bei 6000 rpm und 4°C (Sorvall RC 5B, Rotor GS-3) pelletiert und bis zur Proteinaufreinigung bei -20°C gelagert. III.2.3.2 Zellaufschluss von E.coli Ultraschall mit hoher Energie (hoher Amplitude) erzeugt in Flüssigkeiten kleine Blasen, die zunächst größer werden und dann implodieren. Diese rasch wechselnden Druckänderungen bewirken ein Zerreißen der Membranen und Zellwände beschallter Zellen. Mit Ultraschall kann also ohne Zusatz von Detergenzien oder Enzymen innerhalb von Sekunden ein schneller Zellaufschluss erreicht werden. Da bei diesem Verfahren viel Wärme freigesetzt wird, erfolgte die Ultraschallbehandlung auf Eis. Zum Aufschluss der Zellen wurde das aus 2.2.1 erhaltene Bakterienpellet in entsprechendem Volumen PBS (bei GST-Fusionsproteinen) oder His-Lysepuffer (Bei 6 xHisFusionsproteinen) (siehe Tabelle 7) resuspendiert und zu 5 ml Portionen in 50 ml Zentrifugenröhrchen aliquotiert. Die Suspension wurde 5-10x bei einer Amplitude von 2040 % in einem Branson Sonifier (Digital Sonifier 250-D, Branson, Danbury, USA) beschallt, bis die Zellsuspension klar wurde (sie wirkt opaleszierend). Im Zweifelsfall erfolgte eine mikroskopische Kontrolle der Lyse. Um das Lysat von Zellbestandteilen zu trennen wurde die Suspension für 30 min bei 20.000 g bei 4°C zentrifugiert (Sigma centrifuge 3-18K, Sigma, Osterode, G). III.2.3.3 Proteinaufreinigung III.2.3.3.1 Imobilisierte Metallaffinitätschromatographie Immobilisierte Metallaffinitätschromatographie (IMAC) wurde das erste mal 1975 von Porath und Kollegen (Porath et al. 1975) zur Auftrennung von Proteinen beschrieben und seitdem für die Aufreinigung einer großen Anzahl von Proteinen verwendet (Sulkowski 1985). Kernpunkt der Technik ist die Bindung des Imidazolrings der Aminosäure Histidin an zweiwertige Kationen wie Co2+, Ni2+, Cu2+ oder Zn2+. Zur Aufreinigung von 6x His-getagten Proteinen wurde Ni-NTA Agarose (Qiagen, Hilden, G) und Einweg-Polypropylensäulen (1 bzw 5 ml, Qiagen, Hilden, G) verwendet. Zunächst wurde die Ni-NTA-Agarose mit fünf Säulenvolumen (column volume, cv) His-Lysepuffer äquilibriert. Die Menge verwendeter Matrix richtete sich nach der erwarteten Proteinmenge (5-10 mg Protein/ 1 ml Ni-NTA-Matrix). Nach Bindung des im Rohextrakt aus 2.3.2 enthaltenen Proteins durch einfachen Schwerkrafts-Durchfluss, wurde die Matrix zweimal mit fünf cv Waschpuffer gespült. Die geringe Imidazolkonzentration im His-Waschpuffer diente hierbei der Verdrängung von unspezifisch gebundenen Proteinen. Final erfolgte die Elution des Zielproteins mit 2-3 cv Elutionspuffer, welcher 250 mM freies Imidazol beinhaltete. Alle Aufreinigungsschritte wurden bei 4°C bzw. auf Eis durchgeführt. Die verwendeten Puffer und Lösungen sind Tabelle 7 zu entnehmen. III.2.3.3.2 GST-Aufreinigung Das Prinzip der Aufreinigung von Proteinen die einen GST-Tag besitzen beruht auf der hohen Affinität der mit dem Zielgen fusionierten Glutathion-S-Transferase (GST) aus Schistosoma japonicum zu Glutathion (Smith & Johnson 1988). Alle Aufreinigungsschritte wurden bei 4°C bzw. auf Eis durchgeführt. Zur Aufreinigung von GST-getaggten Proteinen wurde eine Glutathion-Sepharose 4B Matrix (GE Healthcare, St Gilles, UK) und Einweg-Polypropylensäulen (1 bzw 5 ml, Qiagen, Hilden, G) verwendet. 45 III Methoden Zunächst wurde die Glutathion-Sepharose mit fünf Säulenvolumen (column volume, cv) PBS äquilibriert. Die Menge verwendeter Matrix richtete sich nach der erwarteten Proteinmenge (ca. 5 mg Protein/ 1 ml Ni-NTA-Matrix). Nach Bindung des im Rohextrakt aus 2.3.2 enthaltenen Proteins durch schwenkende Inkubation für 1 h bei 4°C, wurde die Matrix zweimal mit fünf cv PBS gespült. Final erfolgte die Elution des Zielproteins mit 2-3 cv GSTElutionspuffer, welcher 30 mM reduziertes Glutathion beinhaltete. Die verwendeten Puffer und Lösungen sind Tabelle 7 zu entnehmen. III.2.3.3.3 Anionenaustauschchromatographie Die Ionenaustauschchromatographie (Ion exchange chromatography, IEX) ist seit den 1960er Jahren eine etablierte Methode zur Trennung von Biomolekülen. Das Prinzip beruht auf der Trennung von Partikeln aufgrund ihrer Netto-Oberflächen-Ladung. Jedes Protein hat aufgrund seines unterschiedlichen Anteils an ionisierbarer Aminosäuren ein anderes pHLadungsverhältnis. Aufgrund dieser Eigenschaft und der daraus resultierenden unterschiedlich starken Interaktion der Moleküle mit einer geladenen Matrix bei definiertem pH, lassen sich Proteine mit dieser Methode sehr gut aufreinigen. Für die Aufreinigung von YopM wurde das aus der Ni-NTA Aufreinigung (2.3.3.1) erhaltene Protein gegen ein adäquates Volumen Anionenaustauschpuffer A über Nacht bei 4°C dialysiert. Verwendet wurde eine UnoQ6-Säule der Firma Biorad (Berkeley, USA) mit einem ÄKTA FPLC-System (GE Healthcare, St Gilles, UK). Bei dem Säulenmaterial handelt es sich um einen starken Anionenaustauscher (-N+(CH3)3). Zunächst wurde die Säule abwechselnd mit je fünf Säulenvolumen Puffer A und Puffer B gespült, bevor mit fünf cv Puffer A äquilibriert wurde. Die Flussrate wurde über den gesamten Lauf konstant auf 2 ml/min gehalten. Nach Applikation der Probe wurde mit fünf cv Puffer A gespült um unspezifisch gebundene Proteine von der Säule abzuwaschen. Die Elution erfolgte in zwei linearen Gradienten mit Anionenaustauschpuffer B, der 1 M NaCl enthielt. Der erste Gradient (0-50 % Puffer B) lief über 15 Säulenvolumen, gefolgt von dem zweiten Gradienten (50-100 % Puffer B) über sechs Säulenvolumen. Die Sammlung des Eluats erfolgte in 2 ml Fraktionen während des ersten Gradienten. Anschließend wurde die Säule mit fünf cv Puffer B gespült, bevor sie entweder erneut in Puffer A äquilibriert oder mit je fünf cv ddH2O und 20 % Ethanol zur Lagerung bei 4°C gewaschen wurde. III.2.3.3.4 Größenausschlusschromatographie Bei der Größenausschlusschromatographie oder auch Gelfiltration genannten Methode werden Moleküle nach ihrer Größe bzw. ihrem hydrodynamischen Volumen aufgetrennt, während sie durch ein poröses Medium wandern, welches in einem definierten Volumen in eine Säule gepackt ist. Der Trennungseffekt beruht hierbei auf den unterschiedlichen Diffussionsvolumina verschieden großer Partikel. Die poröse Matrix erlaubt es kleineren Partikeln einzudringen, was ihre Retentionszeit im Vergleich zu größeren Spezies verlängert. Für analytische Gelfiltrationen wurde eine Superdex 200 10/300 GL, für präparative Aufreinigung eine HiLoad 16/600 Superdex 200 pg (beide GE Healthcare, St Giles UK) verwendet. Zunächst wurde die entsprechende Säule mit zwei cv ddH2O gespült, bevor sie mit weiteren zwei cv des Reinigungspuffers äquilibriert wurde. Welcher Puffer verwendet wurde, richtete sich nach dem aufzureinigenden Protein. Dies ist Tabelle 7 zu entnehmen. Vor der Aufreinigung eines gewünschten Proteins erfolgte ein Lauf mit einem geeigneten Größenstandard (siehe Tabelle 3) und das Ausschlussvolumen der Säule wurde mittels 46 III Methoden Blue-Dextran, welches eine molekulare Masse von 2000 kDa besitzt bestimmt. Zur Größenbestimmung einer unbekannten Probe wurde das Verhältnis des Elutionsvolumens der Probe (Ve) zum Ausschlussvolumen (Vo) der Säule mit den bekannten Markerproteinen verglichen. Das applizierte Probenvolumen entsprach maximal 2 % des Säulenvolumens. Die Flussraten lagen bei 0,4 ml/min (Superdex 200 10/300 GL) bzw. 1 ml/min (HiLoad 16/600 Superdex 200 pg) Molekulargewicht [Da] 10 6 Thyroglobulin -globulin 10 5 Ovalbumin Myoglobin 10 4 Vitamin B 12 3 10 1.0 1.5 2.0 2.5 Ve /Vo Abbildung 9: Kalibrierungsgerade Superdex 200 10/300 GL. Die Abbildung zeigt die Eichgerade der Säule Superdex 200 10/300 GL, die sich aus Proteinen bekannten -4,967x Molekulargewichts ergibt. Mit der daraus resultierenden Formel: y = 3E+08e lässt sich das Molekulargewicht einer unbekannten Probe errechnen. III.2.3.3.5 Aufreinigung der Tobacco Etch Virus-Protease 6x His-TEV-Protease (Tropea et al. 2009) wurde wie beschrieben überexprimiert (2.3.1), die Zellen wurden sonifiziert (2.3.2) und das Protein wurde wie unter 2.3.3.1 und 2.3.3.4 beschrieben mittels Ni-NTA Aufreinigung und Gelfiltration aufgereinigt. Anschließend wurde die Protease mit einem Vivaspin®- Zentrifugenfilter (GE-Healthcare Europe, München, G), auf 2-5 mg/ml ankonzentriert und mittels flüssigem Stickstoff schockgefroren. Die Lagerung des Enzyms erfolgte bei -80°C. III.2.3.3.6 Proteinverdau mittels TEV TEV-Protease wurde benutzt, um den His-Tag eines Proteins zu entfernen. Hierzu wurde zwischen His-Tag und Protein die Erkennungssequenz ENLYFQG eingebracht. Die Protease schneidet am Glutamin und hinterläßt ein nicht natives Glycin am Zielprotein. Das zu schneidende Protein wurde gegen TEV-Reaktionspuffer (sieheTabelle 7) dialysiert und TEVProtease wurde in einem molaren Verhältnis von 1:100 hinzugefügt. Die Reaktion erfolgte typischerweise bei 4°C über Nacht. Am nächsten Tag wurde das Proteingemisch mit einer geeigneten Menge Ni-NTA-Sepharose für 30 min inkubiert, um ungeschnittenes Protein sowie die Protease abzutrennen. III.2.3.4 Bestimmung der Proteinkonzentration Die Konzentrationsbestimmung von Proteinen basiert auf dem Absorptionsmaximum der aromatischen Aminosäuren (Phenylalanin, Tryptophan und Tyrosin) bei 280 nm. Der hierfür benötigte spezifische Absorptionskoeffizient sowie das theoretische Molekulargewicht des Zielproteins wurde mittels ProtParam (Gasteiger et al. 2005) bestimmt. Hierbei wurde die 47 III Methoden Aminosäuresequenz des Zielproteins benötigt. Die Absorption der Proteinlösung wurde an einem Nanodrop 1000 (Peqlab, Deutschland) bestimmt. Zur Messung wurden jeweils 2 µl Probe eingesetzt. Zusammen mit dem Molaren Extinktionskoeffizienten (M-1cm-1) und dem Molekulargewicht des Proteins kann auf der Grundlage des Lambert-Beer´schen-Gesetzes die Konzentration der Proteinlösung bestimmt werden. E = ελ*c*d E: gemessene Extinktion ελ: molarer Extinktionskoeffizient c: Konzentration der Protein Lösung d: Schichtdicke des durchstrahlten Körpers III.2.3.5 SDS-Polyacrylamid-Gelelektrophorese (SDS-PAGE) Die SDS-PAGE ist eine schnelle, hochauflösende Methode zur Auftrennung von Proteingemischen nach ihren Molekulargewichten (Laemmli 1970). Die meisten Proteine binden das anionische Tensid SDS zu negativ geladenen SDS-Protein-Komplexen mit konstantem Ladungs- zu Masse-Verhältnis (1,4 g SDS/g Protein in 1% SDS-Lösung). SDS denaturiert dabei die Proteine – besonders nach Reduktion mit Mercaptoethanol und unterbindet Protein-Protein Wechselwirkungen. Das Gel wirkt als Molekularsieb, welches die Proteine aufgrund unterschiedlicher Größe unterschiedlich schnell passieren können. So kommt es zu einer Auftrennung. Die Porengröße kann durch unterschiedliche Mengen an Acrylamid und Bisacrylamid variiert werden. In der SDS-Gelelektrophorese werden zwei Arten von Gelen kombiniert. Das Sammelgel mit einem Tris-HCl Puffer System (pH 6,8) ist weitporig (4 %) und dient der Konzentration der Probe. Glycinat-Ionen, die als Zwitterionen vorliegen (Gly+/-) dienen als Folge-Ionen, Chlorid-Ionen dienen als Leit-Ionen, da sie schneller als die Glycinat-Ionen zum positiven Pol wandern. Zwischen diesen beiden Ionenarten bewegen sich die Proteine und gelangen gemeinsam an das Trenngel. Das Trenngel (Tris-HCl Puffer System pH 8,8) ist engporig (7,5 % - 16 %) und trennt die Proteine auf. Beim pH-Sprung von Sammel- auf Trenngel entstehen Glycinat-Anionen, die sich zu den Chlorid-Ionen orientieren und ebenfalls schnell zur Anode laufen. Die Proteine können sich so nach ihrer Größe auftrennen. Die Zusammensetzung der Gele ist Tabelle 10 zu entnehmen. Zur Analyse von Proteinproben wurden diese mit SDS-PAGE Ladepuffer (Tabelle 9) versetzt und bei 96°C für 10 min denaturiert, bevor sie auf das Gel aufgetragen wurden. Die angelegte Spannung betrug 80 V während der Einlaufphase in das Sammelgel und 120150 V während der Trennungsphase. III.2.3.6 Coomassie-Färbung von SDS-Gelen Für die Sichtbarmachung und zur Fixierung der Proteine wurde das Sammelgel entfernt und das Trenngel für 1 h in Coomassie Färbelösung schüttelnd inkubiert. Anschließend wurde das Gel über Nacht, mindestens aber für 2 h in Coomassie Entfärbelösung entfärbt, bis der Hintergrund klar und die Proteinbanden deutlich blau zu erkennen waren. Zur Dokumentation wurde das Gel gescannt und mithilfe des Gel dryer 543 (BioRad, München, G) getrocknet. Die Puffer sind Tabelle 9 zu entnehmen. 48 III Methoden III.2.3.7 Western Blot Beim Western Blot werden die Proteine eines nativen oder eines SDS-Gels elektrophoretisch auf eine adsorbierende Membran aus Polyvinylidendifluorid (PVDF, Immobilon, Millipore, Darmstadt, G) übertragen. Benutzt wurde die Halbtrockenzelle OWL HEP-1 (Thermo Scientific, Rockford, USA). Zunächst wurden drei Filterpapiere (190 g/m2, Hartenstein, Würzburg, G) in Transferpuffer (Tabelle 9) getränkt und auf der Kathode platziert. Das SDS-Gel wurde mit ddH2O abgewaschen und auf die Filterpapiere gelegt. Die PVDF-Membran wurde kurz in Methanol geschwenkt und luftblasenfrei auf das Gel gebettet. Abgedeckt wurde dieses „Sandwich“ wiederum mit drei in Transferpuffer geschwenkten Filterpapieren. Die Kammer wurde verschlossen und der Transfer der Proteine erfolgte mit 1.2 mA/cm2 for 1-1.5 h je nach Größe der gewünschten Proteinbande. Vor der weiteren Reaktion des Blots mit HisProbe™HRP (Thermo Scientific, Rockford, USA) wurden die restlichen freien Proteinbindungsstellen der Membran mit 25 mg BSA/ml in TBST für mindestens 1 h geblockt. Zur Bindung des HisProbe™-HRP wurde eine 4 mg/ml Stammlösung 1:2500 in TBST verdünnt und der Blot wurde damit für 1 h bei 4°C schüttelnd inkubiert. Nach vier-maligem Waschen mit jeweils 15 ml TBST wurde die Membran je nach Proteinmenge mit SuperSignal West Femto/ Pico nach Herstellerangaben inkubiert. Die Detektion des emmitierten Lichts erfolgte mittels Röntgenfilmen (Super RX, Fuji medical X-ray film, Fujifilm, Tokyo J), die in einem Curix 60, (Agfa, Mortsel, B) entwickelt wurden. III.2.3.8 Caspase-1 Assay Die Cystein Protease Caspase-1 (Interleukin-1β converting enzyme, ICE) spaltet proteolytisch Proenzyme, wie pro-Interleukin-1β, an der Erkennungssequenz YVAD (Thornberry & Molineaux 1995). Zur Untersuchung eines postulierten inhibitorischen Effektes von YopM auf Caspase-1 wurde ein colorimetrischer Assay durchgeführt. Hierzu wurde das kommerzielle Peptid Ac-YVAD-pNA (Enzo Life Science, Farmingdale, USA) eingesetzt. Der nach der Prozessierung eintretende Farbumschlag wurde photometrisch in einem Microplate Reader (Infinite M200, TECAN, Männedorf, CH) bei 405 nm gemessen. Zu 10 bzw. 50 U Caspase-1 (Enzo Life Science, Farmingdale, USA) in Caspase 1 Puffer (Tabelle 13) wurden 200 µM des Substrats gegeben und die Reaktion wurde für 60 min bei 37°C aufgezeichnet. Zur Analyse der Inhibition von Caspase-1 wurden je 5 bzw. 50 µM YopM aus Y. enterocolitica WA-314, Y. enterocolitica 8081 und Y. pseudotuberculosis YpIII hinzugefügt. Als Kontrolle diente der kommerzielle Inhibitor Z-Val-Ala-DL-Aspfluoromethylketone (BACHEM, Bubendorf, CH). III.2.3.8 GST-Pulldown Zur Analyse der Interaktion von YopM und DDX3 diente der sogenannte GST-PulldownAssay. Hiezu wurde zunächt wie unter III.2.3.3.2 beschrieben GST-YopM sowie GST aufgereinigt und über Nacht in PBS dialysiert. DDX3-Proteine, die einen 6x His-Tag beinhalteten, wurden wie unter III.2.3.1 beschrieben exprimiert. Die aus 5 ml Expressionskultur erhaltenen Bakterienpellets wurden in 1 ml MBP Column Buffer resuspendiert und die Zellen wurden wie unter III.2.3.2 beschrieben aufgeschlossen. Die Lysate wurden mittels SDS-PAGE aufgetrennt und mittels Western Blot analysiert (III.2.3.5; III.2.3.7). Mit Hilfe des HisProbe™-HRP (Thermo Scientific, Rockford, USA) Antikörpers 49 III Methoden wurde die Qualität der Proteine überprüft und die einzusetzende Menge für den Versuch bestimmt. Bevor die GST-Fusionsproteine an die Glutathion-Matrix (Glutathione Sepharose 4B, GE Healthcare, Uppsala, S) binden konnten, musste diese äquilibriert werden. Hierzu wurden je 75 µl Beads in 1,5 ml Eppendorf Reaktionsgefäße überführt und 4x mit je 1 ml PBS gewaschen. Zwischen den Waschschritten erfolgte jeweils ein Zentrifugationsschritt bei 4°C und 500 x g für 3 min (5810R, Eppendorf, Hamburg, G) Anschließend wurden jeweils 40 µg GST-YopM oder GST bei 4°C unter ständigem invertieren für 2 h an die Beads gebunden. Nach vier weiteren Waschschritten mit PD-Bindepuffer, wie oben beschrieben, wurden die Beads mit den vorher analysierten His-Lysaten über Nacht bei 4°C inkubiert. Am nächsten morgen wurden die Beads viermal mit je 1 ml PD-Waschpuffer gewaschen und in jeweils 40 µl SDS-PAGE Ladepuffer für 5 min aufgekocht. Die Proben wurden dann wie unter III.2.3.5 und III.2.3.7 beschrieben analysiert. Die Zusammensetzung der eingesetzten Puffer ist Tabelle 11 zu entnehmen. III.2.3.9 Kd Bestimmung mittels Thermophorese (MST) Das Prinzip der „Microscale Thermophoresis“ (MST) basiert auf der direkten Bewegung von Biomolekülen entlang eines Temperaturgradienten, der Thermophorese genannt wird (Wienken et al. 2010). Eine lokale Temperaturveränderung ΔT führt zu einer lokalen Änderung der Konzentration (Erhöhung oder Erniedrigung) eines Biomoleküls welche durch den Soret-Koeffizienten quantifiziert wird. ( ) Die thermophoretischen Eigenschaften eines Moleküls beruhen hierbei auf dessen Größe, Ladung sowie der Hydrathülle. Kleinste Änderungen eines dieser Parameter durch Interaktionen mit anderen Biomolekülen können hierbei detektiert werden. Folgende Formel beschreibt diesen Umstand: ST = ST : A: A 2 eff Shyd T * DH kT 4 0T Soret-Koeffizient Moleküloberfläche 2 eff : effektive Ladung Shyd : Hydrationsentropie der Molekül/Lösungsmitteloberfläche DH : Debye Hueckel Länge : Dielektrische Konstante Temperaturableitung : Die Messung der Thermophorese wurde in einem Monolith NT.115 der Firma Nanotemper (München, G) in Standardkapillaren durchgeführt. Zunächst wurde das gewünschte Protein mit einem Fluoreszenz-Tag markiert (Monolith™ NT.115 Protein Labeling Kit RED-NHS), welcher die Detektion der Moleküle durch das Gerät erlaubte. Während der Messung wurde mit Hilfe eines Lasers ein Hitze-Impuls von 30 sec appliziert und das 50 III Methoden Thermophoreseverhalten der Probe wurde aufgezeichnet. Ein potentieller Bindungspartner wurde in 16 Verdünnungen zum gelabelten Protein titriert und Änderungen des Thermophoreseverhaltens wurden untersucht. Hierbei detektiert das MST-Signal eine Bindung durch die Quantifizierung der Änderung der normalisierten Fluoreszenz (Amplitude des MST Signals) Bezeichnet den Anteil gelabelter Moleküle, die in einer Bindung vorliegen, berechnet sich die Änderung der Fluoreszenz in Abhängigkeit der Konzentration des Zielmoleküls wie folgt (Jerabek-Willemsen et al. 2011): ( ) ( ) ( ) ( ) der normalisierten Fluoreszenz ungebundener Hierbei entspricht ( ) beschreibt die normalisierte Fluoreszenz der gelabelter Moleküle, Komplexe (gelabelte Moleküle gebunden an ihre Bindungspartner in Sättigung). Unterschiede in diesen beiden Werten erlauben die Bestimmung der gebundenen Fraktion und damit der Dissoziationskonstanten. In den Ergebnissen dieser Arbeit ist entweder direkt geblottet oder nach Subtraktion der Basisfluoreszenz ( ). III.2.4 Methoden zur Strukturaufklärung von Proteinen III.2.4.1 Dynamische Lichtstreuung (DLS) Bei der dynamischen Lichtstreuung handelt es sich um eine Methode mit welcher der hydrodynamische Radius eines Proteins und damit dessen Größe ermittelt werden kann. Bei der DLS betrachtet man die Intensitätsänderung des von einer kolloidalen Lösung emittierten Lichts als eine Funktion der Zeit. Hieraus lässt sich die Größenverteilung von Proteinen bestimmen. Die Messungen wurden an einem SpectroSIZE 300 (Nabitec, Deutschland) durchgeführt. Hiezu wurden ca. 15-20 µl Probe in eine Quarzküvette pipettiert und die Pufferbedingungen wurden in der Gerätesoftware spezifiziert. Das Messintervall betrug 20 x 20 Sekunden. III.2.4.2 Röntgenkleinwinkelstreuung (SAXS) Die Röntgenkleinwinkelstreuung (engl. small angle x-ray scattering, SAXS) ist wie die Diffraktion an Kristallen eine Methode zur Strukturuntersuchung mit Hilfe von Röntgenstrahlung. Im Gegensatz zur Kristallographie werden mit SAXS ungeordnete Strukturen kolloidaler Größe untersucht, wie Proteine in flüssiger Lösung. Diesen Systemen fehlt eine, für hochauflösende Strukturaufklärung notwendige, höhere Ordnung. Desweiteren liegen die Partikel in Lösung unorientiert vor. Mit SAXS erhält man Informationen über Größe, Gestalt und Dispersivität der untersuchten Materialien. Zur SAXS-Messung wurde eine Probe standardmäßig in fünf verschiedenen Konzentrationen zwischen 0,5 und 10 mg/ml in 15-60 µl Volumen eingesetzt. Die Proteine wurden wie zuvor unter 2.3.3 beschrieben aufgereinigt und die Monodispersität der Probe wurde mittels Gelfiltration und DLS (2.3.3.4 und 2.3.8) überprüft. Nur Proben, die zu mehr als 90 % monodispers waren, wurden untersucht. Vor der Messung wurde der Probe 2 mM DTT zur Vermeidung von Strahlenschäden zugesetzt. Die Messungen wurden an Beamline P12 (EMBL, HASYLAB/DESY, Hamburg, Deutschland) durchgeführt. Der Abstand der Probe zum Detektor [2D photon counting Pilatus 2M pixel X-ray detector (Dectris)] betrug 3,1 m. Die Strahlung besaß eine Wellenlänge von 0,1-0,3 nm. Der Bereich der Impulsübertragung 51 III Methoden 0,01<s<0,6 Å-1 wurde abgedeckt (s = 4π sinθ/λ, wobei 2θ der Streuungswinkel war) Vor und nach jeder Probe wurde der Probenpuffer gemessen und zur Skalierung der Probe anhand ihrer Proteinkonzentration eingesetzt. Die initiale Datenprozessierung wurde mit dem Programm Primus (Konarev et al. 2003) durchgeführt. Mit Hilfe der Guinier Annäherung wurde I(0) und der Trägheitsradius Rg ermittelt. Dies ist möglich unter der Annahme, dass bei sehr kleinen Winkeln (s<1,3/Rg) die Intensität I(s) = I(0) exp(-(sRg)2/3) beträgt. Für die Bestimmung von Rg und DMAX aus den Streukurven sowie der paarweisen Verteilung p(r) wurde die Software Gnom (Semenyuk & Svergun 1991) verwendet. Die Erstellung von ab initio-Modellen erfolgte mittels der Programme Dammif (Franke & Svergun 2009) und GASBOR (Svergun et al. 2001). Zur Analyse der Flexibilität von Proteinstrukturen wurde EOM (Bernadó et al. 2007) verwendet. Für den Vergleich der SAXS-Daten mit hochauflösenden Strukturen und Modellen wurde CRYSOL (Svergun et al. 1995) und SASREF (Petoukhov & Svergun 2005) verwendet. III.2.4.3 Kristallisation von Proteinen Die Kristallisation von Proteinen ist ein Vorgang, bei dem Moleküle aus einer übersättigten Lösung in einen festen Phasenzustand gebracht werden. Die Übersättigung einer Proteinlösung wird in der Regel durch Hinzufügen eines Präzipitanten erreicht. Die Konzentration des Präzipitanten wird hierbei möglichst langsam erhöht, entweder durch Diffusion von Wasser aus der Lösung oder durch Diffusion von Präzipitans in die Proteinlösung. Typischerweise werden als Präzipitanten Salze wie Ammoniumsulfat oder Natriumcitrat, und organische Verbindungen wie Polyethylenglykole oder Alkohole verwendet. Desweiteren können Faktoren wie Temperatur, pH-Wert sowie der Zusatz von weiteren Salzen oder Detergenzien eine Rolle bei der Kristallisation spielen. Die am häufigsten angewandte Methode zur langsamen Erhöhung der Konzentration von Protein und Präzipitans stellt die sogenannte Dampfdiffusion dar. Hierbei wird noch einmal zwischen der Methode des „hanging drop“, und der des „sitting drop“ unterschieden. Beim „hanging drop“ wird die Proteinlösung auf ein Deckglas pipettiert, welches umgekehrt über eine mit Reservoirlösung (konzentriertes Puffer/Präzipitans-Gemisch) gefüllte Vertiefung gelegt wird. Beim sitting drop sitzt der Tropfen in einer Vertiefung über der Reservoirlösung. In beiden Fällen wird der Tropfen zusammen mit der Reservoirlösung luftdicht verschlossen, sodass eine Verdampfung der Proteinlösung aufgrund des Konzentrationsgefälles zur Reservoirlösung stattfinden kann. III.2.4.3.1 Probenvorbereitung und initiale Kristallisationsbedingungen Die zur Kristallisation verwendeten Proteine wurden zunächst wie unter 2.3.3 beschrieben aufgereinigt, der Affinitätstag wurde proteoytisch abgespalten (2.3.3.6) und mittels DLS (2.4.1) und SDS-PAGE (2.3.5) auf ihre Reinheit und Dispersität hin überprüft. Zusätzlich wurde evtl. vorhandenes Salz im Proteinpuffer mittels Dialyse entfernt. Die initialen Kristallisations-Screens wurden im „sitting drop“-Verfahren durchgeführt. Hierzu wurden je 500 nl Proteinlösung (c: 10-15 mg/ml) unter Zuhilfenahme eines Pipettierroboters (Honeybee 961 Genomic solutions, UK) in spezielle 96-well-Platten (NeXtal QIA1 μplates 96 Well, Qiagen, Deutschland) pipettiert und 1:1 mit Präzipitantenlösung gemischt. In das Reservoir der Platte wurden 55 µl pure Präzipitantenlösung pipettiert. Die Platten wurden luftdicht verschlossen und bei 20°C oder 4°C gelagert. Verwendet wurden die kommerziellen Kristallisationsscreens PACT premier™, Stura Footprint™, Morpheus (Molecular 52 III Methoden Dimensions, UK) und Classic, Cryos, ComPAS, JCSG+ Suite, AmSO4 (Quiagen, Deutschland). Ein mögliches Kristallwachstum wurde alle drei Tage mikroskopisch untersucht. III.2.4.3.2 Optimierung der Kristallisationsbedingungen Wenn eine initiale Kristallisationsbedingung aus den in 2.4.3.1 beschriebenen Versuchen gefunden wurde, wurde diese optimiert, indem die Präzipitanten oder die Salzkonzentration variiert wurde. PEG Konzentrationen wurden hierbei meist in 1 % Schritten, Salzkonzentrationen in 50 mM Schritten erhöht oder erniedrigt. Zusätzlich wurde in einigen Fällen Glycerol zugesetzt um, die Kristalle vor Frostschäden durch flüssigen Stickstoff zu schützen. Optimierungsansätze wurden zunächst ohne Veränderung der initial eingesetzten Volumina in QIA1 μplates 96 Well (Qiagen, G) unter Zuhilfenahme des Pipettierroboters (Honeybee 961 Genomic solutions, UK) pipettiert. Hierzu wurde dann zunächst ein 96-well Masterblock angesetzt. Ließen sich die Bedingungen im 96-well Format reproduzieren, wurde in MRC Maxi 48-Well Crystallization Plate (Molecular Dimensions, UK) oder in Linbro 24-well XRL Plate weiter optimiert. Hierbei wurden Proteintropfen mit bis zu 4 µl gleichem Volumen an Präziptantenlösung vermischt und über einem Reservoir von 50 oder 500 µl luftdicht verschlossen. Die Platten wurden anschließend bei 20°C oder 4°C inkubiert. III.2.4.3.3 Überprüfung von Proteinkristallen Um zwischen Protein- und Salzkristallen zu unterscheiden, wurden diese mikroskopisch unter UV- Licht mit Hilfe des Systems XtaLight-100 UV-light source (Nabitec GmbH, G), welches an ein CCD Mikroskop (Diversified Scientific Inc., Birmingham, USA) angeschlossen war, untersucht. Hierbei zeigten Proteinkristalle aufgrund ihres Anteils an aromatischen Aminosäuren Fluoreszenz bei Licht der Wellenlänge 300 nm. III.2.4.3.4 Datensammlung unter Verwendung von Synchrotronstrahlung Die Diffraktionsdaten wurden bei 100 K und einer Wellenlänge von 0,979570 unter Verwendung eines PILATUS 6M Dektors an der MX2 Beamline (P14 EMBL Beamline Macromolecular Crystallography II) des PETRA III Speicherrings (DESY, Hamburg, G) gesammelt. Kristalle wurden mittels Nylon Loops unter Stickstoffdampf montiert, um Strahlungsschäden gering zu halten. Kryoprotektion wurde erreicht, indem der montierte Kristall in die entsprechende Reservoirlösung mit 20 % Glycerol getaucht wurde. III.2.4.3.5 Datenprozessierung und Modellbau Die gesammelten Daten wurden mit iMOSFLM (Battye et al. 2011) oder XDS (Kabsch 2010) prozessiert. Die Skalierung der Daten fand mit SCALA (Evans 2006) statt. Für weitere Datenanalysen und das Refinement wurde ccp4 (Winn et al. 2011) verwendet. Die finale Modell-Bildung wurde mit Coot (Emsley et al. 2010) durchgeführt. 53 IV Ergebnisse IV Ergebnisse IV.1 Strukturaufklärung von YopM IV.1.1 Klonierung, Expression und Aufreinigung von YopM aus Y. enterocolitica WA-314 Der annotierte „open reading frame“ (ORF) von YopM wurde, wie unter III.2.2.3 beschrieben, aus dem Virulenzplasmid pYV-WA314 (Accession number: FR687019) amplifiziert und in den Vektor pET303 kloniert. Anschließend wurde 6x CT-His-YopM in E. coli BL21-AI überexprimiert (III.2.3.1) und mittels Immobilisierter Metallaffinitätschromatographie aufgereinigt (III.2.3.3.1). Abbildung 10: Ni-NTA Aufreinigung von 6x CT-His YopM. SDS-PAGE der Aufreinigung von YopM. Das Gel wurde mit Coomassie gefärbt. M: Größenstandard, Molekulargewicht in kDa; 1-6 Protein eluiert mit His-Elutionspuffer, Fraktion 1-6. Das kalkulierte Molekulargewicht von YopM betrug 60 kDa. 6x CT-His-YopM konnte mit einer Ausbeute von ca. 10 mg pro Liter E.coli BL21-AI Kultur exprimiert und mittels Ni-NTA Agarose aufgereinigt werden. Wie Abbildung 10 zeigt, war die Reinheit des erhaltenen Proteins jedoch nicht ausreichend für weitere Analysen, weswegen eine Ionenaustauschchromatographie durchgeführt wurde. Zunächst wurde hierfür das aus der Ni-NTA Aufreinigung erhaltene Eluat gegen ein tausendfaches Volumen Anionenaustauscher Puffer A (Tabelle 7) dialysiert. Die Analyse mittels ProtParam (Gasteiger et al. 2005) ergab für YopM einen isoelektrischen Punkt (pI) von 4,43. Aufgrund dieser Vorhersage wurde eine Anionenaustauschchromatographie bei einem pH-Wert von 6,0 durchgeführt. YopM sollte also mit einer negativen Nettoladung vorliegen und an die UnoQ1-Säule binden, während der Großteil der Kontaminanten mit neutralem oder basischem pI sich im Durchfluss wiederfinden sollte. Die Aufreinigung wurde wie unter III.2.3.3.3 durchgeführt und das Ergebnis wurde mittels SDS-PAGE untersucht. 54 IV Ergebnisse A B 300 80 60 200 40 100 % Puffer B Absorption 280 nm [mAu] 100 20 0 123456 0 10 20 0 30 40 Zeit [min] Abbildung 11: Ionenaustauschchromatographie von YopM. A: Chromatogramm der Ionenaustauschchromatographie von 6x CT-His-YopM mittels UnoQ1 Säule (Biorad, Berkeley, USA. B: SDS-PAGE der Elutionsfraktionen 1-6 aus A; M: Größenstandard, Molekulargewicht in kDa. Abbildung 11 zeigt das Ergebnis der Anionenaustauschchromatographie von YopM. YopM beginnt bei einer Konzentration von 35 % Anionenaustauscher Puffer B zu eluieren. Ein deutlicher Peak ist im Chromatogramm zu erkennen. Abbildung 4 B zeigt die Analyse der Peakfraktionen 1-6 mittels SDS-PAGE. Durch die Chromatographie konnte ein deutlicher Reinigungserfolg im Vergleich zur Ni-NTA Aufreinigung (Abbildung 10) erzielt werden. Es zeigte sich, dass weiterhin eine Proteinbande bei ca. 25 kDa als Kontamination verblieb, weswegen als finaler Aufreinigungsschritt eine Größenausschlusschromatographie durchgeführt wurde. Hierzu wurde eine Superdex 200 10/30 Säule verwendet, da diese über das benötigte Auflösungsvermögen verfügen sollte. A B Absorption 280nm [mAu] 20 15 10 5 1 2 3 4 0 0 5 10 15 Elutionsvolumen Ve [ml] 20 Abbildung 12: Größenausschlusschromatographie von YopM. A: Chromatogramm der Größenausschlusschromatographie von YopM mittels Superdex 200. SDS-PAGE der Elutionsfraktionen 1-4 aus A; M: Größenstandard, Molekulargewicht in kDa. Abbildung 12 zeigt das Resultat der Größenausschlusschromatographie von YopM. Die Reinheit des Proteins konnte noch einmal erhöht werden, indem die Kontaminante bei 25 kDa nahezu vollständig abgetrennt wurde. YopM lag nun prinzipiell in ausreichender Reinheit für röntgenkristallographische Untersuchungen vor. Die SDS-PAGE-Analysen aus Abbildungen 3-5 zeigten jedoch, dass YopM als Doppelbande im Gel lief. Das Vorhandensein verschiedener Spezies eines Proteins ist für Kristallisationsexperimente 55 IV Ergebnisse äußerst nachteilig. Dieser Umstand führte dazu, dass der annotierte Translationsstart von YopM aus Y. enterocolitica WA-314 eingehender untersucht wurde. IV.1.2 Überprüfung des Translationsstarts von YopM aus Y. enterocolitica WA-314 Da YopM in verschiedenen Yersinia-Stämmen in unterschiedlicher Form vorkommt, wurden zunächst die Aminosäuresequenzen ausgewählter Proteine aus der Datenbank „uniprot“ (www.uniprot.org) verglichen. Anschließend erfolgte eine detailliertere Analyse der N-Termini von YopM aus Y.enterocolitica WA-314 und dem nahe verwandten Stamm Y. enterocolitica W22703 (Fuchs et al. 2011). A B C Abbildung 13: Sequenzvergleich ausgewählter YopM-Proteine. Ausgewählte YopM Sequenzen wurden mit Hilfe der Software „CLC Workbench“ (CLC Bio, Qiagen, Venlo, NL) alignt. A: Aminosäurevergleich der ersten 40 Aminosäuren unterschiedlicher YopM-Isoformen aus „uniprot“. B: Vergleich der ersten 40 Aminosäuren von YopM aus Y. enterocolitica WA-314 und Y. enterocolitica W22703 laut Annotation (Accession number pYV-WA-314: FR687019; pYVe227: AF102990) C: Vergleich des annotierten NTerminus von YopM (WA-314) mit dem um 21 Aminosäuren upstream verlängerten N-Terminus von YopM (W22703). Der Sequenzvergleich verschiedener YopM-Isoformen zeigt, dass die N-Termini hoch konserviert sind. Abbildung 6 A zeigt, dass einige Proteine einen um 21 Aminosäuren verlängerten N-Terminus besitzen. Abbildung 6 B zeigt, dass YopM aus Y. enterocolitica WA-314 diesen verlängerten N-Terminus aufweist. Der direkte Vergleich mit YopM aus Stamm 22703 verdeutlicht dies. Ein Blick upstream des annotierten Translationsstart von YopM_22703 offenbarte ein weiteres ATG, 21 Codons entfernt. Verlegte man nun den Translationsstart um diese 21 Codons upstream, führte dies zu einer nahezu identischen Sequenz wie der von YopM_WA-314. Aufgrund dieser Ungereimtheiten in den Annotationen verschiedener YopM-Isoformen wurde beschlossen den tatsächlichen N-Terminus von YopM aus Y. enterocolitica WA-314 experimentell zu untersuchen. 56 IV Ergebnisse Hierzu wurde ein Yop Release-Assay wie unter III.2.1.2 durchgeführt. Die erhaltenen Yops wurden mit Trichloressigsäure präzipitiert und mittels Western Blot auf eine PVDF-Membran übertragen (Abbildung 14). Die YopM-Bande wurde mittels Immunserum gegen YopM identifiziert, ausgeschnitten und mittels Edman-Abbaus analysiert. Das Ergebnis dieser Nterminalen Sequenzierung zeigte für die ersten fünf Aminosäuren: Met-Phe-Ile-Asn-Pro. Aus dieser Erkenntnis heraus wurde YopM ab dem zweiten Startcodon neu amplifiziert und wie beschrieben kloniert. A B M 1 2 M 1 2 130 – 70 – 55 – 40 – 35 – 25 – 100 – 70 – 55 – 40 – 15 – Abbildung 14: Experimentelle Analyse des Translationsstarts von YopM. A: Ergebnis des Yop Release-Assays. M: Größenstandard, Molekulargewicht in kDa; 1: Analyse der freigesetzten Yops mittels SDS PAGE; 2: Western Blot-Analyse mittels YopM Antiserum. B: Heterologe Expression von YopM in BL21 dargestellt mittels SDS-PAGE. M: Größenstandard, Molekulargewicht in kDa. 1: 6x CT-His-YopM mit annotiertem Startcodon; 2: 6x CT-His-YopM mit ermitteltem zweitem Startcodon. Die Testexpression des neu klonierten yopM-Gens mit dem ermittelten zweiten Startcodon zeigte, dass YopM in der SDS-PAGE nicht mehr als Doppelbande vorlag (Abbildung 14 B). Hieraus ergibt sich die in Abbildung 15 dargestellte korrekte Sequenz von YopM. Abbildung 15: Annotierte Aminosäuresequenz von YopM Aminosäuresequenz von YopM aus Y. enterocolitica WA-314. N-Alpha: N-terminale alpha-Helices; LRR1-20: „Leucine Rich Repeats“; C-Cap: C-terminales Abschlussmotiv der LRRs; C-Terminus: unstrukturierter CTerminus Zur weiteren Untersuchung von YopM wurden im Wesentlichen drei Konstrukte verwendet: YopM_Full, welches das Volllängenprotein von Aminosäure 1-506 enthielt, YopM_ΔC, 57 IV Ergebnisse Aminosäure 1-481 und YopM_Core, Aminosäure 34-481. Eine komplette Übersicht aller Konstrukte findet sich in Tabelle 18. IV.1.3 Analytische Größenbestimmung und Dispersitätskontrolle von YopM Nach der Aufreinigung der Proteine wie unter IV.1.1 beschrieben wurde zunächst eine analytische Größenausschlusschromatographie durchgeführt. Diese erlaubt die Bestimmung der Dispersität der Lösung sowie der Größe der vorhandenen Protein-Spezies. Die Größenausschlusschromatographie wurde wie unter III.2.3.3.4 beschrieben durchgeführt. Verwendet wurde die Säule Superdex 200 10/300 GL. Abbildung 16: Analytische Größenausschlusschromatographie von YopM. A: Chromatogramm der Größenausschlusschromatographie dreier verschiedener YopM-Konstrukte. YopM_1-506 eluiert bei einem Volumen von 12,93 ml, YopM_1-481 bei 13,12 ml und YopM_34-481 bei 13,44 ml. Die graue Linie zeigt den Lauf des „Biorad Gel Filtration Standards“. B: SDS-PAGE der jeweiligen Elutionsfraktionen 1-5 aus A; oberes Gel: YopM_1-506, mittleres Gel YopM_1-481, unteres Gel: YopM_34-481. M: Größenstandard, Molekulargewicht in kDa. C: Blot der normalisierten Elutionsvolumina Ve/Vo gegen das Molekulargewicht in Dalton. Die Eichgerade entstand aus dem Fit der Elutionsvolumina der Größenmarker Thyroglobulin (670 kDa), γ-globulin (158 kDa), Ovalbumin (44 kDa), Myoglobin (17 kDa) und Vitamin B 12 (1,35 kDa). Abbildung 16 zeigt das Ergebnis der analytischen Gelfiltration von drei verschiedenen YopMKonstrukten. Alle getesteten Konstrukte eluieren in einem Einzelpeak, d.h. es liegt jeweils nur eine Spezies des Proteins vor. Die Lösung ist monodispers. Desweiteren eluieren die Proteine ihrer Größe nach, in der Reihenfolge ihrer vorhergesagten Molekulargewichte (Abbildung 16 A). Laut ProtParam (Gasteiger et al. 2005) lauten diese für YopM_1-506 (YopM_Full): 57,8 kDa, für YopM_1-481: 54,9 kDa und für YopM_34-481 (YopM_Core): 50,3 kDa. In der denaturierenden SDS-PAGE in Abbildung 16 B sind die Elutionsfraktionen aufgetragen. Hier bestätigten sich die vorhergesagten Molekulargewichte der Konstrukte. Die Auswertung der tatsächlichen Größe der Proteine, unter Zuhilfenahme der aus der Eichgeraden in Abbildung 16 C erhaltenen Gleichung, ergibt jedoch ein anderes Bild. Die, anhand der Elutionsvolumina errechneten Molekulargewichte der Proteine lauten: YopM_158 IV Ergebnisse 506: 119,1 kDa, YopM_1-481: 106,4 kDa, YopM_34-481: 88,1 kDa. Die errechneten Größen deuten darauf hin, dass alle Konstrukte als Dimere vorlagen. Als weitere Qualitätskontrolle wurden YopM_Full sowie YopM_Core mittels dynamischer Lichtstreuung (DLS) wie unter III.2.4.1 beschrieben untersucht. A B Abbildung 17: Dynamische Lichtstreuung von YopM. Heatmap der Größenverteilung der hydrodynamischen Radii von A: YopM_Full und B: YopM_Core über einen Zeitraum von 80 Sekunden. Aus den in Abbildung 17 dargestellten Messungen der dynamischen Lichtstreuung geht hervor, dass sowohl YopM_Full als auch YopM_Core monodispers vorlagen. Der ermittelte hydrodynamische Radius für YopM_Full lag bei 4,4 ± 0,17 nm und für YopM_Core bei 4,2 ± 0,29 nm. Die daraus resultierenden Molekulargewichte ergeben 98,69 kDa für YopM_Full und 88,89 kDa für YopM_Core. Ein weiterer Hinweis für das ausschließliche Vorhandensein von Dimeren. IV.1.4 Strukturanalyse von YopM IV.1.4.1 Kristallisation von YopM 6x CT-His-YopM_Full (Tabelle 18) wurde wie zuvor beschrieben aufgereinigt, mittels Vivaspin® Zentrifugenfilter (GE Healthcare Europe, München, G) mit einem MWCOs von 10 000 kDa auf 10,5 mg/ml ankonzentriert und gegen ein tausendfaches Volumen 50 mM Hepes-Puffer mit einem pH von 7,5 dialysiert. Für die Suche nach initialen Kristallisationsbedingungen wurden die kommerziellen Screens PACT premier™, Stura Footprint™, Morpheus (Molecular Dimensions, UK) und Classic, ComPAS, JCSG+ Suite, AmSO4 (Quiagen, Deutschland) verwendet. 500 nl der Proteinlösung wurden wie in III.2.4.3.1 beschrieben unter Zuhilfenahme eines Pipettierroboters (Honeybee 961 Genomic solutions, UK) in spezielle 96-Well Platten (NeXtal QIA1 μplates 96 Well, Qiagen, Deutschland) pipettiert und 1:1 mit Präzipitantenlösung gemischt. Die Platten wurden bei Raumtemperatur inkubiert und alle drei Tage mikroskopisch untersucht. Nach drei Wochen Inkubation zeigten sich lediglich bei einer Bedingung Kristalle (PACT B12: 0,1 M MES, 0,01 M ZnCl2, 20% w/v PEG 6000 pH6). Diese Kristalle waren lange, dünne Nadeln und konnten nicht in einem größeren Maßstab reproduziert werden. 59 IV Ergebnisse Abbildung 18: Kristalle von YopM_Full. Kristalle des Volllängenproteins YopM mit 6x C-terminalem His-Tag. Gewachsen nach drei Wochen bei einer Tropfengröße von 500 nl Proteinlösung (c: 10,5 mg/ml) gemischt mit 500 nl Präzipitantenlösung (0,1 M MES, 0,01 M ZnCl2, 20% w/v PEG 6000 pH 6) im „sitting drop“-Verfahren über einem Reservoir aus 50 µl purer Präzipitantenlösung. Da der Versuch YopM in Volllänge zu kristallisieren wenig Erfolg brachte wurde YopM_Core für weitere Kristallisationsansätze verwendet. Bei YopM_Core handelt es sich um eine trunkierte Version von YopM der 33 Aminosäuren N-terminal und 23 Aminosäuren C-terminal fehlen. Diese Aminosäuren zeigten in der Kristallstruktur von YopM aus Y. pestis 195/P (Evdokimov et al. 2001) keine Elektronendichte, was ein klarer Hinweis dafür ist, dass diese ungeordnet sind und somit die Kristallisation an sich stören könnten. 6xNT-His-TEV-YopM_Core (Tabelle 18) wurde analog zum Volllängenkonstrukt wie unter IV.1.1 beschrieben kloniert, exprimiert und aufgereinigt. Anschließend wurde der His-Tag wie unter III.2.3.3.6 entfernt. Die Konzentration der Proteinlösung wurde mittels Vivaspin® Zentrifugenfilter (GE Healthcare Europe, München, G) mit einem MWCOs von 10000 kDa auf 10,5 mg/ml eingestellt und mittels Dialyse gegen ein tausendfaches Volumen 50 mM Hepes-Puffer mit einem pH von 7,5 entsalzt. Für die Suche nach initialen Kristallisationsbedingungen wurden die kommerziellen Screens PACT premier™, Stura Footprint™, Morpheus (Molecular Dimensions, UK) und Classic, ComPAS, JCSG+ Suite (Quiagen, Deutschland) verwendet. 500 nl der Proteinlösung wurden wie in III.2.4.3.1 beschrieben unter Zuhilfenahme eines Pipettierroboters (Honeybee 961 Genomic solutions, UK) in spezielle 96-Well Platten (NeXtal QIA1 μplates 96 Well, Qiagen, Deutschland) pipettiert und 1:1 mit Präzipitantenlösung gemischt. Bereits nach drei Tagen Inkubation bei Raumtemperatur fanden sich unter verschiedenen Bedingungen Kristalle. 60 IV Ergebnisse Abbildung 19: Initiale Kristallisationsscreens von YopM_Core. Kristalle des trunkierten YopM_Core ohne His-Tag. Gewachsen nach drei Tagen, bei einer Tropfengröße von 500 nl Proteinlösung (c: 10,5 mg/ml) gemischt mit 500 nl Präzipitantenlösung. A: PACT premier™ B7 (0,1 M MES, pH 6,0, 0,2 M Natriumchlorid, 20 % w/v PEG 6000). B: PACT premier™ C4 (0,1 M PCTP Puffer pH 7,0, 25 % w/v PEG 1500. C: PACT premier™ F11 (0,1 M Bis Tris Propan pH 6,5, 0,2 M Natriumcitrat, 20 % w/v PEG 3350). D: PACT premier™ F12 (0,1 M Bis Tris Propan pH 6,5, 0,2 M Natriummalonat, 20 % w/v PEG 3350) E: Morpheus A8 (0,1 M Natrium-Hepes/MOPS pH 7,5, 0,06 M MgCl2/CaCl2, MPD_P1K_PEG 3350 37,5% w/v) F: ComPas B1(0,1 M MES pH 6,5, 0,2 M Ammoniumsulfat, 22 % w/v PEG 8000). Die initialen Kristallisationsbedingungen, wie in Abbildung 19 dargestellt, wurden reproduziert und optimiert, indem zunächst die Puffer-Art und Konzentration beibehalten, die Salz- und die Präzipitantenkonzentration jedoch variiert wurde (siehe III.2.4.3.2). Diese ersten Ansätze wurden zunächst in QIA1 µplates 96 well (Qiagen, G) ohne Veränderung der ursprünglichen Volumina durchgeführt. Die erfolgreichsten Bedingungen wurden dann im 48- bzw. 24-wellFormat weiter optimiert. Hierbei wurden die Volumina der Proteintropfen auf 2 µl erhöht um das Wachstum ausreichend großer Protein-Einkristalle zu fördern. Da für die Datensammlung mittels Synchrotron-Strahlung eine spätere Behandlung mit flüssigem Stickstoff notwendig war, wurde einigen Optimierungsansätzen zum Schutz vor möglichen Frostschäden Glycerol zugesetzt. Durch die auf diese Weise durchgeführte Optimierung der Bedingung PACT premier™ F11 (Abbildung 19 C) konnten Protein-Einkristalle mit einer Größe von bis zu 1 x 0,4 x 0,02 mm Größe (Abbildung 20 B) hergestellt werden, welche für die Röntgenstrukturanalyse geeignet waren. 61 IV Ergebnisse Abbildung 20: Optimierungsansätze für YopM_Core. Kristalle aus den Optimierungsscreens für YopM_Core. A: 50 mM BisTrisPropane pH 6,5, 0,2 M Na-Citrat, 24 % PEG3350; 1+1 µl Tropfen (Proteinlösung/Präzipitans), 50 µl Reservoir (Maxi Plate, 48-well) B: 50 mM BisTrisPropane pH 6,5, 0,2 M Na-Citrat, 24 % PEG3350, 15 % Glycerol; 2+2 µl Tropfen (Proteinlösung/Präzipitans) 500 µl Reservoir (Linbro Plate, 24-well) IV.1.4.2 Röntgenbeugung, Datensammlung und Analyse Vor der Exposition der aus IV.1.4.1 erhaltenen Proteinkristalle mit Röntgenstrahlung wurden diese in eine Kryoschutz-Lösung (Präzipitantenlösung mit 20 % v/v Glycerol) überführt und in flüssigem Stickstoff schockgefroren. Die in 15 % Glycerol gewachsenen Kristalle konnten direkt schockgefroren werden. Diffraktionsdaten wurden bis zu einer Auflösung von 3,2 Å am Messplatz P14 (EMBL Beamline Macromolecular Crystallography II) des PETRA III Speicherrings (DESY, Hamburg, G) gesammelt. Die Statistiken der Datensammlung und des Refinements sind in Tabelle 25 zusammengefasst. Tabelle 25: YopM_Core: Datensammlung und Refinement Datensammlung Beamline Wellenlänge [Å] Temperatur [K] Raumgruppe Einheitszellparameter: a, b, c [Å] Einheitszellparameter: α, β, γ [°] Auflösungsbereich [Å] Symmetrieunabhängige Reflektionen Rsymm Vollständigkeit der Daten [%] Multiplizität der Daten < I / σ(I) > B-Faktor (Wilson Plot) [Å2] Matthews Koeffizient (VM) [Å3/Da] Lösungsmittelanteil Verfeinerung Auflösungsbereich Rwork / Rfree [%] P14 Beamline Macromolecular Crystallography II EMBL /PETRA III 0.979570 100 C2 210.9, 126.3, 139.9 90, 118.3, 90 40 – 3.2 64045 9.1 (50.5) 99.6 (99.3) 6.6 (5.9) 11.9 (3.3) 95.3 4.0 69.8 40 – 3.2 (3.283 – 3.2) 19.8 / 21.5 (32.6/32.7) 62 IV Ergebnisse Inhalt der asymmetrischen Einheit: Gesamtzahl an Atomen Wassermoleküle RMS Bindungslängen-Abweichung [Å] RMS Bindungswinkel-Abweichung [°] Ramachandran-Plot- Analyse Favorisierte Regionen [%] Erlaubte Regionen [%] Großzügig erlaubte Regionen [%] 14226 59 0.006 1.206 74.4 25.6 0 a Werte in Klammern gelten für die höchste Auflösungsschale Auf Grundlage der bekannten Struktur von YopM aus Y. pestis 195/P (Evdokimov et al. 2001) mit der pdb-Nummer 1jl5 konnte ein Modell erstellt werden, mit dessen Hilfe es möglich war, die Struktur von YopM_WA-314 durch molekularen Ersatz zu lösen. Der Modellbau und die Verfeinerung erfolgten mit Coot (Emsley et al. 2010) und Refmac5 (Winn et al. 2011) bis zu einem finalen R-Faktor von 19,8 % und einem freien R-Faktor von 21,5 %. Das finale Modell wurde mit der Nummer 4OW2 in der pdb-Datenbank hinterlegt. Die geometrische Analyse der Phi- und Psi- Winkel ist in Abbildung 21 dargestellt. Die 3,2 Å Struktur von YopM_WA-314 zeigt vier Moleküle, die in der asymmetrischen Einheit ein Tetramer mit einer Gesamtfläche von 77.112 Å2 [Kalkuliert mit AREAIMOL (Krissinel 2012)] bilden (Abbildung 22). Abbildung 21: Ramachandran-Plot für YopM. Darstellung der Psi- und Phi-Winkel-Verteilung aller Aminosäuren der Struktur von YopM_WA-314 (PDB Nr.: 4OW2). Reste in favorisierten Regionen: 1158 (74,4 %); Reste in erlaubten Regionen: 398 (25,6 %); Anzahl an Aminosäuren außer Glycin und Prolin: 1556; Anzahl an Glycinen: 24; Anzahl an Prolinen 204; Gesamtzahl an Aminosäuren: 1792. Erstellt mit Procheck (Laskowski et al. 1993). 63 IV Ergebnisse Abbildung 22: YopM-Moleküle in der Einheitszelle. Tetramere Struktur von YopM_WA-314 in der asymmetrischen Einheit in Ribbon-Darstellung. Das Tetramer besteht aus vier identischen Monomeren (Ketten A-D), angezeigt in unterschiedlichen Farben. Dargestellt mit USCF Chimera (Pettersen et al. 2004). In der asymmetrischen Einheit interagiert jedes YopM-Monomer über verschiedene Wechselwirkungen mit drei anderen Molekülen. Die Analyse der Kontaktfläche der vier Ketten mittels PDBsum (Laskowski et al. 1997) ist in Tabelle 26 dargestellt. Die wichtigsten Interaktionsflächen liegen hierbei zwischen den Ketten A-B bzw. den Ketten A-C und B-D. Tabelle 26: Intermolekulare Wechselwirkungen des YopM-Tetramers Ketten Beteiligte Reste A–B A–C B–D A–D B–C C–D 19 : 17 20 : 20 20 : 21 2:3 3:3 2:2 Interaktionsfläche [Å2] 1124 1016 1022 122 126 152 H-Brücken 4 13 10 1 - Nichtkovalente Bindungen 69 104 80 6 16 5 Das YopM-Monomer besteht aus zwei N-terminalen Helices gefolgt von einer repetitiven Struktur aus β-Faltblättern, die über elongierte Loops miteinander verknüpft sind. Diese bilden insgesamt 20 Leucin-reiche Wiederholungen (Leucine Rich Repeats, LRR). Abgeschlossen wird die Struktur durch eine weitere Faltblattstruktur, die das sogenannte Cterminale „Capping“ Motiv bildet. 64 IV Ergebnisse A B Abbildung 23: Struktur und Topologie des YopM-Monomers. A: Aufbau des YopM-Monomers aus zwei Alpha Helices (orange) gefolgt von 21 β-Faltblättern (lila), die die LRRRegion bilden und abschließen. Stabilisierende H-Brücken sind in hellblau gezeigt. Dargestellt mit USCF Chimera (Pettersen et al. 2004) B: Topologische Darstellung des YopM-Monomers. Rote Zylinder stellen α-Helices dar, Pfeile zeigen β-Faltblatt-Strukturen. Zahlen indizieren erste und letzte Aminosäure des Motivs. IV.1.4.3 Struktur von YopM in Lösung Da die aus IV.1.3 erhaltenen Ergebnisse daraufhin deuteten, dass YopM in Lösung als Dimer vorliegt und in der Kristallstruktur (Abschnitt IV.1.4.2) ein Tetramer in der asymmetrischen Einheit gefunden wurde, sollte nun mittels Röntgenkleinwinkelstreuung die Struktur von YopM in Lösung untersucht werden. Hierzu wurde YopM wie zuvor beschrieben aufgereinigt. Die Probe wurde bei 20.000 g und 4°C für eine Stunde zentrifugiert (5810R, Eppendorf, G) und mit Hilfe eines 100 nm Zentrifugenfilters (Ultrafree-MC, Millipore, USA) von größeren Partikeln befreit. Anschließend wurden fünf verschiedene Konzentrationen (0,7; 1,4; 2,6; 5,5 und 10,5 mg/ml) eingestellt, die mittels DLS auf Monodispersität überprüft wurden. Die Proben wurden anschließend an Beamline P12 (EMBL, HASYLAB/DESY, Hamburg, G) vermessen. Die erhaltenen Daten wurden auf Strahlenschäden kontrolliert und mit dem Programm Primus (Konarev et al. 2003) der Proteinkonzentrationen entsprechend skaliert. Die Messkurven der Proben wurden durch Subtraktion der Streukurven der reinen Pufferlösungen normalisiert. Das Programm GNOM (Semenyuk & Svergun 1991) lieferte den Trägheitsradius Rg, sowie den maximalen Durchmesser Dmax, welche Aufschluss auf die Größe der Moleküle gaben. Die Ergebnisse der Größenbestimmungen sind in Tabelle 27 zusammengefasst. 65 IV Ergebnisse Tabelle 27: Ergebnisse der SAXS Messung von YopM_Core Konzentration [mg/ml] 0,7 1,4 2,6 5,5 10,4 Rg [nm] 3,8 ± 0,3 3,9 ± 0,2 3,9 ± 0,2 3,8 ± 0,1 3,7 ± 0,1 Dmax [nm] 12 13 12 11 10 VPorod [nm3] 177 170 154 147 144 MW I(0) [kDa] 79 78 79 80 76 MWPorod [kDa] 110 106 96 92 90 Die errechneten Molekulargewichte aus der „Vorwärtsstreuung“ (~78 kDa) und dem Porod Volumen (~99 kDa) legen, bei einem theoretischen Molekulargewicht von 50,3 kDa nahe, dass es sich bei YopM_Core in Lösung um ein Dimer handelt. Diese Annahme wird durch die bereits unter IV.1.3 gewonnenen Ergebnisse bekräftigt. Mit Hilfe der Programme DAMMIF (Franke & Svergun 2009) und SASREF (Petoukhov & Svergun 2005) wurden „ab initio“-beziehungsweise „rigid body“-Modelle anhand der SAXSDaten erstellt. Das Programm CRYSOL (Svergun et al. 1995) diente dem Vergleich der Messdaten mit der theoretischen Streukurve der hochauflösenden Kristallstruktur. Abbildung 24: SASREF-Modell von YopM_Core. A: Strukturüberlagerung des mit Hilfe von SASREF erhaltenen Modells von YopM_Core (blau) mit dem aus den Ketten A und C der 3,2 Å Kristallstruktur resultierenden Dimer (rot). Dargestellt in Ribbon-Repräsentation mit dem Programm PyMol (Schrödinger LLC, USA) B: Vergleich der theoretischen Streukurven des SASREF-Modells (blau) sowie des Dimers aus der Kristallstruktur (rot) mit der tatsächlichen Messkurve (grün). Dargestellt mit SASPLOT (Petoukhov et al. 2012). Das mit Hilfe von SASREF erstellte Dimer-Modell ähnelt sehr deutlich dem tatsächlich in der asymmetrischen Einheit der Kristallstruktur vorkommenden Dimer, gebildet aus den Ketten A und C beziehungsweise B und D (RMSD der Cα-Atome: 0,95 Å). Die mittels Superpose (Winn et al. 2011) kalkulierte RMSD der Cα-Atome des SASREF-Modells und der Ketten A_C der Kristallstruktur beträgt 3,1 Å. Das Modell wirkt weniger gedrängt, was eventuell ein Indiz für einen Effekt der Packung der Moleküle in der Kristallstruktur sein könnte. 66 IV Ergebnisse Abbildung 25: Fit des YopM-Monomers mit den SAXS-Messdaten. Theoretische Streukurve des YopM-Monomers (rot) geplottet gegen die tatsächlichen Messwerte (grün). Dargestelt mit SASPLOT (Petoukhov et al. 2012). Um auszuschließen, dass es sich bei YopM_Core in Lösung um ein Monomer handeln könnte, wurde auch dieses mit CRYSOL untersucht. Der Vergleich mit den Messdaten (Abbildung 25) zeigt, dass die theoretische Streukurve von den tatsächlichen Werten signifikant abweicht. Es ist also eindeutig auszuschließen, dass es sich bei YopM_Core in Lösung um ein Monomer handelt. Abbildung 26: Überlagerung des Kristalldimers mit dem ab initio-Modell. Volumenrepräsentation des mittels DAMMIF erhaltenen ab initio-Modells überlagert mit dem aus den Ketten A und C der 3,2 Å Kristallstruktur resultierenden Dimer in Ribbon-Darstellung. Gerendert mit PyMol (Schrödinger LLC, USA) Die Überlagerung des „Kristalldimers“ von YopM_Core mit der aus dem ab initio-Modell erhaltenen, niedrig aufgelösten Hüllstruktur zeigt ebenso eine gute Übereinstimmung. Es ist also davon auszugehen, dass in der Kristallstruktur von YopM (Abbildung 22) zwei physiologische Dimere (dargestellt durch die Ketten A und C sowie B und D) ein nicht 67 IV Ergebnisse biologisch aktives Tetramer bilden. Bei diesem Homodimer interagieren zwei YopM-Moleküle über eine C-terminale Region, welche die letzten 11 LRRs umspannt. Im Folgenden wurde nun noch einmal die Interface Region zwischen den Ketten AC bzw. BD im Detail untersucht. Abbildung 27: Übersicht der Kontakte zwischen den Ketten A und C bzw. B und D der tetrameren Kristallstruktur. A: Interaktionen der Ketten A und C bzw. B und D der tetrameren Kristallstruktur analysiert mittels PDBsum (Laskowski et al. 1997). Aminosäuren sind als Ovale dargestellt. Hierbei sind positiv geladene Aminosäuren blau hinterlegt, negativ geladene Aminosäuren rot, ungeladene grün, aliphatische grau und aromatische Aminosäuren lila. Blaue Linien zeigen Wasserstoffbrückenbindungen, gelbe Linien nichtkovalente Wechselwirkungen. Die breite der Linien indiziert die Stärke der Bindungen. B: Hervorhebung der an den wichtigsten Bindungen beteiligten Aminosäuren in gelb. Abbildung 27 zeigt eine Übersicht über die molekularen Wechselwirkungen innerhalb des physiologischen Dimers, wie es sich in der Kristallstruktur in den Ketten A und C bzw. B und D wiederfindet. Die Interaktionsfläche der Ketten A und C beträgt demnach 1016 Å2 und umfasst 20 Aminosäuren. Das Interface wird durch insgesamt 13 Wasserstoffbrückenbindungen gebildet und über 104 nichtkovalente Wechselwirkungen stabilisiert. Im Mittelpunkt stehen hierbei Arg 479, welches jeweils zwei H-Brücken zu Ser 401 der gegenüberliegenden Kette ausbildet, und Glu 461, welches ebenfalls in der Lage ist zwei H-Brücken zu Arg 361 zu bilden. Die wichtigsten Interaktionen sind in Abbildung 28 graphisch dargestellt. Eine Übersicht über alle Wasserstoffbrückenbindungen ist in Tabelle 28 gezeigt. 68 IV Ergebnisse Kette A Glu 461 C Asp 481 C Arg 402 A Arg 342 A Arg 361 A Lys 362 C Arg 361 C Asp 399 C Asp 481 A Ser 401 C Arg 479 A Glu 461 A Asp 422 C Kette C His 462 A Abbildung 28: Interfaceregion zwischen dem YopM-Dimer. Extraktion der Ketten A und C aus der tetrameren Kristallstruktur von YopM_Core in Ribbon-Repräsentation. Gerendert mit PyMol (Schrödinger LLC, USA). Die an den wichtigsten H-Brückenbindungen beteiligten Aminosäuren sind herangezoomt und als Sticks dargestellt. Tabelle 28: Wasserstoffbrückenbindungen des YopM-Dimers Atom Aminosäure Kette Atom Aminosäure Kette Abstand [Å] NH1 Arg 342 A O Met 480 C 2,73 NH2 Arg 361 A OE2 Glu 461 C 2,54 OD1 Asp 399 A NH2 Arg 479 C 3,03 OG Ser 401 A NH1 Arg 479 C 2,99 OG Ser 401 A NH2 Arg 479 C 2,76 NH2 Arg 402 A OD1 Asp 481 C 3,27 OD2 Asp 419 A NH2 Arg 479 C 3,3 OE2 Glu 461 A NH2 Arg 361 C 2,52 NE2 His 462 A OD2 Asp 422 C 3,19 NH1 Arg 479 A OG Ser 401 C 3,05 NH2 Arg 479 A OD1 Asp 399 C 3,15 NH2 Arg 479 A OG Ser 401 C 2,53 OD2 Asp 481 A NZ Lys 362 C 3,14 69 IV Ergebnisse IV.2 Überprüfung des inhibitorischen Effekts von YopM auf Caspase-1 Zur Analyse eines postulierten inhibitorischen Effektes von YopM auf Caspase-1 (LaRock & Cookson 2012) wurde yopM aus drei verschiedenen Yersinia-Stämmen wie beschrieben mittels PCR amplifiziert, in den Expressionsvektor pET302 kloniert und in E. coli BL21-AI überexprimiert. Die erhaltenen YopM-Proteine wurden mittels Ni-NTA-Agarose wie unter III.2.3.3.1 beschrieben aufgereinigt und gegen ein tausendfaches Volumen Hepes-Puffer (50 mM Hepes pH 7,5, 100 mM NaCl) dialysiert. Untersucht wurde YopM aus Y. enterocolitica WA-314 (20 LRRs, 58 kDa), YopM aus Y. enterocolitica 8081 (13 LRRS, 42 kDa) und YopM aus Y. pseudotuberculosis YpIII (15 LRRs, 46 kDa). Der inibitorische Effekt von YopM auf das proinflammatorische Enzym Caspase-1 beruht angeblich auf dem Motiv YLTD welches an einer exponierten Stelle auf LRR10 (Y. pseudotuberculosis CO95) liegt. Abbildung 29: Aufreinigung von YopM aus Y. enterocolitica WA-314, 8081 und Y. pseudotuberculosis YpIII A: Sequenzvergleich von Leucine Rich Repeat 10 aus YopM_C092 mit den korrespondierenden Sequenzen aus YopM_YpII, YopM_8081 und YopM_WA-314. B: SDS-PAGE der Elutionsfraktionen nach Aufreinigung über NiNTA-Beads. M: Größenstandard in kDa, 1: YopM_WA-314, 2: YopM_8081, 3: YopM_YpIII. Abbildung 29 A zeigt den Sequenzvergleich dreier verschiedener YopM-Proteine mit der Referenz YopM_CO95. Aus diesem Vergleich geht hervor, dass YopM_WA-314 einen kritischen Aminosäureaustausch von Aspartat zu Alanin im für den inhibitorischen Effekt verantwortlich gemachten Motiv YLTD trägt. YopM_YpIII ist über den gesamten Sequenzbereich von LRR10 identisch mit YopM_CO95; YopM_8081 besitzt das unveränderte Motiv. Zur Untersuchung des inhibitorischen Effekts auf die Proteaseaktivität von Caspase-1 wurde der unter III.2.3.8 beschriebene in vitro Caspase-1-Assay durchgeführt. Als Kontrolle wurde der kommerzielle Inhibitor Z-Val-Ala-DL-AspFluormethylketon (Z-VAD-FMK, BACHEM, Bubendorf, CH) eingesetzt. Das Ergebnis dieses Assays ist in Abbildung 30 dargestellt. 70 IV Ergebnisse A B Caspase-1 Assay 50 µM Caspase-1 Assay 5 µM 0,15 OD405 (YVAD-pNA) OD405 (YVAD-pNA) 0,15 0,1 Blank Caspase_1 Caspase_1/YopM WA-314 Caspase_1/YopM 8081 Caspase_1/YopM YpIII Casase_1/Z-VAD-FMK 0,1 0,05 0,05 0 20 40 60 0 20 40 60 Zeit [min] Zeit [min] Abbildung 30: Caspase-1 Assay Kolorimetrischer Assay zum Umsatz des p-Nitroanilin Substrates YVAD-pNA durch 10 U Caspase-1 über einen Zeitraum von 60 min. A: 200 µM YVAD-pNA ohne Caspase-1 (Blank) bzw. inkubiert mit Caspase-1 sowie Caspase-1 mit 5 µM YopM_WA-314, 5 µM YopM_8081, 5 µM YopM_YpIII und 40 µM Z-VAD-FMK. B: 200 µM YVAD-pNA ohne Caspase-1 (Blank) bzw. inkubiert mit Caspase-1 sowie Caspase-1 mit 50 µM YopM_WA-314, 50 µM YopM_8081, 50 µM YopM_YpIII und 40 µM Z-VAD-FMK. Der Umsatz des Substrats YVAD-pNA durch das Enzym Caspase-1 wurde anhand des freien p-Nitroanilin gemessen. Die Messung erfolgte bei einer Wellenlänge von λ = 405 nm über einen Zeitraum von 60 min. Der Anstieg der Kurve bei Inkubation mit Caspase-1 im Gegensatz zur Leerkontrolle (Blank), bei der nur Puffer zugefügt wurde, zeigt die Reaktion. Die gleichzeitige Inkubation mit 40 µM des kommerziellen Inhibitors Z-VAD-FMK hemmt den Umsatz des Substrats. Dieser Effekt ließ sich mit keinem der aufgereinigten YopM-Proteine nachstellen. 71 IV Ergebnisse IV.3 Interaktion von YopM mit der DEAD-Box-Helikase DDX3 In Experimenten, die vor dieser Arbeit erfolgten, wurde DDX3 als neuer Bindungspartner von YopM in J774-Zellen entdeckt. Darüber hinaus wurde in Co-Immunopräzipitationen festgestellt, dass YopM spezifisch mit der ATPase-Domäne von DDX3 interagiert. Hierauf aufbauend sollte nun eine direkte Interaktion nachgewiesen und diese biochemisch sowie strukturell charakterisiert werden. Zunächst wurde hierzu mittels GST-PulldownExperimenten die Bindestelle von DDX3 an YopM weiter eingegrenzt. Abbildung 31: Kristallstruktur der konservierten Domänen 1 und 2 von DDX3. 2,2 Å Struktur der DEAD-Box Helikase DDX3 (pdb Nummer: 2I4I) mit den konservierten Domänen 1, an der die Bindung von ATP stattfindet (ATPase), und Domäne 2, die hauptsächlich an der RNA-Bindung beteiligt ist (Helikase). Die beiden Domänen sind durch eine unstrukturierte Linker-Region verknüpft (Högbom et al. 2007). IV.3.1 GST-Pulldown Die DEAD-Box-Helikase DDX3 besteht aus zwei strukturierten Domänen, der ATPaseDomäne und der Helikase-Domäne, die durch einen Loop miteinander verbunden sind. N- und C-terminal befinden sich 168 bzw. 82 Aminosäuren lange Bereiche, die ungeordnet sind. Zur Analyse des Bindungsepitops von DDX3 wurden zunächst fünf verschiedene Konstrukte designt, die die ATPase-Domäne beinhalten. Die Bereiche der cDNA, die die Aminosäuren 1-418, 51-418, 101-418, 168-418 und 201-418 einschlossen, wurden wie beschrieben mittels PCR amplifiziert, in den Vektor pET-303 kloniert und in E. coli BL21-AI exprimiert. GST-YopM wurde wie unter III.2.3.3.2 dargestellt aufgereinigt. Anschließend wurde der GST-Pulldown wie unter III.2.3.8 erläutert durchgeführt. Das Ergebnis ist in Abbildung 32 dargestellt. 72 IV Ergebnisse A ATPase N 100 200 Helikase 300 400 500 C 600 His-DDX3_201-418 His-DDX3_1-418 His-DDX3_51-418 His-DDX3_101-418 His-DDX3_168-418 M His-DDX3_1-418 His-DDX3_51-418 His-DDX3_101-418 His-DDX3_168-418 His-DDX3_201-418 B 55 – 43 – 34 – 26 – GST- Pulldown 55 – 43 – 34 – 26 – Input WB α His 88 – GST- YopM GST 26 – Coomassie Abbildung 32: Pulldown von His-DDX3 mittels GST-YopM. A: Schematische Darstellung von DDX3. B: Pulldown der Konstrukte 6x His-DDX3_1-418, 6x His-DDX3_51-418, 6x His-DDX3_101-418, 6x His-DDX3_168-418 und 6x His-DDX3_201-418 mit GST-YopM bzw. GST. GSTPulldown bzw. Input dargestellt im Western Blot, inkubiert mit HisProbe™-HRP (Thermo Scientific, USA). GSTYopM bzw. GST gefärbt mit Coomassie. M: Molekulargewicht in kDa. Abbildung 32 zeigt, dass die als unstrukturiert vorhergesagte Region von DDX3 (1-168) für die Bindung an YopM notwendig ist. So binden die Konstrukte 6x His-DDX3_1-418, 6x HisDDX3_51-418 und 6x His-DDX3_101-418 an GST-YopM, die weiter trunkierten Konstrukte 6x His-DDX3_168-418 und 6x His-DDX3_201-418 jedoch nicht. Die Kontrolle zeigt, dass keines der Konstrukte an GST alleine bindet. Leider war es nicht möglich den unstrukturierten Bereich von DDX3 1-168 bzw. den minimalen Bereich 101-168 in diesem Experiment zu untersuchen, da keine stabilen His-Fusionsproteine im heterologen E. coli Expressionssystem gebildet wurden. Für eingehendere Untersuchungen zur Interaktion von DDX3 und YopM, wurden die drei His-DDX3 Konstrukte (6x His-DDX3_1-418, 6x HisDDX3_51-418 und 6x His-DDX3_101-418) im größeren Maßstab exprimiert und aufgereinigt. IV.3.2 Heterologe Expression und Aufreinigung von DDX3 Nach der Aufreinigung der Proteine mittels Ni-NTA-Agarosse (Abschnitt III.2.3.3.1) wurde eine analytische Größenausschlusschromatographie durchgeführt. Diese erlaubt die Bestimmung der Dispersität der Lösung, sowie der Größe der vorhandenen Protein-Spezies. Die Größenausschlusschromatographie wurde wie unter III.2.3.3.4 beschrieben durchgeführt. Verwendet wurde die Säule HILoad 16/600 Superdex 200. 73 IV Ergebnisse Abbildung 33: Analytische Größenausschlusschromatographie von DDX3. A: Chromatogramm der Größenausschlusschromatographie dreier verschiedener DDX3-Konstrukte. DDX3_1-418 eluiert bei einem Volumen von 80,65 ml, DDX3_51-418 bei 84,13 ml und DDX3_101-418 bei 86,21 ml. Die graue Linie zeigt den Lauf des „Biorad Gel Filtration Standards“. B: SDS-PAGE der jeweiligen Elutionsfraktionen aus A; oberes Gel: DDX3_1-418, mittleres Gel DDX3_51-418, unteres Gel: DDX3_101-418. M: Größenstandard, Molekulargewicht in kDa. C: Blot der normalisierten Elutionsvolumina Ve/Vo gegen das Molekulargewicht in Dalton. Die Eichgerade entstand aus dem Fit der Elutionsvolumina der Größenmarker Thyroglobulin (670 kDa), γ-globulin (158 kDa), Ovalbumin (44 kDa), Myoglobin (17 kDa) und Vitamin B 12 (1,35 kDa). Abbildung 33 zeigt das Ergebnis der analytischen Gelfiltration von drei verschiedenen DDX3 Konstrukten. Alle getesteten Konstrukte eluieren in einem Einzelpeak, d.h. es liegt jeweils nur eine Spezies des Proteins vor. Die Lösung ist monodispers. Desweiteren eluieren die Proteine ihrer Größe nach, in der Reihenfolge ihrer vorhergesagten Molekulargewichte (Abbildung 33 A). Laut ProtParam (Gasteiger et al. 2005) lauten diese für DDX3_1-418: 47 kDa, für DDX3_51-418: 41 kDa und für DDX3_101-418: 36 kDa. In der denaturierenden SDS-PAGE in Abbildung 33 B sind die Elutionsfraktionen aufgetragen. Die Molekulargewichte der Konstrukte anhand ihres Laufverhaltens im SDS-Gel decken sich mit den Vorhersagen. Die Auswertung der tatsächlichen Größe der Proteine unter Zuhilfenahme der aus der Eichgerade in Abbildung 33 C erhaltenen Gleichung bestätigt die Werte ebenfalls. Die anhand der Elutionsvolumina errechneten Molekulargewichte der Proteine lauten: DDX3_1-418: 52 kDa, DDX3_51-418: 38 kDa DDX3_101-418: 31 kDa. Die errechneten Größen deuten wiederum darauf hin, dass alle Konstrukte als Monomere in nativer Lösung vorliegen. Das einzige Konstrukt welches sich auch nach mehreren Tagen als stabil herausstellte, war DDX3_51-418. DDX3_1-418 begann bereits nach kurzer Zeit sehr stark zu degradieren und DDX3_101-418 neigte zu Oligomerisierung. Als weitere Qualitätskontrolle wurden DDX3_51-418 sowie DDX3_101-418 im DLS wie unter III.2.4.1 beschrieben untersucht. 74 IV Ergebnisse A B Abbildung 34: Dynamische Lichtstreuung von DDX3. Heatmap der Größenverteilung der hydrodynamischen Radii von A: DDX3_51-418 und B: DDX3_101-418 über einen Zeitraum von 80 Sekunden. Aus den in Abbildung 34 dargestellten Messungen der dynamischen Lichtstreuung geht hervor, dass DDX3_51-418 sowie DDX3_101-418 einigermaßen monodispers vorlagen. Die ermittelten hydrodynamische Radii lagen bei 2,82 ± 0,38 nm für DDX3_51-418 und 2,91 ± 0,28 für DDX3_101-418. Die daraus resultierenden Molekulargewichte betragen 35,42 kDa bzw 38,04 kDa. IV.3.3 Struktur von DDX3_51-418 in Lösung Als Basis für spätere Untersuchungen zur Struktur des Komplexes aus YopM und DDX3 in Lösung und um Aufschluss über den für die Bindung notwendigen, jedoch als unstrukturiert vorhergesagten Bereich von DDX3 zu bekommen, wurde DDX3_51-418 mittels Röntgenkleinwinkelstreuung untersucht. Hierzu wurde DDX3_51-418 wie zuvor beschrieben aufgereinigt. Die Probe wurde bei 20 000 x g und 4°C für eine Stunde zentrifugiert (5810R, Eppendorf, G) und mit Hilfe eines 100 nm Zentrifugenfilters (Ultrafree-MC, Millipore, USA) von größeren Partikeln befreit. Anschließend wurden fünf verschiedene Konzentrationen (0,7; 1,0; 1,5; 1,8 und 2,0 mg/ml) eingestellt, die mittels DLS auf Monodispersität überprüft wurden. Da das Protein oberhalb der Grenze von 2,5 mg/ml präzipitierte, konnten keine Lösungen mit höheren Konzentrationen hergestellt werden. Die Proben wurden anschließend an Beamline P12 (EMBL, HASYLAB/DESY, Hamburg, G) vermessen. Die erhaltenen Daten wurden auf Strahlenschäden kontrolliert und mit dem Programm Primus (Konarev et al. 2003) der Proteinkonzentrationen entsprechend skaliert. Die Messkurven der Proben wurden durch Subtraktion der Streukurven der reinen Pufferlösungen normalisiert. Das Programm GNOM (Semenyuk & Svergun 1991) lieferte den Trägheitsradius Rg, sowie den maximalen Durchmesser Dmax, welche Aufschluss auf die Größe der Moleküle gaben. Die Ergebnisse der Größenbestimmungen sind in Tabelle 29 zusammengefasst. 75 IV Ergebnisse Tabelle 29: Ergebnisse der SAXS-Messung von DDX3_51-418 Konzentration [mg/ml] 0,7 1,0 1,5 1,8 2,0 Rg [nm] 2,7 ± 0,3 2,7 ± 0,4 2,8 ± 0,2 2,9 ± 0,2 2,8 ± 0,2 Dmax [nm] 9 9 10 10 10 VPorod [nm3] 74 64 79 78 74 MW I(0) [kDa] 23 24 24 31 21 MWPorod [kDa] 46 40 50 48 46 Das anhand des Porod Volumens errechnete Molekulargewicht von ~46 kDa kommt dem theoretischen Molekulargewicht von 41 kDa für ein Monomer ziemlich nahe. Das Molekulargewicht aus der Vorwärtsstreuung liegt etwas unter dem erwarteten Wert. Mit Hilfe von GASBOR (Svergun et al. 2001) konnte ein ab initio-Modell erstellt werden. Das Programm nimmt hierzu eine definierte Anzahl an Sphären, die in ihrem Volumen dem Mittel aller Aminosäuren entsprechen und konstruiert eine Reihe von Modellen, deren theoretisches Streuprofil mit den tatsächlichen Messwerten abgeglichen wird. Ein weiterer Ansatz bestand darin, den flexiblen Teil (51-167) mit Hilfe von CORAL (Petoukhov et al. 2012) an die vorhandene Struktur von DDX3_168-418 zu modellieren. Letztere wurde aus der Struktur 2I4I (Högbom et al. 2007) extrahiert. In einem letzten kombinierten Ansatz wurde ein Modell von DDX3_51-167, welches mit Hilfe der HomologieModellierungssoftware ITASSER (Roy et al. 2010) entstand, manuell in vier Teile geschnitten um Flexibilität zu simulieren. Diese Fragmente wurden zusammen mit der vorher beschriebenen Struktur von DDX3 167-418 unter Zuhilfenahme des Programmes SASREF (Petoukhov & Svergun 2005) zu einem weiteren möglichen Modell verknüpft. Die drei Modelle besitzen eine gewisse Variabilität, gehen jedoch eindeutig auf eine gemeinsame Grundform zurück. Desweiteren zeigen alle Modelle sehr gute Fits im Vergleich der theoretischen Streukurven mit den Messwerten (Abbildung 35), was jedoch zum Teil auf verstärktes Hintergrundrauschen der Messwerte zurückzuführen ist. 76 IV Ergebnisse Abbildung 35: Modelle von DDX3_51-418. Drei auf Grundlage der SAXS Daten entwickelte Modelle von DDX3 mit den korrespondierenden CRYSOL (Svergun et al. 1995)-Fits. A: ab initio-Modell entwickelt mit der Software GASBOR (Svergun et al. 2001). χ = 0,81 B: Modellierung des unbekannten N-terminus mittels CORAL (Petoukhov et al. 2012) χ = 0,86 C: Kombinierter Ansatz aus ITASSER (Roy et al. 2010) und SASREF (Petoukhov & Svergun 2005) χ = 0,86. IV.3.4 Bestimmung der Bindungsaffinität von YopM und DDX3 Zur weiteren Charakterisierung der Interaktion zwischen YopM und DDX3 wurden Untersuchungen zur Bindungsaffinität mittels MST in einem Monolith NT.115 (NanoTemper Technologies, G) durchgeführt (III.2.3.9). Hierzu wurden die Fragmente DDX3_1-418 und DDX3_51-418 exprimiert und mittels IMAC und Größenausschlusschromatographie aufgereinigt. Die so gereinigten Proteine wurden mit Hilfe des Monolith™ NT.115 Protein Labeling Kits RED-NHS (NanoTemper Technologies, G) laut Protokoll mit dem Fluoreszensfarbstoff NT-647 versehen. Das Labeling der Proben wurde mit Hilfe des NanoDrop® ND-1000 (Peqlab, G) spektroskopisch überprüft. Die für das Bindungsexperiment einzusetzende Menge wurde in einer dreifach Messung bei 50 % LED-Power in Standardkapillaren ermittelt. Ebenso wurden verschiedene Pufferzusammensetzungen und Kapillaren getestet, um eine stabile Thermophorese zu gewährleisten. Zur finalen Messung wurden 50 nM gelabeltes Protein in MST-Reaktionspuffer (Tabelle 12) eingesetzt. Das Experiment wurde in hydrophilen Kapillaren durchgeführt. YopM_Full und YopM_Core wurden wie zuvor beschrieben exprimiert und aufgereinigt. In einem Experiment wurden 16 unterschiedliche Konzentrationen von YopM_Full bzw. YopM_Core in einer 1:1 Verdünnungsreihe zu dem gelabelten DDX3-Konstrukt titriert und die Änderung in der Thermophorese wurde gemessen. Der Titrationsbereich für YopM_Full betrug 6,85- 224 000 nM, für YopM_Core 8,48- 278 000 nM. 77 IV Ergebnisse A Kd: 11,6 1,3 µM 50 Kd: 18,1 5,3 µM 60 40 20 0 0 10 0 DDX3_1-418/YopM_Core 80 Fnorm [1/1000] 100 Fnorm [1/1000] B DDX3_1-418/YopM_Full 10 1 10 2 10 3 10 4 10 5 10 6 10 0 Konzentration [nM] 10 1 10 2 10 3 10 4 10 5 10 6 Fluoreszenz Fluoreszenz Konzentration [nM] Zeit [s] Zeit [s] Abbildung 36: Ergebnis der MST von DDX3_1-418 mit YopM_Full bzw. YopM_Core. Dargestellt sind die Ergebnisse der MST-Messungen mit gelabeltem DDX3_1-418. Geblottet ist die Amplitude der normierten Fluoreszenz gegen die Konzentration des ungelabelten YopM_Full bzw. YopM_Core. Darunter dargestellt sind die korrespondierenden Thermophoresekurven des jeweiligen Experiments im Zeitverlauf A: Kd Bestimmung von DDX3_1-418 und YopM_Full. B: Kd Bestimmung von DDX3_1-418 und YopM_Core. Abbildung 36 zeigt das Ergebnis der MST-Experimente von DDX3_1-418 mit YopM_Full bzw. YopM_Core bei einer Laser-Power von 60 %. Es ist eine deutliche Änderung des Thermophoreseverhaltens von DDX3_1-418 in Abhängigkeit der Konzentration von YopM_Full bzw. YopM_Core zu erkennen. Diese äußern sich in einer Amplitude von maximal 110 (YopM_Full) bzw. 70 (YopM_Core) relativen Fluoreszenzeinheiten. Die Analyse der Konzentrationsabhängigkeiten dieser Fluoreszenzänderungen ergibt eine Kd von ca. 12 µM für die Interaktion von YopM_Full mit DDX3_1-418 und eine Kd von ca. 18 µM für die Interaktion mit YopM_Core. Zum Vergleich wurden weitere Experimente mit DDX3_51-418 durchgeführt. 78 IV Ergebnisse A DDX3_51-418/YopM_Core 80 Kd: 9,2 0,8 µM Fnorm [1/1000] 100 Fnorm [1/1000] B DDX3_51-418/YopM_Full 50 40 20 0 0 10 0 Kd: 21,1 5,1 µM 60 10 1 10 2 10 3 10 4 10 5 10 6 10 0 10 1 Konzentration [nM] 10 2 10 3 10 4 10 5 10 6 Fluoreszenz Fluoreszenz Konzentration [nM] Zeit [s] Zeit [s] Abbildung 37: Ergebnis der MST von DDX3_51-418 mit YopM_Full bzw. YopM_Core. Dargestellt sind die Ergebnisse der MST-Messungen mit gelabeltem DDX3_51-418. Geblottet ist die Amplitude der normierten Fluoreszenz gegen die Konzentration des ungelabelten YopM_Full bzw. YopM_Core. Darunter dargestellt sind die korrespondierenden Thermophoresekurven des jeweiligen Experiments im Zeitverlauf A: Kd Bestimmung von DDX3_51-418 und YopM_Full. B: Kd Bestimmung von DDX3_51-418 und YopM_Core. Abbildung 37 zeigt das Ergebnis der MST-Experimente von DDX3_51-418 mit YopM_Full bzw. YopM_Core bei einer Laser-Power von 60 %. Die Analyse der Konzentrationsabhängigkeiten der Fluoreszenzänderungen ergibt ein ähnliches Bild wie zuvor. Die Kd für die Interaktion von YopM_Full mit DDX3_1-418 liegt bei ca. 9 µM und eine für die Interaktion mit YopM_Core bei ca. 21 µM. A 0.5 YopM_Full Kd: 11,9 3,4 µM YopM_Core Kd: 18,1 5,3 µM 0.0 10 0 YopM_Full/DDX3 1.0 Gebundener Anteil 1.0 Gebundener Anteil B DDX3_1-418/YopM 0.5 DDX3_1-418 Kd 11,93 3,4 µM DDX3_51-418 Kd: 9,2 0,8 µM 0.0 10 1 10 2 10 3 10 4 10 5 10 6 10 0 Konzentration [nM] 10 1 10 2 10 3 10 4 10 5 10 6 Konzentration [nM] Abbildung 38: Vergleich der Bindungsaffinitäten. Dargestellt ist der Vergleich der Bindungskurven anhand der gebundenen Fraktionen in Abhängigkeit der Konzentration des Bindungspartners. A: Vergleich der Bindungen von YopM_Full und YopM_Core mit DDX3_1418. B: Vergleich der Bindungen von DDX3_1-418 und DDX3_51-418 mit YopM_Full. Der in Abbildung 38 dargestellte Vergleich der Bindungsexperimente zeigt, dass es keinen Unterschied in den Bindungsaffinitäten von DDX3_1-418 und DDX3_51-418 mit YopM_Full gibt (Abbildung 38 B). YopM_Core bindet marginal schlechter als das Volllängenkonstrukt. Dieser Unterschied ist jedoch vor allem in Anbetracht des statistischen Fehlers zu vernachlässigen (Abbildung 38 A). 79 IV Ergebnisse IV.3.5 Darstellung des Komplexes aus YopM und DDX3 mittels Größenausschlusschromatographie Um die Komplexbildung zwischen YopM und DDX3 zu überprüfen wurden mit verschiedenen Fragmenten der beiden Proteine analytische Gelfiltrationen durchgeführt. Hierzu erfolgte zunächst die Aufreinigung der beiden Bindungspartner wie beschrieben und die Elutionsprofile der einzelnen Proteine wurden aufgezeichnet. Zur Etablierung des Komplexes wurden dann beide Bindungspartner in äquimolaren Mengen zusammengebracht und 30 min auf Eis inkubiert. Anschließend wurde die Probe auf eine Superdex 200 10/300 GL appliziert und der Lauf wurde wie unter III.2.3.3.4 beschrieben durchgeführt. Alle Gelfiltrationsläufe fanden in 50 mM Hepes-Puffer pH 7,5 mit 150 mM NaCl und 2 mM DTT statt. Das Ergebnis der analytischen Größenausschlusschromatographie von YopM_Full und DDX3 1-418, sowie des Komplexes aus beiden Proteinen ist in Abbildung 39 dargestellt. 200 YopM/DDX3 YopM_1-506 DDX3_1-418 150 100 50 0 1 2 3 4 5 6 7 0 5 B M 20 C 1 2 3 4 5 6 7 10 6 70 – 55 – 10 15 Elutionsvolumen Ve [ml] YopM DDX3 40 – 55 – YopM 1-506 55 – DDX3 1-418 Molekulargewicht [Da] Absorption 280nm [mAu] A y 10 5 = 3E+08e-4,967x R² = 0,9812 YopM/DDX3 YopM_1-506 DDX3_1-418 10 4 10 3 1.0 1.5 2.0 2.5 Ve /Vo Abbildung 39: Analytische Größenausschlusschromatographie des Komplexes aus YopM_Full und DDX3_1-418. A: Chromatogramm der Größenausschlusschromatographie. YopM 1-506 eluiert bei einem Volumen von 13,15 ml, DDX3_1-418 bei 14,74 ml und der Komplex bei 12,74 ml. B: SDS-PAGE der jeweiligen Elutionsfraktionen 1-7 aus A; M: Größenstandard, Molekulargewicht in kDa. C: Blot der normalisierten Elutionsvolumina Ve/Vo gegen das Molekulargewicht in Dalton. Die Eichgerade entstand aus dem Fit der Elutionsvolumina der Größenmarker Thyroglobulin (670 kDa), γ-globulin (158 kDa), Ovalbumin (44 kDa), Myoglobin (17 kDa) und Vitamin B 12 (1,35 kDa). Das Chromatogramm der analytischen Gelfiltration in Abbildung 39 A zeigt die Einzelläufe von YopM_Full in grün, DDX3 in blau und dem Komplex aus beiden Proteinen in rot. In allen drei Läufen sind Einzelpeaks zu erkennen, was bedeutet, dass jeweils nur eine Größenspezies in den Lösungen vorlag. Im Vergleich mit YopM_Full zeigt die Komplexkurve eine deutliche Verschiebung nach links, d.h. eine Volumenzunahme. Desweiteren war eine deutlich spätere Elution von DDX3_1-418 festzustellen. Die Analyse der Peakfraktionen mittels denaturierender SDS-PAGE in Abbildung 39 B zeigt, dass sowohl YopM_Full als 80 IV Ergebnisse auch DDX3_1-418 in dem Elutionspeak der Komplexkurve zu finden sind. Aufgrund der Bandenintensität bei ähnlichem Molekulargewicht ist ebenso zu erkennen, dass eine größere Menge YopM als DDX3 im Komplex vorzuliegen scheint. Die Peakfraktionen der beiden Einzelläufe enthalten, wie erwartet, die Proteine YopM_Full bzw. DDX3_1-418. Die Errechnung der Molekulargewichte mittels der Geradengleichung aus Abbildung 39 C spiegelt das zuvor gewonnene Bild wider. Für YopM_Full ergibt sich ein Molekulargewicht von 105 kDa, DDX3_1-418 liegt bei 41 kDa. Die theoretischen Molekulargewichte der Monomere, welche sich auch in der SDS-PAGE darstellen, liegen für YopM_Full bei 58 kDa und für DDX3_1-418 bei ca. 47 kDa. Das errechnete Molekulargewicht des Komplexes liegt bei 135 kDa. Anschließend wurde das Fragment DDX3_51-418 auf seine Bindung zu YopM_Full hin untersucht. 300 YopM/DDX3 YopM_1-506 DDX3_51-418 200 100 0 1 2 3 4 5 6 7 8 0 5 10 15 Elutionsvolumen Ve [ml] B M 55 – 40 – 55 – 40 – 55 – 40 – 20 C 1 2 3 4 5 6 7 8 10 6 YopM/ DDX3 YopM 1-506 DDX3 51-418 Molekulargewicht [Da] Absorption 280nm [mAu] A y 10 5 = 3E+08e-4,967x R² = 0,9812 YopM/DDX3 YopM_1-506 DDX3_51-418 10 4 10 3 1.0 1.5 2.0 2.5 Ve /Vo Abbildung 40: Analytische Größenausschlusschromatographie des Komplexes aus YopM_Full und DDX3_51-418. A: Chromatogramm der Größenausschlusschromatographie. YopM 1-506 eluiert bei einem Volumen von 13,27 ml, DDX3_51-418 bei 15,36 ml und der Komplex bei 12,9 ml. B: SDS-PAGE der jeweiligen Elutionsfraktionen 1-8 aus A; M: Größenstandard, Molekulargewicht in kDa. C: Blot der normalisierten Elutionsvolumina Ve/Vo gegen das Molekulargewicht in Dalton. Die Eichgerade entstand aus dem Fit der Elutionsvolumina der Größenmarker Thyroglobulin (670 kDa), γ-globulin (158 kDa), Ovalbumin (44 kDa), Myoglobin (17 kDa) und Vitamin B 12 (1,35 kDa). Die Untersuchung der Fragmente YopM_Full und DDX3_51-418 zeigt, dass sich auch hier ein Komplex darstellen ließ, der in der Gelfiltration stabil war. Der Peak des Komplexes ist mit 12,9 ml deutlich vor den Einzelpeaks angesiedelt. Das errechnete Molekulargewicht beträgt für den Komplex: 121 kDa, für YopM_Full: 97 kDa und für DDX3_51-418: 28 kDa. Alle drei Elutionen schienen leicht verzögert, jedoch ergab sich ein ähnliches Bild wie bei YopM_Full/DDX3_1-418. 81 IV Ergebnisse 100 YopM/DDX3 YopM_1-506 DDX3_101-418 Absorption 280nm [mAu] 50 0 1 2 3 4 5 6 0 5 B M 55 – 40 – 55 – 40 – 55 – 40 – 10 15 Elutionsvolumen Ve [ml] 20 C 1 2 3 4 5 6 10 6 YopM DDX3 YopM 1-506 DDX3 101-418 Molekulargewicht [Da] A y 10 5 = 3E+08e-4,967x R² = 0,9812 YopM/DDX3 YopM_1-506 DDX3_101-418 10 4 10 3 1.0 1.5 2.0 2.5 Ve /Vo Abbildung 41: Analytische Größenausschlusschromatographie des Komplexes aus YopM_Full und DDX3_101-418. A: Chromatogramm der Größenausschlusschromatographie. YopM 1-506 eluiert bei einem Volumen von 12,93 ml, DDX3_101-418 bei 15,33 ml und der Komplex bei 12,73 ml. B: SDS-PAGE der jeweiligen Elutionsfraktionen 1-6 aus A; M: Größenstandard, Molekulargewicht in kDa. C: Blot der normalisierten Elutionsvolumina Ve/Vo gegen das Molekulargewicht in Dalton. Die Eichgerade entstand aus dem Fit der Elutionsvolumina der Größenmarker Thyroglobulin (670 kDa), γ-globulin (158 kDa), Ovalbumin (44 kDa), Myoglobin (17 kDa) und Vitamin B12 (1,35 kDa). Die Analyse der Komplexbildung aus YopM_Full und DDX3_101-418 zeigt einige Unterschiede zu den vorherigen Experimenten. Zwar lässt sich der Komplex darstellen, jedoch ist eine Tendenz zur Oligomerisierung von DDX3_101-418 zu erkennen. Der Hauptpeak bei 15,33 ml ergibt ein Molekulargewicht von 28 kDa, was etwas geringer ist als die erwartete Masse von 36 kDa. Diese Abweichung ist jedoch vernachlässigbar. Zudem ist ein zweiter, deutlich früherer Elutionspeak bei 13,74 ml zu beobachten, der auf ein Molekulargewicht von ca. 74 kDa hindeutet. Die Auftragung in der SDS PAGE zeigte jedoch lediglich die DDX3-Bande, was ein eindeutiges Indiz für die vermutete Multimerisierung ist. Hinzu kommt, dass im Gegensatz zu den anderen untersuchten Fragmenten, nicht das gesamte Protein im Komplex gebunden war, sondern ein großer Anteil in Fraktion 5 und 6 verblieb. Zuletzt wurde die Komplexbildung des kristallisierten Fragmentes YopM_Core (AS 34-481) Mit dem Fragment DDX3_1-418 untersucht. 82 IV Ergebnisse A Absorption 280nm [mAu] 200 YopM/DDX3 YopM_34-481 DDX3_1-418 150 100 50 0 1 2 3 4 5 6 7 0 5 10 15 Elutionsvolumen Ve [ml] B 55 – 40 – 55 – 40 – 55 – 40 – C 1 2 10 6 3 4 5 6 7 YopM DDX3 YopM 34-481 DDX3 1-418 Molekulargewicht [Da] M 20 y 10 5 = 3E+08e-4,967x R² = 0,9812 YopM/DDX3 YopM_34-481 DDX31-418 10 4 10 3 1.0 1.5 2.0 2.5 Ve /Vo Abbildung 42: Analytische Größenausschlusschromatographie des Komplexes aus YopM_Core und DDX3_1-418. A: Chromatogramm der Größenausschlusschromatographie. YopM 34-481 eluiert bei einem Volumen von 13,85 ml, DDX3_1-418 bei 14,74 ml und der Komplex bei 12,82 ml. B: SDS-PAGE der jeweiligen Elutionsfraktionen 1-6 aus A; M: Größenstandard, Molekulargewicht in kDa. C: Blot der normalisierten Elutionsvolumina Ve/Vo gegen das Molekulargewicht in Dalton. Die Eichgerade entstand aus dem Fit der Elutionsvolumina der Größenmarker Thyroglobulin (670 kDa), γ-globulin (158 kDa), Ovalbumin (44 kDa), Myoglobin (17 kDa) und Vitamin B 12 (1,35 kDa). Abbildung 42 zeigt, dass sich auch mit dem YopM_Core Fragment ein stabiler Komplex mit DDX3_1-418 darstellen ließ. Die errechneten Molekulargewichte liegen bei 85 kDa für YopM_Core, 41 kDa für DDX3_1-418 und 127 kDa für den Komplex. Die gesammelten Resultate deuteten daraufhin, dass ein stabiler Komplex mit allen getesteten Kombinationen möglich war. Dieser Komplex hatte zudem in jedem Fall ein höheres Molekulargewicht als ein Heterodimer aus YopM und DDX3 erwarten ließ. 83 IV Ergebnisse IV.4 Strukturanalyse des Komplexes aus YopM und DDX3 Aufgrund der zuvor gesammelten Ergebnisse wurde die Kombination aus YopM_Core und DDX3_51-418 für weitergehende Untersuchungen zur Komplexstruktur herangezogen. YopM_Core ließ sich zum einen mit einer höheren Ausbeute als das Volllängenprotein in E. coli exprimieren, zum anderen konnte bereits gezeigt werden, dass sich YopM_Core sehr gut kristallisieren ließ. Desweiteren sollte die YopM_Core Kristallstruktur eine gute Basis für Untersuchungen des Komplexes in Lösung darstellen. DDX3_51-418 stellte das am besten geeignete DDX3_Konstrukt dar. DDX3_1-418 war nicht sehr stabil und degradierte teilweise bereits Stunden nach der Aufreinigung aus E. coli. DDX3_101-418 zeigte wie bereits erwähnt Oligomerisierung bzw. eine weniger stabile Bindung zu YopM. YopM_Full und DDX3_51-418 wurden wie beschrieben aufgereinigt und der Komplex wurde mittels Größenausschlusschromatographie überprüft. Vor den Kristallisationsansätzen bzw. vor Experimenten mittels Röntgenkleinwinkelstreuung wurde die Probe ebenfalls mittels DLS überprüft. Abbildung 43: DLS von YopM_Core und YopM_Core/DDX3_51-418. Heatmap der Größenverteilung der hydrodynamischen Radii von A: YopM_Core und B: Komplex aus YopM_Core und DDX3_51-418 über einen Zeitraum von 80 Sekunden. Der Komplex aus YopM_Full und DDX3_51-418 war monodispers in Lösung (Abbildung 43 B) Im Vergleich zu YopM_Core (4,2 nm) zeigt dieser einen erhöhten hydrodynamischen Radius von 4,91 nm. IV.4.1 Kristallisation von YopM/DDX3 Für die Kristallisation wurde eine Lösung des Komplexes mit eine Konzentration von 10,5 mg/ml hergestellt und gegen ein tausendfaches Volumen 50 mM Hepes pH 7,5 über Nacht bei 4°C dialysiert. Für die Suche nach initialen Kristallisationsbedingungen wurden die kommerziellen Screens PACT premier™, Stura Footprint™, Morpheus (Molecular Dimensions, UK) und Classic, ComPAS, JCSG+, Protein Complex Suite (Quiagen, Deutschland) verwendet. 500 nl der Proteinlösung wurden wie in III.2.4.3.1 beschrieben unter Zuhilfenahme eines Pipettierroboters (Honeybee 961 Genomic solutions, UK) in spezielle 96-Well Platten (NeXtal QIA1 μplates 96 Well, Qiagen, Deutschland) pipettiert und 1:1 mit Präzipitantenlösung gemischt. Die Platten wurden bei Raumtemperatur inkubiert und wöchentlich mikroskopisch 84 IV Ergebnisse untersucht. Insgesamt wurden somit 672 Bedingungen getestet. Nach vier Wochen zeigten sich bei der Bedingung JCSG+ D2 (0,1 M Hepes pH 7,5; 0,2 M MgCl2; 30 % PEG400) Kristalle. Abbildung 44: Kristalle des Komplexes aus YopM_Core und DDX3_51-418. Kristalle des Komplexes aus YopM_Full und DDX3_51-418. Gewachsen nach vier Wochen bei einer Tropfengröße von 500 nl Proteinlösung (c: 10,5 mg/ml) gemischt mit 500 nl Präzipitantenlösung (0,1 M Hepes pH 7,5; 0,2 M MgCl2; 30% PEG400) im sitting drop-Verfahren über einem Reservoir aus 50 µl purer Präzipitantenlösung. Um zu überprüfen ob die sehr kleinen Kristalle die gewünschten Proteine enthielten, wurden sie durch mehrfache Überführung in Präzipitantenlösung gewaschen, in SDS-Probenpuffer aufgekocht und mittels SDS-PAGE und Western Blot analysiert. M α DDX3 B α YopM A 130 – 70 – 55 – 40 – 35 – 25 – 15 – Abbildung 45: Analyse der Komplexkristalle. A: Kristalle gewaschen in Präzipitantenlösung (0,1 M Hepes pH 7,5; 0,2 M MgCl2; 30 % PEG400) B: Analyse der Kristalle mittels Western Blot und Antikörpern gegen YopM bzw. DDX3. Die Kristalle wurden in SDS-Probenpuffer aufgekocht, die darin enthaltenen Proteine wurden elektrophoretisch aufgetrennt und auf eine PVDF-Membran geblottet. Die Membran wurde dann zuerst mit YopM-Antikörper analysiert und nach Trocknung der Membran am darauffolgenden Tag mit DDX3-Antikörper inkubiert. 85 IV Ergebnisse Abbildung 45 zeigt, dass die produzierten Kristalle tatsächlich sowohl YopM als auch DDX3 enthielten. Da die Kristalle jedoch für eine umfassende Strukturanalyse zu klein und verwachsen waren, wurden Optimierungsansätze mit der identischen Ausgangslösung durchgeführt. Leider konnte die Bedingung nicht erfolgreich reproduziert werden. Eine nähere Untersuchung der Ausgangslösung mittels DLS und SDS-PAGE zeigte, dass die darin enthaltenen Proteine degradiert und aggregiert waren. Abbildung 46: Überprüfung der Proteinlösung. A: Heatmap der Größenverteilung des hydrodynamischen Radius von YopM_Core/DDX3_51-418 zum Zeitpunkt des initialen Kristallisationsscreens und B: zum Zeitpunkt der Optimierungsansätze. C: Analyse des Proteingemisches mittels SDS-PAGE. IV.4.2 Struktur des Komplexes aus YopM und DDX3 in Lösung Um trotz der Schwierigkeiten bei der Kristallisation aufgrund der deutlich begrenzten Haltbarkeit des Komplexes aus YopM und DDX3 einen Eindruck über dessen Struktur zu gewinnen, wurden SAXS-Experimente an Beamline P12 (EMBL, HASYLAB/DESY, Hamburg, G) durchgeführt. Obwohl DDX3_51-418 ab einer Grenze von 2,5 mg/ml zu präzipitieren begann war es möglich höhere Konzentrationen des Proteins im Komplex mit YopM_Core zu erreichen. Hierzu wurden zunächst YopM_Core und DDX3_51-418 wie zuvor beschrieben aufgereinigt. Danach wurden die einzelnen Proteine zusammenpipettiert und der Komplex wurde mittels Gelfiltration wie unter IV.3.5 beschrieben aufgereinigt. Die Probe wurde bei 20.000 g und 4°C für 10 min zentrifugiert (5810R, Eppendorf, G) und mit Hilfe eines 100 nm Zentrifugenfilters (Ultrafree-MC, Millipore, USA) von größeren Partikeln befreit. Anschließend wurden fünf verschiedene Konzentrationen (0,66; 1,32; 2,65; 5,3 und 10,6 mg/ml) eingestellt, die mittels DLS auf Monodispersität überprüft wurden. Die Proben wurden anschließend vermessen. Die erhaltenen Daten wurden auf Strahlenschäden kontrolliert und mit dem Programm Primus (Konarev et al. 2003) der Proteinkonzentrationen entsprechend skaliert. Die Messkurven der Proben wurden durch Subtraktion der Streukurven der reinen Pufferlösungen normalisiert. Das Programm GNOM (Semenyuk & Svergun 1991) lieferte den Trägheitsradius Rg, sowie den maximalen Durchmesser Dmax, welche beide Aufschluss über die Größe der Moleküle gaben. Die Ergebnisse der Größenbestimmungen sind in Tabelle 30 zusammengefasst. 86 IV Ergebnisse Tabelle 30: Ergebnisse der SAXS-Messung des Komplexes YopM_Core/DDX3_51-418 Konzentration [mg/ml] 0,66 1,32 2,65 5,3 10,6 Rg [nm] 3,9 ± 0,3 4,0 ± 0,2 4,1 ± 0,1 4,1 ± 0,1 4,5 ± 0,1 Dmax [nm] 14 14 14 12 16 VPorod [nm3] 176 182 191 192 210 MW I(0) [kDa] 116 123 131 136 147 MWPorod [kDa] 104 107 112 113 123 Die errechneten Molekulargewichte aus der „Vorwärtsstreuung“ ~130 kDa und dem PorodVolumen 112 kDa stellen eine signifikante Erhöhung im Vergleich zu YopM dar. Die Daten bei sehr kleinen Winkeln wurden zu einer theoretischen Konzentration von 0 mg/ml extrapoliert und mit den Daten der höheren Konzentrationen zur finalen Kurve zusammengeführt. Der Vergleich der Streukurve mit der YopM_Core-Kurve zeigte einen signifikanten Unterschied bei ähnlicher Grundstruktur. Abbildung 47: Streukurven von YopM_Core und YopM_Core/DDX3_51-418. Um nun ein Bild des Komplexes in Lösung zu gewinnen, wurde mit Hilfe des Programmes SASREF (Petoukhov & Svergun 2005) unter Verwendung der YopM_Core Kristallstruktur und der unter IV.3.3 beschriebenen DDX3_51-418-Modelle nach einer Kombination gesucht, welche zu den Messwerten passte. Hierzu wurden in verschiedenen Ansätzen entweder die Komplexkurve alleine oder die Komplexkurve zusammen mit den Einzelkurven verwendet. 87 IV Ergebnisse A B Abbildung 48: Modell des Komplexes aus YopM_Core und DDX3_51-418 GASBOR. Darstellung des Komplexes aus YopM_Core (rot) und DDX3_51-418 (grün) unter Zuhilfenahme des ab initioModells. A: Darstellung der Struktur in kombinierter Ribbon-Repräsentation und Sphärenmodell in drei unterschiedlichen Perspektiven. Erstellt mit PyMol (Schrödinger LLC, USA). B: Fit des Modells (rote Kurve) zu den Messwerten (grüne Punkte). Erstellt mittels CRYSOL (Svergun et al. 1995) χ = 1,6. Abbildung 48 zeigt das Modell des YopM_Core Dimers in Komplex mit dem in IV.3.3 entwickelten DDX3_51-418 ab initio-Modell. Verschiedene Modellierungs-Läufe mit einer oder drei Kurven brachten das gleiche Ergebnis, welches einen guten Fit von χ = 1,6 zeigt. Demnach bindet DDX3_51-418 an der Dimer-Kontaktfläche von YopM_Core und der elongierte Bereich, der wahrscheinlich dem N-Terminus entspricht, interagiert mit der konkaven Seite von YopM. Ein weiterer Ansatz bestand in der Modellierung des Komplexes aus dem YopM_Core-Dimer und dem DDX3_51-418 SASREF-Modell aus IV.3.3. Hierzu wurden ebenfalls mehrere Läufe mit unterschiedlicher Kombination der Messkurven verglichen. 88 IV Ergebnisse A B Abbildung 49: Modell des Komplexes aus YopM_Core und DDX3_51-418 SASREF. Darstellung des Komplexes aus YopM_Core (rot) und DDX3_51-418 (grün und gelb) unter Zuhilfenahme des SASREF-Modells. A: Darstellung der Struktur in Ribbon-Repräsentation in drei unterschiedlichen Perspektiven. Erstellt mit PyMol (Schrödinger LLC, USA). B: Fit des Modells (rote Kurve) zu den Messwerten (grüne Punkte). Erstellt mittels CRYSOL (Svergun et al. 1995) χ = 1,36. Der Ansatz mit dem SASREF-Modell von DDX3_51-418 zeigt ein sehr ähnliches Bild wie zuvor bei der Simulation mit dem ab initio Modell. Hierbei ist deutlich zu erkennen, dass der neu modellierte elongierte N-Terminus an der Dimer-Kontaktfläche bindet und sich in die konkave Seite von YopM einfügt. Der Fit dieses Modells fiel mit χ = 1,36 sogar noch besser aus als der des „ab initio-Modells“. Eine Modellierung eines 1:1 Komplexes aus YopM_Core und DDX3_1-418 mit einem annehmbaren Fit war hingegen nicht erfolgreich. 89 IV Ergebnisse Abbildung 50: Modell des Komplexes aus YopM_Core Monomer und DDX3_51-418. Darstellung eines potentiellen Komplexes aus YopM_Core Monomer (rot) und DDX3_51-418 (grün und gelb) Erstellt mit PyMol (Schrödinger LLC, USA). A: Darstellung des Ansatzes mit dem DDX3_51-418 SASREFModells und korrespondierender Fit χ = 9,6. B: Darstellung des Ansatzes mit dem DDX3_51-418 GASBOR Modells und korrespondierender Fit χ = 8,3. Abbildung 50 zeigt den Versuch einen Komplex aus dem monomeren YopM_Core und DDX3_51-418 darzustellen. Die Simulation konnte kein zusammenhängendes Modell liefern, das den Messwerten entsprach. Ebenso konnte kein 2:2 oder 1:2 (YopM_Core: DDX4_51418) Modell erstellt werden. Dies bekräftigt die Wahrscheinlichkeit des 2:1 Komplexes. 90 V Diskussion V Diskussion Innerhalb der Gattung Yersinia gibt es lediglich drei humanpathogene Arten Y. pestis, Y. pseudotuberculosis und Y. enterocolitica. Alle drei besitzen ein 70 kb großes Virulenzplasmid pYV genannt, welches für das sogenannte Yop-Virulon codiert (Cornelis et al. 1998). Dieses System erlaubt den Bakterien im Wesentlichen die Anheftung an die Wirtszelle mittels Adhäsinen und die Einschleusung von Virulenzfaktoren, den sogenannten Yops, über ein Typ III Sekretionssystem. Während YopE, YopH, YopO, Yop P und YopT hochkonserviert in allen drei Spezies sind (bis zu 96 % Sequenzidentität), findet man in YopM eine deutliche Heterogenität (Boland et al. 1998). Die Unterschiede bei YopM sind in seiner Architektur begründet. Neben einem hochkonservierten N-Terminus mit zwei AlphaHelices und einem ungeordneten aber konservierten C-Terminus, besitzt YopM einen repetetiven Bereich mit einer variablen Anzahl an Leucin-reichen Wiederholungen (LRR). Die Anzahl dieser Repeats reicht von 13 in Y. enterocolitica 8081 (Thomson et al. 2006) bis 21 in Y. pseudotuberculosis IP32953 (Vieux & Barrick 2011). YopM ist einer der wichtigsten Virulenzfaktoren in Yersinia spp., obwohl seine tatsächliche Rolle in der Infektion immer noch unklar ist. Es wurde mit einer Reihe von Interaktionspartnern in Verbindung gebracht. So bindet es die beiden Kinasen RSK1-4 und PKN1-3 in einem ternären Komplex und beeinflusst dadurch deren Phosphorylierungsgrad (McDonald et al. 2003; Hentschke et al. 2010). In einer Vorarbeit wurde bei der Rekonstruktion des Experiments, das zur Entdeckung von RSK1 und PKN2 als Bindungspartner für YopM führte, die DEAD-Box Helikase DDX3 als neuer Interaktionspartner identifiziert. In diesem Experiment wurde ein TAP-getaggtes Konstrukt von YopM aus Y. enterocolitica WA-314 benutzt, welches 20 LRRs besitzt. YopM ist scheinbar in der Lage eine Vielzahl an Proteinen zu binden und diese in höher geordnete Komplexe zu zwingen. Deshalb war es ein Ziel dieser Arbeit durch biochemische und strukturbiologische Ansätze Hinweise über die Art der Interaktion von YopM mit seinen Bindungspartnern zu erlangen. V.1 Struktur von YopM aus Y. enterocolitica WA-314 V.1.1 Aufreinigung von YopM und Translationsstart In dieser Arbeit sollte die Architektur von YopM_WA-314, welches 20 LRRs besitzt, analysiert und mit der bekannten Struktur aus Y. pestis 195/P (YopM_195/P) verglichen werden. Hierzu wurde zunächst wie unter IV.1.1 beschrieben der annotierte ORF aus pYVWA-314 amplifiziert und in den Vektor pET_303 kloniert. Das daraus resultierende 6x Hisgetaggte YopM wurde anschließend in E. coli BL21-AI exprimiert und mittels verschiedener chromatographischer Methoden gereinigt. Abbildung 10 bis Abbildung 12 zeigen den Verlauf dieser Aufreinigungen. Während die Ni-NTA-Aufreinigung noch eine sehr große Anzahl an Unreinheiten aufzeigte, konnte nach dem letzten Reinigungsschritt mittels Größenausschlusschromatographie sauberes Protein gewonnen werden. Es zeigte sich jedoch, dass YopM nach allen Schritten als Doppelbande verblieb. Dies führte dazu, dass der Translationsstart näher untersucht wurde. Wie in Abbildung 13 dargestellt herrscht auch bei anderen in den Datenbanken hinterlegten YopM-Proteinen Uneinigkeit um den Translationsstart. Bereits bei der ersten Beschreibung des yopM-Gens aus Y. pestis KIM5 91 V Diskussion (Leung & Straley 1989) fiel auf, dass es drei mögliche Startcodons für YopM gibt. Die Analyse des transkriptionellen Startpunkts ergab ein Protein mit 367 Aminosäuren, das mit MFINP beginnt. 1996 standen Anne Boland und Kollegen vor dem selben Problem als sie yopM aus Y. enterocolitica W22703 amplifizierten und sequenzierten (Boland et al. 1996). Mittels EDMAN-Sequenzierung des in einem Yop-Release-Assay von den Bakterien in den Überstand sezernierten YopMs konnte gezeigt werden, dass das zweite Startcodon, welches zu den Aminosäuren MFINP führte der korrekte Translationsstart war. Mit der gleichen Methode konnte bewiesen werden, dass der tatsächliche Translationsstart von YopM_WA314 dem zweiten Startcodon entspricht. Die Uneinigkeit in den Datenbanken ist vermutlich auf die fortschreitende Automatisierung der Hochdurchsatzsequenzierung von Bakterien zurückzuführen, bei der einzelne Gene natürlich nicht in dem Maße detailliert untersucht werden, wie es in dieser und anderen Arbeiten von Nöten war. Die Umklonierung des yopM Gens mit dem korrekten Translationsstart führte zur Expression einer einzigen Proteinspezies, welche sich in einer einzelnen Bande im denaturierenden SDS-Gel zeigte (Abbildung 14 B). V.1.2 Kristallisation von YopM Zu Beginn der Arbeit wurde versucht YopM_WA-314 in Volllänge mit einem 6x C-terminalen His-Tag zu kristallisieren. Die Untersuchung von 672 Bedingungen in einem initialen Screen führte lediglich bei einer Bedingung (PACT B12: 0,1 M MES, 0,01 M ZnCl2, 20% w/v PEG6000, pH 6) zu Kristallen. Es handelte sich um lange dünne Nadeln, die sehr langsam wuchsen. Auch die Reproduktion dieser Bedingung führte nicht zu Kristallen, die für eine umfassende röntgenkristallographische Untersuchung geeignet waren. Als Konsequenz aus diesen Versuchen wurde ein neues N-terminal, und C-terminal trunkiertes Konstrukt hergestellt, welches lediglich den als strukturiert bekannten Bereich von Aminosäure 34-481 enthielt (Abbildung 15). Dieses Konstrukt wurde ebenfalls als 6x CT-HisFusionsprotein exprimiert, gereinigt und kristallisiert. Die Suche nach initialen Kristallisationsbedingungen zeigte schnell wachsende Kristalle bei zahlreichen Bedingungen, von denen der Großteil Polyethylenglycol als Präzipitanten verwendete. Viele dieser Bedingungen konnten erfolgreich reproduziert und optimiert werden. Die Untersuchung der Kristalle mittels Röntgenstrahlung ergab jedoch eine maximale Beugung bis 6 Å. Der Versuch die physikalische Auflösung durch Reduktion des Lösemittelanteils (Crystal Dehydration and Salvage Kit, Jena Bioscience, G), die Kristallisation mit Additiven (JBScreen Plus – Additives, Jena Bioscience, G) oder durch Seeding zu erhöhen blieben erfolglos. Erst die Verwendung des Konstruktes, welches einen proteolytisch entfernbaren 6x NT-His-Tag besaß, resultierte in einer Verbesserung der Auflösung bis 3,2 Å. Eine weitere Erhöhung war nicht möglich. Dies könnte zum einen am hohen Lösemittelgehalt von fast 70 % zum anderen an der Flexibilität des stark elongierten Moleküls liegen. Die beschriebene Auflösung reichte jedoch aus, um die Struktur mittels molekularem Ersatz, durch ein modifiziertes Modell der Kristallstruktur von YopM_195/P [1jl5,(Evdokimov et al. 2001)] zu lösen. 92 V Diskussion V.1.3 Struktur von YopM_WA-314 im Kristall und in Lösung Wie bereits 2001 von Evdokimov et al. beschrieben, stellt YopM eine Besonderheit in der Superfamilie der LRR-Proteine dar. Es besitzt mit nur 20 bzw. 22 Aminosäuren die kürzeste Wiederholungseinheit aller Mitglieder der Familie. Diese Besonderheit setzt sich auch in der Architektur der einzelnen Repeats fort. Während die konkave Seite dieser hufeisenförmigen Proteine aus β-Faltblattstrukturen besteht, wird die konvexe Seite bei nahezu allen Vertretern der Spezies durch α-Helices gebildet (Kobe & Deisenhofer 1995). Hier bildet YopM eine Ausnahme. Ein elongierter Loop, der durch eine Polyprolin II Konformation gebildet wird, tritt an die Stelle der alpha-helikalen Struktur (Abbildung 51 A und C oben). Abbildung 51: LRR-Strukturvergleich. Vergleich der LRR-Architektur von A: YopM_WA-314 und B: Internalin B (Marino et al. 1999). C: Von oben nach unten: LRR3 aus YopM_WA-314 (20 As), LRR4_YopM_WA-314 (22 As), LRR2 aus InlB. α-Helices (orange), βFaltblätter lila, Loop-Regionen grau. Dargestellt mit USCF Chimera (Pettersen et al. 2004). Der Unterschied zwischen den einzelnen YopM-Spezies liegt in der Anzahl und Zusammensetzung dieser Repeats. Im Gegensatz dazu sind die beiden N-terminalen AlphaHelices und ein ungeordneter C-terminaler Bereich identisch. Wie bereits erwähnt, variiert die Anzahl der Repeats in den bisher bekannten YopMs von 13 in Y. enterocolitica 8081 bis 21 in Y. pseudotuberculosis IP32953 (Vieux & Barrick 2011). Ein Vergleich der einzelnen Repeats ist in Abbildung 52 dargestellt. 93 V Diskussion A B Y. e. 8081 LRR1 LRR2 LRR3 LRR4 LRR5 LRR6 LRR7 LRR8 LRR9 LRR10 LRR11 LRR12 LRR13 HELELNNLGLSSLPELPPH--L ESLVASCNSLTELPELPQS--L KSLQVDNNNLKALSDLPPS--L EFLAAGNNQLEELPELQNSSFL KIIDVDNNSLKKLPDLPPS--L EFLAAGNNQLEELSELQNLPFL TEIHADNNSLKTLPDLPPS--L KTLNVRENYLTDLPELPQS--L TFLDVSDNIFSGLSELPPN--L YYLDASSNGIRSLCDLPPS--L VELDVRDNQLIELPALPPH--L ERLIASLNHLAEVPELPQN--L KQLHVEHNALREFPDIPES--V : : . : : 20 20 20 22 20 22 20 20 20 20 20 20 20 Y.p. 195/P Y.e. WA314 1 2 3 4 5 6,8 7,9 10 11 12 13 14 15 1 2 3 4 5 6 7 8,11,14,17 9,12,15,18 10,13,14,19 20 C Abbildung 52: Vergleich der LRRs in drei Yersinia-Arten. A: Alignment der Leucine Rich Repeats in YopM aus Y. enterocolitica 8081 nummeriert von 1-13. Konservierte Aminosäuren sind hervorgehoben. Nummern der korrespondierenden Repeats in Y. pestis 195/P in rot, Nummern der korrespondierenden Repeats in Y. enterocolitica WA-314 in grün dargestellt. B: Aufbau und Zusammensetzung der Repeatstruktur in Y. pestis 195/P C: Aufbau und Zusammensetzung der Repeatstruktur in Y. enterocolitica WA-314. Ähnliche Repeats durch Nummern bzw. Farben gekennzeichnet. Beim Vergleich der Repeatstruktur der drei YopMs (YopM_8081; YopM_195/P; YopM_WA314) fällt auf, dass es trotz einer gewissen Degeneration der Aminosäuresequenzen wahrscheinlich einen evolutionären Vorfahren aller drei Proteine gibt. YopM_195/P kann durch Replikation der Repeats 6 und 7 aus YopM_8081 hervorgegangen sein. YopM_WA314 zeigt im Vergleich eine Deletion der Repeats 5 und 6 und eine dreifache Replikation der Repeats 10, 11 und 12. Der jeweils letzte Repeat und der C-Terminus sind wiederum in allen drei Spezies identisch. Bei näherer Betrachtung von YopM_8081 fällt auf, dass hier ebenso Repeat-Wiederholungen zu finden sind. Es ist also durchaus möglich, dass es einen gemeinsamen Vorfahren mit einer noch geringeren Anzahl an LRRs gibt (Vieux & Barrick 2011). Eine Variabilität in Anzahl und Komposition der LRRs wie bei YopM ist keine Besonderheit. So stellen z.B. Variable Lymphozyt Rezeptoren, als Teil des Immunsystems einiger kieferlosen Vertebraten, LRR-Proteine mit einer sehr großen Diversität her (Sutoh & Kasahara 2014; Pancer et al. 2004). Die Variabilität der Zusammensetzung der Repeatbereiche vermittelt hierbei die Möglichkeit verschiedene Antigene zu binden. Zwar ist kein unterschiedliches Bindeverhalten verschiedener YopMs zu den bisher entdeckten Interaktionspartnern bekannt, jedoch ist dies auch nicht ausreichend untersucht. Neben diesen möglichen, funktionalen Unterschieden gibt es jedoch weitere offensichtliche strukturelle Abweichungen in der Geometrie der beiden YopM-Orthologe. So ist das Monomer aus Y. enterocolitica WA-314 deutlich stärker gewunden als das Pendant aus Y. pestis 195/P. Dies führt zu einer Dislokation des C-alpha Rückgrats um bis zu 16 Å. 94 V Diskussion Abbildung 53: Vergleich von YopM_Wa-314 mit YopM_195/P. A: YopM_WA_314 rot, YopM195/P grün. Dargestellt in Ribbon-Repräsentation mit dem Programm PyMol α (Schrödinger LLC, USA). B: Abweichung des C -Rückgrats im direkten Aminosäurevergleich. Ein weiterer interessanter Fakt ist, dass in allen Kristallstrukturen der beiden Orthologe, Tetramere gefunden wurden. YopM_195/P bildet in der Struktur 1jl5 eine nahezu perfekte Helix in der zwei Monomere mit ihren C-Termini zusammenhängen und jeweils einen Strang einer Doppelhelix bilden. Diese Struktur wird durch Ca2+-Ionen stabilisiert, die in hoher Konzentration im Kristallisationsansatz vorhanden waren. Nichtsdestotrotz wird durch diese Architektur ein Großteil der hydrophoben Oberfläche des Monomers gebunden. Das Vorhandensein des Tetramers in Lösung konnte jedoch nicht bewiesen werden (Evdokimov et al. 2001). Evdokimov und Kollegen mutmaßten anhand eines um fünf Repeats verlängerten Modells (YopMe20), dass diese Art der Teramerisierung bei YopM_WA-314 aufgrund seiner Architektur und Monomerlänge nicht möglich sei, außer es änderte sich grundlegend etwas an seiner Geometrie. Interessanterweise ist es tatsächlich möglich, diese Art der Helix durch Überlagerung der C-Termini der vier Ketten des YopM_195/P-Tetramers mit vier Monomeren von YopM_WA-314 darzustellen. Dabei entsteht eine weitere Windung in der Doppelhelix, bei ansonsten gleichbleibender Geometrie (Abbildung 54). Diese Tatsache ist wohl im grundlegenden Aufbau der LRR-Architektur zu suchen. (Enkhbayar et al. 2004). Im Gegensatz zu Evdokimovs Resultaten ist diese kunstvolle helikale Struktur nicht in den Kristallen von YopM_WA-314 aufgetreten. Ob es nun ein Kristallisationsartefakt aufgrund der hohen Calcium-Konzentration darstellt oder dieses Tetramer tatsächlich in vivo existiert, kann zu diesem Zeitpunkt nicht nachgewiesen werden. Es findet sich jedoch eine andere Form von Tetramer in der asymmetrischen Einheit der Kristallstruktur von YopM_WA-314, bei dem zwei Moleküle über C-terminale Regionen miteinander verknüpft sind. Die Art dieser Interaktion wurde unter IV.1.4.3 beschrieben und wird weiter unten diskutiert. 95 V Diskussion Abbildung 54: Vergleich der Tetramerstrukturen der beiden kristallisierten YopM-Orthologe. 2+ A: YopM_195/P-Tetramer mit stabilisierenden Ca -Ionen. Zwei „End an End“-Dimere umeinander gewunden zu einer Doppelhelix. Die Helix bildet einen Tunnel mit einem Durchmesser von 35 Å. B: Theoretisches „HelixTetramer“ von YopM_WA-314. C: Tetramer aus YopM_WA-314. Zwei Monomere überlappen an ihren C-Termini und bilden mit einem weiteren identischen Paar ein Tetramer. Dargestellt in Ribbon-Repräsentation mit dem Programm PyMol (Schrödinger LLC, USA). Die Ergebnisse der analytischen Größenausschlusschromatographie sowie der Untersuchungen mittels dynamischer Lichtstreuung (IV.1.3) legten bereits die Vermutung nahe, dass es sich bei YopM_Full, YopM_ΔC sowie bei YopM_Core in Lösung nicht um Monomere handeln konnte: Die ermittelten Molekulargewichte lagen deutlich höher als für die einzelnen Moleküle erwartet. Die Experimente mittels Röntgenkleinwinkelstreuung bestätigten dieses Bild. Mit Hilfe der gemessenen Streukurve von YopM_Core und des Programms SASREF (Petoukhov & Svergun 2005) konnte ein Dimer-Modell erstellt werden, welches im Wesentlichen der Struktur entspricht, die durch die Ketten A und C bzw. B und D der Kristallstruktur gebildet wird. In dieser Anordnung interagieren zwei YopM-Monomere auf eine Fläche von insgesamt 1016 Å2 über 13 Wasserstoffbrückenbindungen und 104 hydrophobe Wechselwirkungen miteinander (Abbildung 27, Abbildung 28, Tabelle 28). Diese Art der Homodimerisierung ist auch bei Vertretern der kleinen Leucin-reichen Proteoglycane, einer Untergruppe des Superfamilie der LRR-Proteine bekannt (Scott et al. 2004; Scott et al. 2006). Bei Decorin und Biglycan nimmt die interagierende Region nahezu die gesamte Fläche der konkaven Seite des LRRs (ca. 2300 Å2) ein, was zu einer sehr starken Bindung führt. Die Bindung im YopM-Dimer dürfte aufgrund seiner Interaktionsfläche und der Größe 96 V Diskussion des Proteins nicht ganz so stark sein, jedoch ist es in unterschiedlichsten Puffern auch bei hohen Salzkonzentrationen stabil. Dies verdeutlicht die Stärke der Bindung. Abbildung 55: Oberflächendarstellung des YopM-Dimers im Vergleich mit Decorin. A: Struktur des Decorin-Dimers pdb Code: 1XKU im Vergleich mit B: YopM_Core. Dargestellt in Ribbon- und Surface Repräsentation mit dem Programm PyMol (Schrödinger LLC, USA). Die hauptsächlich an der Dimerisierung beteiligten Aminosäuren erstrecken sich von LRR920. Dieser Bereich ist, wie in Abbildung 52 A dargestellt, durch Triplikation der LRRs 10,11 und 12 ausgehend von YopM_8081 entstanden. Aufgrund dessen liegt eine gewisse Abweichung in der Aminosäuresequenz im Vergleich zu YopM_195/P in diesem strukturellen Bereich vor (Abbildung 56, Abbildung 57). Dies trifft vor allem auch wichtige, an der Bildung von stabilisierenden hydrophoben Wechselwirkungen beteiligte Reste. YopM_WA_314 YopM195/P VYLDVRDNQLIELPALPSG--LERLIASFNHLAELPELPPNLYYLDASRNEISSLCDLPEYLGVSNNQLEKLPELQNSSFLKIIDVDNNSLKKLPDLPPSLEFIAAGNNQLEELPELQN **.* :*** :** * .. *: : .. * * :**:***.* :: *..*::..* :* YopM_WA_314 YopM195/P -PSLVDLNVRKNQLIELPALPPDLERLIASFNHLAELPELP--PNLSYLDASRNEISSLC LPFLTAIYADNNSLKKLPDLPLSLESIVAGNNILEELPELQNLPFLTTIYADNNLLKTLP * *. : . :*.* :** ** .** ::*. * * ***** * *: : *..* :.:* YopM_WA_314 YopM195/P DLPPSLVDLNVRKNQLIELPALPPDLERLIASFNHLAELPELPPNLSYLDASRNEISSLC DLPPSLEALNVRDNYLTDLPELPQSLTFLDVSENIFSGLSELPPNLYYLNASSNEIRSLC ****** ****.* * :** ** .* * .* * :: *.****** **:** *** *** YopM_WA_314 YopM195/P DLPPSLVELDVRDNQLIELPALPPHLERLIASLNHLAEVPELPQNLKQLHVEHNALREFP DLPPSLEELNVSNNKLIELPALPPRLERLIASFNHLAEVPELPQNLKQLHVEYNPLREFP ****** **:* :*:*********:*******:*******************:*.***** YopM_WA_314 YopM195/P DIPESVEDLRMD DIPESVEDLRMN ***********: Abbildung 56: Alignment der letzten 11 LRRs von YopM_WA-314 und YopM_195/P. Sequenzvergleich der Interaktionsfläche des YopM_WA-314-Dimers mit der korrespondierenden Region in YopM_195/P. Die für die Bindung hauptsächlich verantwortlichen Aminosäuren sind in gelb hervorgehoben. Aminosäureänderungen an diesen Stellen in YopM_195/P sind rot markiert. Durch Überlagerung des YopM_WA-314-Tetramers mit den C-Termini von vier YopM_195/P Monomeren lässt sich ein analoges Tetramer von YopM_195P erstellen. Die Analyse der Kontaktfläche dieses Modells mit PDBsum (Laskowski et al. 1997) ergibt eine deutlich 97 V Diskussion schwächere Interaktion als bei YopM_WA-314. So werden zwischen den Ketten A und C statt 13 nur noch eine Wasserstoffbrückenbindung gebildet und statt 104 nichtkovalenten Bindungen nur noch 50. Natürlich ist dieses Modell sehr theoretisch. Zusammen mit dem Sequenzvergleich der an der Interaktion in YopM_WA-314 beteiligten Aminosäuren untermauert es jedoch die These, dass es sich bei der hier vorliegenden Dimerisierung um eine Besonderheit von YopM_WA-314 handeln könnte. Dies wird zusätzlich durch die Tatsache unterstützt, dass in der Literatur keinen Hinweis auf Dimerisierung dieses Orthologs zu finden ist. Abbildung 57: Kontaktfläche des YopM_WA-314-Dimers. A: Darstellung der an der Bildung des Dimers beteiligten Aminosäuren in YopM_WA-314 und B: der korrespondierenden Aminosäuren in einem theoretischen Modell aus Monomeren von YopM_195/P. Dargestellt in Ribbon- und Stick Repräsentation mit dem Programm PyMol (Schrödinger LLC, USA). V.2 YopM und Caspase-1 In der Literatur sind mittlerweile eine Reihe putativer Interaktionen von YopM und daraus möglicherweise resultierende Wirkungen auf die Zielzelle beschrieben. Ein mit sehr großer Aufmerksamkeit verfolgtes Beispiel dieser Arbeiten ist der von LaRock und Cookson beschriebene inhibitorische Einfluss von YopM auf Caspase-1 (LaRock & Cookson 2012). Durch direkte Interaktion des vier Aminosäuren großen Restes YLTD auf Repeat 10 (YopM_195/P) soll Caspase-1 gehemmt werden und der ihr nachgeschaltete Prozess der Pyroptose unterbunden werden. LaRock und Cookson zeigten ebenso, dass eine Mutation des involvierten Aspartats zu Alanin den Effekt unterband. In dieser Arbeit wurden nun drei Proteine auf diesen inhibitorischen Effekt in einem in vitroAssay untersucht, der im Detail in der Publikation beschrieben war. Ein Sequenzvergleich der das besagte YLTD-Motiv tragenden Repeats ist in Abbildung 29 gezeigt. Demnach trägt YopM_WA-314 natürlicherweise den als inaktiv beschriebenen Aminosäureaustausch von Aspartat zu Alanin (YLTA), während die beiden Proteine YopM_8081 und YopM_YPIII den gewünschten Effekt erzielen sollten. Abbildung 30 zeigt jedoch, dass selbst mit 50 fach höherer (50 µM) als der minimal beschriebenen Konzentration von 100 nM, keines der getesteten YopM-Orthologe im Stande war die Caspase zu hemmen, während dies mit dem kommerziellen Inhibitor gelang. Da die Proteine identisch behandelt wurden wie in der Arbeit von LaRock und Cookson und auch der Assay 1:1 angesetzt wurde, lässt sich dieses 98 V Diskussion Ergebnis nur schwer erklären. Es kann aus dieser Arbeit also keine Bestätigung für einen in vitro-Effekt von YopM_8081, YopM_YPIII und YopM_WA-314 auf Caspase-1 erfolgen. V.3 YopM und DDX3 DDX3 gehört zur Familie der sogenannten DEAD-Box RNA-Helikasen, die in nahezu allen Bereichen des RNA-Metabolismus, von Transkription und Translation bis zum Abbau von RNA, involviert sind (Linder & Jankowsky 2011). Die Mitglieder dieser Familie besitzen alle eine hochkonservierte Helikase-Kernstruktur die aus zwei Domänen besteht, welche die Bindestellen für ATP und RNA beinhalten (Caruthers & McKay 2002; Singleton et al. 2007; Fairman-Williams et al. 2010). Dieser Kern ist umgeben von variablen Strukturen, die die Spezifität der einzelnen Proteine definieren. Neben den offensichtlichen Funktionen des RNA-Stoffwechsels wird DDX3 unter anderem eine Rolle bei der antiviralen Immunantwort zugeschrieben. Interessanterweise ist die Helikase aber ebenso Ziel mannigfaltiger viraler Manipulation durch z.B. HIV, HCV und Pockenviren (Yedavalli et al. 2004; Ariumi et al. 2007; Schröder et al. 2008). In Experimenten, die vor dieser Arbeit getätigt wurden, konnte das Protein YopM aus Y.enterocolitica WA-314 als erster bakterieller Interaktionspartner von DDX3 identifiziert werden. V.3.1 Einengung des Bindungsepitops von DDX3 In vorangegangenen Co-Immunopräzipitations-Experimenten konnte gezeigt werden, dass die Aminosäuren 1-418 (ATPase-Domäne) YopM binden, das Konstrukt 419-660 (HelikaseDomäne) jedoch nicht. Um die Bindungsstelle einzuengen und stabile Expressionskonstrukte für Röntgenstrukturuntersuchungen zu finden, wurden GST-Pulldowns mit fünf verschiedenen 6x CT-His getaggten DDX3-Konstrukten und GST-YopM_Full durchgeführt. Als Negativ-Kontrolle diente in diesem Versuch reines GST, welches aus dem Leervektor pGEX_4T2 gewonnen wurde. Die in Abbildung 32 dargestellten Ergebnisse zeigen eindeutig, dass zumindest ein Teil des unstrukturierten Bereiches, der sich N-terminal an die ATPase Kerndomäne anschließt, notwendig ist um mit YopM zu interagieren. So bindet das Konstrukt 101-418 an YopM, die weitere Trunkierung bis Aminosäure 168 verhindert jedoch die Interaktion. Dieses Ergebnis ist nicht überraschend, stellen doch die die Kerndomäne umgebenden N- und C- terminalen Bereiche der DEAD Box Helikasen die variablen und damit die Spezifität-determinierenden Bereiche dar. So bindet ebenso das K7-Protein, welches in verschiedenen Pockenviren hochkonserviert ist in einem N-terminalen Bereich von DDX3, dem Aminosäure Bereich 61-90 (Kalverda et al. 2009). Um zukünftig ein minimales Bindungsepitop weiter einzugrenzen müssen weitere C-terminale Trunkierungen von DDX3 getestet werden. Leider konnte ein 6x His getaggtes Konstrukt der Aminosäuren 101-168 nicht in E.coli überexprimiert werden. Die selben Aminosäuren als N-terminales GST-Fusionsprotein zeigten eine sehr gute Expression, jedoch keine Bindung an YopM. Dies ist konform mit früheren Beobachtungen, dass ein Tag am N-terminalen Teil von DDX3 die Interaktion mit YopM stört. Dies könnte in einer allgemeinen Änderung der Faltung oder durch sterische Einflüsse des sehr großen GST-Tags bedingt sein. Folglich könnte zukünftig die Verwendung anderer Affinitäts-Tags oder neuer Konstrukte, die Teile des ATPase-Kerns beinhalten weiteren Aufschluss über das Bindungsepitop liefern. Die Methode des GST-Pulldowns mit E.coli-Lysaten erlaubte die Untersuchung der an der Interaktion beteiligten Aminossäuren, lässt jedoch keine Schlüsse zu, ob es sich zwischen YopM und DDX3 tatsächlich um eine direkte Bindung handelt, da im Lysat neben den 99 V Diskussion überexprimierten Konstrukten zahlreiche weitere E. coli-Kontaminanten vorhanden sind. Um die direkte Interaktion darzustellen und einen Einblick in die Struktur des N-Terminus zu gewinnen, mussten stabile Expressionskonstrukte gereinigt und analysiert werden. V.3.2 Aufreinigung von DDX3 und Struktur in Lösung Die in IV.3.2. dargestellten Ergebnisse zeigen, dass sich die drei Konstrukte DDX3_1-418, DDX3_51-418 und DDX3_101-418, die im GST-Pulldown an YopM banden, aus dem E.coliLysat mittels immobilisierter Metall-Affinitätschromatographie reinigen ließen. Darüber hinaus erwies sich die Proteinlösung in der analytischen Größenausschlusschromatographie und im DLS als monodisperse Lösung aus monomeren Proteinen. Die dargestellte Analyse durch SDS-PAGE ergab jedoch auch, dass alle Proteine eine beginnende Degradation aufwiesen. Für nähere röntgenkristallographische Untersuchungen wurde das Konstrukt DDX3_51-418 gewählt, da es sich stabiler als DDX3_1-418 und DDX3_101-418 zeigte. DDX3_1-418 war bereits nach wenigen Stunden zum größten Teil abgebaut und DDX3_101-418 begann nach kurzer Zeit zu oligomerisieren bzw. zu aggregieren. Die Analyse der Aminosäuren 1-168 von DDX3 in silico lässt vermuten, dass es sich hierbei um einen hochgradig unstrukturierten Bereich handelt. Abbildung 58: Analyse des DDX3 N-Terminus. A: CD-Spektrum eines His-Thrombin getaggten Konstruktes der Aminosäuren 5-167 (Oda et al. 2009). Anteil an Sekundärstruktur: 10 % α-Helix, 30 % β-Faltblatt, 30 % Random Coil. B: Vorhersage der ungeordneten Bereiche nach Aminosäureposition mittels psipred (Buchan et al. 2013) C: Strukturvorhersage anhand der Aminosäuresequenz mittel XtalPred (Slabinski et al. 2007). Schwarze Buchstaben zeigen Loop-Strukturen, rot Helix-Strukturen. Ungeordnete Bereiche sind unterstrichen. Auf Grundlage der Daten der Röntgenkleinwinkelstreuung konnten, auf unterschiedliche Weise, Modelle des DDX3_51-418 Fragments erzeugt werden, die alle eine sehr ähnliche räumliche Struktur besitzen (Abbildung 35). Der modellierte N-Terminus zeigt sich in einem elongierten Fragment, welches sich an den globulären ATPase-Kern anschließt. Mit Hilfe des ITASSER Servers konnte ein sequenzbasiertes Homologiemodell des N-Terminus erstellt werden. Dieses Modell wurde in vier, ca. 30 Reste umfassende Teile zerlegt, um der 100 V Diskussion vorhergesagten Flexibilität zu entsprechen und mit Hilfe von SASREF an die Streukurve angepasst. Das Modell weist eine kurze Helixstruktur auf, die sich an die globuläre Domäne anschließt und dann über einen elongierten Loop aus dem globulären Teil herausragt. Dieses Modell ist in guter Übereinstimmung mit der aus dem ab initio-Ansatz entstandenen Hüllstruktur (Abbildung 59) und den in Abbildung 58 dargestellten Vorhersagen. Es muss jedoch angemerkt werden, dass aufgrund des hohen Anteils an Random-Loop-Strukturen eine exakte Darstellung des N-Terminus mittels SAXS nicht möglich ist. Lediglich Lage und Volumen lassen sich mit hoher Wahrscheinlichkeit abbilden. Abbildung 59: Vergleich der DDX3_51-418 Modelle. Überlagerung der aus dem ab initio-Modell entstandenen Oberfläche mit dem aus einem kombinierten ITASSERund SASREF-Ansatz entstandenen DDX3_51-418 Modell. Dargestellt mit USCF Chimera (Pettersen et al. 2004) in Mesh- und Ribbon Repräsentation. Aminosäuren 51-80 in orange, 81-110 in rot, 111-140 in gelb, 141-167 in grün und 168-418 in blau. V.3.3 Direkte Interaktion von YopM und DDX3 Mit reinen Lösungen der aufgereinigten DDX3- und YopM-Konstrukte ließ sich nun die Interaktion weiter biochemisch charakterisieren. Mittels Thermophorese-Experimenten (IV.3.4) konnte für die Interaktion von YopM_Full mit DDX3_1-418 eine Kd von 11,9 ± 3,4 µM und für die Interaktion mit DDX3_51-418 eine Kd von 9,2 ± 0,8 µM ermittelt werden. Dies legt die Vermutung nahe, dass die ersten 50 Aminosäuren keine Rolle bei der Bindung spielen. Leider konnten für das Fragment DDX3_101-418 keine stabilen Messwerte erhalten werden, jedoch zeigte sich in der Tendenz eine geringere Affinität. Dies stellte sich auch in einer weitaus geringeren Amplitude der Fluoreszenzänderungen dar. Diese Beobachtungen sind konform mit den Schwierigkeiten bei der analytischen Größenausschlusschromatographie mit dem Konstrukt. Der Vergleich der Bindungsstärke von YopM_Full und YopM_Core zu DDX3_1-418 zeigt eine minimale Verschlechterung (11,9:18,1 µM) der Bindungsaffinität des N- und C-terminal trunkierten YopM_Core Konstruktes. Diese Änderung ist jedoch nicht sehr aussagekräftig, da es bei den Messungen Schwankungen von bis zu 5 µM gab. Auf eine Beteiligung der fehlenden Bereiche an der Interaktion kann also nicht geschlossen werden. Zusammenfassend handelt es sich um eine relativ schwache Bindung, die jedoch nicht beispiellos in der Familie der LRR-Proteine ist. Zwar kann es hier zu sehr starken Bindungen im femtomolaren Bereich kommen, wie bei der Hemmung von Ribonuclease A und Angiotensin durch den plazentalen Ribonuclease Inhibitor RNI (Lee et al. 1989). Die Bindungsaffinität des zu YopM strukturell sehr homologen Proteins Internalin A aus Listeria 101 V Diskussion monocytogenes mit E-Cadherin liegt jedoch bei 8 µM (Schubert et al. 2002) und damit sehr nah an der Bindung von YopM und DDX3. Mittels Größenausschlusschromatographie (IV.3.5) konnte ein weiterer Nachweis der direkten Interaktion der beiden Bindungspartner erbracht werden. Zudem diente diese dazu, monodisperse Komplexe der beiden Proteine herzustellen, welche unabdingbar für weiterführende Strukturanalysen waren. V.3.4 Kristallisation des Komplexes Der initiale Kristallisations-Screen des Komplexes aus YopM_Core und DDX3_51-418, bei dem 672 Konditionen im 96 well-Format getestet wurden führte bei einer Bedingung [JCSG+ D2 (0,1 M Hepes pH 7,5; 0,2 M MgCl2; 30 % PEG400)] zu Kristallen. Die Analyse dieser mit SDS-PAGE und Western Blot zeigte, dass beide Proteine enthalten waren (Abbildung 45). Die gewachsenen Kristalle waren allerdings sehr klein und keine Einkristalle, was sie für die Untersuchung mittels Röntgenstrahlung unbrauchbar machte. Die Reproduktion und Optimierung der Bedingungen mit der Ausgangslösung scheiterte daran, dass der Komplex über den verhältnismäßig langen Zeitraum den die Kristalle zum Wachsen benötigten in der Ursprungslösung nicht stabil zu sein schien. Die Proteine degradierten und aggregierten. Dieser Ansatz sollte jedoch in späteren Experimenten aufgegriffen werden. Vorherige Versuche mit anderen Konstrukten scheiterten ebenso. Die Kombination aus YopM_Core und DDX3_1-418 bzw. DDX3_101-418 zeigte eine Reihe von Bedingungen bei denen relativ schnell, große Kristalle wuchsen. Diese Bedingungen waren denen von YopM_Core sehr ähnlich und so ergab die Analyse der Kristalle, dass diese nur noch YopM enthielten und das DDX3-Konstrukt anscheinend in Lösung blieb und degradierte. Hier schien der Komplex also nicht stabil gewesen zu sein. In weiterführenden Experimenten sollte zukünftig die Stabilisierung des Komplexes, beispielsweise durch Quervernetzung der Proteine, im Fokus stehen. Zudem sollte nochmals nach stabileren Expressionskonstrukten von DDX3 gesucht werden. Ein weiterer erfolgversprechender Ansatz könnte die Ko-Expression beider Proteine in E. coli sein, da DDX3 im Komplex deutlich stabiler zu sein scheint. Dies hätte gleichzeitig den Vorteil, dass die zeitintensive Aufreinigung der einzelnen Bindungspartner entfiele und somit schneller frische Ausgangslösungen für Optimierungsansätze erzeugt werden könnte. V.3.5 Struktur des Komplexes in Lösung Im Gegensatz zu den bisher erfolglosen Kristallisationsversuchen des Komplexes konnte ein sehr glaubhaftes Modell dessen Struktur mit Hilfe der Röntgenkleinwinkelstreuung gewonnen werden. Der Vorteil dieser Methode liegt auf der Hand: Da die Messung in Lösung stattfindet, ist es möglich den Komplex unmittelbar vor dem Experiment herzustellen und diesen zu analysieren, bevor es zu Dissoziationserscheinungen oder Degradationen kommen kann. Somit sind theoretisch auch Untersuchungen transienter oder eben nicht sehr stabiler Wechselwirkungen möglich. Die aus den SAXS-Messungen gewonnenen Daten zu Volumen und Molekulargewicht zeigen eine konstante Erhöhung im Vergleich zu YopM_Core (Tabelle 30; Tabelle 27). Diese Erhöhung ist in Übereinstimmung mit den Ergebnissen der Größenausschlusschromatographie und der dynamischen Lichtstreuung (IV.3.5). Hier zeigte sich durch die Größenanalyse ebenso, dass YopM als Dimer vorlag, DDX3 als Monomer und der Komplex-Peak ziemlich exakt der Addition dieser Werte entsprach. Dies wurde sowohl für YopM_Full, als auch für YopM_Core gezeigt. Es deutete darauf hin, dass es sich bei dem Komplex aus YopM und DDX3 um einen 2:1 Komplex handelte. So ähnelt auch die in 102 V Diskussion Abbildung 47 dargestellte Streukurve des Komplexes aus YopM_Core und DDX3_51-418 sehr stark der Kurve von YopM_Core, bei gleichzeitiger Erhöhung von I(0) und damit des Trägheitsradius. Die Erhöhung ist am extrapolierten Schnittpunkt der Kurve mit der Y-Achse zu erkennen. In Kombination mit dem zuvor erhaltenen Modell von DDX3_51-418 war es nun möglich den Komplex auf Basis des YopM_Core Dimers darzustellen (Abbildung 49). In diesem Modell bindet DDX3_51-418 mit einem kleinen Teil der globulären Kerndomäne an die durch Dimerisierung von YopM entstandene, neue Kontaktfläche. Der modellierte elongierte NTerminus ragt in dieser Struktur in die konkave Seite eines der YopM-Proteine. Dieses Modell zeigt einen sehr guten Fit mit einem Chi-Wert von 1,36 bei sehr guten Messwerten die wenig Hintergrundrauschen der Kurve zeigten (Abbildung 49 B). Während das Modell mehrfach mit den Messdaten des Komplexes oder des Komplexes in Kombination mit den Kurven der einzelnen Proteine reproduziert werden konnte, ließ sich kein Modell mit einem YopM-Monomer darstellen (Abbildung 50). Dies bekräftigt das 2:1 Modell zusätzlich. Zudem konnte ein 2:2 Komplex und ein 1:2 Komplex ausgeschlossen werden. Eine detailliertere Analyse des Interface des N-Terminus von DDX3_51-418 mit YopM auf Ebene einzelner Aminosäuren ist anhand des Modells jedoch nicht möglich, da aufgrund des hohen Anteils an Random Coil-Struktur eine gewisse Variabilität in diesem Bereich vorliegt. Versuche den Bereich mit einem flexiblen Teil des N-Terminus zu modellieren, brachten kein einheitliches Ergebnis. Um hier weitere Einblicke in die exakte Kontaktfläche zu erhalten ist eine hochauflösende Kristallstruktur erforderlich. Nichtsdestotrotz ist der Nachweis, dass YopM DDX3 als Dimer bindet, hochinteressant: Zwar deuteten die Ergebnisse des Sequenzvergleichs der Bindungsfläche von YopM_WA-314 mit YopM195/P an, dass es sich bei der beschriebenen Art der Dimerisierung um eine Besonderheit von YopM_WA-314 handelt, es ist jedoch nicht auszuschließen, dass auch die anderen YopM_Orthologe zur Homo-Dimerisierung fähig sind. Dies ist zukünftig ebenso zu untersuchen, wie die Fähigkeit anderer YopM-Spezies DDX3 zu binden. So könnte die durch Triplikation der LRRs 10-12 entstandene neue Kontaktfläche in YopM_WA-314 ebenso die exklusive Bindung zu DDX3 vermitteln. Wie bereits zu Beginn erwähnt, sind für YopM mittlerweile eine Reihe unterschiedlicher Interaktionspartner in der Literatur beschrieben (Hines et al. 2001; Reisner & Straley 1992; LaRock & Cookson 2012). Im Falle der Interaktion mit den beiden Kinasen RSK1 und PKN2 (McDonald et al. 2003) ist zudem gezeigt, dass YopM diese durch gleichzeitige Bindung in einen neuen, ternären Komplex bringt, in dem eine gegenseitige Phosphorylierung stattfindet. In unveröffentlichten Experimenten, die parallel zur vorliegenden Arbeit gemacht wurden, konnte dies mit Y. enterocolitica WA-314 bestätigt werden. Darüber hinaus wurde zudem nachgewiesen, dass YopM in diesem System in der Lage war gleichzeitig RSK1 und DDX3 zu binden (Schnapp, unveröffentlicht). Die Fähigkeit von YopM ein Dimer zu bilden und als solches mehrere Proteine in einen Komplex zu zwingen, könnte hierfür eine gute Erklärung liefern. Dies untermauert eindrucksvoll den Status von YopM als Gerüstprotein. Die Zusammenführung unterschiedlichster Zielproteine in vorher unbekannte Komplexe bestimmt die Relevanz von YopM in der Infektion von Yersinia spp. Die Aufklärung der daraus resultierenden Effekte auf die Wirtszelle kann schließlich zu einem besseren Verständnis der Pathogen-Wirts-Interaktion führen. 103 VI Zusammenfassung VI Zusammenfassung Enteropathogene Bakterien der Gattung Yersinia haben die Fähigkeit entwickelt in lymphatischem Gewebe zu persistieren. Um der Abwehr des Wirts zu entgehen, haben diese Erreger ein sogenanntes Typ-III-Sekretionssystem entwickelt, mit dessen Hilfe sie eine Reihe von Immunmodulatoren, wie das in dieser Arbeit untersuchte YopM, direkt in Zielzellen wie Makrophagen injizieren. YopM-defiziente Yersinia-Mutanten haben kaum Überlebenschancen im Mausmodell (Kerschen et al. 2004). YopM wird mit einer Reihe immunmodulierender Effekte, wie der Stimulation oder der Hemmung der Ausschüttung von Interleukinen (Kerschen et al. 2004), oder der Aktivierung von Kinasen (McDonald et al. 2003) in Verbindung gebracht. Mehrere Interaktionspartner von YopM, extrazelluläre wie auch intrazelluläre, wurden beschrieben (Reisner & Straley 1992; Heusipp et al. 2006; McDonald et al. 2003; LaRock & Cookson 2012). Einer dieser Interaktionspartner ist die DEAD-Box-Helikase DDX3 (Hentschke et al. unveröffentlicht). YopM zeigt selbst in unterschiedlichen Serotypen ein- und derselben Art eine beträchtliche Variabilität v.a. in der Anzahl seiner „Leucine Rich Repeats“ (LRRs), die bei den bisher bekannten Formen von 13 bis 21 reichen kann. YopM aus Y. pestis 195/P (YopM_195/P) besteht aus 15 LRRs und das in dieser Arbeit untersuchte YopM aus Y. enterocolitica WA-314 (YopM_WA-314) besitzt 20 LRRs. Ziel dieser Arbeit war es I) YopM_WA-314 in Lösung allein und nach seiner Interaktion mit DDX3 durch „small angle X-ray scattering“ (SAXS) zu untersuchen; II) YopM_WA-314 zu kristallisieren, um es in die niedrig aufgelösten SAXS-Strukturen modellieren zu können; III) die Proteinbereiche sowohl in YopM als auch in DDX3 zu identifizieren, die für die Interaktion dieser beiden Proteine essentiell sind. Die Kristallstruktur von YopM_WA-314, die in der vorliegenden Arbeit gelöst wurde, zeigte, wie die Kristallstruktur von YopM_195/P, ein Tetramer. Dieses unterscheidet sich jedoch grundlegend von der YopM_195/P-Doppelhelixstruktur. Die Strukturanalyse des YopM_WA314 ergab, dass das Kristall-Tetramer aus zwei physiologischen Dimeren besteht. Über eine Kontaktfläche von ca. 1000 Å2 interagieren hierbei zwei Monomere C-terminal über ihre konkave Seite. Die Bindung wird durch 13 Wasserstoffbrückenbindungen und 104 hydrophobe Wechselwirkungen vermittelt. Auf Grundlage dieser Daten konnte die Interaktion von YopM mit DDX3 näher charakterisiert werden. Hierbei handelt es sich um eine direkte, mäßig affine Bindung mit einer Kd von ~12 μM. Durch GST-Pulldown-Experimente konnte ermittelt werden, dass der flexible, unstrukturierte N-terminus der ATPase-Domäne von DDX3 unabdingbar für die Komplexbildung mit YopM ist. Die Analyse der Interaktion mittels analytischer Größenausschlusschromatographie und Röntgenkleinwinkelstreuung zeigte, dass der Komplex aus dem zuvor beschriebenen YopM-Dimer besteht, welches an der Cterminalen Dimerisierungsfläche ein Monomer von DDX3 bindet. Hierbei ragt der N-Terminus von DDX3 in die konkave Seite eines der YopM-Monomere und stabilisiert die Bindung. Diese Arbeit konnte somit die neue Kristallstruktur von YopM aus Y. enterocolitica WA-314 liefern und zum ersten Mal eine YopM-Struktur in Lösung präsentieren. Ebenso konnte mit Hilfe von SAXS ein sehr glaubhaftes Modell des Komplexes aus YopM und DDX3 erstellt werden. Die Art der hier dargelegten 2:1 Interaktion könnte eine Erklärung dafür liefern, wie YopM in der Lage ist, mehrere Proteine gleichzeitig zu binden und sie, wie für die auch interagierenden Kinasen RSK1 und PKN2 nachgewiesen, in einen ternären Komplex zu 104 VI Zusammenfassung zwingen. Die Analyse der Auswirkung dieser Verbindungen auf die Wirtszelle könnte dabei helfen weiter Licht in die rätselhafte Rolle YopMs in der Yersinien-Infektion zu bringen. VIa Summary Enteropathogenic bacteria of the genus Yersinia are able to persist in lymphatic tissues. To evade killing by the host immune system, the bacteria have developed a so called type III secretion system (TTSS). This system enables the bacteria to inject immune modulators like YopM into target cells like macrophages. YopM plays a major role in virulence in the mouse model and is said to reduce cytokine expression (Kerschen et al. 2004) but its mode of action remains enigmatic. Besides the so far unknown function, many extracellular and intracellular interaction partners for the protein could be described (Reisner & Straley 1992; Heusipp et al. 2006; McDonald et al. 2003; LaRock & Cookson 2012). One of these interaction partners is the DEAD box helicase DDX3 (Hentschke et al. unpublished). While most of the other Yops are highly conserved among species and serotypes, YopM displays certain variations in size and sequence. These differences are due to its variable number of Leucine Rich Repeats (LRRs) which differs from 13 to 21 in known species. YopM from Y. pestis 195/P (YopM_195/P) has 15 LRRs while YopM from Y. enterocolitica WA-314 (YopM_WA-314) which has been examined in this work consists of 20 LRRs. The aim of this study was to I) characterize YopM_WA-314 alone and together with DDX3 in solution via small angle X-ray scattering (SAXS); II) to crystallize YopM_WA-314 as a basis for modelling the complex into the low resolution structure; III) to identify the regions in both proteins that are essential for the interaction. The crystal structure of YopM_WA-314 that was solved in this work shows a tetramer in the asymmetric unit. This tetramer dramatically differs from the one found in Y. pestis. SAXS revealed that this tetramer is built by two physiological dimers. In these dimers two monomers overlap in a C-terminal region of ~1000 Å2. The dimer is stabilized by 13 hydrogen bonds and 104 non bonded interactions. Upon the basis of this structure the interaction of YopM and DDX3 could be further characterized. YopM binds DDX3 directly with moderate affinity with a Kd of ~12 µM. Via GST pulldown experiments it could be demonstrated that the N-Terminus of the Helicase is necessary for establishing the complex. The analysis of the complex with size exclusion chromatography and SAXS revealed that the YopM dimer binds a monomer of DDX3. In this model the globular domain-1 of DDX3 binds to the C-Terminal dimerization site of YopM and the N-terminus of DDX3 extends into the concave site of one YopM and stabilizes the complex. Thus this work presents the novel structure of YopM from Y. enterocolitica WA-314 and for the first time a structure of YopM in solution. Furthermore it is the first time that a reasonable model of the complex of the protein and a binding partner (DDX3) could be established. This 2:1 binding mode of YopM could deliver an explanation for how it deals with the parallel binding of two interaction partners that leads to the formation of a ternary complex, as described in the case of RSK1 and PRK2. The analysis of the influences those interactions might have on the host cells should help to shed light on the enigmatic role of YopM in Yersinia infection. 105 VII Literaturverzeichnis VII Literaturverzeichnis Achtman, M. et al., 1999. Yersinia pestis, the cause of plague, is a recently emerged clone of Yersinia pseudotuberculosis. Proceedings of the National Academy of Sciences of the United States of America, 96(24), pp.14043–8. Aepfelbacher, M. et al., 2003. Characterization of YopT effects on Rho GTPases in Yersinia enterocolitica-infected cells. The Journal of biological chemistry, 278(35), pp.33217–23. Aepfelbacher, M., 2004. Modulation of Rho GTPases by type III secretion system translocated effectors of Yersinia. Reviews of physiology, biochemistry and pharmacology, 152, pp.65–77. Aepfelbacher, M. & Heesemann, J., 2001. Modulation of Rho GTPases and the actin cytoskeleton by Yersinia outer proteins (Yops). International journal of medical microbiology : IJMM, 291, pp.269–276. Aepfelbacher, M., Trasak, C. & Ruckdeschel, K., 2007. Effector functions of pathogenic Yersinia species. Aleksic, S. & Bockemühl, J., 1990. Mikrobiologie und Epidemiologie der Yersiniosen. Immunität und Infektion, 18, pp.178–185. Andersson, K. et al., 1996. YopH of Yersinia pseudotuberculosis interrupts early phosphotyrosine signalling associated with phagocytosis. Molecular microbiology, 20, pp.1057–1069. Andor, A. et al., 2001. YopE of Yersinia, a GAP for Rho GTPases, selectively modulates Rac-dependent actin structures in endothelial cells. Cellular microbiology, 3, pp.301– 310. Ariumi, Y. et al., 2007. DDX3 DEAD-box RNA helicase is required for hepatitis C virus RNA replication. Journal of virology, 81, pp.13922–13926. Battye, T.G.G. et al., 2011. iMOSFLM: a new graphical interface for diffraction-image processing with MOSFLM. Acta crystallographica. Section D, Biological crystallography, 67(Pt 4), pp.271–81. 106 VII Literaturverzeichnis Bella, J. et al., 2008. The leucine-rich repeat structure. Cellular and molecular life sciences : CMLS, 65(15), pp.2307–33. Benabdillah, R. et al., 2004. Identification of a nuclear targeting signal in YopM from Yersinia spp. Microbial pathogenesis, 36(5), pp.247–261. Bernadó, P. et al., 2007. Structural characterization of flexible proteins using small-angle Xray scattering. Journal of the American Chemical Society, 129, pp.5656–5664. Biot, T. & Cornelis, G.R., 1988. The replication, partition and yop regulation of the pYV plasmids are highly conserved in Yersinia enterocolitica and Y. pseudotuberculosis. Journal of general microbiology, 134, pp.1525–1534. Black, D.S. & Bliska, J.B., 2000. The RhoGAP activity of the Yersinia pseudotuberculosis cytotoxin YopE is required for antiphagocytic function and virulence. Molecular microbiology, 37, pp.515–527. Black, R.E. et al., 1978. Epidemic Yersinia enterocolitica infection due to contaminated chocolate milk. The New England journal of medicine, 298, pp.76–79. Bleves, S. & Cornelis, G.R., 2000. How to survive in the host: the Yersinia lesson. Microbes and infection / Institut Pasteur, 2(12), pp.1451–60. Blocker, a et al., 2001. Structure and composition of the Shigella flexneri “needle complex”, a part of its type III secreton. Molecular microbiology, 39(3), pp.652–63. Boland, a et al., 1996. Status of YopM and YopN in the Yersinia Yop virulon: YopM of Y.enterocolitica is internalized inside the cytosol of PU5-1.8 macrophages by the YopB, D, N delivery apparatus. The EMBO journal, 15(19), pp.5191–5201. Boland, a, Havaux, S. & Cornelis, G.R., 1998. Heterogeneity of the Yersinia YopM protein. Microbial pathogenesis, 25(6), pp.343–348. Bolin, I., Norlander, L. & Wolf-watz, H., 1982. Temperature-inducible outer membrane protein of Yersinia pseudotuberculosis and Yersinia enterocolitica is associated with the virulence Temperature-Inducible Outer Membrane Protein of Yersinia pseudotuberculosis and Yersinia enterocolitica Is Associated . 107 VII Literaturverzeichnis Botlagunta, M. et al., 2008. Oncogenic role of DDX3 in breast cancer biogenesis. Oncogene, 27, pp.3912–3922. Bottone, E.J., 1997. Yersinia enterocolitica: the charisma continues. Clinical microbiology reviews, 10(2), pp.257–76. Breitsprecher, D. et al., 2014. Crystal structure of an engineered YopM-InlB hybrid protein. BMC structural biology, 14, p.12. Brem, D. et al., 2001. Functional analysis of yersiniabactin transport genes of Yersinia enterocolitica. Microbiology, 147, pp.1115–1127. Buchan, D.W. a et al., 2013. Scalable web services for the PSIPRED Protein Analysis Workbench. Nucleic acids research, 41, pp.W349–357. Carniel, E. et al., 1996. Characterization of a large chromosomal “ high-pathogenicity island ” in biotype 1B Yersinia enterocolitica . Characterization of a Large Chromosomal “ HighPathogenicity Island ” in Biotype 1B Yersinia enterocolitica. , 178(23). Carter, P.B., Zahorchak, R.J. & Brubaker, R.R., 1980. Plague virulence antigens from Yersinia enterocolitica. Infection and immunity, 28, pp.638–640. Caruthers, J.M. & McKay, D.B., 2002. Helicase structure and mechanism. Current Opinion in Structural Biology, 12, pp.123–133. Chain, P.S.G. et al., 2004. Insights into the evolution of Yersinia pestis through wholegenome comparison with Yersinia pseudotuberculosis. Proceedings of the National Academy of Sciences of the United States of America, 101, pp.13826–13831. Chang, P.-C. et al., 2006. DDX3, a DEAD box RNA helicase, is deregulated in hepatitis virus-associated hepatocellular carcinoma and is involved in cell growth control. Oncogene, 25, pp.1991–2003. Cohen, S.N. et al., 1973. Biologically Functional Bacterial Plasmids In Vitro. , 70(11), pp.3240–3244. Cohen, S.N., Chang, a C. & Hsu, L., 1972. Nonchromosomal antibiotic resistance in bacteria: genetic transformation of Escherichia coli by R-factor DNA. Proceedings of the National 108 VII Literaturverzeichnis Academy of Sciences of the United States of America, 69(8), pp.2110–4. Cordin, O. et al., 2006. The DEAD-box protein family of RNA helicases. Gene, 367, pp.17–37. Cornelis, G.R. et al., 1998. The virulence plasmid of Yersinia, an antihost genome. Microbiology and molecular biology reviews : MMBR, 62(4), pp.1315–52. Cornelis, G.R., 2002. Yersinia type III secretion: send in the effectors. The Journal of cell biology, 158(3), pp.401–8. Cornelis, G.R. & Wolf-Watz, H., 1997. The Yersinia Yop virulon: a bacterial system for subverting eukaryotic cells. Molecular microbiology, 23, pp.861–867. Denecker, G. et al., 2002. Effect of low- and high-virulence Yersinia enterocolitica strains on the inflammatory response of human umbilical vein endothelial cells. Infect Immun, 70, pp.3510–3520. Dewoody, R.S., Merritt, P.M. & Marketon, M.M., 2013. Regulation of the Yersinia type III secretion system: traffic control. Frontiers in cellular and infection microbiology, 3(February), p.4. Drancourt, M. & Raoult, D., 2002. Molecular insights into the history of plague. Microbes and infection / Institut Pasteur, 4(1), pp.105–9. Dukuzumuremyi, J.M. et al., 2000. The Yersinia protein kinase A is a host factor inducible RhoA/Rac-binding virulence factor. The Journal of biological chemistry, 275, pp.35281– 35290. Dunn, J.J., 1988. ompT Encodes the Escherichia coli Outer Membrane Protease That Cleaves T7 RNA Polymerase during Purification. , 170(3). Emsley, P. et al., 2010. Features and development of Coot. Acta crystallographica. Section D, Biological crystallography, 66(Pt 4), pp.486–501. Enkhbayar, P. et al., 2004. Structural principles of leucine-rich repeat (LRR) proteins. Proteins, 54(3), pp.394–403. Evans, P., 2006. Scaling and assessment of data quality. Acta crystallographica. Section D, Biological crystallography, 62, pp.72–82. 109 VII Literaturverzeichnis Evdokimov, a G. et al., 2001. Unusual molecular architecture of the Yersinia pestis cytotoxin YopM: a leucine-rich repeat protein with the shortest repeating unit. Journal of molecular biology, 312(4), pp.807–821. Evdokimov, A.G. et al., 2002. Crystal structure of the Yersinia pestis GTPase activator YopE. Protein science : a publication of the Protein Society, 11, pp.401–408. Evdokimov, A.G. et al., 2000. Overproduction, purification, crystallization and preliminary Xray diffraction analysis of YopM, an essential virulence factor extruded by the plague bacterium Yersinia pestis. Acta Crystallographica Section D Biological Crystallography, 56(12), pp.1676–1679. Fairman-Williams, M.E., Guenther, U.P. & Jankowsky, E., 2010. SF1 and SF2 helicases: Family matters. Current Opinion in Structural Biology, 20, pp.313–324. Franke, D. & Svergun, D.I., 2009. DAMMIF , a program for rapid ab-initio shape determination in small-angle scattering. Journal of Applied Crystallography, 42, pp.342– 346. Fuchs, T.M. et al., 2011. Shotgun sequencing of Yersinia enterocolitica strain W22703 (biotype 2, serotype O:9): genomic evidence for oscillation between invertebrates and mammals. BMC genomics, 12(1), p.168. Fukuda, M. et al., 1997. CRM1 is responsible for intracellular transport mediated by the nuclear export signal. Nature, 390(6657), pp.308–11. Galyov, E.E. et al., 1993. A secreted protein kinase of Yersinia pseudotuberculosis is an indispensable virulence determinant. Nature, 361, pp.730–732. Garzetti, D. et al., 2012. Tracing genomic variations in two highly virulent Yersinia enterocolitica strains with unequal ability to compete for host colonization. BMC Genomics, 13(1), p.467. Gasteiger, E. et al., 2005. Protein Identification and Analysis Tools on the ExPASy Server. In The proteomics protocols handbook. pp. 571–607. Gemski, P. et al., 1980. Presence of a virulence-associated plasmid in Yersinia pseudotuberculosis. Infection and immunity, 28(3), pp.1044–7. 110 VII Literaturverzeichnis Gerlach, R.G. & Hensel, M., 2007. Protein secretion systems and adhesins: The molecular armory of Gram-negative pathogens. International Journal of Medical Microbiology, 297, pp.401–415. Grant, S.G. et al., 1990. Differential plasmid rescue from transgenic mouse DNAs into Escherichia coli methylation-restriction mutants. Proceedings of the National Academy of Sciences of the United States of America, 87(12), pp.4645–9. Grassl, G. a et al., 2003. Interaction of Yersinia enterocolitica with epithelial cells: invasin beyond invasion. International journal of medical microbiology : IJMM, 293(1), pp.41–54. Grosdent, N. et al., 2002. Role of Yops and Adhesins in Resistance of Yersinia enterocolitica to Phagocytosis. , 70(8), pp.4165–4176. Guan, K.L. & Dixon, J.E., 1990. Protein tyrosine phosphatase activity of an essential virulence determinant in Yersinia. Science (New York, N.Y.), 249, pp.553–556. Håkansson, S. et al., 1996. The Yersinia YpkA Ser/Thr kinase is translocated and subsequently targeted to the inner surface of the HeLa cell plasma membrane. Molecular microbiology, 20, pp.593–603. Hanahan, D. & Harbor, C.S., 1983. Studies o n T r a n s f o r m a t i o n o f Escherichia coli with P l a s m i d s Department of Biochemistry and Molec ~ dar Biology. , 0, pp.557– 580. Heesemann, J. et al., 1986. Immunochemical analysis of plasmid-encoded proteins released by enteropathogenic Yersinia sp. grown in calcium-deficient media. Infection and immunity, 54(2), pp.561–7. Heesemann, J. et al., 1993. Virulence of Yersinia enterocolitica is closely associated with siderophore production, expression of an iron-repressible outer membrane polypeptide of 65,000 Da and pesticin sensitivity. Molecular microbiology, 8, pp.397–408. Heesemann, J. & Laufs, R., 1983. Construction of a mobilizable Yersinia enterocolitica virulence plasmid. Journal of bacteriology, 155(2), pp.761–7. Hentschke, M. et al., 2010. Yersinia virulence factor YopM induces sustained RSK activation by interfering with dephosphorylation. PloS one, 5(10). 111 VII Literaturverzeichnis Heusipp, G. et al., 2006. YopM of Yersinia enterocolitica specifically interacts with alpha1antitrypsin without affecting the anti-protease activity. Microbiology (Reading, England), 152(Pt 5), pp.1327–1335. Hines, J. et al., 2001. Structure-function analysis of Yersinia pestis YopM’s interaction with alpha-thrombin to rule on its significance in systemic plague and to model YopM's mechanism of binding host proteins. Microbial pathogenesis, 30(4), pp.193–209. Hinnebusch, B.J. et al., 2002. Role of Yersinia murine toxin in survival of Yersinia pestis in the midgut of the flea vector. Science (New York, N.Y.), 296, pp.733–735. Hinnebusch, B.J., Fischer, E.R. & Schwan, T.G., 1998. Evaluation of the role of the Yersinia pestis plasminogen activator and other plasmid-encoded factors in temperaturedependent blockage of the flea. The Journal of infectious diseases, 178(5), pp.1406–15. Hoffmann, R. et al., 2004. Transcriptional responses of murine macrophages to infection with Yersinia enterocolitica. Cellular microbiology, 6(4), pp.377–390. Högbom, M. et al., 2007. Crystal structure of conserved domains 1 and 2 of the human DEAD-box helicase DDX3X in complex with the mononucleotide AMP. Journal of molecular biology, 372(1), pp.150–9. Hohenester, E., Hussain, S. & Howitt, J.A., 2006. Interaction of the guidance molecule Slit with cellular receptors. Biochemical Society transactions, 34, pp.418–421. Isberg, R.R. & Leong, J.M., 1988. Cultured mammalian cells attach to the invasin protein of Yersinia pseudotuberculosis. Proceedings of the National Academy of Sciences of the United States of America, 85, pp.6682–6686. Isberg, R.R., Voorhis, D.L. & Falkow, S., 1987. Identification of invasin: a protein that allows enteric bacteria to penetrate cultured mammalian cells. Cell, 50(5), pp.769–78. Jerabek-Willemsen, M. et al., 2011. Molecular interaction studies using microscale thermophoresis. Assay and drug development technologies, 9(4), pp.342–53. Juris, S.J. et al., 2000. A distinctive role for the Yersinia protein kinase: actin binding, kinase activation, and cytoskeleton disruption. Proceedings of the National Academy of Sciences of the United States of America, 97, pp.9431–9436. 112 VII Literaturverzeichnis Juris, S.J., Shao, F. & Dixon, J.E., 2002. Yersinia effectors target mammalian signalling pathways. Cellular microbiology, 4(4), pp.201–11. Kabsch, W., 2010. XDS. Acta crystallographica. Section D, Biological crystallography, 66, pp.125–132. Kajava, A. V, 1998. Structural diversity of leucine-rich repeat proteins. Journal of molecular biology, 277, pp.519–527. Kalverda, A.P. et al., 2009. Poxvirus K7 protein adopts a Bcl-2 fold: biochemical mapping of its interactions with human DEAD box RNA helicase DDX3. Journal of molecular biology, 385(3), pp.843–53. Kerschen, E.J. et al., 2004. The plague virulence protein YopM targets the innate immune response by causing a global depletion of NK cells. Infection and immunity, 72(8), pp.4589–4602. Kobe, B. & Deisenhofer, J., 1993. Crystallization and preliminary X-ray analysis of porcine ribonuclease inhibitor, a protein with leucine-rich repeats. Journal of molecular biology, 231, pp.137–140. Kobe, B. & Deisenhofer, J., 1995. Proteins with leucine-rich repeats. Current opinion in structural biology, 5(3), pp.409–16. Konarev, P. V. et al., 2003. PRIMUS : a Windows PC-based system for small-angle scattering data analysis. Journal of Applied Crystallography, 36(5), pp.1277–1282. Koster, M. et al., 1997. The outer membrane component, YscC, of the Yop secretion machinery of Yersinia enterocolitica forms a ring-shaped multimeric complex. Molecular microbiology, 26, pp.789–797. Kresse, H. & Schönherr, E., 2001. Proteoglycans of the extracellular matrix and growth control. Journal of cellular physiology, 189, pp.266–274. Krissinel, E., 2012. Enhanced fold recognition using efficient short fragment clustering. Journal of Molecular Biochemistry. 113 VII Literaturverzeichnis Kwaga, J., Iversen, J.O. & Misra, V., 1992. Detection of pathogenic Yersinia enterocolitica by polymerase chain reaction and digoxigenin-labeled polynucleotide probes. Journal of clinical microbiology, 30(10), pp.2668–73. Laemmli, U.K., 1970. Cleavage of structural proteins during the assembly of the head of bacteriophage T4. Nature, 227, pp.680–685. Lai, M.-C., Lee, Y.-H.W. & Tarn, W.-Y., 2008. The DEAD-box RNA helicase DDX3 associates with export messenger ribonucleoproteins as well as tip-associated protein and participates in translational control. Molecular biology of the cell, 19, pp.3847–3858. LaRock, C.N. & Cookson, B.T., 2012. The Yersinia Virulence Effector YopM Binds Caspase1 to Arrest Inflammasome Assembly and Processing. Cell Host & Microbe, 12(6), pp.799–805. Laskowski, R.A. et al., 1997. PDBsum: A Web-based database of summaries and analyses of all PDB structures. Trends in Biochemical Sciences, 22, pp.488–490. Laskowski, R.A. et al., 1993. PROCHECK: a program to check the stereochemical quality of protein structures. Journal of Applied Crystallography, 26, pp.283–291. Laskowski-Arce, M.A. & Orth, K., 2007. The elusive activity of the Yersinia protein kinase A kinase domain is revealed. Trends in Microbiology, 15, pp.437–440. Lee, C.-S. et al., 2008. Human DDX3 functions in translation and interacts with the translation initiation factor eIF3. Nucleic acids research, 36, pp.4708–4718. Lee, F.S., Shapiro, R. & Vallee, B.L., 1989. Tight-binding inhibition of angiogenin and ribonuclease A by placental ribonuclease inhibitor. Biochemistry, 28, pp.225–230. Leong, J.M., Fournier, R.S. & Isberg, R.R., 1990. Identification of the integrin binding domain of the Yersinia pseudotuberculosis invasin protein. The EMBO journal, 9, pp.1979– 1989. Leslie, A.G.W., 2006. The integration of macromolecular diffraction data. Acta crystallographica. Section D, Biological crystallography, 62(Pt 1), pp.48–57. 114 VII Literaturverzeichnis Leung, K.Y., Reisner, B.S. & Straley, S.C., 1990. YopM inhibits platelet aggregation and is YopM Inhibits Platelet Aggregation and Is Necessary for Virulence of Yersinia pestis in Mice. , 58(10). Leung, K.Y. & Straley, S.C., 1989. The yopM gene of Yersinia pestis encodes a released protein having homology with the human platelet surface protein GPIb alpha. Journal of bacteriology, 171(9), pp.4623–4632. Lian, C.J. et al., 1987. Invasiveness of Yersinia enterocolitica lacking the virulence plasmid: an in-vivo study. Journal of medical microbiology, 24(3), pp.219–26. Linder, P. & Jankowsky, E., 2011. From unwinding to clamping - the DEAD box RNA helicase family. Nature reviews. Molecular cell biology, 12(8), pp.505–16. Mamiya, N. & Worman, H., 1999. Hepatitis C virus core protein binds to a DEAD box RNA helicase. Journal of Biological Chemistry. Marino, M. et al., 1999. Structure of the lnlB leucine-rich repeats, a domain that triggers host cell invasion by the bacterial pathogen L. monocytogenes. Molecular cell, 4(6), pp.1063–72. Matilla, A. & Radrizzani, M., 2005. The Anp32 family of proteins containing leucine-rich repeats. Cerebellum (London, England), 4, pp.7–18. McCoy, M.W. et al., 2010. The C-terminal tail of Yersinia pseudotuberculosis YopM is critical for interacting with RSK1 and for virulence. Infection and immunity, 78(6), pp.2584– 2598. McDonald, C. et al., 2003. The yersinia virulence factor YopM forms a novel protein complex with two cellular kinases. The Journal of biological chemistry, 278(20), pp.18514–18523. McPhee, J.B., Mena, P. & Bliska, J.B., 2010. Delineation of regions of the Yersinia YopM protein required for interaction with the RSK1 and PRK2 host kinases and their requirement for interleukin-10 production and virulence. Infection and immunity, 78(8), pp.3529–39. Michiels, T. et al., 1990. Secretion of Yop proteins by Yersiniae. Infection and immunity, 58(9), pp.2840–9. 115 VII Literaturverzeichnis Michiels, T. & Cornelis, G.R., 1991. Secretion of hybrid proteins by the Yersinia Yop export system. Journal of bacteriology, 173(5), pp.1677–85. Miller, V.L. & Falkow, S., 1988. Evidence for two genetic loci in Yersinia enterocolitica that can promote invasion of epithelial cells. Infection and immunity, 56(5), pp.1242–8. Mills, S.D. et al., 1997. Yersinia enterocolitica induces apoptosis in macrophages by a process requiring functional type III secretion and translocation mechanisms and involving YopP, presumably acting as an effector protein. Proceedings of the National Academy of Sciences of the United States of America, 94, pp.12638–12643. Mittal, R., Peak-Chew, S.-Y. & McMahon, H.T., 2006. Acetylation of MEK2 and I kappa B kinase (IKK) activation loop residues by YopJ inhibits signaling. Proceedings of the National Academy of Sciences of the United States of America, 103, pp.18574–18579. Moffatt, B. a & Studier, F.W., 1987. T7 lysozyme inhibits transcription by T7 RNA polymerase. Cell, 49(2), pp.221–7. Monack, D.M. et al., 1997. Yersinia signals macrophages to undergo apoptosis and YopJ is necessary for this cell death. Proceedings of the National Academy of Sciences of the United States of America, 94, pp.10385–10390. Montagner, C., Arquint, C. & Cornelis, G.R., 2011. Translocators YopB and YopD from Yersinia enterocolitica Form a Multimeric Integral Membrane Complex in Eukaryotic Cell Membranes. Journal of Bacteriology, 193, pp.6923–6928. Mueller, C. a et al., 2005. The V-antigen of Yersinia forms a distinct structure at the tip of injectisome needles. Science (New York, N.Y.), 310(5748), pp.674–6. Mukherjee, S. et al., 2006. Yersinia YopJ acetylates and inhibits kinase activation by blocking phosphorylation. Science (New York, N.Y.), 312, pp.1211–1214. Navarro, L. et al., 2007. Identification of a Molecular Target for the Yersinia Protein Kinase A. Molecular Cell, 26, pp.465–477. Nemeth, J. & Straley, S.C., 1997. Effect of Yersinia pestis YopM on experimental plague. Infection and immunity, 65, pp.924–930. 116 VII Literaturverzeichnis Neyt, C. & Cornelis, G.R., 1999. Insertion of a Yop translocation pore into the macrophage plasma membrane by Yersinia enterocolitica: requirement for translocators YopB and YopD, but not LcrG. Molecular microbiology, 33, pp.971–981. Oberhettinger, P. et al., 2011. The sequence of the pYV virulence plasmid from Yersinia enterocolitica strain WA-314 biogroup 1B serotype O:8. Plasmid, 65, pp.20–24. Oda, S., Schröder, M. & Khan, A.R., 2009. Structural basis for targeting of human RNA helicase DDX3 by poxvirus protein K7. Structure (London, England : 1993), 17(11), pp.1528–37. Orth, K. et al., 2000. Disruption of signaling by Yersinia effector YopJ, a ubiquitin-like protein protease. Science (New York, N.Y.), 290, pp.1594–1597. Orth, K., 2002. Function of the Yersinia effector YopJ. Current Opinion in Microbiology, 5, pp.38–43. Orth, K. et al., 1999. Inhibition of the mitogen-activated protein kinase kinase superfamily by a Yersinia effector. Science (New York, N.Y.), 285, pp.1920–1923. Owsianka, A.M. & Patel, A.H., 1999. Hepatitis C virus core protein interacts with a human DEAD box protein DDX3. Virology, 257, pp.330–340. Palmer, L.E. et al., 1998. YopJ of Yersinia pseudotuberculosis is required for the inhibition of macrophage TNF-alpha production and downregulation of the MAP kinases p38 and JNK. Molecular microbiology, 27, pp.953–965. Pancer, Z. et al., 2004. Somatic diversification of variable lymphocyte receptors in the agnathan sea lamprey. Nature, 430(6996), pp.174–80. Von Pawel-Rammingen, U. et al., 2000. GAP activity of the Yersinia YopE cytotoxin specifically targets the Rho pathway: a mechanism for disruption of actin microfilament structure. Molecular microbiology, 36, pp.737–748. Pepe, J.C. et al., 1995. Pathogenesis of defined invasion mutants of Yersinia enterocolitica in a BALB / c mouse model of infection . These include : Pathogenesis of Defined Invasion Mutants of Yersinia enterocolitica in a BALB / c Mouse Model of Infection. , 63(12). 117 VII Literaturverzeichnis Pepe, J.C. & Miller, V.L., 1993a. The biological role of invasin during a Yersinia enterocolitica infection. Infectious agents and disease, 2, pp.236–241. Pepe, J.C. & Miller, V.L., 1990. The Yersinia enterocolitica inv gene product is an outer membrane protein that shares epitopes with Yersinia pseudotuberculosis invasin. Journal of bacteriology, 172(7), pp.3780–9. Pepe, J.C. & Miller, V.L., 1993b. Yersinia enterocolitica invasin: a primary role in the initiation of infection. Proceedings of the National Academy of Sciences of the United States of America, 90, pp.6473–6477. Perry, R.D. & Fetherston, J.D., 1997. Yersinia pestis--etiologic agent of plague. Clinical microbiology reviews, 10(1), pp.35–66. Petoukhov, M. V & Svergun, D.I., 2005. Global rigid body modeling of macromolecular complexes against small-angle scattering data. Biophysical journal, 89(2), pp.1237–50. Petoukhov, M. V. et al., 2012. New developments in the ATSAS program package for smallangle scattering data analysis. Journal of Applied Crystallography, 45, pp.342–350. Available at: http://scripts.iucr.org/cgi-bin/paper?fs5015. Pettersen, E.F. et al., 2004. UCSF Chimera--a visualization system for exploratory research and analysis. Journal of computational chemistry, 25, pp.1605–1612. Phan, J. et al., 2003. High-resolution structure of the Yersinia pestis protein tyrosine phosphatase YopH in complex with a phosphotyrosyl mimetic-containing hexapeptide. Biochemistry, 42, pp.13113–13121. Pierson, D.E. & Falkow, S., 1993. The ail gene of Yersinia enterocolitica has a serum killing . The ail Gene of Yersinia enterocolitica Has a Role in the Ability of the Organism To Survive Serum Killing. , 61(5). Porath, J. et al., 1975. Metal chelate affinity chromatography, a new approach to protein fractionation. Nature, 258, pp.598–599. Portnoy, D.A. & Falkow, S., 1981. Virulence-associated plasmids from Yersinia enterocolitica and Yersinia pestis. Journal of bacteriology, 148, pp.877–883. 118 VII Literaturverzeichnis Portnoy, D.A., Moseley, S.L. & Falkow, S., 1981. Characterization of plasmids and plasmidassociated determinants of Yersinia enterocolitica pathogenesis. Infection and immunity, 31, pp.775–782. Prehna, G. et al., 2006. Yersinia Virulence Depends on Mimicry of Host Rho-Family Nucleotide Dissociation Inhibitors. Cell, 126, pp.869–880. Reisner, B.S. & Straley, S.C., 1992. Yersinia pestis YopM: thrombin binding and overexpression. Infection and immunity, 60(12), pp.5242–5252. Reuter, S. et al., 2014. Parallel independent evolution of pathogenicity within the genus Yersinia. Proceedings of the National Academy of Sciences of the United States of America, pp.1–6. Rocak, S. et al., 2005. Characterization of the ATPase and unwinding activities of the yeast DEAD-box protein Has1p and the analysis of the roles of the conserved motifs. Nucleic acids research, 33, pp.999–1009. Rosqvist, R., Magnusson, K.E. & Wolf-Watz, H., 1994. Target cell contact triggers expression and polarized transfer of Yersinia YopE cytotoxin into mammalian cells. The EMBO journal, 13, pp.964–972. Roy, A., Kucukural, A. & Zhang, Y., 2010. I-TASSER: a unified platform for automated protein structure and function prediction. Nature protocols, 5, pp.725–738. Ruckdeschel, K. et al., 1997. Yersinia enterocolitica promotes deactivation of macrophage mitogen-activated protein kinases extracellular signal-regulated kinase-1/2, p38, and cJun NH2-terminal kinase. Correlation with its inhibitory effect on tumor necrosis factoralpha production. The Journal of biological chemistry, 272, pp.15920–15927. Rüter, C. et al., 2010. A newly identified bacterial cell-penetrating peptide that reduces the transcription of pro-inflammatory cytokines. Journal of cell science, 123(Pt 13), pp.2190–2198. Saiki, R.K. et al., 1988. Primer-directed enzymatic amplification of DNA with a thermostable DNA polymerase. Science (New York, N.Y.), 239, pp.487–491. Sambrook, J. & Russell, D.W., 2001. Molecular Cloning - Sambrook & Russel. Human Mutation, 18, pp.1–2231. 119 VII Literaturverzeichnis Sansonetti, P.J., 2004. War and peace at mucosal surfaces. Nature reviews. Immunology, 4(12), pp.953–64. Sauvonnet, N., Pradet-Balade, B., et al., 2002. Regulation of mRNA expression in macrophages after Yersinia enterocolitica infection. Role of different Yop effectors. The Journal of biological chemistry, 277(28), pp.25133–42. Sauvonnet, N., Lambermont, I., et al., 2002. YopH prevents monocyte chemoattractant protein 1 expression in macrophages and T-cell proliferation through inactivation of the phosphatidylinositol 3-kinase pathway. Molecular microbiology, 45, pp.805–815. Scharnert, J. et al., 2013. Autonomous translocation and intracellular trafficking of the cellpenetrating and immune-suppressive effector protein YopM. Cellular and molecular life sciences : CMLS, 70(24), pp.4809–23. Scheffzek, K., Ahmadian, M.R. & Wittinghofer, A., 1998. GTPase-activating proteins: Helping hands to complement an active site. Trends in Biochemical Sciences, 23, pp.257–262. Schesser, K. et al., 1998. The yopJ locus is required for Yersinia-mediated inhibition of NFkappaB activation and cytokine expression: YopJ contains a eukaryotic SH2-like domain that is essential for its repressive activity. Molecular microbiology, 28, pp.1067–1079. Schotte, P. et al., 2004. Targeting Rac1 by the Yersinia effector protein YopE inhibits caspase-1-mediated maturation and release of interleukin-1beta. The Journal of biological chemistry, 279, pp.25134–25142. Schröder, M., 2010. Human DEAD-box protein 3 has multiple functions in gene regulation and cell cycle control and is a prime target for viral manipulation. Biochemical pharmacology, 79(3), pp.297–306. Schröder, M., 2011. Viruses and the human DEAD-box helicase DDX3: inhibition or exploitation? Biochemical Society transactions, 39, pp.679–683. Schröder, M., Baran, M. & Bowie, A.G., 2008. Viral targeting of DEAD box protein 3 reveals its role in TBK1/IKKepsilon-mediated IRF activation. The EMBO journal, 27(15), pp.2147–57. 120 VII Literaturverzeichnis Schubert, W.D. et al., 2002. Structure of internalin, a major invasion protein of Listeria monocytogenes, in complex with its human receptor E-cadherin. Cell, 111(6), pp.825– 36. Scott, P.G. et al., 2006. Crystal structure of the biglycan dimer and evidence that dimerization is essential for folding and stability of class I small leucine-rich repeat proteoglycans. The Journal of biological chemistry, 281(19), pp.13324–32. Scott, P.G. et al., 2004. Crystal structure of the dimeric protein core of decorin, the archetypal small leucine-rich repeat proteoglycan. Proceedings of the National Academy of Sciences of the United States of America, 101(44), pp.15633–8. Semenyuk, A. V. & Svergun, D.I., 1991. GNOM – a program package for small-angle scattering data processing. Journal of Applied Crystallography, 24, pp.537–540. Shao, F. et al., 2002. A Yersinia effector and a Pseudomonas avirulence protein define a family of cysteine proteases functioning in bacterial pathogenesis. Cell, 109, pp.575– 588. Shao, F. et al., 2003. Biochemical characterization of the Yersinia YopT protease: cleavage site and recognition elements in Rho GTPases. Proceedings of the National Academy of Sciences of the United States of America, 100, pp.904–909. Singleton, M.R., Dillingham, M.S. & Wigley, D.B., 2007. Structure and mechanism of helicases and nucleic acid translocases. Annual review of biochemistry, 76, pp.23–50. Skrzypek, E. et al., 2003. Application of a Saccharomyces cerevisiae model to study requirements for trafficking of Yersinia pestis YopM in eucaryotic cells. Infection and immunity, 71(2), pp.937–947. Skrzypek, E., Cowan, C. & Straley, S.C., 1998. Targeting of the Yersinia pestis YopM protein into HeLa cells and intracellular trafficking to the nucleus. Molecular microbiology, 30(5), pp.1051–1065. Skrzypek, E. & Straley, S.C., 1996. Interaction between Yersinia pestis YopM protein and human ??-thrombin. Thrombosis Research, 84, pp.33–43. Slabinski, L. et al., 2007. XtalPred: a web server for prediction of protein crystallizability. Bioinformatics (Oxford, England), 23, pp.3403–3405. 121 VII Literaturverzeichnis Smith, D.B. & Johnson, K.S., 1988. Single-step purification of polypeptides expressed in Escherichia coli as fusions with glutathione S-transferase. Gene, 67, pp.31–40. Sodeinde, O. a et al., 1988. Plasminogen activator/coagulase gene of Yersinia pestis is responsible for degradation of plasmid-encoded outer membrane proteins. Infection and immunity, 56(10), pp.2749–52. Soulat, D. et al., 2008. The DEAD-box helicase DDX3X is a critical component of the TANKbinding kinase 1-dependent innate immune response. The EMBO journal, 27(15), pp.2135–46. Stephan, R. et al., 2011. Rapid species specific identification and subtyping of Yersinia enterocolitica by MALDI-TOF Mass spectrometry. Journal of Microbiological Methods, 87, pp.150–153. Straley, S.C. & Perry, R.D., 1995. Environmental modulation of gene expression and pathogenesis in Yersinia. Trends in Microbiology, 3, pp.310–317. Street, T.O., Rose, G.D. & Barrick, D., 2006. The Role of Introns in Repeat Protein Gene Formation. Journal of Molecular Biology, 360, pp.258–266. Sulkowski, E., 1985. Purification of proteins by IMAC. Trends in Biotechnology, 3, pp.1–7. Sun, J.-P. et al., 2003. Crystal structure of the Yersinia protein-tyrosine phosphatase YopH complexed with a specific small molecule inhibitor. The Journal of biological chemistry, 278, pp.33392–33399. Sutoh, Y. & Kasahara, M., 2014. Copy number and sequence variation of leucine-rich repeat modules suggests distinct functional constraints operating on variable lymphocyte receptors expressed by agnathan T cell-like and B cell-like lymphocytes. Immunogenetics. Svergun, D., Barberato, C. & Koch, M.H.J., 1995. CRYSOL – a Program to Evaluate X-ray Solution Scattering of Biological Macromolecules from Atomic Coordinates D . Svergun , C . Barberato and M . H . J . Koch. , pp.768–773. Svergun, D.I., Petoukhov, M. V & Koch, M.H., 2001. Determination of domain structure of proteins from X-ray solution scattering. Biophysical journal, 80, pp.2946–2953. 122 VII Literaturverzeichnis Taylor, R.G., Walker, D.C. & McInnes, R.R., 1993. E. coli host strains significantly affect the quality of small scale plasmid DNA preparations used for sequencing. Nucleic acids research, 21(7), pp.1677–8. Thomson, N.R. et al., 2006. The complete genome sequence and comparative genome analysis of the high pathogenicity Yersinia enterocolitica strain 8081. PLoS genetics, 2(12), p.e206. Thornberry, N.A. & Molineaux, S.M., 1995. Interleukin-1 beta converting enzyme: a novel cysteine protease required for IL-1 beta production and implicated in programmed cell death. Protein science : a publication of the Protein Society, 4, pp.3–12. Trasak, C. et al., 2007. Yersinia protein kinase YopO is activated by a novel G-actin binding process. The Journal of biological chemistry, 282, pp.2268–2277. Treille, G.-F. & Yersin, A., 1894. La peste bubonique á Hong Kong. Annales de lInstitut Pasteur, 8, pp.662–667. Tropea, J.E., Cherry, S. & Waugh, D.S., 2009. Expression and purification of soluble His(6)tagged TEV protease. Methods in molecular biology (Clifton, N.J.), 498, pp.297–307. Trosky, J.E., Liverman, A.D.B. & Orth, K., 2008. Yersinia outer proteins: Yops. Cellular microbiology, 10(3), pp.557–65. Trülzsch, K., Oellerich, M.F. & Heesemann, J., 2007. Invasion and dissemination of Yersinia enterocolitica in the mouse infection model. Advances in experimental medicine and biology, 603, pp.279–285. Turner, J.R., 2009. Intestinal mucosal barrier function in health and disease. Nature reviews. Immunology, 9, pp.799–809. Vantrappen, G. et al., 1977. The interdigestive motor complex of normal subjects and patients with bacterial overgrowth of the small intestine. The Journal of clinical investigation, 59, pp.1158–1166. Viboud, G.I. & Bliska, J.B., 2005. Yersinia outer proteins: role in modulation of host cell signaling responses and pathogenesis. Annual review of microbiology, 59, pp.69–89. 123 VII Literaturverzeichnis Vieux, E.F. & Barrick, D., 2011. Deletion of internal structured repeats increases the stability of a leucine-rich repeat protein, YopM. Biophysical chemistry, 159(1), pp.152–161. Wauters, G., Kandolo, K. & Janssens, M., 1987. Revised biogrouping scheme of Yersinia enterocolitica. Contributions to microbiology and immunology, 9, pp.14–21. Wiedemann, A. et al., 2001. Yersinia enterocolitica invasin triggers phagocytosis via beta1 integrins, CDC42Hs and WASp in macrophages. Cellular microbiology, 3, pp.693–702. Wienken, C.J. et al., 2010. Protein-binding assays in biological liquids using microscale thermophoresis. Nature communications, 1(7), p.100. Winn, M.D. et al., 2011. Overview of the CCP4 suite and current developments. Acta crystallographica. Section D, Biological crystallography, 67(Pt 4), pp.235–42. Woestyn, S. et al., 1994. YscN, the putative energizer of the Yersinia Yop secretion machinery. Journal of bacteriology, 176, pp.1561–1569. Wollert, T., Heinz, D.W. & Schubert, W.-D., 2007. Thermodynamically reengineering the listerial invasion complex InlA/E-cadherin. Proceedings of the National Academy of Sciences of the United States of America, 104(35), pp.13960–5. Wren, B.W., 2003. The yersiniae--a model genus to study the rapid evolution of bacterial pathogens. Nature reviews. Microbiology, 1, pp.55–64. Yao, T. et al., 1999. Suppression of T and B lymphocyte activation by a Yersinia pseudotuberculosis virulence factor, yopH. The Journal of experimental medicine, 190, pp.1343–1350. Ye, Z. et al., 2009. Gr1+ cells control growth of YopM-negative yersinia pestis during systemic plague. Infection and immunity, 77(9), pp.3791–3806. Yedavalli, V.S.R.K. et al., 2004. Requirement of DDX3 DEAD box RNA helicase for HIV-1 Rev-RRE export function. Cell, 119(3), pp.381–92. Yip, C.K. et al., 2005. Structural characterization of the molecular platform for type III secretion system assembly. Nature, 435(7042), pp.702–7. Zink, D.L. et al., 1980. Plasmid-mediated tissue invasiveness in Yersinia enterocolitica. Nature, 283, pp.224–226. 124 VII Literaturverzeichnis Zumbihl, R. et al., 1999. The cytotoxin YopT of Yersinia enterocolitica induces modification and cellular redistribution of the small GTP-binding protein RhoA. The Journal of biological chemistry, 274, pp.29289–29293. 125 VIII Tabellenverzeichnis VIII Tabellenverzeichnis Tabelle 1: Geräte.................................................................................................................................. 23 Tabelle 2: Verbrauchsmittel ............................................................................................................... 24 Tabelle 3: Kits, Enzyme und Reagenzien .......................................................................................... 25 Tabelle 4: Wachstumsmedien ............................................................................................................ 26 Tabelle 5: Antibiotika, Zusätze ........................................................................................................... 27 Tabelle 6: Chemisch-kompetente E.coli ........................................................................................... 27 Tabelle 7: Proteinaufreinigung........................................................................................................... 27 Tabelle 8: Chemikalien und Zusätze.................................................................................................. 29 Tabelle 9: Elektrophorese und Western Blot .................................................................................... 29 Tabelle 10: SDS-Polyacrylamidgele................................................................................................... 30 Tabelle 11: GST-Pulldown .................................................................................................................. 30 Tabelle 12: MST-Puffer ........................................................................................................................ 31 Tabelle 13: Caspase Assay ................................................................................................................ 31 Tabelle 14: E. coli-Stämme ................................................................................................................. 32 Tabelle 15: Yersinia-Stämme.............................................................................................................. 32 Tabelle 16: Plasmide zur prokaryotischen Proteinexpression ....................................................... 32 Tabelle 17: Plasmide zur eukaryotischen Proteinexpression ........................................................ 33 Tabelle 18: Expressionskonstrukte ................................................................................................... 33 Tabelle 19: Oligonukleotide ................................................................................................................ 35 Tabelle 20: Software ............................................................................................................................ 38 ® Tabelle 21: PCR-Ansatz GoTaq ........................................................................................................ 42 ® Tabelle 22: PCR-Programm GoTaq .................................................................................................. 42 Tabelle 23: PCR-Ansatz Phusion-Polymerase ................................................................................. 42 Tabelle 24: PCR-Programm Phusion ................................................................................................. 43 Tabelle 25: YopM_Core: Datensammlung und Refinement ............................................................ 62 Tabelle 26: Intermolekulare Wechselwirkungen des YopM-Tetramers ......................................... 64 Tabelle 27: Ergebnisse der SAXS Messung von YopM_Core ......................................................... 66 Tabelle 28: Wasserstoffbrückenbindungen des YopM-Dimers ...................................................... 69 Tabelle 29: Ergebnisse der SAXS-Messung von DDX3_51-418 ...................................................... 76 Tabelle 30: Ergebnisse der SAXS-Messung des Komplexes YopM_Core/DDX3_51-418 ............ 87 126 IX Abbildungsverzeichnis IX Abbildungsverzeichnis Abbildung 1: Genomvergleich von Y. enterocolitica WA-314 und 8081 (Garzetti et al. 2012). ......... 8 Abbildung 2: Karte des Y. enterocolitica WA-314 Virulenzplasmids (Oberhettinger et al. 2011). ... 10 Abbildung 3: Aufbau des Typ III-Sekretionssystems. ..................................................................... 11 Abbildung 4: Vergleichende Sekundärstruktur von LRR-Proteinen. ............................................. 17 Abbildung 5: YopM_195/P Monomerstruktur. .................................................................................. 18 Abbildung 6: YopM_195/P Kristall-Tetramer. ................................................................................... 19 Abbildung 7: Strukturelle Komposition der DEAD-Box-Helikase DDX3 (Högbom et al. 2007). ...... 20 Abbildung 8: Protein und DNA-Leitern. ............................................................................................ 31 Abbildung 9: Kalibrierungsgerade Superdex 200 10/300 GL. ......................................................... 47 Abbildung 10: Ni-NTA Aufreinigung von 6x CT-His YopM. ............................................................. 54 Abbildung 11: Ionenaustauschchromatographie von YopM. ......................................................... 55 Abbildung 12: Größenausschlusschromatographie von YopM. .................................................... 55 Abbildung 13: Sequenzvergleich ausgewählter YopM-Proteine. ................................................... 56 Abbildung 14: Experimentelle Analyse des Translationsstarts von YopM. .................................. 57 Abbildung 15: Annotierte Aminosäuresequenz von YopM ............................................................. 57 Abbildung 16: Analytische Größenausschlusschromatographie von YopM. ............................... 58 Abbildung 17: Dynamische Lichtstreuung von YopM. .................................................................... 59 Abbildung 18: Kristalle von YopM_Full............................................................................................. 60 Abbildung 19: Initiale Kristallisationsscreens von YopM_Core. .................................................... 61 Abbildung 20: Optimierungsansätze für YopM_Core. ..................................................................... 62 Abbildung 21: Ramachandran-Plot für YopM. .................................................................................. 63 Abbildung 22: YopM-Moleküle in der Einheitszelle. ........................................................................ 64 Abbildung 23: Struktur und Topologie des YopM-Monomers. ....................................................... 65 Abbildung 24: SASREF-Modell von YopM_Core. ............................................................................. 66 Abbildung 25: Fit des YopM-Monomers mit den SAXS-Messdaten. .............................................. 67 Abbildung 26: Überlagerung des Kristalldimers mit dem ab initio-Modell. .................................. 67 Abbildung 27: Übersicht der Kontakte zwischen den Ketten A und C bzw. B und D der tetrameren Kristallstruktur. ........................................................................................................ 68 Abbildung 28: Interfaceregion zwischen dem YopM-Dimer. .......................................................... 69 Abbildung 29: Aufreinigung von YopM aus Y. enterocolitica WA-314, 8081 und Y. pseudotuberculosis YpIII ............................................................................................................ 70 Abbildung 30: Caspase-1 Assay ........................................................................................................ 71 Abbildung 31: Kristallstruktur der konservierten Domänen 1 und 2 von DDX3. .......................... 72 Abbildung 32: Pulldown von His-DDX3 mittels GST-YopM. ........................................................... 73 Abbildung 33: Analytische Größenausschlusschromatographie von DDX3. ............................... 74 Abbildung 34: Dynamische Lichtstreuung von DDX3. .................................................................... 75 Abbildung 35: Modelle von DDX3_51-418. ........................................................................................ 77 Abbildung 36: Ergebnis der MST von DDX3_1-418 mit YopM_Full bzw. YopM_Core. ................. 78 127 IX Abbildungsverzeichnis Abbildung 37: Ergebnis der MST von DDX3_51-418 mit YopM_Full bzw. YopM_Core. ............... 79 Abbildung 38: Vergleich der Bindungsaffinitäten. ........................................................................... 79 Abbildung 39: Analytische Größenausschlusschromatographie des Komplexes aus YopM_Full und DDX3_1-418. ......................................................................................................................... 80 Abbildung 40: Analytische Größenausschlusschromatographie des Komplexes aus YopM_Full und DDX3_51-418. ....................................................................................................................... 81 Abbildung 41: Analytische Größenausschlusschromatographie des Komplexes aus YopM_Full und DDX3_101-418. ..................................................................................................................... 82 Abbildung 42: Analytische Größenausschlusschromatographie des Komplexes aus YopM_Core und DDX3_1-418. .................................................................................................... 83 Abbildung 43: DLS von YopM_Core und YopM_Core/DDX3_51-418. ............................................ 84 Abbildung 44: Kristalle des Komplexes aus YopM_Core und DDX3_51-418. ............................... 85 Abbildung 45: Analyse der Komplexkristalle. .................................................................................. 85 Abbildung 46: Überprüfung der Proteinlösung. ............................................................................... 86 Abbildung 47: Streukurven von YopM_Core und YopM_Core/DDX3_51-418. .............................. 87 Abbildung 48: Modell des Komplexes aus YopM_Core und DDX3_51-418 GASBOR. ................. 88 Abbildung 49: Modell des Komplexes aus YopM_Core und DDX3_51-418 SASREF. .................. 89 Abbildung 50: Modell des Komplexes aus YopM_Core Monomer und DDX3_51-418. ................ 90 Abbildung 51: LRR-Strukturvergleich. .............................................................................................. 93 Abbildung 52: Vergleich der LRRs in drei Yersinia-Arten. ............................................................. 94 Abbildung 53: Vergleich von YopM_Wa-314 mit YopM_195/P. ...................................................... 95 Abbildung 54: Vergleich der Tetramerstrukturen der beiden kristallisierten YopM-Orthologe. . 96 Abbildung 55: Oberflächendarstellung des YopM-Dimers im Vergleich mit Decorin. ................. 97 Abbildung 56: Alignment der letzten 11 LRRs von YopM_WA-314 und YopM_195/P. ................. 97 Abbildung 57: Kontaktfläche des YopM_WA-314-Dimers. .............................................................. 98 Abbildung 58: Analyse des DDX3 N-Terminus. .............................................................................. 100 Abbildung 59: Vergleich der DDX3_51-418 Modelle. ..................................................................... 101 128 X Abkürzungsverzeichnis X Abkürzungsverzeichnis < > °C µg µl µm µM A Abb Amp APS As ATP bp BSA C CaCl2 ca. CC CD cDNA Cm cm d Da dd dH2O d.h. DLS Dmax DMSO DNA dNTP DTT E. coli EDTA EGTA et al. FD G g g GDP GFP GST GTP h HA kleiner als größer als Grad celsius Mikrogramm Mikroliter Mikrometer mikromolar Adenin Abbildung Ampicillin Ammoniumpersulfat Aminosäure Adenosintriphosphat Basenpaar (basepair) Bovine Serum Albumin Cytosin Calciumchlorid circa Coiled-coil Zirkularer Dichroismus (Circular Dichroism) copy DNA Chloramphenicol Zentimeter (centimeter) Tag (day) Dalton doppelt destilliert (double distilled) destilliertes Wasser (distilled water) das heißt Dynamische Lichtstreuung (dynamic light scattering) maximaler Durchmesser Dimethylsulfoxid Deoxyribonucleic acid Deoxyribonucleotide triphosphate (dATP, dCTP, dGTP, dTTP) Dithiothreitol Escherichia coli Ethylendiamintetraessigsäure (ethylenediamine tetra-acetic acid) (ethylene glycol-bis(β-aminoethyl ether)-N, N, N‘, N‘-tetraacetic acid und andere (lat.: „et alteri“) fast digest Guanin Gramm relative Zentrifugalkraft (relative centrifugal force) Guanosindiphosphat Green fluorescent protein Glutathion-S-transferase Guanosintriphosphat Stunde (hour) Hemagglutinin, Peptidsequenz YPYDVPDYA 129 X Abkürzungsverzeichnis H-Brücken HRP I(0) IFN-β IL IP IPTG Kan kbp Kd kDa l LB Wasserstoffbrücken Horseradish peroxidase Vorwärtsstreuung Interferon-beta Interleukin Immunoprezipitation Isopropyl β-D-1-thiogalactopyranosid Kanamycin Kilo-Basenpaare (kilo base pairs) Dissoziationskonstante Kilodalton Liter Luria broth (Luria-Bertani) LPS M MALDI MBP mA MCS mg MES min ml mM mRNA MS MW ms ng nM NO OD ON ORF PAGE PBS PBST PCR pI pM pmol PMSF PP Rac Rg Rh RhoA RNA rpm RT RT-PCR s Lipopolysaccharid molar matrix assisted laser desorption/ionisation Maltose binding protein Milliamper Multiple Cloning Site Milligram 2-(N-Morpholino)ethansulfonsäure Minute Milliliter millimolar messenger-RNA Massenspektroskopie Molekulargewicht (molecular weight) Millisekunde Nanogramm nanomolar Stickoxid (nitric oxide) Optische Dichte über nacht (over night) offener Leserahmen (open reading frame) Polyacrylamid-Gelelektrophorese phosphate buffered saline PBS mit Tween-20 Polymerasekettenreaktion (polymerase chain reaction) isoelektrischer Punkt pikomolar Pikomol Phenylmethylsulfonylfluorid Polyprolin Ras-related C3 botulinum toxin substrate Trägheitsradius (radius of gyration) hydrodynamischer Radius Ras homolog gene family, member A Ribonukleinsäure (ribonucleic acid) Umdrehungen pro Minute (revolutions per minute) Raumtemperatur Reverse Transkriptase PCR Sekunde 130 X Abkürzungsverzeichnis SAXS SD SDS T TAE Taq TBS TBST TEMED Tet TFA TfB TLR Tris TTSS U UV V Y Yop Röntgenkleinwinkelstreuung (small angle X-ray Scattering) Standardabweichung (standard deviation) Natriumlaurylsulfat (sodium dodecylsulfat) Thymin Tris-Acetat-EDTA Thermus aquaticus Tris buffered saline TBS mit Tween-20 N,N,N’,N’-Tetramethylethylendiamin Tetracyclin Trifluoressigsäure Transformationspuffer (transfrmation buffer) toll like receptor Tris-(hydroxymethyl)-aminomethane Typ drei Sekretionssystem (type three secretion system) Uracil Ultraviolett Volt Yersinia Yersinia outer (membrane) protein 131 XI Danksagung XI Danksagung An dieser Stelle möchte ich mich bei Prof. Dr. Martin Aepfelbacher für die Vergabe des interessanten Themas, die Bereitstellung des Arbeitsplatzes, die produktiven Diskussionen und sein ständiges Interesse am Fortschreiten dieser Arbeit bedanken. Herrn Prof. Dr. Wolfgang Streit danke ich für die freundliche Bereitschaft zur Begutachtung dieser Arbeit am Fachbereich Biologie. Mein Dank gilt auch Prof. Dr. Dr. Christian Betzel für die Ermöglichung der Arbeiten zur Strukturaufklärung YopMs am Laboratorium für Strukturbiologie von Infektion und Entzündung, sowie für die Bereitschaft zur Begutachtung der Disputation. Prof. Dr. Julia Kehr danke ich für die Übernahme des Vorsitzes meiner Disputation. Ganz besonderer Dank geht an PD Dr. Markus Perbandt für seine ständige Hilfe und Unterstützung meiner Arbeit, aufbauende Worte, konstruktive Diskussionen (auch mal über Fußball) und nicht zuletzt die tolle Organisation von SDI. Prof. Dr. Hartmut Schlüter und Dr. Marta Kotasinska danke ich für die zahlreichen Tipps bei der Proteinaufreinigung und die freundliche Bereitstellung der „Äkta-Facility“. PhD Alexey Kikhney danke ich für die riesige Geduld bei der Auswertung auch mal nicht so perfekter SAXS-Daten. PD Dr. Moritz Hentschke danke ich für die guten Ideen und Vorarbeiten, besonders zu Beginn meiner Arbeit. Danken möchte ich auch allen SDI-Kommilitonen für die schöne Zeit und die spannenden Diskussionen unter „Leidensgenossen“. Ein riesiger Dank geht auch an das gesamte Institut für Medizinische Mikrobiologie, alle aktuellen und ehemaligen Mitarbeiter, für die super Arbeitsatmosphäre, die freundliche Stimmung, zahlreiche unterhaltsame Kaffeepausen, Feierabendbiere, Festivalbesuche, Konzerte und Wochenendveranstaltungen. Einfach für alles innerhalb und außerhalb des Labors, was diese Arbeit so angenehm gemacht hat. Besonders danke ich hierbei natürlich auch den aktuellen und ehemaligen Mitgliedern der AG Ae: Kirsten Hennings (Wirbelwind), Liane Rauch (Labor-Oberaufseher), Manuel Wolters (Dr. Evil), Stefan Veltel (PreußenMünster), Kerstin Lardong (Kristoffffer), Claudia Trasak (CT-Only), Franzi Krawack (Pfeffi), Laura Berneking (Dr. Laura), Anja Röder (Modern Talking), Marie Schnapp (Amerikaner) und allen anderen für ein inspirierendes Arbeitsumfeld und einen entspannten Laboralltag. Bernd Zobiak danke ich für ein herzliches Willkommen in Hamburg, die vielen gemeinsamen Unternehmungen seit wir uns kennengelernt haben und das ständige Aufmuntern auch in schwierigen Phasen der Doktorarbeit. 132 XI Danksagung Besonders möchte ich natürlich meiner Familie, insbesondere meinen Eltern danken, die meinen gesamten Lebensweg erst ermöglichten und mich immer unterstützt haben. Yvonne möchte ich einfach für alles danken, die ständige Unterstützung, riesige Geduld und für unser tolles gemeinsames Leben. Ohne Dich hätte ich es nicht geschafft. 133 XII Vorveröffentlichungen XII Vorveröffentlichungen Poster mit Teilen des Inhalts dieser Arbeit wurden präsentiert bei: SDI Summer School, Hamburg (01.07.-03.07.11) 3rd National Yersinia Meeting, Tübingen (13.-14.7.2012) 64. Jahrestagung der Deutschen Gesellschaft für Hygiene und Mikrobiologie (DGHM), Hamburg (30.09.-03.10.2012) 134 XIII Eidesstattliche Versicherung XIII Eidesstattliche Versicherung Hiermit erkläre ich an Eides statt, dass ich die vorliegende Dissertationsschrift selbst verfasst und keine anderen als die angegebenen Quellen und Hilfsmittel benutzt habe. Hamburg, 30.05.2014 ____________________________ Andreas Rumm 135