Schulinternes Curriculum Chemie Oberstufe (11/EF +
Werbung

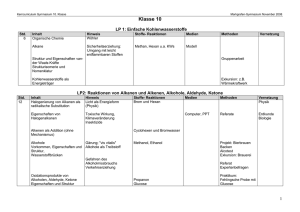
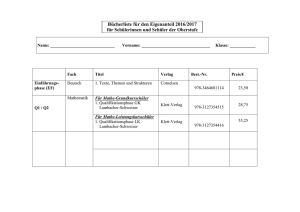
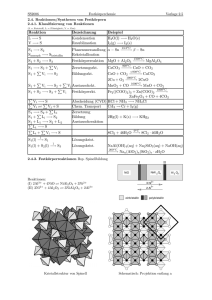
Schulinternes Curriculum Chemie Oberstufe (11/EF + Qualifikationsphase) Stand Oktober 2010 Jahrgangsstufe und Leitthema EF (11) Leitthema: Ablauf und Steuerung chemischer Reaktionen in Natur und Technik Themenfeld Unterrichtsreihen und Unterrichtsgegenstände A– Reaktionsfolge aus der organischen Chemie Unterrichtsreihe: Vom Naturstoff zum Produkt (Alternativen sind möglich: z.B. Vom Alkohol zum Aromastoff) Unterrichtsgegenstände: - Naturstoffe und ihre Extraktion - Alkohole als Lösungsmittel - Homologe Reihe der Alkohole, Nomenklatur, Stellungsisomerie - Molekülbau, Wiederholung Elektronenpaarabstoßungsmodell - Wdh. Stoffmenge, Molbegriff, molare Masse - Eigenschaften der Alkohole (Struktur-Eigenschafts-Beziehungen; hydrophil/hydrophob) - Mehrwertige Alkohole - Alkoholische Gärung (Darstellung von Alkoholen) - Alkohol und Gesellschaft: Wirkungsweise des Alkohols, Probleme des Alkoholismus - Oxidation des Alkohols zum Aldehyd/Keton - Oxidation des Alkohols zur Säure - Oxidationszahlen und Aufstellen von Redoxgleichungen - Wichtige Organische Säuren und ihre Eigenschaften - Esterdarstellung - Wichtige Ester und ihre Eigenschaften (fakultativ: Ausblick: Fette) - Geschwindigkeit chemischer Reaktionen, Definition der Reaktionsgeschwindigkeit - Abhängigkeit des Reaktionsgeschwindigkeit von verschiedenen Faktoren, RGT-Regel, Stoßtheorie - Estergleichgewicht - Verlauf der Gleichgewichtseinstellung - Massenwirkungsgesetz, Gleichgewichtskonstante K - Gleichgewichtsverschiebungen, Prinzip von LeChatelier Exkursionsmöglichkeiten: Besuch einer Brauerei Fachliche/ methodische Qualifikationen Planung, Durchführung und Auswertung – auch quantitativer – Experimente Anfertigung von Versuchsprotokollen Denken in Modellen Rechnen mit Größengleichungen an ausgewählten Beispielen Anwenden des Prinzips der Umkehrbarkeit chemischer Reaktionen Schulinternes Curriculum Chemie Oberstufe (11/EF + Qualifikationsphase) Stand Oktober 2010 B – Ein technischer Prozess C – Stoffkreislauf in Natur und Umwelt 12 Leitthema: Chemie in Anwendung und Gesellschaft C – Analytische Verfahren zur Konzentrations bestimmung Unterrichtsreihe: Ammoniaksynthese Unterrichtsgegenstände: - Ammoniak als Base - Bildung von Ammoniak als Gleichgewichtsreaktion, Beeinflussung des Gleichgewichts - Herstellung der Ausgangsstoffe - Die großtechnische Ammoniaksynthese - Politischer Hintergrund der Entwicklung durch Haber und Bosch - Bedeutung der Ammoniakproduktion für die Landwirtschaft - Ammoniumverbindungen Unterrichtsreihe: Der Kalkkreislauf Unterrichtsgegenstände: - Der natürliche Kalkkreislauf, Chemie der Tropfsteinhöhle - Der technische Kalkkreislauf - Zement und seine Herstellung - Wasserhärte - Kohlensäure und ihre Salze Exkursionsmöglichkeit: Besuch eines Zementwerkes in Geseke Unterrichtsreihe: Spurensuche – Konzentrationsbestimmung Unterrichtsgegenstände: - Konzentrationsbestimmung durch Titration (einfache Endpunkts-Titrationen) - Protolysen von Säuren/Basen; Säure-Base-Konzepte (Brönsted; Ahrrenius in seinen Grundzügen) - Protolysen als Gleichgewichtsreaktionen - Säure-Base-Indikatoren - Autoprotolyse des Wassers, pH- (pOH-) Wert - Säurestärke (pKS-/pKB- Werte) - Leitfähigkeitstitration (fakultativ) - Exkurs: Ionen in Salzen und Lösungen (Wärmekissen im Herbst) (fakultativ) - pH – Wert Berechnung starker und schwacher Säuren - Titrationskurven (stark/stark sowie schwach/stark, und Umkehrung) und Berechnung Donator-Akzeptor-Prinzip Umgang mit Messgeräten Durchführung und Auswertung von Titrationen Fehlerbetrachtung und Bewertung von Messergebnissen Umgang mit Tabellen Erfassung, Darstellung und Auswertung von Messwerten mit dem Computer Reflexion der Problematik von Grenzwertfestlegungen Schulinternes Curriculum Chemie Oberstufe (11/EF + Qualifikationsphase) Stand Oktober 2010 A – Gewinnung, Speicherung, Nutzung elektrischer Energie in der Chemie - Puffersysteme [aktuell nicht Zentralabitur relevant] - Rücktitrationen - pH-metrische und Redoxtitrationen nur LK!!! Unterrichtsreihe: Vom Rost zur Brennstoffzelle Unterrichtsgegenstände: - einfache Elektrolyse im Labor und Faraday-Gesetze - Batterien und Akkumulatoren: Grundprinzip der Funktionsweise - Galvanische Zelle: Vorgänge an Elektroden, Potentialdifferenz - Spannungsreihe der Metalle/ Nichtmetalle: Additivität der Spannungen, Standartelektrodenpotential - Konzentrationsabhängigkeit der Potentiale ohne Berechnung (nur GK) - Nur Leistungskurs: Nernst-Gleichung (quantitative Behandlung) am Beispiel folgender Systeme: o Metall/Metallion o Wasserstoff/Oxoniumion o Hydroxidion/Sauerstoff - Ggf. Nernst- Gleichung (Vgl. jeweiligen Vorgaben zum Zentralabitur) - Einstabmesskette (Rückgriff zum Themenfeld C) Aufstellen und Interpretieren von Redoxgleichungen und Teilgleichungen Herstellen von Beziehungen zwischen elektrochemischen Reaktionen und energetischen Aspekten Übertragen des Prinzips der Umkehrbarkeit auf elektrochemische Reaktionen Quantitatives Arbeiten Mathematisierung quantitativer Versuchsergebnisse Umgang mit Messgeräten Arbeiten mit Tabellen Berücksichtigung von Sicherheitsaspekten beim Umgang mit Gefahrstoffen und Elektrizität Schulinternes Curriculum Chemie Oberstufe (11/EF + Qualifikationsphase) Stand Oktober 2010 13 Leitthema: Chemische Forschung: Erkenntnisse und Produkte Eines des beiden Leitthemen ist zu machen, Auswahl möglich. B– Reaktionswege zur Herstellung von Stoffen in der organischen Chemie Unterrichtsreihe: Vom Erdöl zum Plexiglas (Vom Naturstoff zu technischen Produkten) Unterrichtsgegenstände: - Stoffklassen: Alkane, Alkene, Halogenalkane, Alkanole, Alkanale/Alkanone, Carbonsäuren, Ester - Verknüpfung von Reaktionen zu Reaktionswegen - Reaktionstypen: Einordnung von organischen Reaktionen nach Substitution, Addition, Eliminierung, jeweils einschließlich der Kenntnisse über die charakteristischen Reaktionsschritte) - Unterscheidungsmerkmale bzgl. Der Substitutionsreaktionen 1. Und 2. Ordnung - Aufklärung eines Reaktionsmechanismus: nukleophile Substitution (nur Leistungskurs) - Einfluss der Molekülstrukturen auf das Reaktionsverhalten, Funktionelle Gruppen Makromoleküle in Natur und Technik [Natürliche und Synthetische Werkstoffe] Theoriekonzept: Das Makromolekülkonzept Unterrichtsgegenstände: - Kunststoffe, Bau von Makromolekülen - Reaktionstypen zur Verknüpfung von Monomeren zu Polymeren - Technischer Verfahren zur Herstellung von Kunststoffen - Recycling von Kunststoffen - Struktur-Eigenschafts-Beziehungen - Polyester, Polyamide - Polyurethane (nur LK) - Makromoleküle in der Natur: Proteine, Kohlenhydrate Theoriekonzept: Das Aromatische System Unterrichtsgegenstände: - Aromaten - Azofarbstoffe, Triphenylmethanfarbstoffe, Indigofarbstoffe - Färbeverfahren Farbstoffe und Farbigkeit Denken in molekularen Strukturen Umgang mit verschiedenen Formeltypen Sachgerechter Umgang mit Glasgeräten und Apparaturen in der organischen Chemie Aufstellen und interpretieren von Diagrammen, Schemate, etc. Verbalisieren von Reaktionsabläufen in der organischen Chemie Sicheres Experimentieren