Schutz gegen den Zelltod im Gehirn
Werbung

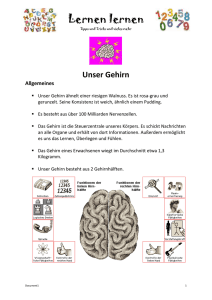
UniForum Wissenschaft und Forschung – Lehre und Studium Schutz gegen den Zelltod im Gehirn Phosphatasen und neuronale Apoptose: Erfolgreiche Kooperation in der Pharmazie führt zur Entdeckung neuer Mechanismen Das menschliche Gehirn zählt etwa 100 Milliarden Nervenzellen. Jede dieser Nervenzellen ist im Schnitt mit 10 000 anderen verbunden, d. h. im Gehirn liegen 1015 Verschaltungen zwischen Nervenzellen (Synapsen) vor. Die große Zahl der Synapsen ebenso wie die Besonderheit der Vernetzung machen die Komplexität des menschlichen Gehirns aus und sind verantwortlich für Kreativität, Emotion, Intelligenz und Sprache. Das menschliche Gehirn dürfte das komplizierteste System im ganzen Universum sein. Man sollte meinen, dass das Gehirn ein sehr robustes Organ ist, und bis zu einem gewissen Grade ist es das auch. Man kann einige Milliarden Nervenzellen verlieren, ohne dass es klinisch erkennbar wird. Doch es gibt auch Erkrankungen des Gehirns, die durch einen massiven Ausfall von Hirnleistungen gekennzeichnet sind. Beim Morbus Alzheimer beispielsweise gehen über Jahrzehnte in bestimmten Gebieten des Gehirns bis über 50 % der Nervenzellen zu Grunde. Die Folge sind Gedächtnis- und Orientierungsstörungen, Störungen der Affektivität bis hin zum völligen Verfall der Persönlichkeit und elementarer körperlicher Funktionen. Beim Schlaganfall dagegen ist der Untergang von mehr oder weniger großen Anteilen des Gehirns ein akutes Problem: Innerhalb von Stunden können Teile des Gehirns absterben. Die beiden Beispiele zeigen, wie komplex und gleichzeitig anfällig das menschliche Gehirn ist. Hohe Pflegekosten In Deutschland gibt es rund eine Million Alzheimerpatienten. Hinzu kommen jährlich etwa 200 000 Schlaganfälle. Das immense Leid Krankheiten sein können. Kein Wunder also, dass die pharmazeutische Industrie an diesen Ergebnissen großes Interesse zeigt und nun neben der Deutschen Forschungsgemeinschaft das Forschungsprogramm finanziell unterstützt. Schutz von Nervenzellen im Gehirn durch einen Wachstumsfaktor: Die Nervenzellen im CA1-Band des Hippocampus der Ratte wurden durch eine reversible Unterbrechung der Blutzufuhr (Ischämie) weitgehend zerstört (links). Eine gesteigerte Expression des Wachstumsfaktors TGF-bβ1 schützt die Neurone (Zhu et al., rechts). dieser Patienten, die enorme Belastung der Angehörigen und die hohen Kosten für Pflege und Therapie signalisieren akuten Handlungsbedarf. Die Kenntnisse der Funktion des Zentralnervensystems wurden während der letzten 20 Jahre zwar geradezu revolutioniert. Es wurden Pharmaka entwickelt, die im Experiment Nervenzellen vor einer Schädigung schützen können. Doch brachten diese ersten Entdeckungen keinen Durchbruch in der Therapie der genannten Krankheiten. In der Forschung werden deshalb weltweit neue Wege gesucht, um Nervenzellen gegen pathologische Schädigungen zu schützen. In Marburg untersuchen Arbeitsgruppen des Fachbereichs Pharmazie die neuroprotektive Potenz von Wachstumsfaktoren. Wachstumsfaktoren sind körpereigene Stoffe, die das Gehirn selbst synthetisieren kann, um unter anderem Neurone vor einer Schädigung zu schützen. Da es sich um große Proteinmoleküle handelt, sind sie nur schwer als Pharmaka ins Gehirn zu bringen; sie können die Bluthirnschranke nicht passieren. Wir haben deshalb versucht, die endogene Synthese dieser Faktoren mit Arzneistoffen zu stimulieren, und konnten nachweisen, dass ihre Expression tatsächlich gesteigert und dadurch das Gehirn vor einer Schädigung geschützt werden kann. Wachstumsfaktoren wirken insbesondere anti-apoptotisch, d. h. sie hemmen den programmierten Zelltod, die so genannte Apoptose. Wir waren natürlich daran interessiert, den Eingriff der Wachstumsfaktoren in die Kaskade des programmierten Zelltodes zu definieren. Die Apoptose wird durch pro-apoptotische Faktoren der Zelle vorangetrieben und durch antiapoptotische Faktoren gehemmt. Diese Faktoren sind meist spezifische Proteine, deren Wirkung die Zelle an- und abschalten kann. Dieses An- und Abschalten erreicht sie durch Phosphorylierung und Dephosphorylierung der Proteine. Besonders an dieser Stelle zahlte sich die Zusammenarbeit der Neurowissenschaftler mit den Phosphatase-Forschern aus. Die Neurowissenschaftler beschrieben die Proteine, die an der Regulation der neuronalen Apoptose beteiligt sind, die Phosphatase-Forscher charakterisierten die für das An- und Abschalten der Proteine verantwortlichen Enzyme. Diese Untersuchungen führten zu völlig neuen Erkenntnissen, die Grundlage für eine kausale Therapie der genannten Neues Enzym entdeckt Einen besonderen Glanzpunkt stellt unsere Entdeckung der Protein-Histidin-Phosphatase dar. Es handelt sich dabei um ein Enzym, das bisher im Säugerorganismus nicht bekannt war. Jetzt wissen wir, dass dieses Enzym in vielen Organismen und Geweben vorkommt und in Neuronen sogar angereicht zu sein scheint. Nach dem ersten Stand der Untersuchungen hat es dort offenbar eine besondere Funktion. Man darf gespannt sein, was sich daraus entwickeln wird. Die Phosphorylierung eines spezifischen Proteins kann darüber entscheiden, ob eine Nervenzelle weiterlebt oder nicht, ob sich eine Demenz entwickelt und die Persönlichkeit eines Menschen zerstört. Inzwischen konnten sechs Patente angemeldet und die Ergebnisse in wissenschaftlichen Spitzenjournalen publiziert werden. Die Kooperation von zwei wissenschaftlichen Arbeitsgruppen hat somit zu einer außerordentlich erfolgreichen Lösung von enormer praktischer Bedeutung geführt. Josef Krieglstein / Susanne Klumpp Frau Professor Klumpp hat soeben einen Ruf nach Münster angenommen. Ihre Marburger Kollegen hoffen, dass sich die ertragreiche Kooperation auch in der neuen Konstellation fortsetzen lässt. 43