Möglichkeiten zur Verwirklichung schaltbarer Fensterscheiben
Werbung

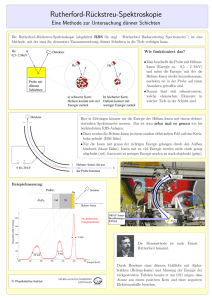
Möglichkeiten zur Verwirklichung schaltbarer Fensterscheiben Jörg Nowoczin, Universität des Saarlandes, Lehrstuhl für Pulvertechnologie von Glas und Keramik, Prof. Dr. R. Clasen in Zusammenarbeit mit Dr. H. Schmitt, Technische Physik, Im Stadtwald (Geb. 38), 66123 Saarbrücken Die Idee der passiven Sonnenenergienutzung beruht darauf, die natürliche Sonneneinstrahlung bei der Beheizung von Gebäuden mit zu nutzen. Hierbei kann es bei hoher Einstrahlung zu einer zu starken Erwärmung kommen. Für diesen Fall muß man Vorsorge-Maßnahmen treffen. Die herkömmlichen Methoden, wie Jalousien oder Vorhänge sind nicht sehr komfortabel. Fensterscheiben, die in ihren optischen Eigenschaften schaltbar sind wären wesentlich günstiger. Deshalb beschäftigen wir uns in unserer Arbeitsgruppe mit elektrochromen Schichten, die sich durch Anlegen einer Spannung in ihren optischen Eigenschaften manipulieren lassen. Für uns kommen hierfür zwei Arten von Materialien in Betracht: die Hydride der seltenen Erden und die Übergangsmetalloxide. Die gewünschte Änderung geschieht durch Ein- bzw. Auslagerung von Ionen, im Fall der Übergangsmetalloxide von Wasserstoff oder Alkalimetallen, in der Regel Lithium, bei den seltenen Erden von Wasserstoff. Elektrochrome Schichten könnten Anwendung in sogenannten „Smart Windows“ finden, deren schematischer Aufbau in Abbildung 1 dargestellt ist. In einem Ionenspeicher können z.B. H+-Ionen gespeichert werden, die durch eine, zwischen zwei optisch transparenten elektronischen Leitern angelegte, Spannung über einen Ionenleiter in die elektrochrome Schicht gelangen. Ionenspeicher elektrochrome Schicht transparenter Leiter transparenter Leiter Ionenleiter Glas Glas + _ Abbildung 1 Metallhydride Seltene Erden bilden durch chemische Reaktion mit Wasserstoff Hydride. In dünnen Yttrium-Schichten konnte Wasserstoff eingelagert und so metallisches Yttrium kontinuierlich in Yttriumhydrid überführt werden. Dies ist zuvor bei Volumenproben nicht gelungen, da diese beim Versuch der Beladung pulverisiert wurden. Es zeigt sich, daß die zuvor metallischen Proben beim Übergang von Yttrium über YH2 nach YH3-δ optisch transparent werden und eine starke Abnahme in der elektrischen Leitfähigkeit zeigen. Die Beladung kann sowohl elektrolytisch als auch katalytisch in einer Wasserstoffatmosphäre geschehen. Die Reaktion läuft nach folgendem Schema ab: Y → YH2 ↔ YH3-δ Hierbei ist nur die Reaktion vom Yttriumdihydrid zum Yttriumtrihydrid reversibel. Es ist also denkbar eine Schicht herzustellen, die in einem schaltbaren Fenster mittels einer elektrischen Spannung vom reflektierenden (YH2) in den transparenten Zustand (YH3-δ) überführt werden kann. Übergangsmetalloxide In Übergangsmetalloxiden können sowohl Wasserstoffionen als auch Alkalimetalle, wie Lithium oder Natrium, eingelagert werden. Die Kristallstruktur bleibt, im Gegensatz zu den Metallhydriden, bei der sogenannten Interkalation weitestgehend erhalten. Diese Interkalation bewirkt eine Änderung der Oxidationsstufe der Übergangangsmetalle und der elektronischen Bandstruktur was zu einer Modifikation der Leitfähigkeit und der optischen Eigenschaften führt. Man unterscheidet zwischen kathodischen und anodischen elektrochromen Übergangsmetalloxiden. Die kathodischen sind im Ausgangszustand optisch transparent und werden durch Interkalation von Ionen absorbierend bzw. reflektierend, während die anodischen vom absorbierenden Zustand in den transparenten Zustand übergehen. In der Anordnung gemäß Abbildung 1 könnte man also den Ionenspeicher durch eine elektrochrome Schicht mit entgegengesetzten Eigenschaften ersetzen, um eine effektivere Einfärbung zu erreichen. Wir beschäftigen uns speziell mit Wolframoxid WO3, einem kathodisch elektrochromen Übergangsmetall. Es sollen amorphe bzw. nanokristalline WO3-Schichten hergestellt werden, die sich schneller mit Ionen beladen lassen als kristalline Schichten. Durch den Einbau von Molybdän soll eine weitere Verzerrung des Kristallgitters erreicht werden, um noch schneller Ionen einlagern zu können. Ein neueres Modell geht davon aus, daß in WO3-y das Wolfram hauptsächlich als W 4+ und W 6+ vorliegt. Während der Einlagerung der Ionen gehen einige W 6+ in W5+ über. Durch sogenannte Small-Polaron-Übergänge zwischen Atomen der Oxidationsstufen W6+ und W 5+ sowie W 5+ und W 4+ kommt es dann zur Absorption von Licht. Die Schichten werden durch reaktives Sputtern hergestellt. Ein Wolfram-Target und ein Substrat befinden sich in einer Kammer die mit Argon und Sauerstoff gefüllt ist. Wenn man zwischen Target und Substrat eine Spannung anlegt werden durch Argon-Ionen einige Atome aus dem Target herausgelöst und reagieren dann mit Sauerstoff zu Wolframoxid, welches sich auf der Substratoberfläche anlagert. Mit Hilfe verschiedener Parameter, wie Gesamtdruck, Sauerstoffpartialdruck und Substrattemperatur, kann man die Eigenschaften der Schichten beeinflussen. Zur Untersuchung der Kristallstruktur der Schichten wird Röntgenstreuung benutzt. Lithium-Interkalation erfolgt elektrolytisch in Lithiumperchloratlösung in Propylencarbonat. Die Interkalation von Wasserstoff geschieht durch die sogenannte „Spill Over“-Methode, bei der die Schichten dünn mit Platin oder Palladium überzogen werden und dann in einer Wasserstoffatmosphäre, abhängig vom Druck, beladen werden. Hierbei kann die Änderung der Struktur während der Einlagerung mit Hilfe von IR-Absorptionsspektren beobachtet werden. Außerdem soll die Absorption und die Leitfähigkeit der Schichten in Abhängigkeit von der Beladung der Schichten untersucht werden. Im weiteren Verlauf der Arbeit soll der Versuch unternommen werden, WO3-Schichten mit Metallhydriden zu kombinieren. Das Metallhydrid würde dann in Abbildung 1 die Position des Ionenspeichers übernehmen und das Wolframoxid die der elektrochromen Schicht. Der Vorteil wäre, daß die Metallhydridschicht im nichttransparenten Zustand reflektierend ist und es so zu einer geringeren Erwärmung der Schichten kommt, wenn sich das Metallhydrid auf der Seite der Sonneneinstrahlung befindet.