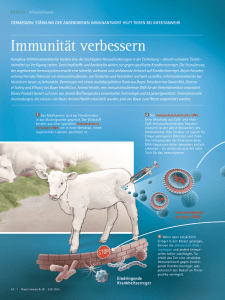
„SOCS-Proteine: Die molekulare Feuerwehr bei Entzündungen“
Werbung

„SOCS-Proteine: Die molekulare Feuerwehr bei Entzündungen“ Edgar Sawatzky, Meike Egert und Maria Stec Es ist Winter. Wieder einmal ist die Hochsaison für Erkältungen angebrochen und infektiöse Viren und Bakterien ringen mit dem Immunsystem um die Vorherrschaft im menschlichen Körper. Doch dieser Kampf ist häufig schnell vorbei, denn eine Erkältung ist meistens nur von geringer Dauer und die betreffenden Personen sind nach kurzer Zeit wieder völlig gesund. Aber wie funktioniert das eigentlich, das Gesundwerden? Dies ist die Geschichte vom Gesundwerden und wie das Gesundwerden auch krank machen kann. Das Immunsystem des menschlichen Körpers hat im Laufe der Evolution eine Vielzahl an Strategien entwickelt, um Erkrankungen erfolgreich zu bekämpfen. Dazu gehören vor allem Entzündungsreaktionen, welche durch ein komplexes Zusammenspiel von verschiedenen Immunzellen ausgelöst werden. Das Ziel einer Entzündungsreaktion ist es, von Viren infizierte Zellen und Bakterien abzutöten oder zu neutralisieren, um eine weitere Ausbreitung der Infektion zu verhindern. Durch die Reaktion des Immunsystems erfolgt zwar zunächst eine Bekämpfung der Erreger im infizierten Gewebe, doch wie klingt sie wieder ab? Als Folge einer dauerhaften Entzündung könnte gesundes Gewebe geschädigt oder im schlimmsten Fall eine Autoimmunerkrankung hervorgerufen werden. Daher hat der Körper Regulationsmechanismen entwickelt, die zum Ende einer Entzündung führen, nachdem die Erreger erfolgreich bekämpft wurden. Einer dieser Mechanismen ist auf die SOCS-Proteine (engl. Suppressor of Cytokine Signaling) zurückzuführen. Diese intrazellulären Moleküle der Immunzellen werden bei Entzündungen gebildet, um deren Verlauf zu steuern. Dabei unterbrechen sie bestimmte Signalwege, die durch Botenstoffe des Immunsystems (Cytokine) ausgelöst werden, und verhindern so, dass es zu weiteren Entzündungsprozessen kommt. SOCS-Proteine sind daher mit dafür verantwortlich, dass eine Entzündung nach einer Krankheit abklingen kann und spielen somit eine wichtige Rolle im Prozess der Genesung. Doch diese Regulationsstrategie zum Abklingen von Entzündungen ist ein zweischneidiges Schwert. Eine Vielzahl von Krankheitserregern vom Grippevirus Influenza A bis hin zum Immunschwächevirus HIV nutzen die SOCS-Proteine, um sich Zutritt in die Zellen zu verschaffen. Dringen die Krankheitserreger in den Körper ein, so erzwingen sie die Bildung der SOCS-Proteine, noch bevor das Immunsystem auf die Infektion reagieren kann. Dies führt dazu, dass die intrazelluläre Signaltransduktion in den Immunzellen unterbrochen wird, ehe es zur wichtigen Entzündung kommen kann, so dass das Immunsystem nur schwach oder gar nicht auf die Infektion reagiert. Was sind SOCS-Proteine? Die Funktion der SOCS-Proteine, Unterdrückung von Entzündungsvorgängen, hat im Bereich der Entwicklung antiinflammatorischer Wirkstoffe großes Interesse hervorgerufen. Diese Proteine werden durch Cytokine induziert und in Immunzellen exprimiert, in denen sie dann intrazellulär ihre Wirkung entfalten [1]. Die wichtigsten an inflammatorischen Prozessen beteiligten Immunzellen sind dabei vorrangig Dendritische Zellen, T- und BLymphozyten, sowie Makrophagen. (Abb.1) Die SOCS-Familie setzt sich aus acht Mitgliedern zusammen, deren primäre Aufgabe in Die Aktuelle-Wochenschau© der GDCh – Fachgruppe Biochemie 11/2013 der Immunregulation liegt. Zu ihr zählen die Proteine SOCS-1 bis 7 und CIS (engl.: Cytokine Inducible SRC homology 2 (SH2)-domain containing protein). Strukturell haben alle Mitglieder eine zentrale SH2-Domäne, sowie eine SOCS-box mit dem serin- und aspartatreichen SADADSADASDS Motiv gemein. Daneben besitzen SOCS-1 und SOCS3 zusätzlich eine Kinaseinhibitorregion (KIR). [2] SOCS-1 und SOCS-3 sind die beiden wichtigsten Immunregulatoren der SOCS-Familie. Ihre Expression findet zell- und stimulationsspezifisch statt, wobei sie durch Interleukine, Interferone, aber auch durch bakterielle Lipopolysaccharide (LPS) induziert werden können. Auf Grund ihrer schnellen Expression und ihrer kurzen Halbwertszeit von 1 bis 2 Stunden sind SOCSProteine sehr effiziente Regulatoren für die Cytokininduzierte Signalweiterleitung innerhalb einer Zelle. Wie und wo genau wirken die SOCS-Proteine? Abbildung 1: Kommen Antigen präsentierende Zellen (APC) mit Mikroben in Kontakt, so stimulieren sie verschiedene Zelltypen wie CD4+, CD8+ oder NK-Zellen. Diese wiederum sekretieren Cytokine, welche an die Rezeptoren einer Vielzahl von Immunzellen binden. Dies führt dazu, dass APCs zu einer erhöhten MHCExpression, B-Zellen zur Antikörperbildung und T-Zellen zur Proliferation angeregt, sowie Makrophagen aktiviert werden. SOCS-Proteine können direkt nach der Bindung der Cytokine diese Effekte auf die einzelnen Zelltypen unterbinden. Gelangen Pathogene in den Körper und kommen bestimmte Immunzellen mit ihnen in Kontakt, so werden, wie bereits beschrieben, verschiedene Cytokine sekretiert, die an Rezeptoren weiterer Zellen binden. Über verschiedene Mechanismen findet schließlich eine Signalübertragung in das Zellinnere statt, wobei der JAK/STAT-Signalweg einen der wichtigsten darstellt. (Abb. 2A) Die Aktivierung des JAK/STAT-Signalweges wird durch Bindung des Cytokins an den entsprechenden Cytokinrezeptor initiiert. Diese Rezeptoren sind Transmembranrezeptoren, welche zwar keine eigene Kinaseaktivität besitzen, jedoch auf der intrazellulären Seite mit einer Klasse von Tyrosinkinasen, den JanusKinasen (JAK), assoziiert sind. Bindet ein Cytokin an seinen Rezeptor, so findet in einem initialen Schritt eine Dimerisierung zweier Rezeptoren statt. Auf Grund der räumlichen Nähe kommt es so zur gegenseitigen Transphosphorylierung der rezeptorassoziierten JAK-Kinasen, die anschließend die Tyrosin-Reste der cytoplasmatischen Domänen der Rezeptoren phosphorylieren können. An diese phosphorylierten Rezeptordomänen können STAT-Proteine (engl.: Signal Transducer and Activator of Transcription) über ihre SH2-Domäne binden und ebenfalls von den JAKs an ihren Tyrosinresten phosphoryliert werden. Nach ihrer Phosphorylierung dimerisieren die STAT-Proteine und dissoziieren vom Rezeptor. Die so aktivierten STATs können anschließend in den Zellkern wandern, wo sie als Transkriptionsfaktoren wirken und die Gentranskription für anti-virale Proteine aktivieren. Die unkontrollierte STAT-Aktivierung kann die Ursache für eine Vielzahl von chronischen Entzündungen und der Entstehung von verschiedenen Tumorarten sein. Um dies zu vermeiden, muss eine hemmende Regulation dieses Signalweges stattfinden. Zu den Negativregulatoren gehört unter anderem die Familie der SOCS-Proteine. Sie sind Feedback-Inhibitoren, die nach der Aktivierung des JAK/STAT-Signalwegs induziert werden und den JAK/STAT-Signalweg danach unterbinden. (Abb. 2B) Die Aktuelle-Wochenschau© der GDCh – Fachgruppe Biochemie 11/2013 Es werden dabei vier unterschiedliche Möglichkeiten zur Hemmung der Signalübertragung mit Hilfe der SOCS-Proteinen unterschieden: [2] Abbildung 2: A: Induktion des JAK/STATSignalweges durch Cytokine: Nach der Bindung der STAT-Proteine an den Transmembranrezeptor und ihrer Phosphorylierung (1), dimerisieren sie und dissoziieren ins Cytosol (2). Diese Dimere können im Zellkern als Transkriptionsfaktoren fungieren (3) und führen u.a. zur Expression von SOCSProteinen. B: Unterbrechung des JAK/STAT-Signalweges durch Bindung der SOCS-Proteine an der SH2Bindedomänen am Rezeptor (1), Bindung an die JAK-Kinasen (2), sowie SOCS induzierter Abbau der JAK-Kinasen (3) und des Cytokinrezeptors (4) durch das Proteasom. [2] I. Durch Bindung an den bereits phosphorylierten Rezeptor mit ihrer SH2-Domäne können SOCSProteine die Bindestelle für STAT-Proteine blockieren, sodass STATs nicht phosphoryliert werden können. II. SOCS-Proteine binden direkt mit ihrer Kinaseinhibitor-Domäne (KIR) an JAK-Kinasen und inhibieren so deren Kinaseaktivität. III.SOCS-Proteine können über ihre SOCS-boxDomäne an die JAKs binden und so deren Abbau durch das Proteasom initiieren. IV.Auf Grund der Bindung von SOCS-Proteinen über die SOCS-box an den Cytokinrezeptor wird dieser durch das Proteasom abgebaut. Bei einer Infektion durch Viren werden als eine der wichtigsten Cytokinfamilien Interferone (IFN) freigesetzt, welche unter anderem den JAK/STATSignalweg induzieren. Sie setzen sich prinzipiell aus zwei Subfamilien zusammen: Die Typ I Interferone (IFNα und IFNβ) werden als Frühantwort auf virale Pathogene von infizierten Zellen gebildet und lösen nach der Bindung an einem Transmembranrezeptor, dem Interferonα/β-Rezeptor, auf einer Zielzelle zwei wichtige Mechanismen aus: 1. Infizierte Zellen präsentieren verstärkt virale Antigene über den MHC-I Proteinkomplex auf ihrer Oberfläche und können so von zytotoxischen T-Zellen (CTL) erkannt und abgetötet werden. 2. Bei nicht infizierten Zellen werden Proteine gebildet, welche die virale Replikation intrazellulär unterdrücken und diese Zellen gegen den Virus quasi immunisieren. Die Wirkung der Typ II IFN (IFNγ) liegt hauptsächlich in der Stimulierung und Aktivierung von diversen Immunzellen, wie Makrophagen, B-Lymphozyten, etc.. Die Kehrseite der Medaille Im Lauf der Evolution haben einige Viren jedoch Mechanismen entwickelt, die gezielt die Immunantwort des Körpers unterdrücken. Dabei spielt vor allem der durch Interferone induzierte Signalweg eine wichtige Rolle, da diese Viren die Expression von SOCSProteinen induzieren und somit die Signalkette nach Bindung der Interferone an den Rezeptor unterbrechen können. [3, 4] Ein bekanntes Beispiel eines solchen Virus ist der Immunschwächevirus HIV-1. Werden beispielsweise Monozyten durch HIV-1 infiziert, so führt die Anwesenheit des viralen Proteins Tat zur Expression von SOCS-2 innerhalb dieser Zellen. Dies hat zur Folge, dass die durch IFNγ ausgelöste Signalkaskade blockiert wird, da SOCS-2 die Tyrosinphosphorylierung von STAT-1 inhibiert, sodass die Zelle nicht oder nur schwach auf die Anwesenheit von IFNγ reagieren kann. Auch bei Makrophagen, einem der wichtigsten Zelltypen für die HIV-1 Replikation, kann in Anwesenheit von HIV-1 Tat eine verstärkte SOCS-Expression nachgewiesen werden. Dabei wird vor allem SOCS-3 exprimiert, welches an den Typ-I IFN-Rezeptorkomplex bindet, sodass keine Signale, die durch Typ-I Die Aktuelle-Wochenschau© der GDCh – Fachgruppe Biochemie 11/2013 Interferone induziert werden, in den Zellkern weitergeleitet werden. Infolgedessen werden keine Proteine gebildet, die die virale Replikation unterdrücken, sodass sich der Virus ungestört in den Makrophagen vermehren kann. Aussicht Auch wenn die Funktion der SOCS-Proteine ursprünglich in einer schützenden Wirkung für einen Organismus liegt, so können sie auch von Viren dazu genutzt werden, um die Chancen für eine Infektion zu verbessern, wie es am Beispiel von HIV-1 gezeigt wurde. Trotzdem, oder gerade deswegen, bieten SOCS-Proteine einen interessanten therapeutischen Ansatzpunkt zur Behandlung von Krankheiten. Auch wenn der momentane Stand der Technik noch nicht ausgereift ist, so könnte doch in siRNA (engl. small interfering-RNA) eine Lösung liegen. Diese RNA bindet gezielt an der mRNA der SOCS-Proteine, sodass diese nicht mehr gebildet werden und so die Immunblockade durch die SOCS-Proteine gebrochen wird. Doch diese Technik bleibt vorerst zumindest für therapeutische Zwecke nur eine Vision, könnte jedoch in nicht all zu ferner Zukunft ein Wundermittel bei der Behandlung des HIV1 Virus darstellen und somit generell ein entscheidender Schritt bei der Heilung viraler Erkrankungen sein. Take-Home-Message: • SOCS-Proteine sind intrazelluläre Moleküle der Immunzellen und werden bei Entzündungen gebildet, um diese runter zu regulieren. • Sie sind Feedback-Inhibitoren, die nach der Aktivierung des JAK/STAT-Signalwegs induziert werden und den JAK/STAT-Signalweg anschließend unterbinden. • Einige Pathogene haben Strategien entwickelt, um SOCS-Proteine gezielt zu induzieren und somit eine Immunreaktion zu unterbinden. • Eine gezielte Hemmung der SOCS-Proteine kann ein Ansatzpunkt für neue Therapien bei der Bekämpfung viraler Erkrankungen sein. Die Aktuelle-Wochenschau© der GDCh – Fachgruppe Biochemie 11/2013 Kontakt: Schlauer Fuchs Der Artikel wurde im Rahmen des Studienprojektes HighChem des Fachbereichs Chemie der Technischen Universität Darmstadt verfasst (s. Woche 2). Die Autoren, Edgar Sawatzky, Meike Egert und Maria Stec, sind Studierende des Fachs Chemie (Master) an der TU Darmstadt Unsere Schlaue-Fuchs-Frage zu diesem Beitrag lautete: Welches sind die wichtigsten an inflammatorischen Prozessen beteiligten Immunzellen? (E-Mail:[email protected], [email protected]). Wissenschaftliche Betreuung: Prof. Dr. Katja Schmitz (E-Mail: [email protected]). Literatur: [1] M. Kubo, T. Hanada, A. Yoshimura, Nature Immunology, 2003, 4, 1169-1176. [2] D. C. Palmer, N. P. Restifo, Trends in Immunology, 2009, 30, 592-602. [3] L. N. Akhtar, E. N. Benveniste, Journal of Virology, 2011, 85, 1912-1921. [4] W. S. Alexander, R. Starr, J. E. Fenner, G. L. Scott, E. Handman, N. S. Sprigg, J. E. Corbin, A. L. Cornish, R. Darwiche, C. M. Owczarek, T. W. H. Kay, N. A. Nicola, P. J. Hertzog, D. Metcalf, D. J. Hilton, Cell, 1999, 98, 597-608. [5] S. M. Cheng, J. C. B. Li, S. S. Lin, D. C. W. Lee, L. Liu, Z. W. Chen, A. S. Y. Lau, Blood, 2009, 113, 5192-5201. [6] L. N. Akhtar, H. W. Qin, M. T. Muldowney, L. L. Yanagisawa, O. Kutsch, J. E. Clements, E. N. Benveniste, Journal of Immunology, 2010, 185, 2393-2404. Die Aktuelle-Wochenschau© der GDCh – Fachgruppe Biochemie 11/2013