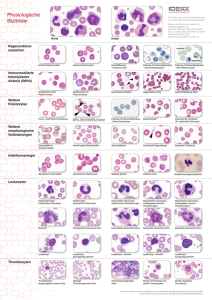
Pluripotente Stammzellen Thrombozyten Neutrophile Eosinophile
Werbung

Pluripotente Stammzellen SCF G-CSF IL-1 IL-6 SCF TPO FLT-3L SCF IL-1 IL-3 IL-6 ? CFU-GEMM B-Stammzelle IL-3 SCF GM-CSF IL-3 SCF IL-11 BFU-E IL-3 SCF CFU-Mega TPO GM-CSF IL-3 IL-6 SCF IL-11 CFU-GM GM-CSF IL-3 CFU-G GM-CSF IL-3 GM-CSF IL-3 CFU-M CFU-Eo CFU-DZ Proerythroblast Megakaryozyt EPO GM-CSF IL-5 GM-CSF M-CSF Eosinophiler Myelozyt Myeloblast Monoblast GM-CSF M-CSF GM-CSF IL-4 TNF-α GM-CSF M-CSF Prothymozyt ? CFU-Baso IL-15 GM-CSF G-CSF IL-6 IL-11 IL-1 IL-2 IL-6 IL-7 Prä-B-Zelle IL-3 CFU-E EPO T-Stammzelle IL-1 IL-6 IL-7 IL-1 IL-2 IL-4 IL-5 IL-6 CFU-DZ IL-2 IL-4 IL-3 IL-4 Basophiler Myelozyt IL-3 IL-4 BLymphoblast TLymphoblast AntigenStimulation AntigenStimulation Retikulozyt Neutrophile Monozyten Erythrozyten DZ Eosinophile Basophile NK-Zelle B-Zellen Thrombozyten IL-3 IL-4 Makrophage Mastzelle Plasmazelle DZ T-Zellen Erythrozyten Neutrophiler Granulozyt Eosinophiler Granulozyt Basophiler Granulozyt Thrombozyten Monozyt B-Lymphozyt T-Lymphozyt Unterscheidung der Leukozyten aufgrund des Nachweises von Differenzierungsantigenen Einteilung nach dem CD-System (Cluster of differentiation) -membrangebundene Glykoproteine -Bisher CD1 bis CD339 vergeben -Alle Leukozyten CD45 positiv (Tyrosinphosphatase) -Alle Leukozyten CD11 und CD18 positiv (Zelladhäsion) -Alle Lymphozyten CD3+ Anwendung: Durchflusszytometrie (FACS) Normalwerte des Differentialblutbilds Anzahl/µl Blut Mittelwert Granulozyten Neutrophile Eosinophile Basophile Monozyten Lymphozyten 4150 165 44 456 2185 Leukozyten 7000 (%) Variation (59) (2) (<1) (7) (31) 712 Ð 7588 0 Ð 397 0 Ð 112 66 Ð 846 1029 Ð 3341 2800 Ð 11200 Aufgaben des Immunsystems - Äußere Abwehr: epitheliale Barrieren (Haut), Atemwegsschleim, Zilienbewegung, saurer pH-Wert (Magen). - Innere Abwehr: Immunsystems. zelluläre und humorale Komponenten des - Schutz des Körpers vor körperfremden Strukturen (pathogene Mikroorganismen und Substanzen), die zur Infektion oder Schädigung des Körpers führen können. Infektion: Eindringen von pathogenen Mikroorganismen in den Körper und ihre Vermehrung. - Erkennung von körperfremden Strukturen (=Antigene) und deren anschließende Elimination. Mechanismen der Antigenerkennung - Opsonisierung: Anlagerung von Komplementfaktoren oder Antikörpern an körperfremde Organismen ⇒ Erleichterung der Phagozytose. Antigenpräsentation: MHC-I oder MHC-II (Major Histocompatibility Complex, Syn.:HLA) Moleküle auf der Oberfläche von antigenpräsentierenden Zellen (Makrophagen, dendritische Zellen) ⇒ körperfremdes Material wird als „fremd“ erkennbar gemacht. Expression von „Toll-like“ Rezeptoren (TLR) auf Monozyten/Makrophagen und Granulozyten, die der Erkennung pathogener Molekülstrukturen dienen ⇒ Aktivierung der Transkriptionsfaktoren HIF und NFκB ⇒ Freisetzung chemotaktisch aktiver Substanzen. TLR 4: bakterielle Lipopolysaccharide (LPS) gramnegativer Bakterien TLR 3 und 7: virale RNA Aufbau des Immunsystems - unspezifisch (angeboren): - zellulär: Granulozyten, Monozyten/Makrophagen, Mastzellen, natürliche Killerzellen (NK-Zellen). - humoral: Komplementsystem, Lysozym, Akute-Phase-Proteine, Zytokine. -spezifisch (erworben): - zellulär: T-Lymphozyten, B-Lymphozyten. - humoral: Antikörper, Zytokine. Steuerung und Koordination der Immunreaktion - Zytokine - Interleukine (IL) - Chemokine - Interferone (IFN) - Tumornekrosefaktor (TNF) - Transforming Growth Factor (TGF) Wirkung wird über Zytokinrezeptoren vermittelt ⇒ Aktivierung Janus-Kinasen (JAK) ⇒ STATs (= signal transducers and activators of transcription) Aufbau des Immunsystems - unspezifisch (angeboren): - zellulär: Granulozyten, Monozyten/Makrophagen, Mastzellen, natürliche Killerzellen (NK-Zellen). - humoral: Komplementsystem, Lysozym, Akute-Phase-Proteine, Zytokine. -spezifisch (erworben): - zellulär: T-Lymphozyten, B-Lymphozyten. - humoral: Antikörper, Zytokine. Unspezifisches zelluläres Immunsystem - Beteiligte Zellen - Granulozyten: 50% im interstitiellen Raum, 30% im Knochenmark - neutrophile - eosinophile - basophile - Mastzellen - Monozyten/Makrophagen - Natürliche Killerzellen (NK-Zellen) Normalwerte des Differentialblutbilds Mittelwert Granulozyten Neutrophile Eosinophile Basophile Monozyten Lymphozyten 4150 165 44 456 2185 Leukozyten 7000 (%) Variation (59) (2) (<1) (7) (31) 712 Ð 7588 0 Ð 397 0 Ð 112 66 Ð 846 1029 Ð 3341 2800 Ð 11200 Erythrozyten Neutrophiler Granulozyt Eosinophiler Granulozyt Basophiler Granulozyt Thrombozyten Monozyt B-Lymphozyt T-Lymphozyt Unspezifisches zelluläres Immunsystem - neutrophile Granulozyten Eigenschaften: - 50% der intravasalen neutr. Gr. zirkulieren frei im Blut, (gehen ins Differentialblutbild ein) - 50% haften an den Gefäßendothelzellen (Lunge und Milz) ⇒ rasche Freisetzung ins Blut bei Bedarf ⇒ schnelle Zunahme der Zahl der neutr. Gr. zu Beginn einer Entzündung. ⇒ „Linksverschiebung” im Differentialblutbild. - bilden mit 50-70% den größten Prozentsatz aller Leukozyten im peripheren Blut. - Lebensdauer: Stunden bis Tage Normalwerte des Differentialblutbilds Mittelwert Granulozyten Neutrophile Eosinophile Basophile Monozyten Lymphozyten 4150 165 44 456 2185 Leukozyten 7000 (%) Variation (59) (2) (<1) (7) (31) 712 Ð 7588 0 Ð 397 0 Ð 112 66 Ð 846 1029 Ð 3341 2800 Ð 11200 Pluripotente Stammzellen SCF G-CSF IL-1 IL-6 SCF TPO FLT-3L SCF IL-1 IL-3 IL-6 ? CFU-GEMM B-Stammzelle IL-3 SCF GM-CSF IL-3 SCF IL-11 BFU-E IL-3 SCF CFU-Mega TPO GM-CSF IL-3 IL-6 SCF IL-11 CFU-GM GM-CSF IL-3 CFU-G GM-CSF IL-3 GM-CSF IL-3 CFU-M CFU-Eo CFU-DZ Proerythroblast Megakaryozyt EPO GM-CSF IL-5 GM-CSF M-CSF Eosinophiler Myelozyt Myeloblast Monoblast GM-CSF M-CSF GM-CSF IL-4 TNF-α GM-CSF M-CSF Prothymozyt ? CFU-Baso IL-15 GM-CSF G-CSF IL-6 IL-11 IL-1 IL-2 IL-6 IL-7 Prä-B-Zelle IL-3 CFU-E EPO T-Stammzelle IL-1 IL-6 IL-7 IL-1 IL-2 IL-4 IL-5 IL-6 CFU-DZ IL-2 IL-4 IL-3 IL-4 Basophiler Myelozyt IL-3 IL-4 BLymphoblast TLymphoblast AntigenStimulation AntigenStimulation Retikulozyt Neutrophile Monozyten Erythrozyten DZ Eosinophile Basophile NK-Zelle B-Zellen Thrombozyten IL-3 IL-4 Makrophage Mastzelle Plasmazelle DZ T-Zellen Unspezifisches zelluläres Immunsystem - neutrophile Granulozyten Funktion: - Phagozyt („Fresszelle”) - werden durch Chemotaxine (Zytokine, Leukotriene, aktivierte Komplementfaktoren) zum Entzündungsherd gelockt. ⇒ Verlassen der Blutbahn ⇒ Einwanderung ins entzündete Gewebe (Emigration). ⇒ Phagozytose von (opsoniertem) körperfremden Material. ⇒ Anschließender Granulozyten. Abbau des phagozytierten Materials im - Freisetzung von Prostaglandinen, die die weitere Entzündungsreaktion beeinflussen. Unspezifisches zelluläres Immunsystem - neutrophile Granulozyten Abbau des phagozytierten Materials in den neutr. Gr. durch: - Enzyme: Lysozym, Hydrolasen, Elastasen, Kollagenasen, die Bakterien zerstören und und Kollagen abbauen, um die Emigration weitere Leukozyten zu erleichtern. - Sauerstoffradikale: gebildet durch NADPH-Oxidasen, wirken toxisch auf Bakterien. Die beim Abbau des phagozytierten Materials entstehende Mischung aus neutr. Gr. Und eingeschmolzenem Gewebe bezeichnet bildet den Eiter (Pus). Neutr. Gr. können Energie durch anaerobe Glykolyse gewinnen ⇒ Voraussetzung für Überleben und Funktionsfähigkeit im Eiter. Granula (ab Promyelozytenstadium) Primäre Granula Myeloperoxidase saure Phosphatase saure Hydrolasen Sekundäre Granula Kollagenase Lactoferrin (Fe-Chelator) Lysozym Tertiäre Granula Gelatinase Glykoproteine für Zelladhäsion Erythrozyten Neutrophiler Granulozyt Eosinophiler Granulozyt Basophiler Granulozyt Thrombozyten Monozyt B-Lymphozyt T-Lymphozyt Unspezifisches zelluläres Immunsystem - eosinophile Granulozyten Eigenschaften: - 2-4% der Blutleukozyten sind eosinophile Granulozyten. - Zahl der Eosinophilen unterliegt zirkadianen Schwankungen (Glukokortikoidsynthese). - Lebensdauer: ca. 4-5 Tage. Funktion: - Phagozytose. - Granula enthalten Substanzen zur Bekämpfung von Parasiten und Würmern. Erhöhte Werte bei Allergien und Autoimmunerkrankungen ⇒ Eosinophilie Eosinophile Granulozyten Vorkommen: Schleimhäute des Magen-Darm-Trakts, Atemwege, Haut Zahl bestimmt durch circadiane Rhythmik frühmorgens - niedrig Mitternacht - höchste spiegelbildliches Verhalten des Cortisols + u. a. Glukokortikoide Glukokortikoide nachts ↓ morgens↑ Eosinophile im Wesentlichen gewebeständig (Zahl wie im Knochenmark) etwa 100 - 400 x höher als im Blut Granula - Major Basic Protein (MBP) eosinophil - eosinophile kationische Protein (ECP) - eosinophile Protein X MBP + ECP → zytotoxisch für Parasiten (Würmer) aktiv. Basophile + Mastzellen → Histaminausschüttung ECP im Serum als Parameter für Aktivierung des Immunsystems → Allergische Erkrankungen Granula enthalten auch Histaminase → Abbau Histamin Eosinophiles Protein X → neurotoxisch für Parasiten, RNASE aktiv. Bildung Leukotriene (LTC4) → - bronchokonstriktorisch, sekretagog Simulation Bildung Eosinophiler durch IL5 (von TH2-Lymphos) Erythrozyten Neutrophiler Granulozyt Eosinophiler Granulozyt Basophiler Granulozyt/ Mastzelle Thrombozyten Monozyt B-Lymphozyt T-Lymphozyt Unspezifisches zelluläres Immunsystem - basophile Granulozyten/Mastzellen Eigenschaften: - mit 0-1% seltenste Granulozytenart. - Lebensdauer: ca. 4-5 Tage. - Zirkulieren im Blut und infiltrieren Gewebe im Entzündungsfall. Mastzellen sind mit basophilen Gr. eng verwandt, zirkulieren jedoch nicht, kommen also nur ortsständig vor und sind größer und reicher an Granula. - Lebensdauer: Wochen bis Monate. Unspezifisches zelluläres Immunsystem - basophile Granulozyten/Mastzellen Funktion: -Beide Zellarten können durch IgE-Antikörper aktiviert werden ⇒Degranulation: Heparin: -aktiviert Lipoproteinlipasen, erleichtert den Abbau von durch Zerstörung von Pathogenen freigesetzten Fetten. - hemmt Blutgerinnung. Histamin: -Vasodilation, erleichtert Anhaftung von Leukozyten an das Endothel, führt aber auch zu Hautrötung und Quaddelbildung. -IgE-vermittelte Soforttypreaktion (allergisches Asthma) Erythrozyten Thrombozyten Neutrophiler Granulozyt Monozyt/ Makrophage Eosinophiler Granulozyt Basophiler Granulozyt/ Mastzelle B-Lymphozyt T-Lymphozyt Unspezifisches zelluläres Immunsystem - Monozyten/Makrophagen Eigenschaften: - Monozyten sind mit 12-20 µm Durchmesser die größten Leukozyten und machen 4-10% der Blutleukozyten aus. - größte Phagozytoseaktivität aller Leukozyten. - zirkulieren 2-3 Tage im Blut und wandern dann in Gewebe ein. - Im Gewebe: unter dem Einfluss von Zytokinen oder Bestandteilen von Mikroorganismen (LPS) kommt es zur Differenzierung zu gewebsständigen Makrophagen (Makrophagenaktivierung). - Dabei kommt es zu einer Vergrößerung der Zellen um den Faktor 5-10 und zu einer Zunahme der Phagozytosekapazität. Unspezifisches zelluläres Immunsystem - Monozyten/Makrophagen Gewebsständige Makrophagen: - Mikrogliazellen im ZNS - Kupfferzellen in der Leber - Alveolarmakrophagen der Lunge - Osteoklasten im Knochen - Histiozyten im Bindegewebe - Mesangiumzellen in der Niere Unspezifisches zelluläres Immunsystem - Monozyten/Makrophagen Funktion: - Erkennung von pathogenen Mikroorganismen über TLRs. - Phagozytose und Abtötung von Mikroorganismen (Lysozym, Peroxidasen, Sauerstoffradikale, Sticktoffmonoxid (NO). - Unterstützung und Steuerung der Entzündungsreaktion durch Freisetzung von Zytokinen: IL-1 (T-Zellproliferation), TNFα (Aktivierung des Endothels ⇒ Leukozytenadhäsion), IL-12 und TGF-β (T-Zellaktivierung). - Antigenpräsentation durch MHC-II-Rezeptoren zur Aktivierung von T-Zellen. ⇒ Schlüsselverbindung zwischen unspezifischem und spezifischem zellulären Immunsystem. NK-Zellen Neutrophiler Granulozyt Eosinophiler Granulozyt Basophiler Granulozyt/ Mastzelle Thrombozyten Monozyt B-Lymphozyt T-Lymphozyt Pluripotente Stammzellen SCF G-CSF IL-1 IL-6 SCF TPO FLT-3L SCF IL-1 IL-3 IL-6 ? CFU-GEMM B-Stammzelle IL-3 SCF GM-CSF IL-3 SCF IL-11 BFU-E IL-3 SCF CFU-Mega TPO GM-CSF IL-3 IL-6 SCF IL-11 CFU-GM GM-CSF IL-3 CFU-G GM-CSF IL-3 GM-CSF IL-3 CFU-M CFU-Eo CFU-DZ Proerythroblast Megakaryozyt EPO GM-CSF IL-5 GM-CSF M-CSF Eosinophiler Myelozyt Myeloblast Monoblast GM-CSF M-CSF GM-CSF IL-4 TNF-α GM-CSF M-CSF Prothymozyt ? CFU-Baso IL-15 GM-CSF G-CSF IL-6 IL-11 IL-1 IL-2 IL-6 IL-7 Prä-B-Zelle IL-3 CFU-E EPO T-Stammzelle IL-1 IL-6 IL-7 IL-1 IL-2 IL-4 IL-5 IL-6 CFU-DZ IL-2 IL-4 IL-3 IL-4 Basophiler Myelozyt IL-3 IL-4 BLymphoblast TLymphoblast AntigenStimulation AntigenStimulation Retikulozyt Neutrophile Monozyten Erythrozyten DZ Eosinophile Basophile NK-Zelle B-Zellen Thrombozyten IL-3 IL-4 Makrophage Mastzelle Plasmazelle DZ T-Zellen Unspezifisches zelluläres Immunsystem Eigenschaften: - natürliche Killerzellen - - werden als CD3 negative Lymphozyten bezeichnet, da ihr Rezeptor nicht mit dem CD3 assoziiert ist. Besitzen keine Antigen-spezifischen Rezeptor. Erkennung infizierter Zellen über unveränderlich kodierten Rezeptor. Funktion: -bekämpfen infizierte Zellen, die kaum MHC-Moleküle exprimieren (Erythrozyten, Nervenzellen, Tumorzellen) oder die von Viren befallen sind, die die Expression von MHC-Molekülen unterdrücken (CMV) ⇒ Erkennung dieser Zellen durch T-Lymphozyten ist erschwert. NKZellen können jedoch das Fehlen von MHC-Molekülen auf infizierten Zellen erkennen (Missing-self-Prinzip). - Ausschüttung von Perforinen ⇒ Bildung Löchern in der Zellwand befallener Zellen ⇒ Zelltod. 5 klassische Entzündungszeichen nach Celsus Entzündung: Antwort eines Gewebes auf einen schädlichen Reiz (äußerer/innerer Reiz). - Rubor (Rötung) und Calor (Überwärmung): lokale Vasodilatation führt zur Steigerung der Durchblutung. - Tumor (Schwellung): Flüssigkeitsaustritt ins Gewebe durch erhöhte Gefäßpermeabilität. - Dolor (Schmerz): Erhöhung des Gewebedrucks, Prostaglandine. - Functio laesa: Beeinträchtigte Funktion des entzündeten Gewebes. Labordiagnostische Hinweise: Erhöhung der Leukozytenzahl (DiffBild) Linksverschiebung, Erhöhte Konzentration von Zytokinen (IL-6) und Akute-Phase-Proteinen, beschleunigte BSG. Emigration (Extravasation) von Leukozyten Einwanderung von Phagozyten aus dem Blutkreislauf ins Gewebe im Rahmen einer Entzündungsreaktion. - Chemotaxis: Anlocken von weiteren Leukozyten durch Freisetzung von Zytokinen aus gewebsständigen Leukozyten. - Margination: Vasodilatation (Histamin, Prostaglandine) ⇒ Verlangsamung des Blutflusses ⇒ Zellen werden zur Gefäßwand gedrängt. - Adhäsion: Freisetzung von IL-1 und TNF-α durch Makrophagen ⇒ Expression von Adhäsionsmolekülen auf Endothelzellen. - Diapedese: Verformung der Leukozyten (IL-8, TNF-α) und amöboider Durchtritt durch die Gefäßwand (IL-8 und Komplementfaktor C5a). - Migration: Wanderung zum Entzündungsort im Gewebe. Phagozytose durch Leukozyten - Erkennung eines opsonierten Fremdkörpers durch Phagozyten (Granulozyten, Makrophagen). - Bildung von Pseudopodien Umschließung des Fremkörpers. (Membranausstülpungen) und - Phagosom: vollständig endozytierter und von der abgeschnürten Plasmamembran umgebener Fremdkörper. - Phagolysosom: enzymhaltige Lysosomen lagern sich an das Phagosom an und verschmelzen mit diesem. - Abbau des körperfremden Materials. - Exozytose von Resten des Abbaus. - Anschließend steht der Phagozyt zur erneuten Phagozytose zur Verfügung. Aufbau des Immunsystems - unspezifisch (angeboren): - zellulär: Granulozyten, Monozyten/Makrophagen, Mastzellen, natürliche Killerzellen (NK-Zellen). - humoral: Komplementsystem, Lysozym, Akute-Phase-Proteine, Zytokine. -spezifisch (erworben): - zellulär: T-Lymphozyten, B-Lymphozyten. - humoral: Antikörper, Zytokine. Unspezifisches humorales Immunsystem - Lysozym - Enstehung: wird beim Zerfall von Phagoyzten aus deren Granula freigesetzt. Außerdem kommt es in der Tränenflüssigkeit vor. - Funktion: Spaltung von Mukopolysacchariden, die sich auf der Zellwand grampositiver Bakterien befinden ⇒ Bakterienzellwand wird porös ⇒ Absterben der Bakterien. Unspezifisches humorales Immunsystem - Akute Phase Proteine - Entstehung: Freisetzung von Zytokinen (z.B. IL-6) durch aktivierte Makrophagen führt zur Bildung von Akute-Phase-Proteine in der Leber - Funktion: Beispiel C-reaktives Protein (CRP). Opsoniert Oberflächenstrukturen von Bakterien und kennzeichnet diese für das Komplementsystem, dessen Aktivierung dann zur Lyse der Bakterien führt. Diagnostik: Konzentrationsbestimmung von CRP im Blut zur Diagnose oder Verlaufskontrolle (Antibiotika) einer Entzündung. Steigt mit einer Verzögerung von ca 6-10 Stunden an und hat eine HWZ von ca. 24 Stunden („hinterherhinken”). ! Beschleunigte BSG! Unspezifisches humorales Immunsystem - Komplementsystem - Familie aus ca. 20 Proteasen (C1-C9 plus Spaltprodukte), die komplementär (ergänzend) zu spezifischen Antikörpern wirken und mit diesen zusammen Fremdzellen durch Lyse (Zellauflösung) abtöten können. - Die Proteasen bilden miteinander verbundene Enzymkaskaden. - Die Aktivierung der Komplementkaskade beginnt mit der Spaltung einer Komponente, wodurch aktive Proteasen entstehen, welche die nachfolgenden C-Komponenten spalten. - Die Komplementkaskade kann über drei verschiedene Wege aktiviert werden. Unspezifisches humorales Immunsystem - Komplementsystem Funktion: - Lyse von Krankheitserregern (Porenbildung) durch den sogenannten Membranangriffskomplex. - Anlockung und Aktivierung verschiedener Leukozyten (C3a ⇒ eosinophile Gr. und C5a ⇒ neutrophile Gr.). - Steigerung der Gefäßpermeabilität (C3a ⇒ Histaminfreisetzung aus Mastzellen) - Opsonisierung von Krankheitserregern (Anlagerung von C3b and Antigen-Antikörper-Komplexe. Unspezifisches humorales Immunsystem - Komplementsystem Klassischer Weg: - Aktivierung durch: Antikörper, die bereits an ein Antigen gebunden sind: Antigen-Antikörper-Komplexe (IgG, IgM). - Erster Schritt: Aktivierung der C1q-Unterheinheit des Faktors C1 ⇒ C1q, C1r, C1s. - weiterer Verlauf: C4 ⇒ C2 ⇒ C3 ⇒ C3b, C3a ⇒ Verbindung (Antikörper) von unspezifischer und spezifischer Abwehr Unspezifisches humorales Immunsystem - Komplementsystem Alternativer Weg: - Aktivierung durch: bakterielle Oberflächenpolysaccharide (LPS) und durch CRP opsonierte Membranoberflächen. - Erster Schritt: Spaltung von C3. - weiterer Verlauf: C3b ⇒ B ⇒ D ⇒ P ⇒ C3 ⇒ C3b, C3a ⇒ C3b is zentraler Faktor, da hier die verschiedenen Kaskaden konvergieren. Außerdem opsoniert C3b selbst pathogene Mikroorganismen ⇒ Phagozytose Unspezifisches humorales Immunsystem - Komplementsystem Lektin-Weg: - Aktivierung durch: Mannose-haltige Kohlenhydrate in der Membran von Bakterien, die durch das im Blut natürlich vorkommende Lektin Mannose-bindendes Protein (MBP) erkannt werden. MBP weist strukturelle Eigenschaften wie C1q (klassischer Weg) auf. - Erster Schritt: Aktivierung von MBP. - weiterer Verlauf: C1v, C1s, C4, C2 ⇒ C3 ⇒ C3b, C3a ⇒ Mündet über C4 und C2 in den klassischen Weg der Komplementaktivierung. Unspezifisches humorales Immunsystem - Komplementsystem Gemeinsame Endstrecke: - C3 ⇒ C3b, C3a ⇒ C5 ⇒ C5b, C5a - C5b initiiert die Polymerisation des Membranangriffskomplex bestehend aus: C5b, C6, C7, C8 und C9 (10-16x) ⇒ Bildung von Poren in der Bakterienmembran ⇒ Lyse mit anschließendem Erregertod durch Einstrom von Ca2+, Na+ und H2O. Unspezifisches humorales Immunsystem - Komplementsystem Genetisch bedingter C3-Mangel: - rezidivierende Infektionen mit verschiedenen pyogenen Bakterien wie Pneumokokken und Meningokokken. - hartnäckige Lungen- bzw. Hirnhautentzündungen bereits in jungem Alter. - mangelnde Opsonisierung von Bakterien mit Komplement C3b, deshalb keine Phagozytose der Bakterien durch Makrophagen. Pluripotente Stammzellen SCF G-CSF IL-1 IL-6 SCF TPO FLT-3L SCF IL-1 IL-3 IL-6 ? CFU-GEMM B-Stammzelle IL-3 SCF GM-CSF IL-3 SCF IL-11 BFU-E IL-3 SCF CFU-Mega TPO GM-CSF IL-3 IL-6 SCF IL-11 CFU-GM GM-CSF IL-3 CFU-G GM-CSF IL-3 GM-CSF IL-3 CFU-M CFU-Eo CFU-DZ Proerythroblast Megakaryozyt EPO GM-CSF IL-5 GM-CSF M-CSF Eosinophiler Myelozyt Myeloblast Monoblast GM-CSF M-CSF GM-CSF IL-4 TNF-α GM-CSF M-CSF Prothymozyt ? CFU-Baso IL-15 GM-CSF G-CSF IL-6 IL-11 IL-1 IL-2 IL-6 IL-7 Prä-B-Zelle IL-3 CFU-E EPO T-Stammzelle IL-1 IL-6 IL-7 IL-1 IL-2 IL-4 IL-5 IL-6 CFU-DZ IL-2 IL-4 IL-3 IL-4 Basophiler Myelozyt IL-3 IL-4 BLymphoblast TLymphoblast AntigenStimulation AntigenStimulation Retikulozyt Neutrophile Monozyten Erythrozyten DZ Eosinophile Basophile NK-Zelle B-Zellen Thrombozyten IL-3 IL-4 Makrophage Mastzelle Plasmazelle DZ T-Zellen Pluripotente Stammzellen SCF G-CSF IL-1 IL-6 SCF TPO FLT-3L SCF IL-1 IL-3 IL-6 ? CFU-GEMM B-Stammzelle IL-3 SCF GM-CSF IL-3 SCF IL-11 BFU-E IL-3 SCF CFU-Mega TPO GM-CSF IL-3 IL-6 SCF IL-11 CFU-GM GM-CSF IL-3 CFU-G GM-CSF IL-3 GM-CSF IL-3 CFU-M CFU-Eo CFU-DZ Proerythroblast Megakaryozyt EPO GM-CSF IL-5 GM-CSF M-CSF Eosinophiler Myelozyt Myeloblast Monoblast GM-CSF M-CSF GM-CSF IL-4 TNF-α GM-CSF M-CSF Prothymozyt ? CFU-Baso IL-15 GM-CSF G-CSF IL-6 IL-11 IL-1 IL-2 IL-6 IL-7 Prä-B-Zelle IL-3 CFU-E EPO T-Stammzelle IL-1 IL-6 IL-7 IL-1 IL-2 IL-4 IL-5 IL-6 CFU-DZ IL-2 IL-4 IL-3 IL-4 Basophiler Myelozyt IL-3 IL-4 BLymphoblast TLymphoblast AntigenStimulation AntigenStimulation Retikulozyt Neutrophile Monozyten Erythrozyten DZ Eosinophile Basophile NK-Zelle B-Zellen Thrombozyten IL-3 IL-4 Makrophage Mastzelle Plasmazelle DZ T-Zellen Aufbau des Immunsystems - unspezifisch (angeboren): - zellulär: Granulozyten, Monozyten/Makrophagen, Mastzellen, natürliche Killerzellen (NK-Zellen). - humoral: Komplementsystem, Lysozym, Akute-Phase-Proteine, Zytokine. -spezifisch (erworben): - zellulär: T-Lymphozyten, B-Lymphozyten. - humoral: Zytokine. Antikörper (aus B-Lymphozyten/Plasmazellen), Spezifisches (erworbenes) Immunsystem - Antigenerkennung und Elimination mit hoher Präzision. - wird getragen durch Lymphozyten. - Charakteristika der erworbenen Immunität: - verzögerte Aktivierung, aber hohe Spezifität der Antigenerkennung (im Vergleich zum angeborenen Immunsystem). - es wird ein zelluläres immunologisches Gedächtnis gebildet (schnellere und stärkere Immunantwort bei erneuter Antigenexposition = Immunität). - hohes Unterscheidungsvermögen zwischen vielen verschiendenen Fremdantigenen aber auch zwischen körperfremden und körpereigenen Strukturen (Autoimmunerkrankungen). Lymphatische Organe - primäre: Thymus (Reifung von naiven T-Lymphozyten), Knochenmark (Bursa-Äquivalent: Reifung von naiven B-Lymphozyten) ⇒ Erlangung der Immunkompetenz. - sekundäre: Lymphgewebe. Milz, „Zusammenbringung” Lymphozyten. LKs, von bronchus- Antigenen und und darm-assoziierte reifen T- und B- -Antigenpräsentation durch Dendritische Zellen und Makrophagen, die aus dem entzündeten Gewebe in die sek. lymphat. Organe einwandern. ⇒Vermehrung (Proliferation) der reifen Lymphozyten in diesen Organen. ⇒ Schwellung der Milz und der Lymphknoten Spezifisches (erworbenes) Immunsystem - Antigene - Antigen: Stoffe und Strukturen, die in der Lage sind eine Immunantwort auszulösen und als immunogen bezeichnet werden. - Epitop/antigene Determinante: Bereich an der Oberfläche des Antigens gegen den Antikörper gebildet werden. - Molekülgröße entscheidet über die Immunogenität eines Stoffes (große Proteine, > 10000 Dalton). - Haptene: Stoffe, die erst nach Anlagerung an große Proteine eine Immunreaktion hervorrufen (Nickel). Spezifisches (erworbenes) Immunsystem - T-Zellen - patrouillieren nach der Reifung im Thymus als Träger der spezifischen zellulären Abwehr zwischen Blutbahn und sekundären lymphatischen Organen. - T-Zell-Rezeptor (TZR) assoziiert mit CD3: dient der Erkennung von Antigenen, die mittels MHC-Molekülen präsentiert werden. ⇒ Aktivierung von T-Zellen ⇒ Proliferation (klonale Expansion) von T-Lymphozyten ⇒ Differenzierung: - CD4 ⇒ T-Helferzellen, nach Ag-Präsentation durch MHC-II (APCs sowie B-Zellen). - CD8 ⇒ Zytotoxische T-Zelle, nach Ag-Präsentation durch MHC-I. MHC-Moleküle - Multi-Protein-Komplexe, die permanent im rauhen ER synthetisiert werden. - Binden im „loading compartment” Teilstrukturen von Antigenen, die zuvor intrazellulär zerlegt wurden. ⇒ MHC-Antigen-Komplexe, die in Vesikeln an die Oberfläche gelangen und dort „präsentiert” werden. - Nur mittels Präsentation in MHC-Molekül-Tasche kann eine T-Zelle Antigene erkennen und über den TZR aktiviert werden (T-ZellRestriktion). - dienen der korrekten Identifizierung körpereigener Zellen, die ein fremdes Antigen au der Oberfläche tragen. MHC-Moleküle unterliegen einem starken genetischen Polymorphismus, kommen also in zahlreichen Variationen vor (Histokompatibilität). Arten von MHC-Molekülen MHC-I Moleküle: - kommen auf fast allen Körperzellen vor. - präsentieren intrazelluläre (endogene) Antigene (virale Antigene). - Zielzelle: CD8 T-Zelle ⇒ zytotoxische T-Zelle MHC-II Moleküle: - kommen auf DZ, Makrophagen (APCs) und B-Lymphozyten vor. - präsentieren Teilstrukturen von Antigenen, die zuvor phagozytiert und im Phagolysosom zerlegt wurden. - Zielzelle: CD4 T-Zelle ⇒ T-Helferzelle (Th1 vs. Th2) T-Zell-Rezeptor - antigenspezifischer Rezeptor, der die Bindung an Antigen-MHCKomplexe ermöglicht. -Wird während der Reifung der T-Vorläuferzellen im Thymus gebildet. - ist mit CD3 assoziiert und bildet einen TZR/CD3-Rezeptorkomplex - ist ein Heterodimer aus den α- und β-Untereinheiten, die den variablen zentralen Teil der Antigenbindungstelle ausmachen. Die peripheren Anteile interagieren mit dem MHC-Komplex. - Ähnlichkeiten mit dem molekularen Aufbau der Immunglobuline, jedoch weisen die Ag-erkennenden Abschnitte des TZRs eine größere Vielfalt auf (1015 verschiedene TZR). - genetische Rekombination der sog. V-, D- und J-Gensegmente, die für die α- und β-Untereinheiten kodieren. - CD4 und CD 8 haben als Korezeptoren verstärkende Wirkung. Reifung der T-Lymphozyten (Thymus) - aus den T-Vorläuferzellen ohne TZR, CD4 und CD8 (doppelt negative Thymozyten) entstehen zunächst doppelt positive Thymozyten, die neben dem TZR/CD3-Komplex sowohl CD4 als auch CD8 exprimieren. - diese doppelt positiven Thymoyzten werden nun in der Rindenregion des Thymus einem Selektionsprozess unterzogen: - positive Selektion - negative Selektion - diese Prozesse stellt das Unterscheidungsvermögen zwischen körpereigen und körperfremd sicher und dient der Vermeidung von Autoimmunität (Induktion von „Selbsttoleranz”) Positive Selektion (Thymus) - Prüfung, ob durch die genetischen Rekombination TZR entstanden sind, die körpereigene MHC-Moleküle (Polymorphismus) ohne Antigenpeptid korrekt und eindeutig als „eigen” erkennen. (MHCRestriktion) - Nur diese Thymozyten dürfen überleben (positive Selektion), da nur diese Zellen körpereigene Zellen, die ein Antigen-MHC-Komplex präsentieren, als fremd erkennen können. - Alle restlichen Thymozyten, die dieses Kriterium nicht erfüllen sterben durch Apoptose. - Im Laufe der positive Selektion verlieren die doppelt positiven Thymozyten auch einen ihrer Korezeptoren (CD4 oder CD8) und werden dann als einfach positive Thymozyten bezeichnet. Negative Selektion (Thymus) - Prüfung, ob Thymozyten körpereigene Antigene erkennen, die ihnen durch MHC-I und-II Moleküle (von DZ) präsentiert werden (in Abwesenheit von kostimulatorischen Signalen). - Alle Thymozyten, die Komplexe aus körpereigenem Antigen (Selbstpeptid) und MHC-Molekülen erkennen ⇒ Apoptose (negative Selektion). - Es wird also sichergestellt, dass das Immunsystem keine körpereigenen Strukturen angreift ⇒ Vermeidung von Autoimmunität, Induktion von Selbsttoleranz. Anschließend wandern die reifen, Thymozyten in die sek. Lymphorgane, wo sie als naïve (ruhende) T-Lymphozyten auf ihre Aktivierung warten. 1. Antigenkontakt (Aktivierung der T-Zellen) - Naive T-Zellen können nicht in entzündetes Gewebe auswandern. - APCs mit Antigen-MHC-Komplex auf ihrer Oberfläche wandern in sek. lymphat. Gewebe ein und treffen auf naive T-Zellen, die mit ihrem TZR/CD3-Rezeptorkomplex den Antigen-MHC-Komplex erkennen. ⇒ klonale Expansion und Differenzierung - Gleichzeitig binden auch die Korezeptoren CD4 und CD8 and die MHC-Moleküle: - CD4 bindet and MHC-II ⇒ CD4-positive Lymphozyten differenzieren zu T-Helferzellen. - CD8 bindet MHC-1 ⇒ CD8-positive Lymphozyten differenzieren zytotoxischen T-Zellen (T-Killerzellen). - Voraussetzung ist ein gleichzeitiges kostimulatorisches Signal. - Ein Teil der T-Helfer- bzw. T-Killerzellen wird zu CD44-positiven TGedächtniszellen (immunologisches Gedächtnis). Bedeutung der Kostimulation - T-Zellen benötigen zu ihrer Aktivierung einen kostimulatorisches Signal. Fehlt dieses Signal, bleiben die T-Zellen inaktiv (anerg). - Beispiel CD28/B7 Komplex: CD 28 befindet sich auf den T-Zellen und B7 auf den APCs. - Die Abhängigkeit der T-Zell-Aktivierung von kostimulatorischen Signalen stell einen weiteren Sicherheitsmechanismus dar, der eine zu einfache Aktivierung und überschießende Immunreaktion verhindert. - Dies ermöglicht eine Immuntoleranz bie Lymphozyten, die den Thymus bereits verlassen haben (periphere Toleranz). Klassen von T-Helferzellen Welche Klasse von T-Helferzellen bevorzugt gebildet wird hängt wahrscheinlich vom Zytokinmilieu ab (IL-12 ⇒ TH1-Zellen, IL-4 TH2Zellen). - TH1-Zellen: sezernieren neben IL-2 auch Interferon γ, dass Makrophagen aktiviert und ihnen hilft, intrazelluläre Erreger abzutöten (proinflammatorisch). Interferon γ hemmt außerdem die Vermehrung von TH2-Zellen. - TH2-Zellen: sezernieren IL-4 und IL-10. IL-4 induziert die Bildung weiterer TH2-Zellen . IL-10 hemmt Makrophagen (antiinflammatorisch). TH2-Zellen sind wichtig für die B-Zell-Aktivierung und damit für die Bildung von Immunglobulinen. Exprimieren den CD 40-Liganden (Interaktion mit B-Zellen) Aktivierung von TH-Zellen (CD4 positiv) Infektion mit Viren, einigen Bakterien Phagozytose extrazell. Mikroorgansimen APC – NK- Zellen - Makrophagen – produzieren IL-12 produzieren IFNγ TH1 Lymphozyten Sekretion IL-2 und IFNγ Produktion IgM und IgG durch B-Lymphozyten Ak-Abhängige Aktivierung von NK-Zellen zelluläre Antwort inflammatorisch produzieren IL-4 und IL-6 TH2 Lymphozyten Sekretion IL-4 Ak-Switch humorale Antwort anti-inflammatorisch 2. Antigenkontakt T-Effektorzellen (T-Helfer- und T-Killerzellen) können im Gegensatz zu den naiven Thymozyten ins Gewebe auswandern. Treffen die T-Killerzellen auf infizierte Zellen, die ihnen „ihr” spezifisches Antigen auf einem MHC-1-Molekül präsentieren binden sie an diese Zelle ⇒ Freisetzung von Perforinen und Serinproteasen (Granzyme) ⇒ Absterben der infizierten Zelle. TH1-Zellen sezernieren nach dem 2. Ag-Kontakt neben IL-2 auch Interferon γ, dass Makrophagen aktiviert und ihnen hilft, intrazelluläre Erreger abzutöten (proinflammatorisch). Interferon γ hemmt außerdem die Vermehrung von TH2-Zellen. T-Zell-abhängige B-Zell-Aktivierung Das gleiche Epitop, das zuvor über einen Antigen-MHC-II-Komplex zur klonalen Expansion von CD4 T-Helferzellen geführt hat, kann auch von B-Zellen durch das passende Paratop ihres Rezeptors erkannt werden. Die B-Zellen nehmen das Antigen über den B-Zellrezeptor (BZR= membranständiges IgM oder IgD) auf, zerlegen es in kleinere Bestandteile und präsentieren die Antigenstrukturen auf MHC-IIMolekülen auf ihrer Oberfläche (Koexpression von CD40) Wird der Antigen-MHC-II-Komplex nun von den (durch klonale Expansion) zahlreich vorhandenen „passenden” T-Helferzellen erkannt und es kommt zur Interaktion. Durch Produktion von Zytokinen aus T-Helferzellen kommt es zur: Proliferation von B-Zellen, Differenzierung von B-Zellen zu Plasmazellen (AK-Bildung), Reifung der Antikörper (Affinitätssteigerung), Klassensprung (statt IgM werden vermehrt IgG und IgE freigesetzt. B-Zell-Reifung im Knochenmark Antigenunabhängige Reifung: Prä-B-Zellen, die den prä-BZR besitzen, entwickeln sich zu unreifen B-Zellen, die IgM und IgD auf ihrer Oberfläche besitzen. Antigenabhängige Reifung: B-Zellen, die IgM und IgD auf ihrer Oberfläche besitzen, werden verschiedenen körpereigenen Antigenen ausgesetzt. B-Zellen, die diese Antigene erkennen, werden durch Apoptose eliminiert (negative Selektion) = Ausbildung von Selbsttoleranz. Die verbleibenden B-Zellen wandern als reife, naive B-Zellen in die sekundären lymphatischen Organe und warten auf ihre Aktivierung. Jede B-Zelle ist also nach der Reifung mit für sie charakteristischen IgD und und IgM bestückt, die ein spezifisches Antigen binden können. B-Zell-Aktivierung T-Zell-unabhängige B-Zell-Aktivierung: Durch Bindung des Antigens and den BZR wird direkt die Proliferation und Differenzierung der B-Zelle zu Plasmazellen ausgelöst. Diese Art der Immunantwort is doch nur schwach ausgeprägt. T-Zell-abhängige B-Zell-Aktivierung: Aktivierung einer B-Zelle durch eine „passende” T-Helferzelle, die durch das gleiche Epitop aktiviert wurde. Antikörper Aufbau: - zwei leichte (light) Ketten -zwei schwere (heavy) Ketten: die schweren Ketten α,δ,ε,γ und µ bestimmen die Immunglobulinklasse, die nach diesen Ketten als IgA, IgD, IgE, IgG und IgM bezeichnet werden. - konstante Teile (Constant) - variable Teile (Variable) - Fc-Fragment: konstante Teile der der schweren Kette (CH2 und CH3) - Fab (Antigen-bindendes Fragment): VH- und VL-Domänen sowie CH1und CL-Domänen Antikörper - Antikörpervielfalt VDJ-Rekombination: - Die variablen Bereiche der H-Ketten (VH) werden von den Gensegmenten V (variable segment), D (diversity segment) und J (joining segment) kodiert. - Die variablen Bereiche der L-Ketten (VL) werden nur von den Segmenten V und J kodiert. - während der B-Zellreifung im Knochenmark werden die Gensegment V,D und J in vielen verschiedenen Kombinationen in VH und VL arrangiert (antigenunabhängig). Antikörper - Antikörpervielfalt Kombination von H- und L-Ketten: Unterschiedliche Kombination der verschiedenen VH und VL. Klassensprung: Statt initial gebildeten IgM, werden von den Plasmazellen die in ihrer Affinität modifizierbaren IgG und IgE gebildet. (T-Zell-abhängiger Prozess). Somatische Hypermutation: B-Zellen können Antikörper durch Punktmutationen in den variablen Bereichen so modifizieren, dass sie das entsprechende Antigen mit gesteigerter Affinität erkennen (Affinitätsreifung). Durch die Rezeptorvielfalt und die Fähigkeit zur klonalen Expansion, können Antigene mit hoher Spezifität und Effizienz bekämpft werden. Antikörper Funktion: - Opsonisierung - Aktivierung des Komplementsystems (Fc-Fragment) - Neutralisation von Antigenen durch Bindung.