Allergie und allergische Krankheiten - Ruhr
Werbung

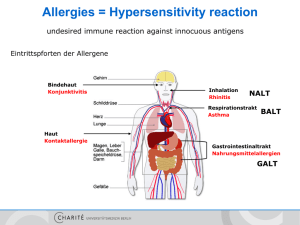
IgE und IgE-vermittelte Krankheiten von Ricarda Rauscher Bochum, 30.10.2014 Einleitung adaptive Immunantwort Allergie = schädliche Immunantwort Hypersensitivität 4 Typen der Hypersensitivität Allergie meist Typ 1 durch IgE-AK vermittelt Betroffene durch harmloses Antigen (Allergen) durch Produktion von IgE-AK sensibilisiert Kontakt mit Allergen löst Aktivierung von IgE-bindenden Zellen aus (Mast-, basophile Zellen) allergische Reaktion kann allerdings auch unabhängig von IgE auftreten (z.B. TLymphozyten Hauptfaktor der allergischen Kontaktdermatitis) 2 Einleitung bilogische Funktion IgE = Immunschutz, speziell bei parasitischen Würmern in Industrieländern hauptsächlich Allergieauslöser ca. Hälfte der Bevölkerung Nordamerikas und Europas Allergien gegen harmlose Umgebungsantigene Pathophysiologie genauer erforscht als physiologische Funktion 3 Sensibilisierung und Produktion von IgE von Plasmazellen in Lyphknoten erzeugt lokal im Bereich allerg. Reaktionen durch Plasmazellen aus Keimzentren IgE vor allem in Geweben durch FcƐRI-Rezeptoren fest an Mastzellen gebunden Bindung eines Antigens führt zur Quervernetzung dieser Rezeptoren und zur Freisetzung chemischer Mediatoren Hypersensibilisierung Typ1 basophile Zellen exprimieren ebenfalls FcƐRI 4 Sensibilisierung und Produktion von IgE Allergeneindrang durch Schleimhäute bestimmte Antigene und ihre Präsentationsart begünstigen IgE-Produktion durch Stimulation von CD4-TH2-Zellen Atmen viele versch. Proteine ein – was ist an Allergenen besonders? meist relativ kleine, gut lösliche Proteine, auf trockenen Partikeln transportiert bei Kontakt mit Schleimhaut eluiert das Allergen vom Partikel und diffundiert in Schleimhaut Immunsystem im Allgemeinen nur in sehr geringen Dosen Allergenen ausgesetzt (z.B. Beifußgewächste 1 µg pro Jahr) wahrscheinlich induziert transmucosale Präsentation niedriger Allergendosen IgE-Antworten von TH2-Zellen besonders effizient Bildung von IgE erfordert IL4 und IL13 produzierende TH2-Zellen kann durch IFN-γ TH1-Zellen gehemmt werden Im Atmungsepithel kommen dendritische Zellen mit Allergenen in Kontakt nehmen Proteinantigene auf und dadurch erfolgt Zellaktivierung Unter bestimmten Vorraussetzungen können auch Mast- oder eosinophile Zellen T-Zellen Antigene präsentieren Differenzierung zu TH2-Zellen 5 Sensibilisierung und Produktion von IgE – Allergien oft durch Enzyme ausgelöst bei Wurmbefall Sezernierung proteolytischer Enzyme Zerstören Bindegewebe stimulieren TH2-Reaktionen besonders wirksam viele Allergene sind Enzyme 6 Sensibilisierung und Produktion von IgE – Allergien oft durch Enzyme ausgelöst Netherton-Syndrom hoher IgE-Spiegel und Mehrfachallergien kennzeichnend Ursache: Mangel das Proteaseinhibitor SPINK5 persistierene entzündliche Hautrötung (Erythrodermie) wiederholte Infektionen der Haut und von anderen Körperregionen sowie zu multiplen Lebensmittelallergien 7 Sensibilisierung und Produktion von IgE – Allergien oft durch Enzyme ausgelöst möglicherweise Proteaseinhibitoren bei bestimmten Allergien als Therapeutika nicht alle Allergien Enzyme (z.B. beim Fadenwurm, dort Allergene sogar Enzyminhibitoren) bei vielen Pflanzen Allergene gefunden, nicht aber ihre Funktion 8 Sensibilisierung und Produktion von IgE – spez. Signale begünstigen bei B-Lymphozyten Isotypwechsel zu IgE Immunantwort zur Produktion von IgE durch 2 Arten von Signalen stimuliert Signale, die native T-Zellen zur Differenzierung zur TH2-Zelle veranlassen 2. Cytokine und Costimulantien von TH2-Zellen, die bei B-Zellen Übergang zur IgE-Produktion anregen 1. Entwickling der nativen CD4-T-Zelle hängt ab von Cytokinen, Antigenen, Antigendosis und Präsentationsweg IL4, IL5, IL9, IL13 TH2-Zelle IFNγ, IL12, IL23, IL27 TH1-Zelle Immunzellen in Haut und Schleimhaut vor allem auf Freisetzung von Cytokinen spezialisiert, die eine TH2-Reaktion auslösen dendr. Zellen, welche Antigene aufnehmen, wandern zu Lymphknoten, wodurch CD4-T-Zellen zu TH2-Zellen werden TH2-Zellen sezernieren IL4, Il5, IL9 und IL13 zur Umgebungsstabilisierug und weiterer Differenzierung von TH2-Zellen 9 Sensibilisierung und Produktion von IgE – spez. Signale begünstigen bei B-Lymphozyten Isotypwechsel zu IgE Hinweise, dass Mischung aus Cyto- und Chemokinen in der Umgebung sowohl die dendritischen als auch die T-Zellen in Richtung der TH2-Differenzierung polarisiert CCL2, CCL7, CCL13 wirken auf aktivierte Monozyten Produktion von IL12 wird unterdrückt Wechselwirkung zwischen AG-präsentierenden dend. Zellen und nativen B-Zellen bei fehlenden Entzündungsreizen, die Differenzierung eher in Richtung auf TH2-Zellen beeinflusst Wenn Entzündungssignale, dendr. Zellen produzieren TH1polarisierende Cytokine Cytokine und Chemokine von TH2-Zellen verstärken TH2-Reaktion und stimulieren den Isotypwechsel der B-Zellen zur Produktion von IgE 10 Sensibilisierung und Produktion von IgE – spez. Signale begünstigen bei B-Lymphozyten Isotypwechsel zu IgE IL4 oder IL13 aktiviert JAK1 und JAK3 bei T- und B-Lymhpocyten Phosphorylierung von STAT6 costimulierende Wechselwirkung zwischen CD40-Liganden der T- Zelle und CD40 der B-Zelle für alle Isotypwechsel unabdingbar 11 Sensibilisierung und Produktion von IgE – spez. Signale begünstigen bei B-Lymphozyten Isotypwechsel zu IgE IgE-Reaktion kann durch Mastzellen und basophile Zellen verstärkt werden 12 Sensibilisierung und Produktion von IgE – Umwelteinflüsse und genetische Faktoren 40% der westlichen Weltbevölkerung neigen dazu, auf eine Vielzahl von Umweltantigenen mit übertrieben starken IgE-Antworten zu reagieren (Atopie) durch mehrere Genloci beeinflusst bei atopischen Menschen höherer Gesamtspiegel an IgE und eosinophilen Zellen im Blut außerdem anfälliger für allergische Erkrankungen Umwelt und die genetische Variabilität bedingen jeweils 50% des Risikos eine Allergie zu entwickeln durch genomweite Kopplungsanalysen Reihe versch. Anfälligkeitsgene für Dermatitis und Asthma entdeckt gibt nur wenige Überschneidungen genetische Prädisposition unterscheidet sich in gewisser Weise 13 Sensibilisierung und Produktion von IgE – Umwelteinflüsse und genetische Faktoren 14 Sensibilisierung und Produktion von IgE – Umwelteinflüsse und genetische Faktoren Komplexität der Genloci macht Identifizierung schwierig • gibt auch Hinweise darauf, dass Gene evtl nur bestimmte Merkmale von allergischen Erkrankungen beeinflussen 15 Sensibilisierung und Produktion von IgE – Umwelteinflüsse und genetische Faktoren In Industrieländern häufen sich atopische Allergien, besonders Asthma am besten durch veränderte Umwelteinflüsse erklärbar veränderter Kontakt mit Infektionskrankheiten in der frühen Kindheit, Umweltverschmutzung, veränderte Allergenkonzentrationen, Veränderung der Ernährung veränderte Kontakthäufigkeit mit mikrobiellen Krankheitserregern zurzeit plausibleste Erklärung für zunehmende atopische Allergien Dieselabgase erhöhen IgE-Produktion um das 20- bis 50-fache, wenn Kombination mit Allergen Cytokinprotuktion der TH2-Zellen verändert sich 16 Sensibilisierung und Produktion von IgE – Umwelteinflüsse und genetische Faktoren Hygienehypothese Kontakt mit mehreren Krankheitserregern während der Kindheit verschiebt das Immunsystem in einen generellen Zustand der TH1-Reaktivität und der Nichtatropie Kinder mit genetischer Prädisposition und hygienischer Umwelt neigen dazu TH2-Reaktionen zu entwickeln, die auf natürliche Weise in der Zeit nach der Geburt überwiegen große Anfälligkeit für atopische allergische Erkrankungen 17 Sensibilisierung und Produktion von IgE – Umwelteinflüsse und genetische Faktoren Kinder mit Bronchiolitisanfällen in Verbindung mit dem RS-Virus neigen stärker dazu, später einmal Asthma zu entwickeln zeigen ein verändertes Verhältnis bei der Cytikonproduktion (weniger IFNγ, mehr IL4) deutet alles darauf hin, dass eine Infektion, die in einer frühen Lebensphase eine TH1- Immunantwort hervorruft, die Wahrscheinlichkeit für eine TH2-Reaktion im späteren Leben verringern dürfte und umgekehrt 18 Sensibilisierung und Produktion von IgE – Umwelteinflüsse und genetische Faktoren gegen Hygienehypothese spricht Infektion mit Helminthen Umformulierung zur Gegenregulationshypothese alle Arten von Infektionen schützen vor Atopien, indem sie die Produktion von Cytokinen wie IL10 und des transformierenden Wachstumsfaktors TGF-β fördern, die sowohl TH1- als auch TH2Reaktionen abschwächen in hygienischer Umgebung leiden Kinder weniger an Infektionen, sodass weniger dieser Cytokine ausgeschüttet werden 19 Sensibilisierung und Produktion von IgE – Regulatorische T-Zellen können allergische Reaktionen kontrollieren mononucleäre Zellen atopischer Patienten neigen bei unspezifischer Stimulation über T-Zell-Rezeptor zu Ausschüttung von TH2-Cytokinen, Gesunde nicht die versch. Typen der regulatorischen T-Zellen besitzen wahrscheinlich alle eine Funktion bei der Beeinflussung von Allergien natürliche regulatorische T-Zellen atopischer Patienten sind z.B. nicht mehr in der Lage, die Produktion von TH2-Cytokinen zu blockieren T-Zellen auch durch IDO aktiviert z.B. von dendr. Zellen sezerniert 20 Effektormechanismen bei allergischen Reaktionen Funktionen Mastzelle: Aktivitäten des Immunsystems auf lokale Infektionen lenken bei Aktivierung Entzündungsreaktion durch Freisetzung chem. Mediatoren, Prostaglandine, Leukotriene und Cytokine bei Allergien unterschiedliche Folgen der IgE-vermittelten Mastzellaktivierung Spätreaktion = Entzündung 21 IgE Effektormechanismen AK aktivieren Effektorzellen, indem sie an Rezeptor binden, der für die konstanten Fc-Domäen spezifisch sind IgE im Gegensatz zu anderen AK schon an Rezeptor gebunden 2 Typen IgE-bindender Fc-Regionen FcƐRI gehört zur Immunglobulinsuperfamilie bindet IgE hoch affin an Mastzellen, basophilen und aktivierten eosinophilen Zellen wenn Vernetzung, durch FcƐRI Aktivierungssignal bei hohen IgE-Konzentrationen erhöhte Expression von FcƐRI an Oberflächen 2. FcƐRII (CD23) C-Typ-Lektin bindet IgE mit geringer Affinität an B-Zellen, aktivierten T-Zellen, Monocyten, Eosinophilen, Blutplättchen, Thymusepithelzelln, follikulären und dendritischen Zellen spielt unter bestimmten Bedingungen bei der Erhöhung des IgE-AK eine Rolle und ist wahrscheinlich auf antigenpräsentierenden Zellen beim Einfangen von Antigenkomplexen mit IgG beteiligt 1. 22 Mastzellen maßgeblich an allergischen Reaktionen beteiligt Mastzellen enthalten zytoplasmatische Granula mit vielen saueren Proteogylkanen stammen von hämatopoetischen Stammzellen ab, reifen aber lokal und halten sich häufig in Nähe von Oberflächen auf wichtigste Faktoren für Wachstum und Entwicklung: Stammzellenfaktor, IL3, TH2-assoziierte Cytokine wie IL4 und IL9 Phosphatidylinositol-3-Kinase wichtig für Aktivierung p110δ-Isoform evtl Ansatz für eine Therapie mit Allergien, welche mit Mastzellen zusammenhängen zeigen in Abhängigkeit von empfangenen Signalen unterschiedliche Reaktionen niedrige Allergenkonzentration hohe Allergenkonzentration allergische Entzündung Immunregulation z.B. durch IL10 23 Mastzellen maßgeblich an allergischen Reaktionen beteiligt Degranulierung innerhalb von Sekunden Histamin: kurzlebiges, vasoaktives Amin Entzündungsreaktion durch Eosinophilen, Basophilen, TH2-Lymphozyten, B-Zellen und dendritische Zellen verstärkt 24 Eosinophilen - Kontrollen zur Verhinderung unpassender toxischer Reaktionen granuläre Leukozyten aus Knochenmark Granula argininreiche basische Proteine nur wenige im Blut, meist in Geweben (besonders Bindegewebe) 2 Funktionen schütten nach Aktivierung hoch toxische Granulaproteine und freie Radikale aus 2. synthetisieren nach ihrer Aktivierung chem. Mediatoren wie Prostaglandine, Leukotriene und Cytokine, die Enzündungsreaktion verstärken 1. Aktivierung und Degranulierung unterliegt strenger Regulation 1. ohne Infektion eosinophile Zellen in Knochenmark nur in geringer Zahl gebildet durch Aktivierung von TH2-Zellen Erhöhung der Entstehungsrate (durch IL5) Eotaxine locken an und aktivieren (CCL11, CCL24, CCL26) Regulation des Aktivierungszustandes 2. 3. im nichtaktivierten Zustand kein FcƐRI-Rezeptor und Schwelle zur Ausschüttung der Granula ist hoch 25 Eosinophilen - Kontrollen zur Verhinderung unpassender toxischer Reaktionen 26 Eosinophile und Basophile verursachen Entzündungen und Gewebeschäden Degranulierung der Mastzellen und TH2-Aktivierung führt zu starker Ansammlung von Eosinophilen und deren Aktivierung Eosinophile können T-Zellen Antigene präsentieren und TH2-Cytokine freisetzen stimulieren außerdem Apoptose von TH1-Zellen dauerhaftes Vorhandensein charakteristisch für chron. allerg. Entzündung Hauptverursacher auftretender Gewebeschäden Basophile ebenfalls im Bereich der Entzündung reagieren auf ähnliche Wachstumsfaktoren wie Eosinophile Hinweise auf wechselseitige Kontrolle bei Reifung der Stammzelpopulation ähnliche Funktion wie Eosinophile exprimieren FcƐRI setzen nach ihrer Aktivierung durch Cytokine oder Antigene Histamin frei 27 allergische Reaktion: Sofort- und Spätreaktion Sofortreaktion innerhalb von Sekunden durch Histamin, Prostaglandinen und anderen vorgefertigten oder schnell synthetisierten Mediatoren verursachen schnelle Zunahme der Gefäßdurchlässigkeit und die Kontraktion glatter Muskulatur Spätreaktion erst nach 8-12 Stunden bei 50% der Patienten durch Histamine, Prostaglandine, Leukotrine, Chemokine, Cytokine aus Mastzellen lenken weitere Leukozyten, darunter Eosinophile und TH2Lymphozyten zum Entzündungsherd zweite Kontraktionphase, durch T-Zellen induziert anhaltende Ödeme und Remodeling chronische allergische Entzündung 28 klinische Auswirkungen in Abhängigkeit vom Ort der Mastzellaktivierung 29 Einatmen von Allergenen - Asthma und Rhinitis Atmungssystem häufigster Eintritt allergische Rhinitis oder Heuschnupfen schwache Allergien Niesen und laufende Nase Aktivierung von Mastzellen in Schleimhaut des Riechepithels intensiver Juckreiz Niesen lokale Ödembildungen Verstopfung und laufende Nase Schleim typischerweise reich an eosinophilen Zellen Ausschüttung von Histaminen Nasenreizung und Niesanfälle allergische Bindehautentzündung (Konjunktivitis) allergische Asthma 30 Einatmen von Allergenen - Asthma und Rhinitis 31 Einatmen von Allergenen - Asthma und Rhinitis wichtiges Merkmal von Asthma: chronische Entzündung der Atemwege durch ständig erhöhte Konzentration von TH2-Lymphozyten, Eosinophilen, Neutrophilen und anderen Leukozyten gekennzeichnet ist verursachen Remodellierung der Atemwege dauerhafte Verengung mit erhöhter Schleimsekretion Ursache von zahlreichen klinischen Asthmafällen bei chronischem Asthma meist Hypersensitivität 32 Einatmen von Allergenen - Asthma und Rhinitis Becherzellenmetaplasie durch TH2-Cytokine wie IL9 und IL13 differenzieren Epithelzellen zu Becherzellen erhöhte Schleimproduktion CCR3, CCL5 und CCL11 verstärken TH2-Reaktion durch Anlocken weiterer TH2-Zellen und Eosinophile TH2-Cytokine induzieren Apoptose und Remodelierung TGFβ 33 Noch Fragen? Ansonsten vielen Dank für die Aufmerksamkeit! 34