Allergies = Hypersensitivity reaction
Werbung
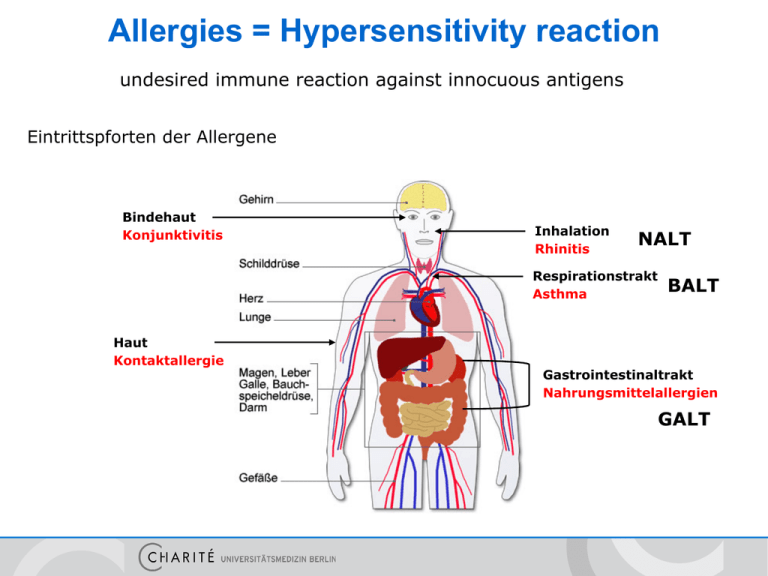
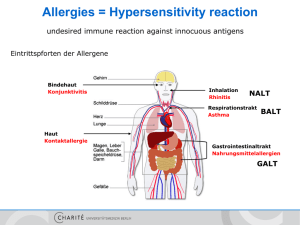
Allergies = Hypersensitivity reaction undesired immune reaction against innocuous antigens Eintrittspforten der Allergene Bindehaut Konjunktivitis Inhalation Rhinitis NALT Respirationstrakt Asthma Haut Kontaktallergie BALT Gastrointestinaltrakt Nahrungsmittelallergien GALT Klassifizierung nach Gell und Coombs Typ-I-Reaktion - IgE vermittelte Soforttyp-Reaktion Typ-II-Reaktion - Zell- oder Matrix-assoziierte Antigene - IgG vermittelt a) Fc-Rezeptor b) verändertes Signalling Typ-III-Reaktion - lösliches Antigen - Immunkomplex-vermittelt Typ-IV-Reaktion - T-Zell-vermittelt (verzögert) Typ-I-Reaktion Effektoren: Antigen: Effektormechanismen: Reaktionszeit: Klinische Beispiele: - Allergische Rhinitis - Allergische Konjunktivitis - Allergisches Asthma IgE Antikörper lösliche Antigene Mastzellaktivierung Sofort-Typ (<30 Minuten) Mast cell + IgE - spezialisierte Zellen in Mukosa / Epithel, in der Nähe von kleinen Gefäßen - oder im Bindegewebe an größeren Gefäßen - Granula enthalten saure Proteoglycane - exprimieren hochaffinen FcεRI - reifen über SCF im Gewebe (Granula) Typ1 Hypersensitivität – 1. Phase = Sensibilisierung 6. Bindung der IgE Antikörper an lokale FcεRI+ Effektorzellen (vor allem Mastzellen) 2. Diffusion in Mukosa Mastzelle 5. Diff. in TH2 3. Aufnahme durch APCs IL-5/9 IL-4 1. Allergenaufnahme TH2/9 IL-4 IL-13 APC CD4+ eosinophiler G. 4. Präsentation der CD4+ B-Zelle 5. Hilfe / Diff. von IgE+ Plasmazellen basophiler G. Typ1 Hypersensitivität – 2. Phase = Effektorphase 2. Diffusion in Mukosa 1. Allergenaufnahme B-Zelle CD4+ 3. Bindung des Allergens an IgE - FcεRI+ -Komplex auf Mastzellen 4. Degranulation der Mastzellen 5. Mediatoren bewirken Rekrutierung weiterer Effektorzellen Effektorfunktionen nach IgE-vermittelter Degranulation und Aktivierung von Mastzellen Exozytose der Granula Histamin Proteasen Dilatation der Gefäße, Kontraktion d. glatten Musk., toxisch Gewebeschädigung Modifikation von Arachidonsäure Prostaglandine Leukotriene Dilatation der Gefäße Sofortreaktion nach Minuten Kontraktion d. glatten Musk. Transkription von Zytokinen und Chemokinen TNF-α CCL11 (Eotaxin) Entzündung, TH2Polarisation, Neubildung von Zellen Leukozytenr ekrutierung, z.B. Eosinophils Spätreaktion nach 3-8 Stunden Mediators of TH2 (TH9) cells Th9 Was macht ein Allergen zum Allergen??? Eigenschaften: - kleine, stabile, stark lösliche Proteine „Carrier“ trockene Partikel transmukosale Aufnahme durch Diffusion geringe Mengen enzymatisch aktiv (Proteasen) Bindegewebsmastzellen bewirken anaphylaktischen Schock Auslöser: - Medikamente: Penicillin - Insektengift - Inhalation - Nahrungsmittel Klassische und neue Therapieansätze symptomatisch - Hemmung Wirkung Mastzellmediatoren (Histaminrezeptorantagonisten, LT-Antagonisten) - Hemmung Freisetzung Mastzellmediatoren (Steroide) - Hemmung Veränderungen der Zielzellen (ß-adrenerge Stimulation) - Hemmung T/B-Zellen (Calcineurinhemmer, Phosphodiesterasehemmer) kausal - Allergenkarrenz - Desensibilisierung - „Reprogramming of tolerance“ Ozdemir et. al. „Specific immunotherapy and turning off the T cell: how does it work?“ Ann Allergy Asthma Immunol 2011 Typ-II-Reaktion - gerichtet gegen Zell- oder Matrixproteine - IgG vermittelt - Pathomechanismen: 1. Komplementlyse und –fixierung 2. Phagozytose über Fc- und Komplementrezeptoren 3. Antikörper-abhängige, zellvermittelte Zytotoxizität durch NK-Zellen oder Eosinophile 4. Veränderung einer Rezeptorfunktion - Beispiele: AB0 Inkompatibilität Rhesus Inkompatibilität … Typ-II-Reaktion Rhesusinkompatibilität anti-D Prophylaxe (anti-Rh+ Serum nach Geburt eines Rh+ Kindes neutralisiert + eliminiert übergetretene väterliche RBCs und verhindert Aktivierung Rhspezifischer B-Zellen in der Mutter Typ-II-Reaktion Antikörper modifizieren Rezeptorfunktion 1. antagonistische Acetylcholinrezeptoren = myasthenia gravis Typ-II-Reaktion Antikörper modifizieren Rezeptorfunktion 1. agonistische TSH-rezeptor AK‘s = Morbus Basedow / Grave‘s disease Typ-III-Reaktion Immunkomplexerkrankung lösliche Antigene in Komplex mit IgG oder IgM z.B. Serumkrankheit Fc-Rezeptoren auf Thrombozyten bewirken Fixierung der Immunkomplexe auf Gefäßwand Typ-IV-Reaktion T-Zellvermittelte Reaktion verzögertem Typs (DTH) z.B. Kontaktdermatitis (Nickel) Typ-IV-Reaktion T-Zellvermittelte Reaktion verzögertem Typs (DTH) Effektorzellen - verzögerter Typ (24-72h) - antigen-spezifische TH1, TH2 oder CD8+ zytotoxische Zellen - zellvermittelte Lyse - Aktivierung und Rekrutierung von Granulozyten und Makrophagen Typ-IV-Reaktion DTH-Reaktion: Ausschüttung von z.B. IFN-γ bewirkt Aktivierung der Keratinozyten, die wiederum Zytokine und Chemokine produzieren und damit weitere Leukozyten rekrutieren. Erstkontakt bewirkt Bildung von memory T-Zellen, die sofort nach wiederholtem Kontakt ins Gewebe einwandern können und dort durch Präsentation von prozessiertem Ag reaktiviert werden. Induktoren einer Type IV Hypersensivität Allergie - Zusammenfassung • Typ I - IgE - Heuschnupfen, Asthma, Anaphylaxie • Typ II/III - IgG - Urtikaria, best. Medikamente • Typ IV - T-Zellen - Kontaktdermatitis • Unterdrückung der Immunantwort durch Hemmung der Mastzellen, Antihistaminika, Steroide, Desensibilisierung Prävention: ausschließl. Stillen in den ersten 4 Monaten, Lactobazillen Autoimmunity Autoimmunität = spezifische, adaptive Immunantwort gegen Selbstantigene Autoimmunerkrankung = Zerstörung oder Schädigung von körpereigenem Gewebe durch einen Autoantigengetriggerten Prozess Diskussion Autoimmunerkrankungen Autoantigen löst chronischen entzündliche Immunantwort aus, z.B. Myasthenia gravis autoentzündliche Erkrankungen Immunantwort gegen Selbstantigene Folge eines chronischen entzündlichen Prozesses, z.B. Rheumatoide Arthritis Autoimmunity Autoimmunerkrankung = chronisch entzündlich, schubweiser Verlauf lokal oder systemisch, familiäre Häufung jedes Organ / Organsystem kann Ziel sein Figure 13-1 Einteilung der Autoimmunerkrankungen - gerichtet gegen organspezifische Antigene (anti-TSH, anti-GAD) - Zerstörung definierter Zielorgane - gerichtet gegen ubiquitär exprimierte Antigene (antinukleäre AK‘s) - Zerstörung vieler Organe Pathogenese der Autoimmunität Suszeptibilitäts-Gene Epigenetik Umweltfaktoren (z.B. Infektionen, Gewebeschädigung) Verlust der „Selbst“-Toleranz Persistenz von funktionell selbst-reaktiven Lymphozyten Aktivierung von selbst-reaktiven Lymphozyten Immunantworten gegen Eigengewebe Ursachen von Autoimmunerkrankungen 1. Versagen der zentralen Toleranz 2. Unterbrechung der klonalen Anergie (Ko-stimulation in Peripherie) 3. Langlebigkeit reaktiver T-Zellen (kein AICD) 4. Verlust von regulatorischen Zellen 5. Kreuzreaktivität (Molekulares Mimikry) 6. Freisetzung von Selbstantigenen nach Gewebezerstörung z.B. DNA 7. Demaskierung kryptischer Selbstantigene durch z.B. Medikamente 8. Deregulierte MHC-Expression z.B. verringerte Expression im Thymus bewirkt verhindert negative Selektion 9. Mutationen / Polymorphismen 10. veränderte Zytokinbalance 11. Infektionen Autoimmunity: postulated mechanisms Multiple genetische Polymorphismen können Ursache für Autoimmunerkrankungen sein. Downloaded from: StudentConsult (on 16 January 2008 09:47 AM) © 2005 Elsevier Autoimmunity: genetic suceptibility Downloaded from: StudentConsult (on 15 January 2008 02:18 PM) © 2005 Elsevier Häufig Assoziation mit MHC Genen - veränderte AgPräsentation im Thymus und oder Peripherie Celiac disease Perfect presentation of deamidated gluten through HLA-DQ2/8 alleles DQ expressed by B cells which are not present within Thymus + no transport of deamidated gluten to the thymus Gene und Autoimmunität Eine Mutation in einem Gen führt nur sehr selten zur Entstehung von Autoimmunerkrankungen Ausnahmen Erkrankung Gen APECED AIRE (Autoimmune polyendocrinopathy candidiasis ectodermal dystrophy IPEX FOXP3 (Immunodysregulation, polyendocrinopathy, enteropathy, X-linked) ALPS (autoimmune lymphoproliferative syndrome) FAS, FASL Mechanismus defekte Expression der Selbstantigene im Thymus defekte Differenzierung von regulatorischen T-Zellen defekte Deletion von selbstreaktiven T- und B-Zellen Mutationsbedingte Störungen der Regulation? Immunaktivierung 1. Entstehung von T- und B-Zellen in primären lymphatischen Organen Regulation 1. Deletion von selbstreaktiven T- und B-Zellen im Thymus (AIRE=APECD) und Knochenmark 2. Erkennung von Pathogenen und Aktivierung des angeborenen Immunsystems 2. Modulation der TLRSignaltransduktion (NOD2) 3. Antigenpräsentation und Aktivierung von Tund B-Zellen 3. Inhibition durch z.B. CD25+ regulatorische T-Zellen (CD25, Foxp3=IPEX) oder negativ regulierende Signalmoleküle (PTPN22) 4. Differenzierung von Effektor-T-Zellen und Plasmazellen und langlebigen GedächtnisZellen 4. Apoptoseinduktion (FasL=ALPS) Autoimmunity: role of infections Downloaded from: StudentConsult (on 15 January 2008 02:43 PM) © 2005 Elsevier Figure 13-26 Autoimmunity: role of infections Molecular mimicry = Ähnlichkeiten (Nachahmen) in der Sequenz oder Struktur zwischen Selbst- und Fremdpeptiden ist ausreichend, um selbstreaktive T- und B-Zellen zu aktivieren Pathogenese RA- exogene Faktoren Umwelteinflüsse § städtische Umgebung erhöht Prävalenz („Life style“ Faktoren) § Rauchen erhöht Prävalenz (z.B. erhöhte Anzahl citrullinierter Peptide in der Lunge) § Exposition mit Siliziumdioxid (Quarz)- häufiger bei Männern; Neurohumorale Einflüsse § Frauen häufiger betroffen § erhöhte Prävalenz bei komplikationsreicher Schwangerschaft (Hyperemesis; Hypertension; Präeklampsie) § Besserung in der Schwangerschaft, Rezidiv postpartum § bei Apoplex oder Nervenläsion Besserung in der betroffenen Extremität Infektionen § EBV, Parvovirus § Proteobakterien; Mycoplasmen Bakterien § vermehrte Bildung citrullinierter Peptide unter Entzündung Pathogenese RA- exogene Faktoren Klareskog et. al. „Smoking, citrullination and genetic variability in the pathogenesis of rheumatoid arthritis?“ Seminars in Immunology 2011 Pathogenese RA- exogene Faktoren Klareskog et. al. „Smoking, citrullination and genetic variability in the pathogenesis of rheumatoid arthritis?“ Seminars in Immunology 2011 Einteilung der Autoimmunerkrankungen nach den Hypersensibilitätstypen Hypersensitivity: immune complexmediates diseases • sytemische Erkrankungen • Neutrophile Granulozyten binden an Immun-Komplexe • Ag-Ak-Komplexe werden bei jeder Immunreaktion gebildet und verursachen dann Krankheiten, wenn sie in zu großem Maße gebildet werden • Schädigungen in Blutgefäßen und Nierenglomerulum • Goodpasture (links) Systemic lupus erythematosus (rechts) Downloaded from: StudentConsult (on 15 January 2008 02:18 PM) © 2005 Elsevier Hygiene Theorie Hygiene Theorie Hypersensitivity Downloaded from: StudentConsult (on 15 January 2008 02:18 PM) © 2005 Elsevier