Die Bedeutung einer regulierten Infiltration von Leukozyten für den
Werbung

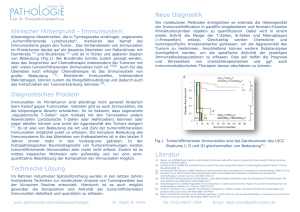
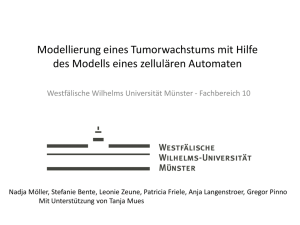
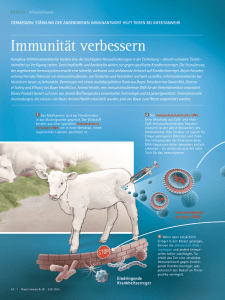
KARDIOLOGIE TOPTHEMA CME Die Bedeutung einer regulierten Infiltration von Leukozyten für den Heilungsverlauf nach einem Herzinfarkt Ein ischämiebedingter Zelltod von Herzmuskelgewebe wie im Falle eines Herzinfarkts erfordert zahlreiche Umbaumaßnahmen zur Gewährleistung essentieller Funktionsleistungen des Herzens. Dieser adaptive Mechanismus, das sog. kardiale Remodelling, wird durch die Infiltration und Akkumulation von Immunzellen initiiert und determiniert. Forscher des Max-Planck-Instituts für Herz- und Lungenforschung identifizierten in Zusammenarbeit mit der Schüchtermann-Klinik und der Kerkhoff-Klinik einen neuen Regulationsmechanismus zur Rekrutierung und Akkumulation von Makrophagen. mie sowie die lokale Stoffwechselrate des ischämischen Herzmuskels bestimmen dabei das Ausmaß des Zelltods und somit die Größe des Myokardinfarktes. Mit zunehmender Dauer der Ischämie entsteht ein irreversibler Herzmuskelschaden, der sich über alle Wandschichten des Myokards erstreckt und häufig mit einem Verlust der ventrikulären Pumpfunktion einhergeht. 0 1h – 4d Neutrophiler Granulozyt (Nph) Monozyt (Mono) Makrophage (Mph) Chemokin für Nph Chemokin für Mono/Mph >4d – 14d Nekrotische Kardiomyozyte Vitale Kardiomyozyte Dedifferenzierte Kardiomyozyte Narbengewerbe Abb. 1 : Schematische Darstellung der Infiltration und Akkumulation von Immunzellen während des kardialen Remodellings nach einem Herzinfarkt. Der Myokardinfarkt ist die Folge einer schlagartig auftretenden und anhaltenden Unterbrechung der herzeigenen Durchblutung (Ischämie), in der Regel bedingt durch einen akuten, arteriosklerotisch-trombotisch induzierten Verschluss der Koronararterien. Beim Herzinfarkt kommt es zu einem ischämiebedingten Untergang (Nekrose) von Herzmuskelzellen (Kardiomyozyten). Die Morphologie des koronaren Versorgungsgebietes, die zeitliche Dauer der Ischä- 16 DZKF 5-2015 TOPTHEMA: KARDIOLOGIE Grundlage der klinisch manifesten Veränderungen des geschädigten Organs sind zahlreiche, komplexe Interaktionen auf genetischer, molekularer und zellulärer Ebene. Der myokardiale Umbau wird als ventrikuläres oder kardiales Remodelling definiert und beschreibt einen evolutionär konservierten Adaptationsmechanismus, um den kardiomyozytären Verlust zu kompensieren und das Ausmaß einer funktionellen Einschränkung möglichst gering zu halten [1]. Der Prozess des kardialen Remodellings ähnelt dabei einer klassischen Wundheilungsreaktion, die durch die Infiltration von zirkulierenden Immunzellen initiiert wird [2]. Initiierung und Koordination von Remodellingprozessen Mechanistisch kommt es infolge einer vermehrten Expression und Sezernierung von pro-inflammatorischen Zytokinen, Chemokinen und Adhäsionsmolekülen zur Transmigration von Leukozyten aus dem Blut durch das Gefäßendothel (E Abb. 1). Immunzellen wandern anschließend entlang eines chemotaktischen Gradienten in das ischämische Myokard, wobei die entsprechenden Chemokine lokal freigesetzt werden [3]. Die Rekrutierung der Immunzellen aus dem Blut in das Infarktareal entspricht einer zeitlich genau determinierten Kinetik und verläuft in verschiedenen KARDIOLOGIE TOPTHEMA CME So sind Ly6C-high Monozyten und daraus entstehende Typ1-Makrophagen maßgeblich an Abbau und Entfernung von nektrotischem Zellmaterial, neutrophiler Granulozyten und der extrazellulären Matrix (EZM) beteiligt, wohingegen Ly6C-low Monozyten/Typ2-Makrophagen den Wiederaufbau der EZM organisieren, indem sie die Proliferation von Fibroblasten und Myofibroblasten sowie die Kollagenbildung und Angiogenese steuern. Es resultiert die Ausreifung eines passageren Granulationsgewebes, das durch eine abklingende Inflammation sowie abnehmende Kapillar- und Myofibroblastendichte gekennzeichnet ist. Eine Quervernetzung von Kollagenfasern sorgt für eine Stabilisierung der Infarktnarbe. Dazwischen kompensieren funktionell überlebende Kardiomyozyten den Verlust der untergegangenen Herzmuskelzellen. Das Ausmaß des kardialen Remodellings ist maßgeblich durch die spatiale Begrenzung der inflammatorischen Antwort, d.h. durch die zeitliche und lokale Präsenz sowie durch die Aktivität von immunmodulatorischen Prozessen determiniert. So belegen Ablationsstudien von Monozyten/Makrophagen einerseits deren pathophysiologische Relevanz für die Wundheilung nach einem Herzinfarkt [5, 6]. Andererseits scheint eine permanent erhöhte Präsenz von Immunzellen die Ausreifung eines stabilen Granulationsgewebes zu stören, woraus eine erhöhte Dilatation und/oder vermehrte Fibrosierung des infarzierten Ventrikels resultiert [7]. Auf Grundlage einer detaillierten pathophysiologischen Kenntnis über diese komplexen humoralen und zellulären Interaktionen, insbesondere durch ein besseres Verständnis von Kontrollmechanismen im Verlauf der kardialen Inflammation, lassen sich innovative molekularbasierte Therapien entwickeln, die bei einem progredienten maladapativen kardialen Remodelling Anwendung finden können. Oncostatin M reguliert die Akkumulation von Makrophagen In früheren Studien des Max-Planck-Instituts für Herzund Lungenforschung wurde Oncostatin M (OSM) als ein wichtiger Modulator des akuten Myokardinfarktremodel- Überlebensrate 100% 80% WT 60% Reg3b–/– + Reg3ß 40% Reg3b–/– 20% 0 10 20 30 Zeit nach Myokardinfarkt (Tage) Makrophagen Zeilen pro mg Infarkt (x103) Stadien oder Wellen. Bereits in den ersten Minuten nach Ischämiebeginn infiltrieren neutrophile Granulozyten das gestresste Myokardareal [4]. Sie phagozytieren tote Myozyten sowie Zelldebris und verdauen das ischämische Myokardareal, indem sie Matrix-Metalloproteinasen (MMPs) und toxische Metabolite sezernieren. Daran schließt sich eine biphasische Monozyten-/Makrophagen-Kinetik, wonach in den ersten Tagen sogenannte proinflammatorische Ly6Chigh Monozyten am Ort der Schädigung dominieren. Zu einer späteren Phase der Wundheilung, d. h. in etwa vier bis sieben Tage nach Eintritt des Infarkts wird dieser Subtyp durch regenerative und reparative Ly6C-low-Monozyten ersetzt [5]. In beiden Fällen gehen mittels Transdifferenzierung Makrophagen mit distinkten Funktionen hervor, die eine zentrale Rolle in der Wundheilung einnehmen. 80 80 Neutrophile Granulozyten * 60 * 20 40 10 20 0 0 WT Reg3b–/– Abb. 2: Die Bedeutung von Reg3b für das Überleben und die Akkumulation von Immunzellen nach Eintritt eines Myokardinfarkts. Die oben aufgeführte Kaplan-Meier-Kurve zeigt die Überlebensraten von Wildtyp-Mäusen (WT, n = 35), Reg3b-defizienten Mäusen (Reg3b–/–, n = 41) und Reg3b–/–-Mäusen, denen zusätzlich rekombinantes Reg3b (n = 38) nach persistenter Ligatur der LAD extern appliziert wurde. Darunter sind absolute Zellzahlen von Makrophagen und neutrophilen Granulozyten pro mg Infarktgewebe in WT und Reg3b–/–-Mäusen (n = 6 für beide Gruppen) abgebildet. Die Quantifizierung dieser Immunzellen basiert auf einer durchflusszytometrischen Analyse (FACS) des Infarkts an Tag 4 nach persistenter Ligatur der LAD. * P < 0.05. lings identifiziert [6]. Bei OSM handelt es sich um ein primär von neutrophilen Granulozyten und proinflammatorischen Typ1-Makrophagen sezerniertes Zytokin der Interleukin-6Klasse. OSM wirkt kardioprotektiv, indem es eine vermehrte Dedifferenzierung von Kardiomyozyten induziert und dadurch die ischämischen Herzmuskelzellen vor dem Untergang schützt. Tierexperimentelle Infarktstudien mit Mäusen, die eine genetische Deletion des korrespondierenden Rezeptors für OSM aufwiesen (Osmr–/–), zeigten zusätzlich, dass OSM die akute inflammatorische Reaktion nach einem Myokardinfarkt reguliert [7]. So war im Infarktbereich bei normalem Gehalt an neutrophilen Granulozyten die Makrophagendichte sowie die Infiltration von monozytären Vorläuferzellen in Osmr–/–-Mäusen deutlich erniedrigt, d. h. die ischämiebedingte leukozytäre Infiltration aus dem Blut in das infarzierte Myokardareal war in einer frühen Phase des kardialen Remodellings negativ beeinträchtigt. Diese abgeschwächte Immunantwort korrelierte mit einer verschlechterten Wundheilung und einer verminderten postischämischen Funktionsleistung. TOPTHEMA: KARDIOLOGIE DZKF 5-2015 17 KARDIOLOGIE TOPTHEMA CME OSM OSM OSM Reg3ß Reg3ß Reg3ß Einlagerung von Kollagenfasern Akkumulierung von Myofibroblasten Ausbildung neuer Gefäße Wundheilung und Formierung einer stabilen Infarktnarbe Neutrophiler Granulozyt Phagozytierende Mph Monozyt Nekrotische Kardiomyozyte Makrophage (Mph) Vitale Kardiomyozyte Abb.3: Modell eines koordinierten kardialen Remodellings durch die OSM-induzierte Produktion von Reg3b. Infolge einer myokardialen Schädigung und des Untergangs von Kardiomyozyten sezernieren infiltrierende Immunzellen das Zytokin OSM. OSM induziert über die Bindung an einen spezifischen OSM-Rezeptor die Dedifferenzierung sowie die Produktion von Reg3b in Kardiomyozyten. Durch die Reg3b-vermittelte Migration von Makrophagen entsteht ein positiver Rückkopplungsmechanismus, der eine zentrale Rolle im Abbau nekrotischer Kardiomyozyten sowie neutrophiler Granulozyten darstellt. Bei einer Hemmung dieser Achse sind nachfolgende Prozesse in der Wundheilung und somit die Ausbildung einer stabilen Infarktnarbe gestört, die letztlich in einer verschlechterten Funktionsleistung und Überlebenschance münden können. Neu identifiziertes Chemokin Reg3b Da OSM allerdings keine chemokinetischen Eigenschaften besitzt, wurde ein weiterer parakrin-sezernierter Faktor vermutet, der bei myokardialer Ischämie durch OSM freigesetzt wird. Zur Identifizierung eines solchen Faktors wurde das Sekretom, definiert als die Gesamtheit aller sezernierten Proteine, von OSM-stimulierten Kardiomyozyten massenspektrometrisch (MALDI-TOF) analysiert. Dabei wurden insgesamt 23 sekretorische, durch OSM differentiell regulierte Proteine, detektiert. Diese Liste beinhaltete allerdings kein bereits bekanntes Chemokin. Demgegenüber wurden zwei Isoformen der Regenerating islet-Derived Proteinfami- 18 DZKF 5-2015 TOPTHEMA: KARDIOLOGIE lie (Reg) identifiziert. In parallel dazu durchgeführten Genexpressionsanalysen von OSM-stimulierten Kardiomyozyten waren ebenfalls mehrere Isoformen der Reg-Familie stark reguliert. Die Untersuchungen wurden dann auf das Familienmitglied Reg3b, von der eine murine und humane Isoform bekannt ist [8], fokussiert. Im gesunden Herzen kommt Reg3b nicht vor. Bei erkrankten Herzen hingegen, wie z. B. bei Patienten mit ischämischer Kardiomyopathie als auch nach einem tierexperimentellem Herzinfarkt, konnte eine vermehrte Expression von Reg3b in dedifferenzierten Kardiomyozyten innerhalb des Infarktbereiches festgestellt werden. In der Osmr–/–-Mutante war nach Myokardinfarkt sowohl die kardiomyozytäre Dedifferenzierung als auch die Expression von Reg3b inhibiert. Diese Ergebnisse ließen vermuten, dass die Aktivierung der OSM/OSMR-Achse eine entscheidende Rolle in der Produktion von Reg3b in Kardiomyozyten einnimmt. Da die Expression von Reg3b im Infarkt mit einer Akkumulation von Makrophagen assoziiert war, wurde ein direkter Effekt von Reg3b auf die Infiltration dieser Immunzellen im ischämischen Herzen postuliert. Funktionelle in vitro und in vivo Analysen ergaben, dass Reg3b die Migration von Makrophagen gezielt fördert, wonach dieses Protein wohl einen entscheidenden Anteil an der verminderten Einwanderung von Makrophagen in Osmr–/–- Mäusen hat. Reg3b-vermittelte Einwanderung von Makrophagen ist entscheidend für Wundheilung und Überleben Die pathophysiologische Relevanz dieser chemokinetischen Eigenschaften von Reg3b wurde letztlich in einem experimentellen Herzinfarktmodell geklärt. Mäuse mit einer genetischen Deletion des Reg3b-Gens (Reg3b–/–) wiesen neben einer verminderten Anzahl an Makrophagen im Bereich des Infarkts eine erhöhte Sterblichkeit auf, infolge einer kardialen Ruptur, die hauptsächlich innerhalb der ersten fünf Tage nach experimenteller Ligatur der linken anterioren deszendierenden Koronararterie (LAD) stattfand (E Abb. 2). Die Rupturen waren durch eine inkomplette Infarktnarbenbildung bedingt, gekennzeichnet durch eine verringerte Anzahl an Myofibroblasten und folglich fehlende Ausreifung der EZM, sowie einer reduzierten Ausbildung neuer Gefäße. Die Ursache einer akuten Herzruptur lag dabei in einer inflammatorischen Dysbalance von Immunzellen (E Abb. 2). Durch das Fehlen von Reg3b als zentralem Chemokin für Makrophagen konnten zugleich neutrophile Granulozyten weitaus weniger mittels Phagozytose entfernt werden, sodass von diesem Zelltyp konsekutiv MMPs freigesetzt wurden. Dies begünstigte eine Instabilität der Infarktnarbe und so die Inzidenz einer Ruptur. Umgekehrt ließ sich die inflammatorische Dysbalance durch eine externe intramyokardiale Applikation von rekombinantem Reg3b in den ischämischen Herzmuskelbereich revertieren, was zugleich mit einem verbesserten klinischen Outcome assoziiert war (E Abb. 2). KARDIOLOGIE TOPTHEMA CME Interaktionen zwischen Kardiomyozyten und Immunzellen Das kardiale Remodelling ist durch den Abbau und die Umstrukturierung des nekrotischen Myokards charakterisiert und wird durch die Infiltration und Aktivität von Immunzellen eingeleitet. Eigene Studienergebnisse belegen, dass die Initiierung und Regulation dieser inflammatorischen Reaktion im Myokard eng miteinander verknüpft sind. In diesem Kontext wird OSM durch die Inflammation lokal vermehrt sezerniert und wirkt als wichtiger Modulator des kardialen Remodellings (E Abb. 3). OSM koordiniert als inflammatorisches Zytokin den Ablauf der Entzündungsreaktion im geschädigten Herzen, indem es aus Kardiomyozyten vermehrt Reg3β freisetzt, das wiederum starke chemokinetische Eigenschaften aufweist. Ist diese Auto-FeedbackSchleife blockiert, resultiert hieraus eine inflammatorische Dysbalance. Dies führt wie im Falle eines Myokardinfarkts zu einer gestörten Makrophagenkinetik mit anhaltendem Gewebeverdau und insuffizienter Ausbildung einer stabilen Infarktnarbe. Die inflammatorische Reaktion verläuft im ischämischen Herzmuskel also nicht autonom, sondern wird durch angrenzende, dedifferenzierte Myokardschichten beeinflusst. Vielmehr noch, die Produktion von Reg3b in vornehmlich dedifferenzierten Kardiomyozyten verdeutlicht, dass Kardiomyozyten eine aktive und zentrale Rolle in der spatialen und temporalen Regulation der inflammatorischen Antwort einnehmen [9]. Im weiteren Verlauf reduzieren dann regenerierende und sich redifferenzierende Kardiomyozyten die Inflammation und steuern somit maßgeblich die myokardiale Gewebshomöostase. Neue Therapieansätze bei Herzerkrankungen Die Identifizierung von OSM und Reg3b, aber auch Kardiomyozyten als zentrale Einflussgrößen der inflammatorischen Antwort und des Heilungsverlaufs ermöglichen neue innovative Therapieansätze, um intrinsische Reparaturvorgänge zu verstärken und das Risiko einer möglichen konsekutiven Herzinsuffizienz zu minimieren [10]. Im Kontext kardiovaskulärer Erkrankungen, wie etwa der Atherosklerose, werden bereits distinkte Chemokine und spezifische Chemokinrezeptorsysteme über den Einsatz antagonistischer Substanzen inhibiert, um die Progression jener Erkrankungen zu minimieren [11]. Umgekehrt sind aber auch Strategien einer zeitlich begrenzten Verstärkung bestimmter Chemokin-Chemokinrezeptor-Signalkaskaden möglich, wie z. B. durch den Einsatz latenter Fusionsproteine [12]. Zusätzlich gilt es, in zukünftigen Studien pharmakologisch-relevante Targetmoleküle zu finden, die insbesondere die Redifferenzierung von Kardiomyozyten fördern. Hierdurch könnten besonders Patienten mit einer chronisch ischämischen Herzerkrankung und eingeschränkter ventrikulärer Funktion profitieren, die einer invasiven Revaskularisationstherapie nur bedingt zugänglich sind. So könnte die Inhibition der kardiomyozytären Dedifferenzierung bei einer persistierenden ischämischen Kardiomyopathie nicht nur die lokale Kon- traktilität steigern, sondern durch Abschwächung der Inflammation das chronische Remodelling zusätzlich abschwächen und dadurch das Ausmaß der ventrikulären Dilatation reduzieren, was sowohl die Prognose als auch die Lebensqualität und die Symptomatik verbessert. Es bestanden keine Interessenkonflikte. LITERATUR 1. Cohn, J.N., R. Ferrari, and N. Sharpe, Cardiac remodeling--concepts and clinical implications: a consensus paper from an international forum on cardiac remodeling. Behalf of an International Forum on Cardiac Remodeling. J Am Coll Cardiol, 2000. 35(3): p. 569–82. 2. Frantz, S., J. Bauersachs, and G. Ertl, Post-infarct remodelling: contribution of wound healing and inflammation. Cardiovasc Res, 2009. 81(3): p. 474–81. 3. Frangogiannis, N.G., Chemokines in the ischemic myocardium: from inflammation to fibrosis. Inflamm Res, 2004. 53(11): p. 585–95. 4. Jung, K., et al., Endoscopic time-lapse imaging of immune cells in infarcted mouse hearts. Circ Res, 2013. 112(6): p. 891–9. 5. Nahrendorf, M., et al., The healing myocardium sequentially mobilizes two monocyte subsets with divergent and complementary functions. J Exp Med, 2007. 204(12): p. 3037–47. 6. Kubin, T., et al., Oncostatin M is a major mediator of cardiomyocyte dedifferentiation and remodeling. Cell Stem Cell, 2011. 9(5): p. 420–32. 7. Lorchner, H., et al., Myocardial healing requires Reg3beta-dependent accumulation of macrophages in the ischemic heart. Nat Med, 2015. 21(4): p. 353–62. 8. Parikh, A., A.F. Stephan, and E.S. Tzanakakis, Regenerating proteins and their expression, regulation and signaling. Biomol Concepts, 2012. 3(1): p. 57–70. 9. Frangogiannis, N.G., The reparative function of cardiomyocytes in the infarcted myocardium. Cell Metab, 2015. 21(6): p. 797–8. 10. Nahrendorf, M., M.J. Pittet, and F.K. Swirski, Monocytes: protagonists of infarct inflammation and repair after myocardial infarction. Circulation, 2010. 121(22): p. 2437–45. 11. Kanzler, I., et al., Anti-inflammatory therapeutic approaches to reduce acute atherosclerotic complications. Curr Pharm Biotechnol, 2012. 13(1): p. 37–45. 12. Mullen, L., et al., Latent cytokines for targeted therapy of inflammatory disorders. Expert Opin Drug Deliv, 2014. 11(1): p. 101–10. AUTOREN Dr. med. Jochen Pöling1,2 Dr. rer. nat. Holger Lörchner1 1 2 Max-Planck-Institut für Herz- und Lungenforschung, Bad Nauheim Schüchtermann-Klinik, Bad Rothenfelde DR. MED. JOCHEN PÖLING Max-Planck-Institut für Herz- und Lungenforschung Abteilung I – Entwicklung und Umbau des Herzens Ludwigstraße 43 61231 Bad Nauheim Tel.: +49 (0)6032/705-1106 Fax: +49 (0)6032/705-1104 Email: [email protected] DR. MED. JOCHEN PÖLING TOPTHEMA: KARDIOLOGIE DZKF 5-2015 19