Extremganzkörperhyperthermie in der Experimentaltherapie der HIV
Werbung

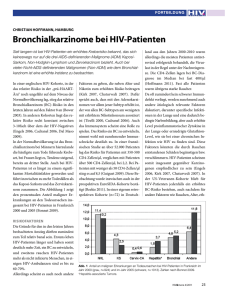
Titelthema: Immunsystem und Viruserkrankungen Extremganzkörperhyperthermie in der Experimentaltherapie der HIV-Infektion A. Suvernev, G. Ivanov, I. Vasilevich, R. Aleinikov, K. Beloborodov, S. Cheresiz, M. Yatvin HI-Virus, das sich aus einer Immunzelle herauslöst Die erste Therapie von Retroviren basierte auf Azidothymidin (AZT), einem chemischen Derivat, das für die Behandlung von AIDS 1987 und asymptomatischer HIV-Infektion 1989 zugelassen wurde. Die Idee, das Konzept der Ganzkörperhyperthermie für die Behandlung von HIV-Infektionen zu nutzen, wurde erstmals im Jahr 1984, auf der 4. Jahrestagung der American Society of Clinical Hyperthermic Oncology, vorgeschlagen [1]; die Veröffentlichung verzögerte sich allerdings, so dass die Ergebnisse erst einige Monate nach Weatherburn [2] im Jahr 1988 veröffentlicht werden konnten [3]. Der Gedanke, Hyperthermie gegen die HIV-Infektion einzusetzen, darf jedoch nicht als Reaktion auf anfängliche Fehlschläge der antiretroviralen Chemotherapie gedeutet werden, sondern als wissenschaftlich fundierter Versuch, sich einer physikalisch-technischen Methode zu bedienen, die in der Onkologie bereits über Jahrzehnte bekannt war. Dieser innovative Ansatz zur Behandlung der Virus-Pandemie war zudem bereits einige Jahre vor Bekanntgabe der enttäuschenden AZT-Studien publik gemacht worden. Da das Kaposi-Sarkom (KS) häufig als sekundäre AIDS-Diagnose gilt, konzentrierten sich die anfänglichen onkologischen Behandlungen von HIV-Patienten auf die AIDS-bezogene Malignität [4]. In mehreren Studien [5] zur Ganzkörperhyperthermie (WBH) bis 42°C und höher konnte keine vollständige Auflösung der Tumore be­ obachtet werden. Jedoch sprachen die Patienten gut auf die WBHBehandlungen an und bei vielen verbesserten sich das virologische Bild und das immunologische Befinden. In weiteren Studien mit verschiedenen Gruppen von HIV-Patienten und unterschiedlichen Behandlungsbedingungen (Warmwasserbad oder extrakorporale WBH-Technologie, Zeit, Temperatur, Zahl der Behandlungen, angewandte Medikationen, Supplemente usw.) wurden zwar grundsätzlich die Sicherheit und Verträglichkeit der Ganzkörperhyperthermie bestätigt, doch waren die therapeutischen Ergebnisse sehr schwankend. In früheren Ausgaben von Die Naturheilkunde [6] berichteten wir bereits über die Ergebnisse der klinischen Studien am Sibirischen Forschungsinstitut für Hyperthermie zur Behandlung von HIV-Patienten mittels der HEATHEAL genannten Methode der Extremganzkörperhyperthermie. Die Ergebnisse sind hier von besonderem Interesse, da sie konsistent eine starke positive Reaktion der gesamten Gruppe belegen, sowohl was Virusmengen und CD4-Werte betrifft, als auch bezüglich des langzeitigen Rückgangs der Erkrankung trotz Abwesenheit von hoch dosierten antiretroviralen Therapien (HAART). Diese Ergebnisse stehen in einem starken Kontrast zu Patientenreaktionen bei eingestellter HAART. Anwendung der Heatheal-Methode bei HIV – Studienergebnisse Um die Auswirkungen der Heatheal-Methode der Extremganzkörperhyperthermie auf die HIV-Infektion untersuchen zu können, wurde auf freiwilliger Basis eine Studiengruppe von 30 HIV-Patienten zusammengestellt. Diese befanden sich in Phase III (latente Infektionsphase, 26 Patienten, 87 %) und Phase IVa (sekundäre opportunistische Infektionsphase, 4 Patienten, 13 %) der Er­ krankung. Jeder Teilnehmer erhielt fünf Wärmebehandlungen bei 24 Die Naturheilkunde 1/2012 42,5 – 43,5°C, drei aufeinanderfolgende Heatheal-Behandlungen im Intervall von 4 – 7 Tagen, eine vierte Behandlung nach zwei ­Monaten und schließlich sechs Monate später die 5. Behandlung. Immunologische und virologische Reaktionen wurden anhand von CD4-Werten (Anzahl der CD4-Lymphozyten pro Mikroliter Blut) und Virenlast (Anzahl der viralen Genome pro Milliliter) bestimmt, die jeweils vor der Studie, nach den ersten 3 Wärmebehandlungen und vor den letzten beiden Behandlungen gemessen wurden. Immunologisch bestand die Studiengruppe aus Patienten ohne ernsthafte Immunschwäche (402 – 765 CD4-Zellen pro Mikroliter), die auf Heatheal positiv ansprachen, wie die allmähliche Wiederherstellung der CD4-Lymphozytenwerte zeigte. Obwohl die Zellwerte nach der Heatheal Behandlung zunächst etwas sanken, kehrten sie am ersten Tag der Nachbehandlung auf den Ursprungswert zurück und stiegen schließlich über eine längere Periode gleichmäßig um 20 % (nach der 3. Behandlung) und 45 % (nach der 4. Behandlung) an. Bei 4 Patienten mit palpablen axillaren Lymphknoten (von etwa 1,5 cm Durchmesser) begannen sich diese nach den ersten 3 Behandlungen zurückzubilden, zwei Monate später waren sie nicht mehr palpabel. Nahezu alle Patienten berichteten über einen verbesserten Gesundheitszustand, größeren Appetit und verminderte Ermüdung. Virologisch betrachtet befanden sich die Patienten vor Studienbeginn in verschiedenen Stufen der Virämie – von mäßig bis stark (8.800 – 1.800.000 virale Genome/ml). In Folge der Heatheal-Behandlungen verringerte sich die Virämie stetig, allerdings schwankte deren Abnahme von Patient zu Patient. Nach drei Wärmebehandlungen war bei über der Hälfte der Patienten (60 %) die Viruslast auf einen zweifach niedrigeren Wert als zu Studienbeginn gesunken, während beim Rest die Virämie um 10 – 40 % reduziert war (Abb. 1A). Zwei Monate darauf, vor der 4. Wärmebehandlung, zeigte die Bestimmung der Virusmenge, dass 90 % der Patienten eine um 90 % reduzierte Virämie aufweisen konnten (Abb. 1B). Dieses Ergebnis deutet auf eine verzögerte Wirkung der Hyperthermie bei HIV-Virämie hin. Bei der letzten Bestimmung der ­Virenlast vor der 5. und abschließenden Wärmebehandlung konnte die ­Virämie – mit der Ausnahme eines einzelnen Patienten – als um 90 – 100 % reduziert gemessen werden (Abb. 1C). Titelthema: Immunsystem und Viruserkrankungen Ausblick Abb. 1A: Reduzierte Virenlast von HIV-infizierten Patienten nach 3 Hyperthermie-Behandlungen Auf Grund des hohen Risikos und der Nebenwirkungen wurden die verschiedenen technischen Ansätze zur Extremganzkörperhyperthermie historisch betrachtet primär als onkologisch-therapeutische Hilfsmittel betrachtet. Gegenwärtig werden verschiedene Verbesserungen bei den unterschiedlichen Versionen der Ganzkörperhyperthermie eingeführt, welche eine relativ sichere Anwendung ermöglichen. Die Heatheal-Technologie der Extremganzkörperhyperthermie ist im Wesentlichen eine Version der von Manfred von Ardenne entwickelten Warmwasserbad-Technik – mit entsprechenden Sicherheitsmodifikationen. Während der letzten Dekade wurden mehr als 3.000 Heatheal-Behandlungen mit minimaler, durch Hyperthermie verursachter, Unverträglichkeit und Neben­ wirkungen durchgeführt, wodurch diese Methode für die experimentelle Behandlung von verschiedenen Erkrankungen inklusive viraler Infektionen (HIV, HCV, Herpes usw.) akzeptabel erscheint. Wie bereits erwähnt, haben die Versuchsreihen, die sich mit der hyperthermischen Therapie von HIV-Infektionen und AIDS beschäftigen, widersprüchliche Resultate erzielt, von einer starken und lang anhaltenden virologischen und immunologischen Reaktion (etwa in der hier dargestellten Studie) bis zu einem nahezu vernachlässigbaren Ergebnis (in anderen Fällen). Zur Weiterentwicklung von reellen multimodalen Ansätzen zur Behandlung von AIDS [7] sind verschiedene Mechanismen, die potenziell verantwortlich sind für die Resultate von WBH bei HIV-Infektion, vorgeschlagen worden. Diese werden aktuell weiter untersucht. Einige der möglichen Mechanismen, die durch Hyperthermie ausgelöst werden, seien im Folgenden angeführt: Abb. 1B: Reduzierte Virenlast von HIV-infizierten Patienten vor Hyperthermie-Behandlung 4 (1) Ganzkörperhyperthermie kann eine Hemmung der Virenproduktion in HIV-infizierten Zellen verursachen [8], die Zahl der latent infizierten HIV-Zellen im Körper kann so entweder beträchtlich reduziert oder gar vollständig eliminiert werden, was etwa durch HAART nicht erreicht werden kann. (2) Die Förderung eines nekrotischen Zelltodes durch Temperaturen von 43 – 44°C kann zur Abgabe von Hitzeschockproteinen (HSP) und HIV-Antigenen in den Kreislauf führen und so die Aufnahme von HSP und viralen Antigenen durch dendritische Zellen (DC) sowie die Ausbreitung zytotoxischer T-Zellen ermöglichen. Es ist erwähnenswert, dass HIV-infizierte T-Zellen auf Wärme empfindlicher reagieren als gesunde T-Zellen [9]. Die infizierten Zellen reagieren durch den Tumor-Nekrose-Faktor (TNF) noch empfindlicher auf eine Erwärmung. Abb. 1C: Reduzierte Virenlast von HIV-infizierten Patienten vor Hyperthermie-Behandlung 5 Jene HIV-Patienten, die antiretroviral nicht reagierten und mittels Heatheal behandelt wurden, können mit den HIV-Non-Progressors (ohne langfristigen Krankheitsfortschritt) verglichen werden, einer kleinen Gruppe von HIV-infizierten Personen, die eine Virämie kontrollieren oder unterdrücken und stabile CD4-Werte aufrechterhalten können sowie für mehr als ein Jahrzehnt nach Serokonversion asymptomatisch bleiben. Einige Patienten unserer Studiengruppe zeigten ebenfalls klinische “Non-Progression” für dieselbe Zeitperiode, was den Vergleich mit „natürlichen“ Non-Progressors noch zutreffender macht. 26 Die Naturheilkunde 1/2012 (3) Das durch Wärme induzierbare 70-kDa Wärmeschockprotein (HSP70) wurde mit dem Schutz der Leukozyten gegen die Zytotoxizität von Entzündungsmediatoren und ihrer verbesserten Überlebensrate bei schweren Infektionen in Verbindung gebracht [10]. Seine Stimulierung und seine schützenden Eigenschaften wurden sowohl in vitro als auch in vivo bei Patienten nachgewiesen, die Ganzkörperhyperthermiebehandlungen bei moderaten Körperinnentemperaturen von 39 – 41°C erhielten. (4) Zellularer Hitze-Schock-Faktor und HIV-Regelung: Die Studie von Rawat & Mitra [11] zeigt, dass Hitze-Schock-Faktor (HSF1) während der HIV-1 Infektion induziert wird und positiv die HIV-1 Genexpression reguliert. Diese Resultate sprechen deutlich für die Extremganzkörperhyperthermie als Therapiemethode für HIV. Titelthema: Immunsystem und Viruserkrankungen (5) RAFT-Lipide & NF-kB Aktivierung: Yan et al. [12] zeigten, dass die Hyperthermie eine schnelle Translokation der IκB Kinase (IKK) und des NF-κB Komplexes in die mit der Plasmamembrane assoziierten RAFT-Lipide in T-Zellen hervorrufen kann. Eine Verdrängung des integralen Membranprotein-Komplexes könnte beträchtlich zu temperaturabhängigen Veränderungen der funktionalen Aktivität von Membran-gebundenen ­Komplexen ­beitragen. Es bedarf weiterer Studien, um der Bedeutung des Vergleichs zwischen der natürlicher Virämie-Hemmung und den durch Hyperthermie induzierten Langzeit-Non-Progressoren gerecht zu werden. Gegenwärtig wird davon ausgegangen, dass in einigen seltene Fällen Patienten imstande sind, ihr antivirales Immunsystem derart zu steuern, dass nur sehr wenige HIV-infizierte CD4-Zellen zirkulieren, während eine starke und dauerhafte Anti-HIV-Reaktion stattfindet (wahrscheinlich gemeinsam mit CD8 zytotoxischen Lymphozyten). Diese Steuerung findet während des Anfangsstadiums der Erkrankung statt, noch vor der Bildung einer großen Zahl von CD4-Zellen, welche die Infektion anheizen [13]. Jene Zellen werden zu Progressoren, welche die Infektion nicht hemmen konnten. Autoren: Prof. Dr. A. Suvernev, Prof. Dr. G. Ivanov, Dr. I. Vasilevich, Dr. R. Aleinikov, Dr. K. Beloborodov, Dr. S. Cheresiz – Siberian Institute of Hyperthermia Prof. Dr. M. Yatvin – Health & Science University, Portland, United States Korrespondierender Autor: Dr. S. Cheresiz, Siberian Institute of Hyperthermia Nagornaya 14a, Iskitim-5 633205 Russia E-Mail: [email protected] Kontakt, Literatur und weitere Informationen: WBH TEC LLC 3705 Winfield Lane, N.W., Washington D.C., 20007, USA Tel.: 001-202-337 6669 Fax: 001-202-337 2823 E-Mail: [email protected] Literatur [1] Yatvin 1987 [2] H. Weatherburn: Hyperthermia and AIDS Treatment, The British Journal of Radiology, vol. 61, No. 729, 1988 [3] Yatvin 1988 [4] Alonso, 1991 und Alonso et al.1992 [5] Steinhart et al. 1996 Mit Kenntnis der mannigfaltigen Auswirkungen der Hyperthermie auf verschiedene Populationen von Immunzellen sowie der Mechanismen, die deren Aktivitäten steuern, kann man die Hypothese aufstellen, dass Ganzkörperhyperthermie die Immunität von Progressor-Patienten auf dieselbe Weise regeln könnte, wie es natürlicherweise in Virämie-Hemmern erfolgt. Im Besonderen kann dies durch selektive Eliminierung der infizierten Zellverbände erreicht werden, die thermolabil erscheinen und die Aktivierung von CD4Zellen stören, während die antivirale Gast-Reaktion durch andere Immunzellenpopulationen und Mechanismen beschleunigt wird. [6] Die Naturheilkunde, 03/2011, Seite 55; Die Naturheilkunde, 06/2011, Seite 38f [7] Yatvin, 1991 [8] Stanley et al., 1990; Iwamoto et al., 1999 [9] Wong et al., 1991 [10] Oehler, 2001 [11] Rawat & Mitra (2011) [12]Yan et al (2008) [13] Saag und Deeks, 2010 Ausführliche Literatur beim Verfasser. Die Naturheilkunde 1/2012 27