Hyperthermie als „targeted“ Therapie
Werbung
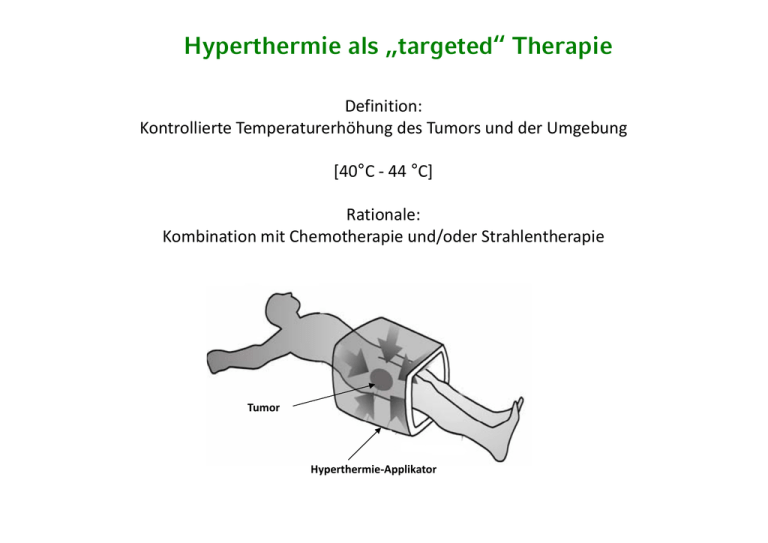
Hyperthermie als „targeted“ Therapie Definition: Kontrollierte Temperaturerhöhung des Tumors und der Umgebung [40°C ‐ 44 °C] Rationale: Kombination mit Chemotherapie und/oder Strahlentherapie Kombination mit Chemotherapie und/oder Strahlentherapie Tumor Hyperthermie‐Applikator Temperatur abhängige Effekte Temperatur‐abhängige Effekte No tumor destruction Clonogenic survival Phenotypic changes Indirect tumor destruction Architectural/vasculature changes Apoptosis Tumor destruction HSPs 37°C 38°C 39°C 40°C 45°C Molecular response Clinical setting Necrosis 41°C 42°C Cell cycle; DNA repair 43°C 44°C Apoptosis / Necrosis Induction of heat shock proteins/HSP-70 membrane expression Thermosensitisation for chemotherapy py and/or radiation Issels, Eur. J. Cancer, 2008 Hyperthermie‐induzierte Hyperthermie induzierte Immuneffekte Immuneffekte 1. Milani and Noessner Cancer Immunol. Immunother. 55:312‐319 (2006) 2. Bendz et al. J. Biol. Chem. 282:31688‐31702 (2007) 3. Bendz H et al. J. Biol. Chem. 283:26477‐ 26483 (2008) 4. Pandya et al. Biol. Chem. 390:305‐312 26483 (2008) 4. Pandya et al. Biol. Chem. 390:305 312 (2009) 5. Milani et al. J. (2009) 5. Milani et al. J. Transpl. Med. 7:50 (2009) Temperatur abhängiger Zelltod 41,5°C 42,5°C 43,5°C 44,5°C 45,5°C Time [min.] Temperatur-abhängiger Zelltod in Kombination mit Chemotherapie 37°C 39°C 42°C ° 41°C Cisplatin Ifosfamide 43°C Cyclophosphamide Time [min.] Thermal Dose Thermal Dose CEM 43°C T90 = Cumulative Equivalent Minutes at 43°C for 90% of Measured Points Surface thermometry Electron field Palpable mass Hyperthermia catheter Eligibility Criteria Eligibility Criteria • Superficial malignancy (≤ 3 cm) depth • Encompassed by applicator (15 x 15 cm area) E db li t (15 15 ) • Expected survival > 6 months p • KPS ≥ 70 • Accessible for thermometry placement • Able to tolerate additional 30 Gy Able to tolerate additional 30 Gy • Metastatic disease allowed Phase‐III‐Study: Duke University Trial (Chest wall Recurrence (2/3), Head/Neck, Melanoma) Therapieprotokoll Brustwandrezidive July 1994 to January 2001 n=122 109 n=109 Test HT n=13 R A N D O M I Z E n=56 n=52 No More HT High HT Low HT Local Control Local Control Clinical Complete Response Rate Clinical Complete Response Rate 100 90 Perce ent Respo onse 80 70 Odds ratio for CR 2.7 (1.2- 5.8) p = 0.02 60 50 40 30 20 10 0 Low High HT Dose Previously Irradiated Patients Previously Irradiated Patients 100 80 60 RT RT + HT 40 20 0 Complete Response 23.5% vs 68.2% Jones et Jones, et.al. al JCO JCO, May 1 1, 2005 Brustwandrezidive Radiatio, HT und Chemotherapie • n=27 • Median 8 Sitzungen, Radiatio 45 gy • 85% vorbestrahlt, 81% Vor‐CTX 85% vorbestrahlt 81% Vor CTX • CR bei 16/20 Pat., • 1‐J. lokal progressionsfrei 76% • CR: Gesamtüberleben 23 Monate • PR: Gesamtüberleben 5,4 Monate PR: Gesamtüberleben 5,4 Monate Zagar, Radiother Oncol 2010 Definition des Zusatzentgelt Hyperthermie § 6 Abs. 2a KHEntgG und Indikationen Entgeltschlüssel: 850 900 63 für teilstationäre Patienten 762 09 001 für stationäre Patienten Regionale Tiefenhyperthermie („regional hyperthermia“; RHT) oder lokale Oberflächenhyperthermie in Kombination mit Chemotherapie und/oder Radiochemotherapie Zeitlich begrenzte Anwendung regionaler Tiefenhyperthermie oder lokaler g g g yp Oberflächenhyperthermie mittels elektromagnetischer Strahlung mit zeitlich abgestimmter systemischer, synergistisch wirksamer Chemotherapie/ g y , y g p / Radiochemotherapie, nach den jeweils aktuellen qualitätssichernden Richtlinien der ESHO (European Society for Hyperthermic Oncology) und der Interdisziplinären Arbeitsgruppe Hyperthermie (IAH) der Deutschen Krebsgesellschaft. Definition des Zusatzentgeltes Hyperthermie Ausschließlich zur Behandlung von Studien‐Patienten Studien Patienten im Rahmen einer ordnungsgemäßen klinischen Prüfung. Die im Rahmen einer ordnungsgemäßen klinischen Prüfung. Die Durchführung und Dokumentation der Therapie erfolgt gemäß eines von einer Ethikkommission genehmigten Prüfplans nach expliziter Aufklärung und Ethikkommission genehmigten Prüfplans nach expliziter Aufklärung und Einwilligung des Patienten. Oder P t k ll P ti t i R h Protokoll‐Patienten im Rahmen einer mit den Kostenträgern abgestimmten i it d K t t ä b ti t Fallserie. Die Durchführung und Dokumentation der Therapie erfolgt nach den Regeln der "Good Clinical Practice" (GCP), dazu gehört auch die Aufklärung und Einwilligung des Patienten. Indikation und Zahl der Hyperthermieanwendungen: 1. Brustwandrezidive (Mammakarzinom) Perkutane Strahlentherapie in Kombination mit regionaler Hyperthermie beim Brustwandrezidiv des Mammakarzinoms (siehe AGO Richtlinie 2012/ Brustwandrezidiv des Mammakarzinoms. (siehe AGO‐Richtlinie 2012/ www.ago‐online.de) Fallserie: RT plus RHT beim Brustwandrezidiv des Mammakarzinoms 10 RHT pro Patientin Behandlung des Brustwandrezidivs (Mammakarzinom) mit p in Kombination mit Hyperthermie yp Strahlentherapie Anmeldung und Anmeldung und Vorstellung der Patientinnen Leitung: Prof. Dr. med. N. Harbeck i f d b k Prof. Dr. C. Belka/OÄ Frau Dr. H. Scheithauer Kompetenzzentrum Hyperthermie der Krankenkassen Klinikum der Universität München Prof. Dr. R. Issels und Dipl.‐Ing. S. Abdel‐Rahman G Gesetzliche Krankenkassen li h K k k











