Wehrhafte Hilfstruppe
Werbung

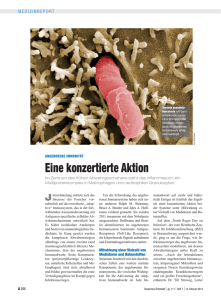
Wissenschaft MEDIZIN Wehrhafte Hilfstruppe Eine junge Disziplin in der Immunologie soll die letzten Geheimnisse des Abwehrsystems lüften. Wissenschaftler hoffen auf passgenaue Waffen gegen Krebs, Aids, Rheuma oder Morbus Crohn. N och verfügt Hochschullehrer Eicke Latz über ein ziemlich spartanisches Büro: Drei Bücher, ein MacBook, ein Telefon – das genügt dem frisch berufenen W3-Professor, um an der Bonner Uni seine Arbeit aufzunehmen. Erst vor ein paar Wochen ist er aus den USA zurückgekommen: Bis vor kurzem forschte er an der University of Massachusetts Medical School. Wenn Latz, 39, und sein Zimmernachbar Veit Hornung, 33, Professor für Klinische Chemie und Pharmakologie, aus ihren Büros treten, stehen sie in einem leeren Flur. Die USA-Heimkehrer sind als erste Wissenschaftler ins nagelneue biomedizinische Forschungszentrum auf dem Bonner Venusberg gezogen; die Kollegen Die Forscher beschäftigen sich mit einer Art Vorhut der Körperabwehr, die eindringende Viren oder Bakterien sofort attackiert. Diese „angeborene“ Immunität galt lange Zeit als primitiver Schutzwall, weit weniger ausgeklügelt als die „erworbene“ oder adaptive Immunität, die darauf beruht, gegen jeden Krankheitserreger eigene maßgeschneiderte Waffen herzustellen und dann die Merkmale jedes bezwungenen Feindes lebenslang im Gedächtnis zu behalten. Wie plump schien dagegen das angeborene Immunsystem, das der Mensch mit Würmern und Seesternen, ja sogar mit Pflanzen und Einzellern teilt. Seine Fressund Killerzellen, so glaubte man, tun nicht Doppelt schützt besser aus komplexer, als jahrzehntelang vermutet wurde. Erst Ende der neunziger Jahre fanden Wissenschaftler heraus, dass die Zellen der angeborenen Abwehr ihre Feinde mittels einer Reihe von Oberflächenproteinen, den Rezeptoren, erkennen. Wie Schlüssel und Schloss fügen sich Rezeptor und Fremdstoff ineinander – für die Zellen ein Startsignal, das beispielsweise eine Entzündung in Gang setzen kann. Vom adaptiven Immunsystem war dieses Prinzip längst bekannt: Auch dessen T-Zellen haben spezifische Rezeptoren, die Viren oder Bakterien erkennen; die B-Zellen wiederum bilden passgenaue Antikörper, die sich an ihren jeweiligen Widersacher heften und ihn unschädlich machen. Erst seit kurzem jedoch weiß man, dass die T- und B-Zellen gar nicht selbst die Entscheidung treffen, ob sie Freund oder Feind vor sich haben. Erst das angeborene Immunsystem macht sie auf Gefahren aufmerksam und hat damit eine Steuerungsfunktion für die adaptive Verteidigungslinie. „Die Entdeckung der ersten Rezeptoren des angeborenen Immunsystems war eine Revolution“, urteilt der Immunologe Luke O’Neill vom Trinity-College in Dub- Die zwei Abteilungen des Immunsystems Erreger TLR und andere Rezeptoren Antikörper Botenstoffe Fresszellen B-Zellen infizierte Körperzelle T-Zellen OLIVER TJADEN Blutgefäß Das angeborene Das angeborene Immunsystem gehört zur Grundausstattung ausstattung fast fast aller aller Organismen. Organismen. Seine Seine Zellen Zellen erkennen und attackieren mittels verblüffend spezifischer Rezeptoren eindringende Fremdstoffe und lösen akute Entzündungsreaktionen oder Fieber aus. Zudem versetzen sie das adaptive Immunsystem system in in Alarmbereitschaft. Alarmbereitschaft. Das adaptive Immunsystem reift erst im Laufe des Lebens heran. Nach einem ersten Kontakt produziert es passgenaue Antikörper für jeden Fremdstoff, die es bei einem weiteren Kontakt sofort aktivieren kann – meist verläuft die Infektion dann unbemerkt. So funktionieren auch Impfungen. Forscher Hornung, Latz: Die Verheißungen klingen fast zu schön, um wahr zu sein kommen erst noch. In den Labors stapeln sich Pappkartons voller Pipetten und Gummihandschuhe; Mikroskope, Chromatografen und Zentrifugen stehen unausgepackt herum. Latz und Hornung sind es gewohnt, die Ersten zu sein. Sie gehören zu den jüngsten Professoren an der Bonner Uni, Latz leitet das deutschlandweit erste „Institut für die Erforschung des angeborenen Immunsystems“, Hornung hat gerade ein begehrtes Stipendium des Europäischen Forschungsrats eingeworben. Vor allem aber ist es ihr Fachgebiet selbst, das reichlich Gelegenheit bietet für Pionierleistungen: Die beiden Mediziner sind Experten für das derzeit wohl heißeste Thema der Immunologie. 152 viel mehr, als mit ihren Mini-Tentakeln feindliche Mikroben zu ergreifen, herunterzuschlingen und daraufhin molekulare Alarmrufe in die Blutbahn zu schwemmen – alles nur, so glaubte man, um der adaptiven Verteidigungsarmee Zeit für den eigentlichen Angriff zu verschaffen. „Das angeborene Immunsystem schien so trivial, dass man es lange einfach übersehen hat“, erklärt Forscher Hornung. Erst seit wenigen Jahren ist klar: Ohne die Zellen des verkannten Systems findet überhaupt keine Immunantwort statt – seine Botenstoffe bringen die sogenannten B- und T-Zellen des erworbenen Immunsystems erst in Schwung. Und: Die vermeintlich tumbe Aushilfstruppe ist weitd e r s p i e g e l 4 9 / 2 0 0 9 lin, „der Forschungszweig ist geradezu explodiert.“ Inzwischen haben die Wissenschaftler festgestellt, dass das Arsenal angeborener Waffen verblüffend vielfältig ist. Rund hundert Rezeptoren haben sie entdeckt; manche davon erkennen charakteristische Sequenzen in der Erbsubstanz von Viren oder Bakterien, andere sind Spezialisten für Proteine, mit denen sich Invasoren als Fremdstoffe verraten. Wieder andere schlagen Alarm, wenn sie typische Merkmale von Parasiten oder Pilzen entdecken. „Wir wissen jetzt viel mehr über die frühesten molekularen Ereignisse, die eine Immunreaktion auslösen“, erklärt Bruce Beutler, Leiter der Abteilung für Genetik ULLSTEIN / REUTERS am Scripps-Forschungsinstitut im kalifornischen La Jolla, „das hat viele Türen geöffnet.“ Beutler ist ein Mann der ersten Stunde: Vor gut zehn Jahren hat er die Funktion des ersten Rezeptors im angeborenen Immunsystem von Säugetieren aufgedeckt: den sogenannten Toll-like Rezeptor 4 (TLR4), der auf Bakteriengifte reagiert. Inzwischen sind beim Menschen elf verschiedene TLR-Varianten identifiziert worden, sie gelten als die wichtigsten Erkennungsstrukturen des angeborenen Immunsystems. Viele TLRs hat Beutlers Kollege Shizuo Akira von der Universität Osaka beschrieben: Das macht den Japaner in der Fachpresse seit Jahren zum meistzitierten Wissenschaftler der Welt – und zugleich, zusammen mit Beutler und ihrem Straßburger Kollegen Jules Hoffmann, zum heißen Kandidaten für den Medizin-Nobelpreis. Die große Hoffnung der Zunft liegt darin, den frühesten Ursprung jeder Immunreaktion zu beeinflussen und sie je nach Bedarf entweder anzustacheln oder einzudämmen. Damit, glauben die Immunologen, hielten sie womöglich Waffen gegen fast jede beliebige Krankheit in Händen: Malariapatienten: Ganz neue Impfstoffe? • Durch Stimulation des angeborenen Immunsystems könnte die körpereigene Abwehr dazu gebracht werden, Krebszellen zu vernichten. Erste Medikamente, die nach diesem Prinzip funktionieren sollen, sind bereits in der Testphase. So will der Pharma-Riese Merck Krebsmedikamente auf TLR-Basis entwickeln. 28 Millionen Euro zahlte der Konzern der US-Firma Idera Pharmaceuticals für entsprechende Lizenzen. • Auch bei der Entwicklung von Impfstoffen spielt das neue Wissen über die angeborene Immunität eine wichtige Rolle. Erst seit kurzem wissen die Pharmakologen, dass die sogenannten Adjuvantien, die Impfstoffe wie etwa die d e r aktuelle Schweinegrippe-Vakzine in ihrer Wirkung verstärken, vor allem das angeborene Immunsystem anschubsen. Mit dem richtigen Zusatzstoff, so die Vision, werden von vielen Schutzimpfungen geringere Dosen und kaum noch Auffrischungen nötig sein. Womöglich lassen sich sogar ganz neue Rezepturen entwickeln, etwa zum Schutz vor Tuberkulose, Malaria oder Aids. • Umgekehrt könnte die Blockade bestimmter TLR-Moleküle und anderer Rezeptoren das Immunsystem bei jenen Krankheiten herunterregeln, bei denen es aus dem Ruder läuft. Insbesondere gilt dies für verheerende Entzündungsreaktionen wie die Sepsis. • Auch Krankheiten, bei denen Immunzellen körpereigenes Gewebe zerstören, sind ins Visier der Forscher gerückt: etwa Rheumatoide Arthritis, Diabetes, Morbus Crohn oder Multiple Sklerose. Immunologe O’Neill hat selbst eine Firma gegründet: Opsona Therapeutics will einen TLR-Blocker auf den Markt bringen, der Entzündungen zum Beispiel nach einem Herzinfarkt eindämmen könnte. „Auf dem Gebiet herrscht Goldgräberstimmung“, sagt Gunther Hartmann, Leiter des Instituts für Klinische Chemie und Pharmakologie in Bonn. Hartmann setzt vor allem auf die Entwicklung neuer Krebstherapien, sein Kollege Hornung interessiert sich für Rezeptoren, die Viren erkennen können. Wissenschaftler Latz wiederum erforscht ein Molekül namens „Nod-like Rezeptor“, das offenbar eine Schlüsselrolle bei Leiden wie Gicht, Arteriosklerose oder Alzheimer spielt. Bessere Impfstoffe, Heilung für alle – die Verheißungen der Trenddisziplin klingen fast zu schön, um wahr zu sein. Der Berliner Rheumatologe Andreas Radbruch, Präsident der Deutschen Gesellschaft für Immunologie, warnt denn auch vor übertriebenen Erwartungen: „Mit dem angeborenen Immunsystem ist es wie mit einem neuen Spielzeug – alle stürzen sich darauf.“ Noch aber wisse niemand genau, was geschieht, wenn man an einzelnen Stellen in das System eingreift: „Gerade weil es so wichtig ist, sind die Nebenwirkungen gezielter Eingriffe schwer vorhersehbar.“ Deutlich zeigt sich dies derzeit zum Beispiel bei der Grippeimpfung. „Unser Bild vom angeborenen Immunsystem ist noch lange nicht komplett“, räumt auch TLR-Papst Beutler ein, „wir müssen alle Moleküle kennen, die bei seiner Funktion eine Rolle spielen.“ Für Beutlers Kollegen Ruslan Medzhitov, Immunologe an der US-Universität Yale, ist das aber nur noch eine Frage der Zeit: „Unser Forschungsgebiet wächst immer noch exponentiell“, sagt er, „wir entdecken praktisch jede Woche etwas Neues.“ s p i e g e l Julia Koch 4 9 / 2 0 0 9 153