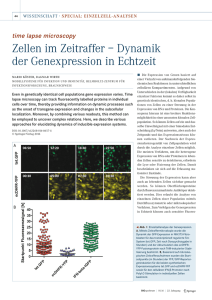
Die Expression des Visinin-like-Protein
Werbung

1 Aus dem Johannes-Müller-Institut für Physiologie der Medizinischen Fakultät Charité – Universitätsmedizin Berlin DISSERTATION Die Expression des Visinin-like-Protein-1 in humanen Geweben und Tumoren sowie seine Korrelation mit klinisch-pathologischen Daten im Plattenepithelkarzinom des Ösophagus zur Erlangung des akademischen Grades Doctor medicinae (Dr. med.) vorgelegt der Medizinischen Fakultät Charité – Universitätsmedizin Berlin von Carla Wickborn aus Magdeburg 2 Gutachter: 1. Prof. Dr. rer. nat. K.-H. Braunewell 2. Prof. Dr. rer. nat. R. Schäfer 3. Prof. Dr. E. Gundelfinger Datum der Promotion: 29.09.2009 3 Meinen lieben Eltern Heidemarie und Volker Wickborn gewidmet 4 Inhaltsverzeichnis 1. Einleitung ............................................................................................................................. 7 1.1. Das Ösophaguskarzinom ....................................................................................................... 7 1.1.1. Epidemiologie des Ösophaguskarzinoms.................................................................... 7 1.1.2. Diagnose und Stadieneinteilung .................................................................................. 9 1.1.3. Pathogenese ............................................................................................................... 12 1.1.4. Risikofaktoren ........................................................................................................... 12 1.1.5. Therapie und Prognose .............................................................................................. 13 2. Molekulare Grundlagen ................................................................................................... 15 2.1. Einflussfaktoren bei der Genese des Ösophaguskarzinoms ................................................ 15 2.2. Kalzium und Kalziumbindungsproteine.............................................................................. 16 2.2.1. Annexine ................................................................................................................... 17 2.2.2. S100-Proteine ............................................................................................................ 17 2.2.3. Neuronale Kalzium-Sensor-Proteine......................................................................... 17 2.3. VILIP-1 ............................................................................................................................... 20 2.4. Ki-67.................................................................................................................................... 20 3. Fragestellung...................................................................................................................... 21 4. Material und Methoden .................................................................................................... 22 4.1. Patienten .............................................................................................................................. 22 4.2. Gewebe ................................................................................................................................ 23 4.3. Antikörper und Reagenzien ................................................................................................. 24 4.3.1. VILIP-1 ..................................................................................................................... 25 4.3.2. Ki-67.......................................................................................................................... 26 4.3.3. 4’, 6-Diamidino-2-phenylindol (C16H15N5.2HCl) ..................................................... 26 4.4. Methoden ............................................................................................................................. 26 4.4.1. Immunhistochemie .................................................................................................... 26 4.4.1.1. Deparaffinisierung, Rehydrierung und Epitopdemaskierung ................................ 27 4.4.1.2. Avidin-Biotinyl-Peroxidase-Komplex-Methode ................................................... 27 5 4.4.2. Immunfluoreszenzfärbung ........................................................................................ 29 4.4.3. Quantifizierung der VILIP-1-Expression .................................................................. 30 4.4.4. Statistische Analysen................................................................................................. 31 5. Ergebnisse .......................................................................................................................... 32 5.1. Immunhistochemie von VILIP-1 in einer Auswahl verschiedener humaner Normalgewebe und Tumore ....................................................................................................................... 32 5.2. Immunhistochemie von VILIP-1 im Normalgewebe und im Plattenepithelkarzinom des Ösophagus ......................................................................................................................... 35 5.3. Immunfluoreszenzfärbung von VILIP-1 im Normalgewebe des Ösophagus ..................... 37 5.4. Immunfluoreszenzfärbung von VILIP-1 im Plattenepithelkarzinom des Ösophagus ........ 39 5.5. Vergleich der VILIP-1-Expression zwischen Normal- und Tumorgewebe des Ösophagus ......40 5.6. VILIP-1 und das Lebensalter .............................................................................................. 40 5.7. VILIP-1 und das Geschlecht ............................................................................................... 40 5.8. VILIP-1 und die Tumorgröße ............................................................................................. 41 5.9. VILIP-1 und der Nodalstatus .............................................................................................. 43 5.10. VILIP-1 und die Differenzierung ...................................................................................... 45 5.11. Immunfluoreszenzfärbung von Ki-67 im Normalgewebe und im Plattenepithelkarzinom des Ösophagus ................................................................................................................... 46 5.12. Vergleich der Ki-67-Expression zwischen Normal- und Tumorgewebe des Ösophagus. 46 5.13. Ki-67 und klinisch-pathologische Charakteristika ............................................................ 47 5.14. Immunfluoreszenz-Doppelfärbung der VILIP-1- und Ki-67-Expression ......................... 49 6. Diskussion .......................................................................................................................... 51 6.1. VILIP-1 im ösophagealen Normalgewebe .......................................................................... 52 6.2. VILIP-1 im ösophagealen Plattenepithelkarzinom ............................................................. 52 6.2.1. VILIP-1 und klinisch-pathologische Charakteristika ................................................ 53 6.2.2. VILIP-1 im Vergleich zu anderen Kalziumbindungsproteinen ................................ 54 6 6.2.2.1. VILIP-1 und die Kalziumbindungsproteine der Annexin-Familie ........................ 55 6.2.2.2. VILIP-1 und die S100-Kalziumbindungsproteine ................................................. 57 6.2.3. VILIP-1 und die Regulation der Genexpression und Signaltransduktion ................. 58 6.2.4. VILIP-1 und die Proliferation ................................................................................... 61 6.2.5. VILIP-1 und die Differenzierung .............................................................................. 63 6.3. Die Rolle von Ki-67 im ösophagealen Gewebe .................................................................. 63 6.4. Das Verhalten von VILIP-1 in einer Auswahl weiterer Karzinome ................................... 64 6.5. Kritische Beurteilung der Ergebnisse .................................................................................. 66 7. Schlussfolgerung ................................................................................................................ 67 8. Zusammenfassung ............................................................................................................. 69 9. Literaturverzeichnis .......................................................................................................... 71 Abkürzungsverzeichnis ............................................................................................................... 84 Erklärung ..................................................................................................................................... 85 Lebenslauf .................................................................................................................................... 86 Danksagung.................................................................................................................................. 88 7 1. 1.1. Einleitung Das Ösophaguskarzinom Das Ösophaguskarzinom ist einer der aggressivsten Tumore des Verdauungstrakts. Weltweit steht es an achter Stelle aller diagnostizierten Tumortypen und es ist der sechsthäufigste Tumor der weltweit zum Tode führt1. Trotz Fortschritten in der Chirurgie und dem Anwenden multimodaler Therapiekonzepte ist die Überlebensrate der Patienten nicht wesentlich verbessert worden. Bei mehr als 90% der Patienten mit Ösophaguskarzinom wird der Tumor erst in einem fortgeschrittenen Stadium entdeckt2. Folglich haben diese Patienten im Allgemeinen die schlechteste Prognose unter jenen mit gastrointestinalen Tumoren3,4. Unter den bösartigen ösophagealen Tumoren sind die häufigsten das Plattenepithelkarzinom und das Adenokarzinom. Zu den seltenen Tumortypen zählen die ösophagealen Sarkome. 1.1.1. Epidemiologie des Ösophaguskarzinoms In der Bundesrepublik Deutschland erkranken jährlich etwa 3.370 Männer und 880 Frauen am Ösophaguskarzinom. Dies entspricht einem Anteil von weniger als 2% aller bösartigen Neubildungen bei Männern und 0,5% bei Frauen. Der Anteil an den Krebssterbefällen ist mit 2,9% bei den Männern und 0,9% bei den Frauen höher (Robert Koch Institut, Schätzung für Deutschland 2000). Deutsche Männer erkranken circa viermal bis fünfmal häufiger und im Mittel 7 Jahre früher als deutsche Frauen. Das mittlere Erkrankungsalter der Männer liegt bei 63 und das der Frauen bei 70 Jahren. Die in der Tabelle 1 dargestellte Inzidenz wird auf die Altersstruktur der europäischen Standardbevölkerung bezogen und die dargestellten Zahlen stützen sich auf Angaben der amtlichen Todesursachenstatistik der alten Länder der Bundesrepublik bis 1990 und ab 1990 für Deutschland insgesamt. Die jährliche altersstandardisierte Inzidenz beträgt in der Bundesrepublik Deutschland 2000 bei Männern 8,4 und bei Frauen 2,1 pro 100.000 Personen. Bei Männern liegt die Mortalität insgesamt bei 7,9 und bei Frauen bei 2,2 pro 100.000 Personen. Innerhalb Europas liegt Deutschland mit diesen Werten für das ösophageale Karzinom im mittleren Bereich. Aufgrund der ungünstigen Prognose des Ösophaguskarzinoms sind die Erkrankungsraten und Sterberaten nahezu identisch (Tabelle 1). Zwischen den einzelnen Ländern und Regionen innerhalb eines Landes zeichnen sich im europäischen Vergleich deutliche Unterschiede ab. Die niedrigste Inzidenz findet sich mit 1,4 8 pro 100.000 in Griechenland, währenddessen in England mit 9,4 pro 100.000 die höchste Inzidenz zu finden ist. Ein Hochrisikogebiet innerhalb Europas findet sich in der französischen Bretagne und Normandie (Calvados-Region), wo die Inzidenzraten für das ösophageale Karzinom mehr als zweimal so hoch sind wie im Rest Europas5. Auch weltweit ist die Häufigkeit der ösophagealen Karzinome regional sehr verschieden. Die weltweite Inzidenz der Plattenepithelkarzinome liegt zwischen 2,5 und 5,0 pro 100.000 Personen für Männer sowie 1,5 und 2,5 pro 100.000 Personen für Frauen6. Zu den bekannten HochRisiko-Regionen gehören die Provinzen Linxian, Henan, Shanxi und Sichuan in Nordchina7, Nord-Iran, die Nord- und Ostküste des Kaspischen Meeres und die Transkei-Region in Südafrika8. Die Inzidenz für China insgesamt hat zwischen 1993 und 1997 bei 11,7 pro 100.000 für Männer und 2,5 pro 100.000 für Frauen gelegen. Im Gegensatz dazu sind es im gleichen Zeitraum in den Vereinigten Staaten nur 5,1 pro 100.000 bei Männern und 1,4 pro 100.000 bei Frauen gewesen (Surveillance and Risk Assessment Division, CCDP, Health Canada). Ebenso sind die Mortalitätsraten regional sehr verschieden. In China liegt die Mortalitätsrate für Männer bei 15,8 und für Frauen bei 7,9 pro 100.000 Einwohner. Im Gegensatz dazu ist die Mortalitätsrate in Nordamerika für Männer bei 5,9 und für Frauen bei 2,0 pro 100.000 Einwohner weitaus niedriger9. Ursachen für die deutlichen geographischen Differenzen sind wahrscheinlich spezifische Umweltfaktoren, Ernährungsgewohnheiten10 sowie Diagnostik- und Therapiemodalitäten. Unter den Ösophagustumoren hat lange Zeit das Plattenepithelkarzinom dominiert. Dies hat sich in den letzten zwei Jahrzehnten gewandelt. Während die Inzidenz des Plattenepithelkarzinoms stabil geblieben ist beziehungsweise abgenommen hat, ist die Inzidenz des Adenokarzinoms angestiegen11,12. Es ist beobachtet worden, dass in der dunkelhäutigen und asiatischen Bevölkerung weiterhin vor allem Plattenepithelkarzinome auftreten, während in der weißen, männlichen Bevölkerung in Nordamerika und Westeuropa die Adenokarzinome stark zunehmen13,14,15. Bei mehr als 80% der an einem ösophagealen Plattenepithelkarzinom Erkrankten handelt es sich um dunkelhäutige Männer, während mehr als 50% der Patienten mit Adenokarzinomen weiße Männer sind5. Nichtsdestotrotz befindet sich das Plattenepithelkarzinom des Ösophagus unter den 10 am häufigsten diagnostizierten Tumoren der Welt16. 9 Alter in Jahren Männer Frauen Inzidenz Mortalität Inzidenz Mortalität < 45 0,4 0,4 0,0 0,1 45 bis < 60 14,7 11,9 2,5 2,0 60 bis < 75 27,9 26,2 5,1 4,8 75 und älter 22,3 30,4 7,7 10,4 insgesamt 8,4 7,9 2,1 2,2 Tab. 1: Inzidenz und Mortalität pro 100.000 nach Altersgruppen in Deutschland. 1.1.2. Diagnose und Stadieneinteilung Die klinische Symptomatik macht sich im Regelfall erst spät bemerkbar. Erstsymptome können progressive Dysphagie, Brustschmerzen, Gewichtsverlust, Fieber bei ösophago-trachealer Fistelbildung oder Heiserkeit bei Rekurrensparese sein. Da eine Dysphagie meist erst auftritt, wenn 2/3 des Ösophaguslumens durch Tumorgewebe verlegt sind beziehungsweise das Restlumen bereits weniger als 1cm misst, wird bei mehr als 90% der Patienten mit Ösophaguskarzinom der Tumor erst in einem fortgeschrittenem Stadium entdeckt2. Dies erklärt teilweise warum diese Patienten im Allgemeinen die schlechteste Prognose unter jenen mit gastrointestinalen Tumoren haben3,4. Die Beurteilung des Erkrankungsstadiums erfolgt anhand von drei Kriterien: Größe und Ausdehnung des Primärtumors (T), Tumorbefall regionaler Lymphknoten (N) und dem Nachweis von Metastasen (M), welche durch das Hinzufügen von Ziffern (0-4) gewichtet werden. Nach der postoperativen histopathologischen Evaluation wird die Stadieneinteilung durch ein p (postoperativ) zusätzlich gekennzeichnet (pTNM). Außerdem erfolgt eine pathologische Einschätzung des Differenzierungsgrades (G). Je undifferenzierter ein Tumor ist, desto größer sind seine Wachstumsgeschwindigkeit, seine Strahlenempfindlichkeit und seine Malignität. Auf diesen Kriterien basierend kann das Erkrankungsstadium und der Behandlungserfolg international standardisiert werden (Abbildung 1 und Tabelle 2). Für die Stadieneinteilung nach UICC (Union International Contre le Cancer, Abbildung 1) und AJCC (American Joint Commission for Classification of Cancer, Tabelle 2)17,18 sowie für die Therapieplanung sind weiterhin bedeutend: die (suprabifurkal/infrabifurkal), Bestimmung der des histologischen Differenzierungsgrad, die Typs, die Infiltrationstiefe Lokalisation und das 10 19 Metastasierungsmuster . Die klinische Stadieneinteilung der AJCC beruht sowohl auf dem TNM-Stadium der UICC, auf der klinischen Prognose als auch auf praktischen chirurgischen Aspekten, wie unter anderem der Resezierbarkeit. Die Entscheidung einer makroskopisch und mikroskopisch gelungenen Exzision im Gesunden (R0) ist dabei ein wichtiger prognostischer Faktor20,21. Stadium TNM- Klassifikationen 0 Tis N0 M0 I T1 N0 M0 II A T2 N0 M0 T3 N0 M0 T1 N1 M0 T2 N1 M0 T3 N1 M0 T4 jedes N M0 IV jedes T jedes N M1 IV A jedes T jedes N M1a IV B jedes T jedes N M1b II B III Tab. 2: Stadieneinteilung des Ösophaguskarzinoms der American Joint Commission for Classification of Cancer (AJCC). 11 Primärtumor (T-Stadium) Tx Primärtumor nicht beurteilbar T0 kein Hinweis auf Primärtumor Tis Carcinoma in situ T1 Tumor infiltriert Lamina propria oder Submukosa T2 Tumor infiltriert Muscularis propria T3 Tumor infiltriert Adventitia T4 Tumor infiltriert benachbarte Organe (Tracheobronchialsystem, Gefäße, Nerven) Regionale Lymphknoten (N-Stadium) Nx regionale Lymphknoten nicht beurteilbar N0 keine lokoregionären Lymphknotenmetastasen N1 Nachweis regionalen Lymphknotenbefalls Fernmetastasen (M-Stadium) Mx Beurteilung des Vorhandenseins von Fernmetastasen nicht möglich M0 kein Nachweis von Fernmetastasen M1 Vorhandensein von Fernmetastasen Tumore des unteren thorakalen Ösophagus (distaler Anteil des Ösophagus, zwischen 32 und 40 cm distal der oberen Schneidezähne) M1a Befall der zöliakalen Lymphknoten M1b andere Fernmetastasen Tumore des mittleren thorakalen Ösophagus (von Trachealbifurkation bis oberhalb des ösophagogastralen Übergangs, etwa 32 cm ab Zahnlinie) M1a nicht anwendbar M1b Befall nicht-regionaler Lymphknoten oder andere Fernmetastasen (viszerale Metastasen) Tumore des oberen thorakalen Ösophagus (ab obere Thoraxapertur bis Trachealbifurkation, circa 18 bis 24 cm ab Zahnlinie) M1a Befall der zervikalen Lymphknoten M1b Befall nicht regionaler Lymphknoten oder andere Fernmetastasen Abb. 1: Stadieneinteilung der Union International Contre le Cancer (UICC). 12 1.1.3. Pathogenese Tumore des Ösophagus gehen überwiegend vom Plattenepithel und in geringem Maße von den mukösen Ösophagealdrüsen, von Magenschleimhautheterotopien oder vom metaplastischen Zylinderepithel des Barrett-Ösophagus und selten auch von den APUD-Zellen (amine precursor uptake and decarboxylation) aus. Zu den epithelialen Tumoren gehören Plattenepithelkarzinome (80-90%) und Adenokarzinome (10-20%), welche sowohl epidemiologische als auch ätiologische Unterschiede aufweisen. Insgesamt gehören ungefähr 95% der ösophagealen Tumore zu den Plattenepithel- und Adenokarzinomen6. Die Plattenepithelkarzinome der Speiseröhre sind größtenteils im mittleren und unteren Drittel des Ösophagus lokalisiert. Nur 1015% finden sich im oberen Drittel. Im Vergleich dazu sind die Adenokarzinome vor allem im unteren Drittel in der Nähe des Mageneingangs lokalisiert22. Da dem Ösophagus eine Serosa als anatomische Barriere fehlt, kann sich der Tumor rasch über die Submukosa, die innere zirkuläre und äußere longitudinale Muskulatur ausbreiten und Nachbarorgane wie die Trachea infiltrieren. Dadurch kommt es zu Komplikationen wie beispielsweise ösophagotrachealen Fisteln. Durch die kontinuierliche oder diskontinuierliche Ausbreitung (skip lesions) entlang von Lymphspalten der Ösophaguswand und Ösophaguskarzinome die folglich schnell sehr gute lymphogen. lymphatische Charakteristisch Drainage, ist eine metastasieren lymphogene Schleimhautmetastasierung und eine intramurale, submuköse Tumorausdehnung, vor allem nach proximal23. Fernmetastasen finden sich bei proximalen Tumoren besonders in der Lunge (venöser Abfluss über Venae thyroideae, Vena azygos oder Vena hemiazygos in die obere Vena cava) und bei distalen Tumoren in der Leber (venöser Abfluss über Vena coronaria ventriculi in die Pfortader)24. 1.1.4. Risikofaktoren Als exogene Risikofaktoren für das ösophageale Plattenepithelkarzinom gelten in Nordamerika und Europa insbesondere Alkohol und Tabak25,26,27. Werden sowohl Alkohol als auch Tabak konsumiert, so erhöhen beide das Risiko synergistisch28. Plattenepithelkarzinome treten vorwiegend in Regionen mit niedrigem sozioökonomischen Status und Mangelernährung (Vitaminmangel) auf. Bei Adenokarzinomen hingegen zeigt sich eine Häufung in wohlhabenden Ländern mit besonders ballaststoffarmer und fetthaltiger (gesättigte Fettsäuren) Ernährung5. 13 Im Gegensatz zum Plattenepithelkarzinom werden als Risikofaktoren für das ösophageale Adenokarzinom vor allem der gastroösophageale Reflux und das Übergewicht gesehen14. Chronische Entzündungen im Rahmen eines gastrointestinalen Refluxes führen zur Entstehung einer intestinalen Metaplasie (Barrett-Ösophagus) und begünstigen damit vor allem die Genese eines Adenokarzinoms15,29. Außerdem bedeutsam sind verschiedenste Arten der Irritation der Schleimhaut wie zum Beispiel heiße Flüssigkeiten, Obstschnäpse (Nitrosamine), Strikturen durch Bestrahlung oder Laugeningestion30,31,32, der Kontakt mit Karzinogenen wie Nitriten, Schimmelpilzgiften (Aflatoxine) oder unausgewogene Ernährung (Zink-33, Vitamin A- sowie Folsäuremangel). Die tägliche Einnahme einer bestimmten Menge Vitamin C (>100mg/d) und Vitamin E (>13mg/d) kann im Gegensatz dazu das Risiko für ösophageale Plattenepithelkarzinome und Adenokarzinome signifikant senken34. Als endogene Faktoren gelten beispielsweise die familiäre palmoplantare Keratose (Tylosis), bei der aufgrund eines autosomal-dominant vererbten Gendefekts Hyperkeratosen an Hand- und Fußflächen und Papillome des Ösophagus bestehen35,36, sowie die glutensensitive Enteropathie (Zöliakie) mit Maldigestion und Malabsorption aufgrund gluteninduzierter Zottenatrophie der Dünndarmschleimhaut37. 1.1.5. Therapie und Prognose Die kurative Therapie ist in erster Linie eine chirurgische Therapie. Abhängig von Tumorlokalisation, Tumorausdehnung und individuellen Patientenmerkmalen sind allerdings nur etwa 50-60% aller Ösophaguskarzinome prognostisch sinnvoll operabel. Die chirurgische Therapie kann mit Chemotherapie und/oder Radiotherapie präoperativ (neoadjuvant) oder postoperativ (adjuvant) kombiniert werden. Eine R0-Resektion ist dabei die wesentliche Voraussetzung für einen kurativen Behandlungserfolg. Da die Ösophaguskarzinome allerdings oftmals submukös entlang der Lymphbahnen wachsen und aufgrund der fehlenden Serosa frühzeitig benachbarte Strukturen infiltrieren, können sie häufig nicht R0 reseziert werden und sind demnach für eine kurative chirurgische Therapie zu weit fortgeschritten. Mehr als 50% der Patienten mit einem ösophagealen Karzinom müssen palliativ behandelt werden, da entweder bereits Fernmetastasen vorhanden sind, der Tumor umgebende Organe und Gewebe soweit infiltriert hat, dass er inoperabel geworden ist, oder die Patienten aufgrund ihrer 14 Multimorbidität nicht operiert werden können. Dafür stehen verschiedenste endoskopische, interventionelle, chirurgische und radiotherapeutische Techniken zur Verfügung38,39,40. Als Prognosefaktoren für die Therapie gelten die Tumorausdehnung, die Tumorlokalisation (je weiter proximal, desto schlechter ist die Prognose), die Zahl der befallenen Lymphknoten (≥ 3 versus < 3), der Gewichtsverlust, die Komorbidität und das Lebensalter des Patienten. Es lassen sich 4 prognostische Gruppen unterscheiden. Zur Gruppe 1 gehören die frühen Tumore (Stadium 0-I). Gruppe 2 setzt sich aus den potenziell resektablen Tumoren zusammen (Stadium II A und IIB). Gruppe 3 besteht aus den lokal fortgeschrittenen Tumoren (Stadium III) und Gruppe 4 aus den bereits metastasierten Tumoren (Stadium IV). Sobald die Tumore nicht mehr chirurgisch resektabel sind, sinkt die 3-Jahres-Überlebensrate von 15-40% für das Plattenepithelkarzinom beziehungsweise 25-45% für das Adenokarzinom auf 10% beziehungsweise 10-15% in der Gruppe 3. Dabei sind deutliche Unterschiede zwischen dem Adenokarzinom und dem Plattenepithelkarzinom zu erkennen (Tabelle 3)41. Obwohl die chirurgische Behandlung in Kombination mit Chemotherapie und/oder Radiotherapie die Überlebensrate der Patienten leicht verbessern kann, bleibt die Mortalität hoch42,43,44. Ebenso ist die Prognose des Plattenepithelkarzinoms des Ösophagus mit einer 5Jahres-Überlebensrate von 10-30% sehr schlecht45. In einem lokal begrenzten Stadium beträgt die 5-Jahres-Überlebensrate 29% während sie auf 2% sinkt, sobald Fernmetastasen vorhanden sind46. Die Prognose ist Lymphknotenmetastasierung47, entscheidend der vom Ausmaß vollständigen der Tumorpenetration, chirurgischen Entfernung der und molekularbiologischen Faktoren abhängig48. Bei Patienten mit intraepithelialem Tumor ist das Risiko der Lymphknotenmetastasierung sehr niedrig und sie haben eine dementsprechend günstigere Prognose49. Gruppe 1 Gruppe 2 Gruppe 3 Gruppe 4 Mediane Überlebenszeit - - 12-14 Monate 6-9 Monate 3-Jahres- Überlebensrate 59-75% 15-40% 10% 0 Mediane Überlebenszeit - - 12-14 Monate 6-9 Monate 3-Jahres- Überlebensrate 80-95% 25-45% 10-15% 0 Plattenepithelkarzinom Adenokarzinom Tab. 3: Prognostische Gruppen für die Therapie der Ösophaguskarzinome. 15 2. 2.1. Molekulare Grundlagen Einflussfaktoren bei der Genese des Ösophaguskarzinoms Die genetische Instabilität spielt eine bedeutende Rolle bei der Progression maligner Tumore50. Durch die Mutation von Kontrollgenen erlangen neoplastische Zellen einen selektiven Wachstumsvorteil, der sie zu klonaler Expansion befähigt51. Die Entwicklung des Ösophaguskarzinoms ist ein multifaktoriell beeinflusster Prozess. Zahlreiche Studien haben versucht, die molekularen Mechanismen, die der Entwicklung zugrunde liegen, aufzuklären. Verschiedenste Onkogene und Tumorsuppressorgene wurden mit der Karzinogenese des Ösophaguskarzinoms in Verbindung gebracht52. Häufig aktivierte Onkogene bei der Tumorgenese ösophagealer Karzinome betreffen die Wachstumsfaktoren (EGF, epidermal growth factor; HGF/SF, hepatocyte growth factor/scatter factor53), Wachstumsfaktorrezeptoren (EGFR/ c-ErbB1)54,55,56,57,58 und Cyclin D159,60,61. Beteiligte Tumorsuppressorgene sind unter anderem p5362,63,64,65,66 und das Retinoblastomprotein67,68. Die Wirkungen der einzelnen Defekte addieren sich und wirken im Rahmen der Tumorgenese synergistisch. Das gemeinsame Resultat ist meist eine verstärkte Stimulation von Proliferation69 und ein zunehmender Verlust der Differenzierung (Abbildung 2). 16 Abb. 2: Zusammenwirken der Protoonkogene und Tumorsuppressorgene im Rahmen der malignen Transformation. 2.2. Kalzium und Kalziumbindungsproteine Kalzium spielt eine entscheidende Rolle für zahlreiche zelluläre Prozesse. Dazu gehören beispielsweise der Zellmetabolismus, die Genexpression, die Signaltransduktion, das Zytoskelett70, die Proliferation, die Differenzierung, die Migration und die Apoptose71,72,73 von normalen und neoplastischen Zellen. Das Kalziumion fungiert bei diesen Prozessen als wichtiger sekundärer Botenstoff. Dementsprechend ist eine exakte Regulation der intrazellulären Kalziumkonzentration, welche im Ruhezustand zwischen 10 und 100 nM freiem Kalzium liegt, von fundamentaler Wachstumsfaktoren, Bedeutung. Zahlreiche Neurotransmitter und extrazelluläre Licht führen Signale über wie sehr Hormone, spezifische Signaltransduktionswege zu einem Anstieg der intrazellulären Kalziumkonzentration. Kalziumsignale werden größtenteils von der Superfamilie der kalziumbindenden Proteine über sekundäre Botenstoffkaskaden in physiologische intrazelluläre Antworten übersetzt73. Durch ihr großes Spektrum an zellulären Funktionen werden Kalziumbindungsproteine mit zahlreichen 17 Erkrankungen unter anderem auch mit der Karzinogenese verschiedenster Tumore in Verbindung gebracht. 2.2.1. Annexine Die Annexine sind eine große Familie kalziumbindender Proteine, die von der Mehrzahl der eukaryotischen Zellen exprimiert werden. Trotz ihrer strukturellen Gemeinsamkeiten verfügen sie über eine Vielzahl verschiedener zellulärer Funktionen. Annexin-1 und -2 sind in der Lage Kalziumkanäle in der Zellmembran zu bilden und sind dadurch entscheidend am Erhalt der Kalziumhomöostase beteiligt74. Sie sind außerdem an Vesikeltransport, Zellteilung, Apoptose, und der Regulation des Wachstums beteiligt. Die Bedeutung der Annexine im Rahmen der Karzinogenese scheint in ihrer Rolle für die Verbindung der Zellmembran mit dem Zytoskelett, dem Erhalt von Zell-Zell-Verbindungen und für die Endozytose der Membranbestandteile zu liegen. Aus diesen Funktionen wird deutlich, dass Annexine die metastatische Kapazität von neoplastischen Zellen beeinflussen können75. 2.2.2. S100-Proteine Eine weitere Familie von Kalziumbindungsproteinen, die eine entscheidende Rolle bei der Genese von Karzinomen zu spielen scheint, ist die S100-Proteinfamilie. Annexin-1 und S100 A11 oder auch Annexin-2 und S100 A10 bilden Heterotetramere, die die intrazelluläre Kalziumkonzentration beeinflussen76. Zu ihren Aufgaben zählen die Regulation von Proliferation, Differenzierung, Motilität, Sekretion, Proteinsynthese und Membranpermeabilität77,78,79. Zu den S100-Proteinen, welche mit Neoplasien in Verbindung gebracht werden, gehören S100 A2, S100 A4, S100 A6 und S100 B. 2.2.3. Neuronale Kalzium-Sensor-Proteine Zu den kalziumbindenden Proteinen gehört unter anderem die Superfamilie der EF-HandProteine, zu denen die Familie der neuronalen Kalzium-Sensor-Proteine (NCS) zählt. Mitglieder der intrazellulären NCS-Proteinfamilie (Abbildung 3) sind an einer Vielzahl von kalziumabhängigen Signalkaskaden beteiligt. Sie sind wichtige Vermittler zwischen den 18 sekundären Botenstoffsystemen, wie beispielsweise Kalzium und cAMP oder auch Kalzium und cGMP in Neuronen73. Die Proteine enthalten EF-Hand-Domänen, welche als Bindungsstellen für Metalle dienen80. An dem in der Abbildung 3 dargestellten Stammbaum werden die phylogenetischen Beziehungen der einzelnen intrazellulären NCS-Proteine zueinander deutlich. Das humane Calmodulin wird dabei Kalziumbindungsproteine als Bezugsprotein verwendet. Zur der Gruppe I Superfamilie gehören die der EF-Hand- retinaspezifischen Guanylatzyklase-aktivierenden Proteine (GCAPs) GCAP-181,82, GCAP-283, GCAP-384 und das Guanylatzyklase-inhibierende Protein (GCIP)85. Die Gruppe II besteht aus den Kaliumkanalinteragierenden Proteinen (KChIPs)86. Gruppe III setzt sich zusammen aus den Gründungsmitgliedern der NCS-Familie – Visinin und Recoverin, dem Frosch-orthologen SModulin (Sensitivität modulierendes Protein)87 sowie s2688. In die Gruppe IV gehören die VILIPs/ NVPs (Visinin-like proteins/ neuronal Visinin-like proteins), die sich aus VILIP-1, VILIP-2, VILIP-3, Hippocalcin und den Neurocalcinen89 aufbauen. Die Gruppe V, die evolutionsgeschichtlich älteste Gruppe, stellen die Frequenine, wie NCS-1 (neuronal CalciumSensor-1)90 und Frequenin aus Saccharomyces cerevisiae91. Die Gruppeneinteilungen basieren auf Aminosäuresequenzen aus der SWISSPROT Datenbank (Spilker et al., 2002a). Es können zahlreiche Zusammenhänge mit pathologischen Prozessen nachgewiesen werden. Die Recoverine beispielsweise spielen bei der Entstehung der Krebs-assoziierten Retinopathie (CAR) eine bedeutende Rolle92, das NCS-1 bei der Genese der Schizophrenie, der bipolaren Störung93,94,95 und bei mentaler Retardierung96 sowie die Familie der VILIPs/ Neurocalcin beim Morbus Alzheimer97,98,99 und der Apoptose72. Es ist kürzlich gezeigt worden, dass die NCS-Proteine außerdem an essentiellen neuronalen Prozessen, wie dem Recycling von Ionenkanälen und Rezeptoren, dem Membrantransport, der Modulation von Ionenkanälen und der Regulation der Apoptose beteiligt sind100,101. Des Weiteren sind sie in der Zytoskelettorganisation, der zellulären Kommunikation und der Differenzierung involviert73. Eine wichtige Bedeutung kommt ihnen außerdem bei der Regulation der Signalübertragung von zahlreichen NCS-Proteinen der N-terminalen Myristoylierung zu102,103,104,105. Durch den Kalzium-Myristoyl-Switch-Mechanismus sind die NCS-Proteine in der Lage, Informationen kalziumabhängig und reversibel vom Zytoplasma zur Zellmembran und zurück zu übermitteln. Für Recoverin konnte der genaue strukturbiologische Mechanismus analysiert werden106. Die Bindung von Kalzium an NCS-Proteine löst dabei eine Veränderung der Proteinkonformation 19 aus. Dies führt zur Präsentation der hydrophoben Polypeptidanteile und des Myristoylrests an der Proteinoberfläche. Dadurch wird die Interaktion mit Zellmembranproteinen ermöglicht. Der Kalzium-Myristoyl-Switch ist zum Transport der Kalziumsignale ein entscheidender und spezifischer Mechanismus. In zahlreichen pathologischen Vorgängen, einschließlich Tumorerkrankungen, findet sich eine beeinträchtigte Kalziumhomöostase. In diesen Prozessen könnte demnach auch die multifunktionale NCS Protein Familie involviert sein107. Abb. 3: Phylogenetischer Stammbaum der NCS Proteine. 20 2.3. VILIP-1 VILIP-1 (Visinin-like Protein-1), ein 22-kDa-Protein, ist Mitglied der neuronalen EF-HandKalziumbindungsproteine und wird hauptsächlich im ZNS exprimiert108. Dort ist es entscheidend bei der Regulation der zellulären Signale während der neuronalen Entwicklung und Differenzierung beteiligt73. Kürzlich ist VILIP-1 auch in verschiedenen peripheren Geweben des Menschen und der Ratte entdeckt worden109. VILIP-1 beeinflusst die Konzentration von zyklischen Nukleotiden durch Interaktion mit Adenylatzyklasen und Guanylatzyklasen110,111. Der Einfluss von VILIP-1 auf cAMP ist unter anderem in neuralen Zelllinien studiert worden. Dadurch ist eine Funktion von VILIP-1 im Rahmen der Zellproliferation und Differenzierung aufgezeigt worden. In mit VILIP-1-cDNA transfizierten Gliomazelllinien kann wie bei anderen Mitgliedern der NCS-Protein-Familie eine kalziumabhängige Membranbindung beobachtet werden. Diese Bindung ist essentiell abhängig von der Myristoylierung des Proteins. Myristoyliertes VILIP-1 wirkt stimulierend auf die basale Zunahme der cAMP Konzentration, währenddessen nicht myristoyliertes VILIP-1 diesen Effekt nicht aufweist112. Außerdem ist in murinen Hauttumoren ein über cAMP vermittelter tumorsuppressiver Effekt von VILIP-1 dargestellt worden125,126. 2.4. Ki-67 Ki-67 ist 1991 als ein nukleäres Nicht-Histon-Protein identifiziert worden113. Die Abwesenheit von Ki-67 in nicht proliferierenden Zellen und seine stetige Expression in hoch proliferativen Zellen hat großes Interesse geweckt. Verschiedene Publikationen haben Ki-67 als Marker für Proliferation bestätigt. Nur sehr wenige Veröffentlichungen beschreiben eine Expression in nicht proliferierenden Zellen114. Das Gen von Ki-67 befindet sich auf dem langen Arm des menschlichen Chromosoms 10 (10q25)115. Durch alternative Splicevorgänge gibt es 2 verschiedene mRNA Varianten, die für 2 Isoformen dieses Proteins kodieren. Einige Ergebnisse aus menschlichen und murinen Zelllinien weisen darauf hin, dass mehrere postsplicingVarianten bestehen und es demzufolge mehrere Isoformen gibt116. Die Intensität der Ki-67Expression variiert während des Zellzyklus. Sie ist schwach während der der G1- und frühen SPhase, nimmt dann im Verlauf zu und erreicht in der Mitose ein Maximum. Während der Anaphase und Telophase beginnt eine schnelle Abnahme der Expression117. Insgesamt ist bis auf eine wichtige Rolle im Zellzyklus wenig über die eigentliche Funktion von Ki-67 bekannt. 21 3. Fragestellung Das Ösophaguskarzinom ist einer der aggressivsten Tumore des Gastrointestinaltrakts. Trotz des Einsatzes multimodaler Therapiekonzepte hat sich die Prognose nicht wesentlich verbessert. Dieser Umstand rechtfertigt die weitere intensive Forschung nach molekularen Markern, die eine Einschätzung der Invasivität und der Prognose frühzeitig ermöglichen, um eine individuelle Optimierung der Therapie zu erreichen. Nachdem das neuronale Kalziumbindungsprotein VILIP-1 auch außerhalb des zentralen Nervensystems nachgewiesen worden ist109 und Veröffentlichungen einer Arbeitsgruppe der Abteilung für Pathologie am Fox Chase Cancer Center in Philadelphia die potentielle Tumorsuppressor-Funktion von VILIP-1 auf Plattenepithelkarzinom-Zelllinien beschrieben haben125,126, wird in dieser Studie untersucht, ob sich die Ergebnisse aus murinen Zelllinien auch auf humanes Gewebe übertragen lassen. Das Verhalten von VILIP-1 wird speziell im primären Plattenepithelkarzinom des Ösophagus analysiert. Es wird dabei untersucht, inwieweit VILIP-1 in der Genese des ösophagealen Karzinoms eine Rolle bei der Tumorsuppression spielt beziehungsweise die migratorischen und proliferativen Fähigkeiten der Zellen beeinflusst. Zunächst erfolgt der immunhistochemische Nachweis der Expression von VILIP-1 in der normalen Ösophagusmukosa. Anschließend wird die Expression von VILIP-1 zwischen ösophagealem Normalgewebe und Tumorgewebe verglichen. Weiterhin werden die Beziehungen zwischen der VILIP-1-Expression und klinisch-pathologischen Parametern der Karzinome analysiert. Dazu gehören die Tumorgröße/Infiltrationstiefe, der Differenzierungsgrad, der regionale Lymphknotenstatus sowie Patientenmerkmale wie Alter und Geschlecht. Da die ungehinderte Proliferation 118 Tumorprogression darstellt einen entscheidenden Faktor der ösophagealen , interessiert besonders der Zusammenhang zwischen der zellulären Proliferation und VILIP-1-Expression. In Anbetracht der bereits vorliegenden Ergebnisse zur Tumorsuppression durch VILIP-1 in murinen Zelllinien und Tumoren wird ein Verlust der VILIP-1-Expression im Rahmen der zunehmenden proliferativen Kapazität der neoplastischen Zellen vermutet. Um diesen Zusammenhang zu eruieren, werden Doppelfärbungen mit Ki-67 durchgeführt. Ki-67 ist ein bereits etablierter Proliferationsmarker, dessen Expression mit der von VILIP-1 verglichen wird. 22 4. 4.1. Material und Methoden Patienten Diese Studie beinhaltet Gewebematerial von 55 Patienten (49 Männer und 6 Frauen) zwischen 47 und 82 Jahren (Durchschnittsalter von 62,3 Jahren) mit primärem Plattenepithelkarzinom des Ösophagus (ESCC, esophagus squamous cell carcinoma). Darunter befinden sich 54 Gewebeproben von Ösophaguskarzinomen und 24 Normalgewebe des Ösophagus (Tabelle 4). Präoperativ wurden unter anderem ein klinisches Staging sowie eine Ösophago-GastroDuodenoskopie mit Biopsie, eine Endosonographie des Ösophagus, ein Röntgen-Thorax, eine CT-Thorax/Abdomen und eine Sonographie des Abdomens durchgeführt. Dadurch können der histologische Tumortyp, die longitudinale Ausdehnung und die horizontale Eindringtiefe des Tumors sowie eventuell regionale Lymphknotenmetastasen und Fernmetastasen bestimmt werden. Eine neoadjuvante Therapie durch Chemotherapeutika oder Bestrahlung, welche die Expression von Proteinen im Gewebe beeinflussen könnte, ist unseres Wissens nicht durchgeführt worden. Die Patienten sind zwischen 1993 und 2004 durch subtotale oder totale Ösophagusektomie und die radikale Entfernung regionaler Lymphknoten behandelt worden. 23 55 100% Weiblich 6 10,9% Männlich 49 89,1% ≤ 60 25 45,5% > 60 30 54,5% Anzahl der Patienten Geschlecht Alter Gewebetyp Normalgewebe 24 Tumorgewebe 54 T-Stadium T1 15 27,8% T2 8 14,8% T3 28 51,9% T4 3 5,6% N0 26 48,1% N1 28 51,9% G1 1 1,9% G2 35 64,8% G3 18 33,3% Nodalstatus Grading Tab. 4: Charakteristika der Patienten und klinisch-pathologischen Merkmale der ösophagealen Plattenepithelkarzinome. 4.2. Gewebe Das Gewebematerial ist während der Operationen entnommen, in 10%igem Formalin fixiert und anschließend in Paraffin gebettet worden. Ein Pathologe hat dieses Gewebe nachuntersucht und klassifiziert. Dreiunddreißig Tumorgewebe und 24 Normalgewebe stammen aus der Tumorbank der Robert-Rössle-Klinik der Charité Berlin. 24 Die Paraffinblöcke werden in 1µm-Scheiben geschnitten und auf beschichtete Adhäsionsobjektträger (Histobond/Marienfelde) gezogen. Anschließend werden sie in einer Mikrowelle getrocknet. Ein Objektträger pro Tumor und Normalgewebe wird mittels der Hematoxylin-Eosin-Methode gefärbt und von einem Pathologen untersucht. Die restlichen 21 Tumorexemplare stammen von einem Tissue Microarray (A218, biomol/PETAGEN). Diese Proben befinden sich alle auf einem Objektträger. Dieser Objektträger ist vor dem Färben über Nacht bei 60°C getrocknet worden und hat die Färbeschritte ebenso wie die restlichen Objektträger durchlaufen. Die Hematoxylin-EosinFärbungen dieser Exemplare werden ebenfalls im Vorfeld pathologisch begutachtet. Alle Gewebe werden über die unten beschriebene Immunfluoreszenzmethode gefärbt und 10 Fälle zusätzlich über die standardisierte Avidin-Biotinyl-Peroxidase-Komplex-Methode. Klinisch-pathologische Informationen zu Tumorgröße, Differenzierung und Lymphknotenstatus sind entsprechend der Kriterien der Klassifikation der Union International Contre le Cancer (UICC) von 1997 evaluiert worden. Ergänzend werden zwei Microarrays (A704/A301 biomol/PETAGEN) mit verschiedenen Normalgeweben und Tumorgeweben über die Avidin-Biotinyl-Peroxidase-Komplex-Methode gefärbt, um die Expression von VILIP-1 in weiteren Geweben und Tumoren exemplarisch einschätzen zu können. Darunter befinden sich Gewebebeispiele von Haut, Niere, Leber, Kolon und Prostata. Die Gewebe auf diesen Microarrays werden ebenfalls vor den Färbungen bei 60°C über Nacht getrocknet. 4.3. Antikörper und Reagenzien Der Nachweis von VILIP-1 erfolgt durch einen spezifischen polyklonalen Antikörper/Ratte, welcher durch die Arbeitsgruppe von Prof. Dr. Braunewell hergestellt wird110. Ki-67 wird mit Hilfe eines monoklonalen Maus-Antikörpers von DAKO Cytomation nachgewiesen. Der biotinylierte Anti-Ratte-(Zweit-)Antikörper/Ziege, der Vectastain Elite ABC Kit und das Vector HRP Substrat DAB (3,3-Diaminobenzidin) sind über Linaris bestellt worden. Als fluoreszenzmarkierte (Zweit-)Antikörper werden Alexa Fluor 488 Ziege, Anti-Ratte-IgG (H+L) und Alexa Fluor 565 Ziege, Anti-Maus-IgG von Molecular Probes Europa verwendet. Das 4’,6-Diamidino-2-phenyindol-2HCL (DAPI) für die Kernfärbung wird über SERVA bezogen (Tabelle 5). 25 Für die Deparaffinisierung werden Xylol und für die Dehydrierung und Rehydrierung der Schnitte Alkohol und Isopropylalkohol von Roth verwendet. Phosphat-gepufferte Saline (PBS) ist einerseits selbst hergestellt worden und wird andererseits über die Biochrom AG (PBS-Dulbecco) bezogen. Zur Herstellung einer 10-fachen PBSStammlösung mit einem pH=7,4 werden 23,56g Na2HPO4/83mM; 3,86g NaH2PO4 *H2O /17mM und 175,32g NaCl/1,5M mit destilliertem Wasser auf 2 Liter aufgefüllt. Primärantikörper Spezies Isotyp Klonalität Hersteller Verdünnung VILIP-1 Ratte IgG polyklonal PD Dr. K.-H. 1:1000 Braunewell Ki-67/MIB-1 Maus IgG monoklonal Dako 1:50 Anti-Ratte Ziege IgG polyklonal Linaris 1:300 Alexa Fluor 488, Ziege IgG polyklonal Molecular 1:1000 Sekundärantikörper Anti-Ratte Alexa Fluor 565, Probes Ziege IgG polyklonal Anti-Maus Molecular 1:1000 Probes Tab. 5: Primärantikörper und Sekundärantikörper. 4.3.1. VILIP-1 Der polyklonale VILIP-1-Antikörper aus Rattenserum ist gegen rekombinantes N-terminal-Hisgebundenes VILIP-1-Fusionsprotein gerichtet119. Die Affinitätsreinigung des polyklonalen Antikörpers gegen VILIP-1-His-Fusionsproteine aus Rattenserum erfolgt über die Bindung der Antikörper an immobilisierte GST-Fusionsproteine (Glutathion-S-Transferase). Abschließend wird eine saure Elution durchgeführt120. Die über die GST-V1-Säulen affinitätsgereinigten Antikörper sind für VILIP-1 hochspezifisch. Sie zeigen beispielsweise keine Kreuzreaktion mit rekombinantem NVP-3 (neuronal Visinin-like protein-3). Das rekombinante NVP-3 weist eine 67%ige Übereinstimmung mit der Sequenz von VILIP-1 auf. Eine leichte Kreuzreaktion besteht indes zum stark homologen NVP-2 (neuronal Visinin-like protein-2), welches über eine 89%ige Übereinstimmung der Sequenz zu VILIP-1 verfügt. Die konzentrierte Antikörperlösung wird aliquotiert und bei -20°C gelagert. 26 4.3.2. Ki-67 Der ursprüngliche monoklonale Ki-67-Antikörper kann nur zur Immunfärbung von proliferierenden Zellen in unfixiertem Gewebe verwendet werden. Im Jahr 1992 ist durch die Entwicklung der neuen MIB-1- und MIB-3-Antikörper auch die Färbung von in Paraffin gebettetem Gewebe möglich geworden. Diese Antikörper binden an das gleiche Epitop wie der ursprüngliche Ki-67-Antikörper. Dies ist im Western Blot über identische Banden nachweisbar121. Die Färbungen von Formalin-fixiertem und in Paraffin gebettetem Gewebe mit MIB-1 und MIB3 werden durch eine Behandlung zur Epitopdemaskierung (Schnellkochtopf oder Mikrowelle)122,123 deutlich verbessert. 4.3.3. 4’, 6-Diamidino-2-phenylindol (C16H15N5.2HCl) DAPI ist eine DNA-spezifische Substanz, welche durch Bindung an Adenin- und Thymin-reiche Sequenzen mit der DNA einen fluoreszierenden Komplex formt. Außerdem ist es in der Lage, nicht-fluoreszierende interkalierende Verbindungen mit doppelsträngigen Nukleinsäuren einzugehen124. Zur Vorbereitung werden vom 4’, 6-Diamidino-2-phenylindol 4µl in 100ml PBS verdünnt und im Kühlschrank bei 4°C gelagert. 4.4. Methoden 4.4.1. Immunhistochemie Zur Charakterisierung von Geweben kann die Verteilung von Antigenen in situ bestimmt werden. Dies ist möglich über immunhistochemische Färbungen, welche auf Interaktionen zwischen Antikörpern und Antigenen beruhen und somit die Verteilung von bestimmten Antigenen in Zellen beziehungsweise Geweben darstellen können. Durch die hohe Spezifität von Antigen-Antikörper-Reaktionen sind immunhistochemische Färbemethoden im Allgemeinen genauer als gewöhnliche histochemische Färbungen. In 27 immunhistochemischen Färbungen verwendete Antikörper gehören hauptsächlich zum IgG-Typ. Sie bestehen aus zwei schweren Ketten vom γ-Typ und zwei leichten Ketten vom κ-Typ oder λTyp. Das von leichten und schweren Ketten gebildete Fab-Fragment trägt die Antigenerkennungsregion. Zur Visualisierung der Antigene können die Sekundärantikörper mit Enzymmarkern oder Fluoreszenzmarkern konjugiert sein. Enzymmarkierungen werden häufig verwendet, da zur Darstellung ein Lichtmikroskop ausreichend ist, die standardisierte Hematoxylin-Eosin-Färbung die histologische Evaluation vereinfacht und die geringe Größe der Peroxidase die Antikörperbindung auch an dicht benachbarten Antigenen nicht beeinträchtigt. Außerdem gibt es zahlreiche Chromogene, die mit der Peroxidase reagieren, Farbprodukte bilden und an der Position des Antigens präzipitieren. 4.4.1.1. Deparaffinisierung, Rehydrierung und Epitopdemaskierung Die Schnitte werden zu Beginn für 20 Minuten in drei mit Xylol gefüllten Küvetten deparaffinisiert und anschließend in einer absteigend konzentrierten Alkoholreihe (96%, 90%, 80%, 70%, 60%, 50%) rehydriert. Die Epitopdemaskierung erfolgt durch eine Behandlung im Schnellkochtopf für 5 Minuten mit Zitratpuffer (pH=6), basierend auf Zitronensäure und Natriumzitrat (Merck) in destilliertem Wasser. Für den Zitratpuffer wird im Voraus eine Stammlösung angesetzt. Diese besteht aus 3,782g Zitronensäure (0,1M) und 24,11g Natriumzitrat (0,1M), welche mit 1000ml destilliertem Wasser aufgefüllt werden. Die Stammlösung wird im Kühlschrank bei 4°C aufbewahrt und bei Bedarf 1:10 verdünnt. Nach dieser Behandlung kühlt der Schnellkochtopf für 15-20 Minuten ab. Daraufhin werden die Schnitte für 5 Minuten in PBS gewaschen und dann in 0,3%igem H2O2, verdünnt in Methanol, für 30 Minuten inkubiert. Dies dient der Blockade der endogenen Peroxidase. Abschließend wird ein erneuter Waschschritt für 5 Minuten in PBS durchgeführt. 4.4.1.2. Avidin-Biotinyl-Peroxidase-Komplex-Methode Die Avidin-Biotinyl-Peroxidase-Komplex-Methode (ABC-Methode) ist eine ImmunperoxidaseFärbetechnik. Sie basiert auf der Fähigkeit des Glykoproteins Avidin, vier Moleküle des Vitamins Biotin physikalisch zu binden. Vermittelt über das Avidin erfolgt die Bindung des biotinylierten Zweitantikörpers an die biotinylierte Peroxidase. Um unspezifische Hintergrundfärbungen zu verringern, erfolgt eine Vorinkubation in normalem 28 Ziegenserum für 20 Minuten. Dieses Serum entspricht der Spezies des verwendetet Zweitantikörpers. Nach Ablauf der Inkubationszeit wird das überschüssige Serum entfernt und die Schnitte direkt ohne vorheriges Waschen mit dem Erstantikörper (Ratte, VILIP-1, 1:1000) vollständig benetzt. Dabei kommt es zur Bindung des VILIP-1-Antikörpers über das Fab-Fragment an das entsprechende Epitop (Dreieck rot/ Abbildung 4A). Die Inkubation der Objektträger mit dem Erstantikörper wird über Nacht bei 4°C im Kühlschrank durchgeführt. Am folgenden Morgen werden die Schnitte nach dem Waschen in PBS mit dem biotinylierten Anti-Ratte-Zweitantikörper (Ziege, 1:300, 2-10 µg/ml) 30 Minuten lang inkubiert (Abbildung 4B). Im Anschluss folgt ein Waschgang und der nächste Inkubationsschritt mit dem Vectastain ABC Reagenz (Avidin-Biotinylierter-Peroxidase-Komplex) für weitere 30 Minuten (Abbildung 4C). Nach erneutem Waschen in PBS wird das Substrat der Peroxidase, das DAB (3,3Diaminobenzidin), für 10 Minuten zugefügt. Dies führt schließlich zur Präzipitation eines braunen Chromogens. Somit sind die Immunkomplexe als Braunfärbung abschließend sichtbar (Abbildung 4D). Die dem DAB-Chromogen normalerweise zuzufügende Nickellösung wird weggelassen, um eine Graufärbung des Farbkomplexes zu vermeiden und so eine bessere Differenzierung gegenüber der Hematoxylin-Eosin-Färbung zu gewährleisten. Zum Abschluss werden die Schnitte in Leitungswasser gewaschen und es erfolgt eine Gegenfärbung mit Hematoxylin-Eosin. Zur Dehydrierung durchlaufen die Objektträger eine aufsteigende Alkoholreihe (70%, 90%, 96%, 96% Isopropylalkohol) und werden vor dem Eindeckeln für 30 Minuten in drei mit Roticlear (Roth) gefüllten Küvetten inkubiert. Abb. 4: Graphische Darstellung der Avidin-Biotinyl-Peroxidase-Komplex-Methode. 29 4.4.2. Immunfluoreszenzfärbung Hierbei werden anfangs die gleichen Schritte wie für die Deparaffinisierung und das AntigenRetrieval in der Immunhistochemie durchgeführt. Danach erfolgt zur Reduktion von unspezifischen Färbereaktionen eine Inkubation in normalem Ziegenserum für 30 Minuten. Das überschüssige Serum wird entfernt und anschließend werden die Schnitte mit dem ersten Erstantikörper (Ratte, VILIP-1, 1:1000, Antikörper orange/ Abbildung 5) für eine Stunde vollständig bedeckt. Der VILIP-1-Antikörper bindet dabei an das intrazytoplasmatisch gelegene Epitop (Dreieck rot/ Abbildung 5). Nach dem Waschen in PBS erfolgt die 30-minütige Benetzung mit dem fluoreszenzmarkierten ersten Zweitantikörper (Ziege, Alexa Fluor 488, AntiRatte, Antikörper blau/ Abbildung 5). Daraufhin werden die Objektträger wieder in PBS gewaschen und es wird die Inkubation mit dem zweiten Erstantikörper (Maus, Ki-67, 1:50, Antikörper gelb/ Abbildung 5) für eine weitere Stunde durchgeführt. Der Ki-67-Antikörper bindet an sein nukleär gelegenes Epitop (Ellipse orange/ Abbildung 5). Ein weiterer Waschdurchgang folgt und abschließend werden die Schnitte für nochmalige 30 Minuten mit dem fluoreszenzmarkierten zweiten Zweitantikörper (Ziege, Alexa Fluor 565, Anti-Maus, Antikörper violett/ Abbildung 5) behandelt. Zum Abschluss wird die Kernfärbung mit 4’,6-Diamidino-2-phenylindol.2HCL (DAPI), welches Kerne intensiv blau färbt, vollzogen. Um den Erfolg der Fluoreszenzfärbung nicht zu gefährden, werden alle Schritte in einer lichtgeschützten Färbekammer durchgeführt und die gefärbten Präparate lichtgeschützt im Kühlschrank bei 4°C gelagert. In allen Immunfärbetechniken werden zur Abschätzung der Spezifität der verwendeten Antikörper positive und negative Kontrollen eingeschlossen. Als positive Kontrolle wird eine identisch behandelte Probe, welche das entsprechende Antigen enthält, eingesetzt. In dieser Arbeit sind als Positivkontrollen Hippokampus-Schnitte aus Rattenhirnen verwendet worden. In jenen ist bereits eine VILIP-1-Expression in der hippokampalen CA1- und CA4-Region sicher nachgewiesen worden108. Als negative Kontrolle dient normale Ösophagusmukosa, die nicht mit dem Primärantikörper inkubiert wird. Diese wird lediglich mit PBS und dem Sekundärantikörper inkubiert und durchläuft anschließend alle weiteren Färbeschritte in gleicher Weise. 30 Abb. 5: Graphische Darstellung der Immunfluoreszenz-Doppelfärbung. 4.4.3. Quantifizierung der VILIP-1-Expression Die Fluoreszenz der gefärbten Gewebeschnitte wird mittels eines Leica-Fluoreszenzmikroskops (Leica DM RA) dargestellt. Dabei erfolgt die Aufnahme der Bilder über eine CCD-Kamera Leica DC200 (768x582 Pixel) und mit Hilfe des Programms Leica-DC-Viewer (Leica, Wetzlar). Die emittierte Fluoreszenz wird von 3 verschiedenen Kanälen entsprechend der Wellenlänge der verwendeten Zweitantikörper aufgenommen (358, 488 und 565 nm). Die mit diesem Fluoreszenzmikroskop aufgenommenen Bilder werden mit Adobe Photoshop 5.5 für Macintosh (Adobe Systems, San Jose, CA) zu einem einzigen Bild übereinandergelegt. Die Gewebeproben werden ohne Kenntnis der klinisch-pathologischen Merkmale des Tumors quantitativ ausgewertet. Dabei werden die spezifischen und unspezifischen Färbereaktionen verglichen und beurteilt sowie die Kontrollen ausgewertet. Unspezifische Färbungen zeigen sich teilweise in der Bindegewebsmatrix. Spezifische Färbungen sind auf das Zytoplasma und den Zellkern der Epithelien beschränkt. Die ösophagealen Normalgewebe und Tumorgewebe werden zunächst hinsichtlich einer vorhandenen oder nicht vorhandenen VILIP-1-Expression analysiert. Anschließend werden die prozentualen Anteile der VILIP-1-Expression und der Ki-67Expression bezogen auf die Zellzahl bestimmt. Dafür werden die Gesamtzahl der Zellen (Kernfärbung über DAPI) und die Anzahl der VILIP-1-positiven Zellen, der Ki-67-positiven Zellen sowie der gleichzeitig VILIP-1 und Ki-67 exprimierenden Zellen in einem Bildausschnitt definierter Größe ermittelt. Pro Gewebeprobe werden 5 Gesichtsfelder ausgezählt. Im Durchschnitt ergibt das pro Fall 245 Zellen. Abschließend werden die Gewebe entsprechend des Anteils ihrer VILIP-1-Expression klassifiziert: ein Anteil von 66 bis 100% entspricht einer starken, von 33 bis 66% einer mittleren und von 1 bis 33% einer schwachen Expression. 31 4.4.4. Statistische Analysen Die erhobenen Daten werden in Microsoft Excel und SPSS (Statistical Product and Service Solution) ausgewertet. Über den Chi-Quadrat-Test werden die Beziehungen zwischen der VILIP-1-Expression (VILIP1 vorhanden=1, VILIP-1 nicht vorhanden=0) und dem Gewebetyp (Normal-/Tumorgewebe), dem Alter, dem Geschlecht, der Tumorgröße (T1-T4), dem Nodalstatus (N0/N1) sowie der Differenzierung (G1-G3) ermittelt. Außerdem wird die mittlere prozentuale VILIP-1-Expression zwischen T1, T2, T3 und T4 über den mehrere Gruppen vergleichenden Kruskal-Wallis-Test analysiert. Unter den untersuchten Geweben befinden sich 23 korrespondierende Normal- und Tumorgewebe jeweils aus ein und demselben Patienten. Um diese Beziehung statistisch zu evaluieren, wird beim Vergleich dieser 23 Normal- und Tumorgewebe ergänzend der McNemarTest angewendet. Die Beziehungen der mittleren prozentualen Ki-67-Expression zu Gewebetyp, Alter, Geschlecht und Nodalstatus werden durch den Mann-Whitney-Test (U-Test) untersucht. Um Zusammenhänge zwischen mehren Gruppen vergleichen zu können, werden die mittlere prozentuale Ki-67-Expression und die Tumorgröße (T1-T4) sowie die Differenzierung (G1-G3) über den Kruskal-Wallis-Test analysiert. Die Ergebnisse werden als Mittelwerte und Standardabweichung (Standard deviation) sowie in Form von Boxplots dargestellt. Dadurch können die Signifikanzen zwischen den verschiedenen Gruppen berechnet und über Sternchen kodiert werden (* p< 0.05; ** p<0.01; *** p<0.001). 32 5. 5.1. Ergebnisse Immunhistochemie von VILIP-1 in einer Auswahl verschiedener humaner Normalgewebe und Tumore VILIP-1-Expression ist vor kurzem auch in Geweben und Tumoren außerhalb des zentralen Nervensystems beschrieben worden109,125,126. Um zu überprüfen, ob VILIP-1 auch in weiteren Geweben und Tumoren exprimiert wird und sich eine Beziehung zu den bisherigen Beobachtungen ableiten lässt, werden einzelne Fälle verschiedener humaner Normal- und Tumorgewebe exemplarisch immunhistochemisch untersucht. Dies ist besonders interessant, da VILIP-1 in Hauttumoren der Maus bereits als mutmaßliches Tumorsuppressorprotein identifiziert werden konnte125. Die VILIP-1-Expression zeigt sich in der Avidin-Biotinyl-Peroxidase-Komplex-Methode in Form brauner Farbpräzipitate (Abbildung 6 und 7). Pro Gewebeexemplar werden 5 repräsentative Bildausschnitte ausgewählt und je nach der Intensität der Färbung und Verteilung der braunen Farbpräzipitate evaluiert. Im Normalgewebe des Kolons finden sich in den Epithelien der Schleimhautkrypten nur leichte Farbpräzipitate. Im Gewebe eines Kolonkarzinoms hingegen stellt sich eine starke VILIP-1Expression dar. Die Expression ist annähernd homogen auf die einzelnen soliden Tumorzellnester verteilt (Abbildung 6 A und B). Im Lebergewebe zeigt sich in den normalen Hepatozyten eine mittlere Expression. Im Vergleich dazu lässt sich in den neoplastischen Hepatozyten eines hepatozellulären Karzinoms eine starke VILIP-1-Expression beobachten (Abbildung 6 C und D). In den Zellen der Haut zeigt sich eine mittlere Expression sowohl im Normalgewebe als auch im Gewebe eines dermalen Plattenepithelkarzinoms. Dabei findet sich eine VILIP-1-Expression vom Stratum basale bis zum Stratum corneum in allen Schichten der normalen Epidermis. Ebenso stellt sich ein nahezu homogenes Verteilungsmuster in den neoplastischen Zellen dar (Abbildung 6 E und F). 33 Abb. 6: Immunhistochemische Färbungen mittels der Avidin-Biotinyl-PeroxidaseKomplex-Methode (Vectastain Elite ABC Kit/Linaris) von Kolon- (A und B), Leber- (C und D) und Hautgewebe (E und F). In der linken Spalte ist das Normalgewebe und in der rechten Spalte das neoplastische Gewebe dargestellt (braune Farbpräzipitate/VILIP-1Expression). 34 Im gesunden Prostatagewebe lassen sich nur diskrete braune Farbpräzipitate nachweisen. Im neoplastischen Gewebe des Prostatakarzinoms hingegen stellt sich eine VILIP-1-Expression etwas deutlicher dar (Abbildung 7 A und B). Im Normalgewebe der Niere findet sich eine leichte VILIP-1-Expression, während die Expression im Gewebe des klarzelligen Nierenzellkarzinoms schließlich vollständig verloren geht (Abbildung 7 C und D). Zusammenfassend findet sich demnach beim Vergleich zwischen Normalgewebe und neoplastischem Gewebe Plattenepithelkarzinom der in den Haut exemplarisch eine untersuchten gleichbleibende Geweben beim VILIP-1-Expression, beim Kolonkarzinom, beim hepatozellulären Karzinom und beim Prostatakarzinom eine zunehmende VILIP-1-Expression sowie beim Nierenzellkarzinom eine abnehmende VILIP-1-Expression im Rahmen der malignen Transformation. Abb. 7: Immunhistochemische Färbungen mittels der Avidin-Biotinyl-PeroxidaseKomplex-Methode (Vectastain Elite ABC Kit/Linaris) von Prostatagewebe (A und B) und Nierengewebe (C und D). In der linken Spalte ist das Normalgewebe und in der rechten Spalte das neoplastische Gewebe dargestellt (braune Farbpräzipitate/VILIP-1-Expression). 35 5.2. Immunhistochemie von VILIP-1 im Normalgewebe und im Plattenepithelkarzinom des Ösophagus Ergänzend zur Tumorgewebe exemplarischen werden mittels Untersuchung der verschiedener humaner Normal- Avidin-Biotinyl-Peroxidase-Komplex-Methode und zehn ösophageale Normal- und Tumorgewebe untersucht. Dabei zeigt sich in allen Normalgeweben eine VILIP-1-Expression in den basalen und parabasalen Zellschichten in Form brauner Farbpräzipitate (Abbildung 8 A und B). Im neoplastischen Gewebe geht die VILIP-1-Expression vollständig verloren oder ist deutlich reduziert (Abbildung 8 D und E). In Ausnahmefällen bleibt die Expression auch unverändert oder ist mittelgradig reduziert (Abbildung 8 F). Der Unterschied zwischen Normalgewebe und Tumorgewebe wird vor allem an der Abbildung 8 C deutlich. Hier stellen sich normale Ösophagusmukosa und neoplastisches Gewebe in unmittelbarer Nachbarschaft dar. Eine eindrucksvolle Reduktion der VILIP-1-Expression im Tumorgewebe ist erkennbar. 36 Abb. 8: Darstellung der VILIP-1-Expression (braune Farbpräzipitate) mittels der AvidinBiotinyl-Peroxidase-Komplex-Methode in mehreren Normalgeweben (A, B) und ösophagealen Plattenepithelkarzinomen (D, E und F). In Abbildung C erkennt man neoplastisches Gewebe in unmittelbarer Nachbarschaft zur normalen Ösophagusmukosa. 37 5.3. Immunfluoreszenzfärbung von VILIP-1 im Normalgewebe des Ösophagus Im Mausmodell konnte an Plattenepitheltumorzelllinien gezeigt werden, dass höhere Malignität mit Verlust der VILIP-1-Expression einhergeht125,126. Um zu kontrollieren, ob sich der beobachtete Verlust der VILIP-1-Expression auch in menschlichem epithelialen Tumorgewebe vergleichbar vollzieht, wird ösophageales Gewebe aus 55 Patienten mittels Immunfluoreszenzfärbung von VILIP-1 analysiert. Darunter befinden sich 54 primäre Plattenepithelkarzinome des Ösophagus (ESCC) und 24 Normalgewebe des Ösophagus. Um die VILIP-1-Expression in den mit Immunfluoreszenz gefärbten Geweben (Abbildung 9) zu analysieren, werden zunächst die Gewebe in VILIP-1 exprimierend (=1) und VILIP-1 nicht exprimierend (=0) klassifiziert. Zur genaueren Quantifizierung der Expression wird die Gesamtzahl an Zellen, welche durch 4’,6-Diamidino-2-phenylindol (DAPI) blau markiert sind, und die Anzahl an VILIP-1-positiven und -negativen Zellen ermittelt. Pro Gewebeexemplar werden dafür 5 charakteristische Regionen ausgewählt und die Zellen eines Gesichtsfeldes ausgezählt. Im Durchschnitt werden 245 Zellen je Gewebeprobe ausgezählt. Aus dem Verhältnis der VILIP-1-positiven Zellen zur Gesamtzellzahl wird die VILIP-1-Expression in Prozent für jedes einzelne Gewebe errechnet. Diese Daten werden zusätzlich in eine semiquantitative Darstellung überführt. Dazu wird zwischen starker VILIP-1-Expression (66-100%), mittlerer Expression (33-66%), schwacher Expression (1-33%) und fehlender Expression unterschieden. Alle 24 untersuchten Normalgewebe zeigen eine Expression von VILIP-1 (Tabelle 6). Davon lässt sich bei insgesamt 14 (58,3%) eine starke Expression und bei 10 (41,7%) eine mittlere Expression beobachten. Eine schwache sowie keine VILIP-1-Expression finden sich im Normalgewebe des Ösophagus nicht. Im Mittel sind 71,6% der ausgezählten Zellen im Normalgewebe VILIP-1-positiv. Vergleichbar mit den immunhistochemischen Färbungen wird VILIP-1 auch in den mit Immunfluoreszenz untersuchten Normalgeweben vorwiegend in den basalen und parabasalen Zellschichten im Stratum germinativum und teilweise im unteren Bereich des Stratum spinosum exprimiert (Abbildung 9 A, C und E). Das restliche Stratum spinosum und das Stratum corneum bleiben ungefärbt. VILIP-1-Expression stellt sich hauptsächlich im Zytoplasma und in der Zellmembran der Epithelzellen dar. 38 Abb. 9: Immunfluoreszenzfärbung von VILIP-1 (grün), Ki-67 (rot) und DAPI (blau) im ösophagealen Normalgewebe (A, C, E) verglichen mit Plattenepithelkarzinomen des Ösophagus (B, D, F). 39 5.4. Immunfluoreszenzfärbung von VILIP-1 im Plattenepithelkarzinom des Ösophagus In den Plattenepithelkarzinomen des Ösophagus, welche über Immunfluoreszenz mit Antikörpern gegen VILIP-1 markiert werden, findet sich eine Reduktion der VILIP-1-Expression beziehungsweise der vollständige Verlust (Abbildung 9 B, D und F). Dieser Verlust wird besonders im Vergleich mit dem Normalgewebe deutlich (Abbildung 9 A, C und E). Die VILIP-1-Expression der neoplastischen Zellen findet sich wie im Normalgewebe hauptsächlich im Bereich des Zytoplasmas und der Zellmembran. Im Gegensatz zu den Normalgeweben, welche alle VILIP-1 exprimieren, sind unter den 54 getesteten Tumorgeweben 34 (63%) positiv und 20 (37%) negativ für eine VILIP-1-Expression (Tabelle 6). Von den 34 VILIP-1-positiven Tumoren zeigen 26 (48,1%) eine schwache und 8 (14,8%) eine mittlere Expression. Eine starke Expression findet sich in den Plattenepithelkarzinomen hingegen nicht. Im Mittel sind 13,5% der ausgezählten Zellen im neoplastischen Gewebe VILIP-1-positiv. VILIP-1 Normalgewebe Tumorgewebe Normalgewebe Tumorgewebe Alter (nur Tumorgewebe) >60 ≤ 60 Geschlecht (nur Tumorgewebe) Männer Frauen T-Stadium T1 T2 T3 T4 Nodalstadium N0 N1 Differenzierung G1 G2 G3 VILIP-1 n gesamt 24 54 23 23 positiv 24 34 23 12 % 100 63 100 52,2 negativ 0 20 0 11 % 0 37 0 47,8 p-Wert Testverfahren 0.001 Chi-Quadrat 0.058 McNemar 30 24 20 14 66,7 58,3 10 10 33,3 41,7 0.529 Chi-Quadrat 48 6 31 3 64,6 50 17 3 35,4 50 0.659 Chi-Quadrat 15 8 28 3 12 8 13 1 80 100 46,4 33,3 3 0 15 2 20 0 53,6 66,7 0.012 Chi-Quadrat 26 28 21 13 80,8 46,4 5 15 19,2 53,6 0.009 Chi-Quadrat 1 35 18 0 25 9 0 71,4 50 1 10 9 100 28,6 50 0.131 Chi-Quadrat Tab. 6: VILIP-1-Expression im Vergleich mit Charakteristika der Patienten und klinischpathologischen Daten. 40 5.5. Vergleich der VILIP-1-Expression zwischen Normal- und Tumorgewebe des Ösophagus Vergleicht man über den Chi-Quadrat-Test die VILIP-1-Expression (VILIP-1-positiv versus VILIP-1-negativ) zwischen den Normalgeweben und Karzinomen, so findet sich ein signifikanter Verlust von VILIP-1 im Tumorgewebe (p=0.001, Tabelle 6). Beachtet man außerdem, dass 23 der Normal- und Tumorgewebe jeweils aus dem gleichen Patienten stammen und vergleicht VILIP-1-positiv versus VILIP-1-negativ innerhalb dieser Fälle unter dem Gedanken einer Abhängigkeit voneinander über den McNemar-Test, so erhält man einen p-Wert von 0.058 für den Verlust der VILIP-1-Expression in korrespondierenden Gewebepaaren (Tabelle 6). 5.6. VILIP-1 und das Lebensalter Es hat sich über den Chi-Quadrat-Test keine signifikante Beziehung zwischen der VILIP-1Expression (VILIP-1-positiv versus VILIP-1-negativ) und dem Alter der Patienten (p=0.529 zwischen ≤ 60 und > 60 Jahren, Tabelle 6) darstellen lassen. Bei den Patienten über dem 60. Lebensjahr sind 20 (66,7%) VILIP-1 exprimierende Tumore zu finden. Davon zeigen 3 (10%) eine mittlere Expression und 17 (56,7%) eine schwache Expression. Zehn (33,3%) der Tumore zeigen keine VILIP-1-Expression. Die durchschnittliche VILIP-1-Expression bei den Patienten über dem 60. Lebensjahr liegt bei 12,5%. Bei den Patienten unter dem 60. Lebensjahr sind 14 (58,3%) der Tumore für VILIP-1 positiv. Unter ihnen zeigen 5 (20,8%) eine mittlere Expression und 9 (37,5%) eine schwache Expression. Zehn (41,7%) Tumore zeigen keine VILIP-1-Expression. Die durchschnittliche VILIP-1Expression bei diesen Patienten liegt bei 14,6%. 5.7. VILIP-1 und das Geschlecht Wenn man die Beziehung zwischen Geschlecht und VILIP-1-Expression (VILIP-1-positiv versus VILIP-1-negativ) über den Chi-Quadrat-Test analysiert, so ergibt sich ebenso kein signifikanter Zusammenhang (p=0.659). Bei den männlichen Patienten findet sich in 31 (64,6%) der untersuchten Tumore eine VILIP-1Expression. Davon zeigen 8 (16,7%) eine mittlere Expression und 23 (47,9%) eine schwache 41 Expression. In 17 (35,4%) Tumoren findet sich keine VILIP-1-Expression. Die durchschnittliche VILIP-1-Expression in den Ösophaguskarzinomen der männlichen Patienten beträgt 14,3%. Unter den weiblichen Patienten sind 3 (50%) VILIP-1-positive Tumore mit schwacher Expression zu finden. In 3 (50%) Fällen zeigt sich keine VILIP-1-Expression. Die durchschnittliche VILIP-1-Expression der Patientinnen liegt bei 7,1%. 5.8. VILIP-1 und die Tumorgröße Die VILIP-1-Expression ist in den untersuchten ösophagealen Karzinomen sowohl innerhalb eines Tumors als auch im Vergleich der Tumore untereinander sehr variabel. Teilweise geht die Expression vollständig verloren, teilweise findet sich eine geringe oder eine mittlere Expression. Unter den T1-Tumoren sind 12 (80%) VILIP-1 exprimierende Tumore. Davon finden sich bei 4 (26,7%) eine mittlere Expression und bei 8 (53,3%) eine schwache Expression. Bei 3 (20,0%) der Tumore findet sich keine VILIP-1-Expression. Alle untersuchten T2-Tumore sind VILIP-1-positiv. Darunter zeigen ein (12,5%) Tumor eine mittlere Expression und 7 (87,5%) eine schwache Expression. Bei den T3-Tumoren ergibt sich eine VILIP-1-Expression in 13 (46,4%) Fällen. Davon stellt sich bei 3 (10,7%) eine mittlere Expression und bei 10 (35,7%) eine schwache Expression dar. In 15 (53,6%) der Fälle findet sich keine VILIP-1-Expression. Die T4-Tumore zeigen lediglich bei einem (33,3%) untersuchten Fall eine schwache VILIP-1Expression. Die zwei (66,7%) weiteren untersuchten T4-Tumore sind negativ für VILIP-1. Die Mittelwerte der prozentualen VILIP-1-Expression betragen 17,4% in T1, 13,3% in T2, 11,7% in T3 und 10,7% in den T4-Tumoren (Abbildung 10). Ein Vergleich der mittleren prozentualen VILIP-1-Expression von T1 bis T4 über den KruskalWallis-Test führt nicht zu einem statistisch signifikanten Ergebnis (p=0.331, Abbildung 10). Da infolge des hohen Anteils an VILIP-1-negativen Tumoren (37%) und der Heterogenität der VILIP-1-Expression die Mittelwerte aus statistischer Sicht schwierig zu vergleichen sind, entschieden wir uns zu einem Vergleich zwischen VILIP-1-positiv (=1) und VILIP-1-negativ (=0) über den Chi-Quadrat-Test. Analysiert man die VILIP-1-Expression in Beziehung zur Tumorgröße (T1-T4) über den ChiQuadrat-Test, so findet sich ein signifikanter Hinweis darauf, dass der Anteil an VILIP-1negativen Tumoren von T1 zu T4 ansteigt (p=0.012, Tabelle 6). Besonders deutlich wird dies zwischen T1/T2 und T3/T4. Sind es unter den T1/T2-Tumoren nur 0-20%, die kein VILIP-1 42 exprimieren, so sind es unter den T3-Tumoren schon 53,6% und unter den T4-Tumoren 66,7%. Dies ist eventuell ein Hinweis auf den Verlust der VILIP-1-Expression mit zunehmender Tumorgröße beziehungsweise Tumorinvasion, insbesondere bei Penetration der Adventitia (T3) und Infiltration der benachbarten Organe (T4) (Tabelle 6, Abbildung 11). Abb. 10: Darstellung der nichtsignifikant abnehmenden mittleren prozentualen VILIP-1Expression mit Zunahme der Tumorgröße, p=0.331 im Kruskal-Wallis-Test. Die Standardabweichung ist in Form der Fehlerbalken aufgeführt. 43 Abb. 11: Darstellung des prozentualen Anteils VILIP-1-negativer Tumore in T1, T2, T3 und T4. In T2 exprimieren alle untersuchten Tumore VILIP-1 (VILIP-1-negativ: 0%). Vergleich VILIP-1-positiv (=1) und VILIP-1-negativ (=0) für T1-T4, p=0.012 im ChiQuadrat-Test. 5.9. VILIP-1 und der Nodalstatus Die Analyse der VILIP-1-Expression (VILIP-1-positiv versus VILIP-1-negativ) in Abhängigkeit vom Nodalstatus im Chi-Quadrat-Test zeigt eine signifikante Abnahme von VILIP-1 in Tumoren mit regionalen Lymphknotenmetastasen (p=0.009, Tabelle 6, Abbildung 12 und 13). Unter den Tumoren ohne regionale Lymphknotenmetastasen finden sich 21 (80,8%) VILIP-1positive Tumore. Bei 7 (26,9%) N0-Tumoren wird eine mittlere Expression und bei 14 (53,8%) eine schwache Expression beobachtet. Bei 5 (19,2%) N0-Tumoren findet sich keine VILIP-1Expression. Unter den Tumoren mit regionalen Lymphknotenmetastasen befinden sich 13 (46,4%) VILIP-1exprimierende Tumore. Davon zeigen ein (3,6%) N1-Tumor eine mittlere Expression und 12 (42,9%) eine schwache Expression. Bei 15 (53,6%) N1-Tumoren fehlt eine VILIP-1-Expression. Die mittlere prozentuale VILIP-1-Expression unter den N0-Tumoren beträgt 20,3% und unter den N1-Tumoren 7,1%. Vergleicht man direkt den Anteil an VILIP-1-negativen Tumoren zwischen N0 und N1, so exprimieren 19,2% der N0-Tumore kein VILIP-1. Unter den N1-Tumoren steigt dieser Anteil bereits auf 53,6% (Abbildung 13). 44 Zusammenfassend ist nach dem Auftreten regionaler Lymphknotenmetastasen (N1) die Anzahl an VILIP-1 nicht exprimierenden Tumoren signifikant höher als vorher. Dies weist eventuell darauf hin, dass der Verlust der VILIP-1-Expression mit zunehmender Malignität wie der Fähigkeit zur lymphatischen Metastasierung einhergeht. Abb. 12: Darstellung von Tumorgewebe ohne regionale Lymphknotenmetastasen (A und C) und mit regionalen Lymphknotenmetastasen (B und D) in Immunfluoreszenzfärbung (VILIP-1/grün, Ki-67/rot, DAPI/blau). 45 Abb. 13: Darstellung des prozentualen Anteils VILIP-1-negativer Tumore in Tumoren ohne regionale Lymphknotenmetastasen (N0) und in Tumoren mit regionalen Lymphknotenmetastasen (N1), p=0.009 beim Vergleich VILIP-1-positiv (=1) und VILIP-1negativ (=0) zwischen N0 und N1 im Chi-Quadrat-Test. 5.10. VILIP-1 und die Differenzierung Ein pathologisches Merkmal, welches keine eindeutige Beziehung zur VILIP-1-Expression im Chi-Quadrat-Test zeigt, ist der Grad der Differenzierung G1-G3 (p=0.131, Tabelle 6). Unter den neoplastischen Geweben befindet sich lediglich ein G1-Tumor, welcher keine VILIP1-Expression aufweist (100%). Bei den G2-Tumoren zeigen insgesamt 25 (71,4%) eine VILIP-1-Expression. Darunter befinden sich 6 (17,1%) mit einer mittleren Expression und 19 (54,3%) mit einer schwachen Expression. Bei 10 (28,6%) Tumoren findet sich keine VILIP-1-Expression. Die G3-Tumore weisen in 9 (50,0%) Fällen eine VILIP-1-Expression auf. Unter ihnen zeigen 2 (11,1%) Tumore eine mittlere und 7 (38,9%) eine schwache Expression. Neun (50,0%) Tumore exprimieren kein VILIP-1. Die mittlere prozentuale VILIP-1-Expression unter den G2-Tumoren liegt bei 15,6% und unter den G3-Tumoren bei 10,1%. Wird nur der Anteil VILIP-1-negativer Tumore zwischen G2 und G3 verglichen, so erhöht sich dieser von 28,6% unter den G2-Tumoren auf 50% unter den G3-Tumoren (Abbildung 14). 46 Abb. 14: Darstellung des prozentualen Anteils VILIP-1-negativer Tumore in G2- und G3Tumoren. 5.11. Immunfluoreszenzfärbung von Ki-67 im Normalgewebe und im Plattenepithelkarzinom des Ösophagus Eine Ki-67-Expression stellt sich in normaler Ösophagusmukosa in den basalen und parabasalen Zellen dar. Dabei beschränkt sich die Färbung auf den Bereich der Zellkerne. Das Zytoplasma und die Zellmembran hingegen weisen keine Ki-67-Expression auf. Dies entspricht der bekannten Lokalisation dieses Nicht-Histon-Proteins im Karyoplasma113. Im Tumorgewebe wird Ki-67 ebenso ausschließlich von den Zellkernen exprimiert. Im Vergleich zum Normalgewebe ist allerdings eine signifikant gesteigerte und innerhalb der soliden Tumorzellnester diffus verteilte Expression zu verzeichnen. 5.12. Vergleich der Ki-67-Expression zwischen Normal- und Tumorgewebe des Ösophagus Analog zu VILIP-1 werden auch die Ki-67 exprimierenden Zellen im Normal- und Tumorgewebe in 5 charakteristischen Regionen pro Gewebeexemplar analysiert, die entsprechenden Gesichtsfelder ausgezählt, die jeweilige Ki-67-Expression prozentual zur ausgezählten Gesamtzellzahl für jedes Gewebeexemplar errechnet und in eine starke, mittlere, schwache und fehlende Expression graduiert. 47 Dabei beträgt der Mittelwert der Ki-67-Expression im Normalgewebe 21,5% und steigt im Tumorgewebe auf 36,6% an. Über den Mann-Whitney-Test (U-Test) ergibt sich ein hochsignifikanter Unterschied der mittleren prozentualen Ki-67-Expression zwischen Normalund Tumorgewebe (p<0.0001, Tabelle 7, Abbildung 15). 5.13. Ki-67 und klinisch-pathologische Charakteristika Die Mittelwerte der prozentualen Ki-67-Expression betragen 31,1% in T1, 35,9% in T2, 37,6% in T3 und 57,4% in den T4-Tumoren. Über den Kruskal-Wallis-Test ergibt sich ein signifikanter Anstieg der mittleren prozentualen Ki-67-Expression mit zunehmender Tumorgröße (T1-T4, p=0.026, Tabelle 7, Abbildung 16). Es gelingt allerdings nicht, signifikante Beziehungen zwischen der Ki-67-Expression und den klinischen Merkmalen Alter (p=0.428) und Geschlecht (p=0.989) sowie den pathologischen Merkmalen Nodalstatus (p=0.457) und Differenzierung (p=0.106) zu ermitteln (Tabelle 7). mittlere n Ki-67 Ki-67 Ki-67 gesamt positiv stark mittel schwach negativ Expression p-Wert Testverfahren Normalgewebe 24 24 0 2 22 0 21,5 Tumorgewebe 54 54 0 33 21 0 36,6 <0.0001 Mann-Whitney Alter (nur Tumorgewebe) >60 30 30 0 19 11 0 37,6 ≤ 60 24 24 0 14 10 0 35,5 0.428 Mann-Whitney Geschlecht (nur Tumorgewebe) Männer 48 48 0 30 18 0 36,7 Frauen 6 6 0 3 3 0 36,2 0.989 Mann-Whitney T Stadium T1 15 15 0 7 8 0 31,1 T2 8 8 0 4 4 0 35,9 T3 28 28 0 19 9 0 37,6 T4 3 3 0 3 0 0 57,4 0.026 Kruskal-Wallis Nodalstadium N0 26 26 0 16 10 0 34,9 N1 28 28 0 17 11 0 38,3 0.457 Mann-Whitney Differenzierung G1 1 1 0 1 0 0 39,4 G2 35 35 0 18 17 0 34,3 G3 18 18 0 14 4 0 41 0.106 Kruskal-Wallis Tab. 7: Ki-67-Expression im Vergleich mit Charakteristiken der Patienten und klinischpathologischen Daten. 48 Abb. 15: Darstellung der signifikant zunehmenden mittleren prozentualen Ki-67Expression im Vergleich zwischen Normal- und Tumorgewebe als Boxplot, p< 0.0001 im Mann-Whitney-Test/U-Test. Abb. 16: Darstellung der signifikant zunehmenden mittleren prozentualen Ki-67Expression mit Zunahme der Tumorgröße als Boxplot, p= 0.026 im Kruskal-Wallis-Test. 49 5.14. Immunfluoreszenz-Doppelfärbung der VILIP-1- und Ki-67-Expression Tumorsuppressoren sind unter anderem an der Regulation der Proliferation beteiligt. Deswegen ist die Beziehung zwischen VILIP-1 und dem Proliferationsmarker Ki-67 analysiert worden. Um die Frage zu beantworten, ob die Abnahme der VILIP-1-Expression im Plattenepithelkarzinom des Ösophagus mit einer Zunahme der Proliferationsrate der Tumorzellen korreliert, wird eine Doppelfärbung von VILIP-1 und Ki-67 durchgeführt (Abbildung 17). Anschließend wird der prozentuale Anteil an VILIP-1-positiven Zellen in heterogen gefärbten Tumorzellnestern mit dem prozentualen Anteil an Ki-67-positiven Zellen (Ki-67-Färbeindex) in Beziehung gesetzt. Vergleicht man die nach dem prozentualen Anteil VILIP-1-positiver Zellen (33-66%=mittlere Expression, 1-33%=schwache Expression, 0%=fehlende Expression) eingeteilten Tumorzellnester bezüglich ihrer mittleren prozentualen Ki-67-Expression, kann keine signifikante Beziehung zwischen der VILIP-1-Expression und der durch die Ki-67-Färbung dargestellten Proliferationsrate bestätigt werden. Es zeigt sich lediglich ein Trend, dass in Tumorzellnestern ohne VILIP-1-Expression die Expression von Ki-67 im Vergleich zu den Tumorzellnestern mit mittlerer VILIP-1-Expression gesteigert ist (Abbildung 18). Zusammenfassend geht demnach die Abnahme der VILIP-1-Expression mit einer leichten, aber nicht signifikanten Zunahme der Ki-67-Expression und damit der proliferativen Kapazität einher. 50 Abb. 17: Immunfluoreszenzfärbung von VILIP-1 (grün), Ki-67 (rot) und DAPI (blau) in soliden Tumorzellnestern ösophagealer Plattenepithelkarzinome. Abb. 18: Darstellung der nichtsignifikant unterschiedlichen mittleren prozentualen Ki-67Expression in soliden Tumorzellnestern in Abhängigkeit vom Ausmaß der VILIP-1Expression. Die Standardabweichung ist in Form der Fehlerbalken aufgeführt. 51 6. Diskussion Die Bedeutung von VILIP-1 als Tumorinvasions-Suppressorprotein ist bereits in murinen Zelllinien und Tumoren beschrieben worden. Nun sollen diese Beobachtungen auch an humanen Normal- und Tumorgeweben überprüft werden. Als Paradigma wird das Plattenepithelkarzinom des Ösophagus ausgewählt. Das ösophageale Plattenepithelkarzinom gehört zu den aggressivsten Tumoren des Verdauungstraktes. Da die Diagnose meist erst in einem fortgeschrittenen Stadium gestellt wird, ist die Prognose der Patienten entsprechend schlecht und ein Großteil der Fälle bereits inoperabel. Trotz großer wissenschaftlicher und klinischer Anstrengungen, wie dem Einsatz aggressiver, multimodaler Therapiekonzepte, hat sich die Situation dieser Patienten nicht wesentlich verbessert. Weiterhin fehlen geeignete Methoden und Marker zur Frühdiagnose und Abschätzung des Risikos beziehungsweise der Prognose sowie der Chemosensibilität und Radiosensibilität. Jenes verdeutlicht die immense Bedeutung weiterer Forschung zu molekularen Einflussfaktoren und den beteiligten Signalwegen. Dies ist die erste Studie, welche eine VILIP-1-Expression im ösophagealen Normalgewebe und Plattenepithelkarzinom des Ösophagus beschreibt und Beziehungen zu klinisch-pathologischen Daten sowie zur proliferativen Kapazität eines Tumors untersucht. VILIP-1 wird als neuronales Kalzium-Sensor-Protein hauptsächlich im zentralen Nervensystem exprimiert108. Erst kürzlich ist eine Expression von VILIP-1 in Geweben außerhalb des ZNS nachgewiesen worden. Über Western Blot-Analysen kann VILIP-1 in humanem Gewebe hauptsächlich im Myokard, Leber, Lunge, Hoden und Ovarien dargestellt werden109. Neben Untersuchungen zur VILIP-1-Expression in Normalgeweben sind bereits Studien zum Verhalten von VILIP-1 in neoplastischen Zellen erfolgt. Es ist die Bedeutung von VILIP-1 für das Wachstum und die Invasivität von murinen Plattenepithelkarzinomzellen der Haut untersucht worden. Dabei ist festgestellt worden, dass VILIP-1, möglicherweise über eine verstärkte Konzentration von cAMP sowie eine verminderte Aktivität von MMP-9 und RhoA, die Invasivität der neoplastischen Zellen reduziert. Die Inhibition der Migration wird des weiteren vermutlich über eine Herabregulation von Fibronectin vermittelt. Ein Verlust der VILIP-1Expression unterstützt demnach die in vivo und in vitro Invasivität von murinen Plattenepithelkarzinomen125,126. Die Ergebnisse implizieren möglicherweise, dass VILIP-1 das Tumorwachstum inhibiert. Somit ließe sich vermuten, dass der Verlust der VILIP-1-Expression den Übergang in die Malignität 52 erleichtern beziehungsweise die Karzinogenese beschleunigen könnte. Diese Hypothese kann nun durch die Ergebnisse unserer Studie zusätzlich unterstützt werden. 6.1. VILIP-1 im ösophagealen Normalgewebe Sowohl in den immunhistochemischen Avidin-Biotinyl-Peroxidase-Komplex-Färbungen als auch in den Immunfluoreszenzuntersuchungen zeigt sich in allen untersuchten ösophagealen Normalgeweben eine VILIP-1-Expression. VILIP-1 wird dabei vorwiegend intrazellulär exprimiert. Vereinzelte extrazellulär fluoreszierende Signale werden durch Vergleich mit den Negativkontrollen als unspezifische Anfärbungen der extrazellulären Bindegewebsmatrix interpretiert. VILIP-1 wird demnach nicht nur im zentralen Nervensystem108 beziehungsweise in weiteren Organen wie Herzmuskel, Leber, Ovarien und Hoden109 exprimiert, sondern auch, wie bislang nicht bekannt, von humanen Plattenepithelien des Ösophagus. Dass VILIP-1 in sehr verschiedenen Zellpopulationen exprimiert wird, lässt eine grundlegende Funktion im physiologischen Zellmetabolismus vermuten. Im Vergleich zu VILIP-1, welches intrazellulär exprimiert wird, sind die ebenfalls zur Superfamilie der EF-Hand-Proteine gehörenden S100-Proteine intrazellulär und extrazellulär zu finden77. Das Kalziumbindungsprotein S100 A2 wird in der Ösophagusmukosa hauptsächlich von Zellen des oberen Stratum spinosum und des unteren Stratum corneum exprimiert. Zellen des unteren Stratum spinosum und die Basalzellschicht zeigen keine S100 A2-Expression134. Die VILIP-1-Expression verhält sich überraschenderweise umgekehrt dazu. In dieser Studie kann eine VILIP-1-Expression vornehmlich in den basalen und parabasalen Zellschichten der normalen Ösophagusmukosa beobachtet werden. Die inverse Expression von VILIP-1 und S100 A2 im normalen Ösophagusgewebe lässt eine differente Funktion bei der physiologischen Ausreifung beziehungsweise der Differenzierung der Zellen annehmen. 6.2. VILIP-1 im ösophagealen Plattenepithelkarzinom Im Vergleich zu normaler Ösophagusmukosa zeigt das ösophageale Plattenepithelkarzinom eine signifikante Reduktion der VILIP-1-Expression (p=0.001 im Chi-Quadrat-Test). Während im neoplastischen Ösophagusgewebe die VILIP-1-Expression deutlich 53 herunterreguliert ist oder vollständig verloren geht, stellt sich in allen untersuchten normalen Plattenepithelien eine intensive Expression in basalen und parabasalen Zellschichten dar. Dies könnte bedeuten, dass VILIP-1 im Zellmetabolismus des normalen Ösophagusgewebes eine Funktion im Rahmen der Differenzierung sowie der regulierten Proliferation und somit der Regeneration innehat. Während der malignen Kaskade, wenn die Zellen zunehmend ihre Differenzierung beziehungsweise die Integrität des Zellverbandes verlieren und unkontrolliert proliferieren, geht die VILIP-1-Expression verloren. Möglicherweise ist der Verlust der VILIP1-Expression ein entscheidender Moment im Ablauf der malignen Kaskade. Diese Hypothese kann zusätzlich durch die Untersuchung der VILIP-1-Expression in Bezug zu klinisch-pathologischen Merkmalen der Karzinome unterstützt werden. 6.2.1. VILIP-1 und klinisch-pathologische Charakteristika Die Analyse der VILIP-1-Expression in Beziehung zur Tumorgröße (T1-T4) zeigt im ChiQuadrat-Test eine signifikante Zunahme der Anzahl VILIP-1-negativer Tumore mit zunehmender Tumorgröße (p=0.012 im Chi-Qiuadrat-Test). Unter den T1/T2-Tumoren sind nur 0-20% der Tumore VILIP-1-negativ und unter den T3/T4-Tumoren bereits 53,6% beziehungsweise 66,7%. Vergleicht man jedoch die mittlere prozentuale VILIP-1-Expression zwischen T1, T2, T3 und T4 im Kruskal-Wallis-Test, so wird eine Signifikanzebene nicht erreicht. Es zeigt sich lediglich tendenziell eine Reduktion der mittleren prozentualen VILIP-1-Expression von T1 zu T4. Allerdings sind die Mittelwerte aufgrund eines sehr hohen Anteils an VILIP-1-negativen Tumoren und der hohen Streubreite schwer verwertbar. Dieser Zusammenhang sollte an einer größeren Stichprobe und unter Verwendung weiterer Methoden zur Absicherung des Ergebnisses überprüft werden. Nachgewiesen ist jedoch die im Chi-Quadrat-Test signifikante Zunahme der Anzahl VILIP-1negativer Tumore mit zunehmender Tumorgröße. Dies könnte ein Hinweis darauf sein, dass VILIP-1 möglicherweise das Wachstum der Tumore hemmt beziehungsweise erst durch den Verlust von VILIP-1 ein verstärktes Tumorwachstum möglich ist. Die Vermutung, dass VILIP-1 die invasiven Fähigkeiten von neoplastischen Zellen hemmt, wird unterstützt durch die Beziehung zwischen VILIP-1-Expression und regionaler Lymphknotenmetastasierung des Tumors. Unter den N1-Tumoren befindet sich eine signifikant höhere Anzahl an VILIP-1-negativen Tumoren als unter den N0-Tumoren (p=0.009 im Chi- 54 Quadrat-Test). Es ist zu vermuten, dass VILIP-1 bedeutend für den Erhalt der Integrität des Zellverbandes ist. Mit dem Verlust von VILIP-1 sind die Zellen möglicherweise fähig, sich aus dem Zellverband zu lösen und zu migrieren, beispielsweise in umgebende Lymphknoten. Als möglicher Mechanismus ist für VILIP-1 in murinen Plattenepithelkarzinomzellen bereits eine hemmende Funktion auf Migration und Zelladhäsion über eine verminderte Expression der Fibronectinrezeptoren beobachtet worden. Zellen mit vermehrter VILIP-1-Expression zeigen verminderte migratorische Fähigkeiten und eine verminderte Zelladhäsion über Fibronectin126. Insgesamt bestätigen die Resultate die Beobachtungen aus vorausgegangenen Experimenten. Dort ist bereits eine Bedeutung von VILIP-1 als Tumorinvasionssuppressor vermutet worden. In diesen Experimenten ist dargestellt worden, dass eine Überexpression von VILIP-1 zu einer cAMP-vermittelten Abnahme von in vivo und in vitro Wachstum und Invasivität von Plattenepithelkarzinomzellen der Maus125 führt. Ein hohes Niveau der VILIP-1-Expression findet sich in weniger aggressiven Tumoren, wohingegen in invasiven Tumoren die VILIP-1Expression signifikant abnimmt oder vollkommen verloren geht125,126. In einer weiteren Studie ist in Zellkulturexperimenten zu nichtkleinzelligen Lungenkarzinomen (NSCLC) ein Verlust beziehungsweise eine niedrige Expression von VILIP-1 in 11 von 12 Zelllinien über Western Blot-Analysen nachgewiesen worden. Im Gegensatz dazu zeigt sich eine signifikant stärkere Expression in normalen bronchialen Epithelien138. Dies ist vergleichbar mit den Ergebnissen dieser Untersuchung zum ösophagealen Plattenepithelkarzinom und ein weiterer Hinweis auf einen Verlust der VILIP-1-Expression und seine mögliche Funktion als Tumorsuppressor im Rahmen der malignen Transformation verschiedener Zelltypen. 6.2.2. VILIP-1 im Vergleich zu anderen Kalziumbindungsproteinen Neben VILIP-1 ist bereits für weitere Kalziumbindungsproteine wie die der Annexin-Familie und den S100-Proteinen eine Bedeutung im Rahmen der Karzinogenese festgestellt worden. Durch den Vergleich mit anderen Kalziumbindungsproteinen lassen sich möglicherweise Rückschlüsse auf die Funktion und Bedeutung von VILIP-1 in neoplastischen Zellen ziehen. 55 6.2.2.1. VILIP-1 und die Kalziumbindungsproteine der Annexin-Familie Vergleichbar mit der Regulation von VILIP-1 ist die der Kalziumbindungsproteine Annexin-1 und -2. Für drei Annexin-1-Isoformen kann im Plattenepithelkarzinom des Ösophagus eine Herabregulation nachgewiesen werden127. Dies ist vergleichbar mit der reduzierten beziehungsweise fehlenden VILIP-1-Expression in den von uns untersuchten Ösophaguskarzinomen. Es zeigt sich weiterhin eine deutlich verminderte Expression von Annexin-1 mit dem Verlust der Differenzierung des Ösophaguskarzinoms128. In einer anderen Studie wird die Expression von Annexin-2 auf mRNA- und Proteinebene mittels RT-PCR und immunhistochemischen Methoden im Normalgewebe und Plattenepithelkarzinom des Ösophagus analysiert. Dabei stellt sich auf beiden Ebenen eine signifikant niedrigere Expression von Annexin-2 im Tumorgewebe heraus. Auch hier lassen sich Parallelen zur Reduktion der VILIP-1-Expression im Ösophaguskarzinom finden. Außerdem ist die Annexin-2-Expression in gering differenziertem Tumorgewebe signifikant niedriger als in gut differenziertem Gewebe127,129. Eine Beziehung zur Differenzierung ist für VILIP-1 in unserer Studie nicht bestätigt worden. Es kann kein signifikanter Zusammenhang zwischen dem G-Stadium des Tumors und der VILIP-1Expression dargestellt werden, wenn auch der Anteil an VILIP-1-negativen Tumoren von 28,6% in G2 auf 50,0% in G3 ansteigt. Die Aussagekraft dieser Beobachtung ist möglicherweise eingeschränkt durch die Tatsache, dass es in der Gruppe der G1-Tumore lediglich einen Fall gibt. Vielleicht wäre eine Abhängigkeit mit einer größeren Fallzahl in dieser Gruppe darstellbar gewesen. Über indirekte Immunfluoreszenz ist eine Translokation von Annexin-1 im Verlauf der Tumorgenese des Plattenepithelkarzinoms des Ösophagus nachgewiesen worden. Während es in normalem Ösophagusgewebe vorwiegend in der Zellmembran, im Zytoplasma und im Zellkern lokalisiert ist, nimmt seine Expression im Tumorgewebe und in den Tumorzelllinien drastisch ab und es zeigt sich eine vorher nicht beobachtete starke Expression in der Kernmembran130. Dies spricht für einen Zusammenhang zwischen der Translokation von Annexin-1 und der Tumorgenese des Ösophaguskarzinoms. Die für Annexin-1 beobachtete Translokation in neoplastischen Zellen könnte ebenfalls für VILIP-1 bedeutsam sein. Die Funktion von VILIP-1 und damit der Verlauf einer Tumorerkrankung könnten davon abhängig sein, in welchem intrazellulären Kompartiment VILIP-1 exprimiert wird. Vielleicht ist auch dadurch die fehlende 56 Beziehung zur Differenzierung der Tumore zu erklären. Möglicherweise hat in fortgeschrittenen Tumorstadien eine Translokation von VILIP-1 stattgefunden. Das könnte bedeuteten, dass bei gleichbleibender Expression das Protein seine Funktion als Tumorsuppressor nicht mehr ausüben kann. Eine Translokation ist für VILIP-1 in ösophagealen neoplastischen Zellen allerdings bisher noch nicht beschrieben worden. Es ist jedoch eine über die Myristoylierung vermittelte kalziumabhängige Translokation von VILIP-1 zwischen Zytosol und Membranoberflächen wie dem Golgi-Apparat nachgewiesen worden110. Um die Frage der Translokation näher zu klären, sind beteiligte Transportmechanismen zwischen der Zellmembran, dem Zytoplasma und dem Golgi-Apparat in neoplastischen Zellen weiter zu analysieren. Da die Annexine wie auch VILIP-1 bedeutend für die Funktion des Zytoskeletts und darüber hinaus für die Endozytose und Zell-Zell-Verbindungen sind, könnte man eine vergleichbare Rolle dieser Kalziumbindungsproteine im Rahmen der malignen Kaskade annehmen. Annexin-1 und -2 beispielsweise binden F-actin (filamentöse Form der Aktinfilamente) und modulieren dadurch Zytoskelett-Verbindungen der Zellmembran131. Annexin-1 ist unter anderem an der Signaltransduktion der EGF-Rezeptor-Tyrosin-Kinase sowie der Proteinkinase C beteiligt. Über die Bindung an die EGF-Rezeptor-Tyrosin-Kinase erfolgt die Inhibition EGF-vermittelter Proliferation. Die über diesen Mechanismus ausgeübte antiproliferative Aktivität des Annexin-1 erklärt möglicherweise den Verlust der Annexin-1Expression im Ösophagus- und Prostatakarzinom, wo es zur Herabregulation mehrerer antiproliferativer und proapoptotischer Proteine kommt131. Ähnlich zu VILIP-1 gibt es allerdings auch beim Annexin-1 Tumortypen, in denen eine verstärkte Expression beobachtet werden konnte. Dazu gehören das Mammakarzinom und das Pankreaskarzinom132. Die Bedeutung dieser differenten Regulation der Kalziumbindungsproteine in unterschiedlichen Tumortypen bleibt bislang unklar. Vergleichbar mit Annexin-1 und Annexin-3 konnte VILIP-1 in den ß-Zellen des Pankreas nachgewiesen werden. Für Annexin-1 und Annexin-3 ist eine kalziumabhängige Induktion der Insulinsekretion beobachtet worden131. Eine vermehrte VILIP-1-Expression in ß-Zellen des Pankreas führt ebenfalls zu einer verstärkten Insulinsekretion133. Dies ist ein weiterer Hinweis darauf, dass für VILIP-1 und einzelne Annexine ähnliche Signaltransduktionswege bestehen könnten. 57 6.2.2.2. VILIP-1 und die S100-Kalziumbindungsproteine Für das Kalziumbindungsprotein S100 A2 sind in vorausgegangenen Studien ähnliche und gegensätzliche Beobachtungen zur VILIP-1-Expression gemacht worden. S100 A2 wird in normalen Epithelien stabil exprimiert. Im Rahmen der Tumorgenese kommt es wie bei VILIP-1 zu einer Reduktion seiner Expression. Dies zeigt sich für neoplastische Zellen des Mammakarzinoms und des ösophagealen Plattenepithelkarzinoms. Im Gegensatz zur VILIP-1-Regulation findet sich für S100 A2 in einer Studie an 116 Plattenepithelkarzinomen des Ösophagus eine Herabregulation der Expression in den frühen Stadien des Tumors (T1a und T1b), in den T2-Tumoren bleibt die Expression dann niedrig und wird während des Übergangs vom T2- zum T3-Stadium mit zunehmender Größe des Tumors vor allem in gut differenzierten großen Karzinomen wieder heraufreguliert134. Bei VILIP-1 hingegen findet sich in unserer Studie eine Zunahme der Anzahl VILIP-1-negativer Tumore mit zunehmender Tumorgröße und somit eine Herabregulation in den fortgeschrittenen Stadien. Gene des Tumorsuppressors p53 und die EGF-Rezeptor-Familie beeinflussen die S100 A2Expression135. Deren Dysregulation könnte zur Initiation einer verstärkten S100 A2-Expression in fortgeschrittenen Tumoren führen. Auch für VILIP-1 ist eine Regulation über EGF nachgewiesen worden. In SCC (squamous cell carcinoma)-Zelllinien erfolgt allerdings eine Reduktion von VILIP-1 nach Zugabe von EGF (Manuskript in Vorbereitung, Schönrath et al.). Ein weiteres Mitglied der S100-Kalziumbindungsproteine ist das S100 A4, welches im Verlauf der Tumorgenese verstärkt exprimiert wird und als Vermittler der Metastasierung diskutiert wird. S100 A4 hemmt in vitro die Proteinkinase C-abhängige Phosphorylierung des Tumorsuppressors p53. Man nimmt an, dass diese Fähigkeit in einen invasiveren Phänotyp resultiert136. Weiterhin führt S100 A4 zu einer Aktivierung der Transkription der MMP-13 und folglich zu einem vermehrten Abbau der extrazellulären Matrix. Auch damit erklärt sich eventuell der fördernde Einfluss von S100 A4 auf die Metastasierung137. Im Gegensatz dazu übt VILIP-1 über eine Induktion von cAMP eine inhibitorische Wirkung auf die Expression von MMP-9 aus125. Dieser Mechanismus führt vermutlich zu einem verminderten Abbau der extrazellulären Matrix und somit zu einer Reduktion der migratorischen Kapazität von neoplastischen Zellen. Durch Herabregulation beziehungsweise Inaktivierung von VILIP-1 könnte es über eine gesteigerte Aktivität der MMP-9 schließlich zu einem vermehrten Abbau der extrazellulären Matrix und zur Metastasierung in regionale Lymphknoten kommen. 58 Dies würde den signifikant höheren Anteil an VILIP-1-negativen Tumoren unter den N1Tumoren im Vergleich zu den N0-Tumoren erklären. Insgesamt sind bei den Proteinen der S100-Familie in den verschiedenen Tumortypen sehr unterschiedliche Beobachtungen gemacht worden. Ein ähnliches Phänomen könnte auch in der Familie der neuronalen Kalzium-Sensor-Proteine (NCS-Proteine) auftreten. Deswegen sollte man neben VILIP-1 auch das Verhalten weiterer NCS-Proteine analysieren und untereinander vergleichen. 6.2.3. VILIP-1 und die Regulation der Genexpression und Signaltransduktion Als wichtiger Baustein zur Klärung der Regulation der Genexpression von VILIP-1 ist kürzlich ein potentieller VILIP-1-Promotor gefunden worden. Es handelt sich dabei um eine DNASequenz, welche ungefähr 2 kb oberhalb des ersten VILIP-1-Exons liegt. Es sind fünf Polymorphismen, welche allerdings nicht mit der VILIP-1-Expression korrelieren, beschrieben worden138. Die Regulation der VILIP-1-Transkription in NSCLC-Zelllinien erfolgt unter anderem mittels verstärkter Methylierung des Promotors. Über die verstärkte Methylierung kommt es zu einer Suppression der Transkription des VILIP-1-Gens. Dies wird vermutlich über eine Beeinträchtigung der Bindung der Transkriptionsfaktoren Sp-1/Sp-3 und/oder NRF-1 vermittelt. Außerdem wird VILIP-1 über eine posttranskriptionelle Modifikation des N-terminalen Endes der Histone reguliert. Eine Hemmung der Transkription erfolgt beispielsweise über eine Deazetylierung von Lysin 9 und 14 sowie Methylierung von Lysin 9 in Histon H3. Im Gegensatz dazu erfolgt eine Aktivierung der Transkription über verstärkte Azetylierung der Histone H3 und H4 sowie Methylierung von Lysin 4 in Histon H3. Vermittelt wird dies über HistonAzetyltransferasen und Histon-Deazetylasen. Es handelt sich dabei um epigenetische Mechanismen. Genetische Mechanismen wie beispielsweise Mutationen eines der vier VILIP-1Exons sowie der Promotorregion sind in den untersuchten Bronchialkarzinomzelllinien an der Regulation der VILIP-1-Expression nicht beteiligt gewesen. Diese Formen der Regulation sind ebenso für das Ösophaguskarzinom zu vermuten. Möglicherweise kommt es während des Fortschreitens der malignen Kaskade zu einer Inhibition der VILIP-1-Genexpression über verstärkte Methylierung des Promotors oder Modifizierung der Histone. Dies sollte in Zellkulturexperimenten weiter untersucht werden. 59 Wachstumsfaktoren, welche die Genexpression von VILIP-1 regulieren, könnten beispielsweise zur Familie der EGF (epidermal growth factor) und ihren Rezeptoren gehören. Tatsächlich ist kürzlich eine Reduktion der VILIP-1-Expression in SCC-Zelllinien nach EGF-Gabe gezeigt worden (Manuskript in Vorbereitung, Schönrath et al.). Dieser Regulationsmechanismus könnte ebenso in ösophagealen Zellen von Bedeutung sein. Möglicherweise kommt es zu einer verminderten VILIP-1-Expression von T1 zu T4 oder N0 zu N1, wenn über EGF die VILIP-1Genexpression inhibiert wird. In vorausgegangenen Studien ist gezeigt worden, dass eine Blockade der EGF-Rezeptoren mit einem monoklonalen Anti-ErbB-2-Antikörper eine Hemmung des in vitro und in vivo Wachstums von mehreren humanen Karzinomzelllinien bewirken kann139. Über spezifische Chemotherapeutika wie die Tyrosin-Kinase-Inhibitoren können solche Wachstumsfaktoren/rezeptoren und somit möglicherweise auch die Regulation von VILIP-1 manipuliert werden. Interessant wäre eine Analyse der Wirkung dieser Inhibitoren auf die Genexpression von VILIP-1 in ösophagealen Zellen. Wie bereits gezeigt werden konnte, führt eine Überexpression von VILIP-1 via Stimulation der Adenylatzyklase zu einer verstärkten cAMP-Synthese und dies wiederum über die Stimulation der Proteinkinase A (PKA) zur Phosphorylierung und somit Inaktivierung des kleinen GTPbindenden Proteins RhoA125, eines entscheidenden Regulators des Zytoskeletts. Eine Inaktivierung von RhoA führt zu einer Verminderung der invasiven Eigenschaften. In mit VILIP-1-cDNA transfizierten Zellen wurde ebenfalls cAMP-vermittelt eine reduzierte Aktivität der MMP-9 und damit eine geringere Fähigkeit der Zellen zum Abbau der extrazellulären Matrix gefunden125. Über diese Wege der Signaltransduktion ist demnach eine Reduktion der invasiven Kapazität von Tumoren durch den Tumorinvasionssuppressor VILIP-1 denkbar (Abbildung 19). Demnach können Tumore, welche verstärkt VILIP-1 exprimieren, durch eine geringere Aktivität von RhoA und MMP-9 die extrazelluläre Matrix nicht oder nur in geringerem Maße abbauen. Dies beeinträchtigt dann möglicherweise das Wachstum des Tumors sowie auch die Fähigkeit zur Metastasierung. Im Gegensatz dazu führt ein Verlust der VILIP-1-Expression zu einer verstärkten RhoA- und MMP-9-Aktivität und könnte somit zu Tumorinvasion und Metastasierung beitragen125,126. Dies sind mögliche Mechanismen, die den von uns nachgewiesenen, signifikant erhöhten Anteil an VILIP-1-negativen Geweben im Ösophaguskarzinom im Vergleich zum Normalgewebe, die 60 signifikant erhöhte Anzahl an VILIP-1-negativen Tumoren unter den N1-Tumoren und die hohe Anzahl an VILIP-1-negativen Tumoren unter den T3/T4-Tumoren erklären würden. Die maligne Transformation der Zellen, das Tumorwachstum sowie die Fähigkeit zur Metastasierung werden möglicherweise durch die Reduktion beziehungsweise den Verlust der VILIP-1-Expression erleichtert. Daran könnte eine Regulation der Signaltransduktion über cAMP und die Proteinkinase A beteiligt sein. Eine vermehrte cAMP-Konzentration infolge einer verstärkten VILIP-1-Expression ist bereits in verschiedenen Zelltypen nachgewiesen worden. Dazu gehören C6-Glioma-Zelllinien110, humane embryonale Nierenzellen140, ß-Zellen des Pankreas133 und Zelllinien dermaler Karzinome125. Eine Verbindung zwischen den Metalloproteinasen und Rho ist durch die Analyse des IntegrinFAK-Signalwegs untersucht worden141. Die Aktivität von Rho und ROCK (Rho-associated coiled-coil forming protein) ist für die Organisation der Integrine zur Adhäsion erforderlich142. Rho-Proteine können den Abbau und Umbau der extrazellulären Matrix regulieren. Dies geschieht durch Modulation der Matrix-Metalloproteinasen (MMP), die zum Abbau der extrazellulären Matrix beitragen, oder durch deren Antagonisten, die Gewebeinhibitoren der Metalloproteinasen (TIMP/ tissue inhibitors of metalloproteinase)143. Ein Übergewicht in der Aktivität der MMP gegenüber TIMP führt dementsprechend zu einem beträchtlichen Abbau der extrazellulären Matrix, was bedeutend für die Invasivität und Metastasierung eines Tumors ist144,145. Die Expression von MMP-1 und MMP-9 ist im Ösophaguskarzinom bereits untersucht worden und es ist ein Zusammenhang mit einer ungünstigeren Prognose gefunden worden146. 61 Abb. 19: Darstellung eines Signaltransduktionsweges für VILIP-1. 6.2.4. VILIP-1 und die Proliferation Zur Analyse der Beziehung zwischen VILIP-1 und der proliferativen Kapazität von Zellen ist eine Doppelfärbung mit dem Proliferationsmarker Ki-67 durchgeführt worden. Ki-67 wird bis auf G0 in allen Phasen des Zellzyklus exprimiert und kann somit die Population sich teilender Zellen darstellen113. Im Ösophagus wird Ki-67 von mitotisch aktiven Stammzellen des Stratum basale und ihren proliferierenden Tochterzellen exprimiert. Im normalen Plattenepithel des Ösophagus ist diese Expression auf 1 bis 3 Zellschichten innerhalb und oberhalb des Stratum basale begrenzt. Diese Zellen differenzieren schließlich in nichtproliferierende Epithelzellen aus, verlieren die Fähigkeit zur Ki-67-Expression und migrieren innerhalb von ungefähr 7,5 Tagen an die Oberfläche147. Aberrante beziehungsweise verstärkte Ki-67-Expression ist dementsprechend ein Hinweis auf eine Störung der normalen Ausreifung der Zellen. Eine VILIP-1-Expression ist ebenfalls überwiegend in basalen und parabasalen Zellen beobachtet worden. Allerdings exprimiert nur ein Teil dieser Zellen auch gleichzeitig Ki-67. Während die Fähigkeit zur VILIP-1-Expression ebenfalls während der Migration zur mukosalen Oberfläche verloren geht, wird es dennoch sowohl von basal proliferierenden als auch von nicht proliferierenden, ruhenden Zellen exprimiert. Dies ist ein Hinweis darauf, dass die Fähigkeit einer Zelle zur Expression von VILIP-1 nicht von der Phase des Zellzyklus abhängt. Die 62 Fähigkeit einer Zelle zur VILIP-1-Expression ist demnach im Normalgewebe bei physiologischem Zellmetabolismus unabhängig von der proliferativen Kapazität. Anzumerken ist allerdings, dass die Expression allein keine Aussage zur Funktion erlaubt. Das bedeutet, dass VILIP-1 trotz nachgewiesener Expression in bestimmten Phasen des Zellzyklus auch in einer inaktiven Form vorliegen kann. Der Ki-67-Färbeindex ist im Tumorgewebe verglichen mit dem Normalgewebe aufgrund der erhöhten Proliferationsrate deutlich verstärkt (p<0.0001 im Mann-Whitney-Test), wohingegen die VILIP-1-Expression im Tumorgewebe herunter reguliert wird oder in 37% der Fälle vollständig verloren geht (p=0.001 im Chi-Quadrat-Test). Es zeigt sich somit ein signifikanter Verlust der VILIP-1-Expression beziehungsweise eine hochsignifikante Zunahme der Ki-67Expression im Tumorgewebe. Diese Ergebnisse deuten auf den ersten Blick auf eine inverse Beziehung zwischen der Expression von Ki-67 und VILIP-1 hin. Das ließe einen Verlust von VILIP-1 im Rahmen der gesteigerten proliferativen Kapazität vermuten. Um nun herauszufinden, ob die VILIP-1Expression wirklich mit der Proliferation korreliert, werden die Unterschiede innerhalb solider Tumorzellnester untersucht. Die Beobachtung, dass innerhalb eines Tumorgewebes die Intensität der VILIP-1-Expression sehr variieren kann, müsste unter dieser Voraussetzung mit dem Nachweis einer inversen Beziehung zur Ki-67-Expression einhergehen. Es zeigt sich jedoch, dass die Ki-67-Expression trotz variierender VILIP-1-Expression annähernd konstant bleibt und dass somit die Proliferation wahrscheinlich unabhängig von der VILIP-1-Expression ist. Es finden sich neben VILIP-1/Ki-67 doppelt exprimierenden Zellen ebenso Ki-67 und VILIP-1 unabhängig voneinander exprimierende Zellen. Tendenziell ist die Expression von Ki-67 in VILIP-1-negativen Tumorzellnestern etwas stärker als in Tumorgewebe mit VILIP-1-Expression (Abbildung 18). Möglicherweise würde sich diese nichtsignifikante Beobachtung an einer größeren Stichprobe bestätigen lassen. Das würde bedeuten, dass VILIP-1 an der Hemmung der Proliferation beteiligt ist und dass somit VILIP-1-positive Tumore eine geringere Proliferationsrate haben. In der Praxis könnte dies Rückschlüsse auf den Krankheitsprogress und die Prognose ermöglichen. Für Tumore mit einer hohen VILIP-1Expression könnte eine günstigere Prognose angenommen werden. Umgekehrt wäre bei Tumoren mit einer niedrigen VILIP-1-Expression eine hohe Proliferationsrate und somit einerseits eine schlechtere Prognose, andererseits aber eventuell eine höhere Chemosensibilität und Strahlensensibilität zu vermuten. 63 6.2.5. VILIP-1 und die Differenzierung Für VILIP-1 ist in C6-Glioma-Zelllinien ein stimulierender Effekt auf die intrazelluläre cAMPKonzentration und die Expression des GFRP (glial fibrillary acidic protein) gezeigt worden. Das cAMP fördert dabei die zelluläre Differenzierung110. Die cAMP-abhängige Wirkung auf die Differenzierung könnte ebenso in neoplastischen Plattenepithelien von entscheidender Bedeutung sein. Denkbar wäre ein stimulierender Effekt von VILIP-1 auf die Ausdifferenzierung der Zellen über cAMP. Eine verminderte VILIP-1Expression könnte somit zur Entdifferenzierung und zur Entwicklung eines aggressiven Phänotyps führen. Diese Zellen wären dann in der Lage, umgebende Gewebe zu infiltrieren und Lymphknotenmetastasen zu bilden. Eine signifikante Beziehung zwischen der VILIP-1-Expression und dem Grad der Tumordifferenzierung (G1-G3) ist in dieser Untersuchung allerdings nicht nachweisbar gewesen (p=0.131 im Chi-Quadrat-Test). Dies könnte einerseits mit der niedrigen Fallzahl (nur ein Tumor im G1-Stadium) und andererseits auch mit der Aktivität von VILIP-1 zusammenhängen. Möglicherweise liegt VILIP-1 bei den entdifferenzierten Tumoren im Stadium G3 in einer inaktiven Form vor. Für einen möglichen Einfluss von VILIP-1 auf die Differenzierung spricht immerhin die Beobachtung, dass der Anteil an VILIP-1-negativen Tumoren von G2 (28,6%) zu G3 (50%) zunimmt (Abbildung 14). Auf molekularer Ebene sollten diese Vermutung sowie die beteiligten Signaltransduktionswege über VILIP-1 und cAMP auch in neoplastischen Zellen weiter untersucht werden. 6.3. Die Rolle von Ki-67 im ösophagealen Gewebe Wie erwartet zeigt sich eine hochsignifikant gesteigerte Expression des Proliferationsmarkers Ki-67 im neoplastischen Gewebe verglichen mit der Ki-67-Expression im Normalgewebe (p<0.0001 im Mann-Whitney-Test). Ebenso wie im Normalgewebe beschränkt sich diese Expression auf den Zellkern. Auffällig ist eine wesentlich diffusere Verteilung der Ki-67positiven Zellen. Während sich die Ki-67-Expression in der gesunden Ösophagusmukosa noch auf die basalen und parabasalen Zellschichten beschränkt, zeigt sich in den Tumorzellnestern eine ungeordnete, gesteigerte Ki-67-Expression. Dieses Verhalten von Ki-67 entspricht den Beobachtungen aus einer anderen Studie mit Ki-67 an ösophagealen Plattenepithelkarzinomen148. Im Gegensatz zu unserer Studie ist dort jedoch eine Beziehung zwischen Ki-67 und der 64 Differenzierung dargestellt worden. Der Ki-67-Färbeindex ist dabei in niedrig differenzierten Tumoren signifikant stärker als in gut differenzierten Tumoren. Übereinstimmend mit den Beobachtungen unserer Studie lässt sich kein Zusammenhang der Ki67-Expression mit dem Geschlecht, dem Alter und der Lymphknotenmetastasierung aufzeigen. Ein signifikanter Zusammenhang ergibt sich in unserer Studie jedoch zwischen der Ki-67Expression und der Tumorgröße (T1-T4, p=0.026 im Kruskal-Wallis-Test). Mit Zunahme der Tumorgröße nimmt auch die Ki-67-Expression zu. Dies ist verständlich, da mit vermehrter proliferativer Kapazität auch ein stärkeres Wachstum des Tumors möglich ist. Insgesamt stellt sich der Zusammenhang von Ki-67 und klinisch-pathologischen Merkmalen in Studien kontrovers dar. Einige Studien können weitere Beziehungen aufzeigen149 und andere Untersuchungen unterstützen mit ihren Resultaten unsere Beobachtungen150. 6.4. Das Verhalten von VILIP-1 in einer Auswahl weiterer Karzinome Im Gegensatz zum Verhalten von VILIP-1 im Plattenepithelkarzinom des Ösophagus scheint dieses Kalziumbindungsprotein in anderen Tumoren unterschiedlich reguliert zu werden. Ähnlich wie beim Ösophaguskarzinom erfolgt auch beim Nierenzellkarzinom in den neoplastischen Zellen eine Herabregulation von VILIP-1 im Vergleich zum Normalgewebe. Beim Kolonkarzinom, hepatozellulären Karzinom und Prostatakarzinom jedoch stellt sich eine Zunahme der VILIP-1-Expression im neoplastischen Gewebe dar. Im Plattenepithelkarzinom der Haut letztendlich bleibt die Expression verglichen mit normaler Epidermis nahezu konstant. Es finden sich demnach alle Regulationsformen der VILIP-1-Expression. Dies lässt in den verschiedenen Tumorgeweben eine unterschiedliche Rolle von VILIP-1 eventuell im Rahmen der Differenzierung oder der Proliferationskontrolle innerhalb eines komplizierten Netzwerkes aus unterschiedlichen Signaltransduktionswegen vermuten. Man sollte davon ausgehen, dass auf zellulärer Ebene zahlreiche komplex vernetzte Kaskaden bei der Initiation der Tumorgenese eine Rolle spielen und es sich nicht um lineare, gleichbleibende Informationsübertragungen handeln kann. Es wäre folglich wichtig, die Bedeutung von VILIP-1 für alle Tumortypen einzeln zu definieren. Man kann also nicht aus einer vermuteten Tumorsuppression in ösophagealen Plattenepithelkarzinomen auf eine allgemeine Tumorsuppression schließen. Die Beobachtung, dass VILIP-1 in einzelnen Tumoren unterschiedlich reguliert wird und anscheinend differente Funktionen ausübt, wird unterstützt durch Untersuchungen zu VILIP-1 an 65 hochinvasiven und niedriginvasiven humanen Neuroblastomzelllinien. Die VILIP-1-mRNA ist in hochinvasiven Neuroblastomzelllinien signifikant stärker nachweisbar als in den niedriginvasiven Zelllinien. Es ist außerdem dargestellt worden, dass sich eine Überexpression von VILIP-1 vor allem im Tumorgewebe von Patienten mit Fernmetastasen findet151. Dies steht im Gegensatz zu den Beobachtungen unserer Studie, wo sich eine signifikant erniedrigte Anzahl VILIP-1-positiver Tumore unten den lymphatisch metastasierten Ösophaguskarzinomen nachweisen lässt. Es sind also deutliche Unterschiede in der Funktion von VILIP-1 in den einzelnen Tumortypen anzunehmen. Eventuell spielt auch hierbei erneut die Aktivität beziehungsweise die Inaktivität von VILIP-1 eine Rolle. Zu diskutieren ist außerdem eine Expression in verschiedenen Kompartimenten der unterschiedlichen Zelltypen. Dies könnte eine unterschiedliche Funktion oder auch Aktivität von VILIP-1 zur Folge haben. Die Beobachtung einer differenten Expression von VILIP-1 in verschiedenen Tumortypen findet sich in ähnlicher Weise auch bei anderen Kalziumbindungsproteinen, zum Beispiel denen der S100-Familie. S100 A2 wird in Plattenepithelkarzinomen des Ösophagus sowie in Mammakarzinomen vermindert exprimiert134. Für S100 B zeigt sich in Melanomen eine verstärkte Expression, wodurch es als Tumormarker eingesetzt werden kann152. Das Protein S100 A4 wird in metastasierenden Epithelien von Nagetieren verstärkt synthetisiert. Durch die Expression von S100 A4 wird die Fähigkeit zur Metastasierung in diesen Zellen gesteigert153. Dies zeigt, dass die Mitglieder der S100-Familie vollkommen verschiedene Funktionen in den einzelnen Tumoren ausüben. Während manche eine tumorsuppressive Funktion ausüben, beschleunigen andere die Tumorprogression. Die Erkenntnis, dass die einzelnen Proteine sehr unterschiedlich reguliert werden und auch verschiedene Funktionen im Rahmen der Tumorgenese (Tumorsuppressor versus Tumorpromoter) haben, sollte beispielgebend für die Analyse der NCS-Familienmitglieder sein. Ein weiterer diesbezüglich interessanter Zusammenhang ist die Tatsache, dass S100 B, welches an der Stimulation des Neuritenwachstums, der Proliferation von Melanomzellen und der Apoptoseinduktion in PC12-Phäochromozytomzellen beteiligt ist154, abhängig von seiner zellulären Konzentration unterschiedliche Funktionen erfüllt. In nM-Konzentrationen fungiert S100 B als Faktor für Wachstum und/oder Differenzierung, während es in µM-Konzentrationen einen bedeutenden Faktor bei der Induktion der Apoptose darstellt155. Die Beobachtung, dass Kalziumbindungsproteine in verschiedenen Konzentrationen differente Effekte haben, könnte 66 auch bei der Funktion von VILIP-1 eine Rolle spielen und möglicherweise die unterschiedliche Regulation in den einzelnen Tumortypen ansatzweise erklären. 6.5. Kritische Beurteilung der Ergebnisse Das späte Diagnosestadium und der schnelle Tumorprogress bei Patienten mit ösophagealen Plattenepithelkarzinomen führen dazu, dass nur wenige Patienten für eine Operation in Frage kommen. Aus diesem Grund und wegen der geringen Überlebensrate stand auch für unsere Studie relativ wenig Gewebematerial zur Verfügung. Eine größere Fallzahl könnte die Sicherheit und Deutlichkeit der Ergebnisse verbessern. Der Zusammenhang der VILIP-1-Expression mit der proliferativen Kapazität, welcher sich nur als Tendenz abzeichnete, ließe sich beispielsweise mit einer größeren Fallzahl eventuell bestätigen. Außerdem wird über das Gewebematerial jeweils nur ein kleiner Ausschnitt des Tumors untersucht. Da die Verteilung der VILIP-1- und Ki-67-Expression sehr heterogen innerhalb eines Tumors sein kann, sind die Aussagen und ihre Verallgemeinerung kritisch zu betrachten. Des Weiteren wäre es interessant, die Regulation von VILIP-1 neben Immunfärbungen auch ergänzend in Western Blot-Analysen zu untersuchen. Zusätzlich könnte eine Analyse der DNA mittels PCR weitere interessante Ergebnisse liefern. Hierbei könnte auch der Einfluss der Inaktivierung des VILIP-1-Promotors über verstärkte Methylierung auf die invasive Kapazität von ösophagealen Plattenepithelkarzinomen in Zelllinienexperimenten näher untersucht werden. Auch wenn die Auswertung ohne Wissen über die klinisch-pathologischen Daten der Patienten und entsprechenden Tumore durchgeführt wurde, hätte eine zusätzliche Auswertung durch einen zweiten Beurteiler eine größere Sicherheit bezüglich der Ergebnisse geben können. 67 7. Schlussfolgerung Die intensive Forschung der letzten Jahre hat zahlreiche neue Erkenntnisse zur zellulären Signaltransduktion, Proliferation und Apoptose im Rahmen der Tumorgenese geliefert. Es ist ein komplexes Netzwerk aus regulierenden Faktoren dargestellt worden. Das Kalziumbindungsprotein VILIP-1 ist nur eines von zahlreichen Proteinen, die möglicherweise eine Bedeutung bei der Tumorgenese haben. Die Funktion von VILIP-1 als Tumorsuppressorprotein, welche in einem tierexperimentellen Modell für Plattenepithelkarzinome bereits beschrieben worden ist, scheint nach den Ergebnissen dieser Studie ebenso im Ösophaguskarzinom des Menschen bedeutsam zu sein. Unsere Beobachtungen wie der erhöhte Anteil VILIP-1-negativer Gewebe unter den Ösophaguskarzinomen im Vergleich mit normaler Ösophagusmukosa sowie die Erhöhung des Anteils VILIP-1-negativer Tumore mit zunehmender Tumorgröße beziehungsweise lymphatischer Metastasierung sprechen für einen hemmenden Einfluss von VILIP-1 auf die Tumorprogression. Grundlage dieser tumorsuppressiven Funktion könnte eine Beeinflussung von Zelladhäsion, Zytoskelett und extrazellulärer Matrix durch VILIP-1 sein. Um weitere Erkenntnisse über die zugrundeliegenden Signaltransduktionswege von VILIP-1 in neoplastischen Zellen zu erlangen, sollte an Zelllinien in Stimulationsexperimenten untersucht werden, welche Wachstumsfaktoren beziehungsweise Signalmoleküle die VILIP-1- Genexpression und Signaltransduktion beeinflussen und wie die unterschiedliche VILIP-1Expression das Verhalten der malignen Zellen in Proliferationsexperimenten und Migrationsversuchen steuert. Hypothetisch können als Signalmoleküle cAMP und cGMP vermutet werden, für die in vorausgegangen Experimenten bereits eine Assoziation mit VILIP-1 nachgewiesen wurde. VILIP-1 könnte vergleichbar auch in neoplastischen Zellen ein physiologischer Regulator der Adenylatzyklase und Guanylatzyklase sein. Es bleibt unklar, welche Rezeptoren und Signalmoleküle neben cAMP und cGMP an Signalkaskaden mit VILIP-1 beteiligt sind und wie genau sie untereinander vernetzt sind. Weiterhin könnten aus hippokampalen Neuronenkulturen bereits gewonnene Erkenntnisse genutzt werden, wo eine reversible kalziumvermittelte Translokation von myristoyliertem VILIP-1 in die Zellmembran und in Membranen des Golgi-Apparats beschrieben wurde156. In nachfolgenden Experimenten sollte geklärt werden, ob eine solche Translokation auch in neoplastischen Zellen stattfindet und inwieweit sie die Funktion von VILIP-1 beeinflusst. 68 Das Verständnis der Funktionen von VILIP-1 könnte in Zukunft auch durch die Analyse von Mutationen, welche die Synthese und Struktur von VILIP-1 beeinträchtigen, detaillierter untersucht werden. Außerdem wäre es bedeutend, die Rolle von VILIP-1 in der Apoptose sowie das Zusammenspiel mit bekannten Apoptose-regulierenden Proteinen wie beispielsweise p53 zu studieren. Insgesamt könnte das Verständnis der molekularen Mechanismen, welche die Tumorinvasion und Metastasierung im Zusammenhang mit der Expression von VILIP-1 beeinflussen, neue diagnostische und therapeutische Herangehensweisen ermöglichen. Bevor VILIP-1 als klinischer Marker zur Charakterisierung der Malignität von Tumoren eingesetzt werden kann, sind neben dieser Studie weitere Untersuchungen an einer größeren Kohorte und mit weiteren molekularbiologischen Methoden notwendig, um die Funktion von VILIP-1 als potentieller Tumorsuppressor zu überprüfen. 69 8. Zusammenfassung Kalzium-Sensor-Proteine sind Schlüsselmoleküle zur Vermittlung von Kalziumsignalen. Sie kontrollieren ein großes Spektrum an zellulären Funktionen. Dazu gehören Proliferation, Differenzierung und Migration, welche entscheidende Prozesse der Tumorgenese darstellen. In diesem Zusammenhang ist kürzlich das Kalzium-Sensor-Protein VILIP-1 aufgrund seiner mutmaßlichen Tumorsuppressorfunktion ins wissenschaftliche Interesse gerückt. Diese Studie analysiert die VILIP-1-Expression in verschiedenen humanen Normalgeweben und Tumoren. Als Paradigma für epitheliale Tumore wird das Plattenepithelkarzinom des Ösophagus gewählt. Das Plattenepithelkarzinom des Ösophagus ist einer der bösartigsten und aggressivsten Tumore des Verdauungstraktes. Trotz zahlreicher Maßnahmen zur Verbesserung der Therapie, bleibt die Prognose der Patienten mit einer 5 Jahres-Überlebensrate von nur 10-30% sehr schlecht. Deswegen ist die intensive Suche nach molekularbiologischen Einflussfaktoren und die Aufklärung der Signalwege in normalen wie in neoplastischen Zellen weiterhin eine wichtige Voraussetzung zur Optimierung von Diagnostik und Therapie und damit zur Verbesserung der Prognose des Ösophaguskarzinoms. In dieser Studie wird VILIP-1 erstmalig in ösophagealem Normalgewebe und im Plattenepithelkarzinom des Ösophagus über Immunfärbungen nachgewiesen und der Zusammenhang zwischen VILIP-1-Expression und klinisch-pathologischen Merkmalen des ösophagealen Plattenepithelkarzinoms untersucht. Insgesamt werden Gewebe von 55 Patienten analysiert. Darunter befinden sich 54 primäre Plattenepithelkarzinome des Ösophagus und 24 Normalgewebe. Als Methoden werden immunhistochemische Färbungen nach der Avidin-Biotinyl-PeroxidaseKomplex-Methode und Immunfluoreszenzdoppelfärbungen mit Antikörpern gegen VILIP-1 und den Proliferationsmarker Ki-67 verwendet. Während alle ösophagealen Normalgewebe eine Expression von VILIP-1 zeigen, nimmt die Anzahl an VILIP-1-negativen Geweben unter den Ösophaguskarzinomen deutlich zu (p=0.001). Die Analyse der Beziehung von VILIP-1-Expression und Tumorgröße zeigt eine signifikante Zunahme des Anteils VILIP-1-negativer Tumore von T1 nach T4 (p=0.012). Lymphatisch metastasierte Tumore (N1) sind signifikant häufiger VILIP-1-negativ als Tumore ohne Lymphknotenmetastasen (N0) (p=0.009). Undifferenzierte Tumore (G3) sind häufiger VILIP-1-negativ als mäßig differenzierte (G2), die Beziehung zwischen VILIP-1-Expression und Differenzierung erreicht allerdings, 70 möglicherweise wegen unzureichender Fallzahlen, kein Signifikanzniveau (p=0.131). Die Analyse der Doppelfärbung für VILIP-1 und den Proliferationsmarker Ki-67 zeigt trotz deutlicher Herabregulation von VILIP-1 und Heraufregulation von Ki-67 im Tumorgewebe keinen inversen Zusammenhang von VILIP-1 und der proliferativen Kapazität der neoplastischen Zellen, wenngleich die Ki-67-Expression in VILIP-1-negativen Tumorzellnestern tendenziell stärker ist als in VILIP-1-positiven Geweben. Insgesamt stützen unsere Ergebnisse die These einer Tumorsuppressorfunktion von VILIP-1 im Plattenepithelkarzinom des Ösophagus. Ergänzend wird eine Auswahl weiterer humaner Normal- und Tumorgewebe über immunhistochemische Microarray-Analysen untersucht. Die Regulation der VILIP-1-Expression in den einzelnen Tumortypen ist sehr unterschiedlich. Es gibt Gewebe mit gleichbleibender VILIP-1-Expression in Normal- und Tumorgewebe (Plattenepithelkarzinom der Haut), mit zunehmender VILIP-1-Expression im Tumorgewebe (Kolonkarzinom, hepatozelluläres Karzinom und Prostatakarzinom) und mit abnehmender VILIP-1-Expression im Tumorgewebe (Nierenzellkarzinom, Plattenepithelkarzinom des Ösophagus). Dieses Phänomen lässt eine unterschiedliche Regulation von VILIP-1 in den Signalkaskaden der verschiedenen Zelltypen vermuten und könnte daraufhin deuten, dass VILIP-1 nur in bestimmten Neoplasien eine Tumorsuppressorfunktion ausübt. 71 9. Literaturverzeichnis 1 Parkin DM, Bray F, Ferlay J, et al. Global cancer statistics, 2002. CA Cancer J Clin. 2005; 55:74-108. 2 Sugimachi K, Ohno S, Matsuda H, et al. Clinicopathologic study of early stage esophageal carcinoma. Surgery 1989; 105:706-710. 3 Kato H. Diagnosis and treatment of eophageal neoplasm. Jpn J Cancer Res 1995; 86:993-1009. 4 Earlam R, Cunha-Melo JR. Oesophageal squamous cell carcinoma: 1. A critical review of surgery. Br J Surg 1980; 67:381-390. 5 de Groot KM. Cancer of the oesophagus – quo vadis? SAMJ 2005; 95, No. 3. 6 Messmann H. Squamous cell cancer of the oesophagus. Best Practice & Research Clinical Gastroenterology 2001; 15:249-265. 7 Yang G, Zhang Z, Liao J, et al. Immunohistochemical studies on Waf1p21, p16, pRb and p53 in human esophageal carcinomas and neighboring epithelia from a high-risk area in northern China. Int J Cancer 1997; 72:746-751. 8 Rose EF. Esophageal cancer in the Transkei: 1955±69. Journal of the National Cancer Institute 1973; 51:7-16. 9 Pisani P, Parkin DM, Ferlay J, Estimates of the worldwide mortality from eighteen major cancers in 1985: implications for prevention and projections of future burden. Int J Cancer 1993; 55:891-903. 10 Yang CS. Research on esophageal cancer in China: a review. Cancer Res 1980; 40:2633-2644. 11 Blot WJ, Devesa SS, Kneller RW, et al. Rising incidence of adenocarcinoma of the esophagus and gastric cardia. JAMA 1991; 265:1287-1289. 12 Blot WJ, McLaughlin JK. The changing epidemiology of esophageal cancer. Seminars in Oncology 1999; 26:2-8. 13 Schlemper RJ, Dawsey SM, Itabashi M, et al. Differences in diagnostic criteria for esophageal squamous cell carcinoma between Japanese and Western pathologists. Cancer 2000; 88:996-1006. 14 Crew KD, Neugut AI. Epidemiology of upper gastrointestinal malignancies. Semin Oncol. 2004; 31:450-464. 72 15 Pera M, Manterola C, Vidal O, et al. Epidemiology of Esophageal Adenocarcinoma. Journal of Surgical Oncology 2005; 92:151–159. 16 Maelandsmo GM, Florenes VA, Mellingsaeter T, et al. Differential expression pattern of S100A2, S100A4 and S100A6 during progression of human malignant melanoma. Int J Cancer. 1997; 74:464-469. 17 Hermanek P. What's new in TNM? Pathol Res Pract 1994; 190:97-102. 18 Hermanek P, Scheibe O, Spiessl B, et al. TNM classification of malignant tumors: the new 1987 edition. Rontgenblatter 1987; 40:200. 19 Lee RG, Compton CC. Protocol for the examination of specimens removed from patients with esophageal carcinoma. A basis for checklists. The Cancer Committee, College of American Pathologists, and the Task Force on the Examination of Specimens From Patients With Esophageal Cancer. Arch Pathol Lab Med 1997; 121:925-929. 20 Roder JD, Busch R, Stein HJ, et al. Ratio of invaded to removed lymph nodes as a predictor of survival in squamous cell carcinoma of the oesophagus. Br J Surg 1994; 81:410-413. 21 Hermanek P, Wittekind C. The pathologist and the residual tumor (R) classification Pathol Res Pract 1994; 190:115- 123. 22 Arbeitsgemeinschaft Bevölkerungsbezogener Krebsregister in Deutschland in Zusammenarbeit mit dem RKI „Krebs in Deutschland, Häufigkeiten und Trends“, Arbeitsgemeinschaft Bevölkerungsbezogener Krebsregister, Saarbrücken 2004. 23 Lam KY, Ma LT, Wong J, Measurement of extent of spread of esophageal squamous carcinoma by serial sectioning. J Clin Patho. 1996; 49:124-129. 24 Hiddemann W, Huber H, Batram CR. Die Onkologie. Teil 2: Spezieller Teil. Solide Tumoren, Lyphome, Leukämien. Springer Verlag 2004. 25 Pöschl G, Seitz HK. Alcohol and Cancer. Alcohol & Alcoholism 2004; 39:155-165. 26 van den Brandt PA, Goldbohm RA. Nutrition in the prevention of gastrointestinal cancer. Best Practice & Research Clinical Gastroenterology 2006; 20:589-603. 27 Bahmanyar S, Ye W. Dietary Patterns and Risk of Squamous-Cell Carcinoma and Adenocarcinoma of the Esophagus and Adenocarcinoma of the Gastric Cardia: A Population-Based Case-Control Study in Sweden. Nutrition and Cancer 2006; 54:171-178. 73 28 Gao YT, McLaughlin JK, Blot WJ, et al. Risk factors for esophageal cancer in Shanghai, China. I. Role of cigarette smoking and alcohol drinking. Int J Cancer 1994; 58:192-196. 29 Buttar NS, Wang KK. Mechanisms of disease: Carcinogenesis in Barrett's esophagus. Nat Clin Pract Gastroenterol Hepatol 2004; 1:106-12. 30 Ribeiro U Jr, Posner MC, Safatle-Ribeiro AV, et al. Risk factors for squamous cell carcinoma of the oesophagus. Br J Surg 1996; 83:1174-1185. 31 Hopkins RA, Postlethwait RW. Caustic burns and carcinoma of the esophagus. Annals of Surgery 1981; 194:146-148. 32 Isolauri J, Markkula H. Lye ingestion and carcinoma of the esophagus. Acta Chirurgica Scandinavica 1989; 155:269- 271. 33 Fong LYY, Jiang Y, Farber JL. Zinc deficiency potentiates induction and progression of lingual and esophageal tumors in p53-deficient mice. Carcinogenesis 2006; 27:1489–1496. 34 Bollschweiler E, Wolfgarten E, Nowroth T, et al. Vitamin intake and risk of subtypes of esophageal cancer in Germany. J Cancer Res Clin Oncol 2002; 128:575–580. 35 Risk JM, Mills HS, Garde J, et al. The tylosis esophageal cancer (TOC) locus: more than just a familial cancer gene. Diseases of the Esophagus 1999; 12:173-176. 36 Marger RS, Marger D. Carcinoma of the esophagus and tylosis. A lethal genetic combination. Cancer 1993; 72:17-19. 37 Ferguson A, Kingstone K. Coeliac disease and malignancies. Acta Paediatrica Supplement 1996; 412:78-81. 38 Mackay S. Management of oesophageal carcinoma. Australian Family Physician 2006; 35:202-206. 39 Siersema PD, Verschuur EM, Homs MY, et al. Palliativa treatment in patients with oesophagus carcinoma. Ned Tijdschr Geneeskd 2005; 149:2775-2782. 40 Homs MY, Kuipers EJ, Siesema PD. Palliative therapy. J Surg Oncol 2005; 92:246-256. 41 Swisher SG, Putnam JB, Feig BW, et al. Staging and sugery of esophageal cancer. In: Markmann A (ed.) Atlas of Cancer, Lippincott Williams & Willkins Philadelphia 2002; 178-187. 74 42 Forastiere AA, Orringer MB, Perez-Tamayo C, et al. Preoperative chemoradiation followed by transhiatal esophagectomy for carcinoma of the esophagus: final report. J. Clinical Oncology. 1993; 11:1118-1123. 43 Poplin E, Fleming T, Leichman L, et al. Combined therapies for squamous cell carcinoma of the esophagus, a Southwest Oncology Group Study (SWOG-8037). J Clinical Oncology 1987; 5:622-628. 44 Stahl M, Wilke H, Fink U, et al. Combined preoperative chemotherapy and radiotherapy in patients with locally advanced esophageal cancer: interim analysis of a phase II trial. J Clinical Oncology 1996; 14:829-837. 45 Nisihira T, Hashimoto Y, Katayama M, et al. Molecular and cellular features of esophageal cancer cells. J Cancer Res Clin Oncol. 1993; 119:441-449. 46 Weir HK, Thun MJ, Hankey BF, et al. Annual report to the nation on the status of cancer, 1975–2000, featuring the uses of surveillance data for cancer prevention and control. J Natl Cancer Inst 2003; 95:1276–1299. 47 Ellis FH Jr, Watkins E Jr, Krasna MG et al. Staging of carcinoma of the esophagus and cardia: a comparison of different staging criteria. Journal of Surgical Oncology 1993; 52:231-235. 48 Lam KY, Ma LT, Pathology of esophageal cancers: local experience and current insights. Chin Med J. 1997; 110:459- 464. 49 Moghissi K. Surgical resection for stage I cancer of the oesophagus and cardia. British Journal of Surgery 1992; 79:935- 937. 50 Mori T, Yanagisawa A, Kato Y, et al. Accumulation of genetic alterations during esophageal carcinogenesis. Hum Mol Genet 1994; 3:1969-1971. 51 Cahill DP, Kinzler KW, Vogelstein B, et al. Genetic instability and Darwinian selection in tumours. Trends Cell Biol 1999; 9:57-60. 52 McCabe ML, Dlamini Z. The molecular mechanisms of oesophageal cancer. International Immunopharmacology 2005; 5:1113–1130. 53 Ren Y, Cao B, Law S, et al. Hepaocyte Growth Factor promotes cancer cell migration and angiogenetic factors expression: A prognostic marker of human esophageal squamous cell carcinomas. Clin Cancer Res 2005; 11:6190-6197. 54 Kitadai Y, Amioka T, Haruma K, et al. Clinicopathological significance of vascular endothelial growth factor (VEGF)-C in human esophageal squamous cell carcinomas. IntJCancer 2001; 93:662-666. 75 55 Schlessinger J. Cell signaling by receptor tyrosine kinases. Cell 2000; 103:211–215. 56 Yarden Y, Sliwkowski MX. Untangling the ErbB signalling network. Nat Rev Mol Cell Biol 2001; 2:127–137. 57 Salomon DS, Brandt R, Ciardiello F, et al. Epidermal growth factor-related peptides and their receptors in human malignancies. Crit Rev Oncol Hematol 1995; 19:183–232. 58 Normanno N, Bianco C, De Luca A, et al. The role of EGF related peptides in tumor growth. Front Biosci 2001; 6:685– 707. 59 Jiang W, Kahn SM, Tomita N, et al. Amplification and expression of human cyclin D gene in esophageal cancer. Cancer Res 1992; 52:2980-2983. 60 Adelaide J, Monges G, Derderiant C, et al. Oesophageal cancer and amplification of the human cyclin D gene CCND1/PRAD1. Br J Cancer 1995; 71:64-68. 61 Naitoh H, Shibata J, Kawaguchi A, et al. Overexpression and localization of cyclin D1 mRNA and antigen in esophageal cancer. Am J Pathol 1995; 146:1161-1169. 62 el-Deiry WS, Tokino T, Velculescu VE, et al. WAF1, a potential mediator of p53 tumor suppression. Cell 1993; 75:817- 825. 63 el-Deiry WS, Harper JW, O’Connor PM, et al. WAF1/CIP1 is induced in p53-mediated G1 arrest and apoptosis. Cancer Res 1994; 54:1169-1174. 64 Gomez-Manzano C, Fueyo J, Kyritsis AP, et al. Adenovirus-mediated transfer of the p53 gene produces rapid generalized death of human glioma cells via apoptosis. Cancer Res 1996; 56:694-699. 65 Lane DP, A death in the life of p53. Nature 1993; 362:786-787. 66 Liu TJ, Zhang WW, Taylor DL, et al. Growth suppression of human head and neck cancer cells by the introduction of a wild-type p53 gene via a recombinant adenovirus. Cancer Res 1994; 54:3662-3667. 67 Huang Y, Meltzer SJ, Yin J, et al. Altered messenger RNA and unique mutational pro- files of p53 and Rb in human esophageal carcinomas. CancerRes 1993; 53:1889–1894. 68 Giacinti C, Giordano A. RB and cell cycle progression. Oncogene 2006; 25:5220-5227. 76 69 Lehrbach MD, Nita ME, Cecconello I, et al. Molecular Aspect of esophageal squamous cell carcinoma carcinogenesis. Arq Gastroenterol 2003; v.40-no.4-out./dez. 70 Lenz SE, Braunewell KH, Weise C, et al. The Neuronal EF- hand Ca2/-Binding Protein VILIP: Interaction with Cell Membrane and Actin- Based Cytoskeleton. Biochem and Biophys Res Comm 1996; 225:1078-1083. 71 Schnurra I, et al. The neuronal calcium sensor protein Vilip-1 is associated with amyloid plaques and promotes cell death and tau phosphorylation in vitro, a link between calcium sensors and alzheimer disease? Neurobiology of disease 2001; 8:900-909. 72 Mercer EA, et al. NAIP interacts with hippocalcin and protects neurons against calcium-induced cell death through caspase-3-dependent and independent pathways. EMBO J 2000; 19:3597-3607. 73 Braunewell KH, Gundelfinger E.D. Intracellular neuronal calcium sensor proteins, a family of EF-hand calcium binding proteins in search of a function. Cell Tissue Res 1999; 295:1-12. 74 Frey BM, Reber BF, Vishwanath BS, et al. Annexin I modulates cell functions by controlling intracellular calcium release. FASEB J 1999; 15:2235-2245. 75 Hayes MJ, Moss SE. Annexins and disease. Biochem and Biophys Res Comm 2004; 322:1166–1170. 76 Thiel C, Osborn M, Gerke V. The tight association of the tyrosine kinase substrate annexin II with the submembranous cytoskeleton depends on intact p11- and Ca(2+)- binding sites. J Cell Sci 1992; 103:733-742. 77 Schäfer BW, Heizmann CW. The S100 family of EF-hand calcium binding proteins: functions and pathlology. Trends Biochem Sci 1996; 21:134-140. 78 Heizmann CW, Cox J. New perspectives of S100 proteins: a multifunctional Ca2+, Zn2+ and Cu2+ -binding protein family. Biometals 1998; 11:383-397. 79 Donato R. Functional roles of S100 proteins, calcium binding proteins of the IIF hand type. BBA 1999; 1450:191-231. 80 Heizmann CW, Hunziker W. Intracellular calcium-binding proteins: more sites than insights. Trends Biochem Sci 1991; 16:98–103. 77 81 Gorczyca WA, Gray-Keller MP, Detwiler PB,et al. Purification and physiological evaluation of a guanylate cyclase activating protein from retinal rods. Neurobiol 1994; 91:4014-4018. 82 Palczewski K, Subbaraya I, Gorczyca WA, et al. Molecular cloning and characterization of retinal photoreceptor guanylyl cyclase-activating protein. Neuron 1994; 13:395-404. 83 Dizhoor AM, Hurley JB. Inactivation of EF-hands Makes GCAP-2 (p24) a Constitutive Activator of Photoreceptor Guanylyl Cyclase by Preventing a Ca2+-induced “Activator-to-Inhibitor” Transition. J Biol Chem 1996; 271:19346–19350. 84 Haeseleer F, Sokal I, Ning L, et al. Molecular Characterization of a Third Member of the Guanylyl Cyclase-activating Protein Subfamily. J Biol Chem 1999; 274:6526–6535. 85 Ning L, Fariss RN, Zhang K, et al. Guanylate-cyclase-inhibitory protein is a frog retinal Ca2+-binding protein related to mammalian guanylate-cyclase-activating proteins. Eur J Biochem 1998; 252:591-599. 86 An WF, Bowlby MR, Betty M, et al. Modulation of A-type potassium channels by a family of calcium sensors. Nature 2000; 403:553-556. 87 Kawamura S, Takamatsu K, Kitamura K. Purification and characterization of S-modulin, a calcium-dependent regulator on cGMP phosphodiesterase in frog rod. Biochem Biophys Res Commun 1992; 186:411-417. 88 Kawamura S, Kuwata O, Yamada M et al. Photoreceptor Protein s26, a Cone Homologue of S-modulin in Frog Retina. J Biol Chem 1996; 271:21359–21364. 89 Wang W, Zhou Z, Zhao W, et al. Molecular cloning, mapping and characterization of the human neurocalcin delta gene (NCALD). Biochem Biophys Acta 2001; 1518:162-167. 90 Nef S, Fiumelli H, de Castro E,et al., Identification of neuronal calcium sensor (NCS-1) possibly involved in the regulation of receptor phosphorylation. J Recept Signal Transduct Res 1995; 15:365-378. 91 Hendricks KB, Wang BQ, Schnieders EA, et al. Yeast homologue of neuronal frequenin is a regulator of phosphatidylinositol-4-OH kinase. Nat Cell Biol 1999; 1:234-241. 92 Polans A, et al. Turned on by Ca2+! The physiology and pathology of Ca2+binding proteins in the retina. Trends Neurosci 1996; 19:547-554. 93 Koh PO, et al. Up-regulation of neuronal calcium sensor-1 (NCS-1) in the prefrontal cortex of schizophrenic and bipolar patients. Proc Natl Acad Sci U S A 2003; 100:313-317. 78 94 Bai J, et al. Abnormalities in the dopamine system in schizophrenia may lie in altered levels of dopamine receptor- interacting proteins. Biol Psychiatry 2004; 56:427-440. 95 Kabbani N, et al. Interaction with neuronal calcium sensor NCS-1 mediates desensitization of the D2 dopamine receptor. J Neurosci 2002; 22:8476-8486. 96 Bahi N, et al. IL1 receptor accessory protein like, a protein involved in X-linked mental retardation, interacts with Neuronal Calcium Sensor-1 and regulates exocytosis. Hum Mol Genet 2003; 12:1415-1425. 97 Schnurra I, et al. The neuronal calcium sensor protein Vilip-1 is associated with amyloid plaques and promotes cell death and tau phosphorylation in vitro, a link between calcium sensors and alzheimer disease? Neurobiology of disease 2001; 8:900-909. 98 Loring JF, et al. A gene expression profile of Alzheimer’s disease. DNA and Cell Biology 2001; 20:683-695. 99 Braunewell KH, et al. Abnormal localization of two neuronal calcium sensor proteins, visinin-like-proteins (vilips) -1 and -3, in neocortical brain areas of Alzheimer disease patients. Dement Geriatr Cogn Disord 2001; 2:110-116. 100 Burgoyne RD, O'Callaghan DW, Hasdemir B, et al. Neuronal Ca(2+)-sensor proteins: multitalented regulators of neuronal function. Trends Neurosci 2004; 27:203-209. 101 Weiss JL, Burgoyne RD. Voltage-independent inhibition of P/Q-Typ Ca2+ channels in adrenal chromaffin cells via a neuronal Ca2+ sensor-1-dependent pathway involves Src family tyrosine kinase. J Biol Chem 2001; 276:44804-44811. 102 Ames JB, Tanaka T, Stryer L, et al. Portrait of a myristoyl switch protein. Curr Opin Struct Biol 1996; 6:432-438. 103 Kobayashi M, Takamatsu K, Saitoh S, et al. Myristoylation of hippocalcin is linked to its calcium-dependent membrane association properties. J Biol Chem 1993; 268:18898-18904. 104 Dizhoor AM, Chen CK, Olshevskaya E, et al. Role of the acylated amino terminus of recoverin in Ca(2+)-dependent membrane interaction. Science 1993; 259:829-832. 105 Ladant D. Calcium and Membrane Binding Properties of Bovine Neurocalcin δ Expressed in Escherichia coli. J Biol Chem 1995; 270:3179-3185. 79 106 Ames JB, Ishima R, Tanaka T, et al. Molecular mechanics of calcium-myristoyl switches. Nature 1997; 389:198-202. 107 Braunewell KH. The darker side of Ca(2+) signaling by neuronal Ca(2+)-sensor proteins: from Alzheimer's disease to cancer. Trends Pharmacol Sci 2005; 26:345-351. 108 Bernstein HG, Baumann B., Danos P., et al. Regional and cellular distribution of neural visinin-like protein immunoreactivities (VILIP-1 and VILIP-3) in human brain. J. Neurocytol 1999; 28:655-662. 109 Gierke P, Zhao C, Linke B, et al. Expression analysis of members of the neuronal calcium sensor protein family: combining bioinformatics and Western blot analysis. Biochem Biophys Res Commun. 2004; 323:38-43. 110 Braunewell KH, Spilker C, Behnisch T, et al. The neuronal calcium-sensor protein VILIP modulates cAMP accumulation in stably transfected C6 glioma cells: amino-terminal myristoylation determines functional activity. J Neurochem. 1997; 68:2129-2139. 111 Braunewell KH, Brackmann M, Schaupp M, et al. Intracellular neuronal calcium sensor (NCS) protein VILIP-1 modulates cGMP signalling pathways in transfected neural cells and cerebellar granule neurons. J Neurochem 2001; 78:1277-1286. 112 Braunewell KH, Gundelfinger ED. Low level expression of calcium-sensor protein VILIP induces cAMP-dependent differentiation in rat C6 glioma cells. Neurosci Lett 1997; 234:139-142. 113 Gerdes J, Li L, Schlueter C, et al. Immunobiochemical and molecular biologic characterization of the cell proliferation- associated nuclear antigen that is defined by monoclonal antibody Ki-67. Am J Pathol 1991; 138:867-873. 114 Van Dierendonck JH, Keijzer R, van de Velde CJ, et al. Nuclear distribution of the Ki-67antigen during the cell cycle: Comparison with growth fraction in human breast cancer cells. CancerRes 1989; 49:2999-3006. 115 Fonatsch C, Duchrow M, Rieder H, et al. Assignment of the human Ki-67 gene (MK167) to 10q25-qter. Genomics 1991; 11:476-477. 116 Scholzen T, Dimmler C, Wohlenberg C, et al. Novel splice forms of the Ki-67 mRNA. Eur J Cell Biol 1997; 72:40-44. 117 Lopez F, Belloc F, Lacombe F, et al. Modalities of synthesis of Ki 67 antigen during the stimulation of lymphocytes. Cytometry 1991; 12:42-49. 118 Kuwano H, Saeki H, Kawaguchi H, et al. Proliferative activity of cancer cells in front and center areas of Carcinoma in situ and invasive sites of Esophageal Squamous-Cell Carcinoma. Int J Cancer 1998; 78:149–152. 80 119 120 Lenz SE, Jiang S, Braun K, et al. Cell Tissue Res. 1996; 283:413-424. Spilker C, Richter K, Smalla KH, et al. The neuronal EF-hand calcium-binding protein visinin-like-protein-3 is expressed in cerebellar purkinje cells and shows a calcium-dependent membrane association. Neuroscience 2000; 96:121129. 121 Key G, Becker MH, Baron B, et al. New Ki-67-equivalent murine monoclonal antibodies (MIB 1-3) generated against bacterially expressed parts of the Ki-67 cDNA containing three 62 base pair repetitive elements encoding for the Ki-67 epitope. Lab Invest 1993; 68:629-636. 122 Shi SR, Key ME, Kalra KL Antigen retrieval in formalin-fixed, paraffin-embedded tissues: An enhancement method for immunohistochemical staining based on microwave oven heating of tissue sections. J Histochem Cytochem 1991; 39:741- 748. 123 Cattoretti G, Becker MH, Key G, et al. Monoclonal antibodies against recombinant parts of the Ki-67 antigen (MIB 1 and MIB 3) detect proliferating cells in microwave-processed formalin-fixed paraffin sections. J Pathol 1992; 168:357363. 124 Kapuscinski JD. DAPI: a DNA-specific fluorescent probe.Biotech Histochem 1995; 70:220-233. 125 Mahloogi H, Gonzalez-Guerrico, AM, De Cicco RL, et al. Graduate decrease of VILIP-1 Expression during mouse skin tumor progression and its role in regulating tumor cell invasive behavior Cancer Res 2003; 63:4997-5004. 126 Gonzalez Guerrico, AM, Jaffer ZM, Page RE, et al. Visinin-like protein-1 is a potent inhibitor of cell adhesion and migration in squamous carcinoma cells. Oncogene 2005; 24:2307-2316. 127 Xia SH, Hu LP, Hu H, et al. Three isoforms of annexin I are preferentially expressed in normal esophageal epithelia but down-regulated in esophageal squamous cell carcinomas, Oncogene 2002; 21:6641–6648. 128 Luo A, Kong J, Hu G, Discovery of Ca2+-relevant and differentiation-associated genes downregulated in esophageal squamous cell carcinoma using cDNA microarray Oncogene 2004; 23:1291–1299. 129 Zhang X, Zhi HY, Zhang J, et al. Expression of annexin II in human esophageal squamous cell carcinoma. Zhonghua Zhong Liu Za Zhi. 2003; 25:353-355. 130 Liu Y, Wang HX, Lu N, et al. Translocation of annexin I from cellular membrane to the nuclear membrane in human esophageal squamous cell carcinoma. World J Gastroenterol. 2003; 9:645-649. 81 131 Gerke V, Moss SE. Annexins: From Structure to Function. Physiol Rev 2002; 82: 331–371 132 Lina HK Lim, Shazib Pervaiz. Annexin I: the new face of an old molecule. FASEB J 2007; 21:968-975. 133 Dai FF, Zhang Y, Kang Y, et al. The Neuronal Ca2+ Sensor Protein Visinin-like Protein-1 is expressed in Pancreatic Islets and Regulates Insulin Secretion. The Journal of Biological Chemistry 2006; 281:21942–21953. 134 Kyriazanos, ID, Tachibana, M, Dhar DK, et al. Expression and prognostic significance of S100A2 protein in squamous cell carcinoma of the esophagus. Onco. Rep 2002; 9:503-510. 135 Desphande R, Woods T, Fu J, et al. Biochemical characterization of S100 A2 in human keratinocytes: subcellular localization, dimerization and oxidative cross-linking. J Invest Dermatol 2000; 115:477-485. 136 Garrett SC, Varney KM, Weber DJ, et al. S100A4, a Mediator of Metastasis. The Journal of Biological Chemistry 2005; 281:677-680. 137 Schmidt-Hansen B, Ornås D, Grigorian M, Klingelhöfer J, et al. Extracellular S100A4(mts1) stimulates invasive growth of mouse endothelial cells and modulates MMP-13 matrix metalloproteinase activity. Oncogene 2004; 23:54875495. 138 Fu J, Fong K, Bellacosa A, et al. VILIP-1Downreglation in Non-small Cell Lung Carcinomas: Mechanisms and Prediction of Survival. PLos ONE 2008; 3:e1689. 139 Normanno N, Bianco C, De Luca A, et al. Target-based agents against ErbB receptors and their ligands: a novel approach to cancer treatment. Endocr Relat Cancer 2003; 10:1–21. 140 Lin L, Braunewell KH, Gundelfinger ED, et al. Functional analysis of calcium-binding EF-hand motifs of visinin-like protein-1. Biochem Biophys Res Commun 2002b; 296:827–832. 141 Palazzo AF, Eng CH, Schlaepfer DD, et al. Localized stabilization of microtubules by integrin- and FAK- facilitated Rho signaling. Science 2004; 303:836-839. 142 Narumiya S, Ishizaki T, Watanabe N. Rho effectors and reorganization of actin cytoskeleton. FEBS lett 1997; 410:68- 72. 82 143 Matsumoto Y, Tanaka K, Harimaya K, et al. Small GTP-binding protein, Rho, both increased and decreased cellular motility activation of metalloproteinase 2 and invasion of the osteosarcoma cells. Jpn J Cancer Res 2001; 92:429-438. 144 Liotta LA, Steeg PA, Stetler-Stevenson WG. Cancer metastasis and angiogenesis: an imbalance of positive and negative regulation. Cell 1991; 64:327-336. 145 Tanaka K, Iwamoto Y, Ito Y, et al. Cyclic AMP-regulated synthesis of the tissue inhibitors of metalloproteinases suppresses the invasive potential of the human fibrosarcoma cell line HT1080. Cancer Res 1995; 55:2927-2935. 146 Murray GI, Duncan ME, O’Neil P, et al. Matrix metalloproteinase-1 is associated with poor prognosis in esophageal cancer. J Pathol 1998; 185:256-261. 147 Karam SM. Lineage commitment and maturation of epithelial cells in the gut. Frontiers Bioscience 1999; 4:286-298. 148 Huang JX, Yan W, Song ZX, et al. Relationship between proliferative activity of cancer cells and clinicopathologic factors in patients with esophageal squamous cell carcinoma. World J Gastroenterol 2005; 11:2956-2959. 149 Youssef EM, Matsuda T, Takada N, et al. Pognostic significance of the MIB-1 proliferation index for patients with squamous cell carcinoma of the esophagus. Cancer 1995; 76:358-366. 150 Takeuchi H, Ozawa S, Ando N, et al. Cell cycle regulators and the Ki-67 labeling index can predict the response to chemoradiotherapy and the survival of patients with locally advanced squamous cell carcinoma of the esophagus. Annals of Surgical Oncology 2003; 10:792-800. 151 Xie Y, Chan H, Fan J et al. Involvement of visinin-like protein-1 (VSNL-1) in regulating proliferative and invasive properties of neuroblastoma. Carcinogenesis 2007; 28:2122-2130. 152 Cochran AJ, Lu HF, Li PX, et al. S-100 protein remains a practical marker for melanocytic and other tumours. Melanoma Res 1993; 3:325-330. 153 Davies BR, Davies MP, Gibbs FE, et al. Induction of the metastatic phenotype by transfection of a benign rat mammary epithelial cell line with the gene for p9Ka, a rat calcium-binding protein, but not with the oncogene EJ-ras-1. Oncogene 1993; 8:999-1008. 154 Zimmer DB, Cornwall EH, Landar A, et al. The S100 protein family: history, function, and expression. J Brain Res Bull 1995; 37:417-429. 83 155 Fano G, Biocca S, Fulle S, et al. The S-100: a protein family in search of a function. Prog Neurobiol 1995; 46:71-82. 156 Spilker C, Dresbach T, Braunewell KH. Reversible translocation and activity-dependent localization of the calcium- myristoyl switch protein Vilip-1 to different membrane compartments in living hippocampal neurons. J Neurosci 2002; 22:7331. 84 Abkürzungsverzeichnis AC Adenylyl Cyclase AJCC American Joint Commission for Classification of Cancer APUD-Zellen Amine Precursor Uptake and Decarboxylation Bcl-2 B-cell lymphoma 2 cAMP cyclic Adenosinmonophospat CAR Cancer Associated Retinopathie cGMP cyclic Guanosinmonophosphat COX-1/-2 Cyclooxygenase-1/-2 CT Computertomographie DNA Desoxyribonukleinsäure EBV Epstein Barr Virus ESCC Esophagus Squamous Cell Carcinoma FAK Focal Adhesion Kinase GCAP Guanylyl Cyclase Activating Protein Gy Gray HGF Hepatocyte Growth Factor HPV Humaner Papilloma Virus LPA Lysophosphatsäure MMP Matrix Metalloproteinase MRT Magnetresonanztomographie NCS Proteins Neuronal Calcium Sensor Proteins PAK Polyzyklische Aromatische Kohlenwasserstoffe PK Proteinkinase pRB Retinoblastomprotein RhoA/B/C Ras homologous A/B/C ROCK Rho-associated Coiled-coil Forming Protein SF Scatter Factor TIMP Tissue Inhibitor of Metalloproteinase UICC Union International Contre le Cancer VEGF Vascular Endothelial Growth Factor VILIP-1 Visinin-like-Protein-1 WT-1/WT-2 Wilms-Tumor-Gene-1/-2 85 Erklärung „Ich, Carla Wickborn, erkläre, dass ich die vorgelegte Dissertationsschrift mit dem Thema: „Die Expression des Visinin-like-Protein-1 in humanen Geweben und Tumoren sowie seine Korrelation mit klinisch-pathologischen Daten im Plattenepithelkarzinom des Ösophagus“ selbst verfasst und keine anderen als die angegebenen Quellen und Hilfsmittel benutzt, ohne die (unzulässige) Hilfe Dritter verfasst und auch in Teilen keine Kopien anderer Arbeiten dargestellt habe.“ Berlin, den 04.06.2009 C. Wickborn 86 „Mein Lebenslauf wird aus Datenschutzgründen in der elektronischen Version meiner Arbeit nicht mit veröffentlicht.“ 87 „Mein Lebenslauf wird aus Datenschutzgründen in der elektronischen Version meiner Arbeit nicht mit veröffentlicht.“ 88 Danksagung Zunächst möchte ich meinem Betreuer PD Dr. Karl-Heinz Braunewell für die Möglichkeit der Mitarbeit in seiner Arbeitsgruppe Signaltransduktion an einem so interessanten Projekt, für seine ständige Bereitschaft Zusammenhänge zu diskutieren und neue Wege zu finden, ganz herzlich danken. Des Weiteren möchte ich mich bei Professor Peter M. Schlag für seine Kooperation mit der AG Signaltransduktion, die Möglichkeit der Arbeit an der Robert-Rössle-Klinik Berlin und der Nutzung der Präparate der Tumorbank danken. Frau Ina Wendler danke ich für die gewissenhafte Einarbeitung in die Immunhistochemie und ihre Hilfe bei allen offenen Fragen. Außerdem gilt mein Dank den Mitgliedern der AG Signaltransduktion, Herr Dr. Congjian Zhao, Herr Dr. Marian Brackmann und Herr Dr. Paul Gierke, die mir jederzeit mit Rat und Tat zur Seite standen und mir in schwierigen Situationen neue Hoffnung gegeben haben. Besonders danke ich auch Judith Enderwitz und Dimitar Ruszev für die Korrektur des Manuskripts, die technischen Hilfen und vor allem für die große Geduld. Ein spezieller Dank geht an meine Familie ohne deren Unterstützung mein Studium und auch diese Arbeit nicht möglich gewesen wären und die mir mit Verständnis jederzeit beiseite standen und mir den nötigen Rückhalt gaben.