Praktikumsreferat Biochemie
Werbung

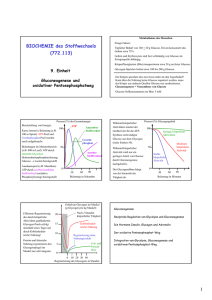
Praktikumsreferat Biochemie Thema: Glycolyse und Gluconeogenese 1. Glycolyse im Überblick Die Glycolyse (gr.: glykys = süß, lysis = auflösen) beschreibt den Abbau von Glucose zu Pyruvat (aerobe Glycolyse = ausreichend Sauerstoff vorhanden) oder Laktat ( anaerobe Gl. = Sauerstoffmangel). CAVE: Für die Glycolyse selbst wird KEIN Sauerstoff benötigt, auch wenn die Unterscheidung von aerober und anaerober Glycolyse dies nahelegt. Man spricht deshalb von aerober Glycolyse, weil hier Pyruvat als Endprodukt entsteht, daß dann im Rahmen der Atmungskette, aerob, vollständig abgebaut werden kann. In den menschlichen Zellen hat die Glycolyse zwei Aufgaben: 1. Abbau von Glucose zur Erzeugung von Energie 2. liefert Bausteine für Biosynthesen (z.B. für Synthese von Fettsäuren und Cholesterin) Eine Besonderheit der Glycolyse ist, daß sie in jeder Zelle ablaufen kann. Da sie im Cytoplasma stattfindet, können sogar hochdifferenzierte Zellen wie die Erys Glycolyse betreiben. Außerdem bietet die Glycolyse die einzige Möglichkeit für unseren Körper, ohne Sauerstoff Energie zu erzeugen. Beim Abbau von Glucose werden Bindungen gespalten, wodurch Energie freigesetzt wird. Unter diesem Gesichtspunkt kann man die Glycolyse in zwei Phasen einteilen: 1. Vorbereitungsphase: Für die ersten 5 Reaktionen der Glycolyse wird Energie in Form von zwei ATP investiert. Das Ergebnis sind 2 Moleküle Glyceral-3-Phosphat pro eingesetztem Glucosemolekül, die dann weiter verstoffwechselt werden. 2. Phase der Energieerzeugung: Durch die nächsten 5 Reaktionen entstehen 2 Moleküle NADH / H+, 4 Moleküle ATP und 2 Moleküle Pyruvat. Die Nettoausbeute an Energie beim Abbau eines Moleküls Glucose bis zum Pyruvat beträgt also 2 ATP. Diese 2 ATP sind verglichen mit der Atmungskette zwar ziemlich dürftig, aber für Zellen wie die Erys (keine Atmungskette) die einzige Möglichkeit, überhaupt Energie zu erzeugen. Außerdem ermöglicht dieser kleine Energiegewinn vielen Zellen, einen kurzen Sauerstoffmangel zu überleben. Zum weiteren Abbau kann Pyruvat zwei Wege einschlagen: • Ist genügend Sauerstoff vorhanden, erfolgt die komplette Oxidation zu CO2 und H2O über die Atmungskette. • Bei Sauerstoffmangel erfolgt die Reduktion zu Laktat, das ins Blut abgegeben wird. Die Glycolyse wird wie alle anderen Stoffwechselwege auch über Enzyme reguliert. Bei einem solch komplexen Vorgang wie der Glycolyse werden aber nie alle Enzyme, sondern nur die der Schlüsselreaktionen reguliert. Diese sogenannten Schlüsselenzyme sind: • Hexokinase, welches die Glucose nach der Diffusion in die Zelle unter ATP-Verbrauch zu Glucose-6-Phosphat phosphoryliert; diese Reaktion ist stark exergon und daher irreversibel • Phosphofructokinase 1, welche einen zweiten Phosphatrest in das Molekül Fructose-6- Phosphat einbaut; auch diese Reaktion ist stark exergon Adrian Knispel -1- 21. März 2003 • Pyruvatkinase, welche vom Phosphoenolpyruvat das Phosphat abspaltet und es auf ADP überträgt; ebenfalls exergon und irreversibel Diese Schlüsselenzyme regulieren die Geschwindigkeit der Glycolyse. Sie arbeiten, verglichen mit anderen Enzymen, recht langsam, verursacht durch eine schwache Wirksamkeit des Enzyms (so phosphoryliert die Hexokinase auch andere Hexosen wie Fructose oder Mannose). Die Geschwindigkeit dieser Reaktion hängt daher nicht vom Substratangebot ab, sondern von der Enzymaktivität, was man eine enzymbegrenzte Reaktion nennt. Die Langsamkeit dieser Reaktion drosselt die Geschwindigkeit der gesamten Sequenz und macht diese Enzyme zu wichtigen Kontrollstellen im Stoffwechselweg. Gibt es mehrere solcher Schlüsselreaktionen, bestimmt der langsamste Teilschritt der Reaktionsfolge die Geschwindigkeit. Dies bezeichnet man als Schrittmacherreaktion. Bei der Glycolyse wird diese von der PFK 1 katalysiert. Wie bereits erwähnt, läßt sich die Glycolyse energetisch in zwei Schritte einteilen. Die ersten 5 Schritte verbrauchen pro Molekül Glucose 2 ATP. An welcher Stelle wird nun aber Energie konserviert? Bei der Oxidation von Glyceral-3-Phosphat zu 1,3-Bisphosphoglycerat entsteht eine energiereiche Säureanhydridbindung am C1. Diese Reaktion ist biochemisch wirklich interessant. Die Aldehydgruppe von Glyceral-3-Phosphat wird nämlich nicht einfach zu einer freien Carboxylgruppe oxidiert. Vielmehr wird die Energie genutzt, um ein Anhydrid aus Carbonsäure und Phosphorsäure zu erzeugen. Dadurch wird die Energie der Oxidation kurzfristig konserviert. Außerdem kann das Coenzym NAD+ reduziert werden, was in der Atmungskette noch einige Moleküle ATP liefert. Bei der nun folgenden Spaltung der Anhydridbindung wir die Energie wieder frei und zur Bildung von ATP aus ADP genutzt. Hierzu überträgt die 3-Phosphoglycerat-Kinase das angeheftete Phosphat auf ADP – es entstehen ATP und 3-Phosphoglycerat. Erst an dieser Stelle führt die Glycolyse zum ersten mal zu einem Energiegewinn. Pro Molekül Glucose sind das 2 ATP. Damit hat die Zelle nun schon mal ihre investierte Energie wieder reingeholt. Da die bei dieser Reaktionskette freiwerdende Energie nicht als Wärme verpufft, sondern für die ATP-Erzeugung genutzt wird, nennt man den Vorgang Substratketten-Phosphorylierung. Diese ist von der oxidativen Phosphorylierung der Atmungskette zu unterscheiden, bei der aus ADP und anorganischem Phosphat ATP hergestellt wird. Eine zweite Substratketten-Phosphorylierung findet bei der Reaktion von Phosphoenolpyruvat zu Pyruvat statt. Hier werden nicht nur 2 ATP gebildet, sondern zusätzlich noch über 30 kJ/mol Energie frei. Damit haben wir aus der Glycolyse 2 Moleküle ATP netto gewonnen. Das in der Glycolyse entstandene Pyruvat hat nun zwei Möglichkeiten, weiter abgebaut zu werden: 1. aerober Abbau zu CO2 und H2O im Mitochondrium 2. anaerober Abbau zu Laktat im Cytoplasma Die Wahl des Weges hängt nun davon ab, ob eine Zelle Mitochondrien besitzt (Erys haben keine) und wenn ja, wieviel Sauerstoff zur Verfügung steht. Ein Grundprinzip des Stoffwechsels jeder Zelle ist, daß jeder verbrauchte Stoff immer nachgefüllt werden muß. Führt also die Glycolyse z.B. dazu, daß NAD+ verbraucht wird, dann muß dieses an anderer Stelle wieder nachgeliefert werden. In unseren Zellen gibt es neben der Glycolyse noch zahlreiche andere Reaktionen, die NAD+ verbrauchen, aber nur zwei, die nennenswerte Mengen erzeugen: 1. Reduktion von Sauerstoff zu Wasser, die mit der Oxidation von NADH/ H+ zu NAD+ in den Mitochondrien im Rahmen der Atmungskette verbunden ist (aerob) Adrian Knispel -2- 21. März 2003 2. Reduktion von Pyruvat zu Laktat im Cytoplasma, bei der gleichzeitig NADH/H+ zu NAD+ oxidiert wird (anaerob) Im Normalfall ist ausreichend Sauerstoff vorhanden, so daß NAD+ in der Atmungskette regeneriert werden kann. Pyruvat wird dabei in die Mitochondrien eingeschleust und dort vollständig zu CO2 und H2O abgebaut (=oxidiert). Bei intrazellulärem Sauerstoffmangel entsteht nun durch die Glycolyse immer mehr NADH/H+ im Cytoplasma, daß aber in der Atmungskette nicht mehr zu NAD+ regeneriert werden kann. Ohne dieses kommt jedoch die Glycolyse zum Stillstand, weil es für die Reaktion von Glyceral-3-Phosphat zu 1,3-Bisphosphatglycerat benötigt wird. Einziger Ausweg ist dann die Reduktion von Pyruvat zu Laktat, bei der gleichzeitig NADH/H+ durch die Laktat-Dehydrogenase (LDH) zu NAD+ oxidiert wird. Für die Entstehung von Laktat in unserem Körper sind zwei Zelltypen wichtig. Unsere Erys sind allein auf die Glycolyse angewiesen, weil sie keine Mitochondrien besitzen und damit keine Atmungskette ausführen können. Sie können also nur über die anaerobe Glycolyse Energie erzeugen. Die LDH reoxidiert das NADH/H+ und gibt das entstehende Laktat ins Blut ab. In unserem Muskelzellen entsteht immer bei einem Sauerstoffmangel vermehrt Laktat. Das ist bei starker Muskelaktivität und Dauerleistungen der Fall. Über die anaerobe Glycolyse kann der Muskel sich so zusätzliche Energie holen. Adrian Knispel -3- 21. März 2003 2.Gluconeogenese im Überblick Die Gluconeogenese ist die endogene Biosynthese von Glucose aus Nicht-Zuckern. Da die Glykogenvorräte unserer Leber beschränkt sind, ist unser Körper in manchen Situationen auf eine funktionierende Gluconeogenese angewiesen. Schon nach einer einzigen Nacht wird sie verstärkt betrieben – so richtig legt sie bei schwerer körperlicher Arbeit los. Zum Aufbau der Glucose werden v.a. die Aminosäure Alanin und Laktat (wie gerade schon besprochen aus den Erys und der arbeitenden Muskulatur) verwendet. Daneben dienen auch andere Aminosäuren und Glycerin der Glucoseneubildung. Die meisten Reaktionen der Glycolyse sind reversibel und laufen bei der Gluconeogenese einfach in die entgegengesetzte Richtung. Die drei Schlüsselreaktionen der Glycolyse allerdings (welche waren das noch gleich?) sind irreversibel und müssen so mit Alternativen ersetzt werden. Daher sind sie natürlich die Schlüsselreaktionen der Gluconeogenese. Obwohl die Gluconeogenese Energie kostet, ist sie eine exergonisch ablaufende Reaktion, die irreversibel ist. Dies wird dadurch ermöglicht, daß die exergonen Reaktionen der Glycolyse durch Umgehungsreaktionen ersetzt werden, die eine andere Gleichgewichtslage besitzen und so ebenfalls exergon sind. Eine vollständige Gluconeogenese können nur die Leber, die Nieren und der Darm betreiben. So betreibt die Leber diesen Stoffwechselweg zur Aufrechterhaltung des Blutglucosespiegels. Sie ist das Stoffwechselorgan überhaupt und somit natürlich auch für die Versorgung der anderen Organe (wie Gehirn) mit Energie verantwortlich. Die Nieren betreiben die Gluconeogenese aus einem ganz anderen Grund. In unseren Zellen entstehen z.B. durch die Glycolyse zwei Moleküle Brenztraubensäure, die bei physiologischem pH dissoziiert als Pyruvat und H+ vorliegen. Unsere Nieren scheiden nun diese Protonen wieder aus. Kommen dort nun viele Säuren an (z.B. metabolische Azidose), nutzen auch die Nieren die Gluconeogenese, um aus je zwei Säuren (Pyruvat und eine Aminosäure) Glucose zu machen. Die Epithelzellen des Dünndarms werden nahrungsbedingt manchmal geradezu von Nährstoffen wie Aminosäuren überschüttet. Sie betreiben als dritte die Glucose-Biosynthese, indem sie einige Aminosäuren in Glucose umwandeln und so bereits im Vorwege bei der Homöostase mitwirken. Möchte man die Glycolyse rückwärts beschreiten, müssen unter Energieverlust die drei Schlüsselreaktionen umgangen werden, weil diese nur in eine Richtung ablaufen. Die Schlüsselreaktionen der Glycolyse sind, wie bereits erwähnt: 1. Phosphoenolpyruvat zu Pyruvat 2. Fructose-6-Phosphat zu Fructose-1,6-Bisphosphat 3. Glucose zu Glucose-6-Phosphat Zu 1.: Diese Reaktion liefert in der Glycolyse nicht nur ATP, sondern auch 30 kJ/mol an freier Energie, wodurch es eigentlich nötig wäre, zwei ATP zu spalten, um den Rückweg zu ermöglichen. Die Zelle bedient sich aber einfach eines Umweges über zwei Reaktionen. Im ersten Schritt wird Pyruvat, das im Cytoplasma entsteht, über einen Symporter ins Mitochondrium geschleust, wo es mit Hilfe der Pyruvat-Carboxylase zu Oxalacetat carboxyliert wird. Da Oxalacetat auch ein wichtiges Zwischenprodukt des Citratcyklus ist, entscheidet sich an diesem Punkt der weitere Weg. Je nach Bedarf wird es entweder zu Glucose aufgebaut (nur bei „Hungerstoffwechsellage“) oder zum Energiegewinn über den Citratcyklus und die Atmungskette abgebaut. Das Oxalacetat wird bei der Gluconeogenese mit Hilfe des sog. Malat-Shuttles zusammen mit NADH/H+ aus dem Mitochondrium ins Cytoplasma befördert, wo dann das Oxalacetat zu Phosphoenolpyruvat decarboxyliert wird. Adrian Knispel -4- 21. März 2003 In diesem zweiten Schritt bildet die Phosphoenolpyruvat-Carboxykinase das Schlüsselenzym. Die Besonderheit hier ist, daß anstelle von ATP als Energielieferant GTP benutzt wird. Die nächsten Schritte bis zum Fructose-1,6-Bisphosphat laufen einfach rückwärts im Vergleich zur Glycolyse. Zu 2.: Die Reaktion von Fructose-6-Phosphat zu Fructose-1,6-Bisphosphat ist die stark exergone Schrittmacherreaktion der Glycolyse. In der Gluconeogenese tritt an die Stelle der PFK 1 die Fructose-1,6-Bisphosphatase. Es entsteht im Cytoplasma unter Phosphatabspaltung Fructose-6-Phosphat, welches mit Glucose-6-Phosphat im Gleichgewicht steht. Letzteres geht in die letzte Reaktion der Gluconeogenese ein. Zu 3.: Das Schlüsselenzym dieser Reaktion, die Glucose-6-Phosphatase, gibt es nur dort, wo auch die Gluconeogenese abläuft (Leber, Nierenrinde, Dünndarmepithel). Dieses Enzym spaltet den letzten Phosphatrest ab, wodurch wir das Endprodukt erhalten – Glucose. Die Glucose-6-Phosphatase befindet sich im Endoplasmatischen Retikulum, dem dritten Zellkompartiment der Gluconeogenese. Die freie Glucose kann dann mittels eines Transporters die Membran der Zelle durchdringen und über die Blutbahn alle Organe erreichen. Die Gluconeogenese benötigt also drei Zellkompartimente: das Cytoplasma, die Mitochondrien und das ER. Welche Ausgangssubstanzen zur Gluconeogenese herangezogen werden, hängt immer von den Anforderungen des Organismus ab. Ständiges Substrat ist Laktat, daß immer in großer Menge z.B. von unseren Erys produziert wird. Der Abbau erfolgt vor allem in der Leber, wo es entweder der Atmungskette zugeführt oder von der Leber in Glucose umgewandelt wird. Hungersubstrate sind Alanin und andere glycogene Aminosäuren, die vor allem aus der Muskulatur stammen. Außerdem benötigt die Leber zur Herstellung von Glucose noch Fettsäuren als Energielieferanten (aus Acetyl-CoA kann man KEINE Glucose herstellen). Daneben fällt beim Abbau von Fetten auch Glycerin an, das ebenfalls zur Leber transportiert und dort als Substrat zur Glucoseherstellung dient. Die Gluconeogenese erfolgt über drei verschiedene Einstiegsmoleküle: 1. Pyruvat, das aus Laktat und Alanin entsteht. Auch andere C3-Aminosäuren werden zu Pyruvat abgebaut und dienen so der Biosynthese 2. Oxalacetat dient vielen C4-Aminosäuren als Transportform 3. Glyceron-3-Phosphat entsteht vor allem aus Glycerin und steigt etwas später in die Reaktionsabläufe ein Das aus dem Erythrocyten- und anaeroben Muskelstoffwechsel stammende Laktat wird mithilfe der LDH im Cytoplasma direkt zu Pyruvat umgewandelt. Laktat, das aus der Muskulatur stammt, wird in der Leber zu Glucose umgewandelt und ans Blut abgegeben, sodaß es erneut vom Muskel aufgenommen werden kann. Wenn unsere Muskulatur also mal anstrengend arbeitet, kann sie diese Glucose natürlich gut gebrauchen. Dieser Zyklus wird nach seinen Entdeckern Gerty und Carl Cori als Cori-Zyklus bezeichnet. In Hungerzeiten ist die wichtigste Vorstufe von Glucose das Alanin aus der Muskulatur. Beim Abbau von Muskelproteinen und deren Aminosäuren entsteht zuerst Pyruvat, welches dann durch die Alanin-Transaminase zu Alanin umgewandelt wird. Alanin gelangt über das Blut in die Leber und wird dort (ebenfalls über die Alanin-Transaminase) in Pyruvat zurückverwandelt. Nun kann auch hier wieder Glucose gebildet werden, die dann mit dem Blut der Muskulatur zur Verfügung gestellt wird. Adrian Knispel -5- 21. März 2003 Welche Energiebilanz können wir nun für die Gluconeogenese erstellen? Sie kostet natürlich wie alle Biosynthesen Energie in Form von ATP. Es müssen insgesamt 3 Reaktionen der Glycolyse umgangen werden, die jeweils 1 ATP kosten: 1. Pyruvat zu Oxalacetat 2. Oxalacetat zu Phosphoenolpyruvat (als GTP) 3. 3-Phosphoglycerat zu 1,3-Bisphosphoglycerat Für ein Molekül Glucose laufen diese Reaktionen zwei Mal ab, was einem Bruttoverlust von 6 ATP entspricht. Da man beim Abbau von Glucose zum Pyruvat wieder 2 ATP gewinnt, beträgt der Nettoverlust also 4 ATP. Die Gluconeogenese ist in allererster Linie für die Konstanz des Blutglukosespiegels verantwortlich. Wie man an der Energiebilanz sieht, läßt sich die Zelle diese Konstanz einiges kosten... Adrian Knispel -6- 21. März 2003 3.Regulation von Glycolyse & Gluconeogenese Zur Regulation der Glycolyse und der Gluconeogenese gibt es unterschiedliche Möglichkeiten. Zum einen kann jede Zelle in einem gewissen Umfang ihre Stoffwechselwege autark regulieren. Dabei werden die Schlüsselenzyme von bestimmten Stoffen kontrolliert, die innerhalb der Zelle gebildet werden und verschiedene Zustände signalisieren. Dies bezeichnet man als allosterische Regulation. Sie sorgt zum einen dafür, daß nur so viele Produkte hergestellt werden, wie gerade benötigt. Eine Leberzelle z.B. kann nur dann Glucose herstellen, wenn sie selbst genügend Energie zur Verfügung hat – ansonsten würde sie sich kaputt arbeiten, und davon hätte sie wenig. Der Körper verwendet zur Steuerung des Stoffwechsels außerdem Hormone. Diese Botenstoffe erreichen über das Blut alle Organe, übermitteln ihre Informationen aber nur an diese, die auch die passenden Rezeptoren für diese Hormone besitzen. Über die Rezeptoren und einen zweiten, nun intrazellulären Botenstoff wird die Botschaft an die Zelle weitergeleitet. Für die Hormone des Stoffwechsels übernimmt meist cAMP die Rolle des second messengers. Das cAMP ist ein allosterischer Aktivator. Ein hoher cAMP-Spiegel in der Zelle ist ein Hungersignal. Es zeigt einen niedrigen Blutglucosespiegel an. Die allosterische Regulation der Glycolyse ist eine intrazelluläre Regulation, die hormonunabhängig funktioniert. Grundprinzip dabei ist eine bei den Schlüsselreaktionen ansetzende Aktivierung oder Hemmung von Enzymen. So wirken Stoffe, die eine gute Energieversorgung der Zelle anzeigen (wie ATP) als Hemmstoffe der Glycolyse. Diesen hemmenden Effekt hat auch Citrat, eine Substanz, an deren Entstehung Pyruvat beteiligt ist. Steigt der intrazelluläre Citratgehalt, wird dieses vermehrt als Baustein für Biosynthesen verwendet. Steigt der Spiegel noch weiter, liegt irgendwann mehr Citrat in der Zelle vor, als für die Biosynthesen verwendet werden kann. Ab diesem Zeitpunkt hemmt Citrat die Glycolyse und damit seine eigene Produktion, um eine Überschwemmung mit Citrat in der Zelle zu vermeiden. ADP und AMP hingegen wirken aktivierend auf die Glycolyse, weil sie ja einen Energiebedarf der Zelle anzeigen. Bei der PFK-1 handelt es sich um eines der kompliziertesten regulatorischen Enzyme. Da sie das erste Schlüsselenzym ist, daß ausschließlich in der Glycolyse arbeitet (Hexokinase kann ja auch andere Stoffe umsetzen), ist sie die wichtigste Kontrollstelle des Stoffwechselweges. Ein allosterischer Stimulator der PFK-1 ist Fructose-2,6-Bisphosphat (gibt es nur in Leber und Muskulatur). Fructose-2,6-Bisphosphat beschleunigt also die Glycolyse. Für dessen Produktion und Abbau verfügen Leber und Muskelzellen über ein bifunktionales Enzym, also ein Enzym mit zwei unterschiedlichen enzymatischen Funktionen. • Ein Teil des Enzyms ist die PFK-2 (nicht verwechseln mit PFK-1!!), die die Herstellung von Fructose-2,6-Bisphosphat katalysiert. • Der zweite Teil des Enzyms ist die Fructose-2,6-Bisphosphatase, die ein Phosphat-Molekül aus Fructose-2,6-Bisphosphat abspaltet, wodurch wieder Fructose-6-Phosphat entsteht. Das bifunktionale Enzym und damit die Glycolyse von Leber und Muskulatur werden genau entgegengesetzt reguliert. Dazu einfach zwei Beispiele: Nehmen wir an, unser Körper befindet sich in Alarmbereitschaft oder im Hungerzustand. Im Blut befinden sich dann die Hormone Adrenalin und Glukagon. Beide bewirken über einen intrazellulären Ansteig von cAMP eine Phosphorylierung interkonvertierbarer Enzyme (diese Enzyme werden in der Glycolyse durch Anhängen eines Phosphates inaktiviert), zu denen auch das bifunktionale Enzym gehört. Wird dieses phosphoryliert, dann - ist in der Leber der PFK-2-Teil inaktiv und die Fructose-2,6-Bisphosphatase aktiv. Die Glycolyse wird also gebremst. Da gleichzeitig über andere Enzyme die Gluconeogenese Adrian Knispel -7- 21. März 2003 - beschleunigt werden kann, kann die Leber also Glucose ins Blut zur Versorgung anderer Organe abgeben. in der Muskulatur ist der PFK-2-Teil dagegen aktiv und die Fructose-2,6-Bisphosphatase inaktiv. Das entstehende Fructose-2,6-Bisphosphat beschleunigt somit die PFK-1Reaktion und so auch die Glycolyse. Gleichzeitig wird über andere Enzyme der Glykogenabbau gefördert, wodurch die Muskulatur viel Energie gewinnt, die sie für ihre Arbeit benötigt. Nehmen wir nun an, der Körper befindet sich in einem gesättigtem Ruhezustand. Im Blut befinden sich dann reichlich Glucose und Insulin, der intrazelluläre cAMP-Spiegel ist niedrig und die interkonvertierbaren Enzyme liegen dephosphoryliert vor. - in der Leber ist nun die PFK-2 aktiv, die Fruktose-2,6-Bisphosphatase dagegen inaktiv. Die Glycolyse läuft also auf Hochtouren. Über andere Enzyme wird gleichzeitig die Gluconeogenese gehemmt und die Glykogensynthese gefördert. Die Leber nimmt also die überschüssige Glucose aus dem Blut auf, baut sie zu Energie ab und legt Glykogenvorräte für schlechte Zeiten an. - in der Muskulatur ist die PK-2 inaktiv und die Fructose-2,6-Bisphosphatase aktiv – die Glycolyse wird gedrosselt und über andere Enzyme gleichzeitig die Glykogensynthese gefördert. Die Muskulatur ruht also und legt Glykogenvorräte für aktivere Zeiten an. Die gegenläufige Reaktion des bifunktionalen Enzyms ist also für die Koordination des Organstoffwechsels durchaus sinnvoll. Die hormonelle Regulation des Kohlenhydratstoffwechsels durch Glucagon und Insulin ist weniger für die Geschwindigkeit der Glycolyse zuständig als die allosterische Komponente, sondern vielmehr für deren Aktivität überhaupt. Glucagon wird bei einem niedrigen Blutglucosespiegel ausgeschüttet und erhöht den cAMPSpiegel in der Leber – alle Signale stehen also auf Hunger. Dies führt nun dazu, daß die interkonvertierbaren Enzyme phosphoryliert und damit in der Glycolyse gehemmt werden, wodurch der Glucoseabbau der Leber gedrosselt wird. Die Glucose kann somit in anderen Organen, die die Glucose dringender benötigen, verstoffwechselt werden. Insulin wird nach Nahrungsaufnahme ins Blut abgegeben und senkt den cAMP-Spiegel der Leber und der Muskulatur. Die Glycolyseenzyme werden dephosphoryliert, der Glucoseabbau in der Leber aktiviert und die Glycolyse in den Muskeln reduziert. Nach Nahrungsaufnahme wird die überschüssige Glucose also in der Leber abgebaut und in Speicherstoffe (Glycogen) umgewandelt. Der Muskel ruht dann auch meist und baut seine Glycogenvorräte wieder auf. Auch die Gluconeogenese wird natürlich allosterisch und hormonell reguliert. Hier ist so z.B. die Pyruvat-Carboxylase für den geschwindigkeitsbestimmenden Schritt verantwortlich. Außerdem fördern ATP und NADH/H+ (Zeichen dafür, daß genügend Energie vorhanden ist) die Gluconeogenese. ADP dagegen hemmt sie. Fructose-2,6-Bisphosphat spielt auch bei der Gluconeogenese eine große Rolle. Allerdings hat es hier einen genau gegenteiligen Effekt: Fructose-1,6-Bisphosphat wird durch dieses Enzym allosterisch gehemmt, während ein Mangel davon einen niedrigen Blutglucosespiegel anzeigt, wodurch die Fructose-1,6-Bisphosphatase aktiviert wird. Dieser Mangel wird in erster Linie durch Glucagon verursacht. Auch die hormonelle Regulation erfolgt gegensinnig zur Glycolyse. Glucagon sorgt über eine Erhöhung des cAMP-Spiegels in der Leber für Phosphorylierung der interkonvertierbaren Enzyme, wodurch die Pyruvatkinase inaktiv und somit die Glycolyse gehemmt , die Gluconeogenese dagegen aktiv ist. Außerdem bewirkt Glucagon eine Induktion aller Schlüsselenzyme der Gluconeogenese. Insulin hemmt über eine Repression die Biosynthese der Schlüsselenzyme der Gluconeogenese. Adrian Knispel -8- 21. März 2003 Zusammenfassend möchte ich noch einmal die wichtigsten Möglichkeiten zur Regulation des Stoffwechselgeschehens aufführen: 1. Der Stoffwechsel wird durch den Organismus gesteuert, der seine Wünsche den Zellen über Hormone mitteilt. 2. Der Stoffwechsel wird innerhalb der Zelle über allosterische Effektoren reguliert, die bestimmte Enzyme aktivieren oder deaktivieren. Wichtig für Glycolyse und Gluconeogenese ist, daß beide Faktoren immer gemeinsam wirken. Wird die Glycolyse gefördert, wird die Gluconeogenese außerdem gehemmt, was ja auch Sinn macht. Dieser gegenläufige Effekt wird von ein- und demselben Enzym, einem bifunktionalen Enzym, gesteuert. Adrian Knispel -9- 21. März 2003