Paraneoplastische neurologische Syndrome
Werbung

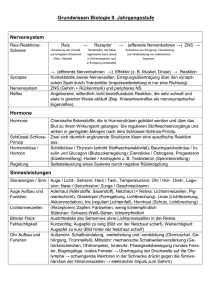
Immunologie Klaus-Peter Wandinger Lübeck Paraneoplastische neurologische Syndrome Klinik und Labordiagnostik In den vergangenen Jahren wurden bei neurologischen Krankheitsbildern zahlreiche neue Autoantikörper identifiziert, von denen ein Großteil Eingang in die Diagnostik gefunden hat. Eine herausragende klinische Bedeutung besitzen dabei Autoantikörper bei paraneoplastischen neurologischen Syndrome (PNS), da sie die frühzeitige Diagnose eines bislang unbekannten Tumorleidens ermöglichen können. Als paraneoplastische neurologische Syndrome (PNS) werden Erkrankungen des zentralen und peripheren Nervensystems bezeichnet, die in unmittelbarem Zusammenhang mit einem Tumorleiden auftreten, jedoch nicht durch den Tumor bzw. seine Metastasen direkt verursacht werden oder als Nebenwirkung auf eine Therapie mit Zytostatika oder durch Bestrahlung zurückzuführen sind [1]. Vielmehr ist eine immunvermittelte Pathogenese der neurologischen Störungen naheliegend, da sich bei vielen Patienten mit PNS spezifische Autoantikörper im Serum nachweisen lassen. Diese Autoantikörper richten sich gegen Antigene, die normalerweise ausschließlich auf der Oberfläche (Membranproteine) oder im Inneren (Zytoplasma oder Nukleus) von Nervenzellen vorkommen. Im Zuge der Entartung (maligne Transformation) werden diese Proteine nun auch von Tumorzellen gebildet. Maligne Zellen unterscheiden sich durch eine Vielzahl veränderter morphologischer, biochemischer und physiologischer Eigenschaften von normalen Körperzellen. Aufgrund dieser Unterschiede, die in Art und Ausmaß sehr stark variieren, können sie vom Immunsystem als „fremd“ erkannt und angegriffen werden. Bei Patienten mit PNS werden im Rahmen dieser antitumoralen Immunantwort auch Antikörper gegen die neuronalen Proteine gebildet, die außerhalb des Nervensystems als unphysiologische, d. h. fremde Strukturen wahrgenommen werden. Bei der Nomenklatur dieser onkoneuralen Antikörper folgt man zwei unterschiedlichen Prinzipien. Zum einen orientiert man sich am Namen des Patienten, bei dem der Antikörper erstmals nachgewiesen wurde (z. B. Hu für Hull, Ri für Richards, Yo für Young, Ma für Margret), während zum anderen das immunhistochemische Färbemuster beschrieben wird (PCA für Purkinje Cell Antibody). Abb: 1: Kernspintomographischer Befund einer Patientin mit „Anti-Ma assoziierter paraneoplastischer Enzephalitis“. Die Pfeile markieren beidseitige, hyperintense Läsionen, die den Entzündungsprozess im Bereich des Hirnstammes widerspiegeln (modifiziert nach Prüss et al. 2008). 266 Fachbeiträge MTA Dialog 4 (2008) Jahrgang 9 Man vermutet, dass in einem Individuum im Laufe seines Lebens viele Zellen zu Tumorzellen entarten. Es ist unbekannt, wie häufig maligne Zellen durch eine effiziente Immunantwort tatsächlich erfolgreich aus dem Körper entfernt werden. In der medizinischen Literatur werden aber zahlreiche Einzelfälle beschrieben, in denen sich ein Tumor von selbst zurückbildete (so genannte Spontanheilungen). Wo ein Tumor jedoch heranwächst und metastasiert, ist das Immunsystem offensichtlich nicht in der Lage, eine ausreichende Abwehr gegen die Tumorzellen zu bilden. Paraneoplastische Syndrome werden bei weniger als 1 % aller Tumorerkrankungen beobachtet. Von besonderer klinischer Bedeutung ist die Tatsache, dass die neurologischen Symptome der Entdeckung des auslösenden Tumors in der Regel Monate bis Jahre vorausgehen. Der Primärtumor ist dann meistens noch sehr klein (z. B. Mikrokarzinom der Mamma) und, im Idealfall, einer kurativen Therapie noch zugänglich. Bei Nachweis der Reaktivitäten AntiHu, Anti-Yo, Anti-Ri, Anti-Amphiphysin, Anti-CV2 oder Anti-Ma2 ist die Wahrscheinlichkeit, dass zum Zeitpunkt der Befunderhebung oder innerhalb der kommenden 5 Jahre ein Tumor nachgewiesen werden kann, größer als 95 %. Diese Antikörper sind deshalb besonders wichtig und werden auch als „PNS-definierende Antikörper“ bezeichnet [2]. In ungefähr zwei Drittel der Fälle ist den Patienten zum Zeitpunkt des Auftretens der neurologischen Symptome ein Tumor noch nicht bekannt. Die immunologische Diagnostik vermag hier einen entscheidenden Beitrag zur Früherkennung von Krebserkrankungen zu leisten. Denn werden im Rahmen der Zuordnung des neurologischen Krankheitsbildes im Labor onkoneurale Antikörper nachgewiesen, so muss eine rasche und gründliche Tumorsuche mittels Ganzkörper-CT, Gastroskopie und Koloskopie, ggf. Positronen-Emissi- ons-Tomographie (PET)/CT-Untersuchung bis hin zu einer Biopsie und operativen Verfahren geführt werden. Lässt sich zum Zeitpunkt der Erstvorstellung kein Tumor nachweisen, so sollten in regelmäßigen Abständen Nachuntersuchungen erfolgen mit dem Ziel, den zugrundeliegenden Tumor im Frühstadium zu diagnostizieren und zu therapieren. Symptome und Verlauf Paraneoplastische neurologische Syndrome können alle Ebenen des Nervensystems betreffen und sind daher bei den meisten Differenzialdiagnosen der Neurologie in Erwägung zu ziehen (Tab. 1). Zu den häufig betroffenen Strukturen zählt das Großhirn (Enzephalon) und Rückenmark (Myelon), das Kleinhirn (Zerebellum), der Hirnstamm (vor allem Rhombenzephalon) und das limbische System (Abb. 1). Gleichermaßen können sich PNS auch im Bereich des peripheren Nervensystems (Neuropathie), der neuromuskulären Synapse (Myasthenia gravis und Lambert-Eaton-Syndrom), des quergestreiften Muskels (nekrotisierende Myositis) sowie der Haut (Dermatomyositis) abspielen. In der Regel sind paraneoplastische Syndrome des Zentralnervensystems mit Antikörpern gegen zytoplasmatische (z. B. CV2, Yo) und nukleäre (Hu, Ri, Ma) Proteine vergesellschaftet, während bei peripheren PNS die Autoimmunantwort Tab. 1: Klinisch relevante paraneoplastische Autoantikörper. Antikörper (Synonym) Anti-Hu (ANNA-1)* Anti-Yo (PCA-1)* Anti-Ri (ANNA-2)* Anti-PNMA1 (Ma1)* Antigen (Molekulargewicht) Hu-Proteine (38 kDa) cdr2, cdr62 (34 kDa und 62 kDa) NOVA (55 kDa und 80 kDa) Ma-Proteine (37 kDa und 40 kDa) Fluoreszenz-Muster Paraneoplastisches Syndrom Enzephalomyelitis sensible Neuropathie Kleinhirndegeneration Zellkerne zentraler und peripherer Neurone Zytoplasma der Purkinjezellen Zellkerne zentraler Neurone Opsoklonus-MyoklonusSyndrom Nervenzellnucleoli Rhombenzephalitis (Hirnstamm) limbische Enzephalitis Anti-PNMA2 Ma-Proteine Nervenzellnucleoli Rhombencephalitis (Ma2, Ta)* (41,5 kDa) (Hirnstamm) limbische Enzephalitis Anti-AmphiAmphiphysin Präsynaptische NervenStiff-Person-Syndrom physin* (128 kDa) enden des Kleinhirns Anti-CV2 CRMP5 Zytoplasma der OligoEnzephalitis (Anti-CRMP5)* (66 kDa) dendrozyten PCA2 Purkinje-Zellprotein Zytoplasma und Dendriten Enzephalitis (280 kDa) der Purkinjezellen Neuropathie Anti-Tr unbekannt Zytoplasma der PurkinjeKleinhirndegeneration (PCA-Tr) zellen, punktartige Färbung der Molekularschicht Anti-mGluR1 metabotroper Glutamat- Zytoplasma der Kleinhirndegeneration rezeptor (ca. 140 kDa) Purkinjezellen Anti-Recoverin Recoverin Photorezeptoren der Retina Retinopathie (23 kDa und 65 kDa) Anti-Titin Titin quergestreifte Muskulatur Myasthenia gravis GAD Glutamatdecarboxylase Körnerschicht des Kleinhirns Stiff-Person-Syndrom (65 kDa und 67 kDa) und Inselzellen (Pankreas) Häufigste Tumore SCLC, Neuroblastom Ovar, Mamma, Uterus Mamma, SCLC Mamma, verschiedene Hoden Mamma, SCLC SCLC, Thymom SCLC M. Hodgkin M. Hodgkin SCLC Thymom Mamma, SCLC, Kolon * PNS-definierende Antikörper. Der Nachweis dieser Antikörper im Serum von Patienten mit entsprechenden neurologischen Symptomen spricht für das Vorliegen eines PNS, selbst dann, wenn zum Zeitpunkt der Diagnose kein Tumor nachweisbar ist. SCLC: kleinzelliges Bronchialkarzinom (small-cell lung carcinoma); CDR: cerebellar degeneration-related antigen; NOVA: neuronal onconeural ventral nervous system antigen. hauptsächlich gegen zelluläre Membranproteine (z. B. Lambert-Eaton-Syndrom: spannungsabhängige Kalziumkanäle, VGCC; Neuromyotonie: spannungsabhängige Kalium- kanäle, VGKC) gerichtet ist. Neben rein neurologischen Ausfällen können auch psychiatrische und unspezifische Symptome auftreten. Aufgrund ihrer Seltenheit werden PNS ® -Taumel-Rollenmischer 349/ Aus dem umfassenden Assistent®-Programm mit mehr als 6000 Assistent®-Produkten für die Arbeit im Labor. Nr. 349/1030: Zehn gleichmäßig drehende PVC-Rollen (herausnehmbar) bieten eine taumelnde Liegefläche für diverse Probefläschchen. Variable Drehzahlregelung – stufenlos von 2 -30 U./min. Nr. 349/530: 5 Rollen, nicht herausnehmbar, 2 -30 U./min. variabel. Nr. 349/580: s. oben,10- 80 U./min. variabel. Info´s beim Fachhandel. Karl Hecht KG Glaswarenfabrik Präzisions-Instrumente und -Geräte – für Arzt und Labor D-97647 Sondheim / Rhön / Germany - Telefon (0 97 79) 808-0 - Telefax (0 97 79) 808-88 CH-8595 Altnau TG / Switzerland - Tel. (071) 6 95 22 22 - Fax (071) 6 95 22 27 F-91430 Igny / Paris - Z.I. 5, Rue Lavoisier - Tél. (01) 69 35 36 50 - Fax (01) 60 19 0715 A-6122 Fritzens / Tirol - Fischerweg 4 - Tel. (0 52 24) 5 26 46-0 - Fax (0 52 24) 5 76 79 Besuchen Sie uns im Internet: http://www.hecht-assistent.de e-mail: info@ hecht-assistent.de ANALYTICA in München (1.- 4. April 2008): Sie finden uns in Halle B 2, Stand-Nr. 230 MTA Dialog 4 (2008) Jahrgang 9 Fachbeiträge 267 Immunologie sible Ausfälle (Taubheitsgefühl, Störung des Lagesinns) ohne Lähmungen im Bereich der Extremitäten (subakute sensible Neuropathie). Bei der limbischen Enzephaa b litis stehen Gedächtnisstörungen, psychische Auffälligkeiten und epileptische Anfälle im Vordergrund. Ein klinisch eindrucksvolles Krankheitsbild ist das Stiffc d Person-Syndrom, das durch eine schmerzhafte Steifigkeit der rumpfnahen Muskulatur mit zusätzlich einschießenden Spasmen bei Schreckreizen gekennzeichnet ist. Wichtige Differene f tialdiagnosen stellen Autoimmunerkrankungen wie die Multiple Sklerose sowie parainfektiöse Erkrankungen dar, bei denen die Symptome im Rahmen der Immunantwort gegen verschievirale oder g h dene bakterielle Erreger entstehen (z. B transverse Myelitis). Die autoimmunvermittelte limbische Enzephalitis muss stets von einer Herpes-Enzephalitis abgegrenzt werden. j Bei letzterer werden i Abb. 2: Nachweis onkoneuraler Autoantikörper mit dem indirekten Immunfluoreszenz- die Nervenzellen des test. (a) Anti-Hu-Antikörper (Synonym ANNA-1: Anti-Neuronale Nukleäre Antikörper): Granuläre Temporalhirns durch Fluoreszenz nahezu aller Neuronenkerne des Kleinhirns, (b) Anti-Hu-Antikörper färben den Plexus direkten Virusbefall myentericus des Darmes an. (c) Anti-Ri Antikörper weisen ebenfalls eine Färbung der Neuronengeschädigt und eine kerne des Kleinhirns auf, jedoch findet hier niemals eine Reaktion mit peripheren Neuronen (Plexus myentericus negativ) statt (d). (e) Fluoreszenz bei Antikörpern gegen CV2 (Oligodendrozyten), (f) unmittelbare medikaAnfärbung der Purkinje-Zellen bei Anti-Yo-Antikörpern (PCA-1: Purkinje-Zellen-Autoantikörper). mentöse Therapie ist PCA-2-Antikörper zeigen eine Färbung des Zytoplasmas und der Dendriten der Purkinjezellen (g), dringend erforderlich. bei Vorliegen von Antikörpern gegen Tr zeigt sich zusätzlich eine fleckige Fluoreszenz in der MoMyasthenie und lekularzellschicht (h). Autoantikörper gegen das Enzym Glutamatdecarboxylase (GAD) rufen eine Stiff-Person-Syndrom Fluoreszenz der Körnerschicht des Kleinhirns (i) sowie der Pankreasinseln (j) hervor. können auch als eigenständige, nicht im klinischen Alltag leicht überse- paraneoplastische Autoimmunerhen. Zu den Beschwerden, bei de- krankungen auftreten. Der zusätznen immer eine paraneoplastische liche Nachweis von Antikörpern geUrsache in Betracht gezogen wer- gen Titin und gegen Amphiphysin den muss, gehören eine langsam deutet bei diesen Krankheitsbildern fortschreitende Stand- und Gang- jedoch immer auf einen zugrundeunsicherheit mit Sprechstörung und liegenden Tumor hin (Tab. 1). Der ggf. Doppelbildern (subakute Klein- natürliche Verlauf paraneoplastihirndegeneration) sowie rein sen- scher Syndrome kann variieren. 268 Fachbeiträge MTA Dialog 4 (2008) Jahrgang 9 Eine spontane Besserung der neurologischen Symptome und sogar eine spontane Tumorregression wurden beschrieben [3, 4]. Oberstes Ziel in der Behandlung von Patienten mit PNS ist die rasche Identifizierung und Entfernung des zugrundeliegenden Primärtumors. Wahrscheinlich aufgrund der oftmals biologisch wirksamen, natürlichen Immunantwort können die Tumore allerdings, wie eingangs beschrieben, für lange Zeit klein und ohne klinische Symptome bleiben. Zur Milderung der neurologischen Beschwerden wird in der Regel eine symptomatische, immunmodulatorische oder immunsuppressive Therapie eingeleitet (z. B. Kortikosteroide, intravenöse Immunglobuline, Plasmapherese), die bezüglich ihrer Wirksamkeit allerdings große Unterschiede zwischen einzelnen Patienten aufweist. Im klinischen Alltag hat sich gezeigt, dass immuntherapeutische Maßnahmen umso mehr Aussicht auf Erfolg haben, je früher sie begonnen werden. Hervorzuheben ist, dass eine Immuntherapie bei der Mehrzahl der Patienten nicht mit einem beschleunigten Wachstum des Tumors einhergeht. Labordiagnostik Aufgrund der herausragenden klinischen Bedeutung besteht die Aufgabe der Labordiagnostik darin, onkoneurale Antikörper im Patientenserum zuverlässig und eindeutig zu erfassen. Um eine größtmögliche Spezifität und Sensitivität der Untersuchung zu gewährleisten wird der Antikörpernachweis daher immer mit zwei unterschiedlichen Testmethoden geführt [2]. Zum einen wird mit Hilfe der fluoreszenzmikroskopischen (indirekte Immunfluoreszenz; IFT) oder lichtmikroskopischen Immunhistochemie untersucht, ob das Patientenserum eine spezifische Reaktivität mit Gewebe neuronalen Ursprungs aufweist. Als Zielstruktur dienen hier die im Zellverbund (in situ) in nativer Form exprimierten Moleküle. Anhand des Bindungsmusters der Autoantikörper auf verschiedenen Geweben lassen sich Rückschlüsse auf das zugrundeliegende Zielantigen ziehen (Abb. 2). Zur Darstellung des größtmöglichen Antigenspektrums wird parallel eine Kombination aus verschiedenen Gewebesubstraten, z. B. Primatenklein- hirn (zentrale Neurone: Purkinjezellen, graue und weiße Substanz in übersichtlicher histologischer Anordnung), Primatendarm (marklose Nerven, autonomes Nervensystem) und peripherer, markhaltiger Primatennerv, eingesetzt. Antikörper gegen das Enzym Glutamatdecarboxylase (GAD), die neben dem Diabetes mellitus auch bei Stiff-Person-Syndrom auftreten, werden zusätzlich auf dem Substrat Primatenpankreas nachgewiesen. Mit Hilfe humaner Epithelzellen (HEp-2) wird untersucht, ob im Patientenserum antinukleäre Antikörper (ANA) vorliegen, die natürlich bei der Interpretation der IFT-Ergebnisse berücksichtigt werden müssten. Zum anderen werden die Patientenproben gleichzeitig mit Membran-basierten Testsystemen (Immunblots) analysiert, bei denen die spezifischen Zielantigene, in nativer oder rekombinanter Form, auf Membranstreifen aufgebracht wurden (Abb. 3). Im „Westernblot“ wird ein Antigenvollextrakt aus Primatenkleinhirn verwendet, das elektrophoretisch aufgetrennt und auf a b c ➤ ➤ ➤ ➤ ➤ ➤ ➤ Abb. 3: Membran-basierte Testsysteme zum Nachweis onkoneuraler Autoantikörper. (a) Westernblot mit Banden an spezifischer Stelle im aufgetrennten Kleinhirnextrakt, die eine Reaktion mit den nativen Antigenen Hu, Yo und Ri anzeigen. Im vorliegenden Testsystem werden die Antikörper gleichzeitig mit zusätzlich aufgetragenen rekombinanten Antigenen erfasst (Kombination Westernblot und Linienblot). (b) Beispiele inkubierter Patientenseren auf einem Linienblot. Die PNS-definierenden Antigene sind in aufgereinigter oder rekombinanter Form einzeln auf der Membran angeordnet. (c) Antikörper gegen neuronale Antigene unbekannter Spezifität zeigen auf dem Westernblot Reaktionen mit dem Kleinhirnextrakt, die keiner definierten Bande zugeordnet werden können (Pfeilspitzen). In der indirekten Immunfluoreszenz können derartige Antikörper anhand ihres atypischen Färbemusters erkannt werden. Ja, ich bin an weiteren Informationen über TM Infinity Lithium interessiert! TM Infinity Lithium Assay Name: Neue Standards in der medizinischen Diagnostik! Straße: TM Infinity Lithium Assay: • • • • Institut: schneller als herkömmliche Methoden routinemäßige Abarbeitung auf allen gängigen Analysensystemen kosteneffektiv in der Anwendung stabiles Reagenz mit langer Haltbarkeit PLZ, Ort: Telefon: Fax: Email: TM Ab 1. März 2008 erhalten Sie die Infinity Tests sowie alle anderen Trace Produkte exklusiv bei Microgenics. Microgenics GmbH, Thermo Fisher Scientific, Spitalhofstraße 94, D-94032 Passau, Tel.: +49 851 88689 0, Fax: +49 851 88689 10, [email protected] Bitte ausschneiden und senden an: Microgenics GmbH Thermo Fisher Scientific Spitalhofstraße 94 D-94032 Passau Immunologie Abb. 4: Zellbefund im Liquor bei paraneoplastischen neurologischen Syndromen. In etwa der Hälfte der Fälle zeigt sich eine geringgradige, lympho-monozytäre Pleozytose (30–40 Zellen/µl). Ein unauffälliger Liquorbefund schließt ein PNS jedoch nicht aus. eine Nitrozellulose-Membran aufgetragen wurde. Die Position der Proteine auf dem Blotstreifen ist dabei von deren Molekulargewicht abhängig. Im Serum vorhandene Autoantikörper reagieren mit ihrem jeweiligen Antigen und werden nach Markierung durch einen sekundären Anti-Human-Antikörper an entsprechender Stelle des Streifens als spezifische Bande nachgewiesen. Alternativ kann auch ein „Linienblot“ eingesetzt werden, bei dem die Antigene einzeln, in aufgereinigter oder rekombinanter Form an klar definierter Stelle auf den Membranstreifen aufgetragen sind (Abb. 3b). Westernblots enthalten das komplette in Primatenkleinhirn vorliegende Antigenspektrum und erlauben neben dem Nachweis bekannter Reaktivitäten auch die Identifizierung antineuronaler Antikörper bislang unbeKurz und bündig ■ PNS werden durch Autoimmunreaktionen gegen Proteine verursacht, die normalerweise ausschließlich im Nervensystem vorkommen, im Zuge der Entartung jedoch auch von Tumorzellen gebildet werden. ■ Paraneoplastische Antikörper können dem Tumornachweis bis zu 5 Jahren vorausgehen. ■ Der Nachweis onkoneuraler Antikörper wird stets parallel mit immunhistochemischen Methoden (Antigene im Gewebeverbund) und Immunoblots (definierte Einzelantigene) geführt. ■ ■ 270 Ein positiver Antikörperbefund besitzt eine außerordentliche Bedeutung für die frühe Diagnose eines verborgenen Tumorleidens und erfordert eine umgehende und intensive Untersuchung der Patienten. Ein Tumor ist in der Mehrzahl der Fälle zum Zeitpunkt des Auftretens der neurologischen Symptome und der onkoneuralen Antikörper noch nicht bekannt. Fachbeiträge MTA Dialog 4 (2008) Jahrgang 9 kannter Spezifität. Diese treten nach Reaktion mit den jeweiligen Zielantigenen als Banden an atypischer Stelle auf dem Membranstreifen zutage (Abb. 3c). Im klinischen Alltag hat sich aufgrund der einfacheren Auswertbarkeit der Einsatz von Linienblots bewährt. Ein Screening mittels indirekter Immunfluoreszenz oder Immunblots alleine kann nicht empfohlen werden. In der IFT können z. B. Reaktivitäten gegen Antigene der Ma-Familie (Ma1 und Ma2/Ta) aufgrund des besonders schwachen Färbeverhaltens leicht übersehen werden, die dann aber anhand des positiven Signals im Immunblot erkannt werden. Umgekehrt zeigen Anti-Tr Antikörper keine Banden im Westernblot und werden nur mit der IFT erfasst. Die Bestimmung onkoneuraler Antikörper erfolgt in erster Linie aus dem Serum. Der zusätzliche Nachweis der Autoantikörper im Liquor mit Berechnung des spezifischen Index kann in Einzelfällen hilfreich sein, da fast alle Antikörper-positiven paraneoplastischen Patienten mit zentraler Symptomatik auch eine intrathekale Synthese aufweisen. In ca. 50 % der Fälle findet sich bei Patienten mit PNS ein entzündlich veränderter Liquor mit geringer lymphomonozytärer Pleozytose, leichter Erhöhung des Gesamtproteins und einer quantitativ oder qualitativ (oligoklonale Banden) nachweisbaren intrathekalen IgG-Produktion (Abb. 4). Ein normaler Befund ist jedoch ebenfalls mit einem PNS vereinbar. Maligne Zellen sind bei PNS definitionsgemäß nicht im Liquor nachweisbar. Abschließend bleibt zu erwähnen, dass sich onkoneurale Antikörper nur bei etwa 50 % der Patienten mit PNS nachweisen lassen, so dass ein negatives serologisches Ergebnis ein PNS keinesfalls ausschließt. weitergeleitet werden. Zu den unlängst neu bei PNS-Patienten beschriebenen Reaktivitäten zählen Autoantikörper gegen den Transkriptionsfaktor Sox1 (Lambert-EatonSyndrom) und das Zinkfingerprotein Zic4 (Kleinhirndegeneration), die beide bei kleinzelligem Bronchialkarzinom beobachtet wurden, sowie gegen den Glutamatrezeptor Gria1 (Kleinhirndegeneration bei M. Hodgkin). Eine Übersicht über den aktuellen Stand der Forschung auf diesem Gebiet ist auf der Homepage der europäischen Expertengruppe für paraneoplastische neurologische Syndrome unter der Internetadresse www.pnseuronet.org zu finden. ■ Literatur 1. Blaes F, Rauer S, Voltz R, Weller M. Paraneoplastische Syndrome. In: Diener HC (Hrsg.): Leitlinien für Diagnostik und Therapie in der Neurologie, 2. Aufl. Georg Thieme Verlag, Stuttgart, 2003, S. 455–460 2. Graus F, Delattre JY, Antoine JC, Dalmau J, Giometto B, Grisold W, Honorrat J, Smitt PS, Vedeler CH, Verschuuren JJ, Vincent A, Voltz R. Recommended diagnostic criteria for paraneoplastic neurological syndromes. J Neurol Neurosurg Psychiatry 2004; 75:1135-1140 3. Prüss H, Voltz R, Gelderblom H, Bohner G, Munz DL, Zschenderlein R, Wandinger KP. Spontaneous remission of anti-Ma associated paraneoplastic mesodiencephalic and brainstem encephalitis. J Neurol; Epub 2008 Jan 23 4. Darnell RB, DeAngelis LM. Regression of small-cell lung carcinoma in patients with paraneoplastic neuronal antibodies. Lancet 1993; 341:21-22 Der Autor: Priv.-Doz. Dr. med. Klaus-Peter Wandinger EUROIMMUN Labordiagnostika AG Seekamp 31 23560 Lübeck Mail: [email protected] Ausblick Es ist davon auszugehen, dass mit zunehmender Kenntnis über paraneoplastische neurologische Syndrome zukünftig weitere neue onkoneurale Autoantikörper identifiziert werden. Patientenseren, die ein atypisches Muster in der immunhistochemischen Untersuchung oder nicht eindeutig zuzuordnende Banden im Westernblot aufzeigen, sollten zur Analyse an ein Speziallabor Der Autor ist Facharzt für Neurologie mit Fachkunde Laboruntersuchungen im Gebiet Neurologie. Er arbeitete und forschte in Deutschland und den USA im Bereich der Immunologie, Neuroimmunologie und Neurologie. Seit 2007 ist er tätig als Direktor des Bereiches Internationale Wissenschaftliche Kommunikation bei der Firma EUROIMMUN.