Der Citratzyklus
Werbung
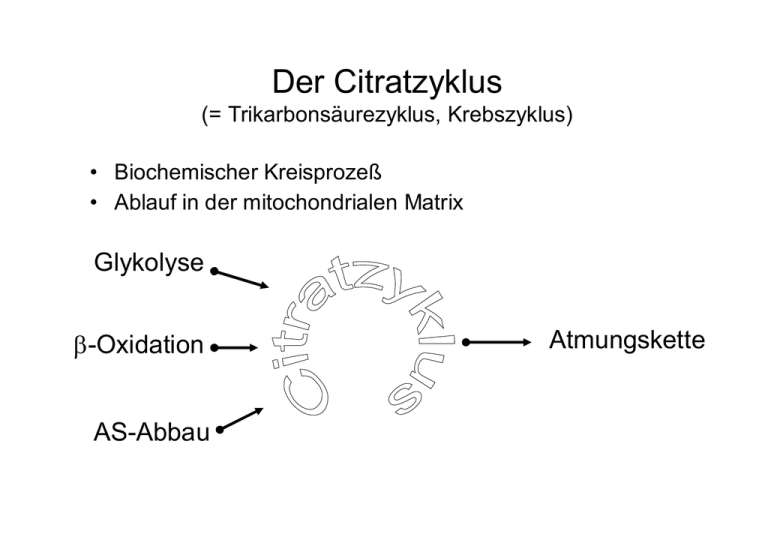
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) • Biochemischer Kreisprozeß • Ablauf in der mitochondrialen Matrix Glykolyse β-Oxidation AS-Abbau Atmungskette Der Citratzyklus Der Citratzyklus: Übersicht Acetat (Acetyl-CoA) Citrat Oxalacetat Oxidative Decarbocylierung Oxidative Decarbocylierung Reduktionsequivalente (3 x NADH, 1 x FADH2) werden in der Atmungskette unter ATP Bildung verbraucht Citrat entsteht durch Kondensation von Oxalacetat und Acetyl-CoA: Citrat wird zu Isocitrat isomerisiert: Gleichgewicht der Reaktion liegt auf Seite des Citrat, jedoch wird Isocitrat aus der Reaktion entfernt! Isocitrat wird durch Oxidation und Decaboxylierung in α-Ketoglutarat übergeführt: Gewinnung von Reduktionsequivalenten: Isocitrat + NAD+ α-Ketoglutarat + CO2 + NADH + H+ Decarboxylierung verschiebt GG der Reaktion! Succinyl-CoA entsteht durch oxidative Decarboxylierung von α-Ketoglutarat: α-Ketoglutarat Dehydrogenase Komplex: Multienzymkomplex, aus 3 Enzymen, ähnlich dem Pyruvat Dehydrogenase Komplex Oxidative Decarboxylierung, es entsteht Succinyl-CoA (vgl. Ox. Decarboxylierung v. Pyruvat: es entsteht Acetyl-CoA) Produkthemmung (durch Succ-CoA) möglich! Regeneration von Oxalactetat durch Oxidation von Succinat : ‚Umwandlung‘ chemischer Energie: Thioesterbindung (Succ-CoA) ⇒ Phosphatesterbindung Regeneration von Oxalactetat durch Oxidation von Succinat : Gewinnung von Reduktionsequivalenten Citratzyklus: Bilanzgleichung Acetyl-CoA + GDP + Pi → 2 CO2 + GTP + 8[H] + CoA-SH Die Kontrolle des Citratzyklus: Allosterische Hemmung der Citrat-Synthase durch ATP Allosterische Aktivierung der IsocitratDehydrogenase durch ADP Produkthemmung, Hemmung durch hohe Energieladung Der Citratzyklus als Sammelbecken des Stoffwechsels: Anaplerotische Reaktionen (Auffüllreaktionen): Zwischenprodukte des Citratzyklus dienen als Vorstufen für die Biosynthese zahlreicher Verbindungen Fehlende Zwischenprodukte müssen gebildet werden! Endoxidation - Atmung • Erfolgt in der Maschinerie der Atmungskette • Enzyme der Atmungskette in der inneren Mitochondrienmembran • Oxidation gekoppelt mit Phosphorylierung = Oxidative Phosphorylierung • Wichtigster Prozess zur ATP Generierung • e- werden von Reduktionsequivalenten auf O2 übertragen Die mitochondriale Atmungskette • Besteht aus vier Enzymkomplexen, die durch zwei mobile eCarrier verbunden sind • Kette von Redoxreaktionen, wobei Wasserstoff und e- von Verbindungen mit negativen Potential (e- - Druck) auf solche mit positiven Potential (e- - Affinität) übertragen • Freiwerdende Energie wird als ATP gewonnen • Wasserstoff + e- werden von NADH + H+ auf O2 übertragen: Überträger von Reduktionsequivalenten: Nicotinamidadenindinucleotid NAD+ ist ein beweglicher Überträger von Wasserstoff bzw. Elektronen Oxidation und ATP-Synthese sind über transmembrane Protonenflüsse gekoppelt: • Stufenweiser Transport von e- auf O2 bewirkt hinauspumpen von H + aus der Matrix • Protonenmotorische Kraft entsteht (pH-Gradient und elektrisches Potential) • Rückfluß der H+ bewirkt Phosphorylierung von ADP zu ATP Oxidation und ATP-Synthese sind über transmembrane Protonenflüsse gekoppelt: Intermembranraum Innere Mitochondrienmembran Mitochondriale Matrix Enzymkomplex I: NADH-Q-Reduktase (NADH-Dehydrogenase) • Übertragung der e- von NADH auf die prosthetische Gruppe, Flavinmononukleotid NADH + H+ + FMN → FMNH2 + NAD+ Mobiler e- Carrier I: Coenzym Q (Ubichinon) FMNH2 + Q → FMN + QH2 NADH-Q Reduktase enthält EisenSchwefel Cluster, Fe wechselt zwischen Fe3+ und Fe2+ e- von FADH2 (siehe Citratzyklus) können hier auf Q übertragen werden (Durch Enzymkomplex II (SuccinatDehydrogenase) Enzymkomplex III: Cytochrom-Reduktase (Ubichinol-Cytochrom-c-Reduktase) eQH2 → Cytochrom b → Cytochrom c Mobiler e- Carrier II Cytochrom: e- übertragendes Protein mit Häm als prosthetische Gruppe: Enzymkomplex IV: Cytochrom-Oxidase (Ubichinol-Cytochrom-c-Oxireduktase) eCytochrom c → Cytochrom a3 → O2 ½ O2 + 2H+ + 2e- → H2O e- - Druck e- - Affinität Ubichinon (Co-Enzym Q): Der Q-Pool ¾Sammelbecken für H+ und e- aus NADH, Succinat u. Fettsre. Abbau ¾Beweglichkeit innerhalb der Membran durch lipophilen Charakter Ubichinon Oxidation und ATP-Synthese sind über transmembrane Protonenflüsse gekoppelt: • Stufenweiser Transport von e- auf O2 bewirkt hinauspumpen von H+ aus der Matrix • Protonenmotorische Kraft entsteht (pH-Gradient und elektrisches Potential) • Rückfluß der H+ bewirkt Phosphorylierung von ADP zu ATP: • Atmungskettenphosphorylierung (Oxidative Phosphorylierung) Energiebilanz: Glukose → H2O + CO2 Palmitat (C16): ATP BOOKKEEPING 7 cycles x 17 ATP/cycle 119 "left over" acetyl CoA 12 ATP and PPi used to "activate" the fatty acid -2 NET ATP Potential 129 200 g Glukose → ca. 40 mol ATP ( 1200 kJ) 200 g Fett → ca. 100 mol ATP ( 3000 kJ) Atmungsquotient: Verhältnis von aufgenommenen O2 und abgegebenem CO2 Veratmung von Glukose: C6H12O6 + 6O2 → 6H2O + 6CO2 1,0 Veratmung von Fettsäure (z.B. Palmitinsäure): Palmitinsre. + 23O2 → 16H2O + 16CO2 0,7 Atmungsquotient: Veratmung von Proteinen: ~ 0,8 Sauerstoffreichere Verbindungen als Glukose (z.B. Oxalsäure): > 1,0 Wichtige Messgröße, Rückschlüsse auf Art des Stoffwechsels möglich Energiegewinn durch Gärung Atmung: e- werden auf O2 übertragen Gärung: e- werden auf org. Moleküle übertragen Energieausbeute bei Gärung ist viel geringer! Verwertung von Glukose: Milchsäuregärung Atmung Alkoholische Gärung Milchsäuregärung: Pyruvat + NADH + H+ → Laktat + NAD+ Laktatdehydrogenase (Oxireduktase) Glykolyse: Reduktionsequivalente entstehen, NAD+ wird verbraucht ⇒ NAD+ muss regeneriert werden, um Glykolyse aufrecht zu erhalten! Milchsäuregärung: Obligat anaerob: Bakterien (Milchsäurebakterien) Fakultativ anaerob: Säugetiere, Mensch O2-Mangel Laktatbildung Blut Leber * Abbau zu CO2 + H2O * Glukoneogenese Alkoholische Gärung: Hefe, Pilze, höhere Pflanzen: Fakultativ anaerob Stoffwechselanpassung bei Abwesenheit von O2 Glukose + 2 Pi + 2 ADP → 2 Ethanol + 2 CO2 + 2 H2O + 2 ATP Alkoholische Gärung: Decarboxylierung NAD+ Regeneration