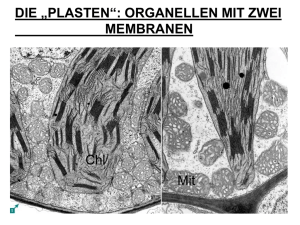
Funktionen der Mitochondrien
Werbung

Vorlesung Biologie für Mediziner WS 2010/11 Teil 1 Zellbiologie (Prof. R. Lill) Themengebiet: Mitochondrien Mitochondrien - Nicht nur Kraftwerke der Zelle • Morphologie • Dynamik des mitochondrialen Retikulums (Fusion / Fission) Mitochondrien - Nicht nur Kraftwerke der Zelle • Morphologie Filme Hefezelle in Zellteilung mit grünen Mitochondrien Movie Egner CrisMito Perkins & Frey Mitochondrium - Cristaestruktur Mitochondrien - Morphologie im EM Muskel Spermium Mitochondrium = Fadenkörperchen Epithelzelle (Schnecke) Mitochondrien • Dynamik des mitochondrialen Retikulums Film (G. Steinberg) NcrassaMito2 Grundwissen Mitochondrien • 4 Kompartimente – Außenmembran, Intermembranraum, Innenmembran, Matrix – Innenmembranauffaltungen: Cristae • Eigener genetischer Apparat – DNA (16.500 bp) , mRNA, tRNA, Ribosomen – Synthese von 13 Proteinen (Mensch), für oxidative Phosphorylierung • Vererbung durch die Mutter • Bekannteste Funktionen – ATP Synthese (Kraftwerk) bei Erwachsenem ca. 60 kg pro Tag – Oxidative Phosphorylierung (= Zelluläre Atmung) – Citratzyklus – Synthese von Eisen-Schwefel Clustern Mitochondrien und Altern • • • “Knock-in” Maus: Trägt eine Mutation der mtDNA Polymerase Folge: Mutationen in mtDNA und damit mtProteinfunktionen Zeigt nach einigen Wochen verfrühte Alterserscheinungen – – – – – – Graues Haar Haarverlust Kyphose Osteoporose Gewichtsverlust Weniger Körperfett N.G. Larsson, 2004 Wie entstehen Mitochondrien ? • Durch Teilung, keine de novo Entstehung • Mitochondrialer Proteinimport (Translokons TOM und TIM) – 98% der Proteine Kern-kodiert – 2% der Proteine mtDNA-kodiert Nukleäre DNA 600-1000 Proteine Präsequenz Reifer Teil N C Typisches Matrixpräprotein TOM TIM AM IMR IM Faltung, Komplex- 13 Proteine bildung mtDN Matrix Amphipathische α-Helix A Proteinimportwege ins Mitochondrium • Matrixproteine (mit Präsequenz) – Cytosolische Chaperone (cytHsp70, Hsp90) – TOM Complex (Rezeptoren, Pore) – TIM23 Complex (Rezeptoren, Pore) – Importmotor (Tim44, mtHsp70-ATP) Pore Sa m – Präsequenzprozessierung (Matrix Prozessierungspeptidase = MPP) – Faltung und Assemblierung (mtHsp70-ATP, Hsp60) Tim44 • Innenmembranproteine – Cytosol. Chaperone & TOM – Kleine Tims (TIM8 Mutation: Dystonie-Taubheit) – TIM22 Complex (Rezeptoren, Pore) • Außenmembranproteine – TOM & SAM Complex • Importiert β-barrel Proteine & Porin) Wie entstanden Mitochondrien in Evolution? • Aus Bakterien Endosymbionten-Hypothese Aufnahme eines Bakteriums in eine Wirtszelle per Endozytose • Bakterien und Mitochondrien weisen Ähnlichkeiten auf in – Proteinen – Ribosomen (Größe 70S; gleiche Antibiotika inhibieren) – biochemischen Funktionen • Oxidative Phosphorylierung • Citratzyklus • Herstellung von Eisen-Schwefel-Clustern Funktionen der Mitochondrien • Kompartiment Funktion – Außenmembran Äußere Hülle, Proteintransport, Poren – Intermembranraum Cytochrome, Faktoren für Apoptose – Innenmembran, Cristae Atmungskette, ATP-Synthase, Proteinimport, Metabolittransport Chemiosmotische Hypothese Mitchell 1961 (Nobelpreis 1978) H+ H+ IMR InnenMembran Matrix e- 1. Oxidation (Verbrennung von Zuckern im Citratcyclus) erzeugt Elektronen H+ 2. Elektronenfluss treibt Protonenpumpe (Elektromotor) 3. Protonen-Rückfluss treibt Rotation eines chem. Motors (Turbine) H+ 4. Rotation treibt ATP-Synthese =Phosphorylierung Funktionen der Mitochondrien • Kompartiment Innenmembran, Cristae Funktion Atmungskette, ATP-Synthase, Proteinimport, Metabolittransport Atmungskette: 4 Komplexe; davon transportieren 3 Protonen Funktionen der Mitochondrien • Kompartiment Innenmembran, Cristae Funktion Atmungskette, ATP-Synthase, Proteinimport, Metabolittransport F1Fo ATP-Synthase Funktionen der F1Fo-ATP-Synthase …. und sie dreht sich doch Nobelpreis für P. Boyer und J. Walker, 1998 Funktionen der Mitochondrien • Kompartiment Funktion • Citratzyklus, β-Oxidation von Fettsäuren, Matrix mtDNA Replikation, Proteinbiosynthese, Hämbiosynthese, Harnstoffzyklus, Biosynthese von Fe/S Proteinen Î BIOCHEMIE Mitochondriale Krankheiten • Sehr unterschiedliche Phänotypen • Betroffene Körperteile Mitochondriopathien • Krankheiten treten oft erst im adulten Stadium auf • Schädigungen nehmen im Alter zu • Schwere der Krankheit hängt von Gewebe ab (O2 Bedarf) Multisystemerkrankungen in Geweben mit hohem Stoffwechsel • Mutationen in mtDNA (entdeckt 1988) oder nukleärer DNA (1995) • Bisher keine Therapiemöglichkeiten mtDNA - ein Teil des Problems • Circuläre DNA – 13 Proteine, tRNAs, rRNAs • Keine Histone (=Verpackung) • Ineffizientes Fehlererkennungsund Reparatursystem • In der Nähe der Atmungskette Ö Schädigung durch Sauerstoffradikale • FOLGE: 10 - 20fach höhere Mutationsrate als bei der chromosomalen DNA Mitochondriopathien - Beispiele • • • • • • MELAS mitochondrial myopathy, encephalopathy lactic acidosis and stroke like episodes Subunit 1&4 of complex I, tRNA(Leu) MERFF myoclonous epilepsy associated with ragged red fibers tRNA(Lys) CPEO chronic progressive external ophtalmoplegia Große Deletionen in mtDNA LHON Leber´s hereditary optic neuropathy Subunit 1&4 of complex I Kern-kodiert Friedreich´s Ataxie mtDNA-kodiert Frataxin (mitochondriale Matrix) Defekt im Eisenstoffwechsel DDP Deafness dystonia peptide Kleines Tim Protein Defekt im Proteinimport