Grundwissen Chemie FOS Technikzweig 13 - FOS-FFB
Werbung

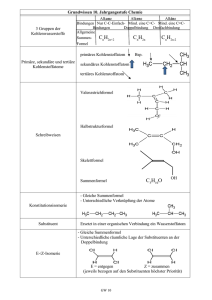
Grundwissen Chemie FOS Technikzweig 13. Jahrgangsstufe Dieses Grundwissen müssen alle Schüler/innen ab dem Zeitpunkt der Erarbeitung im Unterricht für den Rest ihrer Schulzeit beherrschen. Das beinhaltet sowohl das theoretische Wissen als auch die Anwendung auf konkrete Fälle. Das Grundwissen der 11. & 12. Jahrgangsstufe wird weiterhin vorausgesetzt! Struktur und Bindung organischer Moleküle: chiral Konstitutionsisomerie an einem Kohlenstoffatom mit vier unterschiedlichen Substituenten führt zu zueinander spiegelbildlichen Molekülen Z/E-Isomerie ≙ (cis/trans-Isomerie; veraltet) tritt auf, wenn an beiden Enden der Doppelbindung je zwei verschiedenen Substituenten gebunden sind. Die größeren Substituenten können entgegengesetzt (E / trans) oder auf einer Seite der Doppelbindung (Z / cis) angeordnet sein H C CH3 C C H3C Konformationsisomerie H H CH3 C H3C H Z-But-2-en E-But-2-en (cis-But-2-en) (trans-But-2-en) unterschiedliche Raumstrukturen eines Moleküls die durch Drehen um Einfachbindungen entstehen; Beispiel: Ethan in Newmam-Projektion H H C H C HH HH H H H HH H H HH H ekliptisch Blickrichtung entlang der Bindungsachse H H H2 H H2 H2 H2 H H gestaffelt Konstitutionsisomerie unterschiedliche Verknüpfungen (Struktur) der Atome bei gleicher Summenformel. Monomer Einzelbaustein eines Polymers Orbital Räume in denen sich je zwei Elektronen eines Atoms mit hoher Wahrscheinlichkeit aufhalten (> 90 %) Organische Chemie Chemie der Kohlenstoffverbindungen mit Ausnahme der Kohlenstoffoxide COX, der Kohlensäure und ihrer Salze (Carbonate) Polymer ein aus vielen sich wiederholenden Einheiten zusammengesetzter Stoff Polymerisation Verbindung vieler Monomere zu einem Polymer primäre Verbindung das Kohlenstoffatom (das die funktionelle Gruppe trägt) ist mit einem weiteren Kohlenstoffatom direkt verbunden sekundäre Verbindung das Kohlenstoffatom (das die funktionelle Gruppe trägt) ist mit zwei weiteren Kohlenstoffatomen direkt verbunden tertiäre Verbindung das Kohlenstoffatom (das die funktionelle Gruppe trägt) ist mit drei weiteren Kohlenstoffatomen direkt verbunden σ-Bindung Bindungselektronen in einem Orbital entlang der Bindungsachse H H H H -Bindung C C -Bindung entlang der Bindungsachse: H H C Ethan Bindungselektronen in einem Orbital oberhalb und unterhalb bzw. vor und hinter der Bindungsachse -Bindung 1 -Bindung 2 entlang der Bindungsachse: C H C C H -Bindung Ethin Kohlenwasserstoffe: Alkan gesättigter Kohlenwasserstoff mit der allgemeinen Summenformel: CnH2n+2 nur Einfachbindungen, σ-Bindungen; tetraedrisch Alken ungesättigter Kohlenwasserstoff mit der allgemeinen Summenformel: CnH2n Doppelbindungen, 1 σ und 1 -Bindung; planar Alkin ungesättigter Kohlenwasserstoff mit der allgemeinen Summenformel: CnH2n-2 Dreifachbindungen, 1 σ und 2 -Bindungen; linear Aromat cyclische Verbindung mit abwechselnd Doppel- und Einfachbindungen mit 4n +2 -Elektronen (Hückel-Regel) Cycloalkan, -en, -in ringförmige Kohlenwasserstoffe I-Effekt induktiver Effekt, nur über wenige Atome wirksam schiebt oder zieht Elektronen über σ-Bindungen, es entstehen Teilladungen (Partialladungen) M-Effekt mesomerer Effekt, über große Bereiche wirksam schiebt Elektronen in ein konjugiertes -Bindungssystem oder zieht sie heraus, es entstehen Formalladungen Mesomerie beschreibt den tatsächlich vorliegenden Zustand eines Moleküls, der nur durch sog. Grenzstrukturen beschrieben werden kann. Reaktionsmechanismen in der organischen Chemie Addition Anlagerungen von Reagenzien an Substrate, die über mindestens eine Mehrfachbindung verfügen. Auf Kosten der Mehrfachbindung werden zwei neue σ-Bindungen gebildet. Carbeniumion Kohlenstoff-Kation in einer Verbindung, meist als Zwischenprodukt vorhanden Dehydratisierung Eliminierung von Wasser Dimerisierung Verknüpfung zweier Monomere Elektrophil meist positiv geladene Reagenzien mit einer Elektronenlücke, greifen Orte hoher Elektronendichte an (Mehrfachbindungen, Anionen,…) Eliminierung aus einem Substrat werden Atome oder Atomgruppen unter Bildung einer Mehrfachbindung abgespalten. Hydratisierung Addition von Wasser Kondensation Verknüpfung zweier Moleküle unter Abspaltung eines kleinen anorganischen Moleküls, meist Wasser Nucleophil Reagenzien, die über mindestens ein freies Elektronenpaar verfügen, greifen Orte geringer Elektronendichte an (Kationen, positiv teilgeladene Atome,…) Radikal Molekül oder Atom mit einem ungepaarten Elektron Regel von Markownikow Bei Additionsreaktionen an Doppelbindungen wird das Wasserstoffatom immer an das Kohlenstoffatom angelagert, welches bereits mehr Wasserstoffatome trägt. Substitution Atome oder Atomgruppen werden in einem Molekül ausgetauscht Veresterung Bildung eines Esters aus Carbonsäure und Alkohol Funktionelle Gruppen Aldehyd Carbonylgruppe(n) am Kettenende (primär) Alkohol enthält min. eine Hydroxy-Gruppe (-OH); nach Anzahl der Hydroxygruppen unterteilt man in einwertige und mehrwertige Alkohole. Amid enthält min. eine Amid-Gruppe (-CONH2) Amin Verbindungen mit min. einer Aminogruppe (-NH2); die Wasserstoffatome können durch organische Reste ersetzt sein Carbonsäure enthält min. eine Carboxy-Gruppe (-COOH). Carbonylverbindung enthält min. eine Carbonylgruppe (C=O), z.B. Aldehyde (Alkanale) und Ketone (Alkanone) Ester zwei organische Reste sind über ein Sauerstoffatom der Carboxy-Gruppe verbunden Ether zwei organische Reste sind über ein Sauerstoffatom verbunden Fehlingprobe Nachweisreaktion für Aldehyde funktionelle Gruppe gegenüber dem Alkan veränderte Stelle, welche die Reaktionsfähigkeit beeinflusst Halogenalkan enthält min. ein Halogenatom Keton Carbonylgruppe(n) im Ketteninneren (sekundär) Silberspiegelprobe Nachweisreaktion für Aldehyde (Tollens) Thiol enthält min. eine Thiol-Gruppe (-SH); Erdöl fraktionierte Destillation Verfahren zur Auftrennung der Erdölbestandteile nach dem Siedepunkt katalytisches Cracken Aufspaltung langkettiger Kohlenwasserstoffe am PlatinKatalysator unter Kettenbruch und Anlagerung von Wasserstoff Reforming Isomerisierung und Eliminierung an Kohlenwasserstoffen in Benzin, um eine höhere Klopffestigkeit zu erreichen Zucker anomeres Kohlenstoffatom chirales Kohlenstoffatom, das durch die Halbacetalbildung entsteht D- und L-Zucker D-Zucker: unterste Hydroxy-Gruppe in Fischer-Projektion zeigt nach rechts L-Zucker: unterste Hydroxy-Gruppe zeigt nach links Furanose Zucker in Ringform mit 5 Atomen, davon ein Sauerstoffatom glycosidische Bindung Bindung zwischen Zuckermolekülen Halbacetal am gleichen Kohlenstoffatom findet man Ether und HydroxyGruppe Pyranose Zucker in Ringform mit 6 Atomen, davon ein Sauerstoffatom Saccharid Kohlenhydrat, also Zucker(verbindung) α- und β-Zucker α-Zucker: Hydroxy-Gruppe am anomeren Kohlenstoffatom des Halbacetals zeigt in der Haworth-Projektion nach unten β-Zucker: die Hydroxy-Gruppe am anomeren Kohlenstoffatom zeigt nach oben Lipide Fett Dreifachester aus Glycerin (Propan-1,2,3-triol) und drei überwiegend gesättigten Fettsäuren fettes Öl Dreifachester aus Glycerin (Propan-1,2,3-triol) und drei oftmals ungesättigten Fettsäuren natürliche Fettsäure unverzweigt; gerade Anzahl Kohlenstoffatome; an Doppelbindungen immer cis-Konfiguration Ölsäure ungesättigte Fettsäure: C17H33COOH; Doppelbindung an C9 Palmitinsäure gesättigte Fettsäure: C15H31COOH Phospholipid Fett, bei dem eine Fettsäure durch Phosphat ersetzt ist Stearinsäure gesättigte Fettsäure: C17H35COOH Verseifung Spaltung eines Fetts mit Hilfe von Natron- oder Kalilauge; es entstehen Seifen und Glycerin Wachs Ester langkettiger Carbonsäuren Eiweiße Aminosäure Stoff mit Amino- und Carboxy-Gruppe an zwei benachbarten CAtomen Disulfidbrücke Schwefel-Schwefel-Bindung Peptid Verbindung mehrerer bis vieler Aminosäuren Peptidbindung planare Amidbrücke zwischen zwei Aminosäuren pI-Wert isoelektrischer Punkt einer Aminosäure; bei diesem pH-Wert ist die Konzentration der Zwitterionen am größten Primärstruktur gibt die Aminosäure-Abfolge eines Peptids an α-Helix Sekundärstruktur in Schraubenform β-Faltblatt Sekundärstruktur in Zick-Zack-Faltung Sekundärstruktur zeigt geordnete Bereiche der räumlichen Anordnung einer Peptidkette Tertiärstruktur gibt die Anordnung eines Peptids im Raum an Quartärstruktur gibt dieräumliche Anordnung mehrerer Peptidketten an, die sich zusammenlagern Zwitterion Molekül, das eine positive und an anderer Stelle gleichzeitig eine negative Ladung trägt