Die Polymerisation von Hexamethylendiamin und - KAB
Werbung

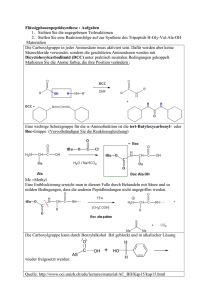
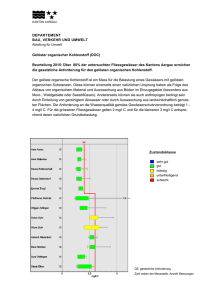
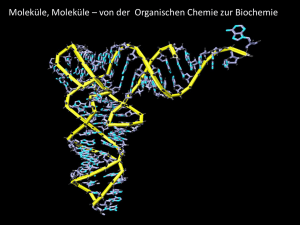
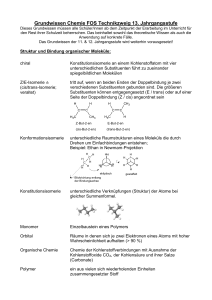
11 Die Polymerisation von Hexamethylendiamin und Sebacinsäuredichlorid Peptid Bindungen kommen in der Natur z.B. in Haaren, Haut und Eiern vor. Auch im Labor lassen sich Moleküle mit einer Peptidbindung synthetisieren. Der US-amerikanische Chemiker Wallace Hume Carothers (1896-1937) nutzte diesen Reaktionsmechanismus aus, um ein Polypeptid ähnlich eines Proteins herzustellen. Hierzu nutzte er jedoch statt Aminosäuren, welche zwei reaktive Zentren, die Amino-Gruppe und die Carboxylgruppe, in einem Molekül vereinen, ein Diamin, hier Hexamethylendiamin und eine Dicarbonsäure, hier Adipinsäure. Die nukleophilen Stickstoffatome der beiden primären Aminogruppen des Hexamethylendiamins greifen bei der Reaktion an das Kohlenstoffatom der Carboxylgruppe an. Dieses ist aufgrund der hohe EN der beiden Sauerstoffatome partiell positiv geladen. Da beide Moleküle sowohl am ersten als auch am letzten Kohlenstoffatom eine funktionelle Gruppe besitzen, kann der Prozess theoretisch beliebig oft wiederholt werden. Dieser Vorgang wird Polykondensation genannt, wobei eine Faser entsteht. Zudem entsteht Wasser. Durch die Chlorierung beider Carboxylgruppen der Adipinsäure entsteht Adipinsäuredichlorid. Da die Elektronegativitätsdifferenz zwischen Kohlenstoff und Chlor deutlich größer ist als die zwischen Kohlenstoff und Sauerstoff, steigt mit der Chlorierung auch die Reaktionsfähigkeit aufgrund einer stärkeren partiellen Ladung, an die das nukleophile Stickstoffatom mit dem freien Elektronenpaar angreifen kann. Dabei entsteht Chlorwasserstoff anstelle von Wasser.