Review: Influenza
Werbung

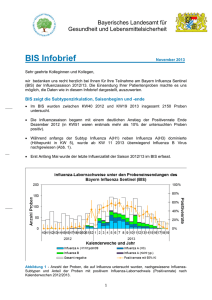
Service für Ärzte / Infektiol. Zeitgeschehen Review: Influenza aus Heft 1/2005 (15. Jahrgang) veröffentlicht am 11. 2. 2005 Aktuelle CME-Fragen Hintergrund Die Influenza oder "echte" Virus-Grippe wird durch Influenza-Viren der Typen A, B oder C hervorgerufen. Plötzlicher Beginn mit hohem Fieber, schweres Krankheitsgefühl und Beteiligung der Atemwege sind die drei klinisch herausragenden Kennzeichen der Infektion. Die Erreger sind speziell im Bereich ihrer Oberflächen-Antigene variabel. Daher hat man selbst nach einer schweren Infektion im folgenden Jahr nur eine geringe (Teil- oder Kreuz-) Immunität, Reinfektionen sind häufig. Da es für Influenza A-Viren Tierreservoire gibt, ist eine Eradikation derzeit nicht möglich. Die nächste Influenzawelle steht vor der Tür, die Fachjournale sind voll davon und selbst in der Laienpresse ist "die Grippe" zum Dauerbrenner geworden. Das sind Gründe genug, auch ein Consilium-Heft dem Thema zu widmen. Virologie und Immunologie Aufbau Influenza-Viren bilden die Familie der Orthomyxoviridae. Man unterscheidet drei antigene Gruppen, die als Typ A, Typ B oder als Typ C bezeichnet werden. Die Typen A und B bestehen aus 8, Typ C aus 7 einsträngigen Gensegmenten, die für 9 (Typ C), 10 (Typ A) oder 11 (Typ B) Virus-Proteine kodieren. Der Typ C lässt sich nur vom Menschen isolieren, Typ B vom Mensch und vom Schwein, Typ A von Menschen, Schweinen, Vögeln, Pferden und sogar von Säugetieren, die im Wasser leben. Diese Eigenschaft, sich in verschiedenen Tierspezies zu vermehren, erlaubt es dem Virus, noch mehr an genetischer Variabilität zu entwickeln. Influenza-Virus Typen A und B haben zwei besonders relevante Pathogenitätsfaktoren (Abbildung 1). Die Neuraminidase (abgekürzt NA) und das Hämagglutinin (abgekürzt HA). Bitte das Bild zur größeren Ansicht anklicken! Abb. 1: Struktur des Influenza A-Virus. Die entscheidenden Pathogenitätsfaktoren und Antigene sind die auf der Hülle sitzende Neuraminidase (NA) und das Hämagglutinin (HA). In der Membran finden sich Transportproteine (M2). Im Inneren tragen Ribonukleoproteine die Erbinformation, die aus dem Nukleocapsidprotein (NP) und Polymeraseproteinen (PB1, PB2 und PA) bestehen. Die wichtigsten Pathogenitätsfaktoren/Antigene Während von Influenza B-Viren nur jeweils ein Subtyp von HA und NA bekannt ist, zeigen Influenza A-Viren eine höhere Variabilität. Das Hämagglutinin (HA) hilft dem Virus beim Haften an der Zelloberfläche. Es fördert außerdem die Freisetzung der Virus-Erbinformation in die Wirtszelle. Bei Influenza A gibt es 15 Varianten (H1-H15). Die Neuraminidase (NA) findet sich auf der Oberfläche des Virus und spaltet Sialinsäure von menschlichen Zellen. Diese Aktivität verhindert, dass aus der Zelle freigesetzte Viren gleich wieder an der Oberfläche der Wirtszelle anhaften und auf diese Weise inaktiviert werden. Bei Influenza A kennt man 9 unterschiedliche Varianten der NA (N1-N9). Beide Pathogenitätsfaktoren, NA und HA, induzieren eine protektive Immunität mit Nachweis spezifischer Antikörper und auch einer Zell-vermittelten spezifischen Abwehr. Die WHO-Nomenklatur bezeichnet Isolate mit Typ/Ort der Isolierung/Stamm-Nummer/Jahr der Isolierung, bei Influenza A zusätzlich HA und NA-Typen. Beispiel: A/Sydney/5/97 (H3N2). Antigen-Variation: Bedeutung für Epidemien Influenza-Viren haben als fundamentales Charakteristikum die Antigen-Variation. Diese Änderung der Antigeneigenschaften der Influenza-Viren betrifft die beiden äußeren Glykoproteine HA und NA. Man bezeichnet kleinere Änderungen als "antigen-drift", größere Änderungen als "antigen-shift". Zur "antigen drift" kommt es praktisch jedes Jahr bei Influenza A- und B-Viren durch Punktmutation in den Genen für HA, NA oder beide. Diese bewirken geringe Änderungen der Viren. In der Folge binden die Antikörper von der Infektion des Vorjahres weniger gut, die Fähigkeit des Menschen zur Neutralisation der Erreger sinkt. Diese schlechtere Immunität erlaubt es dem Virus, jedes Jahr aufs neue empfängliche Wirte zu finden, um sich zu vermehren. Ein "antigen shift" ist erheblich seltener und tritt nur bei Influenza A auf. Die Änderungen in HA und NA sind deutlich größer, man findet plötzlich HA- und NA-Typen, die man in den Jahren zuvor nicht isoliert hatte (Tabelle 1). Nach einer heute gängigen Theorie zirkuliert ein HxNx-Typ solange, bis er in der Population praktisch kaum noch auf empfängliche Personen trifft. Taucht dann ein neuer Virus-Stamm mit völlig anderen HA- und NA-Eigenschaften auf, ist ihm das Feld überlassen. Da es in der Welt-Bevölkerung keine Immunität gibt, kann er sich ohne "Konkurrenz" ausbreiten (Abbildung 2). Bitte das Bild zur größeren Ansicht anklicken! Abbildung 2: Nach einer Pandemie zirkuliert der entsprechende Stamm mit kleineren antigenen Änderungen noch einige Jahre weiter und löst jährliche Epidemien aus. Die Immunität in der Population steigt jedes Jahr, die Epidemien werden kleiner. Das Virus findet schließlich kaum noch empfängliche Personen. Kommt jetzt ein neuer Stamm mit pandemischen Eigenschaften, trifft er auf eine vollständig empfängliche Population und kann sich dort ohne Konkurrenz ausbreiten. Jahr Intervall zwischen Pandemien Typen Schwere der Pandemie 1889 - H2N2 schwer 1901 12 H3N8 mittel 1918 29 H1N1 schwer 1957 39 H2N2 schwer 1968 11 H3N2 mittel ?? ? ? ? Tab. 1: Die letzten 6 Influenza A-Pandemien, interpandemisches Intervall, auslösende Influenza A-Typen und Schwere der Pandemie. Aus: Treanor, 2000 Die genetische Differenz zwischen altem, "epidemischem" Stamm und neuem, "pandemischen" Stamm liegt bei 30% - solche großen Änderungen sind durch Punktmutation nicht zu erklären. Woher kommen dann die Pandemie-Viren? Man fand signifikante Genhomologien zwischen Influenza-Pandemiestämmen des Menschen und Influenza A-Viren von Vögeln. Nach einer gut belegten Theorie kommt es zur Infektion eines Menschen mit einem Vogel-Influenza-Virus und gleichzeitig mit einem "menschlichen" Influenza-Virus. Beide Stämme reassortieren in einem Wirt: Das Vogel-Influenza-Virus liefert die "neuen" HA- und NA-Typen für eine effektive Infektion, das "menschliche" Influenza-Virus liefert die Gene für eine effiziente Vermehrung im Menschen. Dieses Reassortment wird noch dadurch erleichtert, dass das Schwein beide, Menschen- und Vogel-Influenza-Viren beherbergen kann und so als Reservoir für die Erregerausbreitung dienen kann. In Südostasien leben Mensch, Geflügel und Rinder oft unter einem Dach – das könnte erklären, weswegen Pandemien oft von hier ihren Ausgang nehmen. Nach einer zweiten Theorie kann sich das Influenza-Virus z. B. vom Schwein direkt an den Menschen anpassen und sich nach Übertragung effizient in ihm vermehren. Es gibt Belege dafür, dass dieser Mechanismus Ursache der Pandemie im Jahr 1918 war. Epidemiologie Auf der Südhalbkugel der Erde beobachtet man Influenza-Epidemien meist in der Zeit zwischen Mai und September, auf der Nordhalbkugel meist zwischen Dezember/Januar bis Februar/März. Die Gründe für diese Saisonalität sind wenig bekannt – man vermutet als Ursache Umweltfaktoren wie eine klimatisch bedingte bessere Überlebensfähigkeit des Erregers oder aber auch spezifische menschliche Verhaltensmuster, die eine Übertragung optimieren, wie etwa engere Kontakte und dichteres Zusammenleben während der "kalten Jahreszeit". Eine Influenza-Epidemie beginnt zunächst mit einem 2 Wochen andauernden rasanten Anstieg der Fallzahlen, dann sieht man eine Gipfelphase und nach insgesamt 6-8 Wochen ist die "Saison" meist zu Ende. Die ersten Fälle treten bei Kindern auf, es folgen die Infektionen der Erwachsenen. In der zweiten Phase der Epidemie steigt die Zahl der Todesfälle vor allem bei älteren Menschen sprunghaft an ("excess mortality"; Übersterblichkeit). Die Morbiditäts-Alters-Kurve der Influenza hat eine U-Form – betroffen sind vor allem alte Menschen, Säuglinge und Kleinkinder (Abbildung 3). Bitte das Bild zur größeren Ansicht anklicken! Abb. 3: Mortalität, Hospitalisierungen und Arztkontakte ausgelöst durch Influenza. Nach: Glezen Epidemiol Rev. 1996 In einer Untersuchung aus Kiel waren rund 24 % aller wegen Influenza eingewiesenen Kinder 0-1 Jahr, 23,5 % 1-2 Jahre, und ein Drittel 2-5 Jahre alt (s. Tab. 2). Kinder sterben zwar selten an einer Influenza – man schätzt 2-3 Tote / 100.000 im Vergleich zu 30 bis 150 Todesfällen pro 100.000 für ältere Personen – die Morbidität ist bei Kindern aber wenigstens gleich hoch wie bei alten Menschen. Je nach Ausmaß der Epidemie suchen 6 % bis 29 % aller Kinder während einer Influenza-Saison einen Arzt auf. Otitis media und Pneumonie sind dann Diagnosen, die zur Verordnung eines Antibiotikums führen – der Verbrauch von Antibiotika erhöht sich während einer Influenza-Saison um 10 % bis 30 %. Ein erhöhtes Hospitalisierungsrisiko haben vor allem Frühgeborene und Kinder mit kardialer oder pulmonaler Grundkrankheit. Ort [Referenz] Zeit Inzidenz pro 100.000 0 bis < 5 Jahre Inzidenz pro 100.000 5-16 Jahre relatives Risiko 0 < 5/5-16 Houston [Glezen 1993] 1985-90 427 5 85,0 Kalifornien [Mullooly 1982] 1967-73 120 40 3,0 Kalifornien [Izurieta 2000] 1993-97 136 19 7,2 Seattle [Izurieta 2000] 1992-97 90 16 5,6 Kiel [Weigl 2002] 1996-01 123 22 5,6 Kalifornien [Mullooly 1982] 1967-72 470* 210 2,2 Tennessee [Neuzil 2000] 1973-93 382** 40 9,6 Tabelle 2: Internationaler Vergleich der kumulativen Inzidenz Influenza-assoziierter Hospitalisierungen bei Kindern. *Patienten mit Grundkrankheiten. **Patienten mit kardialen Grundkrankheiten. Nach: Weigl et al. 2002. Warum erkranken Kinder so schwer an Influenza? Zum einen ist es häufig der Erstkontakt mit dem Erreger. Zum anderen führt die geringe Größe der Atemwege dazu, dass die Infektion den Luftaustausch stärker behindert als bei Erwachsenen. Kinder spielen aber nicht nur wegen hoher Morbidität im Rahmen der jährlichen Epidemien eine besondere Rolle, sie sind auch "das Feuer der Epidemie" ("fire of the epidemic"). Das Virus wird viel länger und in höherer Keimzahl als bei Erwachsenen ausgeschieden. Kinder sind häufig in Gemeinschaftseinrichtungen untergebracht und sie haben ein (noch) unzureichendes "Hygienebewusstsein": Alles wird angefasst und erst einmal in den Mund gesteckt; Hände werden selten gewaschen. Folglich breiten sich Influenza-Viren in dieser Gruppe sehr rasch und zuerst aus. Kinder bringen dann das Virus mit zu ihren erwachsenen Kontaktpersonen (Eltern und Großeltern). Diese erkranken meist leichter, scheiden wegen ihrer (Teil-) Immunität den Erreger nur über kürzere Zeit aus und haben meist weniger Kontaktpersonen als Kinder. Klinik Krankheitsverlauf Plötzlicher Beginn mit hohem Fieber, Symptome und Befunde einer schweren Allgemeinkrankheit und wenigstens ein Symptom seitens der Atemwege, das sind während der Influenza-Saison die drei führenden Symptome, die an eine Influenza denken lassen sollten. Typische Klinik: plötzlicher Beginn mit hohem Fieber schwere Allgemeinkrankheit Atemwegssymptom Eine Prodromalperiode von 1-2 Tagen geht der Influenza oft voraus. Als Allgemeinsymptom klagen ältere Kinder und Erwachsene über schweres Krankheitsgefühl und Myalgien. Säuglinge und Kleinkinder fallen durch Nahrungsverweigerung und deren Folgen oder durch Apathie auf. Gelegentlich beobachtet man Meningismus. Tabelle 3 stellt Influenza-Symptome bei Kindern und Erwachsenen gegenüber. Die unkomplizierte Erkrankung dauert meist 1-2 Wochen, dieser Wert ist aber ausgesprochen variabel. Kinder [%] Erwachsene [%] Husten 86 90 Halsschmerzen 62 62 Heiserkeit 22 37 Sputum-Produktion 19 41 Coryza 57 82 Niesen 38 67 Plötzlicher Beginn 66 46 Fieber 93 71 < 38,8° C 29 58 > 38,8° C 60 29 Schüttelfrost 37 64 Kopfschmerzen 81 72 Anorexie 69 37 Malaise 68 67 Myalgien 33 62 Bauchschmerzen 31 0 Erbrechen 26 7 Übelkeit 34 4 Diarrhoe 2 0 Tab. 3: Vergleich der Symptome und Befunde bei Erwachsenen und bei Kindern mit Influenza. Nach: Feigin Cherry Komplikationen Die Komplikationen der Influenza sind in Tabelle 4 zusammengefasst. Zahlenmäßig stehen Komplikationen seitens der Atemwege im Vordergrund, bei Kindern die Otitis media, bei alten Menschen die Lungenentzündung. Die Pneumonie durch bakterielle Superinfektion wird meist nach einem ersten Fieberabfall und Besserung durch einen erneuten Fieberanstieg manifest. Die bakterielle Tracheitis ist im Kindesalter ein Notfall, weil insbesondere Frühgeborene und Säuglinge die in der Trachea plötzlich anfallenden Eitermassen nicht abhusten können. Erreger ist meist Staphylococcus aureus. Die akute Myositis betrifft vornehmlich Kinder. Atemwege Primäre Influenza-Pneumonie Superinfizierte bakterielle Pneumonie Krupp (nur bei Kindern) Exazerbation chronischer Lungenkrankheiten (bakterielle) Tracheitis Otitis media Nervensystem Reye Syndrom Enzephalitis Myelitis Fieberkrampf Guillain-Barré Syndrom (kausal?) Myokarditis / Perikarditis Toxic shock-like syndrome (TSS) Akute Myositis (nachfolgend) Meningokokken-Infektionen Tabelle 4: Komplikationen der Influenza Diagnose Während einer Epidemie ist die Diagnose "Influenza" durchaus mit einer Treffsicherheit von rund 85 % (bei Erwachsenen) klinisch zu stellen, wenn die drei oben genannten Hauptsymptome vorliegen. Gelegentlich läuft parallel eine Epidemie mit RS- oder anderen Viren ab (siehe Abbildung 6 weiter unten), dann versagt diese Möglichkeit der Sicherung der Erregerdiagnose. Kommerziell verfügbare Schnelltests haben nach unserer Erfahrung einen unzureichenden Vorhersagewert, speziell zu Beginn und am Ende der Influenza-Saison, wenn es eigentlich auf die mikrobiologische Sicherung der Diagnose ganz besonders ankommt. Für die Praxis sind sie mit rund ¤ 10.- pro Test auch vergleichsweise teuer. In unseren Augen für die Erregerdiagnose am besten praktikabel ist die Kombination aus Kenntnis der aktuellen Erreger-Epidemiologie (z.B. firmen-unabhängig im Internet unter www.PID-ARI.net für 19 Erreger einschließlich RSV) plus der klinischen Symptomatik (siehe oben). Im Einzelfall kann eine Erreger-Diagnose mittels PCR sinnvoll sein. Die Serologie (Hämagglutination; Komplement-Bindungs-Reaktion; idealerweise Nachweis eines Titeranstieges) dauert für das Einleiten einer Therapie in der Regel zu lange, ebenso die Virus-Kultur. Therapie Es ist durchaus bemerkenswert und von den Fakten her kaum verständlich, dass eine Krankheit wie die Influenza selbst bei schwerem Verlauf nur selten kausal behandelt wird. Kinder, die so schwer krank sind, dass sie wegen einer Influenza stationär eingewiesen werden müssen, profitieren von einer Therapie mit Amantadin oder neuerdings auch mit einem Neuraminidase- Hemmer. Bei Therapiebeginn innerhalb von 48 Stunden ab Beginn der Erkrankung sind die Patienten meist innerhalb von 24 Stunden wieder in einem deutlich gebesserten Allgemeinzustand. Amantadin wirkt über eine Interaktion mit dem viralen M2-Protein, einem Ionen-Kanal, der nur bei Influenza A vorkommt. Amantadin behindert so die Freisetzung der Virus-Erbinformation (uncoating). Dosis: 5 mg/kg KG/d (max. 150 mg/d) in 2 ED für 10 Tage (als Saft: InfectoFlu® -Saft; als 100 mg Filmtablette: Amantadin 100 von ct, ratiopharm und TEVA). Amantadin ist seit vielen Jahren verfügbar und die Sicherheit der Anwendung bei Kindern ist seit Jahrzehnten gut belegt. Zu den – bei normaler Nierenfunktion seltenen – Nebenwirkungen zählen Schläfrigkeit und Konzentrationsschwäche, besonders bei älteren Personen. Krampfanfälle sind bei Personen mit einem Krampfleiden unter Amantadin bekannt geworden, bei alten Menschen (Nierenfunktion!) sollte die Dosis reduziert werden. Neuraminidasehemmer inhibieren hochselektiv die NA von Influenza A- und Influenza B-Viren. Aus infizierten Zellen freigesetzte Viren "verklumpen" und werden inaktiviert. Von den beiden derzeit verfügbaren Produkten ist Oseltamivir (Tamiflu ® ) neuerdings zur Therapie ab einem Alter von 1 Jahr zugelassen. Außer gelegentlichen gastrointestinalen Beschwerden wird es meist gut vertragen. Erhältlich sind Saft oder Kapseln à 75 mg; Dosierung: 2 x tgl. bis zu 2 mg/kg, maximal 2 x 75 mg/Tag jeweils für 5 Tage. Details siehe Fachinformation. Reduzierte Dosis bei Niereninsuffizienz. Zanamivir (Relenza ® ) ist erst ab 12 Jahren zugelassen und es werden 2 x tgl. 5 mg über 5 Tage inhaliert. Prophylaxe Chemoprophylaxe Zur Chemoprophylaxe der Influenza sind Amantadin und Neuraminidase-Hemmer zu rund 75 %-90 % wirksam. Der Nachteil des Amantadins und auch des Oseltamivirs – wie neueste Studien aus Japan zeigen – ist, dass mit der Dauer der Anwendung auch die Wahrscheinlichkeit für das Auftreten resistenter Stämme steigt. Daher verbietet sich meines Erachtens eine routinemäßige Dauerprophylaxe. Für Hochrisiko- Kinder, die nicht geimpft werden können, ist die prophylaktische Gabe jedoch nach individueller Abwägung von Nutzen und Risiken vertretbar. Amantadin kann ab 5 Jahren und Oseltamivir ab 13 Jahren eingesetzt werden. Impfung Zweifellos ist die aktive Immunisierung die Methode der Wahl zur Prophylaxe der Influenza, obwohl jährlich neu mit dem vermutlich zirkulierenden Stamm geimpft werden muss. Inaktivierte InfluenzaImpfstoffe sind seit rund 60 Jahren im Gebrauch. Sie werden auf embryonierten Hühnereizellen gezüchtet – in Kürze möglicherweise auch auf Zellkulturen. Man unterscheidet inaktivierte Ganzkeim-Impfstoffe, Spaltimpfstoffe, die neben HA und NA auch noch einige weitere Virusbestandteile enthalten und subunit-Vakzinen, die nur noch aus gereinigtem HA und NA bestehen (Abbildung 5). Eine aktuelle Weiterentwicklung hiervon sind virosomale Vakzine. Sie tragen die Antigene auf der Oberfläche kugelförmiger Lipidteilchen. Aufgrund ihrer dem Virus ähnlichen Form und Größe werden sie als "Virosom" bezeichnet. Verminderte Reaktogenität bei guter Immunität ist der Vorteil der Präparate, die weniger Virusbestandteile enthalten. Bitte das Bild zur größeren Ansicht anklicken! Abbildung 5: Influenza-Impfstoff-Typen: a) Ganzkeim-Impfstoff, b) Split-Impfstoff, c) subunit-Impfstoff und d) Virosomen-Impfstoff. Lebendimpfstoffe zur intranasalen Applikation sind in fortgeschrittenen Stadien der klinischen Entwicklung, ein Produkt ist in den USA bereits für nicht immungeschwächte Personen zwischen 5 und 49 Jahren zugelassen. Es wird aber noch etwas Zeit in Anspruch nehmen, bis das derzeit bei -20° C zu lagernde Produkt "Kühlschrank-fähig" ist und dann auch in Europa angewendet werden kann. Inaktivierte Influenza-Impfstoffe werden als trivalente Produkte, zusammengesetzt nach den Empfehlungen der WHO, angeboten. In diesem Jahr enthält der Impfstoff A/New Caledonia/20/99 (H1N1) A/Fujian/411/2002(H3N2) B/Shanghai/361/2002 Die Wirksamkeit hängt auch vom "match" ab, also davon, wie ähnlich aktuell zirkulierendes Virus und Impfstamm tatsächlich sind. In klinischen Studien werden Wirksamkeitsraten von ca. 60 bis 90 % angegeben – je nach "match" und gewähltem Endpunkt der Untersuchung. Influenza-Impfstoffe sind zugelassen für Kinder ab 6 Monate. Da Kinder in aller Regel noch keine Infektion mit Influenza-Viren hatten, sind bis zum Alter von drei Jahren meist "zwei halbe Dosen" à 0,25 ml im Abstand von 4 Wochen zu applizieren. Details sind dem Beipackzettel des jeweiligen Herstellers zu entnehmen. Moderne Influenza-Impfstoffe werden meist gut vertragen. Leichte lokale Reaktionen werden von 25 % bis 50 % der Impflinge innerhalb der ersten 24 Stunden angegeben, rund 5 % haben mittelgradige bis schwere Schmerzen an der Impfstelle. Allgemeinsymptome wie Myalgien oder Kopfschmerzen werden nach Influenza- Impfung genauso häufig beobachtet wie nach Gabe von Plazebo. Die Reaktogenität ist mit allen Produkten bei Erwachsenen in etwa gleich, nur Kinder haben nach Ganzkeim-Impfstoff häufiger und höher Fieber als Erwachsene. Ein Guillain-Barré-Syndrom (GBS) ist in den USA mit dem Impfstoff der Saison 1976 beobachtet worden in einer Häufigkeit von 1:100.000. Untersuchungen in den Folgejahren ergaben keine erhöhte Inzidenz, wenn auch 1992/93 und 1993/94 ein leichter Anstieg an GBS Fällen beobachtet worden war. Das Risiko für ein impf-assoziiertes GBS wird mit etwas höher als 1: 1 Million Impfdosen angegeben, ohne dass damit die Frage nach dem kausalen Zusammenhang beantwortet wäre. Interessanterweise wird nach Influenza-Impfung kurzfristig der ELISA für HIV und Hepatitis C falsch positiv, der Western Blot bleibt negativ. Impfempfehlungen In Deutschland ist die jährliche Influenza-Impfung von der STIKO empfohlen für alle Personen ab 60 Jahren; für Risiko-Personen mit einer Grundkrankheit (kardial, pulmonal, Leber-, Niere, Diabetes und andere Stoffwechselkrankheiten, multiple Sklerose mit durch Infektionen getriggerten Schüben, Immundefekt mit Restfunktion des Immunsystems, HIV-Infektion); Bewohner von Alters- und Pflegeheimen; Personen mit erhöhter Gefährdung (medizinisches Personal, umfangreicher Publikumsverkehr) Kontaktpersonen zu Risikopatienten; Wenn eine intensive Epidemie droht und der Impfstoff die neue Variante enthält. Weiterhin gilt die STIKO-Regel: "Für einen ausreichenden Impfschutz der von ihm betreuten Personen zu sorgen, ist eine wichtige Aufgabe des Arztes. …" (Epidemiologisches Bulletin 2004:30; 235) Die Umsetzung der STIKO-Empfehlungen ist Sache der Länder. In Niedersachsen und Baden-Württemberg wird derzeit die Grippeimpfung als Routineprophylaxe für alle Personen empfohlen. In den USA ist die Influenza-Impfung aktuell auch für alle Kinder zwischen 6 und 24 Monaten empfohlen – es gibt allerdings momentan nicht ausreichend Impfstoff, um diese Empfehlung umzusetzen. Die amerikanische Empfehlung macht Sinn, weil Kinder eine wenigstens gleich hohe Influenza-Morbidität haben wie Erwachsene, weil sie die relevante Quelle der Epidemie darstellen und weil z. B. für Japan gezeigt wurde, dass ein Influenza-Impfung von Schulkindern einen effizienten Herdenschutz auch für alte Menschen bietet. Kostenersparnis für die Eltern und die Gesellschaft sind weitere Argumente für eine solche Empfehlung. Bitte die Bilder zur größeren Ansicht anklicken! Abbildung 6: zeitlicher Verlauf des Nachweises von 9 Erregern akuter Atemwegsinfektionen bei hospitalisierten Kindern in Mainz, Kiel, Freiburg. Oberes Bild mit Influenza, unteres ohne Influenza: Wegfall der Influenza führt nicht zu einer in der Praxis wahrnehmbaren Verringerung der Anzahl akuter Atemwegsinfektionen. Zwischen Oktober 2002 und Oktober 2004 wurden in 6380 Proben insgesamt 4615 Erreger nachgewiesen – Influenza A steht mit 522 Nachweisen nur an dritter Stelle. Quelle: Dr. Puppe, PID-ARI.net Bei näherem Hinsehen ist aber speziell für Deutschland wenig gut belegt, dass Herdenimmunität zu erwarten ist. Die Morbidität im ambulanten Bereich ist wenig dokumentiert, und vor allem dürfte die Impfung von der Bevölkerung als wenig wirksam wahrgenommen werden. Die beiden folgenden Abbildungen zeigen, dass akute Atemwegsinfektionen nur zu ca. 12 % durch Influenza-Viren ausgelöst werden – gerade im Winter kommt es zu vielen Infektionen mit anderen Erregern. Ein Influenza-Impfprogramm für ein ganzes Land oder alle seine Kinder setzt eine ausgezeichnete begleitende Epidemiologie voraus, um den Erfolg der Anstrengungen für Ärzteschaft wie auch für die Bevölkerung zu dokumentieren. Pandemie Eine Influenza-Pandemie ist rein statistisch alle 27 Jahre zu erwarten – die nächste steht demnach vor der Tür. Legt man die Angaben der Pandemie von 1918 zugrunde, so ist weltweit innerhalb von 1-2 Jahren mit 150 bis 300 Millionen Todesfällen zu rechnen. Nach anderen Modellrechnungen kommt es "nur" zu 2 bis 7,4 Millionen Todesfällen. Damit eine Pandemie entstehen kann, müssen 3 Voraussetzungen erfüllt sein: 1. Es muss ein neues Influenza A-Virus auftauchen, gegen das die Bevölkerung keine Immunität besitzt; 2. dieses "neue" Virus muss sich im Menschen vermehren können und 3. es muss effizient von Mensch zu Mensch übertragbar sein. Von diesen drei Bedingungen erfüllt derzeit das "Vogel-Influenza-Virus" vom Typ H5N1 bereits die ersten beiden. Es stellt daher eine ernste Bedrohung dar. Das für Geflügel hoch-virulente Virus hat sich in den letzten Monaten in sieben Ländern Asiens ausgebreitet, seit Juli auch in China, Thailand, Vietnam, Indonesien und Malaysia. Auch Schweine in China beherbergen mittlerweile H5N1-Stämme. Die WHO hat 1999 ihren Pandemie-Plan vorgestellt , einzelne Länder folgten. Der wichtigste Eckpfeiler im Kampf gegen eine Influenza Pandemie sind Impfstoffe. Mit konventionellen Techniken würden aber wenigstens 8 Monate vergehen, bis sie zur Verfügung stehen. Noch schlimmer: Vogel-Influenza-Viren lassen sich nicht mit konventionellen Methoden anzüchten. Gentechnisch hergestellte Produkte wären die Alternative. Leider: die Patente für die neue Technik liegen in verschiedenen Händen, es gibt Sicherheitsbedenken und der Preis für das Endprodukt ist für viele Länder vielleicht zu hoch. Es ist auch noch zu klären, wie der Impfstoff weltweit verteilt wird. Die USA hatten 1976 die heimische Produktion an Influenza-Impfstoff beschlagnahmt und vom Ausland bereits bezahlte Ware nicht geliefert, um die eigene Bevölkerung schützen zu können. Die Chemoprophylaxe löst das Problem ebenfalls nicht . Amantadin scheint gegen H5N1-Stämme unwirksam zu sein, für die Neuraminidase-Hemmer gibt es nicht einmal einen annähernd ausreichenden Vorrat oder eine adäquate Produktionskapazität. Es ist dargelegt worden, dass die Gefahr durch eine Influenza-Pandemie höher und konkreter ist als die durch Bioterrorismus – dementsprechend sollten wir auch darauf reagieren. Literatur beim Verfasser Ein Influenza-Pandemieplan wurde vom RKI gerade publiziert: www.rki.de/infekt/influenzapandemieplan/pandemieplan_teil1.pdf NEU: Jetzt auch CME-Punkte mit dem "Infektiologischen Zeitgeschehen" Aktuelle CME-Fragen Liebe Leserin, lieber Leser, die Muster-Berufsordnung regelt seit jeher die Pflicht für Ärzte zur regelmäßigen fachlichen Fortbildung. Sie als Ärzte werden nun vom Gesetzgeber verpflichtet Ihre Fortbildung auch zu dokumentieren. Bis zum 30. Juni 2009 müssen Sie 250 Fortbildungspunkte erwerben, wobei ein Punkt 45 Minuten entsprechen soll. Dies besagt das zum 01.01.2004 eingeführte Gesetz zur Modernisierung des Gesundheitswesens (GMG), § 95 d SGB V. CME- Fortbildungspunkte können Sie jetzt auch erwerben, wenn Sie zertifizierte Fragen zum Inhalt des "Infektiologischen Zeitgeschehens" beantworten. Hochwertige Informationen aus erster Hand zu infektiologischen Themen bietet Ihnen InfectoPharm schon lange. Das "Infektiologische Zeitgeschehen" erscheint im 15. Jahr! Auch Fortbildungspunkte erhalten Sie seit geraumer Zeit bei uns. InfectoPharm war bei den ersten, die sich am Modellversuch zur Zertifizierung der ärztlichen Fortbildung beteiligte und zertifizierte Fortbildungsveranstaltungen anbot. Wie bekommen Sie Ihre CME-Punkte von InfectoPharm? Auf der letzten Seite sind 10 Multiple Choice-Fragen von Prof. Schmitt zum Inhalt dieses Heftes. Von den 5 Möglichkeiten ist jeweils eine richtig. Mindestens 7 der 10 Fragen müssen korrekt beantwortet werden. Senden Sie die Seite per Fax an InfectoPharm Arzneimittel und Consilium GmbH, Abteilung Ärzteservice, Fax-Nr.: 06252/964-153. Ihre Faxantworten werden vertraulich ausgewertet. Eine Speicherung der Daten erfolgt nur soweit es für die zertifizierte Fortbildung notwendig ist. Eine Weitergabe der Daten an Dritte ist ausgeschlossen. Bei Erreichen mindestens 70 % richtiger Antworten senden wir Ihnen eine Teilnahmebescheinigung zu. Diese können Sie bei Ihrer Landesärztekammer einreichen. Die erworbenen Punkte zählen zur Kategorie D: Interaktive Fortbildung via Printmedien, Online-Medien, audiovisuelle Medien mit nachgewiesener Qualifizierung und Auswertung in Schriftform. Hierfür werden von den Ärztekammern ein Punkt pro Übungseinheit zuerkannt. Wer kann teilnehmen und wer erkennt die Punkte an? Eine Landesärztekammer hat die Fortbildung stellvertretend zertifiziert. Alle anderen Landesärztekammern erkennen die CME-Punkte an. Jeder Arzt/Ärztin kann teilnehmen. Senden Sie das Fax mit den angekreuzten Antworten und Ihrem Praxis-/Dienststempel an 0 62 52/9 64-1 53. Sie erhalten dann per Post Ihre Bescheinigung zugesandt. Zusätzlicher Service ab 15. März 2005 im Internet Ihre Antworten können Sie ab 15. März 2005 online eingeben. Auf www.CME-Päd.de finden Sie eine Seite mit Antwortmöglichkeit auf alle Fragen. Auch die Inhalte des Infektiologischen Zeitgeschehen werden darüber zugänglich sein, falls Sie das Heft gerade nicht griffbereit haben. Dort werden wir Ihnen auch weiteren Service bieten, wie die Möglichkeit, Ihr Punktekonto online zu führen. Wir hoffen, InfectoPharm macht mit diesem Service ein weiteres interessantes Angebot zur Unterstützung Ihrer Fortbildung. Kommentare, Kritik und Anregungen sind uns willkommen. Sie erreichen uns unter der kostenlosen Hotline 08 00/1 13 64 64 oder per Mail: [email protected] Wir wünschen Ihnen viel Spaß und viel Erfolg bei der Teilnahme an der ersten CME-Version des Infektiologischen Zeitgeschehen. Ihre Prof. Dr. med. Heinz-Josef Schmitt Dr. Andreas Rauschenbach Impressum Herausgeber INFECTOPHARM Arzneimittel und Consilium GmbH Von-Humboldt-Straße 1 64646 Heppenheim Telefon (0 62 52)9 64-0 Telefax (0 62 52)9 64-150 Hotline (0800)1 13 64 64 e-mail: [email protected] Redaktion Dr. Andreas Rauschenbach Erscheinungsweise: 4-mal jährlich Inhalt: Prof. Dr. med. Heinz-J. Schmitt Kinderklinik, Johannes-Gutenberg-Klinik, Langenbeckstr. 1, 55101 Mainz Seitenanfang | Speichern | Versenden | Drucken