700 Thermodynamik 710 Temperatur 720 Wärme und Energie 730
Werbung

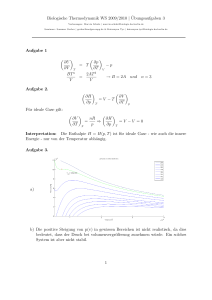
700 Thermodynamik 710 Temperatur 720 Wärme und Energie 730 Chemische Reaktionen 740 Wärmetransport und Transportphänomene um was geht es? Eine neue Grösse: Die Temperatur T Verhalten der Materie als Funktion der Temperatur Energieumwandlung Noch eine neue Grösse: Entropie S Chemische Systeme Transportphänomene: Diffusionsgleichung 711 thermische Ausdehnung von Gasen 711 Ziele • Temperatur mikroskopisch erklären können • Annahmen für ein ideales Gas erklären können • Ideales Gasgesetz anwenden können 711 Theorie Druck Impulsübertrag durch Stösse ``harter Teilchen´´ px dFx p dA x 711 Theorie Druck Impulsübertrag durch Stösse ``harter Teilchen´´ px dFx p dA x dv x d (2mv x ) 2m Fx dt dt 711 Theorie Druck Impulsübertrag durch Stösse ``harter Teilchen´´ px vx = ? x dv x d (2mv x ) 2m Fx dt dt 711 Theorie vx = ? px Geschwindigkeitsverteilung f(v): Anz. Teilchen dN im Intervall v + dv: dN N f (v) dv 711 Theorie vx = ? Normierung von f(v): px f (v ) dv 1 711 Theorie vx = ? Erwartungswert für v2: px v 2 v f (v) dv 2 0 711 Theorie vx = ? Für ideales Gas MaxwellBoltzmann-Verteilung: px Neue Grösse: Temperatur T [T] = Kelvin K 4 m f (v ) 2kT 3/ 2 v e 2 mv 2 2 kT 4 m f (v ) 2kT 3/ 2 v e 2 mv 2 2 kT 0.0025 T= 273 K 0.002 Reihe1 0.0015 Reihe2 Reihe3 Reihe4 0.001 Reihe5 0.0005 T= 2000 K 0 0 500 1000 1500 2000 2500 711 Theorie Erwartungswert für v2: v 2 3 2 mv 2 2 2 kT m v f (v) dv v v e 2kT 0 0 2 2 4 dv 711 Theorie Erwartungswert für v2: v 2 3 2 mv 2 2 2 kT m v f (v) dv v v e 2kT 0 0 2 2 3 2 mv 2 4 2 kT 4 m v e 2kT 0 dv 4 dv 711 Theorie Erwartungswert für v2: v 2 3 2 mv 2 2 2 kT m v f (v) dv v v e 2kT 0 0 2 2 3 2 mv 2 4 2 kT 4 m v e 2kT 0 4 4 m 3 dv 8 2kT 3 2 dv 2kT m 5 2 711 Theorie Erwartungswert für v2: v 2 3 2 mv 2 2 2 kT m v f (v) dv v v e 2kT 0 0 2 2 4 dv 5 mv 2 4 m 4 m 3 2kT 4 2 kT dv v e 2 kT 2 kT 8 m 0 3 2 3 2kT 2 m 3 2 2 5 2 3kT 2kT m m 3 2 711 Theorie vx = ? Erwartungswert für v2: px v 2 v f (v) dv 2 0 1 3 2 mv kT 2 2 711 Theorie Zurück zur Frage nach dem Druck: Impuls px = ? Pro Zeit: Kraft pro Fläche = px Druck p = ? dv x d (2mv x ) 2m Fx dt dt 711 Theorie Zurück zur Frage nach dem Druck: Impuls px = ? Pro Zeit: Kraft pro Fläche = px Druck p = ? dFx …? p dAx N p kT V 711 Theorie Druck p = f(N,V,T) N = Anz. Teilchen V = Volumen px T = Temperatur N p kT V 711 Theorie pV = f(N,T) N = Anz. Teilchen px R = NA·k (mit NA = Avogadrozahl). R = 6.022·1023 (mol-1)·1.38·10-23(JK-1) = 8.31 J mol-1K-1. Chemisch besser Anz. Mol n pV nRT 712 thermische Ausdehnung von Flüssigkeiten und Festkörpern 712 Ziele • thermische Längenausdehnung von Festkörpern berechnen können • thermische Volumenausdehnung von Festkörpern und Flüssigkeiten berechnen können • Grundlagen eines Flüssigkeitsthermometers verstehen 712 Theorie Längenausdehnung l l T l 712 Theorie Volumenausdehnung V V T 712 Theorie Für Festkörper 3 V V T 712 Aufgaben Flüssigkeitsthermometer h=f(T) V= …? V V T 713 Temperaturabhängigkeit des elektrischen Widerstands 713 Ziele • thermische Änderungen des elektrischen Widerstandes berechnen können • Grundlagen der elektrischen Temperaturmessung verstehen 713 Theorie und Aufgaben Temperaturabhängige Änderung des elektrischen Widerstandes R: l R A l A R R T 713 Theorie und Aufgaben Temperaturabhängige Änderung des elektrischen Widerstandes R: l R A l R R T A dR R dT 713 Theorie und Aufgaben Temperaturabhängige Änderung des elektrischen Widerstandes R: l R A l A dR R dT R (T ) R (T1 ) e (T T1 ) 713 Theorie und Aufgaben Temperaturabhängige Änderung des elektrischen Widerstandes R l R A l Achtung – a ist nur in einem begrenzten Temperaturbereich konstant! A dR (T ) R dT 721 Wärmekapazität 721 Ziele • Begriff Innere Energie definieren / anhand von Beispielen erklären können • Temperaturerhöhung bei Wärmezufuhr berechnen können • Begriff Wärmekapazität definieren und für ideale Gase / Kristalle berechnen können 721 Theorie Innere Energie U: Änderung durch Zufuhr von Wärme oder Arbeit dU Q W 721 Theorie Innere Energie U: Änderung durch Zufuhr von Wärme oder Arbeit dU Q W U(T,p) dU 0 p T 721 Theorie Innere Energie U: Änderung durch Zufuhr von Wärme oder Arbeit m dU Q Q dU Q W 721 Theorie Innere Energie U: Änderung durch Zufuhr von Wärme oder Arbeit m dU Q Q dU Q W Q cx m dT x 721 Theorie Wärmekapazität für ideales Gas m dU Q Q 1 3 2 m v RT 2 2 721 Theorie Wärmekapazität für ideales Gas m dU Q Q 1 3 2 m v RT 2 2 3 Q nRT CV nT 2 721 Theorie m dU Q Q Äquipartitionstheorem: Befindet sich ein System vieler Teichen im Gleichgewicht, entfällt auf jeden Freiheitsgrad eine Energie von 1 E RT 2 pro Mol bzw. 1 E kT 2 pro Teilchen 721 Theorie Wärmekapazität für Kristall (Gesetz von Dulong-Petit): m dU Q Q CV 3R 721 Theorie Modellierung eines einfachen Wärmespeichersystems: Auskühlender Körper Q IQ 721 Theorie Modellierung eines einfachen Wärmespeichersystems: Auskühlender Körper Q IQ dQ IQ dt 721 Theorie Modellierung eines einfachen Wärmespeichersystems: Auskühlender Körper Q IQ dQ I Q k (T Tu ) dt 721 Theorie Modellierung eines einfachen Wärmespeichersystems: Auskühlender Körper Q dQ I Q k (T Tu ) dt IQ dT k (T Tu ) dt mc0 721 Theorie Substitution: dT k (T Tu ) dt mc0 Q IQ T Tu d d dT T Tu dt dt dt 721 Theorie Substitution: dT k (T Tu ) dt mc0 Q IQ T Tu d d dT T Tu dt dt dt d k dt mc p 721 Theorie Separation und Integration: d k dt mc p Q IQ d k dt mc p 721 Theorie Separation und Integration d k dt mc p Q IQ d k dt mc p k t const. ln mc p 721 Theorie Separation und Integration d k dt mc p Q IQ d k dt mc p k t const. ln mc p (t ) 0 e k t mc p 722 Phasenübergänge 722 Ziele • Gesetz für reales Gas beschreiben können (Was bedeuten die einzelnen Terme?) • Bedeutung des kritischen Punkt kennen • Energie, welche in Phasenumwandlungen steckt, berechnen können 722 Theorie reales Gas: zwischenmolekulare Kräfte spielen eine Rolle 722 Theorie Isothermen pV nRT 722 Theorie Isothermen “relaes Gas” ( p ...)(V ...) nRT 722 Theorie reales Gas: zwischenmolekulare Kräfte spielen eine Rolle a: Kohäsionsdruck b: Kovolumen an 2 p 2 V V nb nRT 722 Theorie an 2 p 2 V V nb nRT Steigung der Isothermen: p V T const an 2 p 2 V nb nRT V 722 Theorie Steigung der Isothermen: nRT an 2 p (V ) 2 V nb V p V T const ... V an 2 p 2 V nb nRT V 722 Theorie Steigung der Isothermen: nRT an 2 p (V ) 2 V nb V p V T const ... V an 2 p 2 V nb nRT V nRT an 2 p(V ) 2 V nb V 722 Theorie Steigung der Isothermen: p V T const V nRT an 2 2 V nb V an 2 p 2 V nb nRT V nRT an 2 p(V ) 2 V nb V 722 Theorie Steigung der Isothermen: p V T const nRT 2an 2 3 V V nb V an 2 p 2 V nb nRT V nRT an 2 p(V ) 2 V nb V 722 Theorie Steigung der Isothermen: p V T const 2an 2 nRT 3 V nb 2 (V nb) V V 722 Theorie an 2 p 2 V V nb nRT Steigung der Isothermen: p V T const 2an 2 nRT 3 V (V nb) 2 an 2 p 2 V V nb nRT 2an 2 nRT p 3 2 V V ( V nb ) T const 722 Theorie Bedingung für den Trippelpunkt: p 0 V p 0 2 V 2 722 Theorie Stoffe ohne und mit Anomalie flüssig Trippelpunkt fest Druck p Druck p fest flüssig Trippelpunkt gasförmig gasförmig Temperatur T Temperatur T Quelle: https://de.wikipedia.org/wiki/Phasendiagramm#/media/File:He4_de.svg Quelle: https://commons.wikimedia.org/wiki/File:Phasendiagramm_des_Kohlenstoffs.png Hatziantoniou et al. (2005): Phasenübergänge von Lipiden und Liposomen. UserCom 1/2005, 16-18 722 Theorie Q Lv m Q Lf m Phasenübergänge sind mit Bindungskräften assoziert: Grössere räumliche Trennung benötigt Energie, bei Kondensation oder Bildung von Festkörpern wird Energie frei Q LV m Q Lf m 722 Theorie Das Konzept lässt sich auch auf chemische Umwandlungen anwenden: Bsp. Brennwert Q Hm Q LV m Q Lf m 723 Zweiter Hauptsatz der Thermodynamik, Entropie 723 Ziele • Entropie als Ordnungsmass verstehen • thermodynamische Entropie makroskopisch definieren können • Aus Entropiestrom Leistung berechnen können 723 Theorie Was ist der Unterschied? 723 Theorie Was ist der Unterschied? (An-) Ordnung physikalischer Prozess: Diffusion, Wärmeleitung Diese Prozesse sind gerichtet, sie laufen spontan nur in eine Richtung! 723 Theorie physikalisches Ordnungsmass: Entropie Dieses Mass lässt sich mikroskopisch (statistischmechanisch) aus den Zuständen der einzelnen Teilchen berechnen Wie die Temperatur lässt sich die Entropie nur für viele Teilchen definieren. 723 Theorie T1 Qrev T2 Entropie S: die bei einer bestimmten Temperatur reversibel ausgetauschte Wärme Qrev dS Qrev T 723 Theorie T1 Qrev T2 Entropie S: die bei einer bestimmten Temperatur reversibel ausgetauschte Wärme Qrev dS Qrev T Für T2 > T1 gilt: dS 2 dS1 Qrev T2 Qrev T1 0 723 Theorie T1 Oder mit Entropiestrom IS: IS2 1 dS I I Si Q dt Ti i I S1 Für T2 > T1 gilt: T2 I S1 I S 2 723 Theorie T1 Oder mit Entropiestrom IS: IS2 1 dS I I Si Q dt Ti i I S1 Für T2 > T1 gilt: T2 I S1 I S 2 Qrev TdS 723 Theorie Zusammenhang zwischen Entropie und innerer Energie: Qrev TdS W F ds pA ds p dV 723 Theorie Zusammenhang zwischen Entropie und innerer Energie: Qrev TdS W F ds 723 Theorie Zusammenhang zwischen Entropie und innerer Energie: pA ds p dV dU T dS p dV 723 Theorie dU T dS p dV U T S V ,N ,... U p V S ,N ,... Zusammenhang zwischen Entropie und innerer Energie: 723 Theorie dU T dS p dV U T S V ,N ,... U p V S ,N ,... Zusammenhang zwischen Entropie und innerer Energie: Intensive Grössen = Druck p Extensive Grössen Volumen V pV nRT TS = Temperatur Entropie S pot. T Energie dS P T T IS dt 723 Theorie Entropiestrom und Leistung: dS P T T IS dt 723 Theorie Entropiestrom und Leistung: 723 Aufgaben Entropie als generelles Ordnungsmass? S x k log x k k 724 Wärmekraftmaschinen 724 Ziele • Kreisprozesse in einem pVDiagramm darstellen können (isotherm, isobar, isochor,isentrop) • Verrichtete Arbeit aus pVDiagramm herauslesen können • thermodynamischer Wirkungsgrad definieren und berechnen können 724 Theorie Einfaches Modell einer Wärmekraftmaschine nicht-zyklisch arbeitend V T2 zyklisch arbeitend, wenn Wärmebad gewechselt wird 724 Theorie Einfaches Modell einer Wärmekraftmaschine nicht-zyklisch arbeitend V T2 zyklisch arbeitend, wenn Wärmebad gewechselt wird dW F ds mg dh 724 Theorie Einfaches Modell einer Wärmekraftmaschine nicht-zyklisch arbeitend V T2 zyklisch arbeitend, wenn Wärmebad gewechselt wird dW F ds mg dh p dV 724 Theorie Carnotscher Kreisprozess 724 Theorie Isotherme Expansion mit Arbeitsmedium ideales Gas V2 p1 V1 p 2 724 Theorie Isotherme Expansion mit Arbeitsmedium ideales Gas V2 p1 V1 p 2 U A W A Q A 0 724 Theorie Isotherme Expansion mit Arbeitsmedium ideales Gas V2 p1 V1 p 2 U A W A Q A 0 V2 dV QA WA NkT2 V V1 724 Theorie Isotherme Expansion mit Arbeitsmedium ideales Gas V2 p1 V1 p 2 U A W A Q A 0 V2 dV QA WA NkT2 V V1 V2 NkT2 ln V1 724 Theorie adiabatische Expansion: dU p dV mcV dT 724 Theorie adiabatische Expansion: dU p dV mcV dT NkT mcV dT dV V 724 Theorie adiabatische Expansion: NkT mcV dT dV V mcV Nk T2 V 2 dT dV T T V V 1 3 724 Theorie adiabatische Expansion: NkT mcV dT dV V mcV Nk T2 V 2 dT dV T T V V 1 3 V2 T2 mcV ln ln Nk T1 V3 724 Theorie adiabatische Expansion: V2 T2 mcV ln ln Nk T1 V3 3 mcV Nk 2 3 1 2 T2 3 T2 V ln ln ln 2 V3 2 T1 T1 3 2 T2 V 3 V2 T1 724 Theorie Isotherme Kompression: p3 V4 V3 p 4 V4 QC NkT1 ln V3 724 Theorie adiabatische Kompression: V1 T1 V4 T2 3 2 WD U 4 mcV (T2 T1 ) 724 Theorie Bilanz: U total QA WA WB QC WC WD Q A QC 0 T2 T1 724 Theorie Entropie im Carnotschen Kreisprozess: U total QA WA WB QC WC WD Qrev T 0 724 Theorie Entropie im Carnotschen Kreisprozess: T U total QA WA WB QC WC WD S Qrev T 0 724 Theorie Wirkungsgrad im Carnotschen Kreisprozess: T Q A QB QA QA W QB T1 1 1 QA T2 S 724 Theorie Wirkungsgrad im Carnotschen Kreisprozess (Betrachtung Entropiestrom): T Pmech Pmech Ptherm T2 I S (T2 T1 ) I S T2 I S S 724 Theorie Anderer Kreisprozess (einfach zur Berechnung der abgegebenen Arbeit (vom Prozess umschlossene Fläche), aber nicht optimaler Wirkungsgrad) p V 724 Theorie Anderer Kreisprozess (einfach zur Berechnung der abgegebenen Arbeit (vom Prozess umschlossene Fläche), aber nicht optimaler Wirkungsgrad) p W p V V 731 Reaktionsenergie und Enthalpie 731 Ziele • Begriffe exotherme und endotherme Reaktion definieren können • Reaktionsenthalpie für einfache chemische reaktionen berechnen können • Satz von Hess erklären können 731 Theorie Energien bei chemischer Reaktion 731 Theorie Energien bei chemischer Reaktion 731 Theorie Energien bei chemischer Reaktion Def. Reaktionsenthalpie H U p V 731 Theorie Energien bei chemischer Reaktion Def. Reaktionsenthalpie H U p V W U 2 p V U1 H H H 0f (Produkte) 731 Theorie H (Reaktanden) 0 f Berechnung über StandardEnthalpien H H 0f (Produkte) 731 Theorie H (Reaktanden) 0 f Berechnung über StandardEnthalpien Bindu ng Bindungs Bindun Bindungs Bindun Bindungs energie kJ g energie g energie / mol kJ / mol kJ / mol Br-Br 193 C-O 335 I-I 151 C-C 347 Cl-Cl 243 N-H 389 C=C 619 F-F 155 N-N 159 C-H 414 H-Br 364 O-H 463 C-F 485 H-Cl 431 O-O 138 C-N 293 H-H 435 O2 494 732 Chemische Reaktionskinetik 732 Ziele • • • • zeitlicher Verlauf von chemischen Reaktionen modellieren und simulieren können Reaktionen nullter, erster und zweiter Ordnung beschreiben können für einfache Fälle aus chemischer Reaktion kinetische Ordnung bestimmen können Reaktionskinetik bei enzymatischen /katalytischen Reaktionen beschreiben können 732 Theorie Reaktionsgeschwindigkeit: dc c dt Zeit t 732 Theorie Reaktionsgeschwindigkeit ist temperaturabhängig Ansatz: Kollisionstheorie Zeit t 732 Theorie Reaktionsgeschwindigkeit ist temperaturabhängig Anzahl Moleküle T1 T2 Energie 732 Theorie potentielle Energie Aktivierungsenergie Ea Reaktionskoordinate 732 Theorie Kinetik nullter Ordnung dc A k dt 732 Theorie Kinetik nullter Ordnung dc A k dt c c A (t ) kt c A (0) Zeit t 732 Theorie Kinetik erster Ordnung dc A k c A dt 732 Theorie Kinetik erster Ordnung dc A k c A dt c c A (t ) c 0 e Zeit t kt 732 Theorie Kinetik zweiter Ordnung dc A k c AcB dt dc A 2 k c A dt 732 Theorie Kinetik zweiter Ordnung dc A 2 k c A dt dc A 1 c A2 k dt kt c c A 732 Theorie Kinetik zweiter Ordnung dc A 2 k c A dt c dc A 1 c A2 k dt kt c c A Zeit t 1 c A (t ) kt c A ( 0) 1 732 Theorie Weitere Varianten A + 2B Produkte dc A k c A c B2 dt 732 Theorie potentielle Energie Temperaturabhängigkeit der Reaktionskonstante Ea k Ae Reaktionskoordinate E a /( RT ) 732 Theorie katalytische bzw. enzymatische Reaktionen vm c dc ( k m c ) Vd dt 732 Theorie katalytische bzw. enzymatische Reaktionen vm c dc ( k m c ) Vd dt vm c lim c 0 ( k c ) V d m vm c k m Vd 732 Theorie katalytische bzw. enzymatische Reaktionen vm c dc ( k m c ) Vd dt vm c lim c 0 ( k c ) V d m vm c lim c ( k c ) V d m vm c k m Vd vm Vd vm c dc dt ( k m c ) Vd 732 Theorie katalytische bzw. enzymatische Reaktionen c = dc dt c max = vm vm c lim c ( k c ) V d m vm 2 vm c lim c 0 ( k c ) V d m km vm c k m Vd c(t) vm Vd k1 A Y X k2 X Y P k3 2X Z A X k4 2 X Q k5 Z fY 732 Supplement Oszillierende Reaktionen: Belousov-ZhabotinskiiReaktion BZR: A: BrO3X: HBrO2 Y: BrZ: Ce(IV) 732 Supplement k1 A Y X k2 X Y P k3 2X Z A X k4 2 X Q k5 Z fY Oszillierende Reaktionen: Belousov-ZhabotinskiiReaktion BZR dX k1 AY k2 XY k3 AX 2k4 X 2 dt dY k1 AY k2 XY fk5 Z dt dZ k3 AX k5 Z dt dX k1 AY k2 XY k3 AX 2k4 X 2 dt dY k1 AY k2 XY fk5 Z dt dZ k3 AX k5 Z dt 732 Supplement Oszillierende Reaktionen: Belousov-ZhabotinskiiReaktion BZR 732 Supplement Oszillierende Reaktionen: Belousov-ZhabotinskiiReaktion BZR Fig.69. Oszillationsformen in Abhängigkeit des Anfangswertes X0: (a) X0 = 0.2, (b) X0 = 1.5, (c) X0 = 3, (d) X0 = 4; Y0 = Z0 = 0, A = 3; k1 = 1 s1, k = 0.5 s-1, k = 0.175 2 3 -1 s , k4 = 0.175 s-1, k5 = 1 s-1, f = 4; Nummerik: Runge-Kutta-Verfahren, t = 10-3 s. 741 Wärmeleitung 741 Ziele • • • • Wärmestrom und Temperaturprofile für einfache Geometrien berechnen können Die physikalische Bedeutung von Gradient und Divergenz erläutern können Die Bedeutung der einzelnen Terme / Teile der Diffusionsgleichung beschreiben können Zwischen stationären und transienten Lösungen (der Diffusionsgleichung) unterscheiden können 741 Theorie Wärmestrom / Wärmestromdichte x A IQ dQ j dA dt dT j k dx 741 Theorie Wärmestrom / Wärmestromdichte für Stab: x A IQ dT j k dx T j j T dT k dx k x 1 741 Theorie Wärmestrom / Wärmestromdichte für Stab: x A IQ dT j k dx T j j T dT k dx k x 1 T T1 741 Theorie Wärmefluss in 2D und 3D: Wärmediffusion Ansatz: Wärmestrombilanz für ein Masseelement dV I Qx (x) dx dy dz I Qx ( x dx) 741 Theorie dV dx dy dz Wärmefluss in 2D und 3D: Wärmediffusion j x dQ /(dt dy dz ) j x ( x) dy dz j x ( x dx) dy dz 741 Theorie dV dx dy dz Wärmefluss in 2D und 3D: Wärmediffusion j x dQ /(dt dy dz ) j x ( x) dy dz j x ( x dx) dy dz j x j x ( x dx) j x ( x) x dx 741 Theorie j z ( z dz ) dy dx j x ( x) dy dz j x ( x) dy dz Wärmefluss in 2D und 3D: Wärmediffusion j x ( x dx) dy dz j y Q j j dy dx dz z dz dy dx x dx dy dz t x z y j j y j z dx dy dz x x y z 741 Theorie u Q / V Q /( dx dy dz ) Wärmedichte j y Q j j dy dx dz z dz dy dx x dx dy dz t x z y j j y j z dx dy dz x x y z 741 Theorie u Q / V Q /( dx dy dz ) Wärmedichte j x j y j z du j div( j ) dt z x y j y Q j j dy dx dz z dz dy dx x dx dy dz t x z y j j y j z dx dy dz x x y z 741 Theorie Zusammenhang zwischen Wärmestromdichte und Wärmedichte bzw. Temperaturgradient? j x j y j z du j div( j ) dt x y z 741 Theorie Zusammenhang zwischen Wärmestromdichte und Wärmedichte bzw. Temperaturgradient? Ficksches Gesetz j x j y j z du j div( j ) dt x y z j k u k grad (u ) 741 Theorie j x j y j z du j div( j ) dt x y z j k u k grad (u ) u j x k x u j y k y u j z k z 741 Theorie j x j y j z du j div( j ) dt x y z j k u k grad (u ) u j x k x u j y k y 2 2 2 u u u u k 2 2 2 dt y z x u j z k z 741 Theorie 2 2 2 u u u u k 2 2 2 dt y z x dQ dm c T u cT dx dy dz dV dT k 2T 2T 2T 2 2 2 dt c dx dy dz dT k 2T 2T 2T 2 2 2 dt c dx dy dz 741 Aufgaben Lösungen für langer Stab dT k T 2 dt c dx 2 x A IQ dT k 2T 2T 2T 2 2 2 dt c dx dy dz 741 Aufgaben Lösungen für langer Stab dT k T 2 dt c dx 2 x T ( x, t ) T0 e A IQ 1 x 2 t T(x) 741 Aufgaben Lösungen für langer Stab T(x,t) T(x,0) x Je nach Randbedingungen T(x) WärmeReservoir mit T(0,t)=const. stationärer Fall WärmeReservoir mit T(l,t)=const. T(x,t) T(x,0) x T(x) WärmeReservoir mit T(0,t)=const. stationärer Fall Isolation T(x,t) T(x,0) x transiente Lösungen stationäre Lösungen 742 Wärmestrahlung 742 Ziele • von einem Körper in Form von Wärmestrahlung abgestrahlte Leistung berechnen können • Aussagen über EmissionsSpektrum und Temperatur machen können • die Arten des Wärmetransportes kennen 742 Theorie Möglichkeiten des Wärmetransports: Konvektion: Wärme wird mit Material transportiert ? Wärmeleitung (kunduktiv): Wärme wird als molekulare Schwingung durch Stösse im Medium transportiert Strahlung (radiativ): ??? 742 Theorie Experiment / Beobachtung Ein heisses Objekt strahlt Wärme ab Wärmestrahlung Diese Strahlung geht auch durch ein Vakuum hindurch ? Strahlung benötigt kein Medium! 742 Theorie Experiment / Beobachtung Ein heisses Objekt strahlt Wärme ab Wärmestrahlung E Diese Strahlung geht auch durch ein Vakuum hindurch B B E Strahlung benötigt kein Medium! elektromagnetische Strahlung (Kap. 800 & 900) 742 Theorie Experiment / Beobachtung Ein heisses Objekt strahlt Wärme ab Wärmestrahlung Diese Strahlung geht auch durch ein Vakuum hindurch Strahlung benötigt kein Medium! elektromagnetische Strahlung (Kap. 800 & 900) 742 Theorie max b T Wellenlänge des Strahlungsmaximums (Wiensches Verschiebungsgesetz) 742 Theorie max b T P AT Wellenlänge des Strahlungsmaximums (Wiensches Verschiebungsgesetz) 4 abgestrahlte Leistung 742 Theorie max b T P AT Wellenlänge des Strahlungsmaximums (Wiensches Verschiebungsgesetz) 4 abgestrahlte Leistung Material Temperatur / °C Aluminium poliert 170 0.05 Stahl poliert 20 0.16 Kupfer oxidiert 20 0.78 Wasser 0...100 0.95 Emissionszahlen