Hinweise zu den Protokollen für das
Werbung
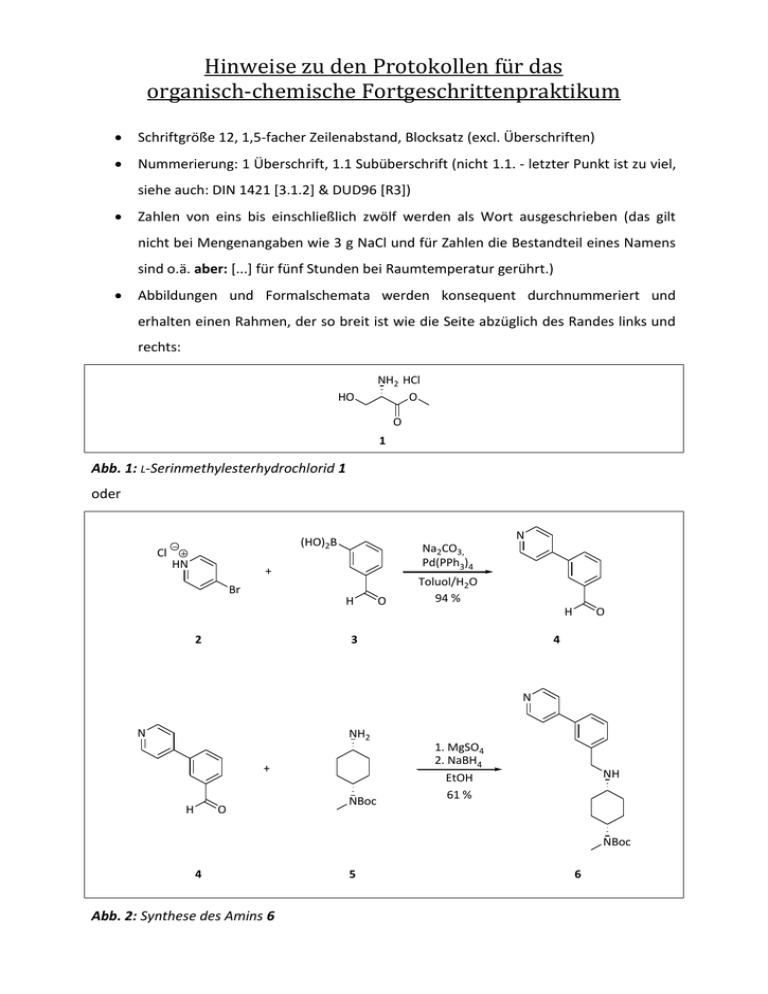
Hinweise zu den Protokollen für das organisch-chemische Fortgeschrittenpraktikum Schriftgröße 12, 1,5-facher Zeilenabstand, Blocksatz (excl. Überschriften) Nummerierung: 1 Überschrift, 1.1 Subüberschrift (nicht 1.1. - letzter Punkt ist zu viel, siehe auch: DIN 1421 [3.1.2] & DUD96 [R3]) Zahlen von eins bis einschließlich zwölf werden als Wort ausgeschrieben (das gilt nicht bei Mengenangaben wie 3 g NaCl und für Zahlen die Bestandteil eines Namens sind o.ä. aber: [...] für fünf Stunden bei Raumtemperatur gerührt.) Abbildungen und Formalschemata werden konsequent durchnummeriert und erhalten einen Rahmen, der so breit ist wie die Seite abzüglich des Randes links und rechts: HO NH2 HCl O O 1 Abb. 1: L-Serinmethylesterhydrochlorid 1 oder Cl N (HO)2B HN Na2CO3, Pd(PPh3)4 + Br H 2 O Toluol/H2O 94 % H 3 O 4 N N NH2 + H O NBoc 1. MgSO4 2. NaBH4 EtOH 61 % NH NBoc 4 Abb. 2: Synthese des Amins 6 5 6 Die Bildunterschrift wird kursiv gesetzt; die Abkürzung „Abb.“, die folgende Zahl(enkombination) und der Doppelpunkt werden fett und kursiv gesetzt kommen in der Bildunterschrift chemische Bezeichnungen vor, die Diskriptoren oder ähnliches enthalten, die im Normaltext kursiv wären, können diese in der Unterschrift zur Unterscheidung normal gesetzt werden (z.B.: Abb 3: Synthese von tert-Butyl-(trans-4-aminocyclohexyl)methylcarbamat) WICHTIG: Strukturen in Abbildungen müssen gleich groß sein. D.h. ein Benzolring in Abb. 1 muss die gleiche Größe haben wie einer in Abb. 5 ! Jede im Protokoll angegebene Struktur erhält eine Nummer, diese wird unterhalb der Struktur angegeben (Zahl wird fett gesetzt); bezieht man sich später im Text auf diese Struktur wird die Zahl wieder fett gesetzt (z.B. [...] so konnte Verbindung 3 als weißer Feststoff in 36 % Ausbeute erhalten werden) WICHTIG: Die Zahlen müssen so vergeben werden, dass die Strukturen nach Reihenfolge ihres Erscheinens im Protokoll nummeriert sind. D.h. die Struktur, die als erste im Protokoll auftaucht bekommt die Nummer 1, die zweite die 2 usw. Hinweis: Basen, Säuren, Katalysatoren und Lösungsmittel werden, damit sie nicht in die Nummerierung eingeschlossen werden müssen, über den Reaktionspfeil platziert. Wiederholt auftretende Strukturen erhalten immer wieder dieselbe Nummer. (vgl. Verbindung 4 in Abb. 2) Nomenklatur: - die Stereodiskriptoren R und S (sowie pro-R und pro-S), l und u, sp-, sc-, ac-, ap-, erythro und threo, cis und cisoid sowie trans und transoid, E und Z (sowie pro-E und pro-Z), P und M, ortho-, meta-, para- und ihre Einbuchstabenabkürzungen o-, m-, p-, das H zur Angabe indizierter Wasserstoffatome, Elementsymbole zur Angabe von Einzelatomen (z.B.: N,N-Dimethylformamid [das Komma zwischen den beiden N ist nicht kursiv]) sowie griechische Buchstaben, die Präfixe n-, sec-, tert-, abeo-, anti-, ent-, epi-, rac-, rel-, syn-, iso-, ipso-, meso-, gem- und vic- werden kursiv gesetzt - die Stereodiskriptoren D und L sowie das M für molar bzw. N zur Angabe der Normalität einer Lösung werden als Kapitälchen gesetzt (z.B. eine 1.8 M L-Glucoselösung) - Es gibt einen Unterschied zwischen Bindestrich und Minus: das Minus ist genauso lang wie der Querbalken des Plus! (L-(+)-Weinsäure, D-(−)-Weinsäure) Experimenteller Teil: die Experimente wurden vor einiger Zeit abgeschlossen, folgerichtig ist die für die Durchführung zu verwendende Zeitform das Präteritum Wörter & Wendungen wie ausgeschüttelt, refluxiert / kochen, am Rotationsverdampfer abgezogen (und weitere) sind Laborsprache – also nicht gut genug für das Protokoll in dem Schriftsprache erwartet wird. Daher besser folgende Wendungen verwenden: - extrahieren, unter Rückfluss erhitzen, [das Lösungsmittel] unter vermindertem Druck entfernen Sätze wie „Ich habe daraufhin die verschüttete produktbeinhaltende Lösung aufgesammelt“ gehören nicht in den experimentellen Teil. Solche Informationen kommen in den Diskussionsteil. „Ich“ ist im experimentellen Teil nicht zu verwenden. Stattdessen ist „man“ zu nutzen. Aktiv durch Passiv ersetzen (z.B.: Es wurden 5.78 g (3.67 mmol, 87 %) von Verbindung 7 erhalten.) Grundsätzlich erfolgt die Angabe der Menge für alle verwendeten Reagenzien immer dreigeteilt: Angabe der Masse in Gramm, der Stoffmenge in mol bzw. mmol oder µmol und die Angabe der Äquivalente z.B.: Ein Gemisch aus 150 mg (819 μmol, 1.0 Äq.) 3-(Pyridin-4-yl)benzaldehyd, 187 mg (819 μmol, 1.0 Äq.) tert-Butyl-(trans-4-aminocyclohexyl)methylcarbamat und 119 mg (989 μmol, 1.2 Äq.) wasserfreiem Magnesiumsulfat in 7.0 ml absolutem Ethanol wurde in ein Druckglas gegeben und für acht Stunden auf 80 °C erhitzt. Bei Flüssigkeiten wird zusätzlich das Volumen angegeben: [...] 3.25 ml (2.37 g, 23.4 mmol, 1.5 Äq.) Triethylamin [...] WICHTIG: Auf signifikante Ziffern achten! Angaben wie 3.4 g (12.345 mmol) sind inkorrekt. Die Stoffmenge wird hier mit fünf signifikanten Ziffern angegeben obwohl die gemessene Größe (Masse) nur mit zwei signifikanten Ziffern bestimmt wurde. Es muss also korrekt heißen: 3.4 g (12 mmol). Da im Praktikum hauptsächlich auf 10 mg genau gemessen wurde, ergibt sich in der Regel also solch eine Angabe: 1.23 g (17.5 mmol, X.X Äq.) Statt 0.123 mol anzugeben ist es besser 123 mmol zu schreiben. Vor dem Prozentzeichen ist stets ein Leerzeichen bzw. schmales Leerzeichen zu setzen; gleiches gilt für Angaben von Temperaturen, dort ist zwischen Zahlenwert und dem Gradsymbol ein Leerzeichen zu setzen (↗ EinhZeitG & DIN 1301 Teil 1) Sollten am Ende einer Zeile einzelne Zahlen oder Präfixe von Namen stehen, sollten diese auf die nächste Zeile verschoben werden; Es ist darauf zu achten, dass Zahlen und Einheiten nicht am Ende einer Zeile getrennt werden DC: Der Rf-Wert wird auf zwei Nachkommastellen angegeben, in Klammern steht das Lösungsmittelgemisch, getrennt durch Schrägstrich und das Verhältnis getrennt durch Doppelpunkt sowie der Zusatz v/v, z.B.: Rf = 0.49 (n-Hexan/Essigester 3:1 v/v) Schmelzpunkte: zur vollständigen Angabe des Schmelzpunktes gehört die Nennung des Lösungsmittels aus welchem das Produkt umkristallisiert wurde Smp.: 134 °C (CH3OH) Kernspinresonanzspektroskopie (NMR): - 1 H-NMR: Angegeben werden zunächst Senderfrequenz und Lösungsmittel (CDCl3, CD3OD, DMSO-d6, D2O und andere) dann folgen die Signale mit ihren chemischen Verschiebungen (zwei Nachkommastellen), beginnend bei niedrigen ppm-Werten. Bei Signalen mit definierten Multiplizitäten (s, d, t, q, dd, ddd, dt, td, tt, u.a.) wird der Signalschwerpunkt angegeben. Bei Multipletts wird der Signalbereich angegeben. Hinter der chemischen Verschiebung folgen in Klammern: Multiplizität abgekürzt als s (Singulett), d (Dublett), t (Triplett), q (Quartett), m (Multiplett), dd (Dublett vom Dublett) etc. Relatives Integral des Signals (Anzahl der H-Atome dieses Signals) bei Dubletts, Tripletts, etc. werden als nächstes die Kopplungskonstante(n) angegeben. Kopplungskonstanten werden in Hertz mit einer Nachkommastelle angegeben. Das J wird kursiv gesetzt. Ganz korrekt wäre eine Angabe wie folgt: xJH,H=7.8 Hz (Wobei das x durch eine Zahl ersetzt werden muss, die angibt, über wie viele Bindungen diese Kopplung zustande kommt. Der Index bezeichnet die koppelnden Kernspezies. Bei Angabe von mehr als einer Kopplungskonstante bei einem Signal (z.B. bei einem Doppeldublett) werden diese nach ihrem Betrag absteigend sortiert angegeben. die Zuordnung zu einem Proton: Hierfür wird die Struktur nicht erneut gezeichnet und mit einer Nummerierung versehen! Es gibt zur Kennzeichnung zwei Möglichkeiten: Man verwendet sinnvolle Abkürzungen für Formelausschnitte wie OCH3, CO2CH3 oder CH2CH3, wobei das/die betreffende/n Wasserstoffatome fett hervorgehoben wird/werden. Oder man bezeichnet ein H z. B. mit H-1, wobei dann allerdings die Nummerierung aus dem Substanznamen hervorgehen muss (IUPAC-Nummerierung der Atome) – H-1, H-2, ... wird auch fett gesetzt. Das Ganze sieht dann z. B. folgendermaßen aus: 1 H-NMR (300 MHz, CDCl3) δ [ppm] = 1.04 (s, 9H, C(CH3)3), 1.34-1.42 (m, 1H, H-7), 2.01 (dd, 1H, 3JHH=6.9 Hz, 2JHH=4.3 Hz, H-2), 7.35-7.46 (m, 3H, Harom) - 13 C-NMR: Analog zum 1H-NMR, aber nur eine Nachkommastelle angeben, bei der Zuordnung die gleiche Nummerierung wie beim 1H-NMR verwenden bzw. das/die betreffende/n C-Atom/e im Formelausschnitt fett setzen Das Ganze sieht dann z. B. folgendermaßen aus: 13 C-NMR (100 MHz, CDCl3): δ = 27.7 (C-3, C-3’), 28.5 (-N-CH3), 28.5 (C(CH3)3), 32.0 (C-2, C-2’), 38.9 (-SO2-CH3), 52.5 (br, C-4), 79.7 (-C(CH3)3), 80.1 (C-1), 155.6 (C=O) Man beachte beim Signal bei 28.5: fett sind das Methyl-C und die 3, weil das Signal drei C-Atome repräsentiert! (br steht für ein verbreitertes Signal) NEU ab WS 2014/15: Interpretieren Sie je eines Ihrer 1H- und 13C-NMR-Spektren IN WORTEN, soweit dies mit eindimensionalen Spektren möglich ist. D.h. schreiben Sie auf, welche Informationen sich daraus ablesen lassen, nutzen Sie: Signallage, Signalgestalt, Integration des Signals. Lehnen Sie sich an den Stil an, den Prof. Berger in >Berger & Sicker, Classics in Spectroscopy – Isolation an d Structure Elucidation of Natural Products< nutzt. Brechungsindex: - wird auf vier Nachkommastellen genau angegeben z.B.: nD20 1.4567 , D und 20 stehen direkt übereinander; die hochgestellte Zahl bezeichnet die Messtemperatur Literaturverzeichnis: Alle verwendeten Literaturstellen müssen zurückverfolgbar sein, das gilt insbesondere für Vergleichsspektren und Literaturangaben von Messwerten. Im fließenden Text werden Literaturverweise in eckigen Klammern gesetzt und hochgestellt immer hinter dem Satzzeichen angegeben.[1] Am Ende des Protokolls werden alle Literaturstellen in der Reihenfolge ihrer Erwähnung im Text aufgeführt. Bei Zeitschriften werden bei allen Autoren die Vornamen abgekürzt, Zeitschriftenbezeichnungen wie international üblich abgekürzt (siehe im Internet z.B. unter: http://www.library.ubc.ca/scieng/coden.html) und kursiv gesetzt, das Erscheinungsjahr wird fettgedruckt, der Jahrgang der Zeitschrift kursiv, dann die Seitenzahlen mit Bindestrich (nicht 1113ff.). Hinter die Literaturangaben wird immer ein Punkt gesetzt. z. B.: [1] Ian B. Seiple, Shun Su, Ian S. Young, Chad A. Lewis, Junichiro Yamaguchi, Phil S. Baran, Angew. Chem. 2010, 122, 1113-1116. Bei Büchern wird angegeben: Autor(en), Titel kursiv gesetzt (in Klammern der Herausgeber falls abweichend – nicht kursiv), Auflage, Verlag, Sitz des Verlages, das Erscheinungsjahr (fett) und die Seitenzahlen mit der Abkürzung S. z.B.: [2] Y. S. Cho, H. J. Kwon in Protein Targeting with Small Molecules: Chemical Biology Techniques and Applications (Hrsg.: H. Osada), Vol. 1, John Wiley & Sons, Hoboken, 2009, S. 81-90. Bei Internetquellen muss die gesamte URL angegeben werden (nicht nur die Hauptseite) und das Datum des Besuches, z.B.: [3] http://de.wikipedia.org/wiki/Zitieren_von_Internetquellen (Stand: 17.06.2014).