I. Transformation durch Aktivierung von zellulären Signal
Werbung
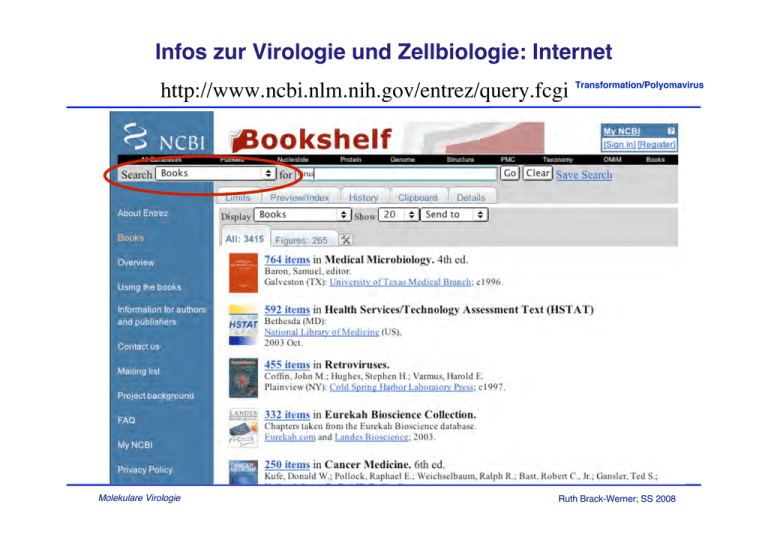
Infos zur Virologie und Zellbiologie: Internet http://www.ncbi.nlm.nih.gov/entrez/query.fcgi Transformation/Polyomavirus Molekulare Virologie Ruth Brack-Werner; SS 2008 Infos zur Virologie und Zellbiologie: Weitere Bücher Transformation/Polyomavirus Molekulare Virologie Ruth Brack-Werner; SS 2008 VORLESUNGSPLAN Transformation/Polyomavirus Thema 1 Transformation ; DNA Viren ; Datum Stunden/Lektor Ort 15.4. 1,5; RBW Gosser HS Genetik ; MW Str. Infektionsphänotypen; DNA Viren 22.4. 1,5; RBW Molekulare Diagnostik 29.4. 1,5 HN 1 DNA Viren 6.5. 1,5 RBW VORLESUNGSFREI (offiziell) 13.5. RNA Virus Vektoren 20.5. 1,5; BS DNA Virus Vektoren 27.5... 1,5 BS Vakzine 3.6. 1,5 BS Antivirale Strategien 10.6. 1,5 RBW Virusevolution 17.6. 1,5 RBW Neurovirologie 24.6. 1,5 RBW “Joker” oder Vorlesungsfrei 1.7. Klausur 8.7. 1,5 RBW, HN Grosser HS Genetik 1RBW: BS: HN: Ruth Brack-Werner: [email protected] Brian Salmon: [email protected] Hans Nitschko: [email protected] 2Parvoviren, Molekulare Virologie Polyomaviren, Pockenviren, Papillomaviren, Herpesviren Ruth Brack-Werner; SS 2008 Beteiligung von Viren an Krebserkrankungen Direkt: Transformation/Polyomavirus Infektion führt zur onkogenen Transformation der Zelle. Beispiel: Rous Sarcoma Virus Indirekt: Infektion von Zelle A führt zu Veränderungen, die die onkogene Transformation der Zelle B begünstigen. Beispiel Humanes Immundefizienzvirus Molekulare Virologie Ruth Brack-Werner; SS 2008 Beispiel für die virus-assoziierte Onkogenese Transformation/Polyomavirus durch indirekte Mechanismen AIDS (HIV) assoziierte Tumorerkrankungen •Kaposi Sarkom: maligne Erkrankung des Gefäss-Systems; Mischung von Endothelzellen und inflammator. Zellen; •AIDS-related lymphomas (ARL); Non-Hodgkin’s Lymphome; in erster Linie B-Zell-Ursprung; oft EBV oder HHV-8 positiv Burkitt’s Lymphom; diffuses gross-zelliges B-Zelllymphom (DLBCL); Primäres ZNS-Lymphom (PCNS) •Cervixkarzinom; Gebärmutterhalskrebs; Epithelzellen Molekulare Virologie Ruth Brack-Werner; SS 2008 Beispiele für Tumor-auslösende RNA Viren Transformation/Polyomavirus Retroviridae RSV, MSV, MuLV; SSV/SSAV; HTLV Verschiedene Tumore und Leukämien Flaviviridae Hepatitis C Virus Leberkarzinome Molekulare Virologie Ruth Brack-Werner; SS 2008 Beispiele für Onkogene DNA-Viren Transformation/Polyomavirus Adenoviridae Adenovirus Hepadnaviridae Papillomaviridae Hepatitis B Virus Epstein Barr Virus HPV 16, -18 Polyomaviridae SV40 Herpesviridae Molekulare Virologie Verschiedene solide Tumore Leber-Karzinome B-Zell Lymphome Cervix Karzinom Verschiedene solide Tumore Ruth Brack-Werner; SS 2008 Krebserkrankungen beim Menschen mit virale Beteiligung Transformation/Polyomavirus Molekulare Virologie Ruth Brack-Werner; SS 2008 Einige gemeinsame Eigenschaften der onkogenen Zell-Transformation durch Viren 1. Transformation/Polyomavirus Infektion führt nicht zum Zelltod; 2. Einmalige Infektion der Zelle ausreichend für ihre Transformation (“single-hit” Mechanismus); 3. Persistente Infektion; Molekulare Virologie Ruth Brack-Werner; SS 2008 Zelltransformation durch Retroviren Transformation/Polyomavirus Transduzierende Viren; Übertragen ein Onkogen; Nicht-transduzierende Viren; Enthalten selber kein Onkogen; Transformation ist auf die Beeinflussung der Expression von zellulären Tumor-assoziierten Genen zurückzuführen. Molekulare Virologie Ruth Brack-Werner; SS 2008 Transformierte Zellen Transformation/Polyomavirus Mögliche Eigenschaften 1. Immortalisation; 2. Morphologische Veränderungen; 3. Verminderte Abhängigkeit von Wachstumsfaktoren; 4. Können bei Nährstoffmangel nicht in die Ruhephase eingehen; 5. Können “ Foci” (= Zellhaufen) bilden; 6. Wachstum ohne Anheftung möglich; 7. Tumorinduktion in Versuchtstieren; Molekulare Virologie Ruth Brack-Werner; SS 2008 Virus-transformierte Zellen Transformation/Polyomavirus Beispiel: Rous sarcoma virus infizierte und transformierte Hühnerzellen Focus A Übereinander wachsende Zellen in Focus A Focus C Normale und transformierte Zellen in Focus C Principles of Virology, 2004. Flint SJ, Enquist LW, Racaniello VR,Skalka AM, 2nd edition. ASM Press. Fig. 18.2. Molekulare Virologie Ruth Brack-Werner; SS 2008 Mechanismen der onkogenen Zelltransformation Transformation/Polyomavirus 1. Dauerhafte Aktivierung von zellulären SignalTransduktionswegen; 2. Eingriff in die Zellzyklus-Kontrolle; 3. Verhinderung der Apoptose. Molekulare Virologie Ruth Brack-Werner; SS 2008 Transformierende Gene/Proteine von DNA Viren Transformation/Polyomavirus Häufige Eigenschaften: 1. Sind häufig regulatorische Proteine, die in der frühen Phase des viralen Replikationszyklus exprimiert werden; 2. Multifunktionell; 3. Interaktion mit zellulären Faktoren ist wesentlich für die Transformation; 4. Die Transformation ist oft das Ergebnis der Zusammenwirkung von mehreren viralen Protein; Molekulare Virologie Ruth Brack-Werner; SS 2008 Tumor-Induktion durch DNA Viren Transformation/Polyomavirus Persistente Virus-Infektion; • Persistenz des viralen Genoms durch Integration in das Wirtszellgenom (z.B. Polyomavirus) oder extrachromosomal als Episom (z.B. EBV) • Dauerhafte Expression von wenigen oder einem viralen Genprodukt; • Molekulare Virologie Transformation ist ein seltenes Ereignis. Ruth Brack-Werner; SS 2008 Mechanismen der onkogenen Zelltransformation I. Transformation/Polyomavirus Dauerhafte Aktivierung von zellulären SignalTransduktionswegen; II. Eingriff in die Zellzyklus-Kontrolle; III. Verhinderung der Apoptose. Molekulare Virologie Ruth Brack-Werner; SS 2008 I. Transformation durch Aktivierung von zellulären Signal-Transduktions WegenTransformation/Polyomavirus Aktivierung von Tyrosin-Kinasen: Beispiel c-Src Myristyl-Kette P X v-src Membranverankerung Kinase Aktivität Protein-Protein Interaktionen: SH3: Prolin-reiche Sequenz SH2: Phosphotyrosine-haltige Sequenz Principles of Virology, 2004. Flint SJ, Enquist LW, Racaniello VR,Skalka AM, 2nd edition. ASM Press. Fig. 18.9A. Molekulare Virologie Ruth Brack-Werner; SS 2008 I. Transformation durch Aktivierung von zellulären Signal-Transduktions Wegen Transformation/Polyomavirus De-Aktiverung durch Phosphorylierung von Y527 Inaktive Konformation: Zusammengehalten durch Interaktion von dem phospyhorylierten Tyrosine 527 mit der SH2 Domäne von c-Src. Aktivierung: Autophosphorlyierung von Y416 durch Bindung von Liganden an SH2 bzw. SH3 Domänen bzw. Dephosphorylierung von Y527D Martin GS. The hunting of the src. 2001. Nature Reviews Molecular Biology 2, 467-475 Molekulare Virologie Ruth Brack-Werner; SS 2008 I. Transformation durch Aktivierung von zellulären Signal-Transduktions WegenTransformation/Polyomavirus Mechanismen zur dauerhafte Aktivierung c-Src: • Beispiel RSV: Transduktion eines Genes das für ein dauerhaft aktiviertes Src-Analog kodiert (v-Src). Martin GS. The hunting of the src. 2001. Nature Reviews Molecular Biology 2, 467-475 Molekulare Virologie Ruth Brack-Werner; SS 2008 I. Transformation durch Aktivierung von zellulären Signal-Transduktions WegenTransformation/Polyomavirus Mechanismen zur dauerhafte Aktivierung c-Src: Beispiel Polyomavirus Mittel-TAntigen: Protein Phosphatase 2a Rekrutierung von verschiedenen zellulären Proteinen zur Aktivierung von Src einerseits (hier PP2A) und von SignalTransduktionskaskaden andererseits Principles of Virology, 2004. Flint SJ, Enquist LW, Racaniello VR,Skalka AM, 2nd edition. ASM Press. Fig. 18.14B. Molekulare Virologie Ruth Brack-Werner; SS 2008 I. Transformation durch Aktivierung von zellulären Signal-Transduktions Wegen Transformation/Polyomavirus Simulation von aktivierten Rezeptoren für extrazelluläre Signale Beispiel: LMP-1 (Latent Membrane Protein 1) von EBV Molekulare Virologie Ruth Brack-Werner; SS 2008 LMP1 simuliert den TNF-Receptor 1 Transformation/Polyomavirus TNFα LMP1 TNF-receptor 1 TRAFs RIP RIP TRAF2 TRADD Anti-apoptotic pathways Survival Transformation Molekulare Virologie TRADD Apoptosis, necrosis Survival Arnd Kieser, AG Signal Transduction, Dept. Gene Vectors, GSF Ruth Brack-Werner; SS 2008 LMP-1 induziert verschiedene Signal-Transduktion Wege Transformation/Polyomavirus LMP-1 (Oligomerisiert) CTAR:- C-terminal activating region of LMP-1 Traf: Tumor necrosis factor receptor associated protein JAK: Janus kinase Tradd: Traf adaptor JNK: Jun N-terminal kinase IkB: Inhibitor of kappa B NFkB: Nuclear factor kappa B STAT: signal transducer and activation of transcription AP-1: Activator protein Principles of Virology, 2004. Flint SJ, Enquist LW, Racaniello VR,Skalka AM, 2nd edition. ASM Press. Fig. 18.13. Molekulare Virologie Ruth Brack-Werner; SS 2008 I. Transformation durch Aktivierung von zellulären Signal-Transduktions Wegen Transformation/Polyomavirus Chung JY et al., 2002. J Cell Sci 115, 679-688 Molekulare Virologie Ruth Brack-Werner; SS 2008 (II) Eingriff in die Zellzykluskontrolle Transformation/Polyomavirus Der Zellzyklus Principles of Virology, 2004. Flint SJ, Enquist LW, Racaniello VR,Skalka AM, 2nd edition. ASM Press. Fig. 18.4. Molekulare Virologie Ruth Brack-Werner; SS 2008 Zellzykluskontrolle: Zyklin/Kinase Komplexe Transformation/Polyomavirus Cyclin B+ cdk2 Zyklin = regulatorische Untereinheit Cyclin A+ cdk2 Zyklinabhängigen kinase = katalytische Untereinheit Principles of Virology, 2004. Flint SJ, Enquist LW, Racaniello VR,Skalka AM, 2nd edition. ASM Press. Fig. 18.5. Mitogene: Wirksam in der G1 Phase bzw. in Go, wo sie den Eintritt in den Zellzyklus bewirken; Molekulare Virologie Ruth Brack-Werner; SS 2008 (II) Inaktivierung von Tumor-SuppressorTransformation/Polyomavirus Proteinen; Rb Protein Eigenschaften des RbProteins 1. Tumor-Suppressor-Protein 2. Im hypo-phosphorylierten Zustand bindet Rb den Transkriptionsfaktor E2F und hemmt die Transkription von E2F-abhängigen Genen; 3. Die Phosphorylierung von Rb durch Zyklin D/Kinasen führt zur Freisetzung von E2F; 4. E2F aktiviert die Expression von verschiedenen Genen: 1. Zykline/Kinasen zur weiteren Phosphorylierung von Rb; 2. Gene für die DNA Synthese und Mitose; 3. E2F Gen Molekulare Virologie Ruth Brack-Werner; SS 2008 (II) Regulation von E2F durch Rb Transformation/Polyomavirus Principles of Virology, 2004. Flint SJ, Enquist LW, Racaniello VR,Skalka AM, 2nd edition. ASM Press. Fig. 18.16A. Molekulare Virologie Ruth Brack-Werner; SS 2008 (II) Freisetzung von an Rb Protein gebundenes E2F durch virale Proteine Transformation/Polyomavirus Abbau von Rb-E2F Komplexen durch SV40 T-antigen Principles of Virology, 2004. Flint SJ, Enquist LW, Racaniello VR,Skalka AM, 2nd edition. ASM Press. Fig. 18.17. Molekulare Virologie Ruth Brack-Werner; SS 2008 (II) Funktionelle Domänen des Rb Proteins Transformation/Polyomavirus Principles of Virology, 2004. Flint SJ, Enquist LW, Racaniello VR,Skalka AM, 2nd edition. ASM Press. Fig. 18.16B. Molekulare Virologie Ruth Brack-Werner; SS 2008 (II) Weitere virale Mechanismen zur Inaktivierung von Rb Transformation/Polyomavirus Förderung der Phosphorylierung von Rb durch Erhöhung des Pools an Zyklin/Kinasen 1. HHV-8 v-Cyclin: • Virus-kodiertes Zyklin; Homolog von Zyklin D2; • Bindet nur sehr schwach an Zyklin-Inhibitoren. 2. HPV E7: • Bindet und inaktiviert den G1 Zyklin-Inhibitor p21Cip1 Molekulare Virologie Ruth Brack-Werner; SS 2008 (III) Hemmung der Apoptose: Inaktivierung Transformation/Polyomavirus von p53 1. Entdeckung auf Grund seiner Bindung an SV40 LT-Antigen; 2. Sensor für Genom-Schäden/Veränderungen; 3. Am häufigsten mutiertes Gen in menschlichen Tumoren; 4. Protein ist in normalen Zellen sehr instabil (Bindung von Mdm-2 katalysiert die Ubiquitinylierung und fördert damit den Abbau von p53 durch Proteasomen); 5. Wird stabilisiert durch Bindung von anderen Proteinen (z.B. Atm) bei Doppelstrang-Brüchen bzw. bei der DNA-Reparatur 6. Transkriptionsfaktor; wirkt als Tetramer; Aktiviert die Expression von Genen die den Zellzyklus anhalten (z.B. den Zyklin-Inhibitor p21Cip1) oder die Apoptose induzieren; Molekulare Virologie Ruth Brack-Werner; SS 2008 (III) p53 Struktur Transformation/Polyomavirus DNA Principles of Virology, 2004. Flint SJ, Enquist LW, Racaniello VR,Skalka AM, 2nd edition. ASM Press. Fig. 18.19. Molekulare Virologie Ruth Brack-Werner; SS 2008 (III) Mechanismen zur Inaktivierung von Transformation/Polyomavirus p53 durchs virale Proteine Principles of Virology, 2004. Flint SJ, Enquist LW, Racaniello VR,Skalka AM, 2nd edition. ASM Press. Fig. 18.21. Molekulare Virologie Ruth Brack-Werner; SS 2008 (III) Mechanismen zur Inaktivierung von Transformation/Polyomavirus p53 durch virale Proteine 1. Beschleunigung des Abbaus von p53 (HPV E6, Adenovirus E1B + E4); 2. Sequestrierung in inaktive Komplexe (SV40 LT); 3. Veränderung der Funktion von p53 durch Interaktion mit viralem Protein (z.B. Bindung führt dazu, dass p53 die Transkription unterdrück, anstatt sie zu aktivieren). Molekulare Virologie Ruth Brack-Werner; SS 2008