Physikalische Chemie für das Lehramt
Werbung

Physikalische Chemie
für das Lehramt
Vorlesungsscript
Ernst-Peter Röth
Version 1.2
Inhaltsverzeichnis
Vorbesprechung
1. Mathematische Grundlagen
Differentiale
Integralrechnung
2. Der erste Hauptsatz der Wärmelehre
Der Joule-Thomson-Effekt
Die Temperaturabhängigkeit isobarer Prozesse
Carnot-Prozeß und Stirling-Motor
Aufgabenbeispiel
3. Der zweite Hauptsatz der Wärmelehre
Das totale Differential der Entropie
Druck- und Temperaturabhängigkeit der Freien Enthalpie
Adiabatische Entmagnetisierung
4. Mehrkomponenten-Systeme
Das chemische Potential
Die Clausius-Clapeyron-Gleichung
Osmose
Destillation
5. Thermochemie
Temperaturabhängigkeit der Gleichgewichtskonstanten / Prinzip von Le Chatelier
Die Richtung chemischer Reaktionen
Die Bestimmung des Aktivtätskoeffizienten
6. Gasgesetze
Stöße auf eine Ebene und mit Partikeln
Die Ableitung des Idealen Gasgesetzes
Viskositätskoeffizient und mittlere freie Weglänge
Knudsenströmung
Diffusion in Gasen
Kinetische Gastheorie und Maxwell-Boltzmann-Verteilung
7. Formalkinetik
Der monomolekulare Zerfall
Bimolekulare Reaktionen
Parallelreaktionen
Folgereaktionen
8. Eyring-Theorie
Grundlagen
Die Ableitung der Eyring-Formel
Der Lindemann-Hinshelwood-Mechanismus
9. Atom-Modelle
Die Schrödinger-Geichung
Der eindimensionale Potentialtopf
Die Energieniveaus der Rotation
Das Elektron im Coulombfeld
Der Tunneleffekt
10. Molekül-Spektren
Schwingungsspektren
Die Quantenzahlen
Näherungsmethoden für Molekül-Orbitale
LCAO-Methode
Elektronengas
Morse-Potential
Beispiele
Rotationsspektren
Normalschwingungen des NO2
Rotationsschwingungsspektrum von HI
11. Statistische Thermodynamik
Die Zustandssumme
Der Energieinhalt von Molekülen
Vorbesprechung
Plan der Lehrveranstaltung
Die Vorlesung im Hauptstudium „Physikalische Chemie für das Lehramt“ schließt sich an
die „Einführung in die Physikalische Chemie“ an, die im Grundstudium gelesen wird. Die
dort besprochenen Themen werden als bekannt vorausgesetzt und sollen jetzt durch
Beispiele vertieft werden.
Da wiederum im Laufe eines einzigen Semesters die gesamte Physikalische Chemie
behandelt werden muß, ist auch jetzt eine Beschränkung auf einen Überblick über die
wichtigsten Themen vorgegeben. Dabei muß auf die speziellen Anforderungen des
Lehramtes Rücksicht genommen werden. In der Schule wird die Physikalische Chemie
nur im geringen Maße im Rahmen des Chemie-Unterrichts gelehrt. Da sie jedoch das
Grundgerüst der Theorie der Chemie bildet, ist für den Lehrer ein Verständnis der
grundlegenden Gleichungen und der Denkweise der Physikalischen Chemie unabdingbar.
Daher soll das Ziel dieser Vorlesung die Vertiefung des Verständnisses für die wichtigsten
Grundbegriffe der Physikalischen Chemie sein.
In Anlehnung an die Stoffeinteilung der „Einführung“ habe ich für die 2-stündige
Vorlesung folgende, mir wichtig erscheinende Punkte herausgegriffen :
Einleitung :
1. Mathematische Grundlagen
Thermodynamik :
2. Der 1. Hauptsatz der Wärmelehre
3. Der 2. Hauptsatz der Wärmelehre
4. Mehrkomponenten-Systeme
5. Thermochemie
Kinetik :
6. Gasgesetze
7. Formalkinetik
8. Die Eyring Theorie
Aufbau der Materie :
9. Atom-Modelle
10. Molekül-Spektren
11. Statistische Thermodynamik
Während in der Vorlesung des Grundstudiums im Abschnitt über die mathematischen
Grundlagen besonders der Begriff des Differentials heraus gearbeitet wurde, soll jetzt der
Schwerpunkt auf die Lösung von Differentialgleichungen gelegt werden. Thermodynamik
und Kinetik sind statistische Theorien, d.h. ihre Gesetze und Regeln gelten für große
Teilchenzahlen (1 Mol = 6∗1023 Teilchen). Diese Theorien beschreiben also das makroskopische (oder molare) Erscheinungsbild der Materie. In der Kinetik wird bei der Ableitung der Gesetze jedoch bereits auf das mikroskopische oder molekulare Bild zurückgegriffen. Die Beschreibung des Aufbaus der Materie bezieht sich dann ausschließlich auf
das einzelne Teilchen. Und schließlich führt die Statistische Thermodynamik dann dieses
Teilchenbild unter Beachtung der statistischen Abbildungsgesetze wieder auf die
makroskopischen Formeln zurück.
Die Physikalische Chemie ist eine relativ abstrakte Wissenschaft. Es werden allgemeine
Gesetze abgeleitet, die für ganze Klassen von Stoffen und Stoffumsätzen gelten. Dabei
werden Begriffe definiert, die entweder in der Umgangssprache nicht vorkommen, wie z.B.
die Entropie, oder aber dort unspezifische Bedeutungen haben (Kraft, Wärme, etc). In der
Vorlesung sollen diese Begriffe erarbeitet werden. Da wir uns in der Vorlesung auf die
Vermittlung der Gedankengänge und der Definitionen der Physikalische Chemie beschränken müssen, soll der Stoff in Themenkreisen abgehandelt werden. Zu Beginn jedes
Themas werden die grundlegenden Formeln, die in der „Einführung“ behandelt wurden, in
knapper Form rekapuliert. Die Studierenden sind gehalten, sich anhand von Lehrbüchern
in den Themenkreis einzulesen, um in der Diskussion mitreden zu können. In der
Diskussion sollen insbesondere auch Fragen zur Didaktik, d.h. zur Vermittlung des
Stoffes, angesprochen werden.
Zu der Vorlesung gehört eigentlich ein einstündiges Seminar mit Übungen. Nach der
Behandlung der Theorie wird darin jeweils besprochen, welche Aufgaben aus dem Gebiet
gestellt werden können, welche neuen Begriffe eingeführt wurden und wo der Praxisbezug
des Stoffes liegt. Da es im Lehrplan für die Studiengänge der Sekundarstufe II nicht
vorgesehen ist, wird dieses Seminar zur Zeit nicht durchgeführt. Zum Erhalt eines
Leistungsscheins werden Übungen wahlfrei angeboten. Alle Studierenden müssen für
den Leistungsschein mindestens eine Aufgabe an der Tafel vorrechnen. Dabei wird
besonderer Wert darauf gelegt, daß dieses Vorrechnen unter didaktischen
Gesichtspunkten erfolgt. Das bedeutet, daß die verwendeten Formeln erklärt und die
Ergebnisse anhand von allgemein verständlichen Beispielen diskutiert werden sollen.
Das zugehörige Praktikum ist zweigeteilt. Im ersten Teil soll in einem „Experimentierkurs“ an einigen Beispielen die praktische Vorgehensweise der Physikalischen Chemie
eingeübt werden. Hierbei wird besonders Wert auf die physikalischen Grundlagen der
Meßtechnik gelegt. Im zweiten Teil soll das Gelernte in Schulversuche umgesetzt werden,
und zwar in 4 Demonstrationen, wie sie innerhalb einer Schulstunde vorgeführt werden,
und in 4 Versuche, die in einem Schülerpraktikum durchgeführt werden können. Die
Teilnahme an dem Praktikum und an dem zugehörigen Seminar ist Pflicht.
Literatur zu einer Vorlesung "Physikalische Chemie für das Lehramt" kann nicht angegeben werden. Insbesondere nicht zu dieser Lehrveranstaltung, da es eines meiner Ziele
ist, Ihr Interesse für das Fachgebiet zu wecken und Sie zu befähigen und ermuntern, auch
die Lehrbücher, egal ob für Schule oder Hochschule gedacht, kritisch zu lesen. Bei der
Vorbereitung der Lehrveranstaltung habe ich im wesentlichen folgende Bücher benutzt :
P.W. Atkins
P.W. Atkins
G. M. Barrow
P. W. Atkins
G. Wedler
B. Harder
K. J. Laidler
„Kurzlehrbuch Physikalische Chemie“
„Einführung in die Physikalische Chemie“
"Physikalische Chemie I, II, III"
"Physikalische Chemie"
„Lehrbuch der Physikalischen Chemie“
"Einführung in die Physikalische Chemie"
"Reaktionskinetik I"
Dies ist nur ein kleiner Auszug aus der Vielzahl von Lehrbüchern der Physikalischen
Chemie. Im Grunde ist es gleichgültig, welches Buch Sie benutzen, da alle die Grundlagen, wie wir sie besprechen werden, erläutern.
Als Formelsammlung für die wenigen mathematischen Ableitungen schlage ich vor :
K. Rottmann
"Mathematische Formelsammlung"
oder irgend eine andere Formelsammlung der Mathematik, die Integraltafeln enthält.
Mathematische Grundlagen
Die Mathematik zur Thermodynamik besteht fast ausschließlich aus der Umwandlung von
einer Energieform in die andere. Allerdings sind diese Umwandlungen meist nicht mit den
integralen Größen, sondern mit infinitesimal kleinen Werten durchzuführen, da die Gesetze der Thermodynamik nur für infinitesimale Bereiche exakt gelten. Daher werden die
Regeln des Rechnens mit Differentialen benötigt.
Differentiale
Funktionen, die mehr als zwei Variable enthalten, wie z. B. die Allgemeine Gasgleichung
p⋅V = n⋅R ⋅ T
die vier Variable (p, V, n und T) enthält, können nicht abgeleitet werden, da der Operator
der Ableitung
d
y
dx
sich per definitionem immer nur auf eine abhängige und eine unabhängige Größe bezieht.
Faßt man die Ableitung gemäß ihrer Definition jedoch als Quotient zweier Differentiale
auf,
∆y dy
d
=
y = lim
∆x →0 ∆x
dx
dx
mit dy=lim (∆y) und dx=lim (∆x)
so kann der Begriff des Differentials ohne Schwierigkeiten auf alle Variablen einer mehrdimensionalen Funktion angewendet werden. Gegeben sei eine Funktion z, die von zwei
Veränderlichen x und y abhängig ist,
z= f ( x, y )
und deren Differential dz durch die Differentiale dx und dy und die Ableitungen von z nach
x und nach y ausgedrückt werden soll. Hierbei ist zu beachten, daß, da eine Ableitung nur
in einer Ebene definiert ist, diese Ebene angegeben werden muß, man führt also eine
partielle Differentiation ein :
d
y
→
dx z =const .
∂ y
∂ x z
Wie bei der Einführung der Differentiation geht man auch bei der Einführung der
Differentiale von Differenzen aus, die dann gegen Null gehen :
dz = lim ∆z
∆z →0
Es gilt dann für dz :
∂ z
∂z
⋅dx +
⋅dy
dz =
∂
∂
x
y
y
x
Die Definition des Differentials ist beliebig auf mehrdimensionale Funktionen erweiterbar :
Für f (xi , i = 1 , ... , n) gilt :
df =
n
∑
i =1
∂ f
⋅ dx i
∂ xi x j ≠i
Rechenregeln
∂ x ∂ y ∂ z dx t ⋅dy t⋅ ⋅dz t
=
=1
∂
y
∂
z
∂
x
t
t
t dy t ⋅dz t ⋅dx t
∂ x
∂ y z
∂ y
∂ z x
∂ z
= −1
∂ x y
Schwarz'scher Satz (Euler's reciprocity theorem)
Bei der Ableitung der Gleichung für das Differential war davon ausgegangen worden, daß
es gleichgültig ist, auf welchem Weg differenziert wird, da P und Q eindeutig bestimmte
Punkte auf der Hyperfläche z = f(x,y) sind. In einem solchen Fall wird dz ein vollständiges
oder totales Differential genannt. P und Q sind dann eindeutig bestimmte Zustände des
betrachteten Systems und f(x,y) wird als Zustandsfunktion bezeichnet.
Aber nicht alle Größen der Thermodynamik sind wegunabhängig. In manchen Fällen
kommt es auf die Prozeßführung an. Zwar sind die Energien, mit denen wir es zu tun
haben werden, immer Zustandsfunktionen, aber die (dimensiosgleiche) Arbeit, die am
System verrichtet wird, ist wegabhängig.
Mit Hilfe des Schwarz'schen Satzes, der hier unbewiesen bleiben muß, kann man herausfinden, ob eine Funktion einen Zustand beschreibt oder ob die Größe wegabhängig ist.
Nur für Zustandsfunktionen darf die Differentiation vertauscht werden :
∂ ∂ ∂ ∂
≡
∂ x ∂ y ∂ y ∂ x
x y
y x
Obwohl hier der exakte mathematische Beweis des Schwarz'schen Satzes nicht vorgeführt werden kann, so ist doch der Sinn verständlich. Die Wegunabhängigkeit muß auch
für mathematische "Wege" gelten. Zweite Ableitungen sind Krümmungen der Hyperfläche.
Der Schwarz'sche Satz beschreibt die Krümmung des Weges von P nach Q. Für eine
Zustandsfunktion Z(x,y) ist für jedes Koordinatenpaar x und y der Wert Z eindeutig
beschrieben. Erst wenn diese Eindeutigkeit dadurch aufgegeben wird, daß ein bestimmter
Weg, d.h. eine genaue Reihenfolge, wie x und y durchlaufen wird, vorgegeben ist, wird
auch die Krümmung vom Weg abhängen und damit die obige Gleichung nicht mehr richtig
sein.
Differentialgleichungen
Eine Gleichung, in der Differentiale vorkommen, wird Differentialgleichung genannt. Meist
können physikalische Gesetze relativ leicht zwischen infinitesimalen Größen definiert
werden, beobachtbar sind jedoch nur die integralen Größen. D.h. wenn ein Vergleich
zwischen Theorie und Experiment angestellt werden soll, muß die Differentialgleichung
integriert werden. Hier soll nur der Fall einer einfachen Eulerschen Differentialgleichung
behandelt werden.
Bevor jedoch auf die Lösung von Differentialgleichungen eingegangen wird, soll ein
Exkurs in die Integralrechnung durchgeführt werden. Die Integration ist die Umkehrung
der Differentiation, es wird also eine Funktion gesucht, zu der eine gegebene Ableitung
paßt. Dies kommt im Normalfall auf ein Erraten der richtigen Funktion hinaus, wobei eine
Formelsammlung von Integralen äußerst hilfreich ist. Durch Zusammenfassen von Ausdrücken und Substitution der entsprechenden Variablen und Parameter können die
meisten Integrale, mit denen wir in der Physikalischen Chemie konfrontiert werden, auf
einen Ausdruck gebracht werden, dessen Lösung in einer Integralsammlung aufgeführt
ist.
Beispiel : Die Boltzmannfunktion
n
2
f (u ) = A⋅a e −au u n −1
2
n
läßt sich integrieren, wenn die Konstante A⋅a 2 aus dem Integral herausgenommen wird
und für n ganze Zahlen eingesetzt werden . Mit x=u folgt dann mit Hilfe der Integraltafel :
+∞
∫e
− ax 2
π
dx =
+∞
∫ xe
− ax 2
dx =
0
+∞
∫x
2
1
2a
e −ax dx =
2
−∞
n=1
a
−∞
1 π
2a a
n=2
n=3
Ein weiteres Beispiel soll die Substitution von Funktionen, die Teil des Integranden sind,
durch Variable zeigen :
α
α
∫ e (A+e )dz
−2 z
−2 z
geht über in
1 2
x2
− ∫ x A + x dx = −
A + x +Const
α
2α
2
wenn man ersetzt
e − az = x
1
(
2
)
Da bei der Differentiation konstante Glieder wegfallen, muß bei der Integration eine Konstante addiert werden. Damit wird jede Integralfunktion zuerst einmal unbestimmt. Um die
Konstante bestimmen zu können, müssen weitere Annahmen, die Randbedingungen,
gemacht werden. Dies bedeutet, daß mindestens ein Punkt (meistens am Rand des
Integrationsgebietes) bekannt sein muß. Wir werden bei der Integration der Eulerschen
Gleichung darauf zurückkommen.
In der Thermodynamik kommt manchmal ein Kreisintegral vor. Dies bedeutet, daß so
integriert wird, daß man zum Ausgangspunkt zurückkehrt. Für Zustandsfunktionen ist
damit ein Kreisintegral also immer gleich Null. Für wegabhängige Funktionen kann ein
Kreisintegral berechnet werden, wenn man es in einen Hinweg und einen Rückweg
aufteilt :
B
A
B
B
∫ f dx = ∫ f dx + ∫ f dx = ∫ f dx − ∫ f dx
A
1
B
2
A
1
A
2
Als Beispiel für ein physikalisches Gesetz in Form einer Differentialgleichung soll jetzt das
Lambert-Beer'sche Gesetz der Lichtabsorption integriert werden. Die Abschwächung des
Lichtes ist proportional zur Lichtintensität I, zur Konzentration C des Absorbens und zur
Weglänge ds. Der Proportionalitätsfaktor sei σ :
dI = − σ ⋅ C ⋅ I ⋅ ds
Das Ergebnis dieser Differentialgleichung ist per definitionem eine e-Funktion :
I = I 0 ⋅ exp(− σ C s )
Es soll jetzt eine der häufigsten Differentialgleichungen der Kinetik besprochen werden :
Die Änderung einer Konzentration C mit der Zeit sei gleich einer Produktionsrate P und
einer Destruktion DC, die proportional der Konzentration ist :
dC
=P − D ⋅ C
dt
Diese inhomogene Differentialgleichung wird gelöst, indem man zuerst die homogene
löst :
dC
=− D ⋅ C
dt
C =C0 ⋅ e − D⋅t
Durch eine Variation der Konstanten, d. h. man nimmt jetzt an, daß die Integrationskonstante C0 ebenfalls von t abhängt und Vergleich mit der Ausgangsgleichung, kann die
inhomogene Gleichung gelöst werden .
Den Sinn dieser Variation der Konstanten kann man leicht begreifen, wenn man sich
vergegenwärtigt, daß während der Abreaktion der Substanz diese gleichzeitig auch
aufgebaut wird. D.h. das C0 wird sich mit der Zeit ändern.
dC − Dt dC
=e ⋅
− D ⋅ e − Dt ⋅ C0 = P − D ⋅ C
dt
dt
also
dC0
= P ⋅ e + Dt
dt
Diese Differentialgleichung wird durch Separation der Variablen gelöst :
∫ dC =∫ P ⋅ e
0
Dt
dt
P
C0 +const.= e Dt
D
Einsetzen :
P
C = e Dt − const. e − Dt
D
Wie bereits gesagt, sind die Lösungen von Differentialgleichungen immer unbestimmt, da
durch die Integration eine Konstante hereinkommt, die durch zusätzliche Bedingungen,
die Randwerte bestimmt werden muß.
Wir wollen zuerst annehmen, daß die Konzentration zum Zeitpunkt t0 = 0 verschwindet.
Damit ergibt sich :
P
C (t0 = 0)= 0 = e 0 −const. e 0
D
oder
const.=
P
D
Die Lösung unserer Differentialgleichung unter Einbeziehung der Randbedingung lautet
also :
C=
Für sehr lange Zeiten
P P − Dt P
− e = (1 − e − Dt )
D D
D
(t → ∞ ) ergibt sich daraus
C∞ =
P
D
Für diese Bedingung gilt dann
Hinreaktion = Rückreaktion
und
dC
=0
dt
d.h. das System befindet sich in einem Gleichgewicht, die Konzentration ist konstant.
Wir gehen jetzt noch einmal zu der allgemeinen Lösung der Euler' schen Differentialgleichung zurück :
Ct =
P
−Const⋅e − Dt
D
und nehmen an, daß zum Zeitpunkt t bereits eine endliche Konzentration Ct vorliegt. Die
Konzentration zum Zeitpunkt t + ∆t ist dann
C (t + ∆t )=
P
−Const⋅e − D (t + ∆t )
D
Die Konstante wird aus der Ausgangsgleichung ausgerechnet und eingesetzt :
also
P
− C (t )− e + Dt e − D (t +∆t )
D
C (t + ∆t ) =
P
D
C (t + ∆t ) =
P
P
− C (t )− e − D∆t
D
D
Mit dieser Lösung der Differentialgleichung lassen sich jetzt auch Systeme lösen, bei
denen P und D selbst von der Zeit abhängen. Man hat dann nur einen so kleinen Zeitraum ∆t zu wählen, daß in diesem P und D als nahezu konstant behandelt werden können.
Zum Abschluß soll noch auf eine Differentialgleichung eingegangen werden, die im Abschnitt "Aufbau der Materie" benötigt wird :
d2 y
=− a 2 y
2
dx
Die Lösung dieser Gleichung ist eine der beiden Funktionen
y = A ⋅sin(ax)
oder
y = B ⋅cos(ax)
Laut einem Lehrsatz der Mathematik ist die allgemeine Lösung eine Differentialgleichung
gleich der Linear-Kombination der speziellen Lösungen, also :
y = A ⋅sin(ax) + B ⋅cos(ax)
Beweis :
dy
dx
d2 y
d x2
= Aa cos(ax) − a B sin(ax)
= Aa 2 sin(ax ) − a 2 Bcos( ax )
= a 2 ( A sin(ax ) + Bcos( ax ) )= − a 2 y
qed.
Der erste Hauptsatz der Wärmelehre
Der erste Hauptsatz der Thermodynamik beschäftigt sich mit der Frage : Ist es möglich,
Energie zu erzeugen ?
Will man einem geschlossenen System von außen Energie zuführen, so geht dies nur
über Wärmezufuhr dq und/oder Volumenarbeit dw=-pdV. Die Energie des Zustands
ändert sich dann um den Betrag dU, der als Innere Energie bezeichnet wird :
dU = dq + dw = dq − p⋅dV
Fragt man nach der Gesamtenergie eines Systems, so muß man zur inneren Energie
noch die potentielle Energie pV hinzurechnen und kommt so zur Definition der Enthalpie
H = U + p⋅V
Die Definition der Enthalpie ist die mathematische Formulierung des 1. Hauptsatzes der
Thermodynamik. Er besagt, daß Energie weder gewonnen noch zerstört, aber in andere
Formen umgewandelt werden kann.
Um die Wärmezufuhr eines Systems zu messen, bedient man sich der Temperaturmessung, wobei eine Proportionalitätskonstante, die molare Wärmekapazität C auftritt :
∆q = C⋅
m
∆T
M
M = Molmasse, m = Einwaage
Da die Wärmeänderung wegabhängig ist, ist auch die Wärmekapazität
C =
1 ∂q
⋅
n ∂ T
n = Molzahl
wegabhängig.
Für adiabatische Prozesse gilt, wie in der Grundvorlesung gezeigt wurde,
p ⋅ V κ = const
mit
κ =
Cp
CV
Der Joule-Thomson-Effekt
Normalerweise werden chemische Vorgänge entweder bei Raumtemperatur oder unter
Erwärmung beobachtet. Es ist relativ einfach aus einem System Wärme abzuführen,
wenn die Systemtemperatur über der Umgebungstemperatur liegt. Will man unterhalb der
Umgebungstemperatur arbeiten, so trifft man auf die gleiche Schwierigkeit, die man hat,
wenn z.B. der Wasserspiegel eines Brunnens gesenkt werden soll : Man braucht eine
Pumpe. Für die Energie hat die Natur im Joule-Thomson-Effekt eine solche Pumpe zur
Verfügung gestellt.
Ein Gas, das im Raum V1unter dem Druck p1 steht, wird durch eine Drossel hindurch in
einen Raum V2 mit Druck p2 gedrückt. Der Vorgang soll adiabatisch, d.h. ohne Wärmezufuhr durchgeführt werden. Für die Volumenarbeit gilt dann :
∆w = − ∫ pdV = − p ∫ dV = − p⋅∆V
p = p1,p2 soll hierbei konstant sein.
Das Ausgangsvolumen wird von V1 auf 0 reduziert, also gilt für die Arbeit am System :
∆w1 = − p1 (0−V1 ) = + p1⋅V1
Entsprechend gilt in der anderen Kammer :
∆w2 = − p2 (V2 −0 ) = − p2 ⋅V2
Für die Innere Energie gilt also, da dq=0 ist :
∆w ges = ∆w2 + ∆w1
∆U = U 2 − U 1 = ∆q + ∆w = 0 − p2V2 + p1 ⋅V1
oder
U 1 + p1⋅V1 = U 2 + p2V2
Dies ist gleichbedeutend mit der Aussage, daß der Vorgang isenthalpisch ist :
dH ≡ 0
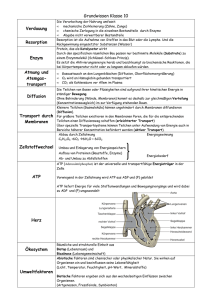
Abbildung 1 : Inversionstemperaturen für N2, H2 und Helium
Im folgenden wird jetzt die Temperaturänderung bei diesem isenthalpischen Vorgang
betrachtet : Für ideale Gase ist der Joule-Thomson Prozeß isotherm, d.h. die
Temperaturen auf beiden Seiten der Drossel sind gleich. Für reale Gase ergibt sich
dagegen ein Temperaturunterschied, der durch den Joule-Thomson-Koeffizienten µ
ausgedrückt wird :
∂T
∂p H
µ JT =
Den Zusammenhang zwischen µJT und anderen Kenngrößen der Thermodynamik erhält
man mit folgenden Überlegungen :
∂T ∂p
p
∂
H ∂H T
Mit
und
∂H
= −1
∂T p
∂H
= Cp
∂T p
∂H
∂V
= V − T
∂T p
∂p T
α=
folgt
µ JT = −
1 ∂V
V ∂T p
V − T ⋅ dV
V
(αT − 1)
=
Cp
Cp
Das Vorzeichen von µJT ist dabei abhängig von den jeweiligen Versuchsbedingungen.
Abbildung 1 zeigt Linien für µJ-T = 0 in Abhängigkeit von Druck und Temperatur für die
Gase N2, H2 und He. Bei Raumtemperatur ist µJT für Helium immer größer als Null, d.h.
Helium erwärmt sich bei isenthalpischer Expansion. Stickstoff dagegen kühlt sich ab,
solange der Arbeitsdruck kleiner als 400 bar ist. Diese Tatsache wird in der LindeKältemaschine zum Herstellen von flüssigem Stickstoff angewendet, die in der Abbildung
2 gezeigt wird. :
Abbildung 2 : Schema einer Luftverflüssigungsanlage
Ein Kompressor verdichtet das Gas. Dabei erwärmt es sich. In einem ersten
Wärmetauscher wird die Überschußwärme an die Umgebung (Zimmertemperatur)
abgegeben. Bei der Expansion durch eine Drossel kühlt sich das Gas dann weiter ab. Das
zurückströmende Gas wird benutzt, um im 2. Wärmetauscher das zuströmende Gas unter
Zimmertemperatur abzukühlen. Der Vorgang wird solange wiederholt, bis das Gas sich
verflüssigt und in einen Auffangbehälter gesammelt werden kann.
Die Temperaturabhängigkeit isochorer Vorgänge
Der Joule-Thomson-Koeffizient erlaubt es jetzt, die Temperaturabhängigkeit der Enthalpie
bei konstantem Volumen auf meßbare Größen zurückzuführen. Bei konstantem Druck
gilt :
∂H
= Cp
T
∂
p
Aus
oder
H = H 0 + ∫ C p dT
∂H
∂H
dH =
dp
dT +
∂T p
∂p T
: dT
V
folgt für konstantes Volumen :
∂H ∂p
∂H
= C p +
∂
p
∂ T V
T ∂T V
Setzt man jetzt die isotherme Kompressibilität κ und den thermischen Ausdehnungskoeffizient α ein,
α =
1
V
κ =−
∂V
∂ T p
1
V
∂V
∂ p T
so folgt mit
∂H
= − C p ⋅ µ JT
∂
p
T
sofort
α
∂H
= C p 1 − µ JT
κ
∂T V
Damit ist die isochore Temperaturabhängigkeit der Enthalpie realer Gase auf die meßbaren Größen Cp, µ JT , α und κ zurückgeführt.
Carnot-Prozeß und Stirling-Motor
1824 führte Carnot einen Kreisprozeß ein, der auf Isothermen und Adiabaten verläuft.
Dieser Prozeß hat den höchsten Wirkungsgrad für die Überführung von Wärme in
mechanische Arbeit. Der Carnot-Prozeß wurde bereits in der Vorlesung des Grundstudiums eingeführt, jetzt sollen die Änderungen der mechanischen Arbeit und der Wärme
berechnet werden.
In vier reversiblen Schritten wird ein ideales Gas zu seinem Ausgangszustand zurückgeführt :
1.
isotherme Expansion von A nach B
2. adiabatische Expansion von B nach C
3. isotherme Kompression von D nach A
4. adiabatische Kompression von D nach A
Das zugehörige Diagramm zeigt die Abbildung 3.
Abbildung 3 : p-V Diagramm des Carnot Prozesses
Im ersten Schritt bei Temperatur To leistet das Gas die Arbeit
B
+ w1 =
B
nRT0
V
dV = n RTo ln B
V
VA
A
∫ pdV = ∫
A
Diese Arbeit muß durch Wärmeaufnahme aus der Umgebung ausgeglichen werden :
− w1 = Q1
Entsprechend wird im Schritt 3 die Wärme Q2 an ein Wärmereservoir der Temperatur Tu
abgegeben :
− w3 = − n RTu ln
VD
= + Q3
VC
In den beiden adiabatischen Schritten wird keine Wärme aufgenommen oder abgegeben,
die entsprechenden Volumenarbeiten sind dabei gegeben durch
C
w2 = ∫ n CV dT = n CV (Tu −To )
B
und
w4 = n CV (To −Tu )
Für die Volumenverhältnisse gilt, da VB und VC sowie VA und VD jeweils auf Adiabaten
liegen.
1
VB Tu κ −1 V A
=
=
VC
VD
To
oder
VB VC
=
V A VD
Beim Durchlaufen des Carnot-Prozesses gewinnt man also die Arbeit :
− wges = w1 + w2 + w3 + w4 =
VB
+ n CV (Tu −To ) −
VA
V
− n RTu ln C + n CV (To −Tu ) =
VD
n RTo ln
= n R (To −Tu ) ln
also
VB
= Q1 − Q3
VC
wges = Q1 − Q3
Der Carnot-Prozeß bietet also eine Möglichkeit, bei Entnahme von Wärme aus einem
Reservoir mit höheren Temperaturniveau und Abgabe auf ein niedrigeres Niveau Arbeit
zu gewinnen (Wärmekraftmaschine).
Umgekehrt läßt sich beim Durchlaufen des Carnot-Prozesses in entgegengesetzter
Richtung durch Arbeitseinsatz eine Wärmepumpe (z.B. für Nutzung der Wärme des
oberen Niveaus zu Heizzwecken) oder eine Kältemaschine (zum Abkühlen des Reservoirs
des unteren Niveaus) modellhaft konstruieren.
wges = − Q1 + Q3
1850 schlug Stirling einen Heißluftmotor vor, der auf Isothermen und Isochoren arbeitet. In
Abbildung 4 ist das entsprechende Diagramm aufgeführt.
Abbildung 4 : Vergleich des Stirling-Prozesses mit dem Carnot-Prozess
Nach dem zweiten Hauptsatz der Wärmelehre ist der Wirkungsgrad des Stirling-Motors
etwas kleiner als der Carnot-Prozesses. Der Unterschied ist jedoch gering, da sie
Adiabaten sehr viel steiler sind als die Isothermen. Konstruktiv ist ein Stirling-Motor
einfacher als ein Carnot-Motor herzustellen.
Aufgabenbeispiel
Ein Mensch von 70 kg produziert im Grundumsatz etwa 6 300 kJ Wärme pro Tag. Um wie
viel Grad würde seine Temperatur pro Tag steigen, wenn er als isoliertes System
-1 -1
betrachtet wird ? Die Wärmekapazität beträgt 4.2 JK g .
∆q = m ⋅ C ⋅ ∆T
∆T =
6.3 ×106 J / d K g
= 21 K / d
7 × 10 4 g ⋅ 4.2 J
Die Temperatur steigt also pro Tag um 21 K, spätsten am vierten Tag würde der Mensch
kochen. In der Realität ist der Mensch aber ein offenes System, das u.a. die produzierte
Wärme über die Verdunstung von Wasser abgibt. Die pro Tag verdunstete Menge an
Wasser lässt sich über die Verdunstungsenthalpie von Wasser (43.4 kJ/mol bei 37°C)
abschätzen.
Bei isobaren Vorgängen gilt :
∆q = n ⋅ ∆H Verdunst
also
6.3 × 10 6 J / d
n=
= 145 mol
4.34 ×10 4 J / mol
Dies entspricht einer Wassermenge von 2.6 l. In der Physiologie wird mit folgenden
Zahlen für die Verdunstung gerechnet:
0.375 l/d über die Haut
0.375 l/d über den Atem
0.100 l/d über den Schweiß
Der Rest der Energie wird zur Aufrechterhaltung der Lebensfunktionen benötigt.
Der zweite Hauptsatz der Wärmelehre
Die zentrale Größe der Thermodynamik ist die Wärme. Aber die Wärme hat den großen
Nachteil, daß sie wegabhängig ist, sie ist keine Zustandsgröße. Mit dem Verfahren des
integrierenden Nenners kann man aus einem nicht totalen Differential ein totales macht,
oder in die Thermodynamik übersetzt : aus einer wegabhängigen Größe eine Zustandsfunktion machen. Für die auf reversiblen Wegen ausgetauschte Wärme ist der "integrierende Nenner" die Temperatur, so daß sich als Definition der neuen Größe S, die
Entropie genannt wird, ergibt :
dS =
dqrev
T
Durch diese Definition bedingt ergibt sich, daß die Entropie S keine physikalische Größe
ist, d.h. keine Größe, die einen Vorgang oder ein Verhalten beschreibt. Die Entropie ist
vielmehr ein Maß für die Wärme, aber auch, wie anderswo gezeigt wird, ein Maß für den
Ordnungszustand eines Systems.
Eine Maschine, die auf reversiblen Wegen arbeitet und die maximal mögliche Arbeit
leistet, ist die Carnot- Maschine, die auf Adiabaten und Isothermen arbeitet. Die geleistete
Arbeit pro zugeführter Wärme, d.h. den Wirkungsgrad η , erhält man, wenn man in einem
Druck-Volumen-Diagramm die vom Kreisprozeß umschlossene Fläche bestimmt :
η=
∑ (−w) =
n R (To − Tu ) ln
q1
q1
VA
VB
=
To − Tu
To
wo To die Temperatur des Reservoirs, aus dem Wärme abgeführt wird, und Tu die
niedrigere Temperatur des zweiten Reservoirs ist.
Da die geleistete Arbeit gleich der Differenz zwischen zugeführter und abgeführter Wärme
ist, gilt auch
η =
und damit
q1 − (− q3 )
q1
q1
q
+ 3 =0
To
Tu
oder
dq
∫ T rev. = ∫ dS
ist eine Zustandsgröße.
Die nutzbare Energie einer Wärme-Kraft-Maschine ist die Differenz zwischen der hineingesteckten Wärme dq und der maximal entnehmbaren Energie der Größe dqrev. :
dG = dq - dqrev.= dH - TdS
dA=
dU - TdS
für isobare Vorgänge
für isochore Vorgänge
Diese nutzbare Energie ist als Differenz zweier Zustandsgrößen wiederum eine Zustandsgröße und wird als "Freie Enthalpie" ∆G für isobare Vorgänge, bzw. als "Freie Energie
oder Helmholtz-Energie" ∆A für isochore Vorgänge bezeichnet. Der Zweite Hauptsatz der
Wärmelehre kann also in Form der Gibbs-Helmholtz-Gleichungen definiert werden.
Das totale Differential der Entropie
Es soll jetzt die Temperatur- und die Druckabhängigkeit der Entropie abgeleitet werden.
Dazu wird mit dem totalen Differential der Entropie begonnen :
∂ S
∂ S
dV +
dT
dS =
∂
∂
V
T
T
V
Aus den Definitionen von Innerer Energie und Entropie folgt :
dU = dq − pdV
dS =
dq
T
also
dS =
dU
pdV
+
T
T
wobei für dU gilt :
∂U
∂U
dU =
dV +
dT
∂V T
∂T V
mit
∂U
= CV
∂T V
Für dS ergibt sich damit :
1
dS =
T
∂U
C
+ p dV + V dT
T
∂V T
Aus dem Koeffizientenvergleich mit der Ausgangsformel folgt :
C
∂S
= V
T
∂T V
oder
dSV =
CV
dT
T
Diese Gleichung folgt allerdings auch sofort aus der Definition der Entropie :
dS =
dq
T
C
∂S
∂q 1
= ⋅ = V
T
∂T V ∂T V T
Aus dem Vergleich des zweiten Koeffizienten folgt :
1 ∂U
∂S
=
+ p
T ∂V T
∂V T
oder
∂U
∂S
=T
− p
∂V T
∂V T
Aus dem Schwarz'schen Satz für die Innere Energie U folgt dann :
∂ ∂U
∂ ∂U
=
∂
T
∂
V
∂
V
∂
T
V T
T V
∂ 2S
T
∂T ∂ V
∂ ∂S
∂S
∂ 2S
∂p
+
T
T
−
=
=
∂V ∂T
∂
V
∂
T
∂
V
∂
T
T
V
V T
wegen
∂U
∂S
= CV = T
∂T V
∂T V
Also
∂S
∂p
=
∂V T ∂T V
Damit gilt für das totale Differential der Entropie :
dS =
und analog
dS =
CV
∂p
dT +
dV
T
∂T V
∂V
dT +
dp
T
∂T p
Cp
Druck- und Temperaturabhängigkeit der Freien Enthalpie
Aus den Definitionen der Freien Enthalpie und der Enthalpie folgt :
G = H - TS
H = U + pV
Daraus folgt
dG = dU + p dV + V dp - T dS - S dT
Es galt aber
T dS = dq = dU + p dV,
also
dG = V dp - S dT
Aus den Koeffizientenvergleich mit
∂G
∂G
dG =
dp +
dT
∂T p
∂p T
folgt
∂G
= V
∂
p
T
und
∂G
= −S
∂T p
Die letztere Formel gibt eine Möglichkeit zum Messen der Entropie aus der Steigung der
Temperaturabhängigkeit der Freien Enthalpie bei konstantem Druck.
Für die Druckabhängigkeit der Freien Enthalpie bei konstanter Temperatur folgt mit :
dG = V dp
Für ideale Gase ergibt sich damit
2
∆Gideal = n RT
dp
p2
n
R
T
=
ln
∫1 p
p1
Für reale Gase kann man über diese Gleichung den Fugazitätskoeffizienten γ definieren :
∆Greal = n RT ln
f2
f1
Die Fugazität f = γ ⋅ p ist ein korrigierter Druck und erlaubt das Arbeiten bei realen
Verhältnissen mit den gleichen Formeln, wie die der idealen Gase.
An dieser Stelle soll darauf hingewiesen werden, daß die Argumente einer Funktion
immer reine Zahlen sein müssen. Eine Aufspaltung
ln
p2
= ln p2 − ln p1
p1
ist also mathematisch sinnlos, da man den Logarithmus von [atm] nicht bilden kann. Es
muß richtiger heißen
ln
p2
p
p
= ln 2 − ln 1
p1
p0
p0
(In manchen Lehrbüchern wird p0 = 1 atm gesetzt und dann die 1 weggelassen. Aus
dieser Schlamperei folgen dann manche Ungereimtheiten, die oft als "Regeln" verkauft
werden.)
Für die Temperaturabhängigkeit folgt analog bei konstantem Druck :
2
∆G p = − ∫ S dT
1
Da S selbst von der Temperatur abhängt, folgt für die Temperaturabhängigkeit der freien
Enthalpie :
2
∆G p = − ∫
1
2 Cp
dT dT
∫
1 T
Adiabatische Entmagnetisierung
Bisher hatten wir nur Volumenarbeit als Möglichkeit kennengelernt, an einem System
Arbeit zu verrichten. Man kann jedoch auch dem System Energie zuführen über
elektrische oder magnetische Arbeiten. Für letztere gilt :
dw = + H dM
wobei H jetzt das Magnetfeld und M die molare Magnetisierung ist. Die adiabatische
Entmagnetisierung wird z.B. angewendet, wenn ein System weiter abgekühlt werden soll,
als es mit dem Joule-Thomson-Effekt möglich ist. In Abbildung 5 ist dies schematisch
dargestellt.
Aus
folgt dann
dU = T dS + H dM
dS =
1
H
dU −
dM
T
T
(1. Hauptsatz)
Abbildung 5 : Zur adiabatischen Entmagnetisierung
und durch Vergleich mit
∂S
∂S
dS = dT +
dM
∂T M
∂M T
nach Einsetzen von
∂U
∂U
dU =
dT +
dM
∂T M
∂M T
ergibt sich
1 ∂U
∂S
=
∂T M T ∂T M
1 ∂U
∂S
=
− H
∂M T T ∂M T
sowie
Aus dem Schwarz'schen Satz für dS kann dann abgeleitet werden :
∂
∂M
∂ 1
1 ∂U
=
T
∂
∂
T
T
T
M
T
1 ∂ 2U
1
=
T ∂M ∂T T
∂U
−
H
∂M
T
M
∂ 2U
1
∂H
−
− 2
∂M ∂T ∂T M T
∂U
− H
∂M T
∂H
∂U
−T
=
− H
∂ T M ∂M T
Für das Differential der Entropie ergibt sich mittlerweile :
dS =
1 ∂U
∂H
dT −
dM
T ∂T M
∂T M
M ist eine Zustandsfunktion, für die gilt :
∂M
∂M
dM =
dT +
dH
∂
∂
H
T
H
T
Und damit erhält man
∂U
∂H ∂M dT ∂H ∂M
−
dS =
−T
dH
∂T M ∂T H T
∂T M ∂H T
∂T M
Für reversible, adiabatische Vorgänge ist dS = 0 und damit
∂H ∂M
+T
∂T
∂ T M ∂H T
=
∂U
∂H ∂M
∂H S
−T
∂T M
∂T M ∂T H
Jetzt werden folgende Wärmekapazitäten eingeführt :
∂S
∂U
CM = T =
∂T M ∂T M
und
∂S
∂U
∂M ∂H
CH = T =
−T
∂T H ∂T M
∂ T H ∂T M
Damit folgt
∂M
−T
∂T
∂T H
=
CH
∂H S
Aus dem Curie’schen Gesetz
M =
A
⋅H
T
folgt
A
∂M
= − 2 H
T
∂T H
und damit
A
∂T
H
= +
CH T
∂H S
Für einen reversiblen adiabatischen Prozeß ergibt sich also folgende Beziehung :
T dT
S
=
A
H dH
CH
S
beziehungsweise in integraler Darstellung
T
2 2
1
A 2
=
H
CH
2
1
Bei einer adiabatischen Entmagnetisierung aus dem Zustand (H/To) nach (0/T) folgt damit
eine Temperaturänderung
(T
2
− T02 ) = −
A
H2
CH
A H2
T = T 1 −
2
C
T
H
0
2
oder
2
0
Da die Curie-Konstante A und die Wärmekapazität bei konstantem Magnetfeld CH positiv
sind, ergibt sich also bei der adiabatischen Entmagnetisierung eine Temperaturabnahme.
Aufgabenbeispiel 1
Ein Mol eines idealen Gases durchläuft den
nebenstehenden Kreisprozeß. Die nachfolgende Tabelle soll vervollständigt werden.
∆U [J]
∆H [J]
∆S [J]
0
?
?
?
-7145
2045
?
?
?
C→A
1380
-1380
?
?
?
A→A
?
?
?
?
q [J]
w [J]
A→B
5100
B→C
?
Zur Berechnung der Zustandsgrößen ∆U, ∆H und ∆S werden folgende Formeln
herangezogen :
∆U = q + w
∆H = ∆U + ∆pV = ∆U + nR∆T
mit R=8.314 J/Kmol
C
∂S
∆S folgt für isochore Prozesse aus
= V nach der Integration zu
T
∂T V
∆SAB = n CV ln(TB/TA)
Für den isothermen Fall C → A wird folgende Rechnung durchgeführt :
dS =
dq dU + dw dU pdV
=
=
+
T
T
T
T
A
mit dU=0 für ideale Gase
A
V
1 nRT
⋅
dV = nR ln A
T V
VC
C
∫ dS = ∆S = ∫
C
Die übrigen Größen ergeben sich, wenn man ansetzt, dass im Kreisprozeß die
Änderungen von Zustandsfunktionen Null sind.
Damit erhält man dann die vollständige Tabelle :
q [J]
w [J]
∆U [J]
∆H [J]
∆S [J]
A→B
5100
0
5100
7129
14.4
B→C
-7145
2045
-5100
-7129
-20.2
C→A
1380
-1380
0
0
5.8
A→A
-665
+665
0
0
0
Aufgabenbeispiel 2
Es soll gezeigt werden, dass nach
Entfernen einer Wand zwischen zwei
Kammern mit gleichen Mengen eines
Gases von verschiedenen Temperaturen
aber gleichen Drucks die Entropie steigt.
Vorausgesetzt wird dabei, dass die Wärmekapazität temperaturunabhängig ist.
Für die Entropie gilt bei konstantem Druck
Ti
Si = ni
∫
0
Cp
T
dT
Die Molzahlen vor dem Entfernen der Wand waren gleich (n1 = n2 = n), nachher befinden
sich also nend = 2n Mol des Gases in der Kammer. Für die Temperaturen gilt
T1 ≤ Tend ≤ T2
Damit gilt für die Entropieänderung :
∆S = S end − (S1 + S 2 ) = 2n
Tend
∫
0
Tend
= 2n
∫
0
Cp
T
Tend
dT − n
∫
0
Cp
T
Cp
T
T1
dT − n ∫
Cp
0
Tend
∫
dT + n
T1
T
Cp
T
T2
dT − n ∫
0
Tend
dT − n
∫
0
Cp
T
Cp
T
dT
T2
dT − n
∫
Tend
Cp
T
dT
2
Tend dT T2 dT
Tend
Tend
T2
= n Cp ∫
− ∫
− ln
= n C p ln
= n C p ln
T1T2
T
T
T
T
T1
1
end
Tend
Mit Tend =
T1 + T2
folgt
2
2
Tend
∆S = n C p ln 2
>0
Tend − ∆2T
qed.
Aufgabenbeispiel 3
Es sollen die theoretischen Wirkungsgrade zweier Dampfmaschinen verglichen werden.
Das Kondensat besitze in beiden Fällen eine Temperatur von 30°C. Die eine Maschine
arbeite bei 5 atm, die andere bei 100 atm. Die Siedepunkte des Wassers sind 152°C bei 5
atm und 312°C bei 100 atm.
Der maximale Wirkungsgrad einer Wärmekraftmaschine ist
η=
Damit ergibt sich sofort :
To − Tu
To
a) 5 atm
b) 100 atm
µ=
425 K − 303K
= 29%
425 K
η=
585 K − 303K
= 48%
585 K
Je höher die Arbeitstemperatur ist, umso größer ist der Wirkungsgrad.
Mehrkomponenten - Systeme
Bisher wurde die Molzahl als eine Konstante angesehen und es wurden nur Ein-StoffSysteme betrachtet. Hat man es jedoch mit Mehr-Stoff-Systemen zu tun, so tragen die
einzelnen Komponenten im Verhältnis ihrer Molzahlen zu den einzelnen Zustandsfunktionen bei, also z. B. zur freien Enthalpie :
∆G = n1 µ1 + n 2 µ 2 + ... =
∑n µ
i
i
Wobei µi das chemische Potential der i-ten Komponente ist.
Im Gleichgewicht ist d ∆G = 0 oder nach Gibbs-Duhem :
∑ n dµ
i
i
=0
Vernachlässigt man die Wechselwirkungen zwischen den Molekülen verschiedener
Substanzen, was z. B. für Gase meist zulässig ist, so erhält man als Gesamtdruck eines
Systems das Daltonsche Partialdruckgesetz
∑p
i
= p ges.
∑p
i
=
aus
RT
V
∑n
i
= n⋅
RT
= p ges.
V
Das Chemische Potential
In der Grundstudium-Vorlesung war das chemische Potential µ eingeführt worden als
molare Freie Enthalpie einer reinen Substanz :
µ=
G
n
Jetzt, wo wir es mit Gemischen aus mehreren Stoffen zu tun haben, müssen die
integralen Größen G und n durch ihre Differentiale ersetzt werden, also
µ=
dG
dn
Für Mehrkomponentensysteme ergibt sich als Freie Enthalpie des Gesamtsystems :
∆G=
∑n µ
i
i
Für das Differential dG gilt dann bei konstantem Druck und konstanter Temperatur
∂G
∂G
dG =
dn1 +
dn 2 + ...
∂
n
∂
n
1 n ( i ≠1)
2 n ( i ≠2 )
In Anlehnung an die ursprüngliche Definition des chemischen Potentials können die
Ableitungen von G nach ni als chemisches Potential der Komponenten i aufgefaßt
werden.
dG = ∑ µi d ni
Das chemische Potential ist jetzt nicht mehr unabhängig von den anderen Komponenten
des Gemischs, da zwischen den Molekülen Wechselwirkungen auftreten, die von den
Konzentrationen abhängen.
Für Gemische idealer Gase gilt für die individuellen Potentiale :
µ i = µ i0 + RT ln
pi
p0
0
wobei µi das chemische Potential der reinen Substanz und pi ihr Partialdruck ist.
Den Sinn des chemischen Potentials erkennt man, wenn man den Zusammenhang
anderer thermodynamischen Größen mit µ untersucht.
Für die Enthalpie gilt
H =G+T S
oder
dH = dG + T dS + S dT
Für die Freie Enthalpie gilt der Fundamentalsatz der Thermodynamik
dG = V dp − S dT + ∑ µ i d ni
Und damit ergibt sich für dH
dH = V dp − S dT + ∑ µ i d ni + T dS + S dT
also
dH = V dp + T dS + ∑ µ i dni
Bei konstantem Druck und konstanter Entropie gibt das chemische Potential also an, wie
die Enthalpie einer Komponente von der Zusammensetzung der Mischung abhängt.
∂H
= µi
∂
n
i p , S , n ( j ≠i )
Die Clausius-Clapeyron-Gleichung
Zur Ableitung der Gleichung für Phasenumwandlungen soll hier, im Gegensatz zur Ableitung in der Vorlesung des Grundstudiums, an die Definition des Wirkungsgrades eines
Carnot-Prozesses angeknüpft werden. Im Druck-Volumen-Diagramm eines realen Gases
können die Adiabaten als praktisch senkrecht (V = const.) angenommen werden, wenn
die Isothermen nicht zu weit auseinander liegen. Wir betrachten jetzt einen CarnotProzeß, der auf den Isothermen T und T + dT abläuft und das Gebiet der vollständigen
Phasenumwandlung umschließt, also von der reinen Gasphase bis zur vollständigen
Verflüssigung geht.
Abbildung 6 : Ableitung der Dampfdruckgleichung aus v.d.Waals-Isothermen.
Laut Definition ist der Wirkungsgrad gleich dem Quotienten aus geleisteter Arbeit -∆w
und hineingesteckter Wärme q. Andererseits gilt auch
η=
(T + dT ) − T
T + dT
=
dT
− ∆w ∆V ⋅ dp
=
=
T + dT
q
q
In der Summe kann dT vernachlässigt werden und die geleistete Arbeit ist die Fläche
unter dem Kreisintegral. Es ergibt sich die differentielle Form der ClausiusClapeyron'schen Gleichung
∆V ⋅ dp dT
=
q
T
oder
dp
∆H
=
dT T ⋅ ∆V
für
q = ∆H Verdampfun g
Setzt man ∆V ≈ V (Gas ) und nimmt ideales Verhalten an, so ergibt sich die (integrale)
Verdampfungsgleichung
ln
p
∆H
=−
+ Const
p0
RT
Osmose
Trennt man eine Mischung vom reinen Lösungsmittel durch eine semipermeable Wand,
die nur das Lösungsmittel durchläßt, so tritt solange Lösungsmittel in die Mischung ein,
bis sich ein thermodynamisches Gleichgewicht eingestellt hat. Dabei baut sich ein
osmotischer Druck in der Lösung auf, der durch folgende Formel definiert ist :
π = p L − p0
L :Lösung,
O :reines Lösungsmittel
Das chemische Potential eines Stoffes ist gegeben durch
p
µ = µ~ + RT ln 0
p
wobei p für das reine Lösungsmittel gleich p0 ist.
Im Gleichgewicht gilt
µL = µ0
L
p
µ~ L + RT ln 0 = µ~ 0
p
L
oder
p
µ~ 0 − µ~ L = RT ln 0 = RT ln(1 − xG ) ≈ − RT xG
p
Die linke Seite ist gleich
µ~ 0 − µ~ L = V ( p 0 − p L ) = − π V
Damit gilt für verdünnte Lösungen das van t'Hoff'sche Gesetz
π=
RT
xG
V
Zur Veranschaulichung der Osmose kann man sich vorstellen, dass die großen Moleküle
zusammen mit der Membran wie Ventile wirken, die den Stofftransport nur in einer
Richtung zulassen. (Abbildung 7)
Abbildung 7 : Mechanismus der Osmose
Destillation
Das Raoult'sche Gesetz beschreibt die Dampfdrücke zweier flüssiger Substanzen, die in
einer Mischung vorliegen :
p A = x A ⋅ p A,r
p B = x B ⋅ p B ,r
mit
xi = Zusammensetzung in der flüssigen Phase und pr = Dampfdruck der reinen
Substanz
Das Dalton'sche Partialdruckgesetz sagt :
pA = y A ⋅ p
pB = y B ⋅ p
mit yi = Zusammensetzung in der Gasphase
Mit p = pA + pB und xA + xB = 1 folgt
yA =
x A ⋅ p A, r
x A ⋅ p A,r + (1 − x A ) p B ,r
oder
xA =
p B,r ⋅ y A
p A,r + ( p B ,r − p A,r )y A
Für den Gesamtdruck p gilt
p = xA pA,r + (1 - xA) pB,r = xA (pA,r - pB,r) + pB,r
und
p=
p B , r ⋅ p A, r
p A,r + ( p B ,r − p A,r )⋅ y A
Die Kurven von p vs xA , bzw. p vs yA ergeben eine Gerade, bzw. eine Hyperbel. Oberhalb
der Geraden liegt für große Drücke nur die flüssige Phase vor, unterhalb der Hyperbel nur
die Gasphase.
Führt man den Gesamtmolenbruch z ein, so ist für die beiden eben beschriebenen Gebiete z identisch mit x bzw. y. Dazwischen liegt ein Zweiphasengebiet, für das gilt :
z ⋅ n = n g ⋅ y + nl ⋅ x
oder
mit
n = n g + nl
nl
z−x
=
ng
y−z
Das bisher entwickelte p-z-Diagramm gilt für konstante Temperaturen. Eine Destillation,
d.h. die Trennung des Gemisches ist hier durch Druckveränderung vorzunehmen.
Das jedoch häufigere Verfahren der Destillation arbeitet bei konstantem Druck durch
Variation der Temperatur. Über die Temperaturabhängigkeit des Druckes kann ein
entsprechendes Diagramm abgeleitet werden.
Reale Mischung haben jedoch manchmal Abweichungen von dem bisher diskutierten
Verhalten. Hier kann immer nur bis zu dem azeotropen Gemisch destilliert werden.
Thermochemie
Die in der Chemie besonders interessierende Größe ist die Freie Enthalpie. Den Mangel,
daß nur Enthalpieänderungen gemessen werden können, hilft man damit ab, daß man die
Enthalpien als Standardenthalpien festlegt.
T
G=G +
0
∫ dG
298
Das Hess'sche Gesetz sagt aus, daß in einem Kreisprozeß die Summe der Standardenthalpien plus der Reaktionsenthalpie gleich Null ist. Dieses Gesetz folgt aus dem 1.
Hauptsatz der Wärmelehre : Für Zustandsfunktionen, also auch für die Freie Enthalpie, ist
das Integral über einen Kreisprozeß gleich Null.
Die Temperaturabhängigkeit der Enthalpie ergibt sich aus der Definition der Wärmekapazität
∂H (T )
C p (T ) =
∂T p
T
oder
H T = H T0 + ∫ C p dT
T0
Und entsprechend für die Innere Energie und die Entropie
T
U T = U T0 + ∫ CV dT
T0
T
Cp
Cp
dq
= ∫ dT = ST0 + ∫ dT
ST = ∫
T
T
T
T0
Für die Freie Enthalpie ergibt sich dann aus der Definition
T
GT = H − T ⋅ S = H T0 − T ⋅ S T0 + ∫ C p dT − T
T0
T
∫
T0
Cp
T
Die Druckabhängigkeit der Freien Enthalpie ergab sich für ideale Verhältnisse zu
G = G 0 + nRT ln
p
p0
dT
Für die Freie Reaktionsenthalpie oder Reaktionswärme, d.h. für die Änderung der Summe
der Enthalpien aller beteiligten Substanzen, ergibt sich dann nach dem Hess'schen Satz
0
∆GRe akt = ∑ Gi = ∆GRe
akt + RT ln
i
Π ( pProdukt / p0 )ν
Π ( pEdukt / p0 ) µ
ΠpProdukt
ist per definitionem gleich der aus dem MassenΠpEdukt
wirkungsgesetz bekannten Gleichgewichtskonstanten Kp.
Der Operand des Logarithmus
Im Gleichgewicht ist ∆GReakt. für einen Kreisprozeß gleich Null und somit
∆G R0
∆H R0 ∆S R0
ln K p = −
=−
+
RT
RT
R
Da in der Thermodynamik nur Gleichgewichte betrachtet werden, ist hier die die Reaktion
definierende Größe die Standardreaktionsenthalpie ∆GR0 . Diese wird daher tabelliert.
Das Differential dieser Gleichung ist die van t'Hoffsche Gleichung
d ln K p
dT
=
∆H R
RT 2
Die Messung thermodynamischer Größen ist meist sehr aufwendig und in einfachen
Versuchen kaum darstellbar. Eine Ausnahme bilden die elektrochemischen Vorgänge
Die pro Formelumsatz geleistete elektrische Arbeit ist
∆E el = U ⋅ I ⋅ t = n ⋅ N A ⋅ q − ⋅ ∆E
aus
I ⋅ t = n ⋅ N A ⋅ q−
wo q- die Elementarladung und U= ∆E eine Potentialdifferenz (= Spannung) ist. Diese
Zellspannung wird auch EMK (Elektro-Motorische Kraft) genannt.
∆Gchem = − n ⋅ F ⋅ ∆E
wo F die Faraday-Konstante ( = N A ⋅ q − ) ist. Und damit gilt auch :
∂∆G
∂ ∆E
∆S = −
= n⋅F
∂T p
∂T p
Man kann also leicht über die Messung der Temperaturabhängigkeit der Zellspannung die
Entropie des Systems bestimmen.
Temperaturabhängigkeit der Gleichgewichtskonstanten und Prinzip von
Le Chatelier
Zur Vereinfachung soll angenommen werden, daß die Reaktionsenthalpie nicht von der
Temperatur abhängt. (In der Realität läßt sich diese Abhängigkeit durch ein
A + BT + C/T2
-Gesetz beschreiben; dies würde jedoch die Gleichungen nur verkomplizieren, ohne daß
etwas prinzipiell Neues beschrieben würde)
Es soll die Reaktion der Ammoniak-Synthese untersucht werden :
N 2 + 3H 2
→
2 N H 3 + ∆H Re aktion
←
Unter Standardbedingungen (298 K, 1 atm) wurden folgende Werte gefunden :
K p = 6 ⋅ 10 5
0
∆H NH
= − 46.1kJ Mol
3
(Standardbildungsenthalpie)
Aus der van t'Hoff'schen Reaktionsgleichung folgt dann durch Integration :
d ln K ∆H R
=
dT
RT2
∆H R dT
∆H 1
∫1 d ln K = ∫1 R T 2 = ∫1 − R d T
2
oder
2
2
ln K 2 − ln K1 = −
∆H R 1
1
−
R T1 T2
ln K T = ln K 298 −
∆H R 1
1
−
R T
298
Für T = 500 K ergibt sich somit
ln K 500 = ln6 ⋅ 10 5 +
2 ⋅ 46.1K 1
1
−
8.314 500 298
Da die Standardbildungsenthalpien von H2 und N2 definitionsgemäß gleich 0 sind, ist die
0
Reaktionsenthalpie gleich 2∆ H NH 3 . Für R wurde 8.314 JK-1 Mol-1 gesetzt.
ln K500 =
K500 =
oder
- 1,73
0,18
Die Gleichgewichtskonstante war gegeben durch
p 2 (NH 3 ) ⋅ p02
Kp =
p ( N 2 ) ⋅ p 3 (H 2 )
Das Prinzip des kleinsten Zwanges (LeChatelier) sagt nun aus, daß bei Druckerhöhung
das System dem Zwang ausweicht. Da das Reaktionsprodukt nur 2 Mol Gasmoleküle
entspricht, die Edukte jedoch 4 Mol entsprechen, wird bei Druckerhöhung also das
Gleichgewicht nach NH3 verschoben (Haber-Bosch-Verfahren).
Für exotherme Reaktionen ist ∆H R < 0 . Aus der van t'Hoff-Gleichung folgt nun, daß bei
dln K dT
Temperatur-Erhöhung
kleiner wird. Und damit wird auch K kleiner, was
oben gezeigt wurde. Anders ausgedrückt bedeutet dies, daß mit
−
∆G
∆H
=−
+ ∆S
T
T
bei exothermen Reaktionen − ∆G T positiv ist. Diese positive Entropie bedeutet also
eine "Triebkraft" für die Reaktion. Bei Temperaturerhöhung wird also diese Triebkraft
schwächer, es wird weniger NH3 gebildet.
Die Richtung chemischer Reaktionen
In einer allgemeinen Betrachtungsweise soll jetzt der Zusammenhang zwischen dem
chemischen Potential und der Richtung, in die ein chemischer Prozeß abläuft, untersucht
werden.
Edukte ⇔ Produkte
Zur Vereinfachung wird angenommen, daß die absolute Änderung der Eduktkonzentration
gleich der der Produkte sei.
d[Edukte] = - dξ
d[Produkte] = + dξ
(Es wird hier mit infinitesimalen Änderungen gerechnet, da das chemische Potential ja von
den Konzentrationen aller beteiligten Substanzen abhängt und damit nur infinitesimale
Änderungen zugelassen werden können. Sonst wäre ξ zeitabhängig.)
Die Änderung der Freien Enthalpie ist damit bei konstantem Druck und konstanter Temperatur gleich :
dG = µEdnE + µPdnP = - µEdξ + µPdξ
oder
∂G
= µ P − µ E
∂
ς
p ,T
Jeder spontane Prozeß verläuft in Richtung abnehmender Energie. Für chemische
Prozesse glit also :
Ist µE > µP verläuft die Reaktion in Richtung der Produkte.
Ist µE < µP verläuft die Reaktion in Richtung der Edukte.
Ist µE = µP befindet sich das System im Gleichgewicht.
Die Bestimmung des Aktivitätskoeffizienten
Die Kräfte zwischen neutralen Teilchen klingen etwa mit einem 1/r6-Gesetz mit der
Entfernung der Teilchen voneinander ab. Geladenen Teilchen dagegen folgen den
Coulomb-Gesetz mit 1/r. Daher ist einzusehen, daß schon bei relativ großen Verdünnungen von Ionen ein starkes Abweichen vom idealen Verhalten zu beobachten ist.
Gleich große Verdünnungen von neutralen Partikeln folgen dann immer noch den
Gesetzen idealer Mischungen. Dies soll an einem Beispiel verdeutlicht werden.
Für einen 1-1-Elektrolyten
z.B.
Ag Cl
→
←
Ag + + Cl −
∆G = − nF ⋅ ∆E
und
gilt :
mit
F = N A ⋅ q−
∆G = ∆G 0 + n RT ln K
Abbildung 8 : Elektrodenprozesse eines 1-1 Elektrolyten
Hierbei ist anstelle von Konzentrationen nun die Aktivität a zu setzen, um den Wechselwirkungen zwischen den Molekülen einer Lösung Rechnung zu tragen.
a+ ⋅ a−
K=
a (neutral)
Die Aktivität a der neutralen Substanz darf gleich 1 gesetzt werden, da Wechselwirkungen
hier noch keine Rolle spielen. Es gilt also :
K = a + ⋅ a − = C + ⋅ C − ⋅ γ ±2
Nach der Debye-Hückel-Theorie ist der Logarithmus des mittleren Aktivitätskoeffizienten
γ ± = (γ + ⋅ γ − )
0.5
proportional der Wurzel aus der Konzentration
lnγ ± = A C0,5
Für die EMK des 1-1-Elektrolyten gilt damit
∆E = ∆E 0 − (RT F ) ln K
= ∆E 0 − (RT F ) lnC 2 − (RT F ) lnγ ±2
Bringt man die meßbaren Größen nach links, ergibt sich
∆E + (2 RT F ) lnC
= ∆E 0 − (2 RT F ) lnγ ±
≈ ∆E 0 − (2 RT F ) ⋅ A ⋅ C 0.5
∆E + (2 RT F ) lnC
0.5
gegen C
läßt sich somit
das Standardpotential ∆E0 (unter idealen Bedingungen) und der mittlere Aktivitätskoeffizient bestimmen. Dies ist in Abbildung 9 gezeigt.
Aus der Geraden der Auftragung von
Die Abweichung von der Geraden bei C > 0.2 ergibt sich, da die Debye-Hückel Theorie
die Proportionalität von ln γ± zu C nur in erster Näherung beschreibt. Nimmt man
weitere Glieder der Funktionsentwicklung hinzu, so lässt sich der Verlauf der Messpunkte
auch für größere Konzentrationen beschreiben.
Abbildung 9 : Konzentrationsabhängigkeit der EMK eines 1-1 Elektrolyten
Der Born-Haber Kreisprozess
Als Beispiel für den Satz von Hess – in einem Kreisprozess ist die Summe der Standardenthalpien gleich der negativen Reaktionsenthalpie – soll hier die Bildung eines ionischen
Festkörpers nach dem Born-Haber Kreisprozess besprochen werden. In Abbildung 10 ist
dieser Prozess dargestellt.
Der Festkörper Kaliumchlorid soll aus seinen Elementen gebildet werden. Dies sind festes
Kalium und gasförmiges Cl2. Im ersten Schritt wird Kalium verdampft; die
Verdampfungsenthalpie beträgt 89 kJ. Danach wird das Chlorgas dissoziert mit einer
Dissoziationsenergie von 122 kJ. Der letzte Schritt, bei dem Verbindungen gelöst werden,
ist die Ionisierung des Metalls. Hierfür werden 418 kJ benötigt.
In den folgenden Schritten werden nacheinander das Elektron mit dem Chloratom und
dann die Ionen miteinander verbunden. Die bei diesen Bindungen freiwerdenden Energien
betragen 349 kJ und 717 kJ. Sie sind negativ zu rechnen, da sie dem System verloren
gehen. Als Ergebnis findet man, dass 437 kJ Reaktionswärme frei werden, dies ist die
Bildungsenthalpie von KCl.
Abbildung 10 : Der Haber-Born Prozess der KCl-Bildung
Gasgesetze
Die Kinetische Gastheorie gilt für ein Gas, das die folgenden fünf Postulate erfüllt :
1) Die Gesetze der Statistik erfüllt sein.
2) Das Volumen der Partikel muß klein gegen das betrachtete Volumen sein.
3) Zwischen den Partikeln soll keine Wechselwirkung herrschen.
4) Inelastische Stöße (= Reaktionen ) sollen nicht vorkommen.
5) Die Teilchen sollen sich zwischen zwei Stößen gleichförmig bewegen.
Aus diesen Postulaten läßt sich die Allgemeine Gasgleichung ableiten.
p ⋅V = n ⋅ R ⋅ T
Hierbei ist V das betrachtete Volumen und n die Molzahl, d.h. die Anzahl der Teilchen
dividiert durch die Avogadro Zahl NA. Damit ist R = NA * k , wo k die BoltzmannKonstante ist.
Gibt man einige der Postulate auf, so muß das Allgemeine Gasgesetz korrigiert werden.
Dann ergibt sich für reale Gase die van der Waals-Gleichung
n2
p + a ⋅ V 2 ⋅ [V − nb] = n RT
Hierbei ist zu beachten, daß die Korrekturfaktoren a und b nicht unabhängig von
Temperatur und/oder Druck sind.
Die Verteilung der Geschwindigkeiten von Gaspartikeln ist die Boltzmann-Verteilung. Die
allgemeine Form dieser Verteilung lautet
f (u ) = A ⋅ a n 2 ⋅ exp(− au 2 ) ⋅ u n −1
A ist hier eine Konstante, die sich aus der Normierung ergibt, und n ist die Dimension für
die die Gleichung aufgestellt wurde. Der Parameter a ist der Formfaktor der Verteilung :
a=
m
2 RT
In Abbildung 11a sind die Boltzmann Verteilungen im 1-, 2- und 3-dimensionalen Raum
dargestellt. Den Einfluss der Temperatur ist in Abbildung 11b für den 3-dimensionalen Fall
gezeigt.
Abbildung 11 : Zur Boltzmannfunktion
Die Verteilungsfunktion hat die Bedeutung einer Wichtung. Jeder der möglichen Werte u
wird entsprechend seiner Häufigkeit gezählt.
Interessiert man sich für die Anzahl der Stöße, die ein Teilchen A mit Teilchen vom Typ B
erleidet, so erhält man für die Stoßfrequenz
Z A = 2 ⋅ σ AB ⋅ u ⋅
NB
V
u ist die Relativgeschwindigkeit zwischen dem Teilchen A und den Teilchen B. NB/V ent-
spricht der Konzentration [B] und σ AB ist der Stoßquerschnitt, der sich aus den
Durchmessern der Moleküle A und B ergibt :
σ AB
d + dB
= π ⋅ A
2
2
Die Gesamtzahl der Stöße, die in der Zeit ∆ t in einem Volumen V geschieht, ist dann :
Z AB = Z A ⋅
N A 0.5
N N
= 2 ⋅ σ AB ⋅ u ⋅ A ⋅ B
V
V V
Die mittlere freie Weglänge λ ist gleich
λ =
u ⋅ ∆t
=
Z A ⋅ ∆t
1
2 ⋅ σ AB ⋅ (N B V )
d.h. der Weg s = u ⋅ ∆t , den ein Teilchen in ∆t zurücklegt, dividiert durch die Anzahl der
Stöße in diesem Zeitraum, ist unabhängig von der mittleren Geschwindigkeit u der
Teilchen. Diese Aussage ist aber gleichbedeutend mit der Aussage, daß die mittlere freie
Weglänge unabhängig von der Temperatur ist.
Stöße auf eine Ebene und mit Partikeln
In der Vorlesung des Grundstudiums hatten wir gesehen, dass die Stoßfrequenz, d.h. die
Anzahl der Stöße pro Zeiteinheit, die ein Molekül (A) durch alle anderen (B) erfährt, gleich
ist zu
Z A = u rel ⋅ σ AB ⋅ C B
mit
u rel = 2 u
Analog zu den Überlegungen zur Anzahl der Stöße auf ein Teilchen ergibt sich für die
Anzahl der Stöße auf eine ebene Fläche F
Z F = 12 u F ⋅ F ⋅ CB = 14 u ⋅ F ⋅ CB
Hier ist wieder CB die Konzentration der stoßenden Teilchen und u deren gemittelte
Geschwindigkeit. Die mittlere Geschwindigkeitskomponente senkrecht zur Fläche F ist nur
halb so groß wie die mittlere Geschwindigkeit, wie aus der Integration aller Geschwindigkeiten über eine Hemisphäre folgt. Der erste Faktor ½ ergibt sich, da nur die Hälfte
aller Teilchen auf die Fläche zu fliegen (die andere fliegt von der Fläche weg).
Die beiden Formeln für die Stoßfrequenz sind gleichwertig und gehen in einander über,
wie man am Beispiel der Stöße von Molekülen auf ein Staubkorn erkennen kann :
Ist das Staubkorn groß, so ist die Relativgeschwindigkeit fast gleich der
Geschwindigkeit der stoßenden Moleküle
u rel = u B
und der Stoßquerschnitt entspricht dem Querschnitt des großen Partikels
σ AB ≈ σ A = π rA2
Für die Stoßfrequenz zwischen diesen beiden Teilchen gilt also
Z A = π rA2 ⋅ u B ⋅ C B
Geht man jetzt davon aus, dass das Staubkorn für ein Molekül wie eine große
Fläche aussieht, deren Größe der Oberfläche einer Kugel
F = 4π rA2
entspricht, dann erhält man für die Stoßfrequenz auf eine Fläche
ZF =
1
4
u ⋅ 4π rA2 ⋅ C B = π rA2 ⋅ u ⋅ C B = Z A
Die Ableitung des Allgemeinen Gasgesetzes
Die uns zugänglichen, d.h. meßbaren Größen sind alle makroskopischer Natur. Wir leben
in einer Welt, deren Größenordnung das Mol ist. In den Vorstellungen (oder Modellen)
jedoch, die wir uns von dem Geschehen zwischen den Partikeln machen, betrachten wir
nur einzelne Teilchen und ihr Verhalten. Um das Partikelmodell auf die molare Welt
abzubilden, brauchen wir mathematische Gesetze, hier die Gesetze der Statistik. Wir
nehmen an, daß wir ein mittleres Verhalten von sehr vielen Partikeln betrachten. Und
damit die Abbildungsgesetze möglichst einfach werden, nehmen wir zusätzlich an, daß die
Bewegung der Teilchen ungeordnet ist, also keine Vorzugsrichtung aufweist. Der
Schwerpunkt unseres Gasensembles bleibt damit in Ruhe. Dies ist keine Einschränkung
der Gasgesetze, es vereinfacht nur die Rechnungen.
Die Kinetische Gastheorie verbindet jetzt die mikroskopischen Attribute der Molekeln :
Anzahl, Masse, Impuls, Energie mit den makroskopischen, meßbaren Größen : Volumen,
Druck, Molzahl und Temperatur. In der folgenden Ableitung soll insbesondere auch
gezeigt werden, an welchen Stellen die einschränkenden Postulate für ein ideales Gas
eingeführt werden müssen.
Fangen wir mit dem Druck in einem Würfel der Kantenlänge l an. Per definitionem ist der
Druck auf eine Wand der Größe A :
p = F/A
Und nach dem 2. Newton'schen Axiom gilt für die Kraft, die ein Teilchen auf die Wand
ausübt :
F = d (m ux ) / dt
ux ist die Geschwindigkeitskomponente eines Teilchens senkrecht zur Wand.
Bislang brauchten wir noch keine Einschränkungen machen, jetzt führen wir ein, daß nur
elastische Stöße zugelassen sind (inelastische Stöße, d.h. Reaktionen der Partikel
untereinander und mit der Wand sind ausgeschlossen). Damit kann das Differential d(mv)
bestimmt werden :
d (m ux ) = 2 m ux
Außerdem nehmen wir an, daß die Partikel unendlich klein sind, also kein Volumen
besitzen. Dann legen sie beim Stoß auf die Wand zwischen zwei Stößen untereinander im
Mittel die Strecke 2 lx in x-Richtung zurück und damit gilt für das Zeitdifferential :
dt = 2 l x u x
Der Druck, den N Teilchen auf eine Wand ausüben, ist also gleich
p =∑
2mu x
mu 2x
mu x2
= N⋅
= N⋅
2l x u x ⋅ A
l⋅A
V
u bezeichnet die mittlere Geschwindigkeit aller Teilchen. Diese ist aufgrund der Maxwell-
Boltzmann-Statistik identisch mit der für ein Teilchen über die Zeit gemittelten Geschwindigkeit.
Für das nach Voraussetzung isotrope Medium gilt
u 2x = u 2y = u 2z
u 2 = u 2x + u 2y + u 2z = 3 u x2
und
Und somit :
p ⋅ V = N ⋅1 3 ⋅ m ⋅ u 2 = 2 3 ⋅ N ⋅ ε trans
wo ε trans =1 2 ⋅ m ⋅ u 2 die Translationsenergie eines Teilchens ist. Die mittlere Tanslationsenergie bei einer Gleichgewichtsverteilung der Energien wird nun zur Definition der
Temperatur herangezogen :
εtrans
= 3/2 kT
Und da der Zusammenhang zwischen Boltzmann-Konstante k und allgemeiner Gaskonstante R gegeben ist durch
R = NA k
folgt aus
p V = 2/3 N εtrans
das Allgemeine Gasgesetz :
pV = nRT
mit N = n * NA
Viskositätskoeffizient und mittlere freie Weglänge
In dem Allgemeinen Gasgesetz hatten wir uns auf ein ruhendes Medium beschränkt. Jetzt
sollen die Verhältnisse bei bewegtem Schwerpunkt des Gases betrachtet werden. Dabei
soll gelten, dass die Strömungsgeschwindigkeit v sehr viel kleiner ist als die Molekülgeschwindigkeit u. Da dann immer noch das Statistik-Postulat gilt, gilt auch das
Allgemeine Gasgesetz.
Gase oder Flüssigkeiten, die an einer Fläche A vorbeiströmen, erfahren eine bremsende
Kraft, die Reibung. Diese Kraft ist proportional der Fläche und dem Geschwindigkeitsgradienten senkrecht zu A :
F =η A
∂v
∂y
Der Proportionalitätsfaktor ist der Viskositätskoeffizient η .
Um diese innere Reibung verständlich zu machen, geht man wieder auf die Kinetische
Gastheorie zurück. Wir denken uns ein Gas aus Schichten der Dicke d aufgebaut. Diese
Schichten sollen vorerst unterschiedliche Strömungsgeschwindigkeiten v besitzen. Verläßt
jetzt ein Molekül die eine Schicht und stößt mit einem Teilchen der benachbarten Schicht
zusammen, so überträgt es seien gesamten Impuls auf die neue Schicht, d.h. die
Schichten üben eine Kraft aufeinander aus. Im Mittel wechseln gleich viele Teilchen aus
einer Schicht in die andere wie umgekehrt, so daß also nur die Impulsänderungen und
nicht die Massenänderungen in Bezug auf die Strömungsrichtung betrachtet werden
müssen.
Für den Impulsübertrag in y-Richtung (senkrecht zur Strömungsrichtung x) ergibt sich
somit :
∆I = m ⋅
∂v
⋅d
∂y
Bei einer Teilchenkonzentration von C = N / V fliegen 1 3⋅ u ⋅ C pro Sekunde durch eine
Fläche A zwischen den Schichten (in beiden Richtungen !). u ist die mittlere Geschwindigkeit eines Teilchens, während v die Strömungsgeschwindigkeit ist. Damit wird der
Gesamtimpulsaustausch, pro Sekunde, d.h. die Kraft, die die Schichten aufeinander
ausüben, gleich
F=
∂I 1
∂v
= u ⋅C ⋅ m ⋅ d
∂t 3
∂y
Dies ist aber die im Anfang definierte Reibung oder Viskosität. Für den Viskositätskoeffizienten folgt dann :
η = 1 3u ⋅ m ⋅ d ⋅ C
η ist also unabhängig von der Strömungsgeschwindigkeit und ihrem Gradienten.
Für die Schichtdicke d wird jetzt die mittlere freie Weglänge λ eingesetzt. Denn wäre
d > λ , so würden Teilchen noch innerhalb ihrer Ursprungsschicht stoßen, also nicht zur
Viskosität beitragen. Und für d < λ würden einige der Teilchen über die benachbarte
Schicht hinausfliegen. Also bleibt nur d = λ und damit
η = 1 / 2 ⋅u ⋅ m ⋅ λ ⋅ C
(Bei der Integration über den Raumwinkel anstelle einer Aufteilung der Flugrichtung in
karthesische Koordinaten ergibt sich ein Faktor 1 / 2 anstatt 1/3.)
Knudsenströmung
Im folgenden soll an einem Beispiel gezeigt werden, daß das Allgemeine Gasgesetz nicht
mehr gilt, wenn das Statistik-Postulat aufgegeben wird. (Bei Aufgabe der anderen
Postulate bleibt das Gesetz prinzipiell gültig, es müssen nur die Variablen p, V, n und T
durch effektive Größen ersetzt werden.)
Wir betrachten jetzt ein Rohr der Länge l und mit einem Durchmesser d. Die Konzentration des Gases, das sich im Rohr befindet sei so gering, daß die mittlere freie
Weglänge größer ist als der Rohrdurchmesser. Dann werden die Moleküle praktisch
ausschließlich mit der Wand stoßen und nicht mehr untereinander. Somit kann sich keine
aerodynamische Strömung ausbilden.
Herrscht jetzt zwischen den Enden des Rohres ein Druckgefälle, d.h. sind die Konzentrationen C vor und hinter dem Rohr unterschiedlich groß, so tritt ein Partikelstrom durch
das Rohr hindurch. Die Strömungsgeschwindigkeit dN/dt ist nach Knudsen gegeben durch
dN 1 A
= ⋅ ⋅ ∆C ⋅ d ⋅ u
dt
3 l
Hier ist A die Querschnittsfläche des Rohrs, l seine Länge und d sein Durchmesser. ∆C ist
der Konzentrationsgradient und u die Molekülgeschwindigkeit.
Aus der Definition der Temperatur, die zwar nicht mehr im Rohr, aber immer noch in den
Vorratsgefäßen gilt,
1 2 ⋅ m ⋅ u 2 = 3 2 ⋅ kT
erhalten wir bei konstanter Temperatur die Beziehung
u ~
1
m
Somit wandern leichtere Moleküle schneller durch das Rohr als schwerere. Bei Atmosphärendruck beträgt die mittlere freie Weglänge etwa 100 nm. Ist jetzt ein Gasgemisch durch eine poröse Wand, deren Porengröße etwa 10 nm beträgt, von einem
Unterdruckgebiet getrennt, so wird sich das Gas entmischen. Auf der Seite des höheren
Druckes bleiben die schweren Moleküle zurück, da die leichteren eine höhere KnudsenStrömungsgeschwindigkeit besitzen. Diese Tatsache wird z.B. bei der Isotopentrennung
verwendet, wobei man viele Trennstufen kaskadenförmig hintereinander schaltet.
Diffusion in Gasen
Nach dem 1. Fick'schen Gesetz
j=
dN dt
dN
= −D⋅
A
dx
ist die Teilchenstromdichte j, d.h. die Anzahl der Teilchen, die pro Zeiteinheit durch die
Fläche A hindurchtreten, proportional dem Konzentrationsgradienten. Die Proportionalitätskonstante ist die Diffusionskonstante D.
Wir nehmen jetzt wieder vereinfachend an, daß 1/3 aller Moleküle sich parallel zum
Konzentrationsgefälle in x-Richtung bewegen. Die durch die Fläche A hindurchtretenden
Moleküle sind bei I bzw. II gestartet. Der Abstand dieser Flächen von der Fläche A sei
jeweils die mittlere freie Weglänge λ . Die Geschwindigkeit aller Teilchen sei u .
Somit fliegen
1 6N I ⋅u ⋅ A ⋅ ∆t
Teilchen von links nach rechts und
1 6N II ⋅u ⋅ A ⋅ ∆t
von rechts nach links. Für die Teilchenstromdichte gilt daher :
j =
dN dt u
= ⋅ (N I − N II )
A
6
Bei einem linearen Konzentrationsgefälle dN/dx gilt aber für die Differenz NII - NI :
N II − N I = 2λ ⋅
dN
dx
Und damit erhalten wir für die Diffusionskonstante unter Einbeziehung des realen Wertes
(1/20.5 ) für die Anzahl der Teilchen, die in x-Richtung fliegen :
D=
1
⋅u ⋅λ
2
Das 2. Fick'sche Gesetz, bzw. die Allgemeine Diffusionsgleichung beschreibt die
Konzentrationsänderung in einem Volumen V. In x-Richtung fließen bei I jI Teilchen
durch die Wand A pro Sekunde in das Volumen hinein und bei II jII Teilchen durch die
gleich große Wandfläche wieder hinaus. (Wir haben hier also nicht mehr ein lineares
Konzentrationsgefälle über den gesamten Volumenbereich angenommen).
Damit ist die Änderung der Konzentration im Volumen V = A dx gleich :
dN V
dj
=−
dt
dx
oder
dN V
d 2N V
= D⋅
dt
dx 2
Bei dreidimensionalen Konzentrationsgefällen gilt allgemein :
d N
N
⋅ = D ⋅ ∇2
dt V
V
oder durch Konzentrationen ausgedrückt
d
C = D ⋅ ∇ 2C
dt
Kinetische Gastheorie und Maxwell-Boltzmann-Verteilung
Es wurden bisher das Allgemeine Gasgesetz in karthesischen Koordinaten abgeleitet.
Dabei trat der Faktor 1/3 auf, der ohne Beweis abgeändert wurde. Im folgenden soll jetzt
auf die korrekte Ableitung eingegangen werden.
Die kinetische Gastheorie führt die beobachtbaren Größen p und T auf molekulare
Größen zurück :
T ~ v2
p ~ mv
1) Um die Mittelwerte numerisch berechnen zu können, müssen die Gesetze der
Statistik gelten : Das System muß sich aus vielen Teilchen mit unregelmäßiger
Bewegung zusammensetzen und das Medium muß isotrop, d.h. in allen Raumrichtungen gleichartig ,sein. Für die mittlere Molekülgeschwindigkeit gilt dann
v 2 = v x2 + v y2 + v z2
mit
v x2 = v y2 = v z2
2) Zur Vereinfachung der Rechnung gehen wir zu Polarkoordinaten über : Für ein
Element der Kugeloberfläche gilt dann
dA =
A
sin ϑ ⋅ dϑ ⋅ dϕ
4π
3) Es wird jetzt danach gefragt, wie viele Partikel in der Zeit dt auf die Fläche dA
auftreffen. Es sind dies alle Teilchen, die sich in einem schiefen Zylinder dV
aufhalten :
dV = dA dh
mit
dh = v cosϑ dt
Die Konzentration ist überall gleich :
N dN
=
V
dV
Aus
C=
folgt
dN dV dA ⋅ dh
=
=
=
N
V
V
=
1 A
⋅
sinϑ dϑ dϕ ⋅ v cosϑ dt
V 4π
Der Anteil der Moleküle, die aus der Richtung (dϑ,dϕ) kommen und die
Geschwindigkeit v besitzen, ist also
dN v ,ϑ ,ϕ = dN v ⋅
Av
sinϑ cosϑ dϑ dϕ dt
4π V
4) Nun kann das Allgemeine Gasgesetz exakt abgeleitet werden :
Für elastische Stöße an einer Wand gilt für die Impulsänderung
d mv = 2mv cos ϑ
Für alle Stöße mit der Geschwindigkeit v aus dem Raumelement (dϑ,dϕ) ergibt sich
also
d mv = (dN v
oder
Av
sinϑ cosϑ dϑ dϕ dt ) ( 2 mv cosϑ )
4π V
dmv / dt
2mv 2
= dpv = dN v
sinϑ cos2 ϑ dϑ dϕ
4π V
A
Integriert über alle Raumrichtungen ergibt sich
dN v
dpv = mv
V
2
1
2π
2π
∫ dϕ
0
2
cos
ϑ
sin
ϑ
d
ϑ
∫0
π /2
Der Ausdruck in den Klammern [ ] ist gleich 1/3, und damit ergibt sich dpv zu
dpv =
1 2 dN v
mv
3
V
Nun wird über alle Geschwindigkeiten integriert
∞
∞
1m 2
1m
p = ∫ dpv =
v
dN
=
N v2
v
∫
3V 0
3V
0
oder
p ⋅V =
2
N ε trans
3
da
1
2
ε trans = m v 2
5) Zur Berechnung des Mittelwerts der Translationsenergie der Teilchen muß die
Verteilungsfunktion bekannt sein. Es wurde vorausgesetzt, daß das Medium isotrop
ist. Dann müssen aber die drei Koordinaten des Geschwindigkeitsvektors unabhängig von einander sein und für ihre Verteilungsfunktion gilt damit
dN
= F ( v ) dv = f ( v x ) f ( v y ) f ( v z ) dv x dv y dv z
N
Da F nur von der Geschwindigkeit und nicht von der Richtung abhängig sein soll,
muß auch die folgende Aussage gelten
F ( v x2 + v 2y + v z2 ) = f ( v x2 ) f ( v 2y ) f ( v z2 )
Diese Forderung wird nur von der e-Funktion erfüllt. Also gilt für die Verteilungsfunktionen :
f (vi ) = Ai e ± a vi
und
F ( v x2 + v 2y + v z2 ) = Ax Ay Az e
± a ( v x2 + v 2y + v z2 )
Die positiven Vorzeichen der Exponentialfunktion können nicht gelten, da die Menge
der Möglichkeiten begrenzt sein muß. Für die Verteilungsfunktion gilt folgende
Normierung
∞
∫ F (v) dv = 1
0
und damit auch
A = (a ) 3 / 2
π
Setzt man jetzt noch die Definition der Temperatur ein
1
mit
2
m < v2 > =
3
2
kT
< v 2 > = ∫ v 2 f ( v ) dv
so erhält man für a :
a=
m
2kT
und für F(v2) ergibt sich
3
2
m −mv
F (v ) = 4π
e
2πkT
2
2
2
kT
v2
Formalkinetik
Die Kinetik beschäftigt sich mit der Beobachtung von zeitlich veränderlichen makroskopischen Größen, wie z.B. der Konzentration. Sie führt diese Veränderungen auf
molekulare Eigenschaften der untersuchten Materie zurück. Um die Einstellung des
Gleichgewichts quantitativ fassen zu können, wird die Reaktionsgeschwindigkeit definiert.
vA =
d [A]
n
m
= − k n [A] [B ]
dt
für die Reaktionen
n A + m B → Produkte
Der Term [A]n [B]m gibt an, wie oft A mit B zusammenstößt. k ist der Proportionalitätsfaktor und das Vorzeichen gibt die Richtung der Reaktion an. Die stöchiometrischen
Größen n und m gehen als Faktoren ebenfalls in die Reaktionsgeschwindigkeit ein.
k ist somit eine vom betrachteten Stoff unabhängige Reaktionskonstante, die ausreicht,
die Reaktion zu beschreiben. (Selbstverständlich neben der chemischen Formulierung.)
Aus der Gleichheit von Stoßzahl (s. ‚Gasgesetze’) und Reaktionsgeschwindigkeit folgt :
k ~ 2 ⋅ σ AB ⋅ u ≡ k gaskinetisch
mit σAB als Stoßquerschnitt und u als mittlere Molekülgeschwindigkeit.
Da nicht jeder Stoß zu einer Reaktion führt, gilt hier nur eine Proportionalität, deren
Konstante immer kleiner als 1 ist, wenn elektrisch neutrale Teilchen betrachtet werden.
Die Reaktionswahrscheinlichkeit soll mit α bezeichnet werden, dann ergibt sich für die
Arrhenius-Gleichung :
k = α ⋅ k gaskin ⋅ e − E A
RT
= k0 ⋅ e −EA
RT
Der präexponentielle Faktor k0 ist also für Reaktionen von Neutralteilchen nur kleiner oder
höchstens gleich der gaskinetischen Reaktionskonstanten kgaskin. Die molare
Entsprechung EA zum Energieschwellwert ε0 wird als Aktivierungsenergie bezeichnet. Für
Reaktionen mit geladenen Teilchen wird k0 größer als kgaskin, da die Stöße aufgrund der
gegenseitigen Anziehung häufiger stattfinden.
Der monomolekulare Zerfall
Bevor das Zeitgesetz des monomolekularen Zerfalls abgeleitet wird, soll abgeschätzt
werden, wie groß die Lebensdauer eines Moleküls ist.
Wir nehmen an, daß sich der präexponentielle Faktor k0 aus der kleinst-möglichen Reaktionszeit einer Dissoziation von etwa 1 psec, d.h. einer Schwingungsperiode, ergibt. Die
mittlere thermische Energie bei 300 K beträgt etwa 1/40 eV. Das sehr schwach
gebundene Ozon hat eine Dissoziationsenergie von 1.1 eV, also etwa den 44-fachen Wert
der thermischen Energie. Damit ergibt sich für die Reaktionskonstante :
k = k 0 ⋅ e − RT0
RT
= 10 +12 e −44 sec −1
bzw. für die Lebensdauer
τ =
1
= 10 −12 e + 44 = 1.3 ⋅ 10 7 s = 150 d
k
Bei diesen schwach gebundenen Teilchen sinkt also die Konzentration in etwa 150 Tagen
auf den e-ten Teil ab.
Sauerstoff hat dagegen eine Bindungsenergie von 5.6 eV, d.h. dem 225fachen der
thermischen Energie. Für Sauerstoff ergibt sich daraus eine Zerfallszeit von
τ = 10 −12 e +255 = 5.2 ⋅ 1085 s = 1.6 ⋅ 10 78 a
Das bedeutet, daß Sauerstoff dem spontanen Zerfall gegenüber inert ist.
Wir wollen jetzt das Zeitgesetz für den monomolekularen Zerfall ableiten. Das klassische
Beispiel für einen derartigen Vorgang ist der radioaktive Zerfall, z.B.
α
226
Ra
→
222
α
Rd
→
3.8 d
1620 a
218
Po
→ ... Pb
3.05 m
Die Reaktionsgeschwindigkeit von Radon ergibt sich also zu
v Rd =
d [Rd ]
= − k [Rd ]
dt
oder allgemein :
vX =
d [X ]
= − k [X ]
dt
Diese Differentialgleichung ist die Definitionsgleichung einer e-Funktion. Ihre Lösung ist
demnach
[X ]t
= Const e − kt
Wie bei jeder Differentialgleichung ergibt sich die Integrationskonstante aus der Randbedingung :
Wir nehmen an, daß zur Zeit t=0 die Konzentration des Stoffes gleich [X]0 gewesen sei.
Somit gilt
[X]t
= [X ]0 e − kt
Das Zeitgesetz für das Produkt wird aus dem Ansatz der Massenkontinuität abgeleitet :
[X]t + [Prod]t = [X]0
Damit folgt dann unmittelbar :
[Prod]t = [X]0 (1-e-kt)
Bimolekulare Reaktionen
Die größte Reaktionskonstante einer bimolekularen Reaktion ergibt sich aus der
Stoßfrequenz. Häufiger als bei jedem Stoß kann diese Reaktion nicht stattfinden. Bei
einem Druck von 1 atm beträgt die Stoßzeit neutraler Moleküle etwa 0,5 nsec. Damit wird
die Reaktionskonstante gleich
1τ
2 ⋅ 10 9 sec −1
=
k =
≈ 10 −10 cm 3 s
19
−3
2.5 ⋅ 10 cm
C1atm
Eine typische bimolekulare Reaktion 2. Ordnung ist die Reaktion gleichartiger Moleküle,
wie z.B.
OH + OH
→
H 2O + O
Der gemessene Wert für die Reaktionskonstante beträgt
k = 1.8 ⋅ 10 −12 cm 3 s
Diese Reaktion läuft also nur etwa bei jedem 50. Zusammenstoß zwischen zwei OH-Radikalen ab.
Die Geschwindigkeit einer Reaktion vom Typ
A + A → Prod.
entspricht
vA =
d [A]
2
= − 2 k [A]
dt
Die Lösung dieser Differentialgleichung erhält man durch die Separation der Variablen,
hier [A] und t :
1
∫ [A] d [A] = − 2 k ∫ dt
2
−
1
+ C = − 2 kt
[A]
1
= C + 2 kt
[A]
Die Integrationskonstante findet man wieder durch Einsetzen der Randbedingung :
1
1
=
+ 2k ⋅t
[A] t [A] 0
Eine der Aufgaben der Kinetik ist es, eine Reaktion über die Geschwindigkeitskonstante k
zu charakterisieren. Für eine Reaktion 1. Ordnung findet man :
1 [X ]t
k = − ln
t [X ]0
Hier muss also nur ein Signal gemessen werden, das proportional zur Konzentration einer
Substanz ist. Die Proportionalitätskonstante braucht nicht unbedingt bekannt sein.
Anders dagegen bei Reaktionen 2. Ordnung. In diesem Fall muß die Konzentration
absolut bekannt sein, will man k bestimmen :
k=
1 1
1
⋅
−
2t [A]t [A]0
Hier tritt jetzt anstelle des Quotienten, bei dem die Proportionalitätskonstante sich heraushebt, die Differenz der Konzentrationen auf, bei der die Proportionalitätskonstante nicht
herausgekürzt werden kann. Man wird es also immer möglichst so einrichten, daß die
untersuchte Reaktion von pseudo-1.-Ordnung ist. D.h. man wird den einen Reaktionspartner im Überschuß ansetzen, so daß sich seine Konzentration praktisch nicht ändert
und damit in die Reaktionskonstante hereingezogen werden darf. Dies gilt selbstverständlich nur, wenn die beiden Stoßpartner ungleich sind. Daher wird die Reaktion 2.
Ordnung in der Praxis nur bei der Rekombination gleicher oder komplementärer Teilchen
auftreten. Unter komplementären Teilchen sind z.B. Ionen unterschiedlicher Ladungsart
zu verstehen :
M
Ar + + e − →
Ar
Da bei einer Rekombination immer der Energieüberschuß abgeführt werden muß, handelt
es sich also praktisch immer um eine Reaktion pseudo-2. Ordnung.
Es soll noch einmal deutlich darauf hingewiesen werden, dass sich die Ordnung einer
Reaktion von der Molekularität unterscheidet. Die Molekularität ist die Summe der
stöchiometrischen Faktoren, die Ordnung einer Reaktion gibt dagegen an, mit welcher
Potenz der Konzentrationen sich die Reaktionsgeschwindigkeit merkbar ändert.
Parallelreaktionen
Wir wollen im folgendem stets annehmen, daß die betrachteten Reaktionen pseudo-1.
Ordnung sind.
Häufig tritt der Fall ein, daß eine Reaktion zwei oder mehr Reaktionskanäle besitzt, deren
Geschwindigkeitskonstanten separat bekannt sein sollen :
1
→
O2 + H 2
2
→
OH + OH
H + HO2
3
→
H 2O + O
5.6 ⋅ 10 −12 cm 3 s
7.2 ⋅ 10 −11 cm 3 s
2.4 ⋅ 10 −12 cm 3 s
Hier besitzt die zweite Reaktion den größten Umsatz, aber auch die beiden Seitenkanäle
dürfen nicht vernachlässigt werden. Für die Reaktionsgeschwindigkeit von H ergibt sich
daraus :
vH =
d [H ]
= − k1 [H ][HO 2 ] − k 2 [H ][HO 2 ] − k 3 [H ][HO 2 ]
dt
Das Radikal HO2 ist gegenüber dem H-Atome meistens im Überschuß vorhanden, da es
weniger reaktiv ist.
Als Lösung der Differentialgleichung ergibt sich somit :
[H ]t
= [H ]0⋅ e − (k1 +k2 +k3 )[HO2 ]t
Es ergibt sich also ein Gesetz wie bei einer einzigen Reaktion, nur daß hier die Geschwindigkeitskonstanten zu einer Gesamtreaktionskonstante addiert werden. Im Beispiel
also :
k ges = 8.0 ⋅ 10 −11 cm 3 s
Folgereaktionen
Für eine Folge von Reaktionen
1
2
A
→
B
→
C
gilt, dass die Konzentration von Stoff A nicht durch die Folgeprodukte B und C beeinflusst
wird, also
[A] = [A]0 e − k t
1
Da das Zwischenprodukt B gebildet wird und dann verschwindet, muß für die Zeitabhängigkeit seiner Konzentration gelten :
[B] = Const.(e − k t − e − k t )
2
1
Und die Konzentration von C erhält man aus
[A]0 = [A] + [B] + [C ]
Für das Zwischenprodukt B hatten wir implizit angenommen, dass seine Bildung schneller
geschieht als seine Abreaktion. Ist das Umgekehrte der Fall, so kann der Umsatz der
Reaktion 2 nur so groß sein, wie der Umsatz der Bildung :
k 2 [B]= k1 [A]
oder
[B] = k k [A]
1
2
Als Beispiel für den monomolekularen Zerfall war der radioaktive Zerfall des Radiums
gegeben :
1
2
Ra
→
Rd
→
Po
→ …
→ Pb
Das zugehörige Differentialgleichungssystem lautet, wenn wir den Zerfall des Radiums bis
zum Blei als einen Schritt (2) betrachten :
d [Ra ]
= − k1 [Ra ]
dt
(1)
d [Rd ]
= + k1 [Ra ] − k 2 [Rd ]
dt
(2)
d [Pb ]
= + k 2 [Rd ]
dt
(3)
Aus (1) erhalten wir sofort :
[Ra ]t
= [Ra ]0 e − k1t
In (2) eingesetzt :
d [Rd ]
= + k1 [Ra ]0 e − k1t − k 2 [Rd ]
dt
Radon ist ein typisches Zwischenprodukt, das zuerst gebildet werden muß und danach
wieder verschwindet. Es folgt daher einem Zeitgesetz der Form
[ X ] = Const ⋅ ( e − K t −e − Lt )
Die Differentialgleichung hat dann die Lösung :
[Rd ]t
=
{
k1
[Ra]0 e −k2 t − e −k1 t
k 2 − k1
}
Hierbei wurde vorausgesetzt, daß zum Zeitpunkt t=0 kein Radon vorhanden war. Die
beiden e-Funktionen beschreiben den Aufbau ( e − k1t ) und den Zerfall ( e − k2t ) des Radons.
Dies gilt für jedes Zwischenprodukt : Es muß gebildet werden und es vergeht. Beide
Vorgänge werden durch eine Exponentialfunktion beschrieben.
Die zeitliche Änderung der Konzentration des Endproduktes Pb braucht nicht durch
Integration der Differentialgleichung 3 berechnet werden. Einfacher geht es über eine
Bilanzgleichung : Die Menge an Substanz muß konstant gleich der Ausgangsmenge sein :
[Ra]0 = [Ra]t + [Rd ]t + [Pb]t
oder
[Pb]
= [Ra ]0 − [Ra ]0 e −k1t −
{
k1
[Ra ]0 e −k1t − e −k2t
k 2 − k1
}
k1
k1
= [Ra ]0 1 − e − k1t −
e − k1t +
e − k 2t
k 2 − k1
k 2 − k1
k2
k1
= [Ra ]0 1 −
e − k1t +
e − k 2t
k 2 − k1
k 2 − k1
Das temporäre Gleichgewicht
Neben dem thermodynamischen Gleichgewicht, d.h. dem Zustand der sich für t=∞
einstellt, wird auch der Begriff ‚temporäres Gleichgewicht’ benutzt. Für ein Gleichgewicht
gilt immer, dass die Konzentrationsänderung gleich Null ist:
d
C=0
dt
Hier müssen also die Umsätze (Reaktionsgeschwindigkeiten) der Hin- und Rückreaktion
gleich sein. Gilt dies nur näherungsweise, ändert sich also der Gesamtzustand nur
langsam, wird von einem temporären Gleichgewicht gesprochen.
Man kann ein temporäres Gleichgewicht auch dadurch erzeugen, dass z.B. durch
kontinuierliche Zugabe der Edukte und Abzug der Produkte, z.B.: im einem Strömungsreaktor, immer die gleichen Konzentrationen im System bestehen. Hier ist also ein Einsatz
von Energie und Masse notwendig, um das Gleichgewicht aufrecht zu erhalten. Ein
solches System im temporären Gleichgewicht ist unsere Atmosphäre, wobei die Energie,
die zur Aufrechterhaltung des temporären Gleichgewichts benötigt wird, von der Sonne
geliefert wird.
Katalyse
Da es nicht möglich ist, im Rahmen dieser Vorlesung ausführlich auf alle Einzelheiten der
Katalyse einzugehen, sollen hier nur die Grundprinzipien der Katalyse behandelt werden.
Katalyse ist nach W. Ostwald ein Prozess, der durch den Zusatz eines Stoffes
beschleunigt abläuft. Der zugesetzte Stoff, der Katalysator, wird dabei nicht
verbraucht.
Man unterscheidet zwischen der homogenen und heterogenen Katalyse. In der ersteren
liegen der Katalysator und die Edukte in der gleichen Phase vor, in der heterogenen
Katalyse ist der Katalysator meistens ein Feststoff. (Im Grundstudium wurde das HaberBosch Verfahren besprochen.)
Wir wollen jetzt annehmen, dass die Vorgänge der Katalyse bis in die Elementarprozesse
aufgeklärt sind, und dass einer dieser Elementarschritte durch den Katalysator beeinflusst
wird. Wie kann man dann die Beschleunigung durch den Katalysator erklären?
In Abbildung 13 ist gezeigt, wie durch Zugabe eines Katalysators der chemische Prozess
beschleunigt wird:
1. Durch den Katalysator wird eine Parallelreaktion möglich und dies
bedeutet bereits eine Beschleunigung des Vorgangs.
2. Am stärksten lässt sich eine Reaktion durch die Verringerung der
Aktivierungsenergie beschleunigen, da diese im Exponenten einer
Exponentialfunktion steht.
3. Bei Stössen mit einer geringen Reaktionswahrscheinlichkeit kann
durch die Parallelreaktion diese Wahrscheinlichkeit vergrößert
werden.
4. Und schließlich kann der Umsatz einer Reaktion (oder die Reaktionsgeschwindigkeit) auch dadurch vergrößert werden, dass die Konzentrationen der beteiligten Stoffe erhöht werden. In der heterogenen
Katalyse hält der Katalysator zum Beispiel ein Edukt fest und erhöht
so dessen Verfügbarkeit.
Abbildung 13 : Möglichkeiten zur Beschleunigung einer Elementarreaktion durch Katalyse.
Ein einfaches Beispiel für eine homogene Katalyse ist der Ozonabbau in der
Stratosphäre. Ohne Katalysatoren verläuft der Ozonabbau ausschließlich über die
Reaktion mit Sauerstoffatomen.
O3 + O → O2 + O2
Fügt man einen geeigneten Stoff X (z.B. OH, NO oder Cl) hinzu, wird dieser durch Ozon
oxidiert, und anschließend das XO durch die Reaktion mit O-Atomen wieder reduziert.
X + O3 → XO + O2
XO + O → X + O2
netto
O3 + O → O2 + O2
In der folgenden Tabelle sind die Vorfaktoren, die Aktivierungsenergien und die Umsätze
für die unkatalysierte und die beschleunigten Reaktionen aufgetragen. (Zur Berechnung
der Umsätze wurden gemessene Konzentrationen der Katalysatoren und der Edukte
eingesetzt. Durch das komplexe Reaktionssystem der Erdatmosphäre sind diese Werte
als vorgegeben anzusetzen.)
3 -1
3 -1
-3 -1
Reaktion
A [cm s ]
EAkt/R [K]
k [cm s ]
Umsatz [cm s ]
O + O3 → 2 O2
1.5 x 10-11
2218
8.8 x 10-15
3.0 x 105
O + NO2 → NO + O2
9.3 x 10-12
0
9.3 x 10-12
2.3 x 103
O3 + NO → NO2 + O2
3.8 x 10
O + HO2 → OH + O2
3.5 x 10-11
O3 + OH → HO2 + O2
1.6 x 10
-12
940
5.5 x 10
1.4 x 10
O + ClO → Cl + O2
7.7 x 10-11
130
5.0 x 10-11
3.8 x 104
O3 + Cl → ClO + O2
2.8 x 10
-11
257
1.2 x 10
-12
1580
0
-14
6
1.9 x 10
1.0 x 10
3.5 x 10-11
2.7 x 103
-14
-11
5
4
1.3 x 10
Eyring - Theorie
Grundlagen
n der kinetischen Gastheorie wurde so getan, als ob die Partikel eines Gases einheitliche
Teilchen wären, die sich wie starre Kugeln oder elastische Bälle verhalten. Aber schon,
wenn das Volumen dieser Teilchen bestimmt werden soll, trifft man auf Schwierigkeiten.
Das Volumen kann einmal aus dem kritischen Daten, d.h. aus dem Kovolumen bestimmt
werden. Zum anderen geht der Durchmesser aber auch in die Stoßzahl ein, und damit
kann auch aus dynamischen Größen, wie z. B. der Viskosität, das Volumen bestimmt
werden. Aber das "statische" und das "dynamische" Volumen der Gaspartikel stimmt nicht
überein.
Da die Gasmoleküle aus einem winzigen Kern und einer diffusen Elektronenwolke
bestehen, können sich die Moleküle "durchdringen" und eine starke gegenseitige
Beeinflussung erfahren. Aber auch, wenn sich die Teilchen noch nicht bis auf Abstände
im Bereich ihres statischen Volumens genähert haben, wirken Kräfte zwischen ihnen, die
die gradlinigen Flugbahnen verändern. Jede solche Veränderung wollen wir als "Stoß"
bezeichnen und als "Stoßdurchmesser" einen mittleren Abstand der Teilchen, bei dem
sich die Partikel messbar beeinflussen.
Außerdem sollte bei dieser Betrachtungsweise eines Stoßes auch klar sein, daß die
gegenseitige Beeinflussung so groß werden kann, daß nicht nur Energie zwischen den
Stoßpartnern ausgetauscht wird. Die Wechselwirkungen können so stark werden, daß die
Teilchen ihre Identität verlieren und neue Partikel gebildet werden. Dabei verweilen die
stoßenden Teilchen auch länger als die reine "Vorbeiflugzeit" beieinander. Die Trajektorien zeigen dann, daß die Stoßpartner umeinander kreisen. Stöße, bei denen neue
Produkte entstehen, sollen in Zukunft als chemisch "reaktiv" angesprochen werden. Alle
anderen Stöße sollen als "elastisch" bezeichnet werden.
Von H. Eyring wurde 1935 der Vorschlag gemacht, den Stoßkomplex oder Übergangszustand, auch wenn er nur die Lebenszeit einer Schwingungsperiode hat, als eine eigene
chemische Verbindung, dem "aktivierten Komplex", anzusehen.
Die Einführung des aktivierten Komplexes, oder des Übergangszustandes, bringt einen
gewaltigen Fortschritt in der Theorie der chemischen Reaktionen mit sich. Aus der
kinetischen Gastheorie erfolgt nun ohne Einschränkung die Bildung des Übergangszustandes, die damit berechenbar wird. Als "chemische Reaktion" bleibt jetzt nur noch der
Zerfall einer hochangeregten Verbindung, der monomolekulare Zerfall, zu bestimmen.
Entsprechend werden heute Experimente durchgeführt, die die Bedingungen aufzeigen
sollen, wie der monomolekulare Zerfall funktioniert. Und die Theorie der Reaktionsdynamik beschäftigt sich mit der Wahrscheinlichkeit dafür, daß ein Übergangszustand in
die Produkte zerfällt. Dabei sind prinzipiell jeweils mindestens zwei Reaktionswege offen,
derjenige, der zu den Produkten führt, und der zweite, der zu den Ausgangspartikeln
zurückführt :
1
→
3
A+ B
AB *
→
C+D
←
2
Ein Beispiel für den Zerfall eines größeren organischen Moleküls zeigt Abbildung 14.
Abbildung 14 : Zerfallswege eines mehratomigen Moleküls
Berechnet man die Kräfte und Energien, die zwischen zwei Atomen bestehen, als
Funktion der Position der Kerne zueinander, so ergibt sich zuerst eine Anziehung
zwischen dem Kern des einen und der Elektronenhülle des zweiten Atoms. Durchdringen
sich die Elektronenhüllen, so stoßen sich sowohl die Kerne als auch die Elektronen ab.
Dazwischen existiert ein Punkt, in dem sich die Kräfte aufheben, d.h. hier ist die Energie
minimal. Die zugehörige Morsekurve wird im Abschnitt über den Molekülaufbau behandelt
werden. Hier genügt es zu wissen, dass sich die Morsekurve aus einem anziehenden und
einem abstoßenden Zweig zusammensetzt. In ihrem Minimum ähnelt sie einer Parabel.
Für mehr als zwei Atome können ähnliche Diagramme für die relative Position der Kerne
zueinander berechnet werden. Trägt man die Abstände eines Kerns zum Schwerpunkt der
übrigen jeweils auf einer Achse eines kartesischen Koordinatensystems auf, so ergibt sich
für die Energie ein n-dimensionales Gebilde, die Energiehyperfläche.
Abbildung 15 : Darstellungen einer zweidimensionalen Energiehyperfläche
Kennt man die Energiehyperfläche (z. B. aus spektroskopischen Daten und ab initioRechnungen), so läßt sich mit statistischen Experimenten (Monte-Carlo-Rechnungen)
entscheiden, welcher Anteil des aktivierten Komplexes in welchen Kanal läuft. Eine
geschlossene Theorie hierzu gibt es zur Zeit noch nicht.
Es soll hier jetzt noch nicht auf die Ableitung der Eyring-Formel für die Reaktionskonstante
eingegangen werden. Als Ergebnis ergibt sich für die Reaktionsgeschwindigkeit
v =α⋅
kT
q#
⋅
⋅ e − ∆ε 0
h q A ⋅ qB
kT
[A][B]
Für die praktische Anwendung bringt diese Gleichung keinen Vorteil gegenüber dem
Arrhenius-Ausdruck, da auch hier ein Faktor α, die "Durchlässigkeit", eingeführt werden
muß, der nur experimentell bestimmbar ist.
Häufig wird die Aktivierungsenergie EA = NA ε0 aus thermodynamischen Größen abgeleitet. Dies bedeutet jedoch einen Bruch im Modell, denn ursprünglich geht die EyringTheorie vom molekularen Bild aus. Beim Übergang zum molaren Bild der Thermodynamik
muß dann über alle möglichen Zustände integriert werden, wobei das ursprüngliche klare
Konzept verwaschen wird.
Der eigentliche Fortschritt, der durch Eyring gegeben wurde, liegt darin, daß die Vorgänge
bei einer chemischen Reaktion deutlich werden, und daß durch reaktionsdynamische
Betrachtungen die Reaktionskonstante im Prinzip berechenbar wird. Eyring mußte sich
1935 noch mit der Einführung molarer Größen bescheiden, während uns heute mit den
Computern Werkzeuge zur Verfügung stehen, die diesen Umweg unnötig machen. Wir
können heute einzelne Stöße simulieren und dann statistische Betrachtungen anstellen,
die zu den molaren Größen führen.
Abschließend sollen noch einige Begriffe, die von Eyring eingeführt wurden, bzw. die mit
der Eyring-Theorie im Zusammenhang stehen, erläutert werden. Dies geschieht anhand
einer zweidimensionalen Hyperfläche, d.h. wir betrachten einen dreiatomigen Übergangszustand. Die Basisvektoren für dieses Gebilde sind neben der Energie ε die Abstände rABC
und rA-BC des Schwerpunktes eines Moleküls (AB oder BC) vom dritten Kern.
Der Weg durch die Talsohle der Energiehyperfläche, d.h. unter der Linie minimaler
Energie wird als Reaktionskoordinate bezeichnet. Mit Hilfe dieser Reaktionskoordinate
kann dann die Reaktion in einer zweidimensionaler Abbildung erklärt werden.
Es muß an dieser Stelle deutlich gemacht werden, daß die Kurve, die gemeinhin in das
Koordinatensystem Energie vs. Reaktionskoordinate eingezeichnet wird, nicht den
Reaktionsverlauf wiedergibt, sondern die Minimal-Energie entlang der Reaktionskoordinate darstellt. Hat ein System (hier aus drei Atomen) eine Gesamtenergie, die kleiner ist
als die Energie des aktivierten Komplexes, so kann der Endzustand nicht erreicht werden,
die Ausgangssubstanzen werden nach dem Stoß zurückgebildet. Erst wenn die Energie
des Edukt-Systems größer ist als das Energiemaximum, können Produkte gebildet werden, die dann ihre Überschußenergie in Stößen oder durch spontane Lichtemission
(Chemolumineszenz) abgeben, um in den Grundzustand zu gelangen.
Die Abbildung 15 zeigt die zweidimensionale Energiehyperfläche für ein dreiatomiges
Teilchensystem in verschiedenen Darstellungsformen. In der perspektivischen Zeichnung
ist die Talsohle des Energiegebirges, d.h. die Linie, die als Reaktionskoordinate bezeichnet wird, dargestellt. Die zweite Zeichnung ist eine Darstellung der Energiehyperfläche in
Form von Höhenlinien. In ihr sind unterschiedliche "Reaktionswege" eingezeichnet. Ist die
Systemenergie nicht für eine chemische Reaktion ausreichend, so wird im Stoß Translationsenergie in Vibrationsenergie und umgekehrt überführt. Aber auch wenn genug Energie im System vorhanden ist, läuft der Reaktionsweg nicht unbedingt über dem Sattelpunkt, d.h. den aktivierten Komplex, in den Produktkanal. Durch die Reflexionen an den
"Energiebergwänden" ist es durchaus möglich, daß das System wieder in den EduktKanal mündet. Durch Monte-Carlo-Rechnungen, bei denen die Systemenergie und die
Aufteilung in translatorische und vibratorische Energie mittels Zufallszahlen zugeordnet
wird, wird dann der Übergang vom mikroskopisch in den makroskopischen Zustand
simuliert.
Die Ableitung der Eyring-Formel
Eyring‘s Theorie geht von folgenden Postulaten aus :
1)
Der aktivierte Komplex wird als ein realer Molekülzustand angesehen, auch wenn er
nicht experimentell faßbar ist. In Bezug auf die Energiehyperfläche liegt er auf einem
Sattelpunkt, d.h. in (n-1) Richtungen hat der Komplex ein Energieminimum, in einer
Richtung, der Reaktionskoordinate, jedoch ein Maximum. Der Sattelpunkt besitzt die
Energie ε*0 .
2)
Es besteht ein thermodynamisches Gleichgewicht zwischen den Ausgangsstoffen
und dem Übergangszustand.
Dieses Postulat ist nicht ganz einsichtig. Der Zerfall in die Produkte kann genauso schnell
sein, wie der in die Edukte. Deshalb wird das 3. Postulat aufgestellt :
3)
Die Produktbildung stört das thermodynamische Gleichgewicht nicht.
Wir nehmen jetzt an, daß trotz unserer Bedenken ein aktivierter Komplex existiert, der die
Postulate 1-3 erfüllt. Dann läßt sich aus dem Massenwirkungsgesetz eine Gleichgewichtskonstante bestimmen :
[AB ]
K =
*
[A][B]
Diese Gleichgewichtskonstante wird nach der statistischen Thermodynamik auch als
Quotient von Zustandssummen ausgedrückt. {Zustandssummen beschreiben die Besetzung der Energiezustände (Translation, Rotation, Vibration und elektron. Anregung)
eines Moleküls. Eine ausführliche Behandlung erfolgt später}
K =
q AB*
q A ⋅ qB
In dieser Gleichung sind die Zustandssummen der Edukte bekannt. Die Zustandssumme
des aktivierten Komplex ist jedoch fast immer unbekannt und muß abgeschätzt werden.
4)
Das 4. Postulat nimmt jetzt Bezug auf die Tatsache, daß der Übergangszustand auf
einem Sattelpunkt liegt. Da dieser Sattelpunkt in n-1-Richtungen ein
Energieminimum darstellt, soll sich der Komplex fast wie ein "normales" Molekül
verhalten. In der Richtung der Reaktionskoordinate geht jedoch eine Schwingung in
eine Translation über.
Wenn die Teile des aktivierten Komplexes zusammenkommen und wieder auseinander
fliegen, führen sie gerade eine Schwingung aus. Die Frequenz ν dieser Schwingung geht
gegen 0. Man zieht daher den Anteil der Schwingung aus der Zustandssumme qAB#
heraus und erhält :
K =
Der Term e
− ∆ε 0* kT
*
q#
kT
⋅
⋅ e − ∆ε 0 kT
hv q A ⋅ q B
beschreibt die Nullpunktsenergie des Sattelpunktes :
∆ε 0* = ε 0* − (ε 0, A + ε 0, B )
Er wurde aus der Gesamtzustandssumme des Übergangszustandes herausgezogen. Mit
dieser Größe erhalten wir eine Deutung der experimentell beobachteten Aktivierungsenergie.
Der Faktor kT hv ergibt sich, da die Besetzung eines Schwingungsniveaus proportional
1
1
kT
zu
ist, und
=
− hv kT
lim
− hv kT
1− e
hν
v →0 1 − e
Es ist zu beachten, daß q# jetzt nicht mehr die gesamte Zustandssumme des aktivierten
Komplexes ist, sondern nur noch die n-1 Schwingungen beschreibt.
5) Nach dem 5. Postulat ist die beobachtete Reaktionsgeschwindigkeit durch die
Geschwindigkeit bestimmt, mit der der aktivierte Komplex in Richtung Produktbildung
die Energieschwelle überquert.
Damit wird die Reaktionsgeschwindigkeit gleich dem Produkt aus der Konzentration des
aktivierten Komplexes und der Frequenz der zum Zerfall führende Schwingung :
[
]
v R = α ⋅v ⋅ AB # = α ⋅ν ⋅
q#
kT
⋅
⋅ e − ∆ε 0
hv q A ⋅ q B
kT
[A][B ]
Hier wurde zusätzlich die Durchlässigkeit α eingeführt, d.h. die Wahrscheinlichkeit, dass
die Potentialschwelle auch wirklich überschritten wird.
An dieser Stelle soll die Ableitung der Eyring'schen Reaktionskonstante abgebrochen
werden. Der nächste Schritt, nämlich die Ersetzung der Nullpunktsenergie ∆ ε#0 durch die
Reakionsenthalpie ∆G verläßt das Teilchenbild und führt daher zu weiteren Schwierigkeiten in der Interpretation der Formel.
Der Lindemann-Hinshelwood Mechanismus
Es soll jetzt das folgende Reaktionssystem berechnet werden :
A
1
→
←
2
B
→
C
3
Alle drei Reaktionsschritte sollen hierbei von 1. Ordnung oder pseudo-1. Ordnung sein.
Dieses Reaktionssystem wird dann durch ein Differentialgleichungssystem mathematisch
beschrieben :
dA
= − k1 A + k 2 B
dt
dB
dA
= + k1 A − k 2 B − k 3 B = −
− k3B
dt
dt
dC
= + k3 B
dt
Ein solches Differentialgleichungssystem läßt sich gerade noch vollständig lösen, wobei
der Lösungsweg hier nur der Vollständigkeit halber aufgeführt ist.
d 2B
dA
dB
= k1 ⋅
− (k 2 + k 3 ) ⋅
2
dt
dt
dt
dB
dB
= − k1 ⋅
+ k 3 B − (k 2 + k 3 ) ⋅
dt
dt
d 2B
dB
+ (k1 + k 2 + k 3 ) ⋅
+ k1k 3 B = 0
2
dt
dt
Für diese homogene Differentialgleichung 2. Ordnung können wir uns aus unserer Erfahrung heraus einen Ansatz überlegen. B ist ein Zwischenprodukt, es muß also zuerst
gebildet und dann wieder abgebaut werden. Beide Vorgänge werden durch Exponentialfunktionen beschrieben, der Gesamtvorgang also durch eine Linearkombination :
B = a ⋅ e − K1T + b ⋅ e − K 2T + c
Außerdem können wir hier gleich die Randbedingungen mit einbeziehen. Da wir es mit
einer Differentialgleichung 2. Ordnung zu tun haben, benötigen wir 2 Randbedingungen :
Als Zwischenprodukt ist [B] an Anfang und am Ende gleich Null. Damit wird unser Ansatz
zu :
(
B = a ⋅ e − K1 t − e − K 2 t
)
(
dB
= a ⋅ − K1e − K1 t + K 2 e − K 2 t
dt
mit
(
d 2B
= a ⋅ K12 e − K1 t − K 22 e −K2 t
2
dt
)
)
Dieser Ansatz wird jetzt in die Differentialgleichung eingesetzt :
(
)
(
)
(
a ⋅ K12 e − K 1t − K 22 e − K 2 t + a ⋅ (k1 + k 2 + k 3 ) ⋅ K12 e − K1 t − K 22 e − K 2 t + a ⋅ k1k 3 ⋅ e − K1 t − e − K 2 t
Die Gleichung kann zuerst durch a gekürzt werden. Außerdem muß die Gleichung für alle
Zeiten gelten. Die Zeitabhängigkeit wird aber durch die e-Funktion ausgedrückt :
e − K 1t (K 12 − (k1 + k 2 + k 3 )K 1 + k1 k 3 ) − e − K 2 t (K 22 − (k1 + k 2 + k 3 )K 2 + k1 k 3 ) = 0
Somit muß, da die Exponentialfunktion selbst nicht Null wird, jeder Koeffizient für sich
gleich Null werden :
K 12 − (k1 + k 2 + k 3 ) K 1 + k1k 3 = 0
K 22 − (k1 + k 2 + k 3 ) K 2 + k1 k 3 = 0
Diese beiden Gleichungen sind jedoch identisch. Ihre Lösungen ergeben sich aus dem
Binominalsatz zu
2
K 1, 2
oder :
k + k2 + k3
k + k2 + k3
= 1
± 1
− k1 k 3
2
2
K 1, 2 =
(
k1 + k 2 + k 3
1 ± 1− x
2
)
mit
x=
4 k1 k 3
(k1 + k 2 + k 3 )2
Da x immer klein ist gegen 1, kann die Wurzel als Reihenentwicklung geschrieben
werden, wobei nach dem 1. Glied abgebrochen wird :
1− x = 1−
x
2
Es ergeben sich also für die Geschwindigkeitskonstanten K1 und K2 :
K 1 = k1 + k 2 + k 3
)
=0
und :
K2 =
k1 + k 2 + k 3
k1k 3
2k1k 3
⋅
=
2
(k1 + k 2 + k 3 )2 k1 + k 2 + k 3
In K1 wurde das Glied mit x weggelassen, da es nach Voraussetzung klein gegen 1 ist.
Außerdem gilt gemäß der Ableitung
K1 >> K2
Wir wollen jetzt unsere Betrachtungen nicht auf die Anfangsvorgänge im Zeitraum
τ1 = 1 K1 , sondern auf den Zeitraum τ2 = 1 K2 , der für den größeren Abschnitt der
Existenz von B gilt, richten. In diesem Zeitabschnitt gilt :
(
)
B = a ⋅ e − K2 t − e − K1 t ≈ a ⋅ e − K2 t
Mit der Geschwindigkeitskonstanten K2 können jetzt ganz unterschiedliche Reaktionen
beschrieben werden. Lindemann und Hinshelwood haben damit die Unimolekularen
Reaktion beschrieben. Da ein Molekül nur im angeregtem Zustand reagiert, muß der
eigentlichen Produktbildung eine Anregung im Stoß mit dem Medium (Lösungsmittel)
vorausgehen. Dabei wird Translationsenergie in interne Energie umgewandelt :
,M
1→
3
A
A*
→
Pr od.
←
2, M
Die Einzelschritte 1 und 2 sind hier von pseudo 1. Ordnung und damit gilt für K2 nach
Einsetzen der bimolekularen Reaktionskonstanten:
K2 =
k1 k3 M
k1 M + k2 M + k3
Desweiteren wollen wir jetzt die Druckabhängigkeit der Konstanten K2 diskutieren. Für geringe Drücke ist der überwiegende Term im Nenner die Reaktionskonstante k3. Die von M
abhängigen Terme können dann vernachlässigt werden, und es ergibt sich
lim K
2
= k1 ⋅ M
M →0
Entsprechend fällt bei hohen Drücken der Term k3 weg und es folgt :
lim K 2 =
M →∞
k1 ⋅ k 3
k1 + k 2
Nun wird dieser asymptotische Wert als k∞ und die Steigung für geringe Drücke mit k0 bezeichnet :
k 0 ≡ k1
k∞ ≡
k1 ⋅ k 3
k1 + k 2
Mit diesen Abkürzungen läßt sich dann die Formel für K2 durch die beobachtbaren Werte
k0 und k∞ beschreiben :
K2 =
k1 ⋅ M
k0 ⋅ M
=
k1 + k 2
k
⋅ M +1 1+ 0 ⋅ M
k3
k∞
Aber unsere Ausgangsbeziehung
A
→
←
B → C
läßt sich auch noch für weitere Reaktionen verwenden, z.B. für die Rekombination. Bei
der Rekombination muß die Überschußenergie abgeführt werden, da sie ausreichen
würde, das entstandene Molekül wieder zu zerstören. (Bindungsenergie = Dissoziationsenergie). Als Reaktionsschema ergibt sich somit :
A+ B
1
→
←
2
AB *
M
→
3
AB
Und für K2 :
K2 =
k1 ⋅ B⋅ k 3 ⋅ M
k1 ⋅ B + k 2 + k 3 ⋅ M
k1B ist hierbei meist klein gegen k3M und wird im Nenner vernachlässigt. Führen wir jetzt
wieder die beobachtbaren Größen k0 und k∞ ein, so folgt :
K2 =
k0 ⋅ B ⋅ M
k ⋅M
1+ 0
k∞
mit
k 0 ≡ k1
und
k∞ ≡
k1 ⋅ k 3
k1 + k 2
Und noch eine weitere Reaktion läßt sich mit einer solchen Formel beschreiben, die
homogene Katalyse, z.B. eine Enzym-katalysierte Reaktion :
1
→
A+ E
AE
←
2
AE + B
→
AB + E
3
Jetzt gilt für K2 :
K2 =
k1 ⋅ E ⋅ k 3 ⋅ B
k1 ⋅ E + k 2 + k 3 ⋅ B
Zuerst soll die Abhängigkeit von K2 von B bei im Überschuß vorhandenem Katalysator
diskutiert werden. Dabei ergibt sich :
k0 =
und
k1 ⋅ E ⋅ k 3
k1 ⋅ E + k 2
k ∞ = k1 ⋅ E
Für K2 folgt damit wiederum
K2 =
k0 ⋅ B
k ⋅B
1+ 0
k∞
Und für die Katalysator-Abhängigkeit bei konstantem B ergibt sich :
k0 =
k1 ⋅ k 3 ⋅ B
k2 + k3 ⋅ B
k∞ = k3 ⋅ B
und
K2 =
k0 ⋅ E
k ⋅E
1+ 0
k∞
Atom-Modelle
Am Ende des 19. Jahrhunderts war man allgemein der Auffassung, alles mechanisch
erklären zu können, also auch die Frage: Wieviel Licht kommt aus dem Loch eines
schwarzen Kastens? Die Beantwortung dieser Frage führte zu den Strahlungsgesetzen
von Stefan-Boltzmann, Wien, Rayleigh-Jeans und Planck. Das Gesetz von Stefan und
Boltzmann besagt :
L=
c0 ⋅a 4
T
4π
d.h.: Die Strahlungsdichte L eines Schwarzen Körpers ist proportional der vierten Potenz
der Temperatur, die im Inneren eines Schwarzen Körpers herrscht. c0 ist die
Lichtgeschwindigkeit.
Das Wien’sche Verschiebungsgesetz ist als Zusammenhang zwischen den Maxima der
Strahlungsdichte bekannt. Für diese gilt die Beziehung :
λmax ⋅T = const ≈ 3000 µm K
Für große Werte von λ ⋅ T zeigen sich Abweichungen vom Wien’schen Verschiebungsgesetz. Hier kann besser das Rayleigh-Jeans-Gesetz
L( λ,T ) =
2 c0 k
λ5
⋅(λ ⋅ T)
angewendet werden, das seinerseits für kleine Werte von λ ⋅ T nicht zutrifft.
Im Jahr 1900 legte Planck eine Strahlungsformel vor, die das Wien’sche Verschiebungsgesetz und das Rayleigh-Jeans-Gesetz als Grenzformen enthält:
L( λ,T ) =
2 c0 ε
λ4
⋅
1
e ε kT − 1
Da die Spektren von Atomen Linien aufweisen, musste Planck annehmen, dass die
Energieaufnahme und -abgabe in dem betrachteten Hohlkörper gequantelt ist. Damit
ergibt sich dann ein einfacher Zusammenhang zwischen der Energie des Lichts und der
Frequenz. Dabei ist h das Planck’sche Wirkungsquantum.
ε = h⋅ν =
h ⋅ c0
h = 6.0 × 10-34 Js
λ
Planck selbst war garnicht glücklich darüber, dass er die Hilfsgröße ‚h‘ einführen musste,
und meinte, dass diese sicher auch noch auf mechanische Größen zurückgeführt werden
wird.
Abbildung 18 : Das Linienspektrum der Balmer-Serie des H-Atoms
Das ‚Werkzeug‘, mit dem man den Aufbau der Materie untersuchen kann, ist die
Spektroskopie. 1885 findet Johann Balmer (Schweizer Lehrer) Die Formel für die
Frequenzen der sichtbaren Linien des Wasserstoff-Spektrums.: Diese Formel wird von
Johannes Rydberg (Schweizer Astronom) verallgemeinert (1890):
ν =
1
λ
1
1
= 109680 2 − 2
n2
n1
Ry
1 1
hν = h ⋅ c0 ⋅ Ry 2 − 2
n1 n2
oder
n 2 > n1
∆E = E1 − E2
Nils Bohr fasste die Ergebnisse der Strahlungs- und Spektroskopieexperimente :
1) Atome bestehen aus Elektronen und Kernen,
2) die Lichtenergie ist gequantelt,
(Rutherford)
(Planck,
Einstein)
3) die Linienspektren entsprechen Termübergängen
(Rydberg, Ritz)
zusammen und stellte 1913 ein hypothetisches Modell vor. Obwohl dieses Modell unbefriedigend ist, da es im Widerspruch zur Maxwell’schen Elektrodynamik steht, hat es sich
doch als ein einfaches und praktikables Modell bis heute erhalten. Insbesondere die
Anordnung der Elemente im Periodensystem kann dadurch erklärt werden.
Die Definition des Auflösungsvermögens eines Mikroskops nach Ernst Abbe hat Werner
Heisenberg verallgemeinert. Er sagte, dass grundsätzlich für die Paare Impuls/Weg bzw.
Energie/Zeit die Unschärfe-Relation gilt:
∆ε ⋅ ∆t≥h
∆x ⋅ ∆p≥h
Im Jahre 1924 wagte Louis de Broglie einen entscheidenden Schritt, der die Entwicklung
der Quantenmechanik auslösen sollte: Er behauptete, dass auch die Materie
Welleneigenschaften besitzt.
λ=
h
m⋅v
Die Schrödinger-Gleichung
Schödinger geht jetzt über die Annahme von Bohr, daß sich die Elektronen auf Bahnen
um den positiven Kern bewegen, hinaus, in dem er dem Konzept der Bahnen das Konzept
der Orbitale entgegensetzt. Orbitale sind Orte der maximalen Wahrscheinlichkeit, ein
Elektron anzutreffen, sagen aber, im Gegensatz zu den Bahnen, nichts über die Bewegungsrichtung der Elektronen aus. Dieses Konzept enthält also die Heisenberg'sche
Unschärferelation, daß nicht gleichzeitig Ort und Impuls (~ Geschwindigkeit) bekannt sein
können.
Während Bohr die Quantenzahlen n und m der Serienformel bestimmten Bahnen zuordnete (und damit bereits bei den Nebenquantenzahlen Schiffbruch erleiden mußte), geben
die heute benutzten Schrödinger'schen Quantenzahlen nur den Energiezustand eines
Elektrons an.
Die Schrödinger-Gleichung kann nicht exakt abgeleitet werden, aber de Analogie zum
Energiesatz der Mechanik kann Einsichten in das Verständnis der Gleichung bringen.
Ersetzt man im Energiesatz der Mechanik
E gesamt = E kin + E pot =
1
⋅ mv 2 + V =
2
den Impuls mv durch den Impulsoperator
Potentialoperator V
ergibt sich
i⋅ ⋅
1
⋅ ( mv ) 2 + V
2m
∂
, die potentielle Energie durch den
∂x
und die Gesamtenergie durch die Energieeigenwerte E
∂2
−
2m ∂x 2
2
+V
, so
=E
Wendet man diese Operatorgleichung auf die Größe Ψ an, so erhält man eine ausführbare Gleichung.
∂2
−
⋅ψ + V ⋅ψ = E ⋅ψ
2m ∂x 2
2
Die Größe ψ, auf die die Operatoren angewendet werden, ist erst einmal beliebig. Sie wird
nur eingefügt, um die Gleichung zu vervollständigen und lösbar zu machen.
Die Ersetzung des Impulses durch den Operator leitet sich aus folgender Überlegung her.
Nach Heisenberg ist :
h = ∆ε ⋅ ∆t =ˆ ∆mv ⋅ ∆x
und damit gilt dann :
∆m⋅v =
h
∆x
oder, wenn 1/∆x durch den Operator ∂ / ∂ x ersetzt wird
h⋅
∂
=ˆ ∆ m ⋅ v
∂x
Die Zustandsfunktion ψ selbst hat keine anschauliche physikalische Bedeutung. Diese
kann sie auch aufgrund ihrer rein mathematisch begründeten Einführung nicht haben. Die
physikalische Bedeutung der Schrödinger Gleichung steckt in den Operatoren. Ψ wurde
nur eingeführt, um die Operator-Gleichung zu vervollständigen. Ψ ist jedoch, ähnlich wie
in der Thermodynamik die Entropie, eine geeignete Größe, mit der gerechnet werden
kann, und die in Kombinationen eine physikalische Bedeutung erhält. Z.B. ist das Quadrat
(in komplexer Schreibweise) gleich der Aufenthaltswahrscheinlichkeit des betrachteten
Partikels :
P = ψ ⋅ψ *
(Es ergibt sich eine Analogie zu der imaginären Einheit i, die in ψ enthalten ist. Auch i hat
keine anschauliche Bedeutung, sein Quadrat ist jedoch eine vorstellbare Zahl : i2 = -1.)
Man kann damit die Schrödinger-Gleichung auch auffassen als eine Gleichung für die Bestimmung
der Aufenthaltswahrscheinlichkeit eines Partikels. Damit ergibt sich nun das grundsätzlich Neue der
Quantenmechanik. Für ein Atommodell heißt dies :
Es wird nicht mehr die Bahn eines Elektrons bestimmt, sondern das zugehörige
Orbital als Ort der maximalen Aufenthaltswahrscheinlichkeit.
Damit ist die Frage: Wie kommt ein Elektron von A
nach B sinnlos, denn hier wird der Orbitalbegriff mit
dem Bahnbegriff gemischt.
Der eindimensionale Potentialtopf
Die Leistungsfähigkeit der Schrödinger Gleichung
soll am Beispiel des eindimensionalen Potentialtopfes demonstriert werden. Der Potentialtopf ist
dadurch definiert, daß im Bereich 0 ≤ x ≤ a das
Potential gleich Null ist, überall sonst dagegen
unendlich.
Damit ergibt sich für die Schrödinger-Gleichung eine Differentialgleichung :
2mE
∂2
⋅ψ = − 2 ⋅ψ = − k 2 ⋅ψ
2
∂x
mit
k2 =
2mE
2
deren partielle Lösung die trigonometrischen Funktionen und allgemein
ψ = A sin(kx ) + B cos(kx )
sind.
Abbildung 18 : Schrödingerfunktion und Aufenthaltswahrscheinlichkeit für den 1-dim.
Potentialtopf.
In Abbildung 18 sind die Wellenfunktion und die Aufenthaltswahrscheinlichkeit für die
untersten Energieniveaus dargestellt. Im untersten Niveau ist die Wahrscheinlichkeit, das
Objekt anzutreffen, in der Mitte des Potentialtopfs am größten. Je größer die Quantenzahl
wird, umso mehr Perioden der Aufenthaltswahrscheinlichkeit passen in den Topf. Das
bedeutet aber, dass die Wahrscheinlichkeit das Partikel anzutreffen, immer weniger
ortsabhängig wird.
Aus den Randwerten
ψ (0) = ψ ( a ) = 0
ergibt sich dann die Lösung für k und damit für die Energieeigenwerte εi :
1)
2)
0 = A sin(0) + B cos(0)
⇒
B≡0
⇒ εi = i2 ⋅
a ⋅ k = i ⋅π
h2
8ma 2
Dies ist die Formel für die Energiezustände einer translatorischen Bewegung in einer
Dimension. In einem dreidimensionalen Raum hat auch die Schrödinger Funktion drei
Dimensionen, genauso wie das Potential und die Energie. Entsprechend muss im
Impulsoperator nach den drei Raumkoordinaten abgeleitet werden und für die Schrödinger Gleichung ergibt sich
∂2
∂2
∂2
Ψ =E Ψ
−
+
+
2m ∂x 2 ∂y 2 ∂z 2
2
Als Ergebnis ergibt sich für die Schrödinger Funktion
Ψges = Ψx Ψy Ψz
und für die Energiewerte
E ges = E x + E y + E z
Die Ψi sind die eindimensionalen Schrödinger Funktion in der entsprechenden Richtung
und für die Energien gilt Analoges.
Die Energie-Niveaus der Rotation
Wir betrachten jetzt ein Teilchen, das sich auf einer
Kreisbahn bewegt, auf der überall das Potential V=0
herrscht. Die zugehörige Schrödinger-Gleichung
lautet :
∂2 ∂2
⋅ψ = E ⋅ψ
−
+
2m ∂x 2 ∂y 2
2
Diese Gleichung entspricht der eines zweidimensionalen Potentialtopfes. Die Lösung
könnte durch Aufspalten der Gleichung nach x und y erhalten werden, wenn nicht die
Kreisbahn
x2 + y2 = r2
vorgeschrieben wäre. Um dieser Einschränkung Rechnung zu tragen, wird zu Polarkoordinaten übergegangen
x = r ⋅ cos φ
y = r ⋅ sin φ
Der Winkel Φ ist hier also variabel und das Potential hängt von r ab. Damit ist der Fall der
Rotation eines starren Körpers auf den Fall des eindimensionalen Potentialtops zurückgeführt.
Der Nabla-Operator geht dabei über in :
∂ ∂
, = ∇ x , y
∂x ∂y
⇒
1
1 ∂
∇φ =
r
r ∂φ
und damit gilt dann für die Schrödinger-Funktion
∂2
−
⋅ψ = E ⋅ψ
2mr 2 ∂φ 2
2
oder umgestellt :
2mr 2 ⋅ E
∂2
⋅
ψ
=
−
= − k 2 ⋅ψ
2
2
∂φ
Die Lösung dieser Differentialgleichung lautet, wie wir gesehen hatten :
ψ = A sin(kφ ) + B cos(kφ )
Nun müssen noch die Randbedingungen eingesetzt werden :
1. Ψ(2π) = Ψ(0) = 0
und
2. Ψ(Φ+2π) = Ψ(Φ)
Damit die erste Randbedingung erfüllt ist, muß gelten :
0 = A sin(j∗0) + B cos(j∗0)
oder B = 0
Der Parameter j entspricht dem Parameter k aus der Gleichung für den Potentialtopf.
Die zweite Randbedingung ergibt dann
Ψ(Φ+2π) = A sin(kΦ+2kπ) =
= A {sin(jΦ) cos(2jπ) + cos(jΦ) sin(2jπ)} =
= A sin(jΦ)
(nach Voraussetzung)
Das gilt für
2 j π = 0, 2 π, 4 π, ...
also
j
= 0, 1, 2, ...
und damit wird für die Energieeigenwerte die folgende Formel erhalten
2mr 2 ⋅ E
= j2
2
oder
E=
2
2mr
2
⋅ j2
Bisher haben wir den starren Rotator betrachtet, bei dem eine Masse m auf einer Kreisbahn des Radius r umläuft. Moleküle dagegen sind freie Rotatoren, bei denen mehrere
Massenpunkte sich um eine Achse durch den Schwerpunkt drehen. In diesem Fall ergibt
sich bei genauerer Betrachtung mit der Rotationsquantenzahl J :
E = J ⋅ ( J + 1) ⋅
2
2mr 2
Das Elektron im Coulomb-Feld
Ein Elektron, das sich im Coulomb-Feld eines Z-fach
geladenen Kerns aufhält, erfährt ein Potential der
Größe
Ze 2 1
V (r ) = −
⋅
4πε 0 r
Anstelle der Masse m eines Teilchens muss die reduzierte Masse µ aus Kern und
Elektron eingesetzt werden :
1
µ
=
1
1
1
+
≈
mK mE
mE
Somit hat die Schrödinger-Gleichung also folgende Form :
2
Ze 2 1
−
⋅∇ ψ −
⋅ ⋅ψ = E ⋅ψ
2µ
4πε 0 r
2
In Polarkoordinaten gilt für die Operator ∇2 :
∂2
∂
1 ∂2 1 1
1
∇ = ⋅ 2 + ⋅ 2 ⋅ 2 +
⋅
r ∂r
r sin ϑ ∂φ
sin ϑ ∂ϑ
2
∂
⋅ sin ϑ ⋅
∂φ
Zur Lösung der Schrödinger-Gleichung separieren wir die Wellenfunktion in einen Teil, der
nur vom Radius abhängt und eine Funktion, in die die Winkel eingehen.
ψ = ψ r ⋅ψ ϑ , φ
Die Lösungen für die winkelabhängige Funktion sind Kugelfunktionen, auf die hier nicht
näher eingegangen wird. Sie ergeben die Form der Orbitale abhängig von den Nebenquantenzahlen.
Für den Radius-abhängigen Teil gilt :
Ze 2 1
∂2
−
⋅
⋅ψ r −
⋅ ⋅ψ r = E ⋅ψ r
2 µr ∂r 2
4πε 0 r
2
Nach Einsetzen der Randbedingungen erhält man für die Energie-Eigenwerte :
1
Z 2 ⋅ e4
E =− 2⋅
n 32 ⋅ π 2 ⋅ ε 02 ⋅
2
1 Z 2 ⋅ e4
=− 2⋅
n 8 ⋅ ε 02 ⋅ h 2
Für die Energiedifferenz zwischen einem Niveau n und einem anderen m ergibt sich die
Rydberg-Formel :
Z 2 ⋅ e4 1
1
∆E =
⋅
− 2
2
2 2
8 ⋅ε0 ⋅ h n
m
also die Beschreibung der Serien-Spektren der Wasserstoff-ähnlichen Atome.
Der Tunneleffekt
Als nächstes wollen wir die Wellenfunktion eines Teilchens im konstanten Potentialfeld
betrachten. Wir beschränken uns wieder auf eine Dimension :
∂2
−
⋅
⋅ ψ + V ⋅ψ = E ⋅ ψ
2 m ∂x 2
2
Da V konstant ist, können wir es mit dem (ebenfalls konstanten) Energie-Eigenwert
zusammenfassen :
∂2
−
⋅
⋅ ψ = (E − V ) ⋅ ψ
2 m ∂x 2
2
Die Lösung dieser Differentialgleichung kennen wir schon, sie lautet :
ψ = c ⋅ e ik x
mit
k2=
(E − V ) ⋅ 2m
2
also :
ψ = c ⋅ e i⋅
( E −V )⋅2 m
2
⋅x
= c ⋅ ei⋅2π x λ
wobei die Wellenlänge λ gegeben ist durch
λ =
h
2 m ⋅ (E − V )
Je größer V wird, um so größer wird also auch λ. Überschreitet V den Energie-Eigenwert
E, so wird der Wert unter der Wurzel positiv und damit α nicht mehr imaginär. Ψ ist dann
eine abklingende Exponentialfunktion :
ψ = c ⋅ e−
(V − E )⋅2 m
2
⋅x
Liegt jetzt eine Energie-Barriere von endlicher Höhe vor, so könnte ein Teilchen, das der
klassischen Theorie gehorcht, diese nicht überschreiten, da ihm die Energie dazu fehlt.
Quantenmechanisch betrachtet hat das Teilchen jedoch durchaus noch eine endliche
Wahrscheinlichkeit, auf der Rückseite der Barriere angetroffen zu werden, es "tunnelt"
also durch den Energieberg.
Der Tunneleffekt zeigt sich bei vielen spektroskopischen Beobachtungen und findet seine
praktische Anwendung in der Halbleitertechnik (Tunneldiode) und bei der Raster-TunnelElektronenmikroskopie.
1. Rechenbeispiel
Gesucht ist die Aufenthaltswahrscheinlichkeit eines Elektrons in einem Potentialtopf von
0.3 nm Länge, sowie die Energieeigenwerte dieses Problems. Wann ist die Energie gleich
k T300K ?
a = 3 ×10 −10 m
⇒
2
i ⋅ π 10
P = 1010 ⋅ sin 2
10 x
3
a
m=9.1×10 −31 kg
h = 6.6 × 10−34 Js ( Js=kg m 2 s −1 )
h2
En = i ⋅
8ma 2
2
=i
(6.6 ×10 )
⋅
8 ⋅ 9.1×10 ⋅ (3 × 10 )
−34 2
2
−10 2
−31
kg 2 m 4 s −2
kg m 2
43.6 ×10 −68
=i ⋅
kg m 2 s −2
−51
655.2 ×10
2
= i ⋅ 0.0665 ×10 −17 kg m 2 s −2
2
= i 2 ⋅ 6.65 ×10 −19
J
Die thermische Energie bei 300 K beträgt:
k = 1.38 × 10−23
JK −1
E = k ⋅ T = 414 ×10 −23 = 4.14 ×10 −21
J
D.h. die mittlere thermische Energie eines Teilchens reicht nicht aus, um ein Elektron
von n = 1 auf n = 2 zu bringen:
4.14 × 10 −21 J < 6.65 × 10 −19 J
Damit gilt für die Aufenthaltswahrscheinlichkeit, daß sich das Elektron bevorzugt im
mittleren Bereich des Potentialtopfs aufhält, da i = 1 ist.
2. Rechenbeispiel
Wie groß sind die Energieeigenwerte eines Stickstoffmoleküls in einem Zimmer (a = 6m) ?
m = 28 g 6 × 1023 = 4.7 × 10−23 g = 4.7 × 10−26 kg
En
h2
2
= n ⋅
2
= n ⋅
8m a 2
43.6 × 10 −68
8 ⋅ 4.7 × 10 −26 ⋅ 36
kg m 2 s −2
= n 2 ⋅ 3.2 × 10 −44 J
Bei 300 K ist damit die Quantenzahl n:
kT300
= 4.41 × 10 −21 J = n 2 ⋅ 3.2 × 10 −44 J
n
oder
n
2
=
=
4.14 × 10 −21
3.2 × 10 −44
13 × 10 22
= 1.3 × 10 23
= 3.6 × 1011
Das heißt aber, daß in die 6m Zimmerlänge 3.6×1011 Perioden hineinpassen, also
daß quasi die Aufenthaltswahrscheinlichkeit überall gleich groß ist.
d = 6m 3.6 ×1013 = 1.6 × 10 −13
m << Φ N 2 = 3.15 ×10 −10 m
3. Rechenbeispiel
Wie groß sind die Energieeigenwerte der Rotation von O2 um eine Achse senkrecht zur
Bindung bei Raumtemperatur ?
Die Masse des Sauerstoffmoleküls beträgt
m
= 32 g 6 × 10 23
=
5.3 × 10 −26 kg
Bei einer Bindungslänge von 2,6 A ist der Radius der Hantel
r
= 1.3 A = 1.3 × 10 −10 m
Für die Energie-Eigenwerte gilt damit :
Eℑ = ℑ( ℑ + 1)
43.9 × 10 −68
h2
(
)
1
=
ℑ
ℑ
+
8 ⋅ π 2 ⋅ 5.3 ×10 −26 ⋅1.69 ×10 −20
8π 2 mr 2
Eℑ = ℑ( ℑ + 1)⋅3.6 ×10 −23
[J ]
Die termische Energie beträgt bei 300 K
k ⋅ T300 = 4.14 × 10 −21 J
Also
4.14 × 10 −21 = ℑ( ℑ + 1)⋅ 3.6 × 10 −23
ℑ( ℑ + 1) ≈ 115
oder ℑ ≈ 11
Bei Zimmertemperatur ist also die Rotation des Sauerstoffmoleküls um eine Achse
senkrecht zur Bindung angeregt.
4. Rechenbeispiel
Wie groß ist die Energie, die benötigt wird, um ein Sauerstoff-Molekül um seine
Bindungsachse rotieren zu lassen ?
-26
kg, aber der Radius der
Die Masse des O2-Moleküls ist wieder gleich 5.3×10
Drehbewegung ist jetzt viel kleiner als im ersten Beispiel.
r = 1.2×10-15
3
M
[m]
mit M=32 als Molekulargewicht des Sauerstoffs, also ist r = 4.76×10-15 m.
Damit wird selbst für J = 1 die Anregungsenergie sehr groß :
43.9 × 10 −68
E = 1⋅ 2 ⋅ 2
= 9.24 × 10 −15
− 26
− 30
8π ⋅ 5.3 × 10 ⋅ 22.7 × 10
[J ]
Bei 300 K war die termische Energie 4.14×10-21 J, um eine Anregungsenergie von
9.24×10-15 J zu erreichen, müßte die Temperatur 2×106 K betragen. Da so hohe Energie
nicht aufgebracht werden können, wird häufig davon gesprochen, daß ein lineares
Molekül nur zwei Freiheitsgrade der Rotation besitzt. Richtiger wäre es, zu sagen, daß nur
zwei termisch anregbare Freiheitsgrade gibt.
5. Rechenbeispiel
Es soll das Ionisationspotential von atomarem Wasserstoff und von Natriumatomen
berechnet werden.
Hierzu wird die Rydberg-Formel benötigt. Die Rydberg-Konstante R0 ergibt sich zu
e4 ⋅ µ
(1.60 ×10 −19 As ) 4 ⋅ 9.11×10 −31 kg
R0 = 2 2 =
= 2.179 ×10 −18 J
−12
2
−34
2
8ε 0 ⋅ h
8 ⋅ (8.85 ×10 As / Vs) ⋅ (6.63 × 10 Js)
Für Wasserstoff ist die Ladungszahl gleich 1 und die Bahn-Quantenzahl m ist ebenfalls
gleich 1. Für eine Ionisation muß das Elektron von der Bahn m=1 auf das Niveau
n= ∞ angehoben werden. Damit ergibt sich für die Ionisationsenergie
1 1
E Ionisation = R0 − = 2.179 × 10 −18 J = 13.60eV
∞ 1
Dabei wurde eingesetzt, daß 1J = 6.24×1018 eV ist. Der gemessene Wert beträgt 13.614
eV. Für andere Atome ist die Übereinstimmung nicht so gut, wie am Beispiel des Natriums
demonstriert werden soll.
Für Natrium ist die Bahn-Quantenzahl m=3. die Kernladungszahl ist 11, aber diese
Kernladung ist durch 10 Elektronen abgeschirmt. Die effektive Kernladungszahl ist also 1.
Damit ergibt sich dann
1 1 1
E Ionisation = 1 ⋅ R0 − 2 = ⋅ 2.179 × 10 −18 J = 1.51 eV
∞ 3 9
Der Tabellenwert für Natrium beträgt aber 5.14 eV., es bleibt also nur anzunehmen, daß
die effektive Kernladungszahl etwa 1.7 beträgt. Dies kann erklärt werden, wenn
berücksichtigt wird, daß die Abschirmung durch die Orbitale nicht vollständig ist.
Molekül - Spektren
Um die Natur der chemischen Bindungen zu verstehen, kann das Problem eines
Elektrons im Feld zweier geladener Kerne in einer klassischen Betrachtungsweise
herangezogen werden. Das System aus zwei positiv geladenen Kernen ist instabil, da sich
die Kerne aufgrund der Coulomb-Kräfte abstoßen :
F~
q1 ⋅ q2
r122
bzw. V ~
q1 ⋅ q2
r12
Diese Kraft ist positiv, d.h. sie ist abstoßend. Bringen wir jetzt ein Elektron hinzu, so wird
die potentielle Energie V erweitert zu :
V ~
q1 ⋅ q2 q1 ⋅ qe qe ⋅ q2
+
+
r12
r1e
re 2
Wenn die Ladungen alle gleich groß sind (q), so gilt
1
1
1
V ~ q 2 ⋅ −
−
r12 r1e re 2
Da sowohl r1e, als auch re2 kleiner als r12 sind, ist das Potential ist negativ und somit das
System stabil.
Befindet sich das Bindungselektron nicht auf der Verbindungslinie der beiden Kerne, so
ändert sich an der obigen Überlegung nichts. Die Coulomb-Kräfte lassen sich jetzt
aufspalten in Komponenten entlang der Kernverbindungslinie und solchen senkrecht
dazu. Für die zum Kernabstand parallelen Kräfte gilt das oben gesagte, die senkrecht
dazu stehenden Kräfte sind wegen der ungleichnamigen Ladungen von Kern und Elektron
immer anziehend.
Schwingungsspektren
Es soll jetzt der Fall betrachtet werden, daß auf das
untersuchte Teilchen eine rücktreibende Kraft nach
dem Hook'schen Gesetz wirkt :
F = Kx
V = F * x ~ x2
Nun setzt man dieses Potential in die Schrödinger-Gleichung ein.
∂2
−
Ψ + Kx 2 ⋅ Ψ = E ⋅ Ψ
2
2m ∂x
2
Die zugehörigen Energie-Eigenwerte ergeben sich dann aus der Lösung der SchrödingerGleichung zu :
1
2
ε v = v + ⋅ hv
mit
v2 =
K
m
wobei K die Kraftkonstante aus dem Hook’schen Gesetz ist. Anders als im Fall der Translation und Rotation enthält die Energie hier ein absolutes Glied 1 2 hν . Dies hat als
Konsequenz, dass auch am Temperatur-Nullpunkt die Moleküle nicht ruhen, sondern
entsprechend ihrer Grundfrequenz schwingen.
Bisher haben wir ein Diatom betrachtet, das nur eine Schwingung ausführen kann. Wird
ein mehratomiges Molekül schwingungsangeregt, so wabbeln aufgrund der Kopplung
zwischen den Schwingungen seine Bausteine herum wie Götterspeise. Für die Bewegungen der Atome gibt es keine Vorzugsrichtung, es sei denn aufgrund von sterischen
Hinderungen. Um Ordnung in diese chaotischen Bewegungen zu bringen, kann jede
Vibration auf einen Satz von Normalschwingungen abgebildet werden. Die tatsächlichen
Bewegungen der Atome ergeben sich dann als Überlagerung (Linearkombination) der
Normalschwingungen.
Die Quantenzahlen
Wir haben jetzt alle Energie-Eigenwerte zusammen :
1 Z 2 me 4
= 2⋅ 2 2
n 8ε 0 h
elektron. Anregung
ε el
Vibration
ε v = v + ⋅ hv
1
2
Rotation
ε J = J ⋅ (J + 1) ⋅
Translation
εi = i2 ⋅
h2
8π 2 I
h2
8ma 2
Die elektronische Anregung benötigt dabei die meiste Energie (3-6 eV, UV-Strahlung),
während Schwingungen durch IR-Strahlung (0.1-1 eV) angeregt werden. Die Rotationsübergänge liegen im Bereich der Mikrowellen-Strahlung. Die atomare Einheit 1 eV
entspricht 1.6*10-19 J oder 96.5 kJ/Mol. Für die Umrechnung in Wellenlängen kann man
sich merken : E [eV] * λ[nm] = 1200
Die laufenden Zahlen n, v, J und i werden als Quantenzahlen bezeichnet. Es gibt genau
drei Quantenzahlen der Translation (i,j,k) und der Rotation (Jx, Jy, Jz) aufgrund der drei
Raumrichtungen. An Quantenzahlen der Vibration (vi) gibt es so viele wie es Normalschwingungen im Molekül gibt.
Für die Quantenzahlen der elektronischen Anregung gehen wir noch einmal zurück zu den
Atomen. Aus der Radius-abhängigen Eigenfunktion ergab sich eine Hauptquantenzahl n.
Da das Coulomb-Potential kugelsymmetrisch ist, hatten wir die Winkel-abhängige
Eigenfunktion separieren können. Sie führt zu zwei weiteren Quantenzahlen l und m :
n
l
m
=
=
0,
= -l, -l+1, ..., 0, ... , l-1, l
1,
1,
2,
2,
3,
...
,
...
(n-1)
l ist die Nebenquantenzahl und m die Magnetische Quantenzahl. m tritt immer dann auf,
wenn eine Vorzugsrichtung (z.B. durch ein elektrisches oder magnetisches Feld) gegeben
ist und dadurch Entartungen aufgehoben werde. Anstatt ‚Nebenquantenzahl‘ sollte man
nach der Einführung der Orbitale besser ‚Formquantenzahl‘ sagen, denn l bestimmt das
Aussehen der Orbitale.
Abbildung 21 : Die Form der Orbitale der Schalen n=1 und n=2.
Vor der quantenmechanischen Klärung der Spektren, hatte man die Serien durch ihre
Eigenschaften (sharp, principal, diffuse, fine) unterschieden. Diese Unterscheidungsmerkmale werden heute den Elektronenorbitalen zugeordnet. So bezeichnet man Elektronen
auf dem Orbital der Nebenquantenzahl l=0 als s-Elektronen, usw. :
l=0
l=1
l=2
l=3
:
:
:
:
s
p
d
f
sharp
principal
diffuse
fine
Im Molekül addieren sich die Quantenzahlen vektoriell und werden dann mit Großbuchstaben geschrieben. Die Molekül-Orbitale bezeichnet man entsprechend mit griechischen
Buchstaben.
Es gibt noch eine weitere Quantenzahl, die Spinquantenzahl 1/2. Auf jedes Energieniveau
passen genau zwei Objekte, die durch ihren Spin unterschieden werden. Im Spektrum
führt diese Tatsache zur Aufspaltung der Linien
Näherungsmethoden für Molekül-Orbitale
LCAO-Methode
Nachdem jetzt alle Möglichkeiten eines Teilchens, Energie aufzunehmen, besprochen
sind, wollen wir uns den Molekülorbitalen zuwenden. Die Berechnung der Molekülorbitale
führt auf ein Vielteilchenproblem, das gar nicht oder nur mit großem Aufwand zu bewältigen ist. Daher wurden Näherungsmethoden entwickelt, von denen hier die LCAOMethode vorgestellt werden soll. (Linear Combination of Atomic Orbitals)
Hierbei werden die Atomorbitale eines Moleküls ohne Verformung einander überlagert.
Damit treten zwei Möglichkeiten der Überlagerung auf : Die Addition der Orbitale und ihre
Differenz. Bei der Addition
ψ M = ψ A +ψB
entstehen im Normalfall bindende Molekülorbitale, bei der Subtraktion antibindende Orbitale :
ψ M = ψ A −ψ B
Abbildung 22 : Überlagerung von s und p Orbitalen.
Als Beispiel werden in Abbildung 22 die 1s-Orbitale (n=1/l=0) des Wasserstoff-Atoms in
einem H2-Molekül überlagert. Die zugehörige Wellenfunktion lautete
ψ n = a ⋅ r n ⋅ e − br
wobei die Parameter a und b von den Nebenquantenzahlen l und m abhängen. (In
unserem Fall sind beide Quantenzahlen gleich 0.) Bindende und antibindende Molekülorbitale zeichnen sich dadurch aus, daß ihre Energien kleiner bzw. größer als die Summe
der Energien der Atomorbitale sind.
In der rechten Hälfte der Abbildung 22 wird demonstriert, wie p-Orbitale die bindenden
und antibindenden Π-Orbitalen des Moleküls bilden.
Elektronengas
Ein zweites Beispiel für die LCAO-Methode ist die Überlagerung der
π-Elektronen
von
aufeinanderfolgenden C=C-Bindung. Die bindenden Orbitale bilden dabei eine "Elektronenwolke" über der C=C-Bindung. Reiht man mehrere C=C-Bindungen aneinander, so
entsteht über das ganze Molekül ein einziges langgestrecktes Orbital für den bindenden
Fall. Die Elektronen verhalten sich dann so, als ob sie sich in einem Potentialtopf der
Länge k⋅a (a = Bindungslänge und k = Anzahl der C-Atome) befänden. Ihre Energieeigenwerten gehorchen dabei der Formel für Teilchen in einem Potentialtopf :
h2
εi = i ⋅
2
8m ⋅ (ka )
2
Dies ist analog den Energieniveaus von Gasmolekülen in einem vorgegebenen Volumen.
Man spricht daher in diesem Fall auch von einem Elektronengas.
Morse-Potential
Die LCAO-Methode ist ein Näherungsverfahren, das für organische Moleküle zu recht
guten Ergebnissen führt, für kleine Moleküle jedoch nur begrenzt anwendbar ist. Für
kleine Moleküle läßt sich das Vielteilchenproblem jedoch auf andere Weise lösen. Für
Diatome erhält man in guter Näherung die Morse-Kurve
ε = De ⋅ (1 − e − β (r −r ) )
0
2
Die Morsekurve setzt sich aus einem abstoßenden Teil und einem anziehenden Ast
zusammen. In der Nähe des Minimums entspricht die Kurve etwa einer Parabel
ε r ≈ De (1 − (1 − β (r − r0 )))2 = De β 2 (r − r0 )2
0
Hier liegt eine harmonische Schwingung vor, da die Schwingungsenergie der potentiellen
Energie einer klassischen, harmonischen Schwingung eines Pendels oder einer Feder
entspricht. Die Energieniveaus der Vibration hatten wir auch mit dem Potential einer
harmonischen Schwingung abgeleitet. Daher haben die Energieniveaus auch immer den
gleichen Abstand hν.
Die Näherung des harmonischen Oszillators gilt aber nur für kleine Schwingungsquantenzahlen. Werden die Auslenkungen größer, so sind die Schwingungen nicht mehr harmonisch, es liegt dann der anharmonische Oszillator vor, bei dem die Abstände der
Schwingungsniveaus mit zunehmender Quantenzahl geringer werden.
Die Abstände werden nicht nur geringer, ab einem Grenzniveau gibt es keine Schwingungen mehr. Da die Dissoziationsgrenze erreicht ist, gehen die Schwingungen in Translationsbewegungen über. Die Schwingungsamplitude wird so groß, dass man nicht mehr
davon sprechen kann, dass die Atome zusammengehören. Hier gibt es also nur eine
endliche Zahl von Vibrtionsniveaus.
Für r ⇒ ∞ , d.h. bei der Separation der Atome, ist die Energie ε gleich De. Da das
Molekül jedoch bereits im Grundzustand die Nullpunktsenergie 1 2 ⋅ hv besitzt, ist die
zur Dissoziation nötige Energie :
D0 = De − 1 2 ⋅ hv
Abbildung 23 : Ausschnitt aus dem Potentialdiagramm des Sauerstoffmoleküls
Elektronenübergänge benötigen etwa 10-15sec, eine Schwingungsdauer liegt dagegen im
Bereich von 10-12sec. Man darf also in einem Potentialdiagramm die Übergänge als
senkrechte Striche einzeichnen (Franck-Condon-Prinzip). Berücksichtigt man noch die
Aufenthaltswahrscheinlichkeit der Schwingung (in der Mitte für kleine Quantenzahlen, an
der Rändern für große), so kann man aus einem Potentialdiagramm ablesen, welche
Übergänge möglich sind, da nur senkrechte Übergänge zwischen den maximalen
Aufenthaltswahrscheinlichkeiten möglich sind.
1. Rechenbeispiel : Rotationsspektren
Aufgabe : Im Mikrowellenspektrum des 12C16O findet sich eine Absorptionsbande für den
Übergang von J=0 nach J=1 bei 3.84235 cm-1. 13C16O besitzt eine entsprechende Bande bei 3.6337 cm-1. Die Bindungslängen der beiden Moleküle
sind zu berechnen.
Lösung :
Die Energieeigenwerte der Rotation sind gegeben durch :
E rot =
2
2I
⋅ J ⋅ (J + 1)
mit I = m ⋅ r
Die Auswahlregel für die Übergänge lautet
∆J = ± 1
Für J = 0
ist
Für den Übergang
E
0
rot
=0
0 →1
,
und für
J=1
erhält man somit für
1
0
hcv~0,1 = E rot
− E rot
=
gilt
1
E rot
=
2 2
2I
∆Erot = hν = h c ν~
2
I
und damit
I =
2
h
=
~
hcv0,1
4π 2 v~c
Für die Rotationsbande von 12C16O erhält man also
mit
h=6.6262*10-34 Js
c=2.9979*108 ms-1 und
ν~ =3.84235*102 m-1 :
I1 = 1.45709 * 10-46 kg m2
Entsprechend für 13C16O :
I2 = 1.52412 * 10-46 kg m2
2
Das Trägheitsmoment einer (klassischen) Hantel mit ungleich schweren Atomen ist
gegeben durch
I = m1r12 + m2 r22 = µ ⋅ a 2
wobei die Bindungslänge a = r1 + r2 und die reduzierte Masse µ = (m1m2 ) (m1 + m2 )
gesetzt ist. Wegen der Hebelgesetzen gilt auch m1 ⋅r 1 = m2 ⋅ r2
Somit ergibt sich für 12C16O :
µ1 =
12 ⋅ 16
= 6.857g
12 + 16
und damit
I
a =
µ
=
1.4571 ⋅ 10 −46 ⋅6.022 ⋅ 10 26
6.857
a = 1.1313 ⋅ 10 −10 m = 1,1313 Å
Entsprechend gilt für 13C16O :
µ2 =
13 ⋅ 16
= 7.1724 g
13 + 16
a = 1,1313 Å
Die Bindungslängen beider Isotope sind also im Rahmen der Meßgenauigkeit gleich.
2. Rechenbeispiel : Die Normalschwingungen des NO2
Für das NO2-Molekül sind zwei Anordnungen der Atome möglich : linear oder gewinkelt.
Die dazugehörigen Normalschwingungen sind in der Abbildung dargestellt. Für ein dreiatomiges Molekül sind vier Normalschwingungen möglich, wobei eine davon zweifach
entartet ist, d.h. zwei Schwingungen besitzen die gleiche Frequenz und damit die gleichen
Energieniveaus.
Um jetzt experimentell zu entscheiden, welches der beiden Modelle richtig ist, überprüft
man die Infrarot-Aktivität der Schwingungen und vergleicht das Ergebnis mit der Anzahl
der beobachteten IR-Absorptionslinien. Ein Photon kann nur dann von einem Molekül
aufgenommen werden, wenn sich dabei dessen Dipolmoment ändert. Aus Symmetriegründen ist dies für jede Streckschwingung eines linearen Moleküls nicht möglich. Damit
dürften bei einer linearen Anordnung der O-N-O Atome nur zwei Absorptionen im
Infrarotspektrum auftreten. Man beobachtet jedoch folgende drei IR-Absorptionen des
NO2-Moleküls :
ν~ = 750 cm-1
= 1323 cm-1
= 1616 cm-1
Somit kann allein durch die optische Spektroskopie geschlossen werden, daß das NO2Molekül gewinkelt sein muß.
Abbildung 24 : Mögliche Schwingungen des NO2
3. Rechenbeispiel : Das Rotationsschwingungsspektrum von HI
Jodwasserstoff
absorbiert im Bereich um
4.5 ⋅ 10 m = 4.5µm . Dieser Bereich ist typisch
für Schwingungsübergänge. Dem Schwingungsübergang v=0 nach v=1 sind Rotationsübergänge überlagert, aus denen man die Molekülparameter Bindungslänge und Kraftkonstante
ableiten kann. Dies soll anhand eines Beispiels
erläutert werden :
−6
Aufgrund der Auswahlregeln, die hier nicht abgeleitet wurden müssen, gilt :
∆J = ± 1
d.h. beim Übergang von v=0, J=0 nach v=1 muss damit J=1 erreicht werden. Dieser
v = 2242.2 cm -1 . Das Niveau v=1, J=1 kann aber auch
Übergang hat die Wellenzahl ~
mit dem Übergang ∆J = − 1
aus v=0, J=2 erreicht werden. In diesem Fall beträgt die
-1
~
Wellenzahl v = 2203.6 cm . Aus diesen beiden Wellenzahlen folgt ein Abstand der
Niveaus v=0, J=0 und v=0, J=2 von ν~ =38.6 cm-1. Die zugehörige Energie wird gemäß
E rot = J ⋅ ( J + 1) ⋅
h2
8π µa
2
2
= h v~ c
berechnet. Die Rotationskonstante B ist definiert durch :
ν~
h
=
B=
8π 2 cµa 2 J ( J + 1)
Für den Energieabstand zwischen v=0, J=0 und v=0, J=2 ergibt sich wegen J=2 und
J(J+1)=6 eine Rotationskonstante von 6.433 cm-1. Aus dieser Rotationskonstanten lässt
2
sich dann das Trägheitsmoment I berechnen und wegen I = µ ⋅ a auch der Kernabstand r ( µ ist die reduzierte Masse ) :
I =
µ=
h
= 4.351 ⋅ 10 −47 kg m 2
8π 2 cB
m I ⋅ mH
= 1.6594 ⋅ 10 −27 kg
m I + mH
a = 1.619 ⋅ 10 −10 m = 1.619 Å
Dieser Kernabstand gilt für das unterste Schwingungsniveau. Für den ersten angeregten
Zustand kann man eine entsprechende Auswertung des Spektrums durchführen, man erhält dann einen Kernabstand von
a = 1.642 Å
Die Kraftkonstante K ergibt sich aus der Beziehung
1
K
v = v~ ⋅ c =
⋅
2π
µ
K = 293 Nm-1
also
Bei einem klassischen Pendel oder einer schwingenden Feder ist bei maximaler Auslenkung xmax die Gesamtenergie gleich der potentiellen Energie :
hν = K x2
aus
Epot = x F = x K x
Daraus ergibt sich dann eine maximale Auslenkung
xmax = 0.122 Å
Für den ersten schwingungsangeregten Zustand findet man entsprechend
xmax = 0.211 Å
Während in den beiden Schwingungszuständen v=0 und v=1 die Kernabstände (Mittelwerte!) also fast gleich sind, ist die maximale Auslenkung im schwingungsangeregten
Zustand fast doppelt so groß wie im Grundzustand. Dies ist der Grund dafür, dass mit
wachsender Temperatur das Kovolumen der Gase zunimmt. Je höher die Temperatur ist,
um so mehr Teilchen befinden sich im angeregten Zustand und beanspruchen
esprechend mehr Platz. Das Kovolumen ist dann der Mittelwert aller Moleküle eines Mols :
b = < NA*VMolek..>
Statistische Thermodynamik
Die Zustandssumme
Bei der Berechnung der Energieeigenwerte der Translation lautete das Ergebnis :
ψ = ψ 0 ⋅ e − ikx = A ⋅ sin (kx )
mit k =
i ⋅π
a
und ε =i 2 ⋅
h2
8ma 2
Dies galt für den eindimensionalen Potentialtopf, für den dreidimensionalen Fall multiplizieren sich die Schrödinger-Funktionen :
ψ ges = ψ x ⋅ψ y ⋅ψ z
und entsprechend gilt dann :
ε = (i x2 + i y2 + iz2 )⋅
h2
8ma 2
Aufgrund der Summenbildung kann es vorkommen, daß Teilchen mit verschiedenen
Quantenzahlen gleiche Energie besitzen :
z.B.
ε=
ε=
ε=
i = {1, 2, 3}
i = {2, 1, 3}
i = {3, 2, 1}
1 + 4 + 9 = 14
4 + 1 + 9 = 14
9 + 4 + 1 = 14
⋅ h 2 8ma 2
usw.
Man spricht in diesem Fall von einer Entartung der Energiezustände. Diese Entartung
muß berücksichtigt werden, wenn die Besetzungswahrscheinlichkeit der Energiezustände
berechnet werden soll. Man darf bei der Summierung also nicht jeden Energiezustand
einfach nehmen, sondern muß mit der Entartung wichten.
Die Besetzungswahrscheinlichkeit der Energieniveaus gibt an, wieviele Teilchen sich in
einer Energiestufe befinden :
fi =
Ni
=
N ges
e −ε i
∑e
j
kT
−ε j kT
Die Abhängigkeit von einer Exponentialfunktion ergibt sich aus der Statistik und Kombinatorik der Möglichkeiten zur Anordnung von n Teilchen auf m Energieniveaus unter
Einschluß des Pauli-Prinzips. Das Pauli-Prinzip besagt, dass jedes Teilchen einen
eigenen Satz von Quantenzahlen hat und dass zu jedem Satz von Quantenzahlen immer
nur ein Objekt gehören kann.
Gehört nun zu einem Energiewert εi mehr als ein Zustand, d.h. ist der Zustand also
entartet, so muß die Entartung gi in die Formel eingehen :
fi =
g i ⋅ e −ε i
∑g
j
⋅e
kT
−ε j kT
j
In Abbildung 26 ist die Besetzung der untersten Niveaus eines harmonischen Oszillators
dargestellt. Die Temperaturen sind dabei so gewählt, dass kT einmal der Schwingungsenergie entspricht, einmal dem Dreifachen und einmal ein Drittel dieser Energie.
Abbildung 26 : Besetzung der untersten Niveaus eines harmonischen Oszillators.
− ε kT
Die Proportionalität zu e i
folgt analog der Boltzmann-Funktion, wo ein solcher
Faktor ja auch in die Verteilungsfunktion eingeht. Es muß allerdings hier darauf hingewiesen werden, daß jetzt die Energiezustände gequantelt sind, während wir bei der
Ableitung der Boltzmann-Funktion von einem kontinuierlichen Energiespektrum der
Translation ausgegangen waren.
Daher wird bei der Berechnung der mittleren Energie eines Teilchens auch nicht integriert,
sondern es wird die Summe über alle (abzählbar unendlich viele) Energiezustände
gebildet :
ε ⋅f
ε=∑
∑f
i
j
i
ε ⋅ g ⋅e ε
∑
=
ε
∑g ⋅e
i
−
i
j
kT
kT
i
−
j
Von der mittleren Energie eines Teilchens des Emsembles kommt man durch Multiplikation mit der Avogadro-Zahl NA zur Energie für 1 Mol der Teilchen. Dabei gilt auch : Die
mittlere Energie eines Teilchens ist gleich dem Mittelwert der Energie von vielen Partikeln.
Die Summe im Nenner enthält alle Information über die Energiezustände eines Systems
von Teilchen. Da wir uns in der Thermodynamik vor allem für die Energie eines Systems
interessieren ist diese Summe von bersonderer Bedeutung. Sie erhält den Namen
„Zustandssumme Q“ (oder englisch ‚partion function’, was besser den Sinn dieser Größe
ausdrückt).
Q=
− ε i kT
Der Faktor ε i ⋅ g i ⋅ e
vereinfachen. Wegen
∑g
i
⋅ e −ε i
kT
im Zähler des Energiemittelwerts läßt sich noch weiter
∂
(
ln ∑ g i ⋅ e −ε
∂T
i
kT
)=
=
1
∑ g i ⋅ e −ε i
1
∑ g i ⋅ e −ε i
kT
kT
⋅
∂
∂T
∑g
i
⋅ e −ε i
kT
ε
⋅ ∑ i 2 ⋅ g i ⋅ e −ε i
kT
=
kT
ε
=
2
kT
folgt für die Energie eines Mols von Teilchen :
E = N A ⋅ ε = kT 2 ⋅
∂
⋅ ln Q N
∂T
Damit ist die aus der klassischen Thermodynamik bekannte Größe ‚Energie‘ mit der
statistischen Größe ‚Zustandssumme‘ verknüpft. Die Statistische Thermodynamik
verbindet die makroskopisch bestimmbaren Größen der Thermodynamik mit den
Energieniveaus und ihren Besetzungswahrscheinlichkeiten, die aus der quantenmechanischen Betrachtung der Atome und Moleküle bestimmt werden.
Der Energieinhalt von Molekülen
Wir gehen jetzt zurück zum 1. Hauptsatz der Thermodynamik. Die Gesamtenergie des
Systems war die Enthalpie H :
H = U + p ⋅V
Der Term p ⋅V ergibt sich aus den Wechselwirkungen der Teilchen untereinander. (Bei
der Ableitung der v.d.Waals-Gleichung hatten wir gesehen, daß p aufgrund der
Wechselwirkungen korrigiert werden muß). Damit bleibt für die Innere Energie U, dass sie
der Energie der einzelnen Teilchen entspricht, also :
E ≡U
Die Innere Energie U ist also die innere Energie der Teilchen !
Wir wollen jetzt die Zustandssummen der verschiedenen Energieformen untersuchen. Für
die elektronische Anregung können wir, da εel sehr groß gegenüber kT ist, setzen :
e −ε el
kT
<< 1
wegen
ε el >> kT
für
n>0
Und damit wird
Qel =
∞
∑g ⋅e ε
−
i
n
kT
≈ g 0 ⋅ e −ε 0
kT
(ε 0 = 0 , g 0 = 1)
=1
n =0
Für die Translation und die Rotation gilt umgekehrt, daß die Energieniveaus sehr eng
beieinander liegen. Damit kann die Summe durch das Integral ersetzt werden :
Q = ∑ gi ⋅ e
−ε i kT
⇒
∞
(−i h
∫ gi ⋅ e
2 2
8 ma 2 kT
) di
0
Da hier die eindimensionale Translation angesprochen ist, gibt es keine Entartung und g
ist gleich 1. Damit folgt
Q=
8ma 2 kT
a
−z2
⋅
e
dz = ⋅ 2πmkT
2
∫
π
h
R
und
E
trans
mit
z2 =
i 2h 2
8ma 2 kT
1
∂
∂
= NkT ⋅
ln Q = Nk T 2 ⋅
ln Q = ⋅ RT
∂T
∂T
2
2
Dies gilt für den eindimensionalen Fall, für den dreidimensionalen werden die Energien
addiert (N=3) :
E trans =
3
⋅ RT
2
Entsprechend gilt für die Rotationsenergie :
1
E rot = f ⋅ ⋅ RT
2
mit
f = Anzahl der anregbaren Rotationen
(Abweichend von den meisten Lehrbüchern wird hier mit f nicht die Anzahl der Freiheitsgrade bezeichnet. Jeder Körper hat prinzipiell 3 Rotationsfreiheitsgrade. Da jedoch wegen
des verschwindenden Trägheitsmoments bei Rotation von Atomen, diese nicht angeregt
werden können, werden sie nicht berücksichtigt. Gleiches gilt für lineare Moleküle in
Bezug auf die Rotation um die Molekülachsen.)
Dieses Ergebnis ist mit dem der klassischen Thermodynamik identisch. Das war zu erwarten, da die Zustände bis zu sehr großen i besetzt sind. Für große Quantenzahlen gilt
immer die klassische Theorie, denn hier wird ja über so viele Teilchen gemittelt, daß ein
fast stufenloser Übergang von dem molekularen zum molaren Bild vollzogen wird.
Für die Zustandssumme der Vibration kann eine entsprechende Rechnung durchgeführt
werden :
∑g
Q=
j
⋅e
− ε j kT
=
∑∑ e
k
− ( v +1 2 )⋅hvk kT
v
Für jede Grundschwingung k gilt ε v = (v + 1 2 ) ⋅ hv
, wobei keine Entartung auftritt.
Das Ergebnis einer geometrischen Reihe ist bekannt :
N
∑ q j −1 =
j =1
1− qN
1− q
Im vorliegenden Fall ist q gleich e
Also gilt für die Zustandssumme
Q = ∑e
− hν k
− hν / 2 kT
k
(qk geht gegen 0, wenn k groß wird)
für q < 1
und q ist kleiner als 1, da h und νk positiv sind.
e − hv / 2 kT
1− 0
⋅
=∑
1 − e −hν / kT
1 − e −hv / kT
Für die Energie einer Normalschwingung ergibt sich somit
EVib
e − hv 2 kt
∂
2 ∂
ln
= N ⋅ kT ⋅
ln QVib = N ⋅ kT ⋅
∂T
∂T 1 − e −hv kt
i
2
i
Der Index i zählt hier die Normalschwingungen.
Nach einer längeren Rechnung erhält man als Ergebnis
EVib = ∑
x ⋅ RT
+ E0
ex −1
mit
x=
ε
kT
=
hv 0
kT
Für die Gesamtzustandssumme eines Moleküls erhält man damit
Q = Q trans ⋅ Q rot ⋅ Q vib ⋅ Q el
und
E gesamt =
3
f
x
RT + RT + ∑ x−1 RT + E0 + E el
2
2
e
≡0
Mit U = E oder U-Uo = E-Eo ist der Zusammenhang zwischen den quantenmechanisch
bestimmten Energiezuständen und den thermodynamisch bestimmten Größen hergestellt
und damit sind alle thermodynamischen Größen aus Molekülparametern berechenbar. Da
dies jedoch einen erheblichen Rechenaufwand bedeutet, muß hier auf die Ableitungen
verzichtet werdenund es wird auf die Lehrbücher verwiesen.
1. Rechenbeispiel
Das Schwingungsenergieschema von HCl besteht aus einem System von Niveaus mit
gleichen Abständen von v~ = 2990 cm-1. Aus dieser Angabe läßt sich das Besetzungsverhältnis zweier benachbarter Energieniveaus berechnen.
Das Besetzungsverhältnis ist nach Boltzmann gegeben durch
N i +1 e − (ε i +∆ε ) / kT
=
= e −∆ε / kT
−ε i / kT
Ni
e
Die Energiedifferenz zwischen zwei Niveaus ergibt sich aus der Wellenzahl
∆ε = h ⋅ν = h ⋅ c ⋅ν~ =
= 6.625 × 10 − 34 Js ⋅ 2.998 × 1010 cm / s ⋅ 2990cm −1 =
= 5.94 × 10 − 20 J
Die termische Energie beträgt bei 298 K und 1000 K:
kT = 1.38×10-23J/K ⋅ 298K = 4.11×10-21J
-23
-20
kT = 1.38×10 J/K ⋅ 1000K = 1.38×10 J
und
Für die Besetzungsverhältnisse ergeben sich also
bei T=298K :
Ni+1/Ni = 5.3×10-7
und bei T=1000K
Ni+1/Ni = 1.35×10-2
Je höher die Temperatur ist, umso gleichmäßiger sind die Niveaus besetzt. Dies zeigt
auch die Abbildung 26.
2.Rechenbeispiel
Zwei Atome verbinden sich in einer Gasphasen-Reaktion zu einem Molekül. Wie sieht die
Temperaturabhängigkeit der Energiedifferenz von Reaktionsprodukt und Reaktanten aus?
Die Energiedifferenz ist für 300 K zu berechnen, wobei angenommen wird, dass bei dieser
Temperatur die Schwingungsenergie gleich 3 kT entspricht.
A + A → A2
Die Atome besitzen ausschließlich Translationsenergie, also
E A = 3 RT
2
Das (lineare) Molekül A2 hat folgende Gesamtenergie
x
RT
E A2 = 3 RT + 2 RT + x
2
2
e −1
mit
x=
ε
kT
=[
3kT
= 3]300 K
kT
Daraus ergibt sich als Reaktionsenergie, die im Stoß an ein drittes Molekül abgegeben
werden muss
x
∆E = E A2 − 2 E A = − 1 RT + x
RT
2
e −1
Für T = 300 K ergibt sich damit ∆E = (-.5 + 0.157) RT = -855 J/Mol.