Wirkung von Antidepressiva abhängig vom Genotyp - Wiley-VCH
Werbung
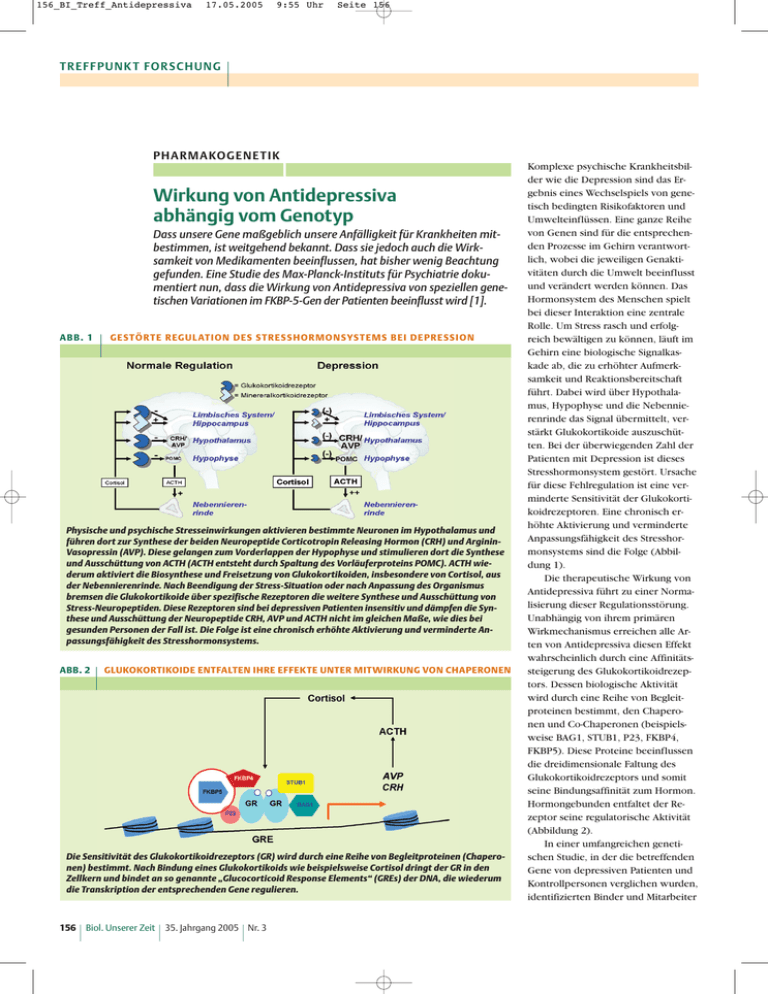
156_BI_Treff_Antidepressiva 17.05.2005 T R E F F P U N K T FO R SC H U N G 9:55 Uhr Seite 156 | PH A R M A KO G E N E T I K | Wirkung von Antidepressiva abhängig vom Genotyp Dass unsere Gene maßgeblich unsere Anfälligkeit für Krankheiten mitbestimmen, ist weitgehend bekannt. Dass sie jedoch auch die Wirksamkeit von Medikamenten beeinflussen, hat bisher wenig Beachtung gefunden. Eine Studie des Max-Planck-Instituts für Psychiatrie dokumentiert nun, dass die Wirkung von Antidepressiva von speziellen genetischen Variationen im FKBP-5-Gen der Patienten beeinflusst wird [1]. ABB. 1 | G E S T Ö R T E R EG U L AT I O N D E S S T R E S S H O R M O N S YS T E M S B E I D E PR E S S I O N Physische und psychische Stresseinwirkungen aktivieren bestimmte Neuronen im Hypothalamus und führen dort zur Synthese der beiden Neuropeptide Corticotropin Releasing Hormon (CRH) und ArgininVasopressin (AVP). Diese gelangen zum Vorderlappen der Hypophyse und stimulieren dort die Synthese und Ausschüttung von ACTH (ACTH entsteht durch Spaltung des Vorläuferproteins POMC). ACTH wiederum aktiviert die Biosynthese und Freisetzung von Glukokortikoiden, insbesondere von Cortisol, aus der Nebennierenrinde. Nach Beendigung der Stress-Situation oder nach Anpassung des Organismus bremsen die Glukokortikoide über spezifische Rezeptoren die weitere Synthese und Ausschüttung von Stress-Neuropeptiden. Diese Rezeptoren sind bei depressiven Patienten insensitiv und dämpfen die Synthese und Ausschüttung der Neuropeptide CRH, AVP und ACTH nicht im gleichen Maße, wie dies bei gesunden Personen der Fall ist. Die Folge ist eine chronisch erhöhte Aktivierung und verminderte Anpassungsfähigkeit des Stresshormonsystems. ABB. 2 | GLUKOKORTIKOIDE ENTFALTEN IHRE EFFEKTE UNTER MITWIRKUNG VON CHAPERONEN Die Sensitivität des Glukokortikoidrezeptors (GR) wird durch eine Reihe von Begleitproteinen (Chaperonen) bestimmt. Nach Bindung eines Glukokortikoids wie beispielsweise Cortisol dringt der GR in den Zellkern und bindet an so genannte „Glucocorticoid Response Elements“ (GREs) der DNA, die wiederum die Transkription der entsprechenden Gene regulieren. 156 | Biol. Unserer Zeit | 35. Jahrgang 2005 Nr. 3 | Komplexe psychische Krankheitsbilder wie die Depression sind das Ergebnis eines Wechselspiels von genetisch bedingten Risikofaktoren und Umwelteinflüssen. Eine ganze Reihe von Genen sind für die entsprechenden Prozesse im Gehirn verantwortlich, wobei die jeweiligen Genaktivitäten durch die Umwelt beeinflusst und verändert werden können. Das Hormonsystem des Menschen spielt bei dieser Interaktion eine zentrale Rolle. Um Stress rasch und erfolgreich bewältigen zu können, läuft im Gehirn eine biologische Signalkaskade ab, die zu erhöhter Aufmerksamkeit und Reaktionsbereitschaft führt. Dabei wird über Hypothalamus, Hypophyse und die Nebennierenrinde das Signal übermittelt, verstärkt Glukokortikoide auszuschütten. Bei der überwiegenden Zahl der Patienten mit Depression ist dieses Stresshormonsystem gestört. Ursache für diese Fehlregulation ist eine verminderte Sensitivität der Glukokortikoidrezeptoren. Eine chronisch erhöhte Aktivierung und verminderte Anpassungsfähigkeit des Stresshormonsystems sind die Folge (Abbildung 1). Die therapeutische Wirkung von Antidepressiva führt zu einer Normalisierung dieser Regulationsstörung. Unabhängig von ihrem primären Wirkmechanismus erreichen alle Arten von Antidepressiva diesen Effekt wahrscheinlich durch eine Affinitätssteigerung des Glukokortikoidrezeptors. Dessen biologische Aktivität wird durch eine Reihe von Begleitproteinen bestimmt, den Chaperonen und Co-Chaperonen (beispielsweise BAG1, STUB1, P23, FKBP4, FKBP5). Diese Proteine beeinflussen die dreidimensionale Faltung des Glukokortikoidrezeptors und somit seine Bindungsaffinität zum Hormon. Hormongebunden entfaltet der Rezeptor seine regulatorische Aktivität (Abbildung 2). In einer umfangreichen genetischen Studie, in der die betreffenden Gene von depressiven Patienten und Kontrollpersonen verglichen wurden, identifizierten Binder und Mitarbeiter 156_BI_Treff_Antidepressiva 17.05.2005 9:55 Uhr Seite 157 | [1] eine Variante des FKBP-5-Gens, die mit therapeutischem Ansprechen auf alle getesteten Antidepressiva korreliert. Patienten, die an einer bestimmten Position innerhalb dieses Gens die Thyminbase auf beiden Allelen (TT-Genotyp) tragen, reagieren bereits nach einer Woche Antidepressiva-Therapie mit deutlicher Linderung der depressiven Symptomatik: Die Stimmung der Patienten besserte sich, ihr Antrieb und ihre Aufmerksamkeit waren erhöht, sie konnten besser schlafen und hatten mehr Appetit, wie mit Hilfe eines standardisierten Bewertungsbogens (Hamilton Depression Rating Scale) erfasst wurde (Abbildung 3). Bei Patienten mit anderen Basenkombinationen wurde diese Wirkung erst nach fünf Wochen erreicht. Die Pharmakogenetik hat sich zur Aufgabe gemacht, Wechselwirkungen zwischen genetischen Faktoren und dem therapeutischen Ansprechen auf Pharmaka aufzuklären. Die Ergebnisse der Studie zeigen, dass diese Wechselwirkungen auch bei der Behandlung der Depression eine wichtige Rolle spielen. Bei komplexen Erkrankungen ist jedoch vor einer eindimensionalen Betrachtung der Kausalzusammenhänge zu warnen. So sprechen Patienten mit dem TTGenotyp des FKBP-5-Gens zwar schneller auf die Behandlung mit konventionellen Antidepressiva an, gleichzeitig berichteten diese Patienten aber auch von einer erhöhten Anzahl an früheren depressiven Episoden. Wahrscheinlich ist dieser Genotyp mit einer leichteren Beeinflussbarkeit der Glukokortikoid-RezeptorSensitivität verbunden, so dass einerseits Antidepressiva effektiver die Regulationsstörung normalisieren und andererseits Umweltfaktoren leichter eine Störung des hormonellen Regulationsgleichgewichtes induzieren können. Im Bereich der Antidepressiva scheint ein Paradigmenwechsel bevorzustehen: Bisher wurden Antidepressiva mit vergleichbarem Wirkmechanismus entwickelt: Sie alle verstärken die Neurotransmitter- freisetzung an bestimmten Synapsen, was dann zu einer Kaskade weiterer Veränderungen im Nervensystem führt. Die moderne Forschung begann in den vergangenen Jahren damit, die depressionsauslösenden Prozesse – wie beispielsweise die Modulation der zentralen Signalübertragung über Hormone des Stresshormonsystems – zu identifizieren. Ziel ist die Entwicklung von Medikamenten – wie beispielsweise CRH1R-Antagonisten – welche in diesem System direkt ansetzen. [1] E.B. Binder et al., Nature Genetics 2004, 36, 1319-25. [2] F. Holsboer, Neuropsychopharmacology 2000, 23, 477-501. [3] F. Holsboer, N. Barden, Endocrine Reviews 1996, 17, 187-205. [4] C.M. Pariante, A.H. Miller, Biological Psychiatry 2001, 49, 391-404. ABB. 3 | T R E F F P U N K T FO R SC H U N G D E R G E N OT Y P B E E I N F LU S S T D E N T H E R A PI E E R FO LG B E I D E PR E S S I O N Bei Patienten mit dem TT-Genotyp an einer bestimmten Position innerhalb des FKBP-5-Gens wirken die zur Behandlung eingesetzten Antidepressiva deutlich schneller, wie mit Hilfe eines standardisierten Bewertungsbogens (HAMD = Hamilton Depression Rating Scale) ermittelt wurde. Barbara I. Meyer, München PROJ E K T E D E S N G F N : FO R S C H U N G Z U M T H E M A „ A F F E K T I V E S T Ö R U N G E N “ | An vier Standorten in Deutschland erforschen Wissenschaftler des Nationalen Genomforschungsnetzes (NGFN) die genetischen Ursachen der Depression und der Manie. Diese beiden Erkrankungsformen werden unter dem Begriff „Affektive Störungen" zusammengefasst. Die Wissenschaftler verfolgen drei Forschungsstrategien: 1) In Bonn, Mannheim und Kiel untersuchen NGFN-Wissenschaftler das Erbgut von Patienten und deren Familien. Mit so genannten Kopplungsanalysen können die Wissenschaftler Chromosomen-Bereiche identifizieren, in denen potenzielle Krankheits-Gene liegen könnten. Alle Sequenzunterschiede, die in diesen Regionen des Genoms vorkommen, werden kartiert und daraufhin untersucht, ob sie an der Krankheitsentstehung beteiligt sind. 2) Wissenschaftler in München vergleichen die Proteinmengen in der Gehirnflüssigkeit von Patienten und gesunden Personen. Hierfür steht die wohl weltweit umfangreichste Sammlung an Proben mit Gehirnflüssigkeit zur Verfügung. Außerdem werden Gehirngewebe verschiedener Mausmodelle auf Unterschiede in ihrer GenAktivität untersucht. Anschließend werden diese Gene und Proteine daraufhin überprüft, ob sie eine Rolle bei der Entstehung der Depression spielen. 3) In Bonn werden Untersuchungen an Maus-Modellen durchgeführt, in deren Erbgut ein DNA-Sequenzabschnitt des menschlichen Genoms eingefügt wurde, der das D-Amino-Acid-Oxidase-Aktivator-Gen beinhaltet. Wissenschaftliche Studien geben Hinweise darauf, dass dieses Gen am Entstehen von Depressionen und Manien beteiligt ist. Mit Hilfe des Mausmodells kann erforscht werden, in welchen Hirnregionen das entsprechende Protein vorkommt, wie es funktioniert und wie pharmazeutische Substanzen wirken, die gezielt in den Krankheitsmechanismus der D-Amino-Acid-Oxidase eingreifen. Beteiligte Institute: Institut für Humangenetik, Universitätsklinikum Bonn (http://bonn.humgen.de) Abteilung für Molekulare Neurobiologie, Universitätsklinikum Bonn (www.meb.uni-bonn.de/ psychiatrie/newpage/index.html) Institut für Klinische Molekularbiologie, I. Med. Klinik, Universität Kiel (www.ikmb.uni-kiel.de) Abteilung für Genetische Epidemiologie, Zentralinstitut für Seelische Gesundheit, Mannheim (www.zi-mannheim.de/58.html) Max-Planck-Institut für Psychiatrie, München (www.mpipsykl.mpg.de) Informationen zum Nationalen Genomforschungsnetz unter www.ngfn.de Nr. 3 35. Jahrgang 2005 | | Biol. Unserer Zeit | 157





