Akutes Koronarsyndrom
Werbung

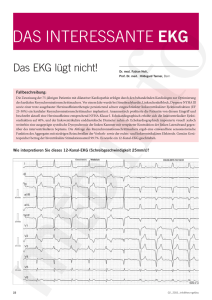
Akutes Koronarsyndrom Aufriss Unter dem Sammelbegriff des akuten Koronarsyndroms, definieren sich die akut lebensbedrohlichen Phasen der koronaren Herzerkrankung, wie die instabile Angina pectoris (IAP), der Non-St-Strecken-Elevations-Myokardinfarkt (NSTEMI), der St-StreckenElevations-Myokardinfarkt (STEMI) und der plötzliche Herztod. Die Einführung dieses Oberbegriffs liegt in der Erkenntnis, dass den genannten Notfallbildern ein gemeinsamer Pathomechanismus zugrunde liegt, der vergleichbare diagnostische und therapeutische Strategien erfordert. Die Übergänge der Krankheitsbilder sind oft fließend, so dass es bei dem Versuch der isolierten Betrachtung der einzelnen Notfallbilder auch mal zum falschen Unterlassen notwendiger Therapien für den Patienten kommen könnte. Hinter dieser Begrifflichkeit finden sich ca. 2 Millionen Notfallpatienten, die jährlich vom Rettungsdienst versorgt und transportiert werden. Bei 300 000 dieser Notfallpatienten handelt es sich um einen endgültigen Gefäßverschluss, dem Myokardinfarkt. Trotz verbesserter Diagnostik und Therapie versterben heute noch fast 40 % dieser Patienten an dem Myokardinfarkt, wobei sich > 60 % der Todesfälle innerhalb der 1 h nach Infarktereignis aufgrund von plötzlich auftretenden Rhythmusstörungen ereignen. Ursachen und Pathophysiologie Der bei weitem überwiegende Teil der Koronarsyndrome entsteht auf dem Boden atherosklerotisch veränderter Koronarien, in Form von Plaqueablagerungen. Ursächlich für die Entstehung von Plaques werden u.a. Endothelschäden verantwortlich gemacht, die eine Einlagerung von Lipiden (Fetten) innerhalb der Gefäßintima ermöglichen. Im weiteren Verlauf heften sich Monozyten und T-Lymphozyten zunächst am Endothel an. Die Monozyten wandeln sich später innerhalb der Plaque zu Makrophagen um, die sich dann wiederum mit den Lipiden durch eine Bioakkumulation in Schaumzellen (Xanthomzellen) umwandeln. Diese werden in der Frühphase als sog. fatty streaks in den Koronargefäßen sichtbar. Bedingt durch diese Ablagerung, kommt es zu einer Verschlechterung der Durchblutung mit dem Resultat einer Ischämie am Myokard. Eine instabile atherosklerotische Plaque mit Neigung zur Ruptur, besteht meist aus einer zunehmenden Masse von Lipiden, die durch ein Bindegewebe vom Gefäßlumen getrennt ist. Diese Ablagerungen unterliegen hohen lokalen Scherkräften. Hier gilt, je dünner die Bindegewebsabdeckung wird, desto höher das Risiko der Ruptur oder Plaquefissur. Die Plaqueruptur führt zum einen zur Einblutung in die Plaque und andererseits zur intraluminalen Thrombose. Die Thrombose wird durch die freie Kommunikation zwischen den Lipiden, der Plaque und den Makrophagen, die reich an Prokoagulantien (gerinnungsbegünstigenden Substanzen) sind, ausgelöst. Folge ist eine zunehmende Einengung des Gefäßlumens, die bis zum kompletten Verschluss des Gefäßes führen kann. Es entsteht eine Ischämie des Myokards. Bedingt durch diese Ischämie im Gewebe werden Nährstoffe nicht mehr vollständig verbrannt, es fallen hierdurch saure Stoffwechselendprodukte an, die bedingt durch die Verengung bzw. den Verschluss nicht ausreichend abtransportiert werden. Die Ansäuerung des Gewebes löst dann den typischen Angina pectoris Schmerz aus. Zusätzlich kommt es zur Funktionsstörung des Gefäßendothels, so dass dessen eigene Vasodilatatoren, z.B. das EDRF (endothelium derived relaxing factor), Antithrombin III fehlen. Erschwerend kommt hinzu, dass im Rahmen der Gerinnung vasokonstriktorische Substanzen wie das Thromboxan A2 (ein Prostaglandin) ausgeschüttet werden. Hält die Ischämie längere Zeit an, entsteht eine Gewebsnekrose, der Myokardinfarkt. Je nach Infarktgröße resultiert eine erhebliche Einschränkung der Leistungsfähigkeit des Herzmuskels (Insuffizienz). Die hypoxische Muskulatur verharrt zunächst in einem dauerkontrahiertem Zustand, wodurch die Dehnbarkeit des betreffenden Ventrikels zusätzlich eingeschränkt wird. Symptome Die größte Gefahr des akuten Koronarsyndroms liegt somit in der Ausbildung eines Myokardinfarktes. Die Diagnostik beruht daher wie die Infarktdiagnostik auf den 3 Säulen Klinik, EKG, Enzymdiagnostik (Labor). Klinik I.d.R finden wir unruhige Patienten vor, die meist über einen retrosternalen Druckschmerz ggf. ausstrahlend in den linken Arm, Oberbauch klagen. Cave: bei älteren oder an Diabetes mellitus erkrankten Menschen, könnte diese Schmerzsymptomatik aufgrund Polyneuropatien fehlen, hier spricht man von einem sog. stummen Infarkt. Mit diesem Druck- und Beklemmungsgefühl stellt sich in den meisten Fällen gleichzeitig ein starkes Angstgefühl ein, das als Todesangst vom Betreffenden geschildert wird. Zusätzlich zur klebrigen, kaltschweißigen Haut und einer auftretenden Dyspnoe klagen viele Patienten über Übelkeit und Erbrechen. EKG Typische EKG-Veränderungen der St-Strecke sind oft richtungsweisend für die Arbeitsdiagnose akutes Koronarsyndrom. Bei > 30 % der instabilen Angina pectoris Patienten zeigen sich Senkungen (Depressionen) des St-Segments. Infarkttypische Veränderungen zeigen im Initialstadium eine beträchtliche T-Erhöhung (Erstickungs-T), das jedoch im Rettungseinsatz nicht mehr zu sehen ist. Danach imponieren St-Streckenhebungen und das pathologische Q (Pardee-Q) als Zeichen einer Nekrose. Von einem Pardee Q spricht man, wenn dieses größer als ¼ der R-Zacke und mindestens 0,04 sek. breit ist. Hierbei liefert das komplett registrierte 12-Kanal-EKG unverzichtbare Dienste. Dieses kann dann auch in der weiteren klinischen Diagnostik und Versorgung heran gezogen werden. Die oft beobachtete Praxis, in der Klinik ein „eigenes“ neues EKG zu schreiben muss in diesem Zusammenhang als unnötig und zeitverzögernd gewertet werden, da sich die Validität eines EKG´s nicht dadurch ändert, das es in einer Klinik geschrieben wird. Cave: wie oben beschrieben, sind auch beim Myokardinfarkt nicht immer typische EKGVeränderungen wie eine St-Streckenhebung oder ein Pardee-Q zu sehen. Hierbei spielt es eine entscheidende Rolle, ob der Infarkt die ganze Dicke der Herzwand durchdringt (transmuraler Infarkt) oder sich auf die Innen- bzw. die Außenschicht (nicht transmuraler Infarkt) beschränkt. Gerade bei dem nicht transmuralen Infarkt wird z.B. kein Pardee-Q sichtbar. Abb. *.*: EKG-Veränderungen a. „Erstickungs-T b. St-Streckenhebung c. Pardee-Q Enzymdiagnostik (Labor) Zur Bestätigung myokardialer Schädigungen werden in der Klinik routinemäßig myokardiale Enzyme oder Herzmarker bestimmt. Die besten laborchemischen Indikatoren stellen das CK MB – Untergruppe der Kreatininkinase die M (“muscle”) und B (“brain”), die sich vorwiegend im Herzen findet Troponin T – ein Teil des kontraktilen Apparates der Muskelzelle Myoglobin – ein Protein, das sich in der quergestreiften Muskulatur wieder findet, dar. Abb. *.*: Darstellung der Enzymdiagnostik im zeitlichen Verlauf Maßnahmen Die Maßnahmen beim akuten Koronarsyndrom lassen sich in zwei Maßnahmenpakete unterteilen. Gerade um den zeitlichen Faktor bei diesem Notfall nicht außer acht zu lassen, jedoch alle Maßnahmen ruhig und konzentriert abarbeiten zu können, erscheint es auch bei Eintreffen des Notarztes sinnvoll, dass die beiden Maßnahmen parallel zueinander abgearbeitet werden. D.h., das RTW-Team arbeitet sein Maßnahmenpaket an der Stelle weiter ab, wo es vor der Übergabe des Notarztes war und der NEF-Fahrer assistiert dem Notarzt bei seinen Maßnahmen. Maßnahmen des RTW-Teams Lagerung des ansprechbaren Patienten in Oberkörperhochlage 30 – 35 °. Diese Lagerung lindert die Atemnot und bewirkt einen verminderten venösen Rückstrom zum ohnehin schon überlasteten Herzen Konsequente Immobilisation und Beruhigung des Patienten O2-Gabe von 4-6 l/min über eine Nasenbrille Notarzt-Ruf, falls noch nicht parallel alarmiert Monitorring bestehend aus kontinuierlicher RR-Messung, EKG, Puls und SaO2 i.v.-Zugang legen z.B. 20 G möglichst periphere um ggf. bei Fehlpunktionen bei einer nachfolgenden Lyse gut komprimieren zu können Laborblutentnahme, um in der Klinik unverzüglich u.a. die oben genannten Enzymdiagnostik zu starten oder ggf. mit einer im Krankenhaus entnommenen Probe gleich einen Trend aufzeigen zu können. Nitroglyzerin 2 Hübe = 0,8 mg s.l. (z.B. Nitrolingual-Spray), wenn der RRsyst. > 100 mmHg liegt, ggf. alle 5 min wiederholen. Nitroglycerin wird wie alle Nitrate im Körper zur eigentlichen Wirksubstanz, dem Stickstoffmonoxid (NO) umgewandelt. Dieses ist identisch mit dem körpereigenen EDRF siehe oben, was bei einem atherosklerotisch veränderten Gefäß nicht mehr gebildet wird. Nitroglyzerin bewirkt im Einzelnen: Vasodilatation v.a. der venösen Gefäße des Lungen- und Körperkreislaufs sowie der größeren Koronararterien, gerade auch in den atherosklerotisch veränderten Gefäßen. Hieraus resultiert eine Vorlastsenkung, was zur Abnahme der Herzarbeit und des O2Verbrauchs führt. Druckentlastung der Innenschichten des Herzmuskels (subendokardiales Myokard) durch verminderte Füllungsdrücke, was zu einer Verbesserung der dortigen Kapillardurchblutung führt. Hemmung der Thrombozytenaggretation und Leukozytenadhäsion Untersuchungen haben gezeigt, dass die frühzeitige Gabe von Nitroglyzerin die Infarktgröße und das Risiko von Kammerflimmern reduziert! (ACC/AHA Task force Report 1990 und folgende) 12-Kanal-EKG schreiben Die Aufgaben des NEF-Teams liegen zum einen in der Aufrechterhaltung der schon getroffenen Maßnahmen des RTW-Teams und zum zweiten in der weiterführenden medikamentösen Behandlung mit dem Ziel der: Begrenzung der Infarktgröße Senkung der Herzarbeit Schmerzbekämpfung Vermeidung von Komplikationen Ggf. Lysetherapie Maßnahmen des NEF-Teams Analgesie und ggf. Sedierung: Morphin 5-10 mg i.v. Die Angst und die Schmerzen bewirken eine starke Ausschüttung von körpereigenen Katecholaminen, die u.a. für das Auftreten von Rhythmusstörungen verantwortlich gemacht werden. Morphin bewirkt durch seine analgetische und sedierende Wirkung eine Abnahme dieser zirkulierenden Katecholamine. Ebenfalls bewirkt es durch seine zentralvenöse Wirkung auf die Gefäße, eine Vor- und Nachlastsenkung. Midazolam 3-5 mg i.v. (z.B. Dormicum), wenn die sedierende Wirkung von Morphin nicht ausreicht. Thrombozytenaggretationshemmung mit Acetylsalicylsäure 100 – 500 mg i.v. (z.B. Aspisol). ASS verhindert die weitere Anheftung von Thrombozyten und hemmt die Synthese des aggretationsauslösend und gefäßkonstriktorisch wirkenden Thromboxan A2 (TxA2). Es verhindert eine Infarktausdehnung und senkt die 50-Stunden-Letalität (Isis 1988)! Antikoagulation: Heparin 5000 IE i.v. (z.B. Liquemin) Cave: Inkompatibilität mit einigen Fibrinolytika beachten. Antiemetikum: bei bestehender Übelkeit Metoclopramid 10 mg i.v. (z.B. MCP) -Blocker: Metoprolol 5-10 mg i.v. (z.B. Beloc) bei stabilen Kreislaufverhälnissen. Metoprolol hemmt selektiv die Erregungsübertragung an den sympatischen 1-Rezeptoren im Herzen. Dieses vermindert durch die Abnahme der Herzfrequenz, der Kontraktilität und der Erregbarkeit, das Risiko auftretender Rhythmusstörungen und senkt den myokardialen O2-Verbrauch. Nitroglycerin: 1-5 mg i.v. wenn RRsyst > 100 mmHg (z.B. Nitrolingual infusl.) Ein immer wieder heftig diskutierter Therapieansatz stellt die präklinische Lyse dar. Indikationen für die Lysetherapie sind: Infarktsymptome sowie ein eindeutiges 12-Kanal-EKG (ST-Streckenhebungen von ≥ 0,1 mV in mindestens 2 zusammenhängenden Extremitätenableitungen bzw. ≥ 2 mV in mindestens 2 zusammenhängenden Brustwandableitungen), Einsetzen des Infarktschmerzes < 3 h und dem Fehlen von relativen und absoluten Kontraindikationen (siehe unten) und einem rüstigen Alter des Patienten. Cave: Das Risiko einer Blutung speziell der Hirnblutung unter Lyse steigt jenseits des 75. Lebensjahr deutlich an. Je früher die Thrombolysetherapie einsetzt, umso günstiger die Prognose. Der Zeitgewinn durch die präklinische Lyse im Vergleich zur stationären Lyse beträgt zwischen 30 und 130 min, im Mittel 60 min. Eine Erfolg versprechende Wiedereröffnung des thrombotisch verschlossenen Koronargefäßes, ist auch über die 3 h Frist hinaus mittels einer Ballondilatation möglich. Die Infarktlimitierung trägt zur Erhaltung der Pumpleistung des Herzens bei. Die Reperfusion birgt allerdings auch einige Probleme wie z.B. ventrikuläre Rhythmusstörungen, sog. Reperfusionsarrhythmien, die sich i.d.R. gut mit Amiodaron 150-300 mg i.v. (z.B.Cordarex®) beherrschen lassen Die Wahl der optimalen Reperfusionsstrategie, also Lyse oder PCI , muss sich nach den lokalen Verfügbarkeiten richten, da derzeit nur ca. 20 % aller Krankenhäuser in Deutschland die Möglichkeit zur PCI bieten. Ist innerhalb von 90 Min nach Eintreffen des Notarztes eine PCI möglich, so ist diese der Lyse vorzuziehen. Welches Präparat zur Lyse sollte vorgehalten werden? Hier kann keine generelle Empfehlung gegeben werden, sondern die Auswahl muss hier in Absprache mit dem weiterbehandelnden Zentrum erfolgen. Als Anspruch gilt, ein Präparat zu wählen, das möglichst unkompliziert in einem oder höchstens zwei Boli verabreicht werden kann, wie z.B. Teneceplase (z.B. Metalyse®). Absolute Kontraindikationen für eine Lysetherapie sind : Schlaganfall in den letzten 6 Monaten (hämorrhagisch zeitunabhängig) Trauma, Operation, Kopfverletzung innerhalb der letzten 3 Wochen Neoplasma oder neurologische ZNS-Erkrankung Gastrointestinale Blutung innerhalb der letzten 4 Wochen Blutgerinnungsstörungen Dissezierendes Aortendissektion Relative Kontraindikationen für eine Lysetherapie sind: Orale Antikoagulatien-Therapie Nicht komprimierbare Gefäßpunktionen Floride Endokarditis Kardiopulmonale Reanimation mit Rippen-/ Sternumfrakturen Aktives Ulkusleiden Schwangerschaft Antikoagulanzientherapie Therapierefraktäre Hypertonie (> 180 mmHg) Fortgeschrittene Lebererkrankung Die Infarktlimitierung trägt zur Erhaltung der Pumpleistung des Herzens bei. Die Reperfusion birgt allerdings auch einige Probleme wie z.B. ventrikuläre Rhythmusstörungen, sog. Reperfusionsarrhythmien, die sich i.d.R. gut mit Lidocain 2 % 100 mg i.v. (z.B. Xylocain®) beherrschen lassen. Bei einem eintretenden oder vorgefundenem Kreislaufstillstand, erfolgt die Reanimation nach dem Advanced Cardiac Life Support (ACLS) Fazit Die Zeit in der bei retrosternalen Schmerzen versucht wurde, eine Differentialdiagnostik durchzuführen, ist zu Ende. Oft ist eine genaue Abgrenzung nicht möglich, da z.B. auch der Patient der auf Nitro-Gabe eine Erleichterung seiner Schmerzen erfahren hat, noch einen Infarkt haben kann. Damit es nicht, wie oft in der Praxis zu beobachten ist, zu einer willkürlichen Zuordnung kommt, gilt heute die frühzeitige Intervention analog der Infarkttherapie.