Pathologie des Respirationstraktes (Teil 2: 1 Std.)
Werbung

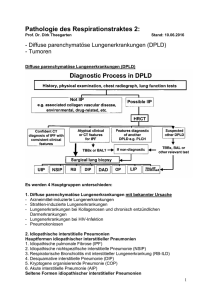
75942149 Pathologie des Respirationstraktes (Teil 2: 1 Std.) PD Dr. Dirk Theegarten Institut für Pathologie, UK Essen WS 2009/10 Internet: www.uni-due.de/~ht0214 Thema: Diffuse parenchymatöse Lungenerkrankungen (DPLD) Einteilung der DPLD: AJRCCM 2002; 165: 277-304 Diagnostisches Vorgehen bei DPLD AJRCCM 2002; 165: 277-304 1 75942149 1. Diffuse parenchymatöse Lungenerkrankungen mit bekannter Ursache - Arzneimittel-induzierte Lungenerkrankungen Strahlen-induzierte Lungenerkrankungen Lungenerkrankungen bei Kollagenosen und chronisch entzündlichen Darmerkrankungen Lungenerkrankungen bei HIV-Infektion Pneumokoniosen (s. Skript Teil 1) Arzneimittel-induzierte Lungenerkrankungen - Ergebnis einer direkten (toxischen oder idiosynkratischen) - oder indirekten Wirkung (thrombembolisch, induzierte Immunsuppression) eines Arzneimittels auf die Lunge - Histologisch oft keine uniformen Muster, - viele Arzneimittel (AM) können mehr als eine pulmonale Reaktion zeigen - Wichtige Informationen: www.pneumotox.com Die definitive Diagnose einer Arzneimittel-induzierten Lungenerkrankung erfordert: - 1. die Einnahme erfolgte in zeitlichem Zusammenhang mit der Lungenerkrankung ohne andere plausible Ursache - 2. nach Einnahmestopp Verschwinden der Erkrankung, bei Wiedereinnahme erneute Erkrankung - 3. das angeschuldigtes AM ist das einzige eingenommene AM - 4. das Krankheitsbild (klinisch, radiologisch, histologisch) ist typisch für das jeweilige AM - 5. möglicherweise: der AM-Spiegel ist abnormal Strahlen-induzierte Lungenschäden Formen: - Akute Pneumonitis (DAD), Strahlenfibrose, wandernde Infiltrate Relevante Faktoren: - bestrahltes Lungenvolumen, Gesamtdosis, Fraktionierung, - vorherige Bestrahlung und / oder gleichzeitige Chemotherapie, Steroidentzug, - Alter, präexistente Lungenerkrankung 2. Idiopathische interstitielle Pneumonien (ATS/ERS Klassifikation 2002) Unterformen: 1. Idiopathische pulmonale Fibrose (IPF)/ kryptogene fibrosierende Alveolitis [= histologisch usual interstitial pneumonia (UIP)] 2. Nichtspezifische interstitielle Pneumonie (NSIP) 3. Kryptogene organisierende Pneumonie (COP) 4. Akute interstitielle Pneumonie (AIP) 5. Respiratorische Bronchiolitis mit interstitieller Lungenerkrankung (RB-ILD) 6. Desquamative interstitielle Pneumonie (DIP) 7. Lymphozytäre interstitielle Pneumonie (LIP) 8. Unklassifizierbare interstitielle Pneumonie Wichtig: Gleiche histologische Muster auch bei anderen Ursachen ! 2 75942149 Radiologie und Differenzialdiagnose (AJRCCM 2002; 165: 277-304) Die Rollen von Klinikern, Radiologen und Pathologen bei der Diagnose von DPLD Kliniker: Vorgeschichte (Exposition, Arzneimittel), Symptome und Zeichen (Alter, Systemerkrankungen) • Radiologen: Kenntnis, Identifikation u. Bericht Muster-spezifischer Veränderungen im HRCT • Pathologen: Kenntnis, Identifikation u. Bericht Muster-spezifischer Veränderungen in der Histologie Final: interdisziplinäre Fallevaluation 3. Granulomatöse diffuse parenchymatöse Lungenerkrankungen - Sarkoidose Nekrotisierende sarkoide Granulomatose Granulomatosen infektiöser Genese Granulomatöse Vaskulitiden (M. Wegener, Churg-Strauss-Syndrom) Exogen allergische Alveolitis (EAA) / Hypersensitivity Pneumonia Sarkoidose Systemerkrankung unklarer Ätiologie, charakterisiert durch nicht-verkäsende Epitheloidzellgranulome in multiplen Organen, in 90% Lunge und Hiluslymphknoten befallen Inzidenz in Europa: 10:100,000. In China und Südostasien weitgehend unbekannt Vermutete Pathogenese: übersteigerte zelluläre Immunantwort auf ein nicht identifiziertes Antigen - Häufung bei jungen Erwachsene, leichtes Überwiegen des weibl. Geschlechtes, Winter und Frühling, Ausbrüche möglich, erhöhtes Risiko bei Medizinalpersonal - Nachweis verschiedener fraglicher Agentien - Genetische Prädisposition - Histologische Stadien der Sarkoidose: - 1. Initialstadium mit lymphozytenreicher Alveolitis und wenigen kleinen Granulomen 3 75942149 2. mittleres Stadium mit floriden zellreichen Granulomen 3. Spätstadium mit Vernarbung der Granulome und Fibrose Klinische Manifestationen: - 1. bihiläre Lymphadenopathie - 2. bihiläre Lymphadenopathie mit Lungenherden - 3. nur Lungenherde mit Übergang in Fibrose - 4. schrumpfende Lungenfibrose - Therapie: Kortikosteroide - Immunologie der Sarkoidose - Verringerung der kutanen verzögerten Immunreaktion (Anergie) - Verstärkte T-Helferzell-Antwort (Th-1) im Herd - Hypergammaglobuminämie (Anstieg zirkulierender Immunkomplexe) - B-Zell-Stimulation - Verminderte Zahl zirkulierender T-Lymphozyten - Verschiebung des CD4/CD8-Zell-Quotienten im Gewebe auf 10:1 (normal = 2:1), in der BAL auf > 3:1 - Freisetzung von IF-gamma, IL-2 u.a. aus Lymphozyten - Freisetzung von TNF-alpha, IL-12, IL-15 u.a. aus Makrophagen Exogen allergische Alveolitis (EAA, Hypersensitivitätspneumonitis) - Immunulogische Reaktion auf inhalierte organische Antigene, selten auch auf einfache Chemikalien Komplexes Syndrom variabler Intensität, Klinik und Verlauf bei genetischer Disposition Farmerlunge in 0,4 – 7% der Landarbeiter, Taubenzüchterlunge in 1 bis 10% der Taubenhalter Kombination einer Typ III- und Typ IV-Reaktion In der Regel NW von Antikörpern (Präzipitine) Lymphozytose in der Lavage Lungenfunktionsstörung radiologische Veränderungen (Aufnahme 4-10 h nach Antigenkontakt) Klinische Untersuchung 4-10 h nach Antigenkontakt: Grippesymptome (91%), Belastungsdyspnoe (83%), Husten (82%), Frösteln (56%), Auswurf (51%), Abgeschlagenheit (47%) Typisches histologisches Bild der EAA: - bronchiolozentrische interstitielle Pneumonie - locker geformte, nicht verkäsende Granulome - Granulationsgewebspröpfe Möglich: NSIP- oder UIP-Muster BAL: - deutliche Lymphozytose (bis über 50%) - erhöhte Mastzellen (> 1%) - CD4/CD8-Quotient unter 1 Akute, subakute und chronische Form 4 75942149 Mögliche Allergene bei der EAA Tierische Allergene: - Vogel, Ratte, Maus, Schwein, Milch, Schalentier, Seidenwurm, Karminrot, Kornkäfer, Protozoen, Fischmehl Bakterien und Pilze: - Kontakt mit Strohdächern, Luftbefeuchtung, Wasserdampf, Sauna, Waschmitteln, Maschinenarbeit, Produktion von Heu und Stroh, Pilzen, Tabak, Käse, Wurst, Zuckerrohr, Holz, Obst, Kork, Wein, Malz, Tomaten, Sommeralveolitis Pflanzliche Allergene: - Sojastaub, Paprika, Holzfasern, Mehle und Getreide, Pyrethrum, Alginat, Kaffee, Tee Arzneimittel: Nitrofurantin, Penizillin, Minocyclin, Amiodaron, Goldsalz, Nomifensin, Nilutamide, Methotrexat, Carbamazepin, … Chemikalien: Isozyanat, Säureanhydrid, Paulis Reagens 4. Andere diffuse parenchymatöse Lungenerkrankungen - Langerhanszell´Histiozytose (Histiozytosis X) Lymphangioleiomyomatose (LAM) Eosinophile Pneumonien Alveolarproteinosen Hämorrhagie-Syndrome Mikrolithiasis Thema: Lungentumoren Epidemiologie und Ätiologie des Lungenkarzinoms Mortalitätsraten: Nigeria: 0,8/100.000, Deutschland: 42,7/100.000, Schottland: 81,9/100.000 Steigerung um das 45 – 60 fache von 1920 – 1980, folgend dem Rauchverhalten Männer : Frauen = 6,4 : 1 60 % der Erkrankten über 60 Jahre und 5 % jünger als 40 Jahre Ursachen: 85 % Inhalatives Zigarettenrauchen 8 % Berufsabhängige inhalative Exposition 5 % „Luftverschmutzung“ (urbaner Faktor, polyzyklische Kohlenwasserstoffe, Azau. Iminoarene) 2 % andere Faktoren Verteilung der Lungenkarzinom-Typen nach dem Geschlecht männlich weiblich Kleinzelliges Karzinom Großzelliges Karzinom Plattenepithelkarzinom Adenokarzinom 44% 28% 20% 9% 22% 42% Vorstufen: Carcinoma in situ, Atypische adenomatöse Hyperplasie TNM-Klassifikation: Tumor, LK T1 Tumor < 3 cm, umgeben von Lungengewebe und der Pleura, ohne Infiltration proximal des Lappenbronchus T2 Tumor über 3 cm, Infiltration der Pleura, des Hauptbronchus bis 2 cm an die Carina oder assoziierte Atelektase / Entzündung T3 Infiltration der Brustwand, Diaphragma, mediastinale Pleura, parietales Perikard, über 2 cm an der Carina, assoziierte Atelektase / Entzündung der ganzen Lunge 5 75942149 T4 Infiltration der Nachbarorgane, maligner Pleuraerguss, Metastase im selben Lappen N1 N2 N3 Metastasen bis zum ipsilateralen Hilus ipsilaterale mediastinale Metastasen (auch subkarinal) kontralaterale oder supraklavikuläre Metastasen Tumorstadien (UICC) Stadium IA Stadium IB Stadium IIA Stadium IIB Stadium IIIA Stadium IIIB Stadium IV T1 T2 T1 T2 T3 T1, T2 T3 jedes T T4 jedes T N0 N0 N1 N1 N0 N2 N1, N2 N3 jedes N jedes N M1 Tumorstadium und Überleben in Prozent beim NSCLC (Chest 2002; 122:1037) Patholog. Stadium 3 J. 5 J. klin. Stadium 3 J. 5 J. pIA (n=511) 80 67 71 61 pIB (n=549) 67 57 46 38 pIIA (n=76) 66 55 38 34 pIIB (n=375) 46 39 33 24 pIIIA (n=399) 32 23 18 13 cIIIB (n=1.030) 7 5 cIV (n=1.427) 2 1 Tumor-Staging: Kleinzelliges Karzinom Limited disease: Befall einer Hemithoraxseite incl. Lymphknoten-Metastasen (hilär - mediastinal – supraklavikulär jeweils ipsi- und kontralateral, ipsilateraler maligner Erguß) – entspr. Stad. I – III Extended disease: ausgedehnter als limited disease – entspr. Stad. IV 6 75942149 WHO-Klassifikation des Lungenkarzinoms Plattenepithelkarzinom Kleinzelliges Karzinom Adenokarzinom Großzelliges Karzinom Adenosquamöses Karzinom Sarkomatoides Karzinom Karzinoidtumor Karzinome vom Speicheldrüsentyp Plattenepithelkarzinom (PECA): Kennzeichen • Größe stark variabel • Grau-weiß bis gelb • meist in Segment- oder Subsegmentbronchien • in 2/3 zentral gelegen • daher meist eher klinisch manifest • Varianten: papillär, klarzellig, kleinzellig, basaloid Prognose des PECA • signifikant besser als beim Adenokarzinom in allen Stadien: 80% vs. 70% 5-JahresÜberleben bei resektablem Stadium I • ausgedehnte Nekrose scheinbar schlechtere Prognose • nur 30% resektabel • bei nicht resektabelen Fällen: Gewichtsverlust, Performance-Status, Metastasenabhängige Symptome • günstig: weibliches Geschlecht • entscheidend: TNM-Stadium und Performance-Status • G1: lokale Ausbreitung • G3: Metastasierung • günstig: peripherer Tumor mit alveolärer Ausbreitung • Biomarker (Cyclin-abhängige Kinasen, Rb, P16INK4a, p53, FHIT, YB-1) Kleinzelliges Karzinom: Kennzeichen • perihiläre Massen mit ausgedehnten Nekrosen • blass weiß • häufige Lymphknotenbeteiligung • in 5% peripherer Rundherd • Variante: Kombination mit anderen Tumortypen Ungünstige Prognose bei: extensive disease, geringem Performance-Status, erhöhtem LDH-, AP-Spiegel, geringem Plasmaalbumin, geringem Natrium-Spiegel Adenokarzinom: Kennzeichen • einzeln oder multipel, sehr grössenvariabel • Makroskopie: 1. peripher (grauweiss mit zentraler Fibrose, am häufigsten), 2. zentral / endobronchial, 3. Pneumonie-artig, 4. diffus bilateral, 5. pseudomesotheliomatös, 6. sekundär: Fibrose, Narbe • Subtypen: azinär, papillär, bronchioloalveolär, solide (Kombination: gemischter Subtyp) • Varianten: fetal, muzinös, muzinöses Zystadenokarzinom, Siegelringzelltyp, Klarzelltyp Prognose: günstig: Milchglasphänomen, Bronchogramm, G1, zentrale Narbe unter 0,5 cm; ungünstig: papillärer Typ, hohe Mitosezahl, Nekrosen 5-JÜ für resezierbares bronchioloalveoläres Ca.: 100% 7 75942149 • Biomarker: p53, p185neu, cyclin D, bcl-2, LOH: 2q, 9p, 18q, 22q Adenosquamöses Karzinom • Definition: histologisch mehr als 10% von jeder Komponente, auch zusätzliche grosszellige Anteile möglich • ca. 0,4 - 4% aller Lungenkarzinome • üblicherweise peripher, möglicherweise mit zentraler Narbe • ungünstigere Prognose als beim Plattenepithel- oder Adenokarzinom Sarkomatoides Karzinom • 0,3 – 1,3 % aller malignen Lungentumoren • zentral oder peripher • pleomorpher Typ: meist Zigarettenraucher, häufig große Tumoren mit Thoraxinfiltration • Varianten: pleomorph, spindelzellig, riesenzellig, Karzinosarkom, Pulmoblastom Prognose: stadienabhängig, ungünstiger als andere Nicht-kleinzellige Karzinome • 5-JÜ (50% Stadium I): 20% • adjuvante Radio-Chemotherapie ohne Effekt Grosszelliges Karzinom: Kennzeichen • ca. 9% aller Lungenkarzinome • grosser peripherer Tumor, Beteiligung von grossen und subsegmentalen Bronchien möglich, oft Thoraxwandinfiltration • blassrot-gelbbraun, häufig mit Nekrosen • basaloider Typ meist exophytisch-endobronchial • Varianten: grosszellig-neuroendokrin, basaloid, lymphoepithelial, klarzellig, rhabdoid, Kombinationen Prognose: Performance-Status und Stadium bei Diagnosestellung, günstig: lymphoepithelialer Typ, ungünstig: basaloider Typ • Prognose des grosszellig-neuroendokrinen Typs entspricht dem des kleinzelligen Karzinoms (incl. Biomarker) Karzinoidtumor 50% inzidentel Klinisch knotiger, gut begrenzter Tumor Schnittfläche gelb-braum Oft Verkalkungen Häufig bronchiale Obstruktion Auch periphere Tumoren möglich Karzinoidtumor: 2 Formen 1. Typisches Karzinoid (TC) weniger als 2 Mitosen pro 10 HPF keine Nekrosen Atypien, erhöhte Zelldichte, lymphozytäres Infiltrat möglich 2. Atypisches Karzinoid (AC) zwischen 2 bis 10 Mitosen pro 10 HPF und / oder mit fokalen Nekrosen Karzinoidtumor: Prognose 5-JÜ Typ. Karzinoid 90-98% Atyp. Karzinoid 61-73% 10-JÜ 82-95% 35-59% 8 75942149 Prognose: stadiumabhängig • ungünstig: AC über 3,5 cm, Gefäßinvasion, Polymorphismus, Mitoserate • günstig: Pallisaden-, Papillenbildung, pseudoglanduläre Formationen Karzinome vom Speicheldrüsentyp • weniger als 1% aller Lungenkarzinome • zentrale Atemwege • keine Assoziation mit dem Zigarettenrauchen • keine Geschlechterpräferenz Formen: • Mukoepidermoid-Karzinom • Adenoidzystisches Karzinom • Epitheliales-Myoepitheliales Karzinom Tumoren der Lunge: Primärtumor oder Metastase Formen von Metastasen: Multiple runde Läsionen, selten isoliert Lymphangitis carcinomatosa Primärtumoren: Niere, Mamma, GI-Trakt, Sarkome Wichtige Differenzialdiagnose 9