SAkAM – Seminar – Bozen, 28.10.2011 "Dermatologiche
Werbung
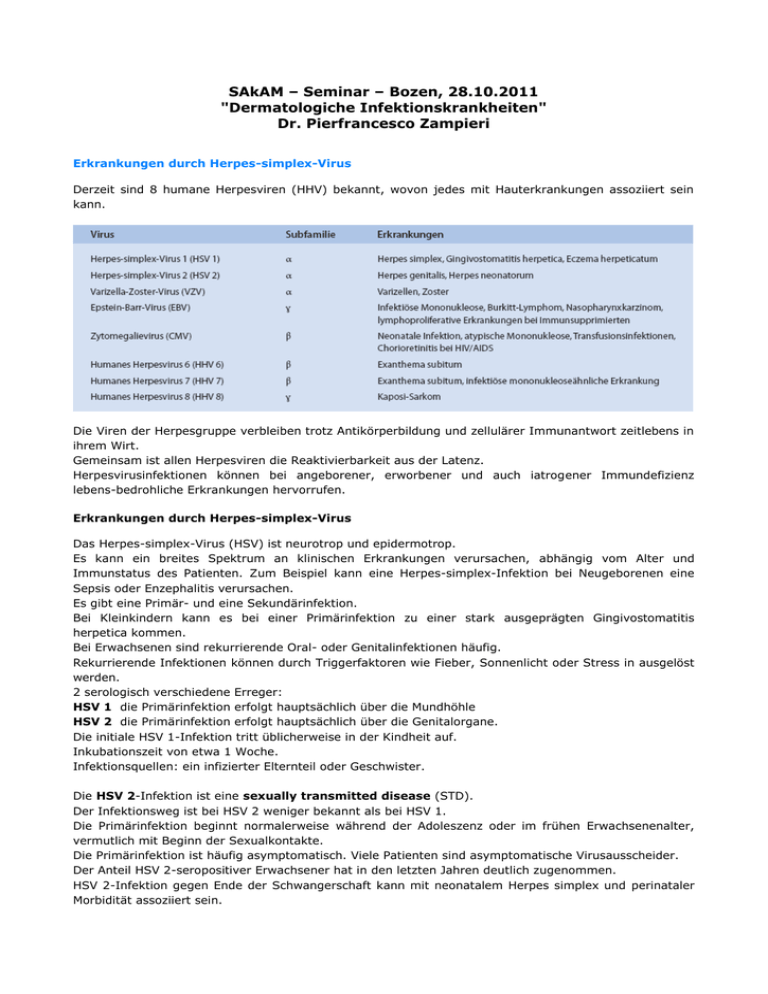
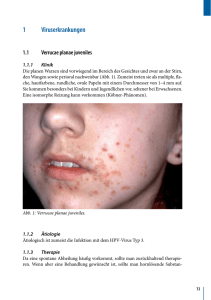
SAkAM – Seminar – Bozen, 28.10.2011 "Dermatologiche Infektionskrankheiten" Dr. Pierfrancesco Zampieri Erkrankungen durch Herpes-simplex-Virus Derzeit sind 8 humane Herpesviren (HHV) bekannt, wovon jedes mit Hauterkrankungen assoziiert sein kann. Die Viren der Herpesgruppe verbleiben trotz Antikörperbildung und zellulärer Immunantwort zeitlebens in ihrem Wirt. Gemeinsam ist allen Herpesviren die Reaktivierbarkeit aus der Latenz. Herpesvirusinfektionen können bei angeborener, erworbener und auch iatrogener Immundefizienz lebens-bedrohliche Erkrankungen hervorrufen. Erkrankungen durch Herpes-simplex-Virus Das Herpes-simplex-Virus (HSV) ist neurotrop und epidermotrop. Es kann ein breites Spektrum an klinischen Erkrankungen verursachen, abhängig vom Alter und Immunstatus des Patienten. Zum Beispiel kann eine Herpes-simplex-Infektion bei Neugeborenen eine Sepsis oder Enzephalitis verursachen. Es gibt eine Primär- und eine Sekundärinfektion. Bei Kleinkindern kann es bei einer Primärinfektion zu einer stark ausgeprägten Gingivostomatitis herpetica kommen. Bei Erwachsenen sind rekurrierende Oral- oder Genitalinfektionen häufig. Rekurrierende Infektionen können durch Triggerfaktoren wie Fieber, Sonnenlicht oder Stress in ausgelöst werden. 2 serologisch verschiedene Erreger: HSV 1 die Primärinfektion erfolgt hauptsächlich über die Mundhöhle HSV 2 die Primärinfektion erfolgt hauptsächlich über die Genitalorgane. Die initiale HSV 1-Infektion tritt üblicherweise in der Kindheit auf. Inkubationszeit von etwa 1 Woche. Infektionsquellen: ein infizierter Elternteil oder Geschwister. Die HSV 2-Infektion ist eine sexually transmitted disease (STD). Der Infektionsweg ist bei HSV 2 weniger bekannt als bei HSV 1. Die Primärinfektion beginnt normalerweise während der Adoleszenz oder im frühen Erwachsenenalter, vermutlich mit Beginn der Sexualkontakte. Die Primärinfektion ist häufig asymptomatisch. Viele Patienten sind asymptomatische Virusausscheider. Der Anteil HSV 2-seropositiver Erwachsener hat in den letzten Jahren deutlich zugenommen. HSV 2-Infektion gegen Ende der Schwangerschaft kann mit neonatalem Herpes simplex und perinataler Morbidität assoziiert sein. Eine Primärinfektion in der späten Schwangerschaft ist als weitaus gefährlicher anzusehen als eine Reaktivierung. Ätiopathogenese. bei der Primärinfektion tritt das HSV über einen lokalen Epitheldefekt ein. Kleine oberflächliche Defekte an der Haut, der Mundschleimhaut, den Konjunktiven oder im Gastrointestinaltrakt können als Eintrittspforten dienen. HSV 1 und HSV 2 werden mittels Schmierinfektion übertragen. Die Antikörperbildung führt nicht zu einer Viruselimination. Stattdessen verbleibt das Virus in den Ganglien der sensiblen Nerven. Therapie. Zusammenfassung antiviraler Substanzen bei Herpesinfektionen. Aciclovir. Dieses Purinnukleosidanalogon gilt bei einer Herpes-simplex-Infektion als wichtiges Medikament. Es interferiert dann mit der viralen DNA-Polymerase. Damit wird die virale Replikation inhibiert, ohne die Wirtszellen ausgeprägt zu schädigen. Aciclovir wird auch zur topischen Applikation (Creme oder Augensalbe) verwendet. Die Effektivität solcher Externa ist allerdings eher als gering einzustufen, da sie zur ausreichenden Virushemmung einerseits bereits in der Frühphase, andererseits in etwa 2-stündigen Abständen aufgetragen werden müssen. Dies ist meist nicht praktikabel. Bei Immunsupprimierten und auch Neugeborenen sollte die i. v. Therapie vorgezogen werden. Aciclovir wird sowohl zur Behandlung von Primär- und Sekundärinfektionen als auch prophylaktisch (in der Frühphase nach einer Knochenmarktransplantation) eingesetzt. Aufgrund der nephrotoxischen Wirkung von Aciclovir ist in manchen Fällen eine Dosisadaptation an die Kreatininclearance erforderlich. Nebenwirkungen (selten): Hepatotoxizität, Knochenmarkdepression, Schwangerschaft und Stillzeit: strenge Indikationsstellung, wobei ein mögliches teratogenes Risiko gegen die mögliche Schädigung durch die Infektion selbst abzuwägen ist. Valaciclovir. Inaktive Vorstufe des Aciclovirs, hat eine höhere orale Bioverfügbarkeit. Nach der Resorption wird Valaciclovir im Intestinaltrakt und in der Leber rasch zu Aciclovir konvertiert. Famciclovir. Hat ein ähnliches Nebenwirkungsprofil wie Aciclovir bei geringerer Toxizität. Ganciclovir. Es ist prinzipiell gegen alle replikanten Herpesviren wirksam, besonders gegen das humane Zytomegalievirus. Hohe Knochenmarktoxizität, besonders mit Granulozytopenie. Brivudin. Ist im Gegensatz zu Aciclovir weder nephrotoxisch noch hepatotoxisch. Foscarnet. Arzneimittel für aciclovirresistente Herpesviren, wird insbesondere bei immunsupprimierten Patienten eingesetzt. Impfung: es wurden eine Reihe von verschiedenen Herpes-simplex-Vakzinen gegen HSV 1 und HSV 2 entwickelt, deren nachweisbarer Erfolg bisher ausblieb. Therapieschemata des Herpes simplex PRIMÄRE INFEKTION mit HSV Gingivostomatitis herpetica Synonyme. Stomatitis aphthosa, Mundfäule Klinik. Überwiegend sind Kleinkinder betroffen, selten ältere Säuglinge oder junge Erwachsene. Kontakt- oder Tröpfcheninfektion durch Personen mit anderen herpetischen Erkrankungen. Kleine Endemien können in Gemeinschaften von Kindern (Kindergarten, Krankenhaus) auftreten Inkubationszeit von 2–7 Tagen dann akutes Krankheitsbild mit Fieber, Abgeschlagenheit, Erbrechen, schmerzhafte Mundschleimhautveränderungen mit behinderter Nahrungsaufnahme. Hinzu treten zahlreiche Aphthen, die sich aus Bläschen entwickeln. Regionale Lymphknoten meist schmerzhaft geschwollen. Verlauf. Oft ist bereits nach 10 Tagen Heilung eingetreten. Die Prognose ist im Allgemeinen gut; gefürchtete Komplikation: Meningoencephalitis herpetica. Differenzialdiagnose. Anguläre Cheilitis (Perleche) kann anfänglich Ähnlichkeit mit einer Gingivostomatitis herpetica haben. Orale Kandidose; habituelle Aphthen; Impetigo contagiosa in der perioralen Region, betrifft aber nicht die Mukosa. Herpangina: nicht so ausgeprägt. Sekundäre Infektion mit HSV Herpes simplex und Herpes-simplex-Rezidive Synonyme. Fieberbläschen, Gletscherbrand Klinik. HSV-Rezidive werden meist durch Triggerfaktoren verursacht: z.B. Infekte, Fieber, körperliche Anstrengung, psychischen Stress; Sonnenlicht (bzw.UV) Exposition. Inkubationsyeit: 2–5 Tagen; Prodromi: Spannungsgefühl und Juckreiz, gelegentlich auch Schmerzen an. Anschließend treten isolierte oder gruppiert stehende Bläschen auf einem erythematösen, ödematösen Hof auf Nach wenigen Tagen rupturieren die Bläschen und hinterlassen polyzyklisch begrenzte Erosionen, auf denen sich Krusten bilden. Nach einigen Tagen fallen die Krusten ab. Abheilung in der Regel ohne Narben. Bakterielle Sekundärinfektionen mit Impetiginisation können zu flach-narbiger Abheilung führen. Die Lymphknoten können geschwollen und druckdolent sein. Krankheitsdauer liegt zwischen 7 und 14 Tagen. Lokalisation: am häufigsten perioral (Herpes simplex labialis), im Gesicht (Naseneingang, Wangen, Ohrläppchen, Augenlidern), Identische klinische Bilder können auch am übrigen Körper vorkommen. Der Herpes kann die Mundschleimhaut betreffen. Zu einer Nagelbettentzündung durch Herpes simplex kommt es nicht selten durch Selbstinokulation von Patienten mit Herpes labiales die an den Fingernägeln kauen. Die Herpes-simplex-Erkrankung der Hornhaut nimmt eine besondere Stellung ein. Sie wird in der Ophthalmologie in 3 verschiedene Formen eingeteilt: Keratitis dendritica: Befall des Hornhautepithels; Keratitis interstitialis: tiefe Entzündung des Hornhautstromas; Endotheliitis oder Keratitis disciformis: Infektion des Hornhautendothels. Das Herpesvirus kann auch andere Augenabschnitte befallen, insbesondere die Konjunktiva, die Uvea (Herpesuveitis) und die Retina (Herpesretinitis). Komplikation: Eczema herpeticatum. Im Rahmen von Erkrankungen mit defekter epidermaler Barrierefunktion (z.B. atopisches Ekzem) oder mit Immunschwäche (AIDS) kommt es zu einer raschen HSV-Ausbreitung. Diese kann entweder von Zelle zu Zelle, lymphogen oder hämatogen erfolgen. Es handelt sich um eine generalisierte HSV-Infektion mit Allgemeinsymptomatik. Erythema multiforme. Bei manchen Patienten mit Herpes simplex recidivans tritt 5–14 Tage nach der Herpesinfektion, meist einem Herpes simplex labialis auf. Es handelt sich um ein Exanthem, vorwiegend an Handrücken, Unterschenkeln und Füßen, seltener am Rumpf verteilt. Auch Schleimhautbeteiligungen im Mund und am Genitale sowie an den Konjunktiven können auftreten. Die Erkrankung kann mit Fieber und allgemeinem Krankheitsgefühl einhergehen. Differenzialdiagnose. Am Mundwinkel ist Perleche (Faulecken; Angulus infectiosus) zu erwägen. Manchmal ist es, besonders bei größeren Herden im Gesicht, schwierig von einem Herpes zoster zu unterscheiden. Ein abortiver Herpes zoster mit nur wenigen Bläschen kann ebenfalls differenzialdiagnostische Schwierigkeiten bereiten. Kleinblasige Impetigo contagiosa. Herpes simplex recidivans am Nagelorgan von Fingern oder Zehen kann mit Panaritien verwechselt werden. Cheilitis attinica und beginnendes squamozelluläres Epiteliom an der Unterlippe und am Lippenrot (Anamnese). Therapie Topisch: mehrere topische Virostatika werden angeboten, haben sich jedoch bei kritischer Überprüfung kaum oder nicht krankheitsverkürzend erwiesen. Sie enthalten Aciclovir, Penciclovir oder Idoxuridin. Besser adstringierende Externa anwenden. Auch die lokale Kühlung wird von manchen Patienten als angenehm empfunden. Alkoholische Lösungen (z.B. Umschläge mit Äther). Systemisch: meist reicht eine orale Therapie mit Aciclovir oder Valaciclovir aus. Herpes genitalis Er kann sowohl Ausdruck einer Primärinfektion als auch einer Sekundärinfektion durch HSV sein. 80–90% der Fälle sind durch HSV 2, 10–20% der Fälle durch HSV1 verursacht. Klinik. Es gibt verschiede lokalisierte Herpesvarianten: Vulvovaginitis herpetica Cervicitis herpetica Proktitis herpetica Urethritis herpetica Balanoposthitis herpetica Beteiligung des Penisschafts, der Glutäal-, der Perineal- und der Perianalregion. Die primäre Infektion beim Herpes simplex genitalis erfolgt meist asymptomatisch. Bei einem symptomatischen Verlauf treten meist gruppiert angeordnete kleine Bläschen auf entzündlich geröteter und ödematöser Haut oder Schleimhaut auf, die zunächst klar erscheinen, später eintrüben, dann erodieren und gelegentlich auch in polyzyklisch begrenzte Ulzerationen übergehen können. In der Mehrheit der Fälle kommt es zur regionalen Lymphadenitis mit vergrößerten und druckdolenten Lymphknoten. Dem Krustenstadium folgt innerhalb von 8–12 Tagen narbenlose Abheilung. Patienten mit einem durch HSV 2 bedingten Herpes genitalis entwickeln signifikant häufiger Rezidive als Patienten mit genitaler HSV 1-Infektion. Differenzialdiagnose. Erosionen oder Ulzera bei Geschlechtskrankheiten (Ulcus molle, Ulcus durum,Granuloma venereum, Lymphogranuloma venereum). Therapie Wie bei Herpes simplex. Erkrankungen durch Varizella-Zoster-Virus (VZV) Das VZV ruft sowohl die Primärerkrankung Varizellen als auch die Sekundärinfektion Zoster hervor. Da diese Erkrankungen vom selben Erreger verursacht werden, ist es möglich, dass eine Varizelleninfektion durch Kontakt zu einem Zoster-Patienten hervorgerufen wird. Daher sollten Patienten mit Zoster nicht mit Patienten mit primärer oder sekundärer Immunsuppression in Kontakt gebracht werden. Üblicherweise ist die Kontagiosität des Zoster gering. Die Varizellen stellen die Erstinfektion mit dem VZV bei einem seronegativen Individuum dar. Obwohl durch die Erkrankung eine weitgehende Immunität ausgelöst wird, persistieren die Erreger in den sensiblen Ganglien lebenslang. Beim Zoster handelt es sich entweder um die Folge einer Reinfektion oder –wahrscheinlich häufiger– um eine endogene Reaktivierung des zuvor erworbenen VZV. Das Virus befällt normalerweise nur einen sensiblen Nerv und dessen Dermatom, seltener 2 oder mehr Dermatome. Weltweit nimmt die Erkrankungsrate an Zoster zu; etwa 20% aller Menschen sind betroffen Ursachen liegen sicher in der höheren Lebenserwartung, daher auch die Zunahme von Patienten mit akquirierter oder iatrogener Immunsuppression. Zoster kommt in jedem Lebensalter vor. Die Vorstellung, dass der Zoster eine Erkrankung des höheren Lebensalters sei, gilt heutzutage nicht mehr; etwa 1/4 aller Zoster-Patienten sind jünger als 40 Jahre. Normalerweise rezidiviert die VZV-Infektion nur einmal im Leben. Patienten, die in einem frühen Lebensalter einen Zoster entwickeln, sollten bezüglich ihres Immunstatus untersucht werden. Ätiopathogenese vom Zoster: endogene Reaktivierung des VZV, wobei das Virus nach der Erstinfektion in den sensiblen Ganglien persistiert und nach Jahren oder Jahrzehnten durch örtliche oder systemische Provokation reaktiviert wird. Bei der Reaktivierung des VZV wird ein größerer Teil des Ganglions zerstört. Dies führt zum akuten Zoster-Schmerz. Die Entzündung im Nervengewebe kann Narben verursachen, welche so die postzosterische Neuralgie auslösen. Der akute Zoster-Schmerz kann bereits etwa 4–5 Tage vor der Hauteruption einsetzen und zeichnet sich meist durch stechenden oder brennenden Charakter aus; üblicherweise sistiert er nach 4 Wochen. Von einer postzosterischen Neuralgie wird gesprochen, wenn die Schmerzen länger als 4 Wochen nach abheilen der Hautveränderungen fortbestehen. Die postzosterische Neuralgie tritt bei 15–30% aller an Zoster-Erkrankten auf. Die Häufigkeit steigt deutlich mit dem Alter an. Besondere Manifestationen des Zoster Zoster ophthalmicus Zoster im Ausbreitungsgebiet des ersten Trigeminusasts; bei ca. der Hälfte der Patienten treten okulare Komplikationen auf. Der Befall der Nasenspitze deutet auf die Beteiligung des N. nasociliaris und damit einen okularen Mitbefall hin. Alle Patienten mit einem Zoster ophthalmicus sollten augenärztlich bezüglich Konjunktivitis, Episkleritis, Iritis, Keratitis oder Chorioretinitis und Augenmuskellähmungen untersucht und nachkontrolliert werden. Therapie der Varizellen Topisch: austrocknende Maßnahmen wie Zinkoxidlotionen sind meist ausreichend. Bei Impetiginisation ist eine frühzeitige antiseptische Externatherapie indiziert. Systemisch: der unkomplizierte Varizellenverlauf erfordert keine innerliche Behandlung. Schwere Varizellenverläufe, Immunmangelzustände sowie Varizellen während der Schwangerschaft und bei Neugeborenen stellen eine Indikation zur Aciclovirtherapie dar. Weitere Empfehlungen. Bei Varizellenexposition einer varizellentiternegativen Schwangeren kann durch die Gabe von VarizellaZoster-Immunglobulin in bis zu 80–90% der Fälle eine mütterliche Varizellenerkrankung abgeschwächt oder sogar verhindert werden, wenn die Prophylaxe spätestens 72–96 h nach Exposition erfolgt. Außerdem scheint die Postexpositiosprophylaxe die Infektionsrate des ungeborenen Kindes zu reduzieren. Therapie des Zosters. Der Zoster wird antiviral und – so weit erforderlich– antiphlogistisch, analgetisch oder auch antiinfektiös behandelt. Topisch: im Initialstadium sind austrocknende Maßnahmen angezeigt. Nach dem Eintrocknen der Bläschen sind Cremes, später Salben mit antiseptischem Zusatz anzuwenden. Im Gesicht sollte keine Zinkschüttelmixtur angewendet werden, da die Zinkpartikel leicht in das Auge übertragen werden und zu Reizungen führen.. Systemisch eine interne Therapie sollte spätestens 72 h nach Auftreten der Hautsymptome eingeleitet werden. Therapieschemata des Zoster PYODERMIEN Infektionen der Haut und der Hautanhangsgebilde, welche durch Eitererreger, zumeist Staphylokokken und Streptokokken, verursacht werden. Impetigo contagiosa Epidemiologie. Staphylococcus aureus ist heute der führende Erreger und kann auch mehrheitlich bei den kleinblasigen Varianten isoliert werden. Die Bedeutung von Streptococcus pyogenes, vorzugsweise Gruppe A, hat dagegen deutlich abgenommen. Übertragung von Mensch zu Mensch erfolgt insbesondere durch Schmierinfektion. Ätiopathogenese. Invasion von Eitererregern in oberflächliche Epidermisschichten. Die Übertragung erfolgt über direkten Kontakt von Haut zu Haut. Das Eindringen der Erreger wird durch vorbestehende Mikroläsionen, in Form von kratzbedingten Mikrotraumen, oder vorbestehenden Erkrankungen wie einem atopischen Ekzem, einer Skabies oder Windpocken begünstigt. Klinik. Überwiegend im Gesicht, jedoch auch an allen anderen Körperstellen, entstehen zunächst kleine rote Makulä, die rasch in stecknadelkopfgroße, prall gespannte, wasserklare Bläschen übergehen, die von einem schmalen Entzündungshof umgeben sind. Bei der kleinblasigen Impetigo contagiosa ist die Bläschendecke sehr dünn und platzt rasch. Aus dem Blasengrund setzt eine starke Exsudation ein, die nach Eintrocknen zu Krustenbilung führt. Im Vordergrund des klinischen Bilds stehen daher honiggelbe Krusten auf gerötetem Untergrund. Die großblasige Impetigo contagiosa (Synonym:bullöse Impetigo) ist durch das Vorhandensein intakter Blasen charakterisiert, die sich auch auf unbefallener Haut ausbilden können. Nach Zerstören der Blasendecke erscheinen gerötete erodierte, feuchte Flächen. Verkrustungen wie bei der kleinblasigen Impetigo fehlen im Allgemeinen. Manchmal, insbesondere bei starker Ausdehnung, besteht ein ausgeprägter Juckreiz, der die weitere Ausbreitung der Erkrankung fördert. Meistens fehlen die Allgemeinsymptome. Die Abheilung erfolgt narbenlos. Häufig bleiben vorübergehende Resterytheme zurück. Differenzialdiagnose Die klinisch honiggelben Erscheinungen bereiten nur ausnahmsweise differenzialdiagnostische Schwierigkeiten. Nicht einfach ist manchmal die Abgrenzung zwischen Impetigo oder sekundär impetiginisierten Dermatosen, insbesondere Herpes simplex (polyzyklisch begrenzte Erosionen); in der Anamnese häufig die Angabe von Rezidiven. Therapie. Haupsächlich lokal mit fusidinsäurehaltigen Medikamenten als Mittel der Wahl Systemische Therapie (orale Gabe von Antibotikum) nur bei sehr ausgedehntem Hautbefall oder bei Allgemeinsymptomatik. Erysipel Häufige akute Infektionskrankheit der Haut, insbesondere des Gesichts und der Extremitäten, ist bei erstmaligem Auftreten in der Regel mit Fieber und Schüttelfrost verbunden. Ätiopathogenese. In etwa 80% sind Streptokokken, bevorzugt β-hämolysierende Streptokokken der Gruppe A, daneben aber auch Vertreter der Gruppen B, C und G, auslösend. Darüber hinaus kommen eine Vielzahl weiterer Bakterien in Betracht, so Staphylococcus aureus oder gramnegative aerobe sowie anaerobe Erreger. Der Erreger tritt meist durch eine Hautstelle mit gestörter Barrierefunktion ein, z.B. Tinea pedum, Ulcus cruris venosum, Bagatellverletzungen, bei Rhagaden und Erosionen etwa am Naseneingang, bedingt durch chronische Entzündung (chronische Rhinitis). Risikogruppen sind Patienten nach größerem Trauma (Operation, Fraktur, Strahlentherapie), bestehende Adipositas permagna, Herzinsuffizienz oder übermäßiger Alkoholkonsum. Beim Erysipel wird der lymphatische Hautabfluß beteiligt und gestört, sodass sich sehr oft ein Lymphödem entwickeln kann. Klinik. Die gewöhnlich asymmetrische Erkrankung beginnt unter dem Bild einer akuten Dermatitis mit Spannungsgefühl und Druckschmerz. Rasch folgen flächenhafte intensive Rötung und Schwellung (Lymphödem), die peripher wachsen, aber stets zur Umgebung hin scharf begrenzt bleiben ("segno dello scalino"). Typisch sind zungenförmige oder unregelmäßige Ausläufer. Das betroffene Gebiet ist heiß. Periphere Ausbreitung mit Lymphangitis, Lymphadenitis mit Fieber bis zu 40°C und Schüttelfrost begleitet. Die Blutsenkungsgeschwindigkeit ist stark erhöht; im Blutbild lässt sich eine neutrophile Leukozytose feststellen. Auf dem Erythem können Bläschen und große Blasen auftreten (Erysipelas vesiculosum et bullosum). Besonders an den stasisabhängigen Körperpartien kann das Erysipel hämorrhagisch-blasig werden. Selten ist die nekrotische Verlaufsform (Erysipelas gangraenosum). Besonders häufig und gefährlich ist ein Gesichtserysipel, wenn es über dem Nasensattel beginnt und eine schmetterlingsförmige Ausbreitung mit beidseitigem Lidödem annimmt. Ausdehnung auf Orbita und Sinus sagittalis mit Sinusthrombose sind als mögliche Komplikationen gefürchtet. Das Erysipelas phlegmonosum entsteht als schwerste Krankheitsform auf der Basis von infektiösen Entzündungen mit Abszessen. Vielfach sind dann auch Staphylokokken nachzuweisen. Besonders gefährdet sind die Augenlider (Lidnekrose) sowie Orbita und Mittelohr. Differenzialdiagnose. In erster Linie ist die akute Kontaktdermatitis (kein Fieber, keine Erhöhung der Blutsenkungsgeschwindigkeit, häufig allergische Streuphänomene, Juckreiz) abzugrenzen. Auch ein mit starker Entzündungsreaktion einhergehendes Erythema migrans kann in seltenen Fällen differenzialdiagnostische Schwierigkeiten bereiten. Beginnender Herpes zoster im Gesicht kann von einem Erysipel schwer abzugrenzen sein. Erysipeloid sitzt bevorzugt an den Händen, weist einen mehr blauroten Farbton auf und entwickelt sich langsamer. Fieber besteht nicht. Die Berufsanamnese ist hilfreich. Hypodermitis nach Trauma oder bei chronisch-venöser Insuffizienz ist lokalisiert, die Konsistenz, bei der Palpation, ist hart. Verlauf ohne Fieber und Lymphknotenschwellung. Verlauf. Bei rechtzeitiger adäquater Behandlung kommt es zur Abheilung, wobei aber chronische Schwellungszustände, bedingt durch Okklusion von Lymphgefäßen, zurückbleiben können. Bei manchen Patienten entwickelt sich in identischer Lokalisation von Zeit zu Zeit immer wieder ein Erysipel: chronisch-rezidivierendes Erysipel. Die Intervalle zwischen den Manifestationen können wenige Wochen betragen. Ursachen für chronisch-rezidivierende Erysipele sind nicht erkannte oder nicht sanierte Eintrittspforten, zumeist eine mazerative Tinea pedum. Zusätzliche Risikofaktoren sind kongenitales Lymphödem, chronisch-venöse Insuffizienz und eine periphere Verschlusskrankheit. Auch die Entwicklung eines Toxinschocksyndroms im Rahmen eines Erysipels ist möglich. Therapie. Durch die Gabe von Antibiotika ist rasche Besserung zu erreichen, das weitere Fortschreiten der Erkrankung wird verhindert. Bei ausgeprägten Fällen mit schwerer Allegemeinsymptomatik ist eine i. v. Behandlung empfehlenswert. Topisch. Antiseptika (Chlorhexidinglukonatlösung) werden eingesetzt; fusidinsäurehaltige Externa (Cremen, keine Salben) können appliziert werden. Im Fall einer Gangrän sind oft eine nekrolytische Therapie oder chirurgische Versorgung angezeigt. Weitere Empfehlungen. Bettruhe mit Ruhigstellung und Hochlagerung des erkrankten Körperabschnitts; elastische Kompressionsbandage. Beim chronisch rezidivierenden Erysipel sollten prädisponierende Faktoren ausgeräumt werden. Mögliche Eintrittspforten (wie mazerative Interdigitalmykose) sowie bestehende Risikoerkrankungen (wie Gefäßerkrankungen) sollten saniert bzw. behandelt werden. Lyme-Borreliose Synonyme. Borrelia-burgdorferi-Infektion, disease. europäische Zeckenborreliose, Erythema-migrans-Krankheit, Lyme Definition. Das Krankheitsbild wird nach internationaler Vereinbarung als Lyme-Borreliose bezeichnet. In Abhängigkeit von der infizierenden Art von Borrelia burgdorferi und der Immunreaktion kommt es zu verschiedensten Organmanifestationen, am häufigsten an Haut, Gelenken, Herzmuskel sowie zentralem und peripherem Nervensystem. Epidemiologie. Die Übertragung von Borrelia burgdorferi ist an Vektoren gebunden. Hauptvektoren sind Schildzecken der Gattung Ixodes, wie Ixodes ricinus in Europa. Mit erheblichen regionalen Unterschieden beherbergen 4–60% dieser Zecken Borrelia burgdorferi in ihrem Mitteldarm. Nicht nur die ausgewachsenen Tiere, sondern auch die vorausgehenden Entwicklungsstadien, vor allem die Nymphen können den Erreger übertragen. Hierzu ist eine Saugzeit von mehreren Stunden erforderlich. Der Stich selbst bleibt wegen seiner Schmerzlosigkeit und der geringen Größe von Larven und Nymphen (etwa 1 mm) häufig unbemerkt. Als mögliche Vektoren von Borrelia burgdorferi kommen neben Schildzecken auch Stechbremsen (Tabaniden) in Betracht. Jedoch ist die Saugzeit sehr kurz, sodass es selten zur Übertragung kommt. Durch Gensequenzanalysen lassen sich 4 humanpathogene Arten von Borrelia burgdorferi sensu lato unterscheiden: Borrelia burgdorferi sensu stricto, Borrelia afzelii, Borrelia garinii und Borrelia valaisiana Vorkommen und Krankheitsassoziationen der humanpathogenen Borrelia-burgdorferi-Arten Klinik. Die Borreliaburgdorferi - Infektion zeichnet sich durch eine große Vielfalt von Krankheitsmanifestationen aus. Die unterschiedlichen Verläufe sind nicht nur durch die individuell unterschiedliche Immunreaktion auf Borrelien zu erklären, sondern auch auf die verschiedenen Arten mit unterschiedlichem Organtropismus zurückzuführen. In Nordamerika wird häufiger ein schwererer Verlauf mit deutlichen Anzeichen einer systemischen Infektion, multiplen Erythemata migrantia und Arthritiden durch Borrelia burgdorferi sensu stricto beobachtet. In Europa treten häufiger neurologische Symptome in Verbindung mit Borrelia-garinii-Infektion auf. Am häufigsten wird Borrelia afzelii aus Erythema migrans und Acrodermatitis atrophicans nachgewiesen. Der Verlauf der Infektion wird in 3 Stadien eingeteilt. Verlauf der Lyme-Borreliose Stadium I: lokalisierte Frühinfektion. Während des Saugakts der Zecke werden Borrelien in das Gewebe des Wirtsorganismus übertragen. Klinisch wird diese Auseinandersetzung von Erregern mit der Immunabwehr als mehr oder weniger starke Entzündungsreaktion. Die Entzündung kann im Erscheinungsbild äußerst variabel sein. Erythema migrans Klinisch ist ein randbetontes wanderndes Erythem mit zentrifugaler Ausbreitung um die Einstichstelle der Zecke herum, das sich nach einem freien Intervall von wenigen Tagen bis einigen Wochen (mittlere Inkubationszeit 10 Tage) zunächst homogen entwickelt. Die Einstichstelle der Zecke kann als kleine Papel oder polsterartige blau-rötliche Schwellung erkennbar bleiben. Meist blasst das Erythem zentral ab und schreitet zentrifugal mit hell-rötlichem Randsaum fort. Es kann in wechselnder Intensität über viele Monate bestehen bleiben (Erythema chronicum migrans). In seltenen Fällen kann es spontan oder nach ungenügender antibiotischer Behandlung rezidivieren. Etwa 1/3 der Patienten klagen über lokalen Juckreiz, seltener über Hitzegefühl oder brennende Schmerzen im Herd. Abweichende Varianten sind häufig. Insbesondere an den Beinen sind in frühen Stadien flammend rote, erysipelähnliche Veränderungen möglich. Etwa 2/3 der Patienten klagen über grippeähnliche, auf eine Allgemeininfektion hindeutende Beschwerden. Am häufigsten sind Krankheitsgefühl, Abgeschlagenheit oder Kopfschmerzen, seltener flüchtige, wandernde Gelenkschmerzen, Myalgien sowie leichtes Fieber. Die Abgrenzung von hyperergischen Insektenstichreaktionen kann schwierig sein. Fehlender Juckreiz und langsam zunehmende Entzündung sprechen für eine frühe Hautborreliose. Flammend rote Erytheme werden als mitigiertes Erysipel, fixe toxische Arzneimittelreaktion oder Hypodermitis verkannt. Eine nur leicht schuppende randbetonte Tinea corporis könnte in Erwägung gezogen werden. Infektion während der Schwangerschaft. Borrelia burgdorferi kann die Plazentaschranke überwinden und zur Infektion des Fetus führen. Das Risiko hierfür ist nach prospektiven Untersuchungen von Schwangeren gering. Es wurden aber einzelne Fälle von intrauterinem Fruchttod sowie kongenitalen Defekten des Neugeborenen beschrieben. Schwangere sollten nach einem Zeckenstich besonders sorgfältig klinisch und serologisch überwacht und so früh wie möglich behandelt werden. Therapie. Es ist besonders wichtig, dass ausreichend hoch dosiert und ausreichend lang behandelt wird. Die Frühinfektion sollte 2–3 Wochen, Spätmanifestationen 3–4 Wochen behandelt werden. Therapie der Wahl bei Erythema migrans sind: Doxycyclin 2 x 100 mg/Tag oder Amoxicillin 4 x 500 mg/Tag. Doxycyclin ist bei Kindern unter 9 Jahren und in der Schwangerschaft sowie Stillzeit kontraindiziert. Diese Patienten erhalten Amoxicillin. MYKOSEN Einführung Mykosen sind durch Pilze bedingte Infektionskrankheiten; Dermatomykosen sind Pilzerkrankungen der Haut und der angrenzenden Schleimhäute. Bei den Dermatomykosen lassen sich unterscheiden: oberflächliche Mykosen Dermatophytosen und kutane Mykosen subkutane Mykosen die medizinisch relevanten Pilze sind: Dermatophyten, Hefe- und Schimmelpilze (D-H-S-System). Die medizinisch relevanten Dermatophyten gehören unterschiedlichen Gattungen an: Trichophyton mit den Hauptvertretern Trichophyton rubrum und Trichophyton mentagrophytes, Microsporum unter anderem mit Microsporum canis, Epidermophyton mit Epidermophyton floccosum. Unter den Hefepilzen hat Candida albicans eine zentrale Bedeutung, des Weiteren ist die lipophile Hefe Malassezia furfur (Pityrosporum ovale) zu erwähnen. Diagnostisches Vorgehen. Die Diagnose einer Mykose gründet sich auf klinische und laboratoriumsmedizinische Untersuchungen: klinisches Bild, mikroskopische Untersuchung (Nativpräparat), mykologische Kultur. Oberflächliche Mykosen Sie werden vor allem von Hefen hervorgerufen; die Hauptrolle spielt Malassezia furfur. Pityriasis versicolor Eregger: die lipophile Hefe Malassezia furfur. Starkes Schwitzen bei Seborrhö begünstigt das Auftreten. Klinik. Prädilektionsstellen sind die talgdrüsenreiche Brust und Rückenmitte. Man findet scharf umschriebene, milchkaffeefarbene oder bräunliche oder depigmentiert-wießliche (Pityriasis versicolor alba) Flecke. Differenzialdiagnose. Vitiligo und Pseudoleukoderme sind abzugrenzen. Dermatophytosen Die durch Dermatophyten hervorgerufenen Erkrankungen werden als Dermatophytosen oder Tinea bezeichnet. Letzterer Begriff wird durch Angabe der Lokalisation qualifiziert. Bei Befall des Fußes spricht man beispielsweise von Tinea pedis. Tinea capitis Mit diesem Begriff wird die Dermatophytose von behaartem Kopf, Augenbrauen und Augenwimpern bezeichnet. Klinisches Bild unterschiedlich je nach Pilzgattung. Tinea barbae Heute recht seltenen Dermatophyteninfektion der Bartregiones entsteht insbesondere bei Kontakt mit infizierten Großtieren, speziell Rindern. Tinea faciei und Tinea corporis Die Erkrankung tritt vor allem bei Kindern und Jugendlichen auf. Erwachsene werden, wenn überhaupt, vor allem im Rahmen ausgedehnter Tineaerkrankungen betroffen. Alle Dermatophytengattungen können das Krankheitsbild hervorrufen. Z. B. Microsporum canis bei Kindern nach Kontakt mit weitgehend erscheinungsfreien Spieltieren, speziell Katzen. Unter den Trichophyten sind Trichophyton rubrum und Trichophyton mentagrophytes anzuführen. Klinik. Insbesondere bei Kindern können scharf begrenzte, scheibenförmige, sich zentrifugal ausbreitende bogige Herde entwickeln. Bemerkenswert sind die Abheilung der Herde im Zentrum und ihr peripheres Fortschreiten. Dadurch entstehen charakteristische Ringformen. Es besteht Juckreiz. Differenzialdiagnose. Psoriasis vulgaris, Mycosis fungoides, nummuläres Ekzem, Ekzematide, Rosazea. Entscheidend ist stets der Pilznachweis. Tinea manus Auffällig sind die Einseitigkeit oder deutliche Asymmetrie der Hauterscheinungen. Differenzialdiagnose. Handekzeme unterschiedlicher Genese (doppelseitig), Psoriasis palmaris (Psoriasis an anderer Stelle). Tinea pedis Synonyme Fußmykose, Fußpilzerkrankung, Athletenfuß Die Tinea pedis ist eine der häufigsten dermatologischen Erkrankungen. Die verursachenden Pilze sind fast ubiquitär. Ihre Sporen sind monatelang in der Umwelt virulent, beispielsweise in Schuhen, Holzrosten der Schwimmbäder und Turnhallen, Badematten und Hotelteppichen. Eine wichtige Prophylaxe ist die Fußhygiene, insbesondere das sorgfältige Abtrocknen der Zehenzwischenräume nach dem Baden oder Duschen und das Tragen möglichst offener Schuhe. Klinik. Das klinische Bild entspricht dem der Tinea manus. Am häufigsten sind die intertriginöse und die squamös-hyperkeratotische Tinea pedis, seltener die dyshidrosiforme und am Fußrücken die erythematöse Variante. Differenzialdiagnose. Ekzeme unterschiedlicher Genese (doppelseitig), Psoriasis plantaris (Psoriasis an anderer Stelle), plantare Hyperkeratosen. Verlauf. Bei Fußmykosen meist über Jahre chronisch intermittierend. Als wichtige Komplikation sind Erysipele der Unterschenkel zu nennen, für die Erosionen und Rhagaden zwischen den Zehen die häufigste Eintrittspforte darstellen Tinea unguium Alternativ wird auch der Begriff Onychomykose verwendet. Unter den Nagelerkrankungen machen Onychomykosen 18–40% aus. Sie betreffen Erwachsenen. Die Tinea unguium betrifft häufiger die Füße als die Hände zunächst einzelne Nagelorgane. Differenzialdiagnose. Psoriasis vulgaris des Nagelorgans, traumatische, mechanisch-bedingte Onychodystrophie. 20% der Kandidosen Pilzerkrankungen durch Erreger der Gattung Candida. In der Regel betreffen sie Haut und angrenzende Schleimhäute. Unter der Vielzahl von Candidaarten kommt Candida albicans die wesentliche Bedeutung zu. Der Keim gehört zur normalen Flora. Insbesondere in der Mundhöhle und am äußeren Genitale lässt sich nicht selten Candida albicans nachweisen, ohne dass Krankheitserscheinungen bestehen. Der bloße Nachweis des Erregers in menschlichem Untersuchungsmaterial stellt daher noch keine Indikation zur antimykotischen Behandlung dar. Sie ist nur angezeigt, wenn weitere Gründe sie notwendig machen, z.B. entzündliche Veränderungen oder die Gefahr der Generalisation bei extremer Abwehrschwäche. THERAPIE DER MYKOSEN Richtige Behandlung setzt eine exakte Diagnose durch den Nachweis des Erregers im Nativpräparat und in der Kultur voraus. Die Behandlung richtet sich nach der Lokalisation (freie Haut, intertriginös, behaarter Kopf, Nägel), der Akuität (akute oder chronische Entzündung), der Tiefe der Infektion (oberflächlich oder tief) und schließlich nach der Kontagiosität (bei Mikrosporie ist auch die Notwendigkeit des Schutzes der Umgebung zu bedenken). Systemische Therapie. Zur peroralen Therapie der Dermatophytosen der freien Haut sowie des Kapillitiums – hier speziell ist eine systemische Therapie unverzichtbar – stehen 3 unterschiedliche Antimykotikasubstanzklassen zur Verfügung: Griseofulvin, Azole wie Itraconazol und Fluconazol Allylamin (Terbinafin). Griseofulvin ist ein Schmalspektrumantimykotikum, das im Wesentlichen nur Dermatophyten erfasst. Entsprechendes gilt für Terbinafin. Terbinafin hat einen Durchbruch in der Therapie der Tinea unguium gebracht. Bei Ketoconazol und Itraconazol sowie Fluconazol handelt es sich um Breitspektrumantimykotika. Alle Substanzen gelangen nach Aufnahme über den Magen-Darm-Trakt in die Blutbahn und dann in erheblichem Umfang in die Haut. Therapeutisch kommt insbesondere der Anreicherung in der Hornschicht Bedeutung zu, dem Sitz der Erreger. Literatur-Quelle: Braun Falco, Plewig, Wolff, Burgdorf, Landthaler: "Dermatologie und Venereologie" 5. Auflage – Speringerverlag