1 - Ihre Homepage bei Arcor
Werbung

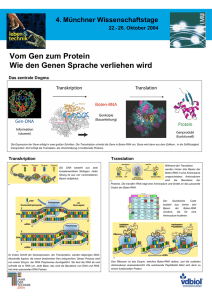
1) Der Unterschied zwischen Hämoglobin A und Hämoglobin S besteht in ihren Aminosäuresequenzen: bei Hämoglobin A befindet sich an der 6. Stelle des Ausschnitts der Aminosäurekette ein Glutaminsäure (Glu), während sich in der Kette des Hämoglobin S ein Valin (Val) befindet. 2)2. Das Hämoglobin entsteht durch Transkription der Information des Gens und die darauffolgende Translation am Ribosomen. Die Transkription funktioniert folgendermaßen: Die DNS-Kette, auf welcher sich die zu transkibierende genetische Information befindet, bezeichnet man als „codogenen Strang“. Der transkibierte Strang (die Transkription geschieht durch komplementäre Basenpaarung) heißt mRNS-Strang. Daraufhin kann man in der Code-Sonne ablesen, welche Basensequenz im mRNS-Strang welche Aminosäure codiert. Die Basentripletts GUU, oder GUC oder GUA verschlüsseln beispielsweise die Aminosäure Valin (Val), welche sich am Anfang der Aminosäuresequenz sowohl im Hämoglobin A als auch im Hämoglobin S, befindet. Durch die Translation (auch als „Proteinbiosynthese“ bezeichnet) der (genetischen) Information der mRNS entsteht schließlich eine Polypeptidkette, wobei es sich meistens um Enzyme handelt – in diesem Fall jedoch um ein Hämoglobin-Molekül. Dieser Vorgang läuft folgendermaßen ab: Am Ribosomen befinden sich zwei Bindungsstellen für beladene tRNA, die P- und die ABindungsstelle. Um die Proteinbiosynthese zu starten, lagert sich eine mit der Aminosäure Methionin beladene tRNA (durch komplementäre Basenpaarung) an das Startcodon der mRNA an, der sich bei der P-Bindungsstelle befindet. Daraufhin bindet sich eine weitere mit einer Aminosäure beladene tRNA an die noch freie A-Bindungsstelle - hier die Aminosäure Histidin. Es folgt die Verknüpfung der beiden freigewordenen Aminosäuren (das Methionin bindet sich an das Histidin), wobei die tRNA der P-Bindungsstelle aminosäurefrei frei wird und sich ablöst. Diese tRNA wandert ins Cytoplasma und die mRNA wird um ein Codon verschoben. Die tRNA der A-Bindungsstelle, an der sich die beiden verknüpften Aminosäuren (die Peptidkette) befinden, muss in die frei gewordene P-Bindungsstelle wechseln. An die freie ABindungsstelle kann nun eine mit Leucin beladene tRNA geknüpft werden, usw. (bis die Peptidkette fertig gebaut ist). 3) Der Unterschied zwischen den beiden Hämoglobinmoleküle kam durch Genmutation zustande. Solche Mutationen geschehen beispielsweise durch Wegfall einer Base aus dem codogenen Strang (die anderen Basen rücken dann dementsprechend auf und es entstehen neue Basentriplette) oder durch Austausch einer oder mehrerer Basen aus dem codogenen Strang durch eine bzw. mehrere andere Basen. Die Folge eines solchen Wegfalls oder Austausches ist z.B. der Verlust der Funktion des Enzyms (wenn es sich bei dem Protein um ein Enzym handelt). Die weitere Folge ist dann außerdem folgende: Durch Transkription der Information des Gens, verändert sich die Codierung der Aminosäuresequenz durch die Basentriplette. Vermutlich ist die Genmutation bei Hämoglobin A durch den Austausch von zwei Thymin bei dem 6. Basentriplett durch zwei Adenin im codogenen Strang zustande gekommen. Dadurch entstand durch die Transkription im sogenannten Hämoglobin S ein komplementäres Basentriplett mit zwei Uracil, anstatt wie beim Hämoglobin A mit zwei Adenin. Der Wegfall einer oder mehrerer Basen ist ziemlich ausgeschlossen, da sehr viele Basen wegfallen müssten bzw. die Abstände zwischen den Basen, die wegfallen müssten zu groß wären, damit die Aminosäure Glu durch das neuentstandene Basentriplett codiert würden. – Außerdem kommt diese Art der Genmutation häufig in Malaria gefährdeten Gebieten vor, auch wenn generell solche bleibenden bzw. vererbbaren Genmutation ziemlich selten vorkommen normalerweise werden leichte Genmutationen, die beispielsweise durch die Strahlung bei Röntgenaufnahmen hervorgerufen werden, durch Enzyme wieder behoben - es wäre also unwahrscheinlich, dass so viele Basen wegfallen, bzw. gerade diejenigen, die für die Form des Hämoglobin-Moleküls verantwortlich sind. – Der „Virus“ wäre dann sicher nicht so weit verbreitet. 4) Dieses Hämoglobin-Molekül kann offenbar verschiedene Merkmale und Eigenschaften ausbilden. In diesem Fall ist dies durch Genmutation bedingt. – In einem Fall nimmt das Hämoglobin seine „normale“ runde Form an, in dem anderen jedoch eine Sichelform. Die Idee der klassischen Genetik, dass aus einem Gen ein Merkmal ausgebildet werden könne (bzw. dass ein Basentriplett auf dem codogenen Strang die Position einer Aminosäure im Protein bestimmt) ist durch die Genmutation im Grunde widerlegt, da man in diesem gedanklichen (theoretischen) Modell die Vorgänge der Transkription und der Translation, die zum Bereich der molekularen Genetik gehören, außer Acht lässt. Außerdem geschieht die Genmutation beispielsweise durch Wegfall oder Ersatz einer Base im codogenen Strang durch eine andere Base – diese Möglichkeit wird durch das klassische Modell ausgeschlossen, bzw. existiert nicht und wird somit negiert.