Document
Werbung

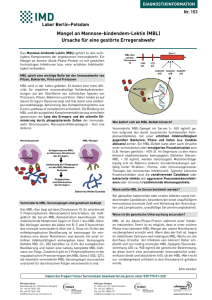
Mannose-binding-Lectin Defizienz, Tourette-Syndrom, ADHSyndrom und Multiple Sklerose Abstract In dieser Kasuistik wird die Krankengeschichte des jetzt 35-jährigen Mannes A. dargestellt, der auf Grund einer kompletten MBL-Defizienz an schweren Infekten im Säuglings- und Kleinkindalter litt, als Heranwachsender an einem Tourette-Syndrom, nachfolgend an einem ADH-Syndrom und einer Multiplen Sklerose. Es werden die einzelnen Krankheitsbilder beschrieben und pathophysiologische Zusammenhänge dargestellt. Eine Histaminämie kann nicht sicher zugeordnet werden. Inhaltsverzeichnis 1. Ziel der Arbeit Seite 2 2. Fallbeschreibung Seite 2 2. Labor Seite 3 4. Diagnose Seite 4 4.1. MDL-Defizienz Seite 4 4.1.1. Zusammenfassung Seite 9 4.1.2 Literatur Seite 9 4.2 Tourette-Syndrom Seite 11 4.2.1 Zusammenfassung Seite 13 4.2.2. Literatur Seite 14 4.3. ADHS-Syndrom und Histaminämie Seite 16 4.3.1. Zusammenfassung Seite 20 4.3.2. Literatur Seite 20 4.4. Multiple Sklerose Seite 22 4.4.1. Zusammenfassung Seite 23 4.4.2. Literatur Seite 24 1 5. Epikrise Seite 24 6. Therapie Seite 25 6.1. 7. 7.1. 1. Literatur Schlussfolgerungen Literatur Seite 25 Seite 25 Seite 27 Ziel der Arbeit: Es sollen pathophysiologische Zusammenhänge zwischen den genannten Erkrankungen dargestellt werden, um eventuell eine kausale Therapie abzuleiten 2. Fallbeschreibung: Anamnese: Ein männlicher Patient A., 1979 geboren, wurde als 16 Tage alter Säugling aus Chile nach Deutschland adoptiert. Der leibliche Vater wird in Schilderungen vor Ort als sozial auffällig mit der Berufsbezeichnung „Student“ beschrieben. T. selbst war bei der ersten Ansprache in Chile freundlich, äußerst lebhaft, vom Ernährungszustand leicht reduziert, mit einer deutlichen Bronchitis. Ansonsten waren körperliche Auffälligkeiten nicht feststellbar. In Deutschland angekommen, erwies er sich der Junge als hoch empfindsam bis schreckhaft, er litt an erheblichen Ein- und Durchschlafstörungen. Dieses Verhalten wurde zunächst auf die Umstellung der Umgebung und auf das unterschiedliche Klima zurückgeführt. Im Verlauf der Zeit war jedoch eine Besserung dieser Störung und auch der bronchitischen Infekte nicht erkennbar. Im Gegenteil: Es kam zu rezidivierenden Fieberschüben mit eitrigen Tonsillitiden, schweren Bronchitiden bis zur Pneumonie, so dass z.T. hoch dosierte Antibiotikabehandlungen notwendig wurden. Schließlich musste im Alter von 2 Jahren nach einem Anstieg der Retentionsparameter als Zeichen der Nierenbeteiligung bei Streptokokkenangina tonsillektomiert werden. Danach besserte sich der körperliche Zustand leicht und die Zahl und Schwere der Infekte ging zurück. Dennoch blieb eine gewisse Anfälligkeit, die auch heute noch besteht. Erwähnenswert ist eine Masernimpfung im Alter von 1 Jahr, die in eine 2 schwere Masernerkrankung mit delirantem Fieber mündete, ferner ein Pfeifer’sches Drüsenfieber, das über ca. 2 Jahre mit geschwollenen nuchalen Lymphknoten persistiert. Die psychische Entwicklung war von Beginn an gestört. A. war unkonzentriert, nicht gruppenfähig, auch in der Schule auffällig durch impulsives, unkontrolliertes Verhalten. In der Pubertät kam es dann zu einer Verstärkung der beschriebenen Symptome mit dissozialem Abgleiten. 1987- 1991 bestand ein Tourette-Syndrom mit einfachen vokalen und motorischen Tics. Die Vorstellung bei verschiedenen Fachkollegen ergab keine eindeutige psychiatrische Erkrankung. 2001 erfolgte die Diagnose einer sozialen Phobie anlässlich eines stat. Aufenthaltes in der psychosomatischen Fachklink in Bad Pyrmont. 2004 wurde erstmalig ein ADHS-Syndrom in den Rheinischen Kliniken des LVR Köln festgestellt und 2009 durch eine Fachkollegin bestätigt. Die Diagnostik erfolgte hier nach den Brown ADD-Scales, den Wender-Utah-Rating-Scales, den ADD in the Workplace in deutscher Fassung, Gespräche und einem Anamnesebogen. Es wurde eine Therapie mit Methylphenidat eingeleitet. 2008 wurde in der Neurologischen in Köln Merheim eine Encephalitis disseminata mit schubförmiger Verlaufsform, entsprechend EDSS 1,5-2,0, diagnostiziert mit einem vermuteten Bestehen seit 2005. Zunächst wurde mit Interferon Beta 1a (Avonex) behandelt, nach mehreren Schüben unter dieser Therapie erfolgte die Umstellung auf Tysabri. Seit dieser Zeit ist der Patient progressionsfrei. Jetzige Beschwerden und Einschränkungen: ADHS: Unruhe, Übererregbarkeit, Konzentrationsstörungen, massive Schlafstörungen Multiple Sklerose: eingeschränkte Motorik der rechten Hand, Schwäche und leichte Spastik linkes Bein bei eingeschränkter Gehstrecke von bis zu 500 m. Stolper- und Fallneigung. Müdigkeit, Abgeschlagenheit, allgemeine körperliche Schwäche. 3 3. Labor ASL vom: 03.06.91 ASL 213, 17.08.92; ASL 502 U/ml, 14.03.94 ASL 265 U/ml Mannose binding lectin vom: 07.03.13 <50 ng/ml (> 450), 09.07.13 MBL < 50 ng/ml Methyhistamin i.U. vom: 07.03.13 11,4 UR (normal < 0,6), vom 04.04.13 13,2 UR, vom 09.07.13 11,4 UR Histamin i.P. vom: 04.04.13 1,1 (normal < 0,8), vom 09.07.13 1,4 Diaminooxidase vom: 07.03.13 >30 SE (normal 3.0 – 10, Histaminintoleranz <3) Vitamin B6 vom: 07.03.13 92,3 ng/dl (normal 7 – 30), vom 04.04.13 74,3 Mastzelltryptase vom: 07.03.13 1,32 µg/l (geom. Mittelwert 3,8), vom 04.04.13 1,7 Gesamt IGE vom: 04.04.13 30 U/ml (normal bis 25) Eosinophile vom: 04.04.13 8 %(normal bis 6) 4. 4.1. Diagnosen: 1. MDL- Defizienz 2. Z.n. Tourette-Syndrom 3. ADHS-Syndrom 4. Multiple Sklerose MDL-Defizienz A. leidet seit seiner Geburt an einer Infektionsneigung, wie oben ausführlich dargestellt. Retrospektiv kann ein genetisch bedingter Immundefekt vermutet werden: Es fand sich ein 4 Titer des Mannose binding Lectin (MBL) <50 (normal>450 ng/ml). Damit besteht ein MBLassoziierter homozygoter Immundefekt. Funktion des MBL Abb. 1 aus (1) Das MBL ist ein Protein des angeborenen Immunsystems in Vertebraten. Es gehört zu den wichtigsten Komponenten der angeborenen Immunabwehr. MBL wird in der Leber gebildet. Es besitzt eine hohe Affinität für repetitive Mannose-haltige Kohlenhydratverbindungen auf der Oberfläche von zahlreichen Spezies von Protozoen, Pilzen, Bakterien und Viren. Daher bindet es auf diesen Erregern (Opsonierung) und löst damit eine antikörperunabhängige Aktivierung des Komplementsystems aus (Lectin-pathway of complement activation). Die Bindung von MBL und die ausgelöste Komplementaktivierung vermitteln gemeinsam die Lyse des Erregers und die schnelle Elimination durch phagozytierende Zellen der Immunabwehr (Granulozyten, Monozyten/Makrophagen) - first line defense. (s. Abb. 1) Das MBL-Gen liegt auf dem Chromosom 10. Es sind derzeit 5 Polymorphismen (Genvarianten) beschrieben, die maßgeblich die Serum-MBL-Konzentration beeinflussen. Drei inaktivierende Mutationen liegen im Exons 1 des MBL-Gens. Bei Vorliegen werden die Allele mit B, C und D bezeichnet, das normale unveränderte Allel mit A. Etwa ein Drittel der mitteleuropäischen Bevölkerung ist heterozygot für mindestens eine dieser Mutationen, was 5 Abb. 2 aus (1) bereits mit einer erhöhten Infektanfälligkeit einhergehen kann. Homozygote Defekte (BB, CC, DD) betreffen ca. 0,3% der europäischen Bevölkerung und haben eine nahezu komplette MBL-Defizienz zur Folge. Zusätzlich gibt es 2 Polymorphismen in der regulatorischen Promoterregion des MBL-Gens, die ebenfalls verminderten MBL-Serumspiegel verursachen und damit für die klinischen Folgen verantwortlich sind (1). s. Abb. 2 Man unterscheidet 7 Halotypen, die nach Bevölkerungsgruppen und -wanderungen unterschiedlich verteilt sind. In Südamerika bei den Mapuches, einem Indianerstamm, der auch in Chile, dem Herkunftsland von A. vorkommt, finden sich der funktionale Halotyp HYPA mit 48% und der defekte LYPB mit 43% (2). Eine erste Veröffentlichung über das MBL fand sich 1968 bei Miller, ME (3), der über eine gestörte Phagozytose bei rekurrenten bakteriellen Infektionen berichtete, 1989 wurde die physiologische Funktion des MBL dargestellt (4). Das MBL wird benötigt in dem Zeitraum vom Verlust der passiv von der Mutter erhaltenen Antikörper ab dem 6. Lebensmonat bis zur Ausbildung eines eigenen ausgereiften immunologischen Abwehrsystems ab dem 18. Lebensmonat. Dieses war für A. die 6 Haupterkrankungszeit und erreichte ihren Höhepunkt mit der Tonsillektomie im Alter von 2 Jahren. In einer Untersuchung erkrankten 13 von 17 homozygoten Kindern an schweren Infektionen, 6 mit einer Septikämie. Bei heterozygot erkrankten Kindern bleibt der Immundefekt zumeist unbemerkt auf Grund der Redundanz des Immunsystems, jedoch ist auch hier eine erhöhte Anfälligkeit für Infektionen gegeben (5). Verschiedene Autoren sehen einen Zusammenhang zwischen einem Mangel an MBL und verschiedenen Autoimmunerkrankungen betreffend den Systemischen Lupus erythematodes, der rheumatoiden Arthritis und dem M. Crohn (6). Eine Fallbeschreibung berichtet von einer 27-jährigen Frau mit MBL-Defizit unter der Nachweisgrenze und einem Auftreten von Multipler Sklerose vom schubförmig remittierenden Verlauf (7). Weitere Berichte wurden in der Literatur nicht gefunden und sind meiner Kenntnis nach nicht vorhanden. Das MBL gehört, wie bereits dargestellt, zum Komplementsystem. Das Komplementsystem ist Teil des angeborenen Immunsystems und zudem ein effektiver Bestandteil antikörpervermittelter Immunität (8). Es besteht aus über 30 Einzelfaktoren, von denen der Großteil im Plasma gelöst, ein kleinerer Teil zellgebunden ist. Die Funktion des Komplementsystems lässt sich in drei Hauptgruppen aufteilen: a) Erregerabwehr: Opsonierung von Pathogenen durch „Markierung“ Aktivierung und Chemoattraktion von Leukozyten Bildung von Anaphylatoxinen Lyse von Pathogenen und Zellen b) Bindeglied zwischen angeborener und erworbener Immunität: Verstärkung der Antikörperantwort Stimulation des immunologischen Gedächtnisses c) Entsorgung von „Abfall“: Beseitigung von Immunkomplexen „Abräumen“ apoptotischer Zellen Bislang sind drei verschiedene Aktivierungswege des Komplementsystems bekannt: a) der „Klassische Weg“ 7 C1q-vermittelt b) der „Lektin-Weg“ vermittelt durch Mannan-bindendes Lektin und andere Collectine c) der „Alternative Weg“ vermittelt durch Bindung des „spontanaktiven“ Komplementfaktors C3 an z.B. ein Pathogen Abb. 3 aus (6) In jedem dieser Aktivierungswege sind einzelne Bestandteile, vergleichbar mit dem Gerinnungs- und Fibrinolysesystem, in Form einer getriggerten Enzymkaskade hintereinandergeschaltet. Die enzymatisch aktiven Komplementkomponenten liegen zunächst in einer Proenzymform (Zymogen) vor, die erst nach proteolytischer Spaltung 8 ihre Funktion wahrnehmen. Alle drei Wege münden in einer gemeinsamen Endstrecke, aus der sich der „membran-attacking-complex (MAC)“ generiert. Die Wirkung des MAC führt zur Porenbildung in der Zellmembran der Zielzelle, die durch die Störung der Homöostase zum Zelluntergang führt oder aber auch Enzymen den Weg in die Zelle ermöglicht.(8). Der Lektin-Weg, der an dieser Stelle von Bedeutung ist, besteht aus dem Mannan-bindenden Lektin und seinen Serin-Proteasen MASP1 und MASP2 sowie anderen Collectinen, die dann in den Klassischen Weg einmünden. Es ist funktionell und strukturell vergleichbar mit dem C1q, das seinerseits den Initiator des klassischen Weges darstellt (9). Wenn der Lektinweg wegen eines MBL-Mangels oder -ausfalls nicht ausreichend gut funktioniert, wird dieses durch die entsprechende Verstärkung der anderen Komplementkaskaden ausgeglichen. Dadurch erhöht sich die Zunahme der Antikörper, die als Ausgangsprodukt des klassischen Weges benötigt werden. Die stark erhöhte Anzahl an sich im Umlauf befindlichen Antikörper erhöht proportional das Erkrankungsrisiko von Autoimmunerkrankungen. Anderseits besteht die Aufgabe des Komplementsystems in der Beseitigung von Zelltrümmern apoptotischer Zellen. Auch dieser Mechanismus ist bei einer Komplementdefizienz gestört und kann zu einer Autoimmunerkrankung prädisponieren. Dieses wurde untersucht für C1q und MBL, wobei sich beide Substanzen an apoptotische Zellbestandteile binden und diese unreifen dendritischen Zellen präsentieren (10). Bekannt ist ein hoher Anteil an Erkrankungen an Systemischem Lupus erythematodes (SLE) bei Patienten mit einem Komplementsystemdefekt, insbesondere das C1q-Komplement betreffend. Hier ist mit einer Erkrankungsrate von 95 % zu rechnen. Auch MBL-defiziente Patienten erkranken vermehrt an SLE, wobei die Schwere des Mangels mit der Schwere der Erkrankung korreliert (11). Die Multiple Sklerose scheint zu einem höheren Spiegel an MBL zu führen und damit zu einer Aktivierung des Lectin binding Pathway (12). Die Pathophysiologie dieser Zusammenhänge ist noch nicht vollständig entschlüsselt. 4.1.1. Zusammenfassung: Das Komplementsystem hat sicherlich eine immunkontrollierende und -modulierende Funktion, die bei entsprechendem Defekt oder Mangel geschwächt ist (13). Das MBL-Defizit spielt eine bisher möglicherweise unterschätzte Rolle im immunologischen Geschehen und der Entstehung der autoimmunen Erkrankungen. Insbesondere die Multiple Sklerose blieb 9 bisher weitgehend unbeachtet. So sollte bei entsprechend Erkrankten der Spiegel des MBL bestimmt werden, zumal wenn eine Infektneigung beobachtet wird. Auch sollte vor Einleitung einer immunsuppressiven Therapie der MBL-Titer beachtet werden. 4.1.2. Literatur 1. übernommen aus http://www.imd-berlin.de/fuer-einsender/fachinformationen-fueraerztediagnostikinfos/infektionskrankheiten/mannose-bindendes-lektin-mblmangel.html 2. Casanova,J.L., Abel, L. 2004. Human Mannose-binding Lectin in Immunity Friend, Foe, or Both? JEM vol. 199 no. 10: 1295-1299 3. Miller, M.E., J. Seals, R. Kaye, and L.C. Levitsky. 1968. A familial, plasma associated defect of phagocytosis: a new cause of recurrent bacterial infections. Lancet. 2:60–63 4. Super, M., S. Thiel, J. Lu, R.J. Levinsky, and M.W. Turner. 1989. Association of low levels of mannan-binding protein with a common defect of opsonisation. Lancet. 2:1236– 123. 5. Summerfield JA, Sumiya M, Levin M, Turner MW. 1997. Association of mutations in mannose binding protein gene with childhood infection in consecutive hospital series. 1997.BMJ. 314(7089):1229-3) 6. Pettigrew,HD, Teuber,SS, Gershwin, ME. 2009. Clinical Significance of Complement Deficiencies. Ann NY Acad Sci 1173: 108-123, Thiel S, Fredriksen PD,Jensensius JC. Clincal manifestations of mannan binding lectin deficiency. Mol Immunol 43 (1-2): 8696 (2006) 7. Malhotra GK, Kobayashi R, Poole JA. Absence of mannose-binding lectin in a female with relapsing-remitting multiple sclerosis.2012. sr Med Assoc J. 14(5):333-334 8. Walport MJ. 2001. Complement First of Two Parts. N Engl Med 344(14): 1058-66 9. Murphy KM, Travers P, Walport M. Janeway Immunologie: Spektrum Akademischer Verlag; Aufl. Heidelberg 2002 10. Nauta JA,Castellano C., Xu W, Woltmann AM,Bottias MC,Dha AR, Koote C,Roos A. 2004. Opsonization with C1q and mannose bindinding lectin targets apoptotic cells to dendritic cells.J Immunol 173(5): 3044-50 10 11. Garred PA, Voss A, Madsen HO, Junker P. 2001. Association of mannose-binding lectin gene variation with desease severity and infections in a population based cohort odf systemic lupus erythematodes patients. Genes Immun 2(8): 442-50 12. Kwok JY, Vaida F., Augst RM, Yu DY, Singh KK. 2011. Mannose binding lectin mediated complement pathway in multiple sclerosis. J Neuroimmunol. 239(1-2) 98-100 13. Ju JH, Teh BK, Wang Ld, Wang YN, Tan YS, Lai MC, Reid KB. 2008.The classical and regulatory functions of C1q in immunity and autoimmunity. Cellular & Melcular Immunology 5(1):9-21 4.2. Tourette-Syndrom, andere Tic-Störungen und Zwangstörung 1987 bis 2001 bestand bei A. ein Tourette-Syndrom mit einfachen motorischen und vokalen Tics. Nach dem Diagnoseschlüssel ICD 10 (F95.2) ist das Tourette-Syndrom eine kombinierte vokale und motorische Tic-Störung und durch das Vorkommen von mindestens zwei motorischen und vokalen Tics gekennzeichnet. Ein Erkrankungsbeginn wird im Kindes- oder Jugendalter gefordert mit einer Erkrankungsdauer von mindestens einem Jahr (1). Dieses trifft auf A. zu. An Komorbiditäten werden beschrieben: ADHS mit 50-90%, ferner Zwänge und Ängste, Impulskontrollstörungen, emotionale Dysregulation, Störung des Sozialverhaltens, Autismusspektrumstörungen, Teilleistungsstörungen. Bei Erwachsenen findet man neben Zwangssymptomen oft Autoaggressionen, Depressionen und Schlafstörungen (2), (3). 1998 wurde in den USA wurde eine Entität beschrieben, die einen Kausalzusammenhang zwischen einer obsessiven Zwangstörung (OCD), Tourette-Syndrom und einer kürzlich vorausgegangen Infektion mit beta-hämolysierenden Streptokokken darstellt (4). Es war das Ergebnis einer 10 jährigen Forschungsarbeit mehrerer Mitarbeiter des National Institute of Mental Health (NIMH), Bethesda MD, USA. Die Erkrankung wurde PANDAS genannt (Pediatric Autoimmune Neuropsychiatric Disorders Associated with Streptococcal Infections). Es wird davon ausgegangen, dass Antikörper, die bei Streptokokkeninfektionen des Hals- und Rachenraums bzw. des Mittelohrs Scharlach, Otitis media) gebildet werden und gegen die Zelloberfläche der Bakterien gerichtet sind, mit speziellen Strukturen des Gehirns kreuzreagieren 11 insbesondere den Basalganglien, die für die Koordination von Bewegungen zuständig sind (5). Dadurch kommt es zu Verhaltensänderungen und Störungen der Motorik sowie zu einer Zwangsstörung mit plötzlichem, oft fulminantem Beginn, die unbehandelt chronifizieren und lebenslang persistieren kann (6). So sei auch ein Teil der Fälle von Zwangs- und Ticstörungen im Erwachsenenalter eventuell bei entsprechender genetischer Disposition die Folge eines in der Kindheit erworbenen PANDAS-Syndroms (7). Das NIMH ruft zu einer Studie auf, in der die infolge einer Streptokokken-Infektion gebildeten schädlichen Antikörper durch intravenöse Gabe Gammaglobulin inaktiviert werden sollen. Einbezogen werden sollen Kinder zwischen 4 und 12 Jahren mit OCD mit und ohne TicStörung. Die Studie wird im Jan. 2016 beendet. Damit wäre erstmalig eine kausale Therapie des PANDAS-Syndroms möglich (8). Der Unterschied zwischen einer Zwangstörung und einem Tourette-Syndrom (Tic-Störung) wird in einer Dissertation der Universität Marburg von Julia Behrend 2008 dargestellt (9). Nach der ICD 10-Klassifizierung besteht die Hauptsymptomatik der Zwangsstörung (Obsessive Compulsive Disorder, OCD) in Zwangsgedanken und Zwangshandlungen. Zu den Zwangsgedanken gehören: Zwangsideen, Zwangsimpulse, Grübelzwang und Zweifel, zu den Zwangshandlungen der Reinlichkeitszwang, der Kontrollzwang, der Ordnungszwang, der Berührzwang, der Zählzwang und verbale Zwänge (10). Das Tourette-Syndrom wurde bereits oben ausführlich beschrieben. Es gibt eine Komorbidität von Tic- und Zwangsstörungen und es wird ein gemeinsamer genetischer Defekt für beide Störungen diskutiert. Diese Annahme wird durch Zwillings- und Familienstudien unterstützt (11). Der Erkrankungsbeginn der Ticstörung geht der Entwicklung der Zwangstörung voraus (12). Das PANS-Syndrom (Pediatric Acute-Onset Neuropsychiatric Syndrome) bezeichnet den akuten dramatischen Beginn einer OCD, Zwangsstörung, mit akuten psychiatrischen Symptomen, laut Swedo et al. werden zusätzlich mindestens zwei der folgenden psychiatrischen Symptome gefordert: 1. Ängstlichkeit 2. Emotionale Labilität und/oder Depression 3.Reizbarkeit, Aggression und/oder der Situation unangemessen aufsässiges Verhalten 12 4. Rückentwicklung in der Verhaltensentwicklung/Reife (bei Kindern und Jugendlichen) 5. Verschlechterung der Schul- bzw. Arbeitsleistungen oder Dysgraphie 7. Somatische Symptome wie z.B. Schlafstörungen, Enuresis (Bettnässen) und/oder eine Änderung in der Häufigkeit des Wasserlassens 8. Weitere neurologische-psychiatrische Auffälligkeiten wie Trennungsängste, kognitive Defizite, Gedächtnisprobleme, u.ä. Das PANS-Syndrom wird getriggert durch eine infektiöse Erkrankung (PITANDS-Pediatric Infection-Triggered Autoimmun Neuropsychiatric Disorder) oder andere nicht infektiöse Trigger. Außerdem darf die Erkrankung nicht besser erklärt durch eine bekannte neurologische oder medizinische Störung, wie Sydenham Chorea, Systemischer Lupus erythematodes, Tourette Syndrom oder andere (13). Abb. 4 aus (13) Das obige Schema verdeutlicht noch einmal die vorgenommene Einteilung. 4.2.1. Zusammenfassung: A. erkrankte an einem Tourette Syndrom. Wie zuvor ausführlich beschrieben, liegt eine MBLDefizienz vor. Bis zum 2. Lebensjahr wurde häufige Infekte, Bronchitiden, insbesondere 13 Tonsillitiden durchgemacht, die im 2. Lebensjahr zur Tonsillektomie führten. Danach kam es zu einer Verbesserung des Gesundheitszustandes und zu einem Nachlassen der Infekthäufigkeit, wobei eine erhebliche Empfindlichkeit für Infekte bestehen blieb. Im Alter von 8 – 12 Jahren bestand ein Tourette-Syndrom, das sich unbehandelt zurückbildete. Zwangstörungen wurden nicht beobachtet. Der ALS aus dieser Zeit zeigte 1991 einen Wert von 213, 1992 502 und 1994 265 U/ml. Ein erneuter Streptokokkeninfektion ist anzunehmen, wobei ein Zusammenhang mit dem Tourette-Syndrom möglich ist. Damit könnte ein PANDAS-Syndrom vorliegen. Gleichzeitig kam es zum Auftreten neuropsychychiatrischer Symptome mit Ängstlichkeit, emotionaler Labilität, Reizbarkeit, Aggression und/oder der Situation unangemessen aufsässigen Verhalten, Rückentwicklung in der Verhaltensentwicklung/Reife, erhebliche Verschlechterung der Schulleistungen, somatische Symptome wie z.B. Schlafstörungen, Enuresis (Bettnässen), kognitive Defizite, Gedächtnisprobleme und Verschlechterung einer bestehenden Rechtschreib- und rechenschwäche. Damit könnte es sich um ein PITCANS-Syndrom handeln mit einer nicht durch Streptokokken ausgelösten Infekt-Triggerung. Auch wenn die Zuordnung zu den oben beschriebenen Klassifizierungen nicht eindeutig zu treffen ist, da die Erkrankung lange zurückliegt, ist doch eine infektiöse Triggerung des Tourette-Syndrom bei nachgewiesenem Immundefekt wahrscheinlich. Als Komorbidität entwickelte sich im Alter von 14 Jahren ein ausgeprägtes ADHS-Syndrom, das bis dato akut ist und mit Methylphenidat behandelt wird. Zusätzlich besteht eine ausgeprägte Schlafstörung. 4.2.2. Literatur 1. Aus http://www.dimdi.de/static/de/klassi/icd-10-gm/kodesuche/onlinefassungen /htmlgm2013/block-f90-f98.htm 2. Ludolf AG, Roessner V., Münchau A.,Müller-Vahl K. 2012 .Tourette-Syndrom und andere Tic-Störungen in Kindheit, Jugend und Erwachsenenalter. DÄ 109 (48): 821827 3. Khalifa N, von Knorring AL. 2006. Psychopathology in a Swedish population of school children with tic disorders. Am Acad Child Adolesc Psychiatry: 45(11):1346-53 4. Susan E. Swedo, M.D.; Henrietta L. Leonard, M.D.; Marjorie Garvey, M.D.; Barbara Mittleman, M.D.; Albert J. Allen, M.D., Ph.D.; Susan Perlmutter, M.D.; Sara Dow, B.A.; 14 Jason Zamkoff, B.A.; Billinda K. Dubbert, M.S.N.; Lorraine Lougee, L.C.S.W. 1998. Pediatric Autoimmune Neuropsychiatric Disorders Associated With Streptococcal Infections: Clinical Description of the First 50 Cases. Am J Psychiatry 155: 264-271. 5. Maini B, Bathla M, Dhanjal GS, Sharma PD. 2012.Pediatric autoimmune neuropsychiatric disorders after streptococcus infection. Indian J Psychiatry. 54(4): 375-7 6. Swedo SE, Leonard HL, Rapoport SL. 2004. The Pediatric Autoimmune Neuropsychiatric Disorders Associated With Streptococcal Infection (PANDAS) Subgroup: Separating Fact From Fiction: Pediatrics. 113(4):907-11 7. Marconi D, Limpido L, Bersani I, Giordano A,Bersani G.2009. PANDAS: a possible model for adult OCD pathogenesis. Riv Psichiatr. 44(5):285-98. 8. http://clinicaltrials.gov/ct2/show/NCT01281969: Intravenous Immunoglobulin for PANDAS (Pediatric Autoimmune Neuropsychiatric Disorders Associated With Streptococcal Infections), Verified August 2012 by National Institutes of Health Clinical Center (CC) 9. http:// www.tourette-gesellschaft.de/download/ Zusammenhaengezwangsundticstoerungen 10. Schafetter Ch. 2004. Allgemeine Psychopathologie: Eine Einführung. Thieme, Stuttgart: 149 ff 11. Billett, E.A., Richter, M.A. & Kennedy, J.L. (1998). Genetics of obsessive-compulsive disorder. In: R.P. Swinson, M.M. Antony, S. Rachman &M.A. Richter (Ed.), ObsessiveCompulsive Disorder. Theory, Research, andTreatment. (pp. 181–206). New York: Guilford Press. 12. Peterson, BS, Pine, DS, Cohen,P. Brook, JS. 2001. Prospective, Longitudinal Study of Tic, Obsessive-Compulsive, and Attention-Deficit/Hyperactivity Disorders in an Epidemiological Sample. Journal of theAmerican Academy of Child and Adolescent Psychiatry. 40(6) 685–695, Cohen, JD,. Leckman,JF. (1994). Developmental Psychopathology andNeurobiology of Tourette ́s Syndrome. Journal of the American Academy of Child and Adolescent Psychiatry: 33(1) 2–15 13. Swedo SE, Leckman JF, Rose NR. 2012. From research subgroup to clinical Syndrome: Modifying the PANDAS criteria to describe PANS (prediatric Acute-onset Neuropsychiatric Syndrome) Pediatr Therapeut, 2:2. 15 4.3. ADHS-Syndrom und Histaminämie 2004 wurde bei A. erstmals die Diagnose eines ADHS-Syndroms gestellt. Der eigentliche Beginn der Erkrankung erfolgte wahrscheinlich sehr viel früher, ohne dass die klinischen Symptome dieser Erkrankung zugeordnet werden konnten. Das ADH-Syndrom ist eine heute anerkannte psychiatrische Erkrankung und gehört zu den Hyperkinesien. Kernsymptome sind: „Störung der Aufmerksamkeit mit Mangel an Ausdauer bei Leistungsanforderungen und die Tendenz, Tätigkeiten zu wechseln, bevor sie zu Ende gebracht wurden, unruhiges Verhalten insbesondere mit der Unfähigkeit, stillsitzen zu können, Impulsivität z. B. mit abrupten motorischen und /oder verbalen Aktionen, die nicht in den sozialen Kontext passen“ (1). Überzufällig häufige Koerkrankungen sind: Entwicklungsstörungen der Sprache, des Lesen und der Rechtschreibung, Tic-Störungen sowie, teils sekundär, Störungen des Sozialverhaltens und emotionale Störungen (wie bei A. oben beschrieben). Eine Prävalenz der Störung wird mit 1-7% bis zum Erkrankungsalter von 17 Jahren angegeben. Jungen sind häufiger betroffen als Mädchen (2, 3, 4). Die Ätiologie der Erkrankung ist noch nicht vollständig geklärt. Jedoch spielen genetische Faktoren eine große Rolle: 65-90% der phänotypischen Varianz sind auf genetische Faktoren zurückzuführen (5, 6). Biologische Verwandte haben ein 3-5 fach höheres Risiko, ebenfalls an ADHS zu erkranken und biologische Eltern leiden relativ häufig an ADHS (18%) (7). ADHS kann auch erworben sein. Einige Erkrankte können an beiden Formen gleichzeitig leiden: genetisch und erworben. Es ist zur Zeit jedoch nicht möglich, beide Erkrankungstypen voneinander diagnostisch zu unterscheiden. Beide zeigen das gleiche Verhalten und beide sind mit den gleichen Medikamenten behandelbar. Zu den externen, also erworbenen Ursachen, zählen prä-, peri- und postnatale Ereignisse, die zu einer Schädigung des Gehirns führen. Eine andere Ursache könnte das fetale AlkoholSyndrom sein, das zu einer erheblichen Aufmerksamkeitsstörung, Impulsivität und Hyperaktivität bei den Geschädigten führt. Diese Kinder leiden an einem 16 volumenreduzierten präfrontalen und temporalen Cortex, Hirnregionen, die die Aufmerksamkeit und Impulsivität steuern (8). Auch mütterliches Rauchen während der Schwangerschaft ist assoziiert mit einem ADH-Syndrom (9). Stoffwechselstörungen der Mutter (z.B. Diabetes mellitus oder Phenylketonurie) können eine Hirnschädigung verursachen, die ein ADHS-gleiches Verhalten hervorruft (10). Traumata, die das temporale oder präfrontale Hirn betreffen, sind zu nennen (11). Meningitis und Encephalitis gehören dazu. Ferner Autoimmunreaktionen, wie unter 4.2 auf Seite 11 beschrieben. Ein Zusammenhang zwischen einer atopischen Dermatitis, Asthma und allergischer Rhinitis und ADHD scheint möglich. So fand sich bei Kindern mit atopischer Dermatitis ein 43% Risiko, an ADHS zu erkranken (12). Ähnliche Befunde wurden aus Taiwan mitgeteilt. Hier wurden Kinder unter 18 Jahren untersucht. Die stärkste Korrelation fand sich zur allergischen Rhinitis, unabhängig vom Alter und Geschlecht. Allergische Komorbiditäten erhöhten das Risiko für ADHD (13). Bei A. finden sich klinisch Zeichen einer allergischen Rhinitis, eine häufige, teils spastische Bronchitis als Zeichen einer exogenen Allergie. Laborchemisch war das IGE erhöht mit 30 SE U/ml (normal bis 25), im Differentialblutbild zeigten sich 8 Eosinophile. Das ADH-Syndrom kann als eine Störung der Neurotransmitterfunktion von Dopamin und Norepinephrin betrachtet werden . Bildgebende Untersuchungen ergaben, dass bei den betroffenen Personen im Vergleich zu Gesunden um etwa 70% erhöhte Bindungskapazitäten der präsynaptischen Dopamintransporter bestehen, die vermutlich auf eine genetisch erhöhte Expression derselben zurückzuführen sind und durch Methylphenidat, welches den Transporter blockiert, deutlich reduziert werden kann (14). Weitere Untersuchungen zeigten strukturelle und funktionelle (rechtsbetonte) Auffälligkeiten im Bereich des präfrontalen Kortex, des anterioren Gyrus cingulus sowie der Basalganglien und ihren Verbindungen. Bei A. wurde ein erhöhter Histamin-Spiegel im Serum gefunden: 1,1 ED µg/l (normal <0,80), entsprechend erhöht war die Methylhistaminausscheidung im Urin am 07.03.13 mit 11,40 UR µg/mmol Krea/mˆ2KO (normal <6,6) und nach histaminarmer Ernährung am 04.04.13 mit einem 13,2 UR µg/mmol Krea/mˆKO. Die Diaminooxidase-Konzentration war entsprechend der geforderten Abbauleistung mit >30 (normal 3 – 10) erhöht. Das vorliegende Ergebnis 17 stellt einen erhöhten Histamingehalt des Blutes mit funktionierendem Abbau dar. Mastzellen fanden sich bei der Lymphozytendifferenzierung nicht. Das Histamin wird in Vertebraten biochemisch aus der Aminosäure L-Histidin zu Histamin decarboxyliert durch die L-Histidin Decarboxylase, einem Vitamin B6 abhängigem Enzym. Der weitere Metabolismus von Histamin erfolgt weniger über die Oxydation, unter Wirkung der Diaminooxidase (DAO) zu Imidazolacetaldehyd, größtenteils jedoch über die Methylation und die N-Methyltransferase (HMT) zu Methylhistamin, welches im Urin ausgeschieden wird. (10). Ein Polymorphismus in menschlichem HMT (THr105Ile) mit reduzierter Enzymaktivität und erhöhtem Histamin-Level ist möglicherweise ein auslösender Faktor für einige Formen von M. Parkinson, Urticaria und Hyperaktivitäts-Erkrankungen (15). Histamin spielt eine zentrale Rolle im angeborenen und adaptiven Immunsystem: in der Allergie und Entzündung, eng verbunden mit der Mastzellfunktion, in der Immunmodulation bezüglich der T- Zellfunktion und Autoimmunität (16). Die Histaminsynthese , -übertragung und –funktion wird kontrolliert von einer Vielzahl von Signalen des Immunsystems und moduliert selbst Zytokine und Interferonnetzwerke und die Interferonfunktion (17). Histamin ist im zentralen Nervensystem ein wichtiger Neurotransmitter. Der Histamingehalt in verschiedenen Organen und Zelltypen variiert sehr stark. Hohe Histamin-Konzentrationen finden sich unter anderem in den Gewebsmastzellen der Haut, der Mukosa der Bronchien und des Gastrointestinaltraktes sowie in den basophilen Granulozyten des Blutes. Ferner sind erhöhte Konzentrationen in bestimmten Neuronen des Gehirns vorhanden. Unter physiologischen Bedingungen sind im Blut und anderen Körperflüssigkeiten nur geringe Mengen freien Histamins nachweisbar, in der Cerebrospinalflüssigkeit sind dagegen höhere Konzentrationen messbar. Histamin ist normalerweise nicht in der Lage, die Blut-Hirn-Schranke zu überwinden. Daher muss neuronales Histamin lokal in den Zellkörpern des hinteren Hypothalamus synthetisiert werden. Die Speicherung des Histamins erfolgt in peripheren Geweben überwiegend in den Granula der Mastzellen und basophilen Granulozyten, im zentralen Nervensystem außerdem in Sympatosomen histaminerger Neurone (18). Es werden in chronologischer Reihenfolge der Entdeckung 4 Neurotransmitter (H1-4) unterschieden, deren Verteilungsdichte und Funktion sehr unterschiedlich sind. Alle vier Histamin-Rezeptoren sind heptahelikale Membranproteine und an intrazelluläre G-Proteine gekoppelt, die eine Signaltransduktion der Histaminwirkung in die Zelle bewirken. So kann das Histamin an verschiedenen Organen eine unterschiedliche Wirkung entfalten. Die Dichte 18 von H3 Rezeptoren ist im zentralen Nervensystem wesentlich höher als in peripheren Geweben. Sie ist jedoch nur etwa 1/3 so hoch wie die von H1- und H2 Rezeptoren. Allerdings besitzt Histamin eine höhere Affinität zum präsynaptischen Histamin H3 als zu den postsynaptischen H1- und H2- Rezeptoren. Eine besondere Stellung scheinen die H3Rezeptoren einzunehmen: Die Stimulation des Rezeptors führt zu einer autoregulativen Freisetzung und Synthese über einen negativen Feedback, gleichzeitig fungiert er als Heterorezeptor mit inhibitorischer Funktion bei der Freisetzung von Neurotransmittern aus noradrenergen, dopaminergen, serotonergen und peptidogenen Neuronen im ZNS (19). In der Hypophyse wird über H3 Rezeptoren außerdem der negative Feedbackmechanismus der durch Histamin ausgelösten Freisetzung des adrenocorticotrope Hormons, des luteinisierenden Hormons, von Prolactin und Vasopressin gesteuert. Die Histaminwirkungen im Gehirn sind vielfältig: Es werden die Sekretion von Hormonen gesteuert, der Schlaf-Wachrhythmus wird beeinflusst, ebenso Gedächtnis- und Lernprozesse, ferner Nahrungsaufnahme und Übelkeit (20). Histamin ist außerdem beteiligt an immunogenen Prozessen sowie Autoimmunerkrankungen. Mastzellen als Ort der Histaminspeicherung sind involviert in die Verstärkung des Schweregrades von Multipler Sklerose (MS) und der experimentellen autoimmunen Encephalomyelitis (EAE). So zeigen mastzelldefiziente Mäuse weniger stark ausgeprägte encephalitische Erkrankungen als die immunkompetente Kontrollgruppe sowohl für die progressive als auch für die schubförmig-remittierende Form (21). Die Empfänglichkeit für EAE ist abhängig von der Expression von H1 Rezeptoren . Diese finden sich auf Th1 Zellen in zentralen Läsionen, die durch EAE im Tierversuch verursacht wurden. Sie sind notwendig für die volle Ausprägung der Erkrankung. H1 Antagonisten führen nicht überraschenderweise zu einer Verbesserung der Krankheit (22). CD4 von H1Rezeptor freien Mäusen produzierten weniger IFN-ɣ und mehr IL-4 (dieses induziert die Differenzierung von naiven CD4+T-Zellen zu Th2 Zellen) (23). Außerdem ist Histamin einer der wenigen Neurotransmitter, der in der Lage ist, die Blut-HirnSchranke andauernd zu öffnen. Der Anstieg der Permeabilität wird vermittelt durch H2 Rezeptoren, die Reduktion durch H1 –Rezeptoren (24). Somit scheint das Histamin über die cerebralen Rezeptoren einen großen Einfluss auszuüben auf die Ausprägung des Schweregrades der multiplen Sklerose. Bei A. finden sich gleichzeitig Zeichen einer Allergie (klinisch als Rhinitis und spastischer Bronchitis) mit 19 einer Eosinophilie von 8% und einer Ges. IGE von 30 U/ml (normal bis 25 U/ml). Es sind Arbeiten in der Literatur bekannt, die einen erhöhten Histaminspiegel bei gleichzeitiger Eosinophilie und klinisch bestehender Allergie (Asthma, atopische Dermatatis und allergische Rhinitis) feststellten (25). Inwieweit dieser erhöhte Histaminwert im Serum auch Auswirkung auf die Ausprägung der MS bei A, hatte und ob er bereits vor Auftreten der MS vorhanden war, lässt sich nicht mehr nachvollziehen, da keine Messungen aus dieser Zeit bekannt sind. Histamin hat über die cerebralen Rezeptoren, hier besonders die H1 und H3 Rezeptoren, unter anderem Einfluss auf das Verhalten, ADHD und soziale Funktionen. Insbesondere der H3-Rezeptor ist deshalb das Ziel von intensiver pharmakologischer Forschung zur Entwicklung von Präparaten zur Beeinflussung der o.g. Störungen. 4.3.1. Zusammenfassung: 2004 wurde bei A. ein ADHS diagnostiziert. Möglicherweise ist die Genese ursprünglich genetisch bedingt bei Unruhe als Kleinkind und abweichendem auffälligen sozialen Verhalten, sowie erheblichen cognitiven Defiziten, wie oben beschrieben, im Stadium des Heranwachsenden. Eine Triggerung ist sehr wahrscheinlich bei schweren Infekten (PANDAS-Syndrom oder PITANDS?) bei kompletter MBL-Defizienz, sowie einer möglichen Encephalitis nach einer Masernimpfung. Ferner wurde bei A. wurde ein erhöhter Plasmahistaminspiegel gefunden. Es ist nicht bekannt, ob der Histaminspiegel bereits vor Auftreten des ADHS oder der Multiplen Sklerose erhöht war. In dem Fall des damaligen Vorhandenseins wäre eine Beteiligung des Histamins an der Entstehung beider Erkrankungen, wie oben beschreiben, zu diskutieren. Der zum gegenwärtigen Zeitpunkt erhöhte Spiegel kann ätiologisch nicht sicher zugeordnet werden. Es sind erhöhte Histaminspiegel in der cerebrospinalen Flüssigkeit bei an multipler Sklerose erkrankten Patienten nachgewiesen worden. Leider wurden keine Plasmahistaminspiegel gemessen (26,27). In einer Arbeit von Stevenson wird der Zusammenhang zwischen Genpolymorhismen der Histaminmethyltransferase, des Dopamintransporters und der Symptomatik des ADHS bei Kleinkindern in Bezug auf bestimmte Nahrungszusätze festgestellt. Dieses weist noch einmal auf den erheblichen Einfluss des Histamins, aber auch des Dopamins bei der ADHS-Symptomatik hin. Ferner könnten die Ernährungsweise oder auch andere Umwelteinflüsse auf die Symptomatik einwirken. (28). Leider wurde auch hier kein Plasmahistamin bestimmt, so dass kein unmittelbarer Bezug auf den beschriebenen Krankheitsfall genommen werden kann. 20 4.3.2. Literatur 1. http://www.bundesaerztekammer.de/downloads/ADHSkurz.pdf 2. Buitelaar JK: Epidemiological aspects: What have we learned over the last decade? In: Sandberg, S (Hg.): Hyperactivity and attention disorders of childhood. Cambridge. UK: Cambridge University Press 2002, Co; 30-63 3. Barkley RA, Fischer M, Smallish L, Fletcher K: The persistence of attention-deficit / hyperactivity disorder into young adulthood as a function of reporting source and definition of disorder. J Abnorm Psychol 2002; 111(2): 279-89 4. Huss M: Vorbereitung der Erhebung und Auswertung zur Prävalenz des Aufmerksamkeits-Defizit-Hyperaktivitäts-Syndroms (ADHS) in Deutschland im Rahmen des Kinder- und Jugend-Surveys des Robert-Koch-Instituts. Abschlussbericht an das Bundesministerium für Gesundheit und soziale Sicherung (BMGS). Bonn: BMGS 2004 5. Langner I, Garbe E, Banaschewski T, and Mikolajczyk RT. 2013. N-Twin and Sibling Studies Using Health Insurance Data: The Example of Attention Deficit/Hyperactivity Disorder (ADHD). PLoS One 8(4): e62177 6. Levy F, Hay DA, McSteven M, Wood C, Waldmann I. 1997. Attention-Deficit Hyperactivity Disorder: A Category or a Continuum? Genetic Analysis of a LargeScale Twin Study. J Am Acad Child Adolesc Psychiatry 36(6): 737-44 7. Sprich S, Biederman J, Crawford MH, Mundy E, Faraone SV. 2000. Adoptive and Biological Families of Children and Adolescents With ADHD. J Am Acad Child Adolesc Psychiatry 39(11): 1432-37 8. Sowell ER, Thomson PM, Mattson SN, Tessner KD, Jernigan TL, Riley EP, Toga AW. 1996. Regional brain shape abnormalities persist into adolescence after heavy prenatal alcohol exposure. Cereb Cortex 12: 856-865 9. Milberger S, Biedermann J, Faraone EV, Chen L, Jones J.1996. Is maternal smoking a risk factor for attention deficit hyperactivity disorder in children?. Am J Psychiatry 153: 1138-1142 10. Antshel KM, Waisbren SE. 2003. Timing is everything: executive functions in children exposed to elevated levels of phenylalanine. Neuropsychology 17: 458-468 11. Max JE, Mathews K, Manes FF, Robertson B, Fox PT, Lancaster JL, Lasing AE, Schatz A, Collings N. 1998. Attention deficit hyperactivity disorder and neurocognitive correlates after childhood stroke. J Am Acad Child Psychiatry 37: 841-847 12. Schmitt J, Apfelbacher C, Heinrich J, Weidinger S, Romanos. 2013. Association of atopic eczema and attention-deficit/hyperactivity disorder - meta-analysis of epidemiologic studies. Z Kinder Jugendpsychiatr Psychother 41(1):35-42 21 13. Shyu CS, Lin HK, Lin CH, Fu LS. 2012. Prevalence of attention-deficit/hyperactivity disorder in patients with pediatric allergic disorders: a nationwide, population-based study.. J Microbiol Immunol Infect 45(3): 237-42 14. Krause KH, Dresel S, Krause J, Kung HF, Tratsch K. 2000. Increased striatal dopamintransporter in adult patients with attention deficit hyperactivity disorder: Effect of methylphenidate as measured by single photone emission computed tomography. Neuroscience letters 285: 107-110 15. Leurs R, Lindsay BH, Patrizio B, Haas LH in Basic Neurochemestry, publ. by Elsevier Inc., 2012: 323-341 16. Pedotti, R, De Voss J, Steinman L, Galli SJ. 2003. Involvement of both ‘allergic’ and ‘autoimmune’ mechanisms in EAE, MS and other autoimmune diseases. Trends Immunol 24(9): 479 -84 17. Haas HL, Sergeva OA, Selbach A.. 2008. Histamine in Nervous System. Physiol Rev 88(3): 1183-1241 18 Menghin S. 2004 Analoge des Histaprodefens als potente und selektive Agonisten des Histamin H1-Rezeptors aus http://www.diss.fu-Berlin.de/diss/receive/ FUDISS_thesis_ 000000001233 19. Tibor M. 2003. N-Substituted Piperidines and Analogues as Structural Elements of Novel Histamine H3-Receptor Antagonists aus http://www.diss.fuberlin.de/diss/receive/FUDISS_thesis_000000001066 20. Onodera K, Yamatodan A, Watanabe T, Wada H. 1994. Neuropharmacology of the Histaminergic Neuron System in the Brain and its Relationship with Behavioral Disorders. Prog. Neurobiol. 42,685-702 21. Secor VH, Secor WE, Gutekunst CA, Brown MA. 2000. Mast Cells Are Essential for Early Onset and Severe Disease in a Murine Model of Multiple Sclerosis. J Exp Med. 191(5): 813–822. 22. Pedotti R, DeVoss, JJ, Youseff S,Mitchell D, Wedemeyer J. 2003. Madanat R, Garren H, Fontoura P, Tsai M, Gall St, Sobel RA, Steinman L. Multiple elements of the allergic arm of the immune response modulate autoimmune demyelination. Proc Natl Acad Sci USA 100(4): 1867-1872 23. Passani MB, Ballerini C. 2012. Histamine and neuroinflammation: insights from murine experimental autoimmune encephalitis. Front Syst Neurosci 6(32): 242-249 24. Abbott NJ. 2000. Inflammatory Mediators and Modulation of Blood-Brain-Barrier Permeability. Cell Mol Neurobiol 20(2): 131-147 25. Kimura K., Adachi M, Kubo K, Ikemoto Y. 1999. The basal plasma histamine level and eosinophil count in allergic and non-allergic patients. Fukuoka Igaku Zasshi 90(12): 457-63 22 26. Kallweit U., Aritake K., Bassetti CL, Blumenthal St, Hayaishi O,Linnebank M, Baumann CR, Urade Y. 2013. Elevated CSF histamine levels in multiple sclerosis patients. Fluids and Barriers of the CNS 10(1): 19 27. Tuomisto L, Kilpeläinen H, Riekkinen P. 1983.Histamine and histamine-Nmethyltransferase in the CSF of patients with multiple sclerosis. Agents and actions 13(2-3):255-257 28. Stevenson J, Sonuga-Barke E, McCann D, Grimshaw K, Parker KM, Rose-Zerilli M,Holloway JW, Warner JO. The Role of Histamine Degradation Gene Polymorphisms in Moderating the Effects of Food Additives on Children’s ADHS Symtoms. Am J Psychiatry 167(9): 1108-1115 4.4. Multiple Sklerose Seit 2005 leidet A. an einer Multiplen Sklerose (MS). Die Symptomatik der MS ist bekannt und wird nicht weiter beschrieben. Auch die Ausprägung der MS bei A. ist oben ausführlich dargestellt. Die MS wird den Autoimmunerkrankungen zugerechnet (1) Sie ist ein Beispiel für eine durch T-Zellen verursachte chronische Erkrankung des Nervensystems, die durch eine zerstörende Immunantwort gegen mehrere Antigene aus dem Gehirn hervorgerufen wird: das basische Myelinprotein, das Proteolipoprotein und das Myelin-Oligodendrocyten-Glykoprotein. Lymphozyten und andere Blutzellen durchqueren normalerweise nicht die Blut-HirnSchranke, wenn sich aber das Gehirn und seine Blutgefäße entzünden, wird die Blut-HirnSchranke permeabel. So können aktivierte CD4-zellen, die für Gehirnantigene spezifisch sind und α4:β1-Integrin exprimieren, an zelluläre Adhäsionmoleküle der Gefäße an der Oberfläche des aktivierten Venolenendothels binden. So ist es den T-Zellen möglich, das Blutgefäß zu verlassen. Sie treffen dann wieder auf ihr spezifisches Autoantigen, das auf Miklogliazellen (den makrophagenähnliche Phagozyten des Nervensystems), die als antigenpräsentierende Zellen fungieren. Hier greift das Natalizumab ein, der erste Vertreter der Selektiven Adhäsionsmolekül-Inhibitoren in der MS-Therapie. Natalizumab ist ein rekombinanter, humanisierter Antikörper, dessen Zielantigen die humanen α4-Integrin Untereinheiten sind (2). Die betroffenen Areale sind stark von T-Zellen und Makrophagen infiltriert. Diese produzieren Cytokine und Interferone, die die Entzündung noch weiter verstärken, so dass weitere T-Zellen, B-Zellen, Makrophagen und dendritische Zellen zur Läsionsstelle gelenkt werden. Autoreaktive B-Zellen produzieren mit Unterstützung mit der Unterstützung durch T-Zellen Autoantikörper gegen Myelinantigen. Aktivierte Mastzellen setzen Histamin frei, das ebenfalls zur Entzündung beiträgt. Diese Aktivitäten führen 23 zusammen zur Demyelinisierung und Störung der neuronalen Funktion. (3, z.T. wörtlich zitiert). Wodurch wurde der zerstörende Prozess der T-Zellen in Gang gesetzt? A. leidet an einer MBL-Defizienz, wobei ein kompletter MBL-Mangel besteht. Auf S. 6 dieser Arbeit wurden die Funktionen des Komplementsystems beschrieben. Wichtig scheint für die Genese der MS bei A.: 1.die mangelhafte Funktion des Komplementsystems verursacht eine Zunahme der sich im Umlauf befindlichen Antikörper 2. die Beseitigung von Zelltrümmern apototischer Zellen ist gestört Durch beide Faktoren können ignorante Lymphozyten, d.h. Zellen, die körpereigene Antigene mit relativ geringen Affinität binden, zu Autoimmunreaktionen angeregt werden. Apoptotische Fragmente können zusätzlich entstehen durch rezidivierende Infekte, wie A. sie in der Kindheit und auch später, wenn auch in geringerer Zahl, durchlaufen hat (4). 4.4.1. Zusammenfassung A. ist an einer Multiplen Sklerose erkrankt. Wie oben dargestellt, ist mit großer Wahrscheinlichkeit der Immundefekt im Sinne der beschriebenen MBL-Defizienz ursächlich anzusehen. Da nur eine Arbeit bekannt ist mit einer ähnlichen Kasuistik (s.u. 4.2.1 (7)), die homozygote MBL-Defizienz mit einer Prävalenz von 0,3% jedoch relativ häufig auftritt, erscheint es wichtig, bei an MS erkrankten Patienten grundsätzlich den MBL-Titer mitzubestimmen, um diesen für die Genese der MS wichtigen Parameter zu bestätigen oder auszuschließen. 4.4.2. Literatur 1. Murphy K, Travers P, Walport M. 2009. Immunologie. Spektum, Akademischer Verlag 7. Auflage: p 773 2. http://tysabri.de/index.php?inhalt=tysabri.wirkmechanismus 3. Murphy K, Travers P, Walport M. 2009. Immunologie. Spektum, Akademischer Verlag 7. Auflage: p 785 4. Murphy K, Travers P, Walport M. 2009. Immunologie. Spektum, Akademischer Verlag 7. Auflage: p 759 5. Epikrise Bei dem Patienten A. wurde ein MBL-Mangel festgestellt. Die nachfolgenden Erkrankungen, wie rezidivierende Infekte und das Tourettesyndrom, sind wahrscheinlich Folge dieses Immundefektes. Auch das ADH-Syndrom lässt sich hier einordnen. Selbst die Genese der 24 Multiple Sklerose lässt sich ableiten. Lediglich die Histaminämie konnte nicht sicher zugeordnet werden. Sie könnte ihre Ursache sowohl in der Stresssymptomatik des ADHS haben oder auch durch die chronische Entzündung durch die Multiple Sklerose unterhalten werden. 6. Therapie A. wird trotz des Immundefektes mit Natalizumab behandelt. Dieses wurde mit dem ärztlichen Dienst der Herstellerfirma Biogen, vertreten durch Herrn Dr. Emmerich, besprochen. Zur Vorbeugung einer möglichen progressiven multifokalen Leukencephalopathie wurden engmaschige serologische Kontrollen des Titers auf JCV (John Cunningham Virus) in vierteljährlichen Abständen vereinbart. Der Titer war bisher negativ. Unter der Therapie mit Natalizumab ist es zu keiner weiteren Progression der Multiplen Sklerose gekommen. Das ADH-Syndrom wird mit Methylphenidat in hoher Dosis therapiert, dieses jedoch mit nur unzureichender Wirkung. Vielleicht liegt eine Ursache des Therapieversagens in der persistierenden Histaminämie. Möglicherweise könnte hier die Einnahme eines Antihistaminikums Abhilfe schaffen. Einen vielversprechenden Ansatz bietet der sich in der klinischen Prüfung befindliche inverse H3-Rezeptor-Agonist Pitolisant. Es wurde bisher in vielen präklinischen Studien bei Erkrankungen getestet, bei denen ein gestörtes Neurotransmittergleichgewicht zugrunde liegt. Dieses sind unter anderem Narkolepsie, M. Alzheimer, ADHS, Schizophrenie, Epilepsie und der neuropathischer Schmerz. In den klinischen Studien (Phase III) wurde Pitolisant in der Harmony I und II-Studie gegen EDS (excessive daytime sleepness) bei Narkolepsie getestet, ferner EDS bei Schlafapnoesyndrom (Harosa I- und II-Studie) und EDS bei M. Parkinson (Harps I- und IIStudie). In einer Phase II-Studie zeigte Pitolisant prokognitive Effekte bei der Schizophrenie (1),(2),(3). Schon nach einem Monat sank der Epworth Sleepness Scale, ein Indikator für Tagesschläfrigkeit, auf den Normwert von 10 und blieb dort stabil (Langzeitstudie über neun Monate). Da die Antihistaminika auf vielfältige Weise in das Immunsystem eingreifen, muss bei Patienten, die gleichzeitig an einer Autoimmunerkrankung erkrankt sind, auf eine mögliche Progression geachtet werden. Im Tiermodell reduzieren die H1-Blocker die Schwere des Erkrankungsgrades der experimentellen Encephalomyelitis (5). Eine Arbeit aus dem Jahr 2005 untersucht die Inzidenz von Multipler Sklerose nach Einnahme von H1 Rezeptoren: Das Risiko, an Multipler Sklerose zu erkranken, war nicht signifikant erhöht bei Einnahme nicht sedierender H1-Blocker, es war signifikant erniedrigt bei Einnahme 25 sedierender H1 Blocker. Vor der Verabreichung des inversen H3-Agonisten Pitolisant bei Multipler Sklerose und anderen Autoimmunerkrankungen sollten die Auswirkungen deshalb zunächst im Tierversuch geklärt werden. 6.1. Literatur 1. http://www.clinicaltrials.gov 2. Stark H. 2011. Neue Generationen von Antihistaminika. PZ: 32: 1-14 3. Ebenshade TA, Browman KE, Bitner RS, Strakhova M, Cowart MD, Brioni JD. 2008. The histamine H3 receptor: an attractive target for the treatment of cognitive disoders. Br J Pharmacol 154: 1166-1181 4. Vohora D, Bhownik M. 2012. Histamine H3 receptor antagonists/inverse agonists on cognitive and motor processes: relevance to Alzheimer’s disease, ADHD, Schizophrenia and drug abuse. Front Syst neurosci 6(72):1pp 5 Dimitriadou V, Pang X, Theoharides TC. 2000. Hydroxizine inhibits experimental allergic encephalomyelitis (EAE) and associated Brain mast cell activation. Int J Immunopharmacol 22: 673-684 6 Alonso A, Jick AA, Hernan MA. 2006. Allergy, histamine 1 receptor blockers, and the risk of multiple sclerosis. Neurology 66: 572-575 7. Schlussfolgerungen 1. Das ADH-Syndrom kann verschiedene Ursachen haben: genetische und erworbene. Beide Faktoren können bei einer betroffenen Person vorhanden sein. Im Fall A. mag eine zunächst eine genetische Ursache in Frage kommen. Dafür sprechen die Unruhe im Säuglingsalter mit deutlichen zusätzlichen Verhaltensstörungen im Kleinkindalter. Eine Familienanamnese ist nicht zu erheben, da die Eltern unbekannt sind. Als exogener Faktor ist das PANDAS-Syndrom (PITANDS?) zu nennen, das durch kreuzreagierende Streptokokkenantikörper bei kompletter MBL-Defizienz gekennzeichnet ist, die kreuzreagieren mit Strukturen der Basalganglien, und die genetisch bedingte Veranlagung getriggert haben. 2. Die MBL-Defizienz war mit großer Wahrscheinlichkeit die Ursache für das ADHSyndrom als Folgeerkrankung des Tourette-Syndroms, es war mit großer Wahrscheinlichkeit auch ursächlich für die Erkrankung an Multipler Sklerose. Ein pathogenetischer Zusammenhang zwischen ADHS und Multipler Sklerose lässt sich eventuell über den erhöhten Plasmahistamin herstellen. Dieses ist in aus der Literatur jedoch nicht sicher zu belegen und wäre interessant für weitere Untersuchungen. 3. Da die MBL-Defizienz für diesen Casus in der Krankengschichte von A. einen erheblichen und für das weitere Leben prägenden Einfluss hatte, sollte im 26 Analogschluß die Indikation zur Diagnostik einer MBL-Defizienz generell großzügig gestellt werden. So sollte die Bestimmung des MBL-Titers erfolgen bei unklaren, sich häufenden bakteriellen Infektionen im Kleinkindalter und generell vor immunsupprimierenden Maßnahmen wie Chemotherapie, Transplantationen oder großen Operationen, auch im Erwachsenenalter. Auch das ADH-Syndrom, die Multiple Sklerose oder andere Autoimmunerkrankungen könnten eine Indikation zur Bestimmung dieses Titers sein. 4. Eine großzügige Bestimmung des Plasmahistamintiters bei verschiedenen Erkrankungen wäre sicher hilfreich zur weiteren Diagnostik und Therapie bestimmter Erkrankungen, da hier Basisdaten fehlen. Nur eine Arbeit aus dem Jahr 1998 nimmt sich dieses Themas in einer kleinen Kohorte (55 Fälle) an (1). Auch fehlen valide Daten über den Plasmahistaminspiegel bei ADHS und bei der Multiplen Sklerose 7.1. Literatur 1. Jackson JA, Riodan HD, Neathery S, Revard C. 1998. 1998. Histamine Levels in Health and Desease. J Orthomol Med 13(4): 236-240 Dr. A. Schrapp Zeisbuschweg 1 51061 Köln, den 09.10.2013 27