r-Prozess (rapid) ausschliesslich bei allen Elementen A> 209
Werbung
Einführungsvorlesung - Stracke
Isotope sind Nuklide mit gleicher Ordnungszahl (=Anzahl der Protonen Z), aber unterschiedlicher Massenzahl
(A,Anzahl der Nukleonen). Verschiedene Isotope eines Elements haben eine unterschiedliche Anzahl an
Neutronen, N.
Isobare sind zwei Nuklide mit der gleichen Zahl der Nukleonen.
Bsp.: 40Ca, 40Ar, 40K sind Isobare
Notation:
Z
N
A
N=Nukleonen=Z+Neutronen
Z= Ordungszahl=#Protonen
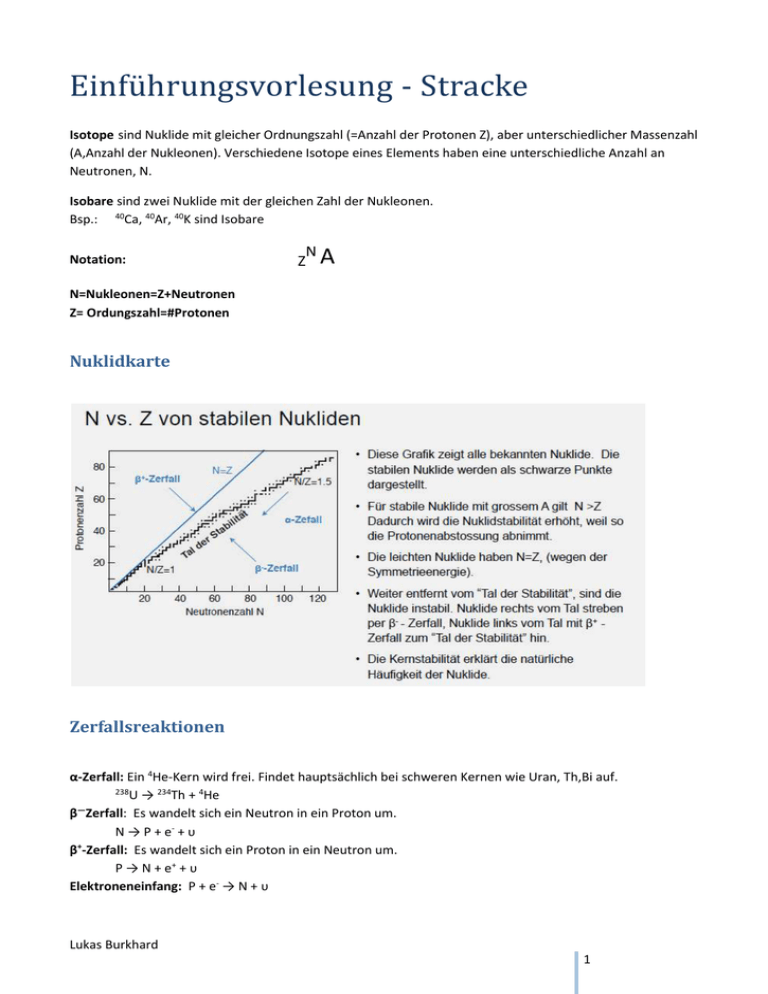
Nuklidkarte
Zerfallsreaktionen
α-Zerfall: Ein 4He-Kern wird frei. Findet hauptsächlich bei schweren Kernen wie Uran, Th,Bi auf.
238
U → 234Th + 4He
β—Zerfall: Es wandelt sich ein Neutron in ein Proton um.
N → P + e- + υ
+
β -Zerfall: Es wandelt sich ein Proton in ein Neutron um.
P → N + e+ + υ
Elektroneneinfang: P + e- → N + υ
Lukas Burkhard
1
Nukleosynthese in Sternen (Stracke)
Die Enstehung der Elemente im Persiodensystem ist den Sternen zuzuschreiben. 99% der Masse in unserem
Sonnensystem ist in der Sonne eingeschlossen. Refraktäre und häufig im solaren Urnebel vorhandene
Elemente sind die häufigsten Elemente der Gesamt-Erde.
Gesamterde
Fe
O
Si
Mg
Ni
S
Ca
Al
%-Anteil
35
30
15
13
2.4
1.9
1.1
1.1
Erdkruste
O
Si
Al
Fe
Mg
Ca
K
Na
%-Anteil
46
28
8
6
4
2.4
2.3
2.1
EK+Mantel
Si
Fe
Mg
Ca
O
Al
k.A.
k.A.
k.A.
k.A.
k.A.
k.A.
Chemische Zusammensetzung der Erde: Wichtigste 7 Elemente, aus Press/Siever/Folien Geochemie
Die Häufigkeit der Elemente wird mit Spektralanalyse bestimmt. Dieses Spektrum wird durch
Absorbtionslinien der einzelnen Elente in der Photosphäre und Chromosphäre überlagert, und man nimmt
der Einfachheit halber an, die beiden Sphären seien chemisch gleich wie die ganze SonneDie Photosphäre ist
die unterste Schicht einer Sternatmosphäre. Aus ihr stammt sowohl das kontinuierliche Spektrum des
sichtbaren Lichts als auch die Absorptionslinien eines Sternspektrums.
Die Chromosphäre (griech: Farbschicht) ist eine relativ dünne Masseschicht der Sonne, die überwiegend aus
Wasserstoff und Helium besteht.
Abbildung 1: Absorbtionslinien
Kometen sind Bruchstücke von Planetesimalen und ähneln der Zusammensetzung der Sonne recht stark, mit
Ausnahme der volatilen Elemente H, He, Li, C, N, O, S und den Edelgasen.
Die Zusammensetzung der Erdkruste wurde wahrscheinlich eher durch Aufbau und Struktur der Mineralien
bestimmt, als durch die Häufigkeit und die Masse
der Elemente.
Primordiale Nukleosynthese
Bezeichnet die Phase kurz nach dem Urknall.
Photonen, Neutronen und Protonen und Elektronen
standen im Gleichgewicht, wobei die Photonen so
energiereich sind, dass sie die Kernteilchen zu
spalten vermochten. Am Ende diese
Gleichgewichtsphase begann die Kernfusionen
abzulaufen ->Entstehung 2H / 3H und He, auch Li,
Be, B, die aber zum grossen Teil wieder zerfallen.
Die Dynamik dahinter ist von der Dichte und der
Lukas Burkhard
2
Abbildung 2: Hertzsprung-Russel-Diagramm
Temperatur gesteuert. Massenzahlen von 5 und 8 sind instabil.
4
He + 4He ≠ 8A
4
He + H ≠ 5A
Finally : Im Universum sind 25% 4He und 75% H.
Produktion der Elemente in Sternen
Die Bethe-Weiszäcker-Formel
Term 1:
Anziehung durch starke Kernkraft, nur Nachbarn untereinander, E α Massenzahl
Term 2:
(Kern) = A*V(Nukleon) α R3 und Oberfläche S α R2 = A2/3. Der Oberflächenterm
beschreibt das Verhältnis zwischen Volumen und Oberfläche
Abstossung untereinander
Term 3:
Term 4:
Term 5:
Stabilisierung schwerer Kern durch Anreicherung von Neutronen?
Destabilisierung bei unterschiedlichem Z & N ?
Paarbildung von Nukleonen unterschiedlichen Spins
Lukas Burkhard
3
Der Wirkungsquerschnitt σ
Gibt die Wahrscheinlichkeit an, mit der Kernreaktionen ablaufen, vergleichbar mit der
Geschwindigkeitskonstanten einer chemischen Reaktion.
→ Formel siehe V2 S. 21
H-Brennen
Ab einer Temperatur von 107 Kelvin beginnt die Kernfusion von Protonen. Es gibt 2 Zyklen:
1. 4 1H = 4He
Total des CNO-Zyklus
2. und die Proton-Proton-Reaktion.
Metallizität von Sterne
Metall heisst in diesem Zusammenhang alles, was nicht H oder He ist. Tendenziell sind junge Sterne weniger
metallisch. Ältere gebären sich aus den Aschen von explodierten Sternen und sind somit eher angereichert
an schweren „metallischen“ Elementen.
He-Brennen
In Roten Riesen: Temperatur bei ca. 108 Kelvin. Zwei He verschmelzen zu einem 8Be (t1/2=10-16ss). Dieses
kann mit einem He zu 12C fusionieren, was das Ergebnis des Zyklus ist. Der Prozess dauerst sehr lange, da
wegen der Halbwertszeit simultan 3 He zusammenstossen müssen. Folgereaktionen sind Bildung von 20Ne,
16
O, 24Mg die alle durch den α-Prozess entstehen. (α-Teilchen=4He). Weitere Fusionen werden durch die
Coulomb-Barriere verhindert.
C-Brennen: reichert O, Mg, und Ne im Kern an bis C aufgebraucht ist, dauert einige 103 Jahre
Ne-Brennen: näxste Stufe nach C-Brennen, wenn ein roter Riese zu einem weissen Zwergen wird und seine
äusseren Hüllen abstösst.
O-Brennen: dauert wenige Jahre bis O verbraucht ist, Abkühlung und Komprimierung des Sterns
Si-Brennen: letztes Stadium, Ni, Co und Eisen, dauert nur einige Stunden bis Tage. Stern kolabiert und endet
in einer Supernova.
Als Coulombwall oder Coulombbarriere wird das Potential bezeichnet, gegen das ein positiv geladenes Teilchen
anlaufen muss, um in den Atomkern zu gelangen. Es heißt so, weil es auf der zwischen zwei elektrischen Ladungen
wirkenden Coulombkraft beruht.
C-Ne-O-Si-Brennen
Kurz: Kohlenstoff-Brennen. Der Stern kontrahiert. Die Fusionsprozesse sind in Schalen angeordnet. Der letze
Prozess, der noch Energie liefert geht bis 56Fe. Der Stern muss mind. 4 Sonnemassen haben und ein
Temperatur von 6x 108 Kelvin erreichen
Dauer: einige Stunden bis Tage
Lukas Burkhard
4
Energetik von Kernreaktionen
𝑧1∗𝑧2∗𝑒 2
𝑊 = 4𝜋𝑒
0 (𝑅1+ 𝑅2 )
ε0 = 1.418 x 10 -39 C2/eV/nm
e=1.6x10-19 C
Ekin=3/2 k*T
k=8.6173x10-5eV/K
R=R0*A1/3 (fm=femtometer)
W ist die kinetische Energie, die man braucht um eine Kernfusion auszulösen. In Sternen ist Ekin > W.
Neutroneneinfang : Elemente schwerer als A=56
Voraussetzung sind freie Neutronen. Dazu braucht man rote Riesen oder Supernovae.
N-Einfang -> instabiler Kern
β- Zerfall: N -> P + e- + υ (Neutrino)
s-Prozess (slow)
ist langsam weil neuer Kern gleich wieder zerfällt bevor ein neues Neutron addiert wird. Die Addition kann
über mehrere Isotope verlaufen bevor ein β- Zerfall stattfindet. Zeitraum: 1000 Jahre und mehr.
r-Prozess (rapid)
ausschliesslich bei allen Elementen A>209Bi. Diese Addition ist schneller als die intermediären instabilen
Isotope zerfallen können. Ausnahmen: 94,96Zr
p-Prozess
144
Sm entsteht durch diesen Prozess. Es ist ein sog. Shielded Isotop, d.h. es wird in der Nuklid-Karte von
anderen stabilen Isotopen abgeschirmt und ist deswegen selten gebildet worden.
Lukas Burkhard
5
Die geochemischen Eigenschaften der
Elemente (Stracke)
Einteilung
Die Einteilung ist nicht strikt. Es ist ausserdem die chemische Umgebung mitzuberücksichten, da z.B.
Sauerstoff als Oxid eher refraktär ist, kann aber auch als Gas vorhanden sein und ist dann volatil.
Die Kondensationstemperatur hängt ausserdem von der Konzentration des Stoffs i, dessen Umgebung, vom
Druck und der Temperatur ab.
Chemisches Potential
Ableitung der Gibbs’schen Energie nach der Stoffmenge. Man benutzt die Gleichung für das chemische
Potential um Aktivität (Partialdruck bei Gasphasen=~Stoffmenge) und (Kondensations-)Temperatur in
Beziehung zu setzen. Im Gleichgewicht ist die Gibbs-Energie 0 und die chemisches Potentiale der i Stoffe sind
in allen Phasen/Komponenten gleich.
Refraktäre: haben eine hohe Kondensationstemperatur und sind deshalb im Sonnensystem häufg. Dazu
zählen die Elemente Si, Fe, Mg, Ca, O, Al als die Wichtigsten.
Volatile: solche mit einer tiefen Kondensationstemperatur wie He, H, Edelgase. Sie bilden vermehrt
gasförmige Komponenten. Ein Element ist volatil falls seine Tc niedrig ist.
Diese Eigenschaft hängt mit der Bildungsenergie der Komponenten zusammen, die das Element
bildet (Kristalle, Minerale), und wird als Gitterenergie (El) bezeichnet.
Rekonstruktion der Zusammensetzung des solaren Urnebels
Die initiale Solarnebelzusammensetzung entspricht der ZS der Photosphäre unserer Sonne - so die Annahme.
Wenn man das Volumen des solaren Urnebels bestimmt (weiss?), kann man mit der idealen GG die
Partialdrücke der Elemente rechnen. Weil Wasserstoff so enorm häufig ist und erst am Ende der
Kondensationfolge etwas damit passiert, ist der approximierte Totaldruck gleich dem WasserstoffPartialdruck (selbst He wird vernachlässigt).
Goldschmitt-Klassifikation
atomophile: in Atmosphäre/Hydrospäre; und kommen bei 25°C/1 atm flüssig oder gasförmig vor: C,N,H
siderophile: Im Kern angereichert und häufig Metallphasen, meist Übergangsmetalle: Fe, Ni, Co, Mn, W
chalkophile: meist Übergangsmetalle, die sich gerne mit Schwefel verbinden: Cu, Zn, Ag, S,Cd
lithophile: Silikatphasen und Oxide, in Kruste und Mantel angereichert: Gruppe 1-5, B, Al, Si, F, Cl, Th, U
Siderophile und lithophile unterscheidet man auch aufgrund der Bildungsgibbsenergie eines Elements mit
Sauerstoff. In der Reaktion reinen Eisens Fesolid mit einem Elementoxid ist das Element dann lithophil, wenn
die Reaktion endergonisch ist also nicht spontan stattfindet. Siderophile haben eine geringe Affinität zu
Sauerstoff, hohe EN und Ionisationsenergie. → V3 Folie 41f.
Lukas Burkhard
6
PGE
HREE
LREE
LILE:
HFSE:
REE:
PGE:
K, Rb ,Cs, Sr (Strontium), Ba
Hf4+, Zr4+,Nb5+, Ta5+. Sie sind schwer löslich (in Wasser?)
Oxidationszahl 3+, Ausnahme Ce4+ und Eu2+ (Eu2+ ist wichtig in der Petrologie)
platin group elements, sind im Erdkern zu finden
Lukas Burkhard
7
Die Erde und der Aufbau der Planeten
(Bourdon)
Zusammensetzung der Elemente hängt ab von
Der initialen Häufigkeit der Elemente im Urnebel
Dem Abstand von der Sonne
Der Grösse der Planeten (grössere können Atmosphäre halten)
Mit zunehmendem Abstand zur Sonne nehmen die volatilen im Vergleich zu den refraktären Elementen
zu, die Dichte ab.
Chondrite sind die erst kondensierten Zeugen des Sonnensystems. Die Erde ist im Vergleich zu Kohligen
Chondriten an volatilen Elementen verarmt. Vielleicht wegen der Temperaturzonierung in Urnebel oder
wegen der Bildung der Gasplaneten. Ca. 1-10 Ma nach der Bildung der Protosonne fand die sog. T-TauriPhase statt, eine Phase wo Sonnenwinde volatile Elemente ins All wegblasen können. Man kann
annehmen, dass unsere Gasplaneten zuvor entstanden sein müssen. Die letzte Phase der Erdenstehung
fand später statt, als nur noch wenig volatile Elemente vorhanden waren: 30-100 Ma nach CAI (4.568
Ga)
Planetenenstehung
Nach Abkühlung des solaren Urnebels finden bildet sich eine Scheibe senkrecht zur Rotationsachse, wobei
Staubkörner sich zu grösseren Gebilden und schliesslich Planetesimalen formen. Dieser Prozess ist rätselhaft,
da die minimale Grösse eines Klumpens ca. 10km betragen muss, damit 2 kolldierende Planetesimale durch
Gravitation zusammenwachsen können. Wichtig ist bei diesen Prozessen die Impulserhaltung. Mit
Ausnahme der Venus drehen alle Planeten vom Nordpol gesehen im Gegenuhrzeigersinn um ihre eigene
Achse.
Datierungen
Chondren: millimetergrosse Silikatkügelchen in undifferenzierten (Stein-)Meteoriten. Die Chondren sind
aufgeschmolzen worden und schnell wieder abgekühlt. Das Ausgangsmateriel für die Chondren könnte die
Matrix selbst sein.
Chondren: Relative Datierung mit dem 26Al/27Al-Verhältnis
β—Zerfall: 26Al -> 26Mg + e+ + υ; 26Al entstand in einer Supernova (→ Orionnebel), gelangte in die Gaswolke
vor der Bildung des Sonnensystems und hat eine Halbwertszeit von 0.76 Ma. Obwohl das Isotop schon lange
„gestorben“ ist, kann man damit datieren. Bsp. Aus den Folien:
Lukas Burkhard
8
Meteoriten
In der Initialphase des Sonnensystems entstand in kleinen Asteroiden ein Metallkern (EisenMeteorite).Danach bildeten sich basaltische Schmelzen an der Oberfläche -> Achondrite haben keine
Chondren und sind magmatische Gesteine.
Daraus resultierten differenzierte Köper mit metallischem Kern und silikatischem Mantel.
Diese Asteroide wurden durch Kollision zerstört. Chondrite haben eine ähnliche Zusammensetzung wie die
Sonne, enthalten aber weniger volatile Elemente. Sie stammen von undifferenzierten Asteroiden.
CAI: Calcium-Aluminium rich inclusions; bestehen hauptsächlich aus Ca,Al,Ti-Oxiden.
Kerngrössen der Planeten
Kerngrössen nehmen von innen nach aussen ab. Innere Planeten halten einen grösseren Eisenkern als die
äusseren.
Lukas Burkhard
9
Chemische Differenzierung und Bildung
des EK (Bourdon)
Was befindet sich im Erdkern?
Beispiele aus der Vorlesung sagen, dass das Material im Erdkern wegen höheren seismischen
Geschwindigkeiten deutlich dichter sein muss als im Mantel. Der Mantel ist im Vergleich Meteoriten (18%)
an Eisen verarmt (6%). Weil Eisen nicht volatil ist, muss es also im Kern stecken. Es ist allerdings längst nicht
alles Eisen in den Kern gewandert, ein Teil befindet sich natürlich im Mantel plus weitere Hauptelemente,
die die Dichte verringern. Eine Prämisse für die Differenzierung ist ein Magmaozean nach der Bildung der
Erde. Die nötige Wärme für das Aufschmelzen stammt aus der Akkretionsenergie sowie dem Aufheizen
durch Reibung während der Differenzierung (Gravitationsenergie).
Berechnung des Eisengehaltes im EK
Man benötigt dazu verschiedene „Boxen“, resp. Reservoire. BE steht für Bulk earth und meint die gesamte
Erde, PM= primitive mantle (peridotite z.B.). Weil Al und Mg lithophil sind, gibt es im Kern kein Mg und Al.
Das ist die Annahme. Man stellt diese Bilanz auf.
Das (Fe/Mg)BE der gesamten Erde wird aus aus Meteoriten
berechnet(A). (Fe/Mg)pm kann man wahrscheinlich aus
Mantelgesteinen durch Messung ermitteln
Berechnung des Siliziumgehaltes im EK
geht genau analog mit einer Massenbilanz (Si/Mg)BE = …
Man muss sich wieder überlegen, dass Silizium nicht 100% lithophil ist und deswegen im Kern vorkommt,
was für Mg nicht der falle ist. In den Folien steht, Al/Mg für BE liest man aus der Grafik. Für die Rechnung
braucht man aber Si/Mg-Verhältnisse. Für den PM kein Problem, man kann es Messen. Für BE unklar: Grafik
zeigt ja primitive Peridotite (Also für PM).
Daten aus Folie:
Fe=77%
Si=7%
Ni=5%
O=4%
S=2%
Lukas Burkhard
10
Prozess der Kernentstehung
Mit der Vorstellung eines geschmolzenen Mantels, der sich differenziert, passt die Beobachtung, dass sich
zunehmend refraktäre Elemente im Mantel immer stärker abgereichert sind (im Vergleich zu Meteoriten).
Es stellt sich die Frage wie tief dieser Magmaozean war. Die siderophilen Elemente müssen sich vom Magma
differenziert haben und auf den Grund des Ozeans gesunken sein, wo ein chemisches Gleichgewicht
zwischen Schmelze und festem Mantel herrschte. Modelle mit Verteilungskoeffizienten Schmelze/Gestein
für ein Bar stimmen nicht mit den Beobachtungen überein.
Als Beispiel sind Nickel und Cobalt im Mantel fast gleich
häufig. Die Verteilungskoeffizienten, die druckabhängig sind,
nähern sich für diese beiden Elemente gegen 30GPa an,
sodass man die Grenze auf eine Tiefe von ca. 1000km setzen
kann. Es stellt sich die Frage ob die anderen Siderophile mit
diesem Modell übereinstimmen.
Late veneer hypothesis
Die sehr siderophilen Elemente (Edelmetalle Palladium, Gold, Rubidium, Rehnium) sind viel häufiger als man
mit obigem Konzept berechnet. Späte Ankömmlinge (Meteoriten mit chondritischer ZS) könnten dem
Erdmantel nach der Kernbildung Masse zugefügt werden.
Alter der Kernbildung
Auch wenn es vielleicht sinnlos für manchen ist, schreibe ich hier die Gleichungen auf und versuche sie
nachzuvollziehen.
Uran-Blei-Methode
Zerfallsgleichung in einem geschlossenen System:
𝑇(𝑡) = 𝑇(0) + 𝑇𝑜𝑐ℎ𝑡𝑒𝑟𝑛𝑢𝑘𝑙𝑖𝑑𝑒 (𝑛𝑎𝑐ℎ 𝑍𝑒𝑖𝑡 𝑡)
→ 𝑁(𝑡) = 𝑁(0) ∗ 𝑒 −𝜆𝑡
𝑇(𝑡) = 𝑇(0) + [𝑁(0) − 𝑁(𝑡)] = 𝑇(0) + 𝑁(0) ∗ [1 − 𝑒 −𝜆𝑡 ]
→ 𝑁(0) = 𝑁(𝑡) ∗ 𝑒 𝜆𝑡
𝑇(𝑡) = 𝑇(0) + 𝑁(𝑡) ∗ [𝑒 𝜆𝑡 − 1]
Lukas Burkhard
11
Zerfallsgleichungen für Uran-Blei-Methode:
238
U → 206Pb
und
235
U → 207Pb
→ x-Achse
→ y-Achse
Die beiden Verhältnisse werden gegeneinander geplottet. Eine Gerade ergibt sich, wenn das Alter alle
Proben gleich ist. Aus der Steigung lässt sich das Alter berechnen.
μ=238U / 204Pb(stabiles Isotop)
Meteoriten und Proben von der Erde sind auf einer Linie zu finden und somit etwas gleich alt. Das Alter gibt
an, wann Uran zu zerfallen begann und das Reservoir geschlossen wurde! Das ist ganz wichtig. Wenn ich es
richtig verstanden habe, ist das System erst geschlossen, als die Kernbildung abgeschlossen war. Denn Blei
ist volatil und wurde während der Akkretion verflüchtig und später auch in den Kern eingebaut (chalkophil).
Uran bliebt im Mantel weil es lithophil ist. Kommen so diese verschiedene Müs zustande? Was bedeuten
sie? Da blicke ich nicht durch
Hf-W-Methode
182Hf
→ 182W + e-
Hafnium ist eine lithophiles Element, während Wolfram siderophil ist.
Hf/Wsilikat> Hf/Wchondrit Die Kernbildung separierte die beiden Elemente. Im Kern gibt es kein Hf.
Hf/Wmetall=kern =0
Lukas Burkhard
12
Verteilung der Elemente (Stracke)
Einige Definitionen
Lattice strain model: das elektrostatische Feld der Liganden um ein Atom (Kristallfeld) ist für das chemische
und physikalische Verhalten wichtig, v.a. für die Übergangsmetalle. Die meisten sind oktaedrisch koordiniert
und die Ligaden werden als Punktladungen angenommen, die die d-Orbitalstruktur des ÜbergangsmetallKations beeinflussen. Um Aussagen über das chemische Verhalten zu machen, sind auch ElementSubstitutionen in Mineralien wichtig, das Verhältnis zwischen Ladung und Grösse eines Kations darüber
entscheidet, ob ein Element im Mineral (in)kompatibel ist.
KFSE: Kristallfeldstabilisierungsenergie: Ein Mass wie stabil die Elektronen in die Orbitale eingefüllt sind. Je
höher die KFSE, desto energetisch stabiler ist der Komplex.
Low spin state: es werden zuerst die energieärmeren (den Liganden abgewandten) Orbitale doppelt
besetzt., hohe KFSE
high spin state: es werden alle Orbitale mit Elektronen positiven spins besetzt -> niedrige KFSE
Viele Übergangsmetalle sind in diesen Zustand und haben magnetische Eigenschaften sowie versch. Farben.
Verteilungskoeffizienten
Bei einer Kation-Substitution ist die Gibbs-Energie gleich der Gitterenergie ΔGstrain.
Verteilungskoeffizienten sind von der Temperatur T, dem Druck und der Zusammensetzung abhängig.
Lattice-strain Gleichung
Lukas Burkhard
13
Na=6.022*1023
R=8.314 JK-1mol-1
[E]=GPa
[r0]= Å=10-10m
[T]=K
-4πNa= -910.17
Anwendung und Beispiele
Siehe Folie 10 V6
Lukas Burkhard
14
Differenziation des Erdmantels und der
Krust (Stracke)
Erkruste:
Erdmantel:
innerer Kern:
äusserer Kern:
0.8% des Volumens der Erde und 0.4% der Masse
83% des Volumens und 67% der Masse
1.7% der Masse
30.8% der Erdmasse
Spurenelemente
Wieder eine Bilanzierung:
{PM}={Chondrit}-{volatile Element bei der Akkretion verloren}-{siderohile:Kernbildung}
{Kruste}={PM}-{siderophile: Mantel}
Die kontinentale Kruste wird eingeteilt in eine LCC (lower cont. Crust) und eine Oberkruste UCC. Die untere
ist im Schnitt basaltisch, die obere granitisch bis granodioritisch. Beide zusammen andesitisch. Das Wort
stammt vom Gebirge der Anden, und tönt schon an, dass Subduktionsvulkanismus (IAB’s) eine wichtige Rolle
für die Bildung kontinentaler Kruste spielt, da man aus der Schmelze des PM ein Basalt erhält. Alte Kratone
sind meist umrandet von jüngeren Krustenteilen. Die ozeanische Kruste ist von der Zusammensetzung her
viel homogener als die kontinentale Kruste.
Mithilfe von Elementhäufigkeiten kann man den Prozess der Krustenbildung im Sinne einer Bilanzierung wie
oben verstehen. Die kontinentale Kruste ist an inkompatiblen Elementen angereichert, die Spidergrams des
Mantels sind komplementär zur Kruste, woraus man schliessen kann, dass die kontinentale Kruste insgesamt
durch partielles Aufschmelzen des PM entstanden ist. Die Spurenelementzusammensetzung der OC ist dem
Mantel ähnlicher, sie entsteht aus Schmelzen des depleted mantle (PM minus kont. Kruste). Der DM ist aber
keinesfalls der ganze Erdmantel, nur der oberer Erdmantel. Siehe V7 folie 36
Etwa 66% des Mantels ist durch part. Aufschmelzen abgereichert worden.
Unregelmässigkeiten bei den Spurenelementen im Vergleich zu Modellrechnungen(orange und hellgrün):
Pb ist angereichert in der Kruste
Ta&Nb (Niob) sind abgereichert.
Der andere beteiligte Prozess: IAB
Lukas Burkhard
15
Plg kann gut einbauen: Sr2+ (Strontium) und Eu2+.
X
y
x < y → chemisch weiter entfernt. Weg lower zu upper crust: Plg wurde wegfraktioniert.
Prozess
Pb+ ; Ta/Nb -
Primitive Mantle
??
?? Subduction Factory reichert Pb an etc.
underplating
LCC
melting
CC
OC ~ DM (depleted mantle
Subduc
.
H2o + xx frac. = plg(Eu2+) → LCC angereichert
Lukas Burkhard
UCC
16
Probleme
Wenn man die untere Kruste als Ausgangsmaterial der UCC nimmt, müssten beide zusammen basaltische ZS
haben, sie hat aber andesitische ZS. Die obere Kruste ist etwa 13 km mächtig und soll laut Folien aus etwa
14% Schmelze der LCC enstanden sein. Das würde eine durchschnittliche Dicke der Kruste von 90km
ergeben. Die Erklärung ist, dass die Unterkruste bei vielen Subduktionszyklen wegerodiert wurde und im
Mantel verschwand
→ Kruste wird dünner
→ Kruste wird felsischer
Älteste Kratone (Archaikum; >2.5Ga )sind anders entstanden. Dort ist z.B. Eu nicht abgereichert und IAB
haben keine grosse Rolle gespielt.
Zusammenfassung von Stracke
Lukas Burkhard
17
Die Entstehung der Atmosphäre
(Bourdon)
Primitive Atmosphäre
Die primitive Atmosphäre bestand aus Wasserstoff und Helium.
Die Gravitationskraft war nicht stark genug, um diese Gase zu
halten. Die heutige Atmosphäre ist aus dem Erdmantel entgast:
N, S, O, Edelgase
Iod-Xenon-Methode
129
Β—Zerfall:
I → 129Xe
stabile Isotope: 130Xe, 129Xe, 127I
τ=16Ma
Man stelle sich vor, zu einem Zeitpunkt entsteht die
Atmosphäre durch Ausgasung. Im Mantel befinden sich alle
Isotope von Iod und Xenon, aber nur Xenon gast aus. Wenn nun Jod noch im Mantel vorhanden ist, wird
Xe129/Xe130 und I/Xe im Mantel grösser. Wegen der kurzen Halbwärtszeit muss die Atmosphäre noch vor
5τ nach dem Zeitpunkt entstanden sein, als der Zerfall
begann. Sonst würde man keine Xe/Xe Unterschiede in den
Rerservoiren feststellen. Weil kein Jod in der Atmosphäre
vorhanden ist, wird kein Xe129 gebildet, und Xe/Xe bleibt
konstant.
Initailer pCO2
In den Vorlesungsunterlagen ist eine Gleichung/Modell
hergeleitet, die unter Annahme eines Gasgleichgewichts
(Henry) zwischen Magmaozean und Atmosphäre ein Druck
von 54bar voraussagt. Würde man allen Kohlenstoff in
Karbonaten und und organischen verbindungen
freisetzten, käme man auf die gleiche Zahl. Das ist eher ein
Zufall.
Zusammensetzung der Gase
Die Zusammensetzung ist abhängig von der Fugazität der Gase. Die Fugazität ist das gleich wie die Aktivität
bei Konzentrationen in Lösungen. Man muss also den Druck eines Gases bei sehr hohen Drücken korrigieren,
weil es sich um reale Gase handelt und die Gasteilchen dann miteinander interagieren. Der korrigierte Druck
von Gasen bestimmt also in Reaktionen, wo das Gleichgewicht liegt. Meist ist mit Sauerstoff-Fugazität auch
der Redox-Zustand gemeint.Als die Erde entstand, wurde O von Eisen (und Metallen) kontrolliert. Als die
Atmosphäre mit dem Mantel im Gleichgewicht stand, gab es ein wenig mehr O und der Zustand war nicht
mehr so stark reduziert, aber es gab viel freies Eisen, die Fugazität wird vom ausgasenden Mantel
kontrolliert. Die Bindung des vielen CO2 in Karbonaten und die Kondensation des Wassers, das auch CO2
bindet, häuften N2 an. Dafür musste die Leuchtkraft der Sonne schwächer sein als heute. Der Sauerstoff, der
Lukas Burkhard
18
heute 21% ausmacht, wurde durch Photosyntheses gebildet, gelangte aber erst ind die Atmosphäre, als das
meiste Eisen in den Ozeanen oxidiert war → sedimentäre Uranitlagerstätten.
Lukas Burkhard
19
Chemische Wechselwirkungen an der
Erdoberfläche (Bourdon)
Lukas Burkhard
20











