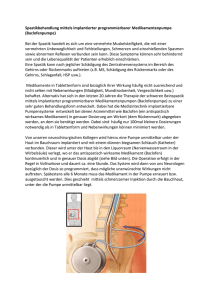
Spastik - evidentia
Werbung

ADDITIONAL SLIDE KIT BOTULINUMTOXIN BEI SPASTIK Autor: Dr. med. Christian Kätterer Supervision: PD Dr. med. Manuel Meyer Letzte Aktualisierung: Dezember 2012 Zur Verfügung gestellt durch: Ipsen Pharma GmbH * Dieses Additional Slide Kit wurde von einem unabhängigen Team von Neurologen erstellt und dient ausschliesslich Informationszwecken. Autoren und Aktualisierung Autor: Dr. med. Christian Kätterer Supervisor: Dr. med. Manuel Meyer Letzte Aktualisierung: Dezember 2012 BOTULINUMTOXIN BEI SPASTIK 2 Inhalt 1. Definition, Ursache und Klinik Seite 06 2. Epidemiologie der Spastik 13 3. Therapieoptionen 17 4. Botulismus 27 5. Wirkungsmechanismus Botulinumtoxin 32 6. Zulassung und Indikationen 39 7. Präparate & Dosierungen 45 8. Definition des Behandlungsziels 56 9. Weitere praxisrelevante Aspekte der Therapie 63 10. Nachsorge 71 11. Sicherheit 75 12. Referenzen 77 BOTULINUMTOXIN BEI SPASTIK 3 Gebrauchshinweise Ansichtsoptionen des Slide Kits Folien Folien Bildschirmansicht: Klicken Sie im Menü ‚Ansicht‘ auf ‚Normalansicht‘. Folien inkl. Notizen Folien und Notizenseiten mit Hintergrundinformationen Bildschirmansicht: Klicken Sie im Menü ‚Ansicht‘ auf ‚Notizenseite‘. BOTULINUMTOXIN BEI SPASTIK 4 Inhalt 1. Definition, Ursache und Klinik Seite 06 2. Epidemiologie der Spastik 13 3. Therapieoptionen 17 4. Botulismus 27 5. Wirkungsmechanismus Botulinumtoxin 32 6. Zulassung und Indikationen 39 7. Präparate & Dosierungen 45 8. Definition des Behandlungsziels 56 9. Weitere praxisrelevante Aspekte der Therapie 63 10. Nachsorge 71 11. Sicherheit 75 12. Referenzen 77 BOTULINUMTOXIN BEI SPASTIK 5 1. Definition, Ursache und Klinik Spastik: Begriff und Ursachen Spastik Aus dem Griechischen (spasmos, «Krampf») geschwindigkeitsabhängig erhöhter Dehnungswiderstand des willkürlich nicht aktivierten Skelettmuskels Synonym: Spastizität Ursachen Läsionen im Gehirn oder/und im Rückenmark (Schädigung des ersten Motoneurons der Pyramidenbahn) BOTULINUMTOXIN BEI SPASTIK 6 1. Definition, Ursache und Klinik Spastik: Pathophysiologie Läsion deszendierender motorischer Bahnen Verschiedene plastische Adaptationsprozesse setzen ein: • Beeinträchtigte Reflexfunktionen • Veränderte muskuläre Mechanismen Eine initial schlaffe Lähmung wird zunehmend spastisch. [Dietz und Sinkjaer, 2007] Die Übererregbarkeit des spinalen Dehnungsreflexes ist demnach nur ein (kleiner) pathophysiologischer Bestandteil der Mechanismen, die zur Spastik führen. BOTULINUMTOXIN BEI SPASTIK 7 1. Definition, Ursache und Klinik Spastik: Diagnostik/1 Anamnese Identifikation möglicher Ursachen inklusive Traumata oder Infekte, die schon Monate zurückliegen können. Begleiterscheinungen erfragen, z.B. spinaler Läsionen. Neurologische Untersuchung Nebst der eigentlichen Identifikation der Spastik sind zwei Untersuchungsschritte massgeblich: 1. Topische Diagnostik (Lokalisation der Schädigung?) 2. Suche nach zentralnervösen Begleitsymptomen Cave: Zervikale Myelopathien beginnen häufig mit einer spastischen Paraparese der Beine. BOTULINUMTOXIN BEI SPASTIK 8 1. Definition, Ursache und Klinik Spastik: Diagnostik/2 Zusatzuntersuchungen Folgende Untersuchungen können je nach anamnestischen Angaben und klinischen Befunden sinnvoll sein: • Elektromyoneurographie • Sensibel und motorisch evozierte Potentiale • Computer-Tomographie, Magnetresonanz-Tomographie (Rückenmark, Schädel) • Blutuntersuchungen, Lumbalpunktion • Molekulargenetik BOTULINUMTOXIN BEI SPASTIK 9 1. Definition, Ursache und Klinik Spastik: Diagnostik/3 Modifizierte Ashworth-Skala Passive Durchbewegungen der zu untersuchenden Muskelgruppen. 0 Kein erhöhter Tonus 1 Leichte Tonuserhöhung, die an einem „catch and release“ erkennbar wird oder an einem minimalen Widerstand am Ende des Bewegungsausmaßes, wenn das betroffene Gliedmass in Flexion oder Extension bewegt wird. 2 Leichte Tonuserhöhung, die an einem „catch“ erkennbar wird, der gefolgt wird von einem minimalen Widerstand durch den restlichen (weniger als die Hälfte des) Bewegungsweg. 3 Stärker ausgeprägte Tonuserhöhung durch die meisten Anteile des Bewegungsweges, die betroffenen Gliedmaßen sind aber leicht beweglich. 4 Erhebliche Erhöhung des Muskeltonus, passive Bewegung ist schwierig. BOTULINUMTOXIN BEI SPASTIK 10 1. Definition, Ursache und Klinik Spastik: Diagnostik/4 Tardieu-Skala Der Patient liegt entspannt auf dem Rücken. Rasche und langsame passive Bewegungen. 0 Kein Widerstand während der passiven Bewegung durch das volle Bewegungsausmass 1 Leichter Widerstand während der passiven Bewegung ohne klaren Stopp in einer bestimmten Winkelstellung 2 Klarer Stopp in einer bestimmten Winkelstellung, der die passive Bewegung unterbricht, aber dann nachlässt 3 Erschöpflicher Klonus in einer bestimmten Winkelstellung (der kürzer als 10 Sekunden dauert, wenn die Position gehalten wird) 4 Unerschöpflicher Klonus in einer bestimmten Winkelstellung (länger als 10 Sekunden, wenn die Position gehalten wird) BOTULINUMTOXIN BEI SPASTIK 11 Inhalt 1. Definition, Ursache und Klinik Seite 06 2. Epidemiologie der Spastik 13 3. Therapieoptionen 17 4. Botulismus 27 5. Wirkungsmechanismus Botulinumtoxin 32 6. Zulassung und Indikationen 39 7. Präparate & Dosierungen 45 8. Definition des Behandlungsziels 56 9. Weitere praxisrelevante Aspekte der Therapie 63 10. Nachsorge 71 11. Sicherheit 75 12. Referenzen 77 BOTULINUMTOXIN BEI SPASTIK 12 2. Epidemiologie der Spastizität Häufigkeit der Spastik am Beispiel des ischämischen Schlaganfalls • Inzidenz des ischämischen Schlaganfalls: 150 – 200 pro 100‘000 [Wade 1992; Kolominsky-Rabas et al., 1998; Bakhai 2004] • 24% Spastizität in der ersten Woche [Wissel et al., 2010] • 19-38% Spastizität im ersten Jahr [Watkins et al., 2002; Sommerfeld et al., 2004] • 4-9% Spastizität nach einem Jahr so schwerwiegend, dass sie behandelt werden sollte [Leathley et al., 2004] BOTULINUMTOXIN BEI SPASTIK 13 2. Epidemiologie der Spastizität Prävalenz invalidisierender Spastik 1 Jahr nach Schlaganfall http://www.stroke.org/site/DocServer/StrokePerceptions_FinalSurveyResults_2006.pdf?docID=1941 BOTULINUMTOXIN BEI SPASTIK 14 2. Epidemiologie der Spastizität Bedeutung für die Praxis Die Prävalenz der Post-Stroke-Spastik (PSS) 1 Jahr nach Schlaganfall variiert zwischen 17 und 38%. [Lundström et al., 2008; Watkins et al., 2002] 1 Jahr nach Stroke [Watkins et al., 2002] • Stroke Patienten mit Spastik sind signifikant funktionell mehr beeinträchtigt als solche ohne. • Patienten mit PSS sind signifikant häufiger in Institutionen betreut als Patienten ohne PSS. [Leathley et al., 2004] BOTULINUMTOXIN BEI SPASTIK 15 Inhalt 1. Definition, Ursache und Klinik Seite 06 2. Epidemiologie der Spastik 13 3. Therapieoptionen 17 4. Botulismus 27 5. Wirkungsmechanismus Botulinumtoxin 32 6. Zulassung und Indikationen 39 7. Präparate & Dosierungen 45 8. Definition des Behandlungsziels 56 9. Weitere praxisrelevante Aspekte der Therapie 63 10. Nachsorge 71 11. Sicherheit 75 12. Referenzen 77 BOTULINUMTOXIN BEI SPASTIK 16 3. Therapieoptionen Therapieoptionen bei Spastik – Übersicht Spastisches Syndrom Funktionelle Einschränkung Ashworth Skala / Tardieu Skala Gelenkstatus Physikalische Therapie Systemische Medikation Fokale Therapie Physiotherapie Antispastika Gips Muskelrelaxantien Botulinumtoxin A intramuskulär Johnson-Splintschiene Sedativa (Phenylblockade) Neurolyse Tenotomien BOTULINUMTOXIN BEI SPASTIK 17 3. Therapieoptionen Stufentherapie in Abhängigkeit der Lokalisation und Ausbreitung Generalisierte Spastik Regionale Spastik Fokale Spastik Physiotherapie Physiotherapie Physiotherapie Orale medikamentöse Therapie Intrathekale BaclofenTherapie Botulinumtoxin [www.dgn.org, Wissel et al., 2009] BOTULINUMTOXIN BEI SPASTIK 18 3. Therapieoptionen Physiotherapie Basis jeder Therapie ist Physiotherapie, je nach Patient auch Ergotherapie (auch additiv zu jeder Therapie) Evidenzgrad: Niedrig (unethisch, Physiotherapie den Patienten vorzuenthalten) Ziele: - Training motorischer Funktionen - Vermeidung von Kontrakturen Dauer: Je nach Verlauf der Spastik bis lebenslänglich, bei schwerer Spastik wöchentlich mindestens 2x 30-45 Minuten, Anleitung zu selbständigen Übungen [Wissel et al., 2011] BOTULINUMTOXIN BEI SPASTIK 19 3. Therapieoptionen Orale und intrathekale Therapie/1 Orale Therapie Indikationen: - Schwere Spastik bei mehrheitlich immobilen Patienten - Unterstützung der Physiotherapie - Erleichterung der Pflege - Vermeidung von Kontrakturen Mechanismus: - Abnahme der Exzitation von Motoneuronen rein symptomatisch Dosierung: - Baclofen: 3x5 mg bis 30-80 mg täglich - Tizanidin: 3x2 mg bis 12-24 mg täglich (cave: Überdosierung kann zu Zunahme der Funktionseinschränkung und zur Physiotherapie-Verunmöglichung führen) [Wissel et al., 2011] BOTULINUMTOXIN BEI SPASTIK 20 3. Therapieoptionen Orale und intrathekale Therapie/2 Intrathekale Infusions-Behandlung [Wissel et al., 2011] BOTULINUMTOXIN BEI SPASTIK 21 3. Therapieoptionen Orale und intrathekale Therapie/3 Intrathekale Infusions-Behandlung Indikationen: - Ausgeprägte und chronische Para- oder Tetraspastik spinaler oder zerebraler Genese - Medikamentöse Behandlung und Physiotherapie unzureichend wirksam oder toleriert Mechanismus: - Abnahme der Exzitation von Motoneuronen rein symptomatisch Dosierung: - Baclofen intrathekal: Dosisanpassung nach monitorisierter (Atmung, Blutdruck) intrathekaler Bolusinjektion (meist 25-100 µg) individuell stark unterschiedliche Zieldosis BOTULINUMTOXIN BEI SPASTIK 22 [Wissel et al., 2011] 3. Therapieoptionen Botulinumtoxin A (BoNT/A) Grundsätzliche Aspekte einer Indikationsstellung für Botulinumtoxin • Spastik ist schwer, beeinträchtigt Pflege oder Funktionen und verursacht Komplikationen. • Andere Behandlungsstrategien (physikalisch, systemisch-medikamentös) sind ausgeschöpft, ineffizient oder führen zu Nebenwirkungen. • Die Spastik zeigt ein fokales Muster. • Behandlungs- und Erwartungsziele sind abgesprochen und realistisch (Goal-attainment). • Etablierte Kontrakturen sind ein Behandlungsausschluss. • Fachphysiotherapeutische Behandlung ist simultan gewährleistet. • Behandlungs- und Folgefinanzierung ist sichergestellt. • Behandlungsdokumentation und Verlaufskontrollen erfolgen standardisiert. - Über 70 klinische Studien stützen die Empfehlung zu BoNT/A - Der Einsatz von oralen Antispastika vor BoNT/A wird nicht mehr empfohlen. [Wissel et al., 2009] BOTULINUMTOXIN BEI SPASTIK 23 3. Therapieoptionen Botulinumtoxin A (BoNT/A) Allgemeine Behandlungsziele bei Spastik 1. Kontrakturprophylaxe 2. Schmerzreduktion 3. Verbesserung der motorischen Funktionen und somit Pflege-Erleichterung BoNT A hat in mehreren kontrollierten Studien gezeigt, dass eine lokale Behandlung den spastischen Muskeltonus reduzieren und passive Funktionen verbessern kann. Studien, die individualisierte BoNT-A-Behandlungen mit abgestimmten Kombinationen in Verbindung mit anderen Therapien untersuchen, konnten größere Effekte und auch funktionelle Verbesserungen zeigen. [Wissel et al., 2003; Wissel et al., 2011] BOTULINUMTOXIN BEI SPASTIK 24 3. Therapieoptionen Wie wird die Behandlung mit BoNT/A-Injektionen zu einem Behandlungserfolg? Symptomadäquate Muskelauswahl multi-professionelles Reha-Team Genaue Lokalisation der Injektionen kontrollierte Injektion Einsatz zusammenwirkender Wirkprinzipien multi-professionelles Reha-Team Realistische Behandlungsziele Absprache mit Patient & Pflegenden: Zieldefinition! BOTULINUMTOXIN BEI SPASTIK 25 Inhalt 1. Definition, Ursache und Klinik 2. Epidemiologie der Spastik 13 3. Therapieoptionen 17 4. Botulismus 27 5. Wirkungsmechanismus Botulinumtoxin 32 6. Zulassung und Indikationen 39 4. Präparate & Dosierungen 45 5. Definition des Behandlungsziels 56 6. Weitere praxisrelevante Aspekte der Therapie 63 7. Nachsorge 71 8. Sicherheit 75 9. Referenzen 77 BOTULINUMTOXIN BEI SPASTIK Seite 06 26 4. Botulismus Geschichte • Hungersnöte und Zerfall der Ordnung und Hygiene zu Kriegszeiten • Mysteriöse Krankheit nach Konsum von Würsten Botulismus („botulus“ ist das lateinische Wort für Wurst) Napoleonische Kriegswirren BOTULINUMTOXIN BEI SPASTIK 27 4. Botulismus Geschichte Erstbeschreiber: Justinus Kerner (deutscher Arzt, 1786-1862) Beschreibung der damalig epidemischen Erkrankung: • Lähmung der Muskulatur • Bewegungsstörung der Speiseröhre • Hauttrockenheit Justinus Kerner • Abnahme des Speichels u.a. Schrift von 1817: Krankheitserreger unterbricht Nervenleitungen Schrift von 1822: Vorwegnahme der therapeutischen Anwendung des Botulinumtoxins vorweg (bei Übererregung des Nervensystems, Verkrampfungen, Sialorrhoe) Erst 150 Jahre später wird seine Vision Realität. BOTULINUMTOXIN BEI SPASTIK 28 4. Botulismus Geschichte Identifikation des Krankheitserregers durch van Ermengen (1897) Bacterium Clostridium Botulinum • Natürlich vorkommendes, harmloses Bakterium • In Sauerstoff-freier Umgebung Produktion von 8 verschiedenen Toxinen • Toxin Typ A hat grösste therapeutische Wirkung • Grosse Moleküle (Glykoproteine) • Medizin: aufwändige Isolation/Aufbereitung des Botulinum-Toxins BOTULINUMTOXIN BEI SPASTIK 29 4. Botulismus Clostridium Botulinum Geschichte: Clostridium Botulinum BOTULINUMTOXIN BEI SPASTIK 30 Inhalt 1. Definition, Ursache und Klinik Seite 06 2. Epidemiologie der Spastik 13 3. Therapieoptionen 17 4. Botulismus 27 5. Wirkungsmechanismus Botulinumtoxin 32 6. Zulassung und Indikationen 39 7. Präparate & Dosierungen 45 8. Definition des Behandlungsziels 56 9. Weitere praxisrelevante Aspekte der Therapie 63 10. Nachsorge 71 11. Sicherheit 75 12. Referenzen 77 BOTULINUMTOXIN BEI SPASTIK 31 5. Wirkungsmechanismus Botulinumtoxin Wirkungsmechanismus Endplattenregion Wirkmechanismus BoNT/A blockiert selektiv die Verbindung zwischen Nerv und Muskel an der an der motorischen Endplatte Muskel einer Maus Synaptischer Spalt Motorische Endplatte BOTULINUMTOXIN BEI SPASTIK 32 5. Wirkungsmechanismus Botulinumtoxin Botulinumtoxin blockiert präsynaptisch die ACh-Ausschüttung [Abbildung in Anlehnung an Dickerson und Janda, 2006] BOTULINUMTOXIN BEI SPASTIK 33 5. Wirkungsmechanismus Botulinumtoxin Proteinstruktur Botulinomtoxin Serotypen und ihre intrazellulären Zielpunkte Sero-Type Target-Protein A SNAP-25 B VAMP C1 SNAP-25 / Syntaxin D VAMP E SNAP-25 F VAMP G VAMP BOTULINUMTOXIN BEI SPASTIK 34 5. Wirkungsmechanismus Botulinumtoxin Effekte auf zusätzliche Neurotransmitter Substanz P Welch et al. Sensitivity of embryonic rat dorsal root ganglia neurons to Clostridium botulinum neurotoxins. Toxicon 2000; 38: 245-258. Glutamat Cui et al., Subcutaneous administration of botulinum toxin A reduces formalin-induced pain. Pain 2004; 107: 125-133. Calcitonin gene-related peptide (CGRP) Durham et al. Regulation of calcitonin gene-related peptide secretion from trigeminal nerve cells by botulinum toxin type A: implications for migraine therapy. Headache 2004; 44: 35-42. BOTULINUMTOXIN BEI SPASTIK 35 5. Wirkungsmechanismus Botulinumtoxin Erkenntnisse aus der klinischen Anwendung • Verlässliche Substanz mit vielseitigem therapeutischem Einsatz • Bislang keine wesentlichen Nebenwirkungen • Nur vorübergehende und lokale Wirkung • Vollständiger Abbau der Substanz • Ungefährlich, weil kleinste Dosierung (0.5-100 Nanogramm) • Pharmakologische Grundsatz nach Paracelsus eingehalten • Abstand der therapeutischen Dosis zur tödlichen Dosis grösser als bei Aspirin oder Insulin BOTULINUMTOXIN BEI SPASTIK 36 5. Wirkungsmechanismus Botulinumtoxin Antikörper-induziertes Therapie-Versagen Btx A Dysport® <1% [Naumann et al., 2012; Mejia et al., 2005] «old» BOTOX® 5% [Dressler et al., 2000] Btx B NeuroBloc® Bei Patienten mit Btx-A-Antikörpern >40% [Dressler et al., 2003] Bei de novo-Patienten >18% [Elan SPC] Geschwärzte Felder enthalten Fachinformationen, die für Ärzte bestimmt sind. Diese sind nur in der Datei sichtbar, die nach Registrierung als ärztliche Fachperson heruntergeladen werden kann. BOTULINUMTOXIN BEI SPASTIK 37 Inhalt 1. Definition, Ursache und Klinik Seite 06 2. Epidemiologie der Spastik 13 3. Therapieoptionen 17 4. Botulismus 27 5. Wirkungsmechanismus Botulinumtoxin 32 6. Zulassung und Indikationen 39 7. Präparate & Dosierungen 45 8. Definition des Behandlungsziels 56 9. Weitere praxisrelevante Aspekte der Therapie 63 10. Nachsorge 71 11. Sicherheit 75 12. Referenzen 77 BOTULINUMTOXIN BEI SPASTIK 38 6. Zulassung und Indikationen Botulinumtoxin A (BoNT/A) Botulinumtoxin A-Zulassungen (Kompendium 2012) Dystonien: Blepharospasmus, Spasmus hemifacialis, fokale Dystonien, Torticollis Korrektur des Strabismus bei Patienten über 12 Jahren Fokale Spastik, einschliesslich der oberen Extremitäten, nach Schlaganfall Dynamische Spitzfussstellung (Equinus-Deformität) ohne Retraktion und ohne bedeutende Atrophie aufgrund spastischer Störungen bei Patienten mit infantiler Zerebralparese, die 2 Jahre und älter sind Primäre Hyperhidrosis axillae bei Erwachsenen Harninkontinenz infolge neurogener Detrusorhyperaktivität in Zusammenhang mit einer neurologischen Erkrankung (wie z.B. Rückenmarksverletzung, Multiple Sklerose) bei Erwachsenen BOTULINUMTOXIN BEI SPASTIK 39 6. Zulassung und Indikationen Indikationen für eine Behandlung mit Botulinumtoxin Pädiatrie Neurologie Neuro-Urologie NeuroRehabilitation Ophthalmologie SpeichelManagement Blepharospamus (off-label) Strabismus Spastizität Cerebralparesen Fokale Spastik - nach Stroke - nach NeuroTrauma - bei MS (off-label) - bei spinalem Trauma DetrusorSphinkerDyssynergie NOD Hemispasmus facialis (off-label) Fokale Dystonien BOTULINUMTOXIN BEI SPASTIK 40 6. Zulassung und Indikationen Mögliche Einsatzgebiete von Botulinumtoxin (Auswahl) Hemmung der neuroglandulären Transmission Hemmung der Schweißproduktion Kontraktionshemmung der glatten Muskulatur Kontraktionshemmung des M. detrusor Sialorrhoe Hyperhidrosis Analfissur, ant. Rektocele, Achalasie Neurogene Blasenstörung Lähmung der quergestreiften Muskulatur Zerebralparese Dystonie Spastik BOTULINUMTOXIN BEI SPASTIK 41 6. Zulassung und Indikationen Behandlung der Spastik: Evidenz nach Zielgebiet/1 Lokalisation Effekt Studie/ Evidenzklasse Ätiologie Fallzahl Spastik der Hand Tonusreduktion 8 Klasse 1b 4 Klasse 1b 4 Klasse 1a Schlaganfall Schlaganfall, Trauma, MS ICP Metaanalysen (2-11 Studien) 24-148 20-52 Pflegeerleichterung 2 Klasse 1b Schlaganfall 126-148 Schmerzreduktion 2 Klasse 1b 1 Klasse 2b 1 Klasse 1a Schlaganfall Schlaganfall Schlaganfall 24-126 126 Tonusreduktion 7 Klasse 1b 3 Klasse 1b Schlaganfall Schlaganfall, Trauma, MS, ICP, Hypoxie, Tumor, degenerative Erkrankungen 24-148 21-52 Funktionsverbesserung 1 Klasse 1b Schlaganfall, Trauma, MS, degenerative Erkrankungen 50 Armbeugespastik [Wissel et al., 2012] BOTULINUMTOXIN BEI SPASTIK 42 6. Zulassung und Indikationen Behandlung der Spastik: Evidenz nach Zielgebiet/2 Lokalisation Effekt Studie/ Evidenzklasse Ätiologie Fallzahl Spastik der Schulter Tonusreduktion 1 Klasse 2b Schlaganfall 17 Schmerzreduktion 2 Klasse 1b 2 Klasse 2b Schlaganfall Schlaganfall 20-29 17-22 Verbesserung des pROM 2 Klasse 1b 2 Klasse 2b Schlaganfall Schlaganfall 20-29 17-22 Adduktorenspastik Kniestreckspastik Tonusreduktion und Pflegeerleichterung 1 Klasse 1b 1 Klasse 1b MS MS 74 9 Spastischer Fuss Tonusreduktion Schlaganfall, Trauma 23 Schlaganfall Schlaganfall, Tumor, Trauma, ICP, Hypoxie 45-235 23-52 Schmerzreduktion und Funktionsverbesserung 2 Klasse 1b 2 Klasse 1b [Wissel et al., 2012] BOTULINUMTOXIN BEI SPASTIK 43 Inhalt 1. Definition, Ursache und Klinik Seite 06 2. Epidemiologie der Spastik 13 3. Therapieoptionen 17 4. Botulismus 27 5. Wirkungsmechanismus Botulinumtoxin 32 6. Zulassung und Indikationen 39 7. Präparate & Dosierungen 45 8. Definition des Behandlungsziels 56 9. Weitere praxisrelevante Aspekte der Therapie 63 10. Nachsorge 71 11. Sicherheit 75 12. Referenzen 77 BOTULINUMTOXIN BEI SPASTIK 44 7. Präparate & Dosierungen Geschwärzte Felder enthalten Fachinformationen, die für Ärzte bestimmt sind. Diese sind nur in der Datei sichtbar, die nach Registrierung als ärztliche Fachperson heruntergeladen werden kann. Botulinumtoxin Typ A Dysport® Botox® (Hersteller: Ipsen) (Hersteller: Allergan) Lösung in NaCl Therapeutische Äquivalenz bei 3:1 (Trend zu 2:1 bis 2.5:1) BOTULINUMTOXIN BEI SPASTIK 45 7. Präparate & Dosierungen Wirkungseintritt und pharmakologische Kenndaten Substanz • Toxindiffusion im Muskel nach i.m. Injektion innert 1-3 Tagen • Wirkungseintritt innert 4-7 Tagen • EMG • Nachweisbare Chemodenervation, resp. Polyphasie bei Reinervation / nach Injektion Wirkungsmaximum nach 14 Tagen bis 4 Wochen • Applikation single point oder multipoint • Wirkungsdauer 10-16 Wochen • • Reinjektionsintervalle von 90 Tagen wegen Risiko der AK-Induktion (<0,5%) Elektrostimulation (niederfrequent) nach Injektion kann Wirkung von Botulinumtoxin verstärken [Frasson et al., 2005] • Verdünnung in NaCl 0.9% (2.5 ml) • Injektionstechnik nach anatomischen Richtlinien • Ultraschallunterstützte Injektion (Pädiatrie, zunehmend auch Neurologie) BOTULINUMTOXIN BEI SPASTIK 46 7. Präparate & Dosierungen Kontraindikationen • Neuromuskuläre Erkrankungen (z.B. Myasthenia gravis oder Lambert Eaton Syndrom) • Pharmaka mit Beeinträchtigung der neuromuskulären Übertragung (z.B. Aminoglycosid und Makrolidantibiotika) • Schwangerschaft und Stillzeit • Einnahme von Gerinnungshemmern, resp. Medikamenten, die Gerinnung beeinträchtigen • Generalisierte oder polysegmentale Spastik • Etablierte Kontrakturen • Mangelnde Verfügbarkeit physiotherapeutischer Nachsorge • Neurodegenerative Erkrankungen (Ausnahme ALS bei fokaler Spastik) • Infekt mit systemischer Beteiligung • (Fehlende Kostengutsprache) BOTULINUMTOXIN BEI SPASTIK 47 7. Präparate & Dosierungen Geschwärzte Felder enthalten Fachinformationen, die für Ärzte bestimmt sind. Diese sind nur in der Datei sichtbar, die nach Registrierung als ärztliche Fachperson heruntergeladen werden kann. Dosierungen Botulinumtoxin Typ A Dysport® (Ipsen) Botox® (Allergan) Zulässige Höchstdosis Zulässige Höchstdosis pro Behandlungssitzung 400 Units (gemäss Registrierung) = 4 Violen à 100 Units (im Einzelfall kann eine Behandlungsdosis von 600 Units noch zulässig sein) • Zervikale Dystonie: 500 Units • Armspastik : 1000 Units • Blepharospasmus: 120 Units / Auge • Hemifacialer Spasmus: wie Blepharospasmus Neuropädiatrie: 6 Units pro kg KG • Dynamischer Spitzfuss (Kinder ab 2 Jahre): 10-max. 20 Units/kg KG, maximal 500 Units pro Patient BOTULINUMTOXIN BEI SPASTIK Dosierungen pro Muskel: von 5 - 7,5 Units M.orbicularis bis zu 150 Units (M. iliopsoas) gemäss Referenztabellen 48 7. Präparate & Dosierungen Geschwärzte Felder enthalten Fachinformationen, die für Ärzte bestimmt sind. Diese sind nur in der Datei sichtbar, die nach Registrierung als ärztliche Fachperson heruntergeladen werden kann. Dosierung der BoNT/A-Produkte Maximale empfohlene Dosis pro Injektionssitzung bezogen auf verschiedene BoNTA-Präparate bei intramuskulärer Injektion 1.000 MU Dysport® 600 MU Botox® Maximale empfohlene Dosis pro Injektionsstelle bezogen auf verschiedene BoNT-APräparate bei intramuskulärer Injektion 125 MU Dysport® 50 MU Botox® [Wissel et al., 2011] BOTULINUMTOXIN BEI SPASTIK 49 7. Präparate & Dosierungen Dosierung der BoNT/A-Produkte/1 Indikation Abotulinumtoxin A (MU) Onabotulinumtoxin A (MU) M. biceps brachii 100-360 40-120 M. brachialis 75-240 30-80 M. brachiordialis 75-240 30-80 M. deltoideus 50-180 20-60 M. flexor carpi radialis 15-225 5-75 M. flexor carpi ulnaris 15-150 5-50 M. flexor digitorum profundus 15-225 5-75 M. flexor digitorum superficialis 15-225 5-75 M. flexor pollicis longus 15-150 5-50 Mm. interossei manus 7.5-30 je Muskel 2.5-10 je Muskel M. pectoralis major 100-300 25-100 M. pronator teres 30-150 10-50 M. opponens pollicis 7.5-30 2.5-10 M. teres major 75-150 25-50 M. triceps brachii 120-360 40-120 Spastik und Extremitätendystonie – Obere Extremität [Wissel et al., 2011] BOTULINUMTOXIN BEI SPASTIK 50 7. Präparate & Dosierungen Dosierung der BoNT/A-Produkte/2 Indikation Abotulinumtoxin A (MU) Onabotulinumtoxin A (MU) M. adduktor longus, brevis 150-225 je Muskel* 50-75 je Muskel* M. adduktor magnus 150-225* 50-75* M. biceps femoris 150-225* 50-75* M. extensor digitorum longus 75-150* 25-50* M. extensor hallucis longus 75-225* 25-75* M. flexor digitorum longus 150-225* 50-75* M. flexor hallucis longus 60-120* 20-40* M. gastrocnemius med., lat 90-240 je Kopf* 30-80 je Kopf* M. gracilis 150-225* 50-75* M. iliopsoas 150-300* 50-100* M. rectus femoris 150-225* 50-75* M. semimembranosus 150-225* 50-75* M. semitendineus 150-225* 50-75* M. soleus 75-225* 25-75* M. tibialis posterior 75-225* 25-75* M. Vastus medialis, intermedius, lateralis 75-225 je Muskel* 25-75 je Muskel* Spastik und Extremitätendystonie – Untere Extremität [Wissel et al., 2012] BOTULINUMTOXIN BEI SPASTIK 51 7. Präparate & Dosierungen Dosierung der BoNT/A-Produkte/3 Indikation Abotulinumtoxin A (MU) Onabotulinumtoxin A (MU) 15-30 Units/kg KG bei pes equinus und Adduktorenspastik* 4 Units/kg KG bei single level, z.B. pes equinus 20-30 Units/kg KG bei Multilevelansatz* M. levator scapulae 60-225 20-75 M. scalenus anterior, medius, posterior 60-90 je Muskel 20-30 je Muskel M. semispinalis capitis 60-150 20-50 M. splenius capitis 60-300 20-100 M. sternocleidomastoideus 60-150 20-50 M. trapezius, pars ascendens 60-225 20-75 30-180 je Auge 10-60 je Auge M. masseter 30-150* 10-50* M. temporalis 30-150* 10-50* Spastik bei infantiler Zerebralparese Zervikale Dystonie Blepharospasmus M. orbicularis oculi Kieferschlussdystonie [Wissel et al., 2012] BOTULINUMTOXIN BEI SPASTIK 52 7. Präparate & Dosierungen Dosierung der BoNT/A-Produkte/4 Indikation Abotulinumtoxin A (MU) Onabotulinumtoxin A (MU) M. pterygoideus lateralis 15-75* 5-25* M. digastricus, venter anterior 15-60* 5-20* Mm. vocalis/arytenoideus 0.75-7.5* 0.25-2.5* M. crioarytaenoideus posterior 3.75-13.5* 1.25-4.5* M. orbicularis oculi 15-150 5-50 Platysma 15-90 5-30 M. mentalis 7.5-15 2.5-5 M. splenius capitis 60-150* 20-50* M. semispinalis capitis 60-150* 20-50* M. flexor carpi radialis 30-120* 10-40* M. flexor carpi ulnaris 30-90* 10-30* M. extensor carpi radialis 30-60* 10-20* M. extensor carpi ulnaris 30-60* 10-20* Kieferöffnungsdystonie Spasmodische Dysphonie Hemifazialer Spasmus Essenzieller Tremor [Wissel et al., 2012] BOTULINUMTOXIN BEI SPASTIK 53 7. Präparate & Dosierungen Dosierung der BoNT/A-Produkte/5 Indikation Abotulinumtoxin A (MU) Onabotulinumtoxin A (MU) Axilla 90-225* 30-75 Planta palmae 90-150* 30-50* Glandula parotis 30-90* 10-30* Glandula submandibularis 30-90* 10-30* 250-500* 100-300* 150-350* 100-150* Hyperhidrose Sialorrhö Neurogen überaktive Blase Detrusor vesicae Detrusor-Sphinkter Dyssynergie Sphinkter vesicae Chronische Migräne Hals- und Kopfmuskeln gesamt 155-195 *Off-Label-Use (Stand August 2011) [Wissel et al., 2012] BOTULINUMTOXIN BEI SPASTIK 54 Inhalt 1. Definition, Ursache und Klinik Seite 06 2. Epidemiologie der Spastik 13 3. Therapieoptionen 17 4. Botulismus 27 5. Wirkungsmechanismus Botulinumtoxin 32 6. Zulassung und Indikationen 39 7. Präparate & Dosierungen 45 8. Definition des Behandlungsziels 56 9. Weitere praxisrelevante Aspekte der Therapie 63 10. Nachsorge 71 11. Sicherheit 75 12. Referenzen 77 BOTULINUMTOXIN BEI SPASTIK 55 8. Definition des Behandlungsziels Formulierung des Behandlungsziels - Empfehlungen zur Dokumentation/1 Vor einer BoNT-A-Therapie sollte eine standardisierte Evaluation in den Ebenen der ICF erfolgen und auf dieser Basis realistische Behandlungsziele formuliert werden. [Turner-Stokes & Ward, 2002] Erfassung des Muskeltonus (Spastizität) und der Gelenkbeweglichkeit: Quantitative Beurteilung des Muskeltonus mittels der Ashworth- [AS] oder der mod. Ashworth-Skala [MAS] oder der Resistance to Passive Movement Skala [REPAS] [Bohannon & Smith 1987; Brashear et al. 2002; Platz et al. 2008] Quantitative Beurteilung der Gelenkbeweglichkeit: Range of Motion (passive und aktive ROM) BOTULINUMTOXIN BEI SPASTIK 56 8. Definition des Behandlungsziels Formulierung des Behandlungsziels - Empfehlungen zur Dokumentation/2 Schmerz und Mobilität Quantitative Beurteilung des Schmerzes: Visuelle Analogskala (VAS) oder 11-Point-Box-Skala (11PB) [Jensen et al., 1998] Quantitative Beurteilung der Mobilität mit und ohne Hilfsmitel: Functional Ambulation Classification (FAC); Esslinger Transfer-Skala (ETS); 10Meter-Test (Zeit/ Schritte); 3- bzw. 6-Minuten-Gehstrecke; Timed-Up-And-Go-Test (TUG) [Holden et al., 1984; Podsiadlo et al., 1991; Runge et al., 2001] BOTULINUMTOXIN BEI SPASTIK 57 8. Definition des Behandlungsziels Formulierung des Behandlungsziels - Empfehlungen zur Dokumentation/3 Erfassung „passiver Funktionen“ und der Pflegefähigkeit Semiquantitative Erfassung „passiver Funktionen“ mittels der Disability Assessment Skala (DAS) Semiquantitative Pflegeskalen: Handhygiene oder Intimhygieneskala, Caregiver Burden Fragebögen BOTULINUMTOXIN BEI SPASTIK 58 8. Definition des Behandlungsziels Formulierung des Behandlungsziels - Empfehlungen zur Dokumentation/4 Erfassung der Handfunktion und der Zielerreichung Standardisierte Handfunktionstests (Box-Block-Test [B&BT], Action Research Arm Test [ARAT], Nine-Hole-Peg-Test [NHP], Jebsen-Taylor Test [JTT ], Upper extremity performance test for the elderly [TEMPA] Mindestens ein klinisch & zeitlich definiertes Ziel mit dem Patienten/ Pflegenden formulieren, das dem Behandler realistisch erscheint: Geeignete Skala zur Abbildung von Individualzielen ist die Goal Attainment Skala (GAS) [Bakheit et al., 2004; Ashford & Turner-Stokes, 2006] BOTULINUMTOXIN BEI SPASTIK 59 8. Definition des Behandlungsziels Beispiel: Spastik nach Schlaganfall 126 Patienten bei Z.n. Schlaganfall und Spastizität mit fokaler Behinderung: Wahl des primären Interventionsziel: Vereinbarung vor BoNT/A Behandlung [Brashear et al., 2002] BOTULINUMTOXIN BEI SPASTIK 60 8. Definition des Behandlungsziels Goal Attainment Scale Zieldefinition mit der Zielerreichungsskala Goal Attainment Scale = GAS Die individuellen Ziele sollen SMART sein: S pezifisch (für den Patienten spezifisch sein) M essbar (beurteilbare messbare Ziele abbilden) A ngemessen (i.S. von erreichbar und realistisch sein) R essource sensitive (mit den Ressourcen erreichbar sein) T imed (im angemessenen Zeitraum erreichbar sein) • • • • Das Individual-Ziel wird mit einer validen & reliablen Methode erfasst. Gute Korrelation mit Standardverfahren (z.B. Barthel Index, MMSE) Gute Inter-Rater Reliabilität und hohe Sensitivität für Änderungen Messung auf dem Aktivitätsniveau (nicht auf der Funktionsebene) [Wissel et al., 2011] BOTULINUMTOXIN BEI SPASTIK 61 Inhalt 1. Definition, Ursache und Klinik Seite 06 2. Epidemiologie der Spastik 13 3. Therapieoptionen 17 4. Botulismus 27 5. Wirkungsmechanismus Botulinumtoxin 32 6. Zulassung und Indikationen 39 7. Präparate & Dosierungen 45 8. Definition des Behandlungsziels 56 9. Weitere praxisrelevante Aspekte der Therapie 63 10. Nachsorge 71 11. Sicherheit 75 12. Referenzen 77 BOTULINUMTOXIN BEI SPASTIK 62 9. Weitere relevante Aspekte der Therapie Injektionspunkte obere Extremität/1 [Abb. in Anlehnung an «Anatomic Guide for Electromyographer»] BOTULINUMTOXIN BEI SPASTIK 63 9. Weitere relevante Aspekte der Therapie Injektionspunkte obere Extremität/2 [Abb. in Anlehnung an «Anatomic Guide for Electromyographer»] BOTULINUMTOXIN BEI SPASTIK 64 9. Weitere relevante Aspekte der Therapie Injektionspunkte untere Extremität [Abb. in Anlehnung an «Anatomic Guide for Electromyographer»] BOTULINUMTOXIN BEI SPASTIK 65 9. Weitere relevante Aspekte der Therapie Methoden für kontrollierte BoNT Injektionen Anatomisch • Anatomische Landmarken, Inspektion & Palpation • Nadelbewegung während der Bewegung des Gelenkes Neurophysiologie • EMG • Elektrische Muskelstimulation Bildgebung • Röntgen • CT / MRI • Sonographie BOTULINUMTOXIN BEI SPASTIK 66 9. Weitere relevante Aspekte der Therapie Muskelauswahl, Dosierung und Injektion Injektionsmethoden M. pronator teres M. flexor carpi radialis Anatomische Lokalisation, Elektromyographie, Elektrostimulation, Bildgebung (Sonographie, CT, MRT) [Wissel, Fheodoroff & Huber, 2002] BOTULINUMTOXIN BEI SPASTIK 67 9. Weitere relevante Aspekte der Therapie Muskelauswahl, Dosierung und Injektion Sonographische Injektionskontrolle: Unterarm [Wissel, Fheodoroff & Huber, 2002] BOTULINUMTOXIN BEI SPASTIK 68 9. Weitere relevante Aspekte der Therapie BoNT/A Behandlung – Injektionsvolumen und Injektionstechnik • Verdünnung: 1–5 ml NaCl 0,9% / Viole (bei funktionellem Ziel, kleinen Muskeln / einzelnen Faszikeln: kleinere Volumina) • Endplattenregion bekannt: Gezielte Injektionen empfohlen (soweit es der Patientenkomfort zulässt) • Muskeln mit diffuser / unbekannter Endplattenverteilung: Höhere Anzahl von Injektionsstellen und größere Volumina empfohlen [Gracies et al., 2009] • Injektionen nach klinischen Kriterien nicht ausreichend genau [Chin & Graham, 2003] • EMG-kontrollierte Injektionen: Kein Nachweis einer besseren Lokalisationsgüte bei Spastizität. • Empfohlene Techniken: Repetitive elektrische Stimulation oder Muskelsonographie • Muskelsonographie wird als Referenzmethode diskutiert [Berweck & Heinen, 2004, Molloy et al., 2002] BOTULINUMTOXIN BEI SPASTIK 69 Inhalt 1. Definition, Ursache und Klinik Seite 06 2. Epidemiologie der Spastik 13 3. Therapieoptionen 17 4. Botulismus 27 5. Wirkungsmechanismus Botulinumtoxin 32 6. Zulassung und Indikationen 39 7. Präparate & Dosierungen 45 8. Definition des Behandlungsziels 56 9. Weitere praxisrelevante Aspekte der Therapie 63 10. Nachsorge 71 11. Sicherheit 75 12. Referenzen 77 BOTULINUMTOXIN BEI SPASTIK 70 10. Nachsorge Regelmässige Konsultationen MMAS (Modified Modified Ashworth Scale) GAS (Goal Attainment Scale) • Macht Schluss mit dem 1+ Rating (Hauptgrund von Irrtümern und Uneinstimmigkeit) • Misst die Erreichbarkeit individueller Behandlungsziele • Patient und Therapieteam legen 2 persönliche Zielsetzungen/ Aktivitäten fest • Sehr gute Inter-rater reliability (Vergleichbarkeit) • Klare Definitionen für Anwender, leicht in der Anwendung • Messung basierend auf einer 5 Punkte Skala in festgelegten Zeitabständen [Mc Crory et al., 2009] [Ansari et al., 2009] BOTULINUMTOXIN BEI SPASTIK 71 10. Nachsorge Evaluation bei nicht erreichtem Therapieziel • War die Muskelauswahl angemessen? • Wurden die Muskeln getroffen? • War die Dosierung ausreichend? • Standen bindegewebig fixierte Bewegungssegmente der Zielerreichung im Weg? • Waren die Behandlungsziele unrealistisch? • Liegen BoNT-Antikörper vor? [Wissel und Kempf, 2012] BOTULINUMTOXIN BEI SPASTIK 72 10. Nachsorge Post-stroke Spastikbehandlung – Nachsorge • Ambulante Patienten nach Stroke alle 3 Monate im Follow up beurteilen PSS relevant? • Einfache Untersuchungsprotokolle und standardisierte Dokumentation verwenden [Brashear et al., 2003] • Videodokumentation! • Spastikuntersuchung unter Ruhebedingungen ist nicht geeignete Basis für Therapieplanung mit BoNT. • Botulinumtoxin-Therapie sollte zunächst beginnen mit der Abschwächung assoziierter Spastikmuster an der OE¹¹ [Ward et al., 2005] • Laufende Nachanpassung des Injektionsprotokolls nach funktionellem Verlauf BOTULINUMTOXIN BEI SPASTIK 73 Inhalt 1. Definition, Ursache und Klinik Seite 06 2. Epidemiologie der Spastik 13 3. Therapieoptionen 17 4. Botulismus 27 5. Wirkungsmechanismus Botulinumtoxin 32 6. Zulassung und Indikationen 39 7. Präparate & Dosierungen 45 8. Definition des Behandlungsziels 56 9. Weitere praxisrelevante Aspekte der Therapie 63 10. Nachsorge 71 11. Sicherheit 75 12. Referenzen 77 BOTULINUMTOXIN BEI SPASTIK 74 11. Sicherheit Sicherheit der BoNT/A Behandlung • Die hohe Sicherheit von BoNT/A konnte in Meta-Analyse (37 kontrollierte klinische Studien) und im Langzeitverlauf nachgewiesen werden. [Naumann & Jankovic, 2004; Mejia et al., 2005] • In kontrollierten Studien keine BoNT/A-assoziierten Todesfälle • In großen kontrollierten Studien sowie Meta-Analyse keine signifikanten unterschiedlichen Häufigkeiten von Nebenwirkungen im Vergleich zu Placebo und bislang keine produktspezifisch erhöhten Nebenwirkungsraten nachzuweisen [Rosales und Chua-Yap, 2008] • Inzidenz neutralisierender AK gegen BoNT/A: Sehr niedrige Raten [Yablon et al., 2007; Muller et al., 2009] • Mindestabstand zweier BoNT/A-Behandlungen: 3 Monate weiterhin zu empfehlen [Dressler, 2004] BOTULINUMTOXIN BEI SPASTIK 75 Inhalt 1. Definition, Ursache und Klinik Seite 06 2. Epidemiologie der Spastik 13 3. Therapieoptionen 17 4. Botulismus 27 5. Wirkungsmechanismus Botulinumtoxin 32 6. Zulassung und Indikationen 39 7. Präparate & Dosierungen 45 8. Definition des Behandlungsziels 56 9. Weitere praxisrelevante Aspekte der Therapie 63 10. Nachsorge 71 11. Sicherheit 75 12. Referenzen 77 BOTULINUMTOXIN BEI SPASTIK 76 12. Referenzen Referenzen Arzneimittelkompendium der Schweiz 2011 (www.documed.ch) Dressler et al., 2000 Anatomic Guide for the Electromyographer“ Delagi, Perrotto et al., 1975 und 1980 by Charles C Thomas Publisher (Springfield , Illinois, USA), ISBN 0-398-03951-8 Dressler et al., 2003 Dressler et al., 2004 Ashford & Turner-Stokes, 2006 Durham et al. Regulation of calcitonin gene-related peptide secretion from trigeminal nerve cells by botulinum toxin type A: implications for migraine therapy. Headache 2004; 44: 35-42. Bakhai 2004 Elan SPC Bakheit et al., 2004 Frasson Emma et al., Mov Disorder 2005 May; 20 (5): 624-29 Nerv stimultation boosts Botulinum Toxin Action in spasticity Ansari NN.et al. NeuroRehabilitation.2009; 24(3): 225-229 Berweck & Heinen, 2004 Gracies et al., 2009 Bohannon RW, Smith MB: ROM, Range of Movements Physical Therapy 1987; 67:206-207 Holden et al., 1984 Brashear et al. 2002 Jensen et al., 1998 Brashear Allison :Use of botulinum toxin type A in posttroke spasticity Expert Review of Neurotherapeutics, May 2003, Vol.3, No 3 Pages 271-277 Kolominsky-Rabas et al., 1998 Leathley MJ. et al., Clin Rehabil.2004;18(4):438-443 Lundström E. et al., Eur.J Neurol.2008; 15(6):533-39 Chin & Graham, 2003 Mc Crory P. et al., J.Rehabil Med.2009;41(7)536-544 Cui et al., Subcutaneous administration of botulinum toxin A reduces formalin-induced pain. Pain 2004; 107: 125-133. Mejia et al., 2005 Dickerson JT, Janda KD. The Use of Small Molecules to Investigate Molecular Mechanism and Therapeutic Targets for Treatment of Botulinum Neurotoxin A Intoxication. ACS Chem Biol 2006; 1(6):359359. Molloy et al., 2002 Dietz V, Sinkjaer T. Spastic movement disorder: impaired reflex function and altered muscle mechanics. Lancet Neurol 2007;6:725– 733. Naumann et al., 2003 BOTULINUMTOXIN BEI SPASTIK Muller et al., 2009] Nakayama H. et al., Arch Phys Med Rehabil. 1994:75 (4): 394-398 Naumann & Jankovic, 2004 77 12. Referenzen Referenzen Parker VM et al., Int.Rehabil.Med.1986:8(8): 69- 73 Wissel et al., 2010 Patrick Emily et al., School of Physiotherapy, The University of Sydney, Sydney, Australia, The Tardieu Scale differentiates contracture from spasticity whereas the Ashworth Scale is confounded by it; Clin Rehabil February 2006 vol. 20 no. 2 173-182 Wissel et al., 2011 Wissel und Kempf, 2012 Yablon et al., 2007 Platz et al. 2008 Podsiadlo et al., 1991 Runge et al., 2001 Sommerfeld et al., 2004 www.stroke.org/site/DocServer Perceptions-FinalSurveyResults-2006 Turner-Stokes & Ward, 2002 Wade 1992 Ward A. et al., Cost-effectiveness of botulinum toxin type a in the treatment of post-stroke spasticity. J Rehabil Med 2005;37:252–257 Watkins CL. et al., Clin Rehabil. 2002;16(5):515-522 Welch et al. Sensitivity of embryonic rat dorsal root ganglia neurons to Clostridium botulinum neurotoxins. Toxicon 2000; 38: 245-258. Wissel, Fheodoroff & Huber, 2002 Wissel J, Benecke R, Erbguth F, Heinen F, Jost WH, Naumann M, et al. Konsensus-Statement zur fokalen Behandlung der Spastizität mit Botulinumtoxin. Neurol Rehabil 2003;9:242– 243. Wissel Jörg et al., J Rehabil Med 2009; 41: 13-25 European Consensus table on the use of Botulinum Toxin Type A in adult Spasticity BOTULINUMTOXIN BEI SPASTIK 78