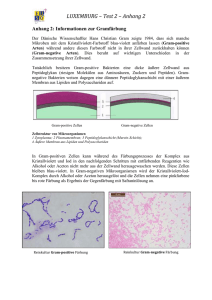
Basallamina
Werbung

Zell-Adhäsion & Extrazelluläre Matrix Kapitel 19 1164 – 1202 Christian Knapp 2008 1 / 70 Extrazelluläre Matrix (ECM) Netz aus Proteinen und Polysacchariden außerhalb der Zellen kann Haupdeterminante der physikalischen Eigenschaften von Gewebe sein; z.B. Knochen, Haut, Knorpel, Glaskörper entwicklungsgeschichtlich älteste ECM ist die Basallamina 2 / 70 Drei Arten der zellbezogen Organisation der Basallamina 3 / 70 Basallamina (BL) „zweidimensionale“ Schicht hauptsächlich aus Glykoproteinen 40-120 nm dick kann Metabolismus, Wachstum, Differenzierung von Zellen beeinflussen manche Zelle leiten Apoptose ein, sofern kein Kontakt zur BL besteht = „Anchorage Dependence“ (gilt für die ECM allgemein) 4 / 70 Basallamina von Epithelzellen rasterelektronenmikroskopische Aufnahme 5 / 70 Zusammensetzung der BL gewebsspezfisch typische Komponenten in allen BL Glycoproteine: Laminin, Typ 4 Collagen, Nidogen Proteoglykan: Perlecan 6 / 70 Hauptbestandteile der extrazellulären Matrix im Vergleich Protein in grün Glycosaminoglycan in pink 7 / 70 Basallamina Anordnung und Bindungsverhältnisse der Komponenten 8 / 70 Laminin Das Verbindungsstück zwischen Integrinen und Basallamina 9 / 70 Laminin Organisator der BL über Disulfidbrücken verbundes Heterotrimer zahlreiche unterschiedliche Monomere (jeweils ca. 1500 AS) gewebsspezifische Kombinationen zahlreiche Bindungsdomänen für ECM-Komponenten und Rezeptoren (z.B. Integrine) 10 / 70 weitere BL-Komponenten Typ 4 Collagen gibt Zugfestigkeit Perlecan & Nidogen vernetzen BL-Komponenten bei Formen der Epidermolyse „Schmetterlingskrankheit“ sind BL-Komponenten defekt 11 / 70 Basallamina Anordnung und Bindungsverhältnisse der Komponenten 12 / 70 Neuromuscular Junction Die Basallamina lotst die Regeneration nach Zerstörung 13 / 70 Integrin dynamische Verbindung zwischen extrazellulärer Matrix und Cytoskelett 14 / 70 Integrine Zelloberflächenrezeptoren (neben Dystroglykan) für zahlreiche ECM-Komponenten oder Zelloberflächenproteine anderer Zellen (nicht nur für BL) nonkovalentes Dimer Monomere sind Transmembran-Glykoproteine unterschiedliche Alpha- & Beta-Ketten 24 Kombinationen im Menschen nachgewiesen 23 binden an Actinskelett, eines bindet an Keratin in Hemidesmosomen 15 / 70 Integrin Rezeptor und dynamischer Anker Aktivierung sowohl von Innen als auch von Außen möglich 16 / 70 Integrin kann somit mechanische Signale in beide Richtungen leiten Aktivitätszustände basieren auf einer Art allosterischer Regulation Talin-Bindungsstelle auf Beta-Kette wird bei Aktivierung/Entfaltung frei, Talin kann auch mit Alpha-Kette um Bindungsstelle konkurrieren 17 / 70 Signalpathway aktiviert Integrin Rezeptoren aktivieren Talin Talin aktiviert Integrin 18 / 70 Signalpathway aktiviert Integrin somit können auch molekular Signale in mechanische Umgewandelt werden oder umgekehrt Zelle kann Anhaftung schnell regulieren z.B. Blutplättchen bei der Gerinnung (Form der Gerinnungsstörung, wenn Integrin defekt) Leukozyten bei der Anhaftung an Blutgefäße (bei „leucocyt adhesion deficiency“ Integrin defekt) Lymphozyten bei der Bindung an APC 19 / 70 Lymphozyt bindet APC über Integrin erster Kontakt über Integrin Bindung von T-Zell-Rezeptor an MHC gibt Signal zur Stabilisierung von Integrin-ICAM-Bindung 20 / 70 Hemidesmosom verankert Epithelzellen in der Basallamina Achtung ! Keratinfilamente Defekt in einer der Komponenten führt zu Epidermolyse 21 / 70 Fokale Adhäsion Integrine haben schwache Affinität zu Liganden wird kompensiert hohe Konzentration von Integrinen Ansammlungen von Integrin-Actinskelett-Komplexen sind „focal adhesions“ für Verankerung in ECM bzw. Substraten mit Keratinskelett sind es Hemidesmosome für Verankerung von Epithelzellen in der BL 22 / 70 Fokale Adhäsion & Focal Adhesion Kinase FAK verringert die Bindung der Focal Adhesions 23 / 70 Focal Adhesion Kinase rekrutiert durch Talin phosphoryliert sich selbst, bietet Bindungsstellen für weitere Signalproteine Art der Umwandlung mechanischer in molekulare Signale Bindungen der Integrine an ECM werden verringert bzw. dynamischer Manche Krebszellen exprimieren vermehrt FAK, führt zu mehr Migration 24 / 70 manche Signale durch Integrine aufgenommen, werden nur lokal weitergeleitet z.B. für Actinpolymerisierung durch Rho-GTPasen Bsp.: während Wachstums eines Axons reagiert Spitze auf Attractants und Repellents in ECM, beeinflusst Wachstumsrichtung dementsprechend 25 / 70 Ausbreitungsabhängige Apoptose Zelle bindet mit Integrinen an Fibronectin auf Substrat nur wenn Bindungsstellen vorhanden und „verstreut“ sind leitet die Zelle die Apoptose nicht ein ist in vivo Schutzmechanismus 26 / 70 Extrazelluläre Matrix des Bindegewebes 27 / 70 Collagen und Fibroblasten der ECM im Rasterelektronenmikroskop andere Komponenten wurden Enzymatisch verdaut 28 / 70 Collagen und Fibroblasten der ECM die ECM wird hauptsächlich von Fibroblasten aufgebaut Knochen von Osteoplasten, Knorpel von Chondroblasten Grundsubstanz bilden Glycosaminoglykane (GAG), entweder frei als Hyaluronan oder gebunden als Proteoglykane gegen Druckbelastung eingelagert sind v.a. fibrilläre Proteine v.a. fibrillenbildendes Collagen Typ 1 gegen Zugbelastung 29 / 70 Hyaluronan bzw. Hyaluronsäure aus bis zu 25.000 Disacchariden zieht Kationen an, hochgradig hydratisiert faltet sich nicht kompakt, nimmt daher großes Volumen ein 30 / 70 Hyaluronan einziges Glucosaminoglycan ohne Sulfatgruppen und nicht an Protein gebunden besteht aus bis zu 25.000 Disacchariden zieht Kationen an, liegt hochgradig hydratisiert vor behindert Diffusion im allgemeinen nicht (gilt auch für Proteoglykane) wird durch Komplex in der Membran direkt aus Zelle heraussynthetisiert 31 / 70 Proteoglykane sind Proteine mit gebundenen GAG-Ketten sehr heterogen Kernprotein durch Ribosome ins ER synthetisiert, dort und im Golgi-Apparat werden GAG-Ketten angebaut, danach sekretiert GAG-Ketten aus Disacchariden aus Aminozucker und Glucuronsäure, tragen oft Sulfatgruppen ebenfalls negativ geladen, hochgrad hydratisiert 32 / 70 Proteoglykane im Vergleich und ein Glykoprotein Protein in grün Glycosaminoglycan in pink Decorin vermittelt Bildung von Collagenfibrillen, hat nur eine GAG-Kette 33 / 70 Aggrecan besteht aus ca. 130 GAGSulfat-Ketten das Core-Protein besteht aus ca. 3000 AS ist der Hauptbestandteil der ECM von Knorpel bildet mit Hyaluronan Aggregate 34 / 70 Aggrecan-Hyaluronan-Aggregate 100 Aggrecan-Moleküle binden 1 Molekül Hyaluronan nonkovalent Masse ca. 100 MDa (10^8 Da) Volumen entspricht Bakterium 35 / 70 Proteoglykane können Aktionsradius, Lebenszeit und Aktivität von Signalmolekülen/Proteasen etc. beeinflussen, durch Bindung oder Monomerisierung Bsp.: Chemokine werden an Blutgefäßwand immobilisiert, um Leukozyten anzulocken Proteoglykane wirken als Corezeptoren, indem sie Liganden binden und Rezeptoren präsentieren 36 / 70 Collagenfibrille eingebettet in Glycosaminoglykan Diffuses Netzwerk aus Proteoglykanen und Hyaluron dunkle Bereiche/Punkte sind Coreproteine 37 / 70 Collagen rund 25% der Proteinmasse in Säugern v.a. in Haut und Knochen fibrilläres Protein mit Seilstruktur lang und unflexibel zahlreiche Isoformen Gene enthalten zahlreiche repetitive Abschnitte Typ 1 Collagen am häufigsten 38 / 70 Struktur eines Collagen-Moleküls Triple-Helix aus jeweils 1000 Aminosäuren !keine Alpha-Helix! Jede 3. AS ist Glycin, da Rest ins Innere der Triplehelix ragt. Die anderen AS sind meistens Prolin und Hydroxyprolin. 39 / 70 Fibroblast umgeben von Collagenfasern Collagen wird u.a. von Fibroblasten in einem vergrößerten ER synthetisiert. 40 / 70 Synthese von Procollagen 41 / 70 von Procollagen zur Collagenfaser 42 / 70 Procollagen Pro-Alpha-Ketten werden einzeln mit Propeptiden synthetisiert. Durch Propeptide wird das Molekül löslich, außerdem leiten sie Modifikationen im ER/Golgi. Nach Sekretion werden Propeptide durch extrazelluläre proteolytische Enzyme abgespalten. Collagen wird dadurch unlöslich und lagert sich zu Fibrillen zusammen. inter- & intramolekulare Lysin-Crosslinks zwischen Ketten und Collagenen werden gebildet. Besonders viele Crosslinks in Achillessehne 43 / 70 Hydroxylierung von Prolin unter Mangel an Ascorbinsäure (Vitamin C) kann Prolin nicht hydroxyliert werden dadurch lagern sich Pro-Alpha-Ketten nicht stabil aneinander und werden noch in Zelle abgebaut. Also kein neues Collagen produziert. Collagen in ECM unterliegt jedoch Turnover. Körper verliert somit Collagen, die Haut wird fragil, Zähne werden locker. Vitamin C Mangelerkrankung heißt Skorbut 44 / 70 fibrillenbindendes Collagen vermittelt Fibrillenorganisation nonhelicale Bereiche knicken das Molekül 45 / 70 Organisation von Collagenfibrillen im Knochen und in der Haut 46 / 70 Ausrichtung der Fibrillen ist gewebsspezifisch Cytoskelett kann Ausrichtung der Fibrillen während Sekretion und in Membrantaschen regulieren andere ECM-Komponenten können gewisse Ausrichtungen unterstützen. oder durch „Ziehen“ im nachhinein 47 / 70 Fibroblasten reorganisieren Collagen-Gel Stücke embryonischen Gewebes auf Substrat mit Collagen-Gel kultiviert. Fibroblasten organisieren Collagen zu Collagenfasern Annahme: In vivo sekretieren Fibroblasten erst Collagen und reorganisieren es danach 48 / 70 Elastin-Fasern aus Elastin; sehr hydrophobes ca. 750 AS Protein, reich an Prolin und Glycin, hat einen „random coil“Bereich, der für Elastizität verantwortlich ist Collagen-ähnliche Synthese, Precursor ist hydrophiles Tropoelastin, wird nach Sekretion quervernetzt. 49 / 70 Elastin ist Hauptbestandteil der Aorta ca. 50% der Trockenmasse Während Entwicklung wird Elastin u.a. von Fibrillin organisiert. Defekt führt zu Marfan‘s Syndrom 50 / 70 Fibronectin Disulfidbrücken verbinden Dimer, unterschiedliche Monomere durch alternatives Splicing, Domänen binden unterschiedliche Liganden, Typ III Domäne mit RGD-Sequenz für Bindung an Integrin 51 / 70 Fibronectin Typ III Domäne unter Zugbelastung wird eine verborgene Binding-Site frei. Diese bindet darauf weitere Fibronectin-Moleküle. Es bilden sich kovalent verbundene FibronectinFibrillen, aber nur dort, wo gebraucht. 52 / 70 Fibronectin-Fibrillen an der Zelloberfläche Fibronectin liegt löslich als Monomer z.B. im Blut vor, oder als unlösliche Fibrillen an Zelloberflächen 53 / 70 RGD-Motiv Argenin-Glycin-Aspartat ist eine Peptidsequenz die durch einige Integrine gebunden wird. Fibronectin Typ 3 Domäne hat RGD-Motiv auch zahlreiche andere ECM-Proteine z.B. Gerinnungsfaktoren Substrate mit Peptiden mit RGD-Motiv können von Zellen gebunden werden 54 / 70 Abbau von extrazellulärer Matrix notwenig für Wachstum und Migration von Zellen sowie Remodellierung und Turnover Proteasen verdauen ECM-Proteine Metalloproteasen oder Serinproteasen manche Proteasen sind spezifisch z.B. Collagenasen, Gesamtgerüst wird nicht gefährdet unspezifische Proteasen müssen kontrolliert werden; 55 / 70 Kontrolle unspezifischer Proteasen viele unspezifische Proteasen werden als inaktive Precurser sekretiert, dann durch weitere AktivatorProteasen geschnitten und aktiviert z.B. Plasminogen ist Precursor von Plasmin Plasmin löst Thromben wird durch freie Plasminogen-Aktivatoren geschnitten, die lokal sekretiert werden 56 / 70 Kontrolle unspezifischer Proteasen Plasminogen kann auch durch rezeptorgebundene Aktivatoren aktiviert werden. z.B. von Axonen während des Wachstums oder Krebszellen 57 / 70 Kontrolle unspezifischer Proteasen weitere Möglichkeiten Sekretion von Inhibitoren, um ECM lokal zu schützen Eingrenzung des Wirkungsradius durch Verankerung in der Membran 58 / 70 Pflanzliche Zellwände ECM bei Pflanzen pflanzliche Zellen haben (im allgemeinen) eine starre Zellwand, sie migrieren nicht Zellen haben ihren Ursprung in Meristemen, während Wachstums ist Zellwand flexibel, die Primärwand danach wird verdickt und gehärtet, u.a. durch Einlagerung von Lignin, einem netzwerkartigen Polymer aus Phenolderivaten 59 / 70 Anordnung pflanzlicher Zellen und Zellwand dünne Zellwand, da noch im Wachstum 60 / 70 Die Zelle bestimmt ihre Form durch die Zellwand A. schützendes Trichom, einer einzelne Zelle B. Oberfläche eines Blatts, Zellen ineinander verhakt C. Xylem-Kanäle für Wassertransport 61 / 70 Zusammensetzung nach dem gleichen Grundprinzip wie tierische ECM hochgradig hydratisierte Grundsubstanz gegen Druckbelastungen: Pektin lange fibrilläre Komplexe gegen Zugbelastungen: Cellulose Pflanzliche Zellwände bestehen hauptsächlich aus Kohlenhydraten und enthalten keinen/kaum Stickstoff die Zellwand muss teilweise einem Turgordruck standhalten, der 10 Atmosphären (5x Reifendruck) entspricht 62 / 70 Pektin verzweigtes Polysaccharid hauptsächlich aus Galacturonsäure negativ geladen, zieht Kationen (Calcium) an, hochgradig hydratisiert in Marmelade ;) 63 / 70 Cellulose unverzweigtes Polysaccharid aus mehr als 500 Einheiten Glucose über Beta1-4 Verknüpfungen ca. 40 Moleküle Cellulose bilden über Wasserstoffbrücken Mikrofibrillen, die mehrere Mikrometer lang werden können 64 / 70 Primäre Zellwand Mikrofibrillen liegen schichtweise parallel, werden durch Glykane (verzweigte Polysaccharide) quervernetzt Fibrillen sind starr und unelastisch in Pektin eingelagert 65 / 70 5% Protein nach Trockenmasse für Turnover und Remodellierung der Zellwandkomponenten 66 / 70 Die Zellausdehnung wird von der Zellwand definiert Mikrofibrillen sind nicht dehnbar, können jedoch ihre Lage zueinander ändern 67 / 70 Die Zellausdehnung wird von der Zellwand definiert epidermale Wurzelzellen im Wachstum 68 / 70 Synthese von Cellulose Cellulose-Synthase ist in Membran eingelagert. Cellulose wird (wie Hyaluronan) direkt aus der Zelle heraussynthetisiert. Substrat ist UDP-Glucose direkt nach/während Synthese bilden sich Fibrillen selbständig 69 / 70 Modell zur Steuerung der Orientierung der Microfibrillen geordnete Synthese von Mikrofibrillen funktioniert auch ohne MTs, eine Reorientierung jedoch nicht. MTs wie Leitplanken 70 / 70