Präsentation ()
Werbung

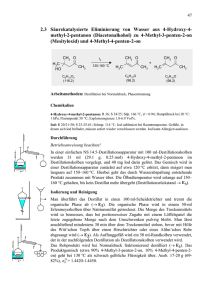
Aspirin „Medizin deines Lebens“ Experimentalvortrag zur Organik SS 2008 Angela Herrmann Gliederung 1. Einführung 2. Darstellung 3. Was gibt es für Aspirinsorten? 4. Schulrelevanz 2 1. Einführung 1. Einführung Kurze Geschichte des Aspirins: • Schon die Ägypter, Griechen und Germanen machten sich den Wirkstoff des Aspirins zu Nutzen. • Der Wirkstoff ist Salicylsäure und wurde aus den Rinden der Weide (lat.Salix) oder der Spirstaude gewonnen. • Vor etwa 100 Jahren entwickelte der Chemiker Felix Hoffmann die Darstellung von Acetylsalicylsäure. 4 1. Einführung Kurze Geschichte des Aspirins: • Bayer meldete 1899 das Patent für Aspirin an. • A steht für Acetyl und spir für Spirstaude, aus welcher früher Salicylsäure gewonnen wurde. • Jährlich werden etwa 50.000 Tonnen hergestellt. 5 1. Einführung Demo 1 pH-Wert-Vergleich 6 1. Einführung Demo 1 Auswertung: HO O O OH NH OH O CH3 CH3 O O Salicylsäure Aspirin HO Paracetamol 7 1. Einführung Wirkungsweise des Aspirins: Arachidonsäure hemmt Cox-1 & -2 Aspirin Prostaglandine Schmerz 8 2. Darstellung 2. Darstellung Versuch 1: Darstellung von Acetylsalicylsäure 10 2. Darstellung von Aspirin Versuch 1 Reaktionsgleichung: O O OH O O <H+> OH + H3C O CH3 OH O CH3 O + O H3C OH Die konzentrierte Schwefelsäure dient lediglich als Katalysator. 11 Reaktionsmechanismus 2. Darstellung O Versuch1 OH OH = O H3C OH H O O O CH3 O R + + H R + H C H3C O H3C CH3 O O - H+ CH3 O + HO O H O O H3C R H CH3 O O R 12 Fortsetzung 2. Darstellung O O H3C H Versuch 1 O + -H CH3 O H3C O O - + O CH3 + H+ O R R O O CH3 + H3C OH O R 13 2. Darstellung Versuch 2 Stärkenachweis 14 2. Darstellung Versuch 2 Auswertung: I2 (aq) + I-(aq) I I I I In- (aq) I braun Polyiodid lagert sich in die Stärkehelix ein und bildet einen blauvioletten ChargeTransfer-Komplex. 15 2. Darstellung Versuch 3 Haltbarkeit von Aspirin 16 2. Darstellung Versuch 3 Auswertung: • Die Veresterung ist eine reversible Reaktion • D.h. Aspirin zersetzt sich zu Salicylsäure und Essigsäure (die Essigsäure kann man auch riechen) O OH O O CH3 O OH O + H2O OH + H3C OH • Deshalb soll man die Tabletten kühl lagern und nach dem Verfallsdatum nicht mehr verwenden. 17 3. Aspirinsorten Versuch 3 • Salicylsäure bildet mit FeCl3 einen violetten Chelatkomplex und kann so nachgewiesen werden: O - HO O O O OH - Fe 3+ O - O HO 18 3. Aspirinsorten 3. Aspirinsorten Aspirinproduktpalette: 20 3. Aspirinsorten Demo 2: Aspirin Protect 21 3. Aspirinsorten Aspirin Migräne: • Für Migränepatienten • Brausetablette (enthält NaHCO3) • Enthält Pufferstoffe (Natriumhydrogencitrat/Citronensäure) 22 3. Aspirinsorten Aspirin Direkt/Effekt: • Kautablette/Granulat – ohne Wasser einnehmbar • Enthält Aromastoffe für besseren Geschmack. • Enthält Pufferstoffe zur verbesserten Löslichkeit von Acetylsalicylsäure. 23 3. Aspirinsorten Versuch 4: Aspirin Plus C 24 3. Aspirinsorten Versuch 4 Auswertung: Tillmanns Reagenz: (2,6-Dichlorphenolindophenol) Protonierte Form: (+ 2 H+) Cl N blau - + O Na O Cl Cl N rosa + C HO OH Cl 25 3. Aspirinsorten Versuch 4 Reduzierte Form: Cl NH farblos HO OH Cl Oxidation von Vitamin C: HO O HO HO HO O OH - 2 e-; -2 H+ O O HO O O 26 3. Aspirinsorten Aspirin Plus C: • Stärkt zusätzlich das Immunsystem • Brausetablette • Wirkstoff gelangt schneller in die Blutbahn, da er schon im Glas gelöst wird. 27 3. Aspirinsorten Aspirin Complex: • Enthält neben Acetylsalicylsäure noch Pseudoephedrin: OH CH3 HN CH3 • Gegen Erkältung • Bewirkt ein Abschwellen der Nasenschleimhaut. 28 3. Aspirinsorten Versuch 5: Aspirin Forte 29 3. Aspirinsorten Versuch 5 Auswertung: Coffein wird zunächst durch Oxidation der Methylgruppen zu Xanthin umgesetzt: O H3C O O CH3 H N N + N CH3 N N N H2O 2 O H + N 3 CO 2 + H2O N H Xanthin 30 3. Aspirinsorten Versuch 5 Xanthin wird unter Säurekatalyse hydrolisiert: O HN O O H N N H NH H2O O O H NH H HN N H O NH2 O O N H NH H NH H2O; H+ H HN <H+> N O H HN -NH4+ O O N H O 31 3. Aspirinsorten Versuch 5 Nun findet erneut eine Oxidation mit anschließender Hydrolyse statt und es entsteht Aloxan: O H O NH H HN O O N H O H2O2 H HN - H2O; -CO2 O N H NH2 H2O2 O - 2 H2O Uramil O O NH HN O N H O + H2O; H+ - NH4+ O HN O N H O Aloxan 32 3. Aspirinsorten Versuch 5 Aloxan und die Enol-Form des Uramils reagieren nun zur Purpursäure: O O O H2N HN O N NH HN + O N H O HO N H O - H2O O O NH N H O HO N H O Durch Zugabe von Ammoniak entsteht das Ammoniumsalz der Purpursäure: Murexid. O O O N HN O N H OH O N H N + NH3 NH O O HN O + NH4 NH N H - O O rotviolett N H O 33 3. Aspirinsorten Aspirin Forte: • Verstärkt und beschleunigt die Wirkung von Acetylsalicylsäure. • Coffein regt an 34 3. Aspirinsorten Demo 2: Aspirin Protect 35 3. Aspirinsorten Demo 2 Aspirin Protect: • Löst sich nicht im Magen (saures Milieu), • sondern erst im Dünndarm (basisches Milieu). • Schützt somit die Magenschleimhaut vor mechanischer Wirkung des Aspirins. 36 3. Aspirinsorten Demo 2 Aspirin Protect: • Enthält weniger Wirkstoff als eine herkömmliche Aspirintablette. • Eignet sich für Langzeiteinnahme. • Wird hauptsächlich zum Senken des Herzinfarkt- und Schlaganfallrisikos verwendet. 37 4. Schulrelevanz 4. Schulrelevanz Lehrplan (Hessen G8) • G11: Veresterung/Verseifung • G12: Großtechnische Chemie – Untersuchung und Wirkungsweise eines Arzneistoffes. • G12 (LK): Komplexchemie 39 Vielen Dank.
![6.3.1 1-Oxa-spiro[2.5]octan - Institut für Organische Chemie](http://s1.studylibde.com/store/data/001356875_1-96e669e5c88ad586db9f9f199d424d05-300x300.png)