Diagnose, Differenzialdiagnose und Therapie der Sarkoidose
Werbung

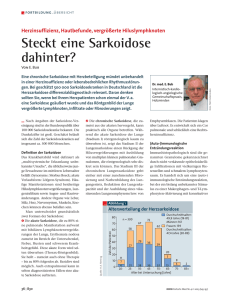
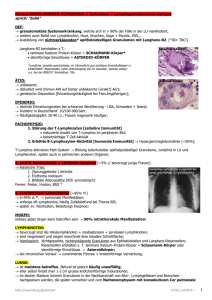
MEDIZIN Diagnose, Differenzialdiagnose und Therapie der Sarkoidose Antje Prasse ZUSAMMENFASSUNG Hintergrund: Die Sarkoidose ist eine granulomatöse Entzündung unklarer Ursache. Die Prävalenz beträgt in Deutschland etwa 46/100 000. Methode: Diese Arbeit basiert auf einer selektiven Literaturrecherche in PubMed. Ergebnisse: Von einer Sarkoidose wird dann ausgegangen, wenn keine anderen Ursachen, wie Infektionen oder Fremdkörper, die granulomatöse Entzündung erklären können. Histologisch werden epitheloidzellhaltige, nichtverkäsende Granulome nachgewiesen. Neue diagnostische Techniken, wie Positronenemmissionstomographie und Magnetresonanztomographie, bieten heute deutlich verbesserte Möglichkeiten zur Erfassung des Organbefalls und zur Einschätzung der Krankheitsaktivität. Das klinische Spektrum der Sarkoidose ist variabel und wird durch das individuell verschiedene Organbefallsmuster bestimmt. Häufig besteht eine systemische Entzündungsreaktion mit subfebrilen bis febrilen Temperaturen, Nachtschweiß, Gewichtsabnahme, Leistungsminderung und Müdigkeit. Die Spontanheilungsrate ist hoch. Der alleinige Nachweis eines Organbefalls stellt noch keine Therapieindikation dar. Hingegen besteht bei symptomatischem Herzbefall oder bei Beteiligung des Zentralnervensystems eine eindeutige Therapieindikation. Für die Erstlinientherapie werden orale Kortikosteroide eingesetzt, die jedoch als Dauertherapie nicht selten zu erheblichen Komorbiditäten führen. Schlussfolgerung: Die Versorgung von Patienten mit Sarkoidose, besonders der komplizierten Formen, erfordert eine enge Zusammenarbeit der Primärversorgung mit einem interdisziplinären, spezialisierten Zentrum. ►Zitierweise Prasse A: The diagnosis, differential diagnosis, and treatment of sarcoidosis. Dtsch Arztebl Int 2016; 113: 565–74. DOI: 10.3238/arztebl.2016.0565 Abteilung für Pneumologie, Medizinische Hochschule Hannover; Fraunhofer Institut für Toxikologie und Experimentelle Medizin (ITEM), Hannover; Deutsches Zentrum für Lungenforschung, DZL BREATH, Hannover: Prof. Dr. med. Prasse Deutsches Ärzteblatt | Jg. 113 | Heft 33–34 | 22. August 2016 D ie Sarkoidose ist eine häufige unter den seltenen Erkrankungen und kommt weltweit vor (1). Die Prävalenz der Sarkoidose liegt in Europa zwischen 1–64/100 000 (1). In Skandinavien tritt die Erkrankung öfters auf als in Südeuropa. Zwei deutsche Studien berichten übereinstimmend von einer Prävalenz von etwa 46/100 000 (2, 3). Die Sarkoidose kann in jedem Lebensalter auftreten. Es gibt einen Manifestationsgipfel im jungen Erwachsenenalter und einen zweiten, kleineren um das 60. Lebensjahr (4). Frauen erkranken statistisch häufiger als Männer (5). Vor allem im Frühjahr, seltener auch im Herbst, kommt es zu einer Häufung an Erstmanifestationen, insbesondere der akut auftretenden Form der Sarkoidose (4, e1). 3 Punkte cme Teilnahme nur im Internet möglich: aerzteblatt.de/cme Methodik Auf Basis wissenschaftlicher und klinischer Erfahrungen der Autorin wurde eine selektive Literaturrecherche ab 1960 in PubMed durchgeführt. Eingeschlossen wurden Reviews, randomisierte kontrollierte Studien, Registerstudien, fallkontrollierte Studien, Leitlinien und Fallberichte. Lernziele Die Leser des Beitrags sollen nach Lektüre des Beitrags wissen ● wie eine Sarkoidose richtig diagnostiziert wird ● wann man eine Organmanifestation der Sarkoidose behandelt ● welche Verlaufsparameter bei der Behandlung von Sarkoidosepatienten eingesetzt werden können und ● wie ihre Wertigkeit im Therapie-Monitoring ist. Definition und Differenzialdiagnose Die Sarkoidose ist eine granulomatöse Entzündung, die nicht durch eine andere Ursache, wie beispielsweise eine Infektion oder Fremdkörper, verursacht wird und stellt somit eine Ausschlussdiagnose dar (Grafik 1, Epidemiologie Die Prävalenz der Sarkoidose liegt in Europa zwischen 1–64/100 000. Es gibt einen Manifestationsgipfel im jungen Erwachsenenalter. 565 MEDIZIN Algorithmus zur Diagnosestellung einer Sarkoidose, modifiziert nach Baughman et al. (26). DD, Differenzialdiagnose GRAFIK suggestiver klinischer und radiologischer Befund Biopsie des betroffenen Organs/Lunge keine Granulome nicht-verkäsende riesenzellhaltige Granulomen keine Sarkoidose keine Sarkoidose Ausschluss anderweitiger Ursachen (Kasten 1) Screening auf Organbeteiligung nur 1 Organ betroffen mögliche Sarkoidose DD anderer Granulomatose mehr als 1 Organ betroffen Sarkoidose 566 Kasten 1) (6). Histologisch ist sie gekennzeichnet durch epitheloidzellhaltige, nicht-verkäsende Granulomen, die durch den Pathologen zumeist gut von anderen systemischen granulomatösen Veränderungen abgegrenzt werden können (6, 7). Problematisch ist die Abgrenzung gegenüber Mykobakteriosen, insbesondere den atypischen Mykobakteriosen, deren Granulome häufig nicht zentral einschmelzen, und bestimmten, in Deutschland jedoch seltenen Pilzerkrankungen, wie der Kokzidiose und der Histoplasmose (7). Bei vorwiegendem Befall des lymphatischen Systems ist eine wichtige Differenzialdiagnose die Katzenkratzkrankheit sowie die Toxoplasmose. Die zumeist im Rahmen einer Berufserkrankung auftretende chronische Berylliose und granulomatöse Veränderungen bei Immundefekten und Krebserkrankungen lassen sich über die Histologie gar nicht abgrenzen (6). Auch die Differenzialdiagnose gegenüber den sehr seltenen erblichen Erkrankungen, wie dem Blau-Syndrom, ist histologisch nicht möglich (e2). Medikamente können eine granulomatöse Entzündung analog zur Sarkoidose auslösen. Bei Gabe von rekombinantem Interferon (IFN)-α oder IFN-β kann eine Sarkoidose entstehen (8). In Einzelfällen wurde zudem berichtet, dass gegen Tumornekrosefaktor (TNF)-α gerichtete Antikörpertherapien eine granulomatöse Entzündung hervorrufen können (9). Dies ist insofern pa- radox, da Infliximab erfolgreich zur Behandlung der Sarkoidose eingesetzt wird und das Fehlen von TNF-α eigentlich den Aufbau von Granulomstrukturen erheblich behindert. Definition Die Sarkoidose ist eine granulomatöse Entzündung, die nicht durch eine andere Ursache, wie beispielsweise eine Infektion oder Fremdkörper, verursacht wird und stellt somit eine Ausschlussdiagnose dar. Pathogenese Die Ursache der Sarkoidose ist bisher ungeklärt. Aufgrund der Heterogenität der Erkrankung geht man davon aus, dass eine Vielzahl an verschiedenen Auslösern die Sarkoidose triggert. Pathogenese Die Ursache der Sarkoidose ist bisher ungeklärt (10). Aufgrund der Heterogenität der Erkrankung geht man davon aus, dass eine Vielzahl von verschiedenen Auslösern die Sarkoidose triggert. In 4 % der Fälle tritt die Sarkoidose familiär auf, und die genetische Veranlagung ist ein zentraler Faktor. So erkranken Schwarze häufiger und schwerer als Kaukasier in den USA, und Japaner zeigen Unterschiede in der Prävalenz an bestimmten Organmanifestationen im Vergleich zu Europäern (e3). Darüber hinaus sind Umwelteinflüsse bekannt. In Europa und Asien besteht ein deutliches Nord-Süd-Gefälle in der Prävalenz der Sarkoidose (e4). Klinik Die Klinik der Sarkoidose wird durch das jeweilige Organbefallsmuster getragen. Häufig besteht eine systemische Entzündungsreaktion, die mit subfebrilen bis febrilen Temperaturen, Nachtschweiß, Gewichtsabnahme, Leistungsminderung und Müdigkeit (Fatigue) einhergehen kann (11). Deutsches Ärzteblatt | Jg. 113 | Heft 33–34 | 22. August 2016 MEDIZIN Die Angaben über Organbefallshäufigkeiten schwanken von Studie zu Studie stark unter anderem aufgrund ethnischer Einflüsse und der Tatsache, dass der Organbefall häufig inapparent und in Abhängigkeit von den gewählten Untersuchungsmethoden mehr oder weniger leicht detektierbar ist (Tabelle) (12, 13). Meistens findet sich eine Sarkoidose mit Lungenmanifestation (4, e5). Eine Vielzahl von Studien belegen, dass das Lungenparenchym und die mediastinalen Lymphknoten in über 90 % aller Patienten betroffen sind. Relativ häufig ist auch der Befall der übrigen Lymphknotenstationen, der Leber und der Augen bei etwa 15–20 % aller Patienten (e6). Die Haut ist bei Kaukasiern in etwa 15 % der Fälle betroffen (4, 14). Aufgrund neuer Untersuchungstechniken (Magnetresonanztomographie [MRT]/18-Fluordeoxyglukose-Positronenemissionstomographie [18F FDG-PET]) ist der Nachweis von Herz- und muskuloskelettalen Manifestationen deutlich gestiegen (10–20 %) (15). Eine Herzbeteiligung wurde ohne diese neuen Techniken zuvor bei 2–7 % aller Patienten nachgewiesen, liegt jedoch in Autopsiestudien > 20 % (16). Eine Beteiligung des Zentralnervensystems tritt bei etwa 5–10 % der Patienten auf (17). Eine chronische Sinusitis besteht bei etwa 5 %. Besondere Organbefallskonstellationen Die Trias aus Sprunggelenksarthritis, mediastinaler Lymphadenopathie und Erythema nodosum wird als Löfgren-Syndrom bezeichnet. Der gleichzeitige Befall von Speicheldrüsen (Parotitis), Uveiitis, mediastinalen Lymphknoten und unter Umständen Facialisparese wird als Heerfordt-Syndrom bezeichnet (e7). Der Lupus pernio beschreibt den Gesichtshautbefall im Rahmen der Sarkoidose. Diagnostik Bildgebende Verfahren Die neuesten Entwicklungen im Bereich der Bildgebung, vor allem PET und MRT, führen zu einer deutlich verbesserten Detektion des Organbefalls durch die Sarkoidose (15, 18). Die verbesserte Detektion ist jedoch auch problematisch, weil der Nachweis eines Organbefalls noch keine Therapieoption darstellt und die Patienten dadurch oft erheblich verunsichert werden. Die Einordnung der klinischen Relevanz der bildgebenden Befunde wird für den behandelnden Arzt zunehmend komplexer. Insgesamt stehen zahlreiche bildgebende Verfahren zur Diagnostik zur Verfügung. Ein Lungenbefall ist in der einfachen Röntgenübersicht bereits gut Lungenbeteiligung Eine Vielzahl von Studien belegen, dass das Lungenparenchym und die mediastinalen Lymphknoten in über 90 % aller Patienten betroffen sind. Nur sehr selten findet sich eine Sarkoidose ohne Lungenmanifestation. Deutsches Ärzteblatt | Jg. 113 | Heft 33–34 | 22. August 2016 KASTEN 1 Differenzialdiagnose bei Systemerkrankung mit Nachweis epitheloidzellhaltiger Granulome ● Tuberkulose (Infektion mit M. tuberculosis) ● atypische Mykobakteriosen ● Pilzinfektionen, Histoplasmose, Kokzidiose ● Infektion mit Bartonellen, Toxoplasmose, Brucellen ● Sarkoidose-ähnliche Läsionen bei Krebserkrankungen ● Sarkoidose-ähnliche Läsionen bei Immundefekten ● Sarkoidose-ähnliche Läsionen, die mit Medikamenten assoziiert sind ● Hartmetall-assoziierte Granulomatose ● chronische Berylliose ● systemische Vaskulitiden ● rein pulmonal: exogen allergische Alveolitis, Silikose darstellbar. Die Abdominalorgane und oberflächliche Lymphknotenstationen lassen sich mit dem Ultraschall beurteilen. In der hochauflösenden Computertomographie (HRCT) lässt sich der Lungenparenchymbefall und die mediastinale Lymphadenopathie optimal jedoch mit entsprechender Strahlenbelastung aufzeigen (e8). Oft besteht eine erhebliche Diskrepanz zwischen radiologisch nachgewiesenem Befallsausmaß und fehlender beziehungsweise nur geringer Beeinträchtigung der Lungenfunktion, insbesondere bei feinnodulärem Verschattungsmuster (19, e9). Ein Befall des Herzens und des Zentralnervensystems lassen sich mit Hilfe der MRT nachweisen und im Verlauf kontrollieren (20, e10). Zur Suche nach Organbeteiligungen kann die GanzkörperMRT herangezogen werden (21). Diese wird jedoch nur an wenigen Zentren angeboten. Eine weitere Option bei der Suche nach Organbeteiligungen ist das 18F-FDGPET (Abbildung 1) (e11–e13). Hiermit werden alle entzündlich-aktiven Organbeteiligungen sehr gut erfasst. Zur Beurteilung, ob eine Beteiligung des Herzens und des Zentralnervensystems vorliegt, bedarf es jedoch einer anderen Aufnahmestrategie und viel Erfahrung, da beide Organe hoch stoffwechselaktiv sind. Bioptische Sicherung Es besteht Konsensus, dass eine bioptische Sicherung der Sarkoidose bei Erstdiagnose anzustreben ist, da eine spätere Diagnosesicherung insbesondere unter Therapie häufig erschwert ist und eine etwaige Thera- Bildgebung Die neuesten Entwicklungen im Bereich der Bildgebung führen zu einer deutlich verbesserten Detektion des Organbefalls durch die Sarkoidose. 567 MEDIZIN TABELLE Unterschiedliche Manifestationsformen nach Organ geordnet Organe* Befunde Lunge (> 90 %) mediastinale Lymphadenopathie parenchymaler Befall (Alveolen/Interstitium), Lungenfibrose bronchialer Befall (etwa 10 %, dann häufig obstruktiv) pleuraler Befall (selten) pulmonale Hypertonie (bei Kaukasiern selten) Leber (etwa 15–20 %) Leberparenchymbefall nodulär, Zirrhose Gallengangsbefall, Cholestase, biliäre Zirrhose selten Gefäßbefall/Stenosierung durch Lymphknoten portale Hypertonie Haut (etwa 15 %) lokalisierter Hautbefall, meist papulös Lupus pernio (Gesichtshautbefall) Narbensarkoidose, zum Beispiel durch Tattoos Erythema nodosum (histologisch kein Granulom, unspezifisch) Erythema anulare Herz (etwa 2–5 %) Reizleitungssystem (häufig, Rechts-/Linksschenkelblock, AV-Blockierungen) Myokardbefall (Cave: ventrikuläre Tachykardien) Perikardbefall (selten) Niere (etwa 5 %) Nierensteine, postrenales Nierenversagen (Hyperkalzämie) interstitielle Nephritis zentrales Nervensystem (etwa 5 %) noduläre Läsionen Befall der Hypophyse (häufig mit Diabetes insipidus) Enzephalopathie Befall der Meningen peripheres Nervensystem (etwa 5 %) Facialisparese, anderweitige Hirnnervenausfälle Mononeuritis multiplex Polyradikulitis Polyneuropathien Auge (etwa 15–20 %) Tränendrüsenbefall granulomatöse Konjunktivitis anteriore Uveitis (Iridozyklitis, Trabekulitis mit Glaukom) intermediäre Uveitis posteriore Uveitis (Chorioiditis, Periphlebitis retinae) Optikusneuritis Orbitagranulome Knochen (etwa 1 %) noduläre Läsionen zystische Läsionen mit Gelenkbeteiligung (M. Jüngling) zentral nekrotisierende Herde in der Schädelkalotte (bei Kaukasiern sehr selten) Knochenmarkbefall * Die angegebenen Prozentangaben für die Organbeteiligungen sind einer Fallkontrollstudie aus den USA entnommen (26). 568 cherung. Aufgrund des sehr häufigen Lungenbefalls und des einfachen Zugangsweges über die Bronchoskopie erfolgt die bioptische Sicherung zumeist in der Lunge. Hierbei können sowohl die mediastinalen Lymphknoten mittels Ultraschall-gesteuerter Feinnadelpunktion (EBUS) als auch das Lungenparenchym mittels transbronchialer Biopsie (TBB) sehr gut erreicht werden (Abbildung 2) (e14–e16). Die Kombination beider Methoden erzielt die höchste diagnostische Trefferquote mit > 90 % (e16). Da die Bronchoskopie mit EBUS eine sehr komplikationsarme Untersuchungsmethode ist, die die mediastinalen Lymphknoten sehr gut erfasst, empfiehlt es sich, diese Methode beim Löfgren-Syndrom zur Diagnosesicherung einzusetzen (24, 25, e15–e17). Darüber hinaus sollte im Rahmen einer Bronchoskopie eine bronchoalveoläre Lavage (BAL) entnommen werden (25). Diese zeigt in der Differenzial- und Immunzytologie typischerweise eine CD4-Lymphozytose (25) und ermöglicht mikrobiologische Untersuchungen zum Ausschluss einer Infektion. Bei Punktion eines anderen Organs sollte nicht vergessen werden, natives Gewebematerial auch an die Mikrobiologie zu schicken. Trotz Einsatz von PCR-gestützten Verfahren ist nach wie vor Formalin-fixiertes Gewebe nur begrenzt zum Ausschluss einer floriden Infektion geeignet (22). Für alle in Frage kommenden Erreger ist die kulturelle Anzucht der Goldstandard (e18). Der Tine-Test oder die neueren auf IFN-Produktion (IGRA) gestützten Testverfahren schließen weder eine floride Tuberkulose mit 100 %iger Sicherheit aus noch erfassen sie atypische Mykobakteriosen (5). Organscreening Jedem klinischen Hinweis auf eine mögliche Organbeteiligung muss sorgfältig nachgegangen werden (Kasten 2). Bei Erstdiagnose sollte immer eine Abklärung von Lunge, Herz und Augen durch einen spezialisierten Facharzt erfolgen. Die meisten Organmanifestationen treten innerhalb von zwei Jahren nach Erstmanifestation auf, so dass insbesondere zu Beginn der Erkrankung ein jährliches Organscreening erfolgen sollte. pienotwendigkeit im weiteren Verlauf nicht abgeschätzt werden kann (22, 23). Die häufig eingesetzten Biomarker „Angiotensin-Converting Enzyme“ (ACE) und „soluble Interleukin-2-Rezeptor“ (sIL-2R) sind unspezifisch und eignen sich nicht zur Diagnosesi- Verlauf Bioptische Sicherung Aufgrund des sehr häufigen Lungenbefalls und des einfachen Zugangsweges über die Bronchoskopie erfolgt die bioptische Sicherung zumeist in der Lunge. Verlauf Die Prognose der Sarkoidose ist häufig gut. Die Spontanheilungsrate, insbesondere beim Löfgren-Syndrom und asymptomatischen Organbefall, ist sehr hoch (85 %). Die Prognose der Sarkoidose ist häufig gut. Die Spontanheilungsrate, insbesondere beim Löfgren-Syndrom und asymptomatischem Organbefall, ist sehr hoch (85 %). Generell treten die meisten Spontanheilungen in den ers- Deutsches Ärzteblatt | Jg. 113 | Heft 33–34 | 22. August 2016 MEDIZIN ten sechs Monaten nach Krankheitsbeginn auf (13, 26, 27). Empfohlen werden im ersten Jahr nach Diagnosestellung Verlaufskontrollen in 3 Monatsintervallen, bei gutem Verlauf ohne Therapieindikation in den nachfolgenden 3–5 Jahren jährlich (5, 26, 28). Bei etwa 10 % der Patienten kommt es zu einem progredienten Krankheitsverlauf trotz immunsuppressiver Therapie (5, 26, 27). Ein erhebliches Problem stellt im Langzeitverlauf die Komorbidität durch die Kortikosteroidtherapie dar. Häufig treten eine erhebliche Adipositas und in der Folge die Komplikationen eines metabolischen Syndroms auf (5, 29, e19). Die Mortalität ist bei Sarkoidose gering erhöht (1). Vor allem der Befall des Herzens und des zentralnervensystems können zum Tode führen (1). In Europa und den USA erfolgen aufgrund einer Sarkoidose etwa 3 % aller Lungentransplantationen (30, e20). Indikationen hierzu sind vor allem die aus der Sarkoidose entstehende Lungenfibrose, zystische Umwandlungen mit Mycetomen oder eine pulmonale Hypertonie (30, e21, e22). Ein nicht unerheblicher Anteil plötzlicher Herztode bei jungen Erwachsenen soll auf die Sarkoidose zurückgehen (16, e23, e24). Neben zerebralen Insulten infolge einer Beteiligung des Zentralnervensystems ist insbesondere die Ausbildung einer (sehr seltenen) Leukenzephalopathie gefürchtet und dann in der Regel tödlich (31, e25). KASTEN 2 Screening auf Organbefall ● Routine – – – – – – – körperliche Untersuchung Röntgenaufnahme des Thorax Lungenfunktion, Diffusionskapazität Sonographie des Abdomens Echokardiographie EKG, 24-h-EKG Messung der Calciumkonzentration im Urin und im Serum – Kreatinin und Harnstoff in Serum – GOT, GPT, AP, Gamma-GT ● optional – MRT bei Verdacht auf Befall des Zentralnervensystems – MRT bei Verdacht auf Muskelbefall – 18F FDG-PET bei Verdacht auf diffusen Knochenbefall/ oder zur Suche AP, Alkalische Phosphatase; 18F FDG-PET; 18-Fluordeoxyglukose-Positronenemissionstomographie; Gamma-GT; Gamma-Glutamyl-Transferase; GOT, Glutamat-Oxalacetat-Transaminase; GPT, Glutamat-PyruvatTransaminase; MRT, Magnetresonanztomographie Therapie Bei der Therapieentscheidung ist vor allem die hohe Rate an Spontanheilungen, das häufige Auftreten asymptomatischer Organbeteiligungen und die erheblichen Nebenwirkungen der Kortikosteroidtherapie zu berücksichtigen (5, 26). Unstrittig ist, dass höhergradige Herzrhythmusstörungen, Herzmuskelbeteiligung und ein ZNS-Befall eine klare Indikation zur Therapieeinleitung darstellen. Es besteht ein internationaler Konsensus, dass ansonsten nur symptomatische Organbeteiligungen, die potenziell in einer chronischen Schädigung des Organes münden, behandelt werden sollten (5, 12, 22, 28). Für die Lungensarkoidose wird zum Beispiel eine ausführliche Diagnostik mittels Lungenfunktion und Belastungstests (meist Ergometrie) einer Therapieentscheidung vorangestellt (5, 12). Nur bei signifikanter Einschränkung der Lungenfunktion sowie der Diffusionskapazität und hieraus resultierender Einschränkung der körperlichen Belastbarkeit wird eine Indikation zur Therapie gesehen. In Analogie erfolgt auch die Abklärung anderer Organfunktionen. Für die Leber wird eine Indikation zur Therapie gesehen, wenn die Transaminasen über das Dreifache der Norm erhöht sind (28). Nur sehr selten ist isoliert das biliäre System betroffen. In diesem Fall wird die alkalische Phosphatase (AP) als Leitenzym herangezogen. Hyperkalzämien treten häufig im Rahmen der Sarkoidose auf und beruhen auf einer vermehrten Produktion von aktivem Vitamin-D3 (Calcitriol) durch das Enzym 1-α-Hydroxylase, welches von Makrophagen in Granulomen gebildet wird (32). Hyperkalzämien, die sich nicht durch Meidung von Sonnenlicht und diätetische Maßnahmen normalisieren, stellen eine klare Therapieindikation dar. Aufgrund der Hyperkalzämieneigung sollte bei Sarkoidosepatienten keine Osteoporoseprophylaxe mittels Calcium- und Vitamin-D-Substitution erfolgen. Bei Nachweis einer Osteoporose wird zur primären Therapie mit Bisphosphonaten geraten (32). Eine Augenbeteiligung, die nicht durch lokale Immunsuppressiva-Therapie modulierbar ist, ist eine weitere häufige Therapieindikation (e6, e26). Mortalität Die Mortalität ist bei Sarkoidose gering erhöht. Vor allem der Befall des Herzens und des Zentralnervensystems können zum Tode führen. In Europa und den USA erfolgen aufgrund einer Sarkoidose etwa 3 % aller Lungentransplantationen. Indikationen für die Therapie sind • höhergradige Herzrhythmusstörungen, Herzmuskelbeteiligung und ein ZNS-Befall • symptomatische Organbeteiligungen, die potenziell in einer chronischen Schädigung des Organs münden. Deutsches Ärzteblatt | Jg. 113 | Heft 33–34 | 22. August 2016 569 MEDIZIN a b c d 18 Abbildung 1: F FDG-PET Befunde bei Multiorganbefall. a) Lungen- und Milzbefall; b) Diffuser Knochen- und Lymphknotenbefall; c) Ausgeprägter Lymphknoten- und Milzbefall. Zudem auch Knochenmark- und Leberbeteiligung. d) Ausgeprägter, diffuser Muskelbefall und geringer Lymphknoten- und Leberbefall. 570 Für die Sarkoidose wurde bisher keine Therapie durch die Europäische Aufsichtsbehörde zugelassen. Die Standardtherapie stellt die orale Kortikosteroidtherapie dar (29). Die Studienlage zur Kortikosteroidtherapie ist nach heutigen Gesichtspunkten jedoch unzureichend. Es existiert nur eine randomisierte, placebokontrollierte, multizentrische Studie aus Finnland, die eine orale Kortikosteroidtherapie über drei Monate gefolgt von 15 Monaten inhalativer Kortikosteroidtherapie bei Sarkoidosepatienten mit Röntgentyp I und II untersucht hat. Die Studie ergab eine signifikant bessere forcierte Vitalkapazität und einen gebesserten Röntgenbefund 5 Jahre nach Studienbeginn bei den Patienten, die mit Kortikosteroiden behandelt wurden (33). Die Durchführung weiterer multizentrischer, placebokontrollierter Studien zum Wirkungsnachweis der systemischen Kortikosteroidtherapie wird jedoch von allen Fachgesellschaften derzeit als unethisch abgelehnt. Bei erstmaligem Therapiebeginn wird eine Dosis Prednison von 0,5 mg pro kg Körpergewicht (KG) von den meisten Experten eingesetzt (28, 29). Eine Ausnahme stellt einzig die Neurosarkoidose dar, bei der höhere Dosen zur Überwindung der Blut-HirnSchranke angewendet werden (17). Von den aktuellen Leitlinien wird empfohlen, bei Indikation zur systemischen Kortikosteroidtherapie diese für mindestens 6 Monate einzusetzen und im Verlauf über 6 Monate die Dosis schrittweise auszuschleichen (28). Sollte es während der schrittweisen Reduktion oberhalb einer Erhaltungsdosis von 7,5 mg zu einer Reaktivierung kommen (27), ist der Einsatz einer immunsuppressiven Kombinationstherapie mittels Methotrexat oder Azathioprin zu überlegen (22, 27). Diese beiden Medikamente werden primär zur Zweitlinientherapie eingesetzt mit dem Ziel Kortikosteroide einzusparen. Eine vor kurzem publizierte Studie belegt, dass die immunsuppressive Wirkung von Methotrexat und Azathioprin als etwa gleich gut einzuschätzen ist (34). Auch diese Studie erfolgte jedoch weder kontrolliert noch verblindet und vergleicht lediglich retrospektiv erhobenene Daten zweier Zentren mit unterschiedlichen Therapiestrategien. Bei jungen Patienten ist der Einsatz von Azathioprin und Methotrexat jedoch problematisch, insbesondere wenn Kinderwunsch besteht. Hier sollte in jedem Fall eine ausführliche Aufklärung und Beratung vor dem Einsatz erfolgen. Neben der teratogenen Toxizität haben beide Medikamente, vor allem bei Langzeitgabe, das Risiko einer Knochenmarks- und Leberschädigung, weshalb ein regelmäßiges Monitoring des Differenzialblutbildes und der Transaminasen unter der Therapie erfolgen muss. Beide Medikamente können zudem gastrointestinale Ne- Standardtherapie Die Standardtherapie der Sarkoidose stellt die orale Kortikosteroidtherapie dar. Die Studienlage zur Kortikosteroidtherapie ist nach heutigen Gesichtspunkten unzureichend. Zweitlinientherapie Einsatz einer immunsuppressiven Kombinationstherapie mit Hilfe von Methotrexat oder Azathioprin. Diese beiden Medikamente werden primär zur Zweitlinientherapie eingesetzt mit dem Ziel Kortikosteroide einzusparen. Deutsches Ärzteblatt | Jg. 113 | Heft 33–34 | 22. August 2016 MEDIZIN b a c Abbildung 2: Zytologische und histologische Befunde bei Sarkoidose a) transbronchiale Biopsie der Lunge mit Nachweis von epitheloid- und riesenzellhaltigen, nicht verkäsenden Granulomen b) Nachweis eines Granuloms mit Hilfe der ultraschallgesteuerten Nadelbiopsie eines mediastinalen Lymphknotens c) Ausstrich einer bronchoalveolären Lavage (BAL): Typischerweise findet sich eine Vermehrung der CD4+-T-Lymphozyten (kleine, runde Zellen mit großem Kern und wenig Zytoplasma). Die übrigen Zellen sind überwiegend Alveolarmakrophagen mit einem großen Zytoplasmaanteil. benwirkungen hervorrufen. Teilweise verlaufen diese fulminant und treten unmittelbar nach Therapiebeginn auf. Sollten solche Unverträglichkeiten oder Kontraindikationen für Methotrexat und Azathioprin vorhanden sein, kann auch eine Kombinationstherapie mit Leflunomid oder Mycophenolat Mofetil erwogen werden (29, e19, e27), hierzu ist die Datenlage jedoch ebenfalls sehr unzureichend. Sollte trotz immunsuppressiver Therapiekombination ein Krankheitsprogress feststellbar und dieser auf eine vermehrte Entzündungsaktivität zurückzuführen sein, ist es internationaler Konsensus, eine Anti-TNF-α-Antikörpertherapie mit Infliximab oder Adalimumab zu erwägen (5, 26, e19). Studien zeigen, dass nur die Anti-TNF-α-Antikörpertherapien wirksam sind, die auch die membranständige Form des TNF-α blockieren. In einer doppelblinden, placebokontrollierten, multizentrischen klinischen Studie zur additiven Therapie mit Infliximab konnte eine signifikante Verbesserung der forcierten Vitalkapazität um 2,5 % nach 24 Wochen, im Vergleich zum Placeboarm jedoch keine Besserung der Lebensqualität gezeigt werden (35). Eindrücklich war die ebenfalls signifikante Verbesserung der Hautbeteiligung (falls vorhan- Anti-TNF-alpha-Antikörpertherapie Sollte trotz immunsuppressiver Therapiekombination ein Krankheitsprogress mit vermehrte Entzündungsaktivität feststellbar sein, ist eine Anti-TNF-alphaAntikörpertherapie mit Infliximab oder Adalimumab zu erwägen. Deutsches Ärzteblatt | Jg. 113 | Heft 33–34 | 22. August 2016 den) unter Infliximab in dieser Studie (e28). Fallserien und die eigene klinische Erfahrung der Autorin zeigen zudem eine sehr gute Wirksamkeit bei der Neurosarkoidose (35). Die Infliximabtherapie kann in einer Dosierung von 3 mg/kg/KG entweder in Kombination zu Prednison + Azathioprin/Methotrexat oder in einer Dosierung von 5mg/kg/KG in Kombination mit alleiniger Kortikosteroidgabe erfolgen. Meist handelt es sich um eine länger angelegte Therapie über 1 Jahr (36, 37). In Deutschland ist die Therapie mit Infliximab bei der Sarkoidose nicht zugelassen und stellt eine Off-label-Therapie dar. Auf Basis der ausgeführten Datenlage muss für jeden einzelnen Patienten ein Antrag bei der zuständigen Krankenkasse zur Kostenübernahme gestellt werden. Therapiemonitoring und Biomarker Vor Therapieeinleitung sollte ein Biomarker und eine dem Organbefall entsprechende Untersuchungsmethode für die Beurteilung eines etwaigen Therapieansprechens festgelegt und dokumentiert werden. Zahlreiche Biomarker werden zur Evaluation von Organfunktionen erfolgreich eingesetzt. Die entzündliche Aktivität der Sar- Biomarker Die entzündliche Aktivität der Sarkoidose wird gut durch den löslichen Interleukin-2-Rezeptor alpha (sIL-2R oder sCD25) sowie Neopterin erfasst, so dass diese zum Therapiemonitoring eingesetzt werden können. 571 MEDIZIN koidose wird gut durch den löslichen Interleukin-2-Rezeptor α (sIL-2R oder sCD25) sowie Neopterin erfasst, so dass diese zum Therapiemonitoring eingesetzt werden können (38). Jedoch variieren die Blutspiegel erheblich, je nach befallenem Organ. Bei Niereninsuffizienz sind die sIL-2R-Spiegel falsch hoch (e29). Fazit Die Sarkoidose ist eine seltene Erkrankung, die durch eine erhebliche Heterogenität geprägt ist. Eine initiale histologische Sicherung und der Ausschluss einer floriden Infektionserkrankung sowie anderer granulomatöser Prozesse ist bei der Diagnosestellung unabdingbar. Der Nachweis einer Sarkoidose stellt per se keine Notwendigkeit zur Therapie dar. Vielmehr empfiehlt es sich, basierend auf der Funktionsdiagnostik des jeweiligen betroffenen Organs, die Therapieindikation sorgfältig zu evaluieren und gegebenenfalls im Verlauf zu steuern. Zumeist spricht die Sarkoidose gut auf eine Kortikosteroid-Monotherapie an. In etwa 10 % der Fälle kommt es jedoch zu einem steroidrefraktären progredienten Krankheitsbild. Interessenkonflikt Prof. Prasse erhielt Honorare für die Durchführung von klinischen Auftragsstudien von Novartis. 9. Shin JI, Kim DS: Development of sarcoidosis during anti-TNF-alpha treatment: what is the mechanism? Clin Exp Rheumatol 2009; 27: 1054; author reply 5. 10. Moller DR: Potential etiologic agents in sarcoidosis. Proc Am Thorac Soc 2007; 4: 465–8. 11. Gvozdenovic BS, Mihailovic-Vucinic V, Ilic-Dudvarski A, Zugic V, Judson MA: Differences in symptom severity and health status impairment between patients with pulmonary and pulmonary plus extrapulmonary sarcoidosis. Respir Med 2008; 102: 1636–42. 12. Kirsten D: Lungensarkoidose: aktuelle Diagnostik und Therapie. Dtsch Med Wochenschr 2013; 138: 537–41. 13. Baughman RP, Teirstein AS, Judson MA, et al.: Clinical characteristics of patients in a case control study of sarcoidosis. Am J Respir Crit Care Med 2001; 164: 1885–9. 14. Wanat KA, Rosenbach M: Cutaneous sarcoidosis. Clin Chest Med 2015; 36: 685–702. 15. Lynch JP, 3rd, Hwang J, Bradfield J, Fishbein M, Shivkumar K, Tung R: Cardiac involvement in sarcoidosis: evolving concepts in diagnosis and treatment. Semin Respir Crit Care Med 2014; 35: 372–90. 16. Kandolin R, Lehtonen J, Airaksinen J, et al.: Cardiac sarcoidosis: epidemiology, characteristics, and outcome over 25 years in a nationwide study. Circulation 2015; 131: 624–32. 17. Segal BM: Neurosarcoidosis: diagnostic approaches and therapeutic strategies. Curr Opin Neurol 2013; 26: 307–13. Manuskriptdaten eingereicht: 21. 10. 2015, revidierte Fassung angenommen: 9. 5. 2016 18. Teirstein AS, Machac J, Almeida O, Lu P, Padilla ML, Iannuzzi MC: Results of 188 whole-body fluorodeoxyglucose positron emission tomography scans in 137 patients with sarcoidosis. Chest 2007; 132: 1949–53. LITERATUR 19. Koyama T, Ueda H, Togashi K, Umeoka S, Kataoka M, Nagai S: Radiologic manifestations of sarcoidosis in various organs. Radiographics 2004; 24: 87–104. 1. Gribbin J, Hubbard RB, Le Jeune I, Smith CJ, West J, Tata LJ: Incidence and mortality of idiopathic pulmonary fibrosis and sarcoidosis in the UK. Thorax 2006; 61: 980–5. 20. Aggarwal NR, Snipelisky D, Young PM, Gersh BJ, Cooper LT, Chareonthaitawee P: Advances in imaging for diagnosis and management of cardiac sarcoidosis. Eur Heart J Cardiovasc Imaging 2015; 16: 949–58. 2. Scharkoff T: Epidemiologie der Sarkoidose. Pneumologie 1993; 47: 588–92. 21. Hostettler KE, Bratu VA, Fischmann A, Tamm M, Studler U: Wholebody magnetic resonance imaging in extrathoracic sarcoidosis. Eur Respir J 2014; 43: 1812–5. 3. Pabst S, Skowasch D, Grohe C: Sarkoidose. Pneumologie 2012; 66: 96–109; quiz 10. 4. Loddenkemper R, Kloppenborg A, Schoenfeld N, Grosser H, Costabel U: Clinical findings in 715 patients with newly detected pulmonary sarcoidosis—results of a cooperative study in former West Germany and Switzerland. WATL Study Group. Wissenschaftliche Arbeitsgemeinschaft für die Therapie von Lungenkrankheiten. Sarcoidosis Vasc Diffuse Lung Dis 1998; 15: 178–82. 5. Valeyre D, Prasse A, Nunes H, Uzunhan Y, Brillet PY, Muller-Quernheim J: Sarcoidosis. Lancet 2014; 383: 1155–67. 6. Myers JL, Tazelaar HD: [Challenges in pulmonary fibrosis: 6–Problematic granulomatous lung disease]. Thorax 2008; 63: 78–84. 7. Rosen Y: Pathology of sarcoidosis. Semin Respir Crit Care Med 2007; 28: 36–52. 572 8. Buss G, Cattin V, Spring P, Malinverni R, Gilliet M: Two cases of interferon-alpha-induced sarcoidosis Koebnerized along venous drainage lines: new pathogenic insights and review of the literature of interferon-induced sarcoidosis. Dermatology 2013; 226: 289–97. 22. American Thoracic Society: Statement on sarcoidosis. Joint Statement of the American Thoracic Society (ATS), the European Respiratory Society (ERS) and the World Association of Sarcoidosis and Other Granulomatous Disorders (WASOG) adopted by the ATS Board of Directors and by the ERS Executive Committee, February 1999. Am J Respir Crit Care Med 1999; 160: 736–55. 23. Judson MA, Thompson BW, Rabin DL, et al.: The diagnostic pathway to sarcoidosis. Chest 2003; 123: 406–12. 24. Agarwal R, Srinivasan A, Aggarwal AN, Gupta D: Efficacy and safety of convex probe EBUS-TBNA in sarcoidosis: a systematic review and meta-analysis. Respir Med 2012; 106: 883–92. 25. Costabel U, Bonella F, Ohshimo S, Guzman J: Diagnostic modalities in sarcoidosis: BAL, EBUS, and PET. Semin Respir Crit Care Med 2010; 31: 404–8. Deutsches Ärzteblatt | Jg. 113 | Heft 33–34 | 22. August 2016 MEDIZIN 26. Baughman RP, Culver DA, Judson MA: A concise review of pulmonary sarcoidosis. Am J Respir Crit Care Med 2011; 183: 573–81. 27. Baughman RP, Judson MA: Relapses of sarcoidosis: what are they and can we predict who will get them? Eur Respir J 2014; 43: 337–9. 28. Judson MA: The treatment of pulmonary sarcoidosis. Respir Med 2012; 106: 1351–61. 29. Grutters JC, van den Bosch JM: Corticosteroid treatment in sarcoidosis. Eur Respir J 2006; 28: 627–36. 30. Taimeh Z, Hertz MI, Shumway S, Pritzker M: Lung transplantation for pulmonary sarcoidosis. Twenty-five years of experience in the USA. Thorax 2016; 71: 378–9. 31. Jamilloux Y, Néel A, Lecouffe-Desprets M, et al.: Progressive multifocal leukoencephalopathy in patients with sarcoidosis. Neurology 2014; 82: 1307–13. 32. Baughman RP, Janovcik J, Ray M, et al.: Calcium and vitamin D metabolism in sarcoidosis. Sarcoidosis Vasc Diffuse Lung Dis 2013; 30: 113–20. 33. Pietinalho A, Tukiainen P, Haahtela T, Persson T, Selroos O, Finnish Pulmonary Sarcoidosis Study Group: Early treatment of stage II sarcoidosis improves 5-year pulmonary function. Chest 2002; 121: 24–31. 34. Vorselaars AD, Wuyts WA, Vorselaars VM, et al.: Methotrexate vs azathioprine in second-line therapy of sarcoidosis. Chest 2013; 144: 805–12. 35. Baughman RP, Drent M, Kavuru M, et al.: Infliximab therapy in patients with chronic sarcoidosis and pulmonary involvement. Am J Respir Crit Care Med 2006; 174: 795–802. 36. Russell E, Luk F, Manocha S, Ho T, O’Connor C, Hussain H: Long term follow-up of infliximab efficacy in pulmonary and extrapulmonary sarcoidosis refractory to conventional therapy. Semin Arthritis Rheum 2013; 43: 119–24. 37. Hostettler KE, Studler U, Tamm M, Brutsche MH: Long-term treatment with infliximab in patients with sarcoidosis. Respiration 2012; 83: 218–24. 38. Prasse A, Katic C, Germann M, Buchwald A, Zissel G, Müller-Quernheim J: Phenotyping sarcoidosis from a pulmonary perspective. Am J Respir Crit Care Med 2008; 177: 330–6. Anschrift für die Verfasser Prof. Dr. med. Antje Prasse Medizinische Hochschule Hannover Abteilung für Pneumologie Carl-Neuberg-Straße 1, 30625 Hannover [email protected] Zitierweise Prasse A: The diagnosis, differential diagnosis, and treatment of sarcoidosis. Dtsch Arztebl Int 2016; 113: 565–74. DOI: 10.3238/arztebl.2016.0565 @ The English version of this article is available online: www.aerzteblatt-international.de Zusatzmaterial Mit „e“ gekennzeichnete Literatur: www.aerzteblatt.de/lit3316 oder über QR-Code Weitere Informationen zu cme Dieser Beitrag wurde von der Nordrheinischen Akademie für ärztliche Fort- und Weiterbildung zertifiziert. Die erworbenen Fortbildungspunkte können mit Hilfe der Einheitlichen Fortbildungsnummer (EFN) verwaltet werden. Unter cme.aerzteblatt.de muss hierfür in der Rubrik „Persönliche Daten“ und bei der Registrierung die EFN in das entsprechende Feld eingegeben werden und durch Bestätigen der Einverständniserklärung aktiviert werden. Die 15-stellige EFN steht auf dem Fortbildungsausweis. Wichtiger Hinweis Die Teilnahme an der zertifizierten Fortbildung ist ausschließlich über das Internet möglich: cme.aerzteblatt.de. Einsendeschluss ist der 13. 11. 2016 Einsendungen, die per Brief oder Fax erfolgen, können nicht berücksichtigt werden. Die cme-Einheit „Diagnostik und Therapie von Nagelerkrankungen“ (Heft 29–30/2016) kann noch bis zum 16. 10. 2016 bearbeitet werden. Die cme-Einheit „Stillen und Beikost“ (Heft 25/2016) kann noch bis zum 18. 9. 2016 bearbeitet werden. Deutsches Ärzteblatt | Jg. 113 | Heft 33–34 | 22. August 2016 573 MEDIZIN Bitte beantworten Sie folgende Fragen für die Teilnahme an der zertifizierten Fortbildung. Pro Frage ist nur eine Antwort möglich. Bitte entscheiden Sie sich für die am ehesten zutreffende Antwort. Frage Nr. 1 Frage Nr. 7 Wodurch ist die Sarkoidose histologisch gekennzeichnet? a) durch Ulzerationen der oberen Schleimhautschichten b) durch granulozytäre Infiltration c) durch eine nekrotisierende Vaskulitis d) durch epitheloidzellhaltige, nicht-verkäsende Granulome e) durch Hyper- und kräftige Parahyperkeratose Welche Diagnostik ist Bestandteil der Routinediagnostik beim Screening auf Organbefall bei Sarkoidose? a) Lungenfunktionstest b) Magnetresonanztomographie c) Herzkatheteruntersuchung d) 24-h-Blutdruckmessung e) Phlebographie des Becken- und Beinbereichs Frage Nr. 2 Welche Befunde lassen sich mit einer Sarkoidose vereinbaren? a) Der Tine-Test ist negativ und der IGRA positiv. b) Die Polymerasekettenreaktion und Kultur auf Mycobacterium tuberculosis ist positiv, säurefeste Stäbchen jedoch nicht nachweisbar. c) Der Kveim-Test ist negativ. d) Mehrere Organe sind betroffen, histologisch nichtverkäsende Granulome wurden nachgewiesen und es erfolgte ein Ausschluss einer anderweitigen Ursache. e) Atypische Mykobakterien wurden mit Hilfe der Polymerasekettenreaktion nachgewiesen. Frage Nr. 3 Was versteht man unter der Trias des Löfgren-Syndroms? a) Nystagmus, Intentionstremor und Dysarthrie b) Miosis, Ptosis und Enophthalmus c) Struma, Exophthalmus und Tachykardie d) juvenile Arthritis, chronische Herzinsuffizienz und Psoriasis e) Sprunggelenksarthritis, mediastinale Lymphadenopathie und Erythema nodosum Frage Nr. 4 Welcher Befund ist für die Diagnosesicherung einer Sarkoidose zwingend erforderlich? a) Die Diagnose ist alleine anhand des klinischen Befundes zu stellen. b) Anhand der Thoraxaufnahme mit Hilfe der hochauflösenden Computertomographie kann der geübte Radiologe die Diagnose zweifelsfrei sichern. c) Im Zuge der Diagnose sollte immer eine Kultur auf Mykobakterien angelegt werden. d) Allein ein erhöhter ACE-Spiegel ist diagnoseweisend. e) Mit Hilfe einer genetischen Untersuchung kann die Diagnose sicher gestellt werden. Frage Nr. 5 Welche Medikamente werden zur Zweitlinientherapie bei der Sarkoidose eingesetzt? a) Ibuprofen und Diclofenac b) Methotrexat und Azathioprin c) Calciuminhibitoren und Antibiotika d) Adalimumab und Infliximab e) Mitoxantron, Cyclophosphamid Frage Nr. 6 Was ist die zurzeit bei erstmaligem Therapiebeginn iinitial eingesetzte Standardtherapie bei der Sarkoidose? a) 1 mg kg/KG Prednison für 1 Monat, dann Reduktion auf 0,5 mg kg/ KG für 1 Monat b) 0,5 mg kg/KG Prednison und 150 mg Azathioprin für 6 Monate c) 600 mg Rifampicin, 300 mg Isoniazid, 2 000 mg Pyrazinamid für 4 Monate d) 0,5 mg kg/KG Prednison mit Calcium und Vitamin-D-Supplementation e) 0,5 mg kg/KG Prednison für 1 Monat, dann schrittweise Reduktion über insgesamt 6 Monate 574 Frage Nr. 8 Bei einem 23-jährigen Patienten diagnostizieren Sie anhand der Symptom-Trias ein Löfgren-Sydrom. Wie gehen Sie vor? a) Sie leiten sofort eine Kortikosteroidtherapie ein. b) Sie klären den Patienten ausführlich auf und sagen ihm, dass weitere Kontrollen nicht mehr notwendig seien, da das Löfgren-Syndrom eine sehr hohe Spontanheilungsrate habe. c) Sie schicken den Patienten unverzüglich zum Dermatologen zwecks Diagnosesicherung. d) Sie bestimmen den genetischen Polymorphismus für BTNL2 und behandeln in Abhängigkeit von dem Ergebnis mit Kortikosteroiden oder nicht. e) Sie klären den Patienten über die Prognose auf und empfehlen zunächst eine histologische Sicherung mittels Bronchoskopie (EBUS) sowie die symptomorientierte Behandlung mit nichtsteroidalen Antiphlogistika und gelenkabschwellender Lokaltherapie. Frage Nr. 9 Bei einem 68-jährigen Patienten mit neudiagnostizierter Sarkoidose mit Lungen- und Leberbefall erheben Sie folgende Befunde: Vitalkapazität 85 %, CO-Diffusionkapazität 73 %, PaO2 in Ruhe: 78 mm Hg, GOT: 40 U/L, GPT: 50 U/L. Der Gamma-InterferonTest ist positiv, im Sputum sind keine säurefesten Stäbchen nachweisbar. Die Kulturen auf Mykobakterien sind negativ. Wie gehen Sie vor? a) Sie leiten sofort eine Kortikosteroidtherapie ein. b) Zur Diagnosesicherung veranlassen Sie ein 18F FDG-PET zur Fokussuche. c) Sie revidieren die Diagnose zur aktiven TBC und leiten eine antimykobakterielle Vierfach-Kombinationstherapie ein. d) Weder der Lungen- noch der Leberbefall stellen eine Indikation zur Einleitung einer Prednisontherapie dar. Sie empfehlen vorerst regelmäßige Kontrollen. e) Für die Behandlung mit Azathioprin und Methotrexat liegt eine Kontraindikation vor, deshalb befürworten Sie die Kombinationstherapie mit Infliximab. Frage Nr. 10 Bei Ihnen stellt sich erstmals ein Patient mit bekannter Sarkoidose und kürzlich durchgemachtem akutem Nierenversagen infolge von Harnaufstau bei Nierensteinen vor. Wie gehen Sie vor? a) Vor Einleitung einer Prednisontherapie weisen Sie den Patienten zur Nierenbiopsie stationär ein, da Sie einen Befall der Nieren durch die Sarkoidose vermuten. b) Sie bestimmen Calcium im Urin und Serum und raten primär zum Verzicht von Milchprodukten und Meidung von Sonnenlicht. c) Sie vermuten eine Störung im Parathormonstoffwechsel und überweisen den Patienten zum Endokrinologen. d) Sie raten zur Einleitung einer Prednisontherapie und empfehlen eine Vitamin-D-Substitution zur Osteoporoseprophylaxe. e) Ein Zusammenhang zwischen der Sarkoidose und dem Steinleiden besteht Ihrer Meinung nach nicht und Sie schicken den Patienten gleich weiter zum Urologen. Deutsches Ärzteblatt | Jg. 113 | Heft 33–34 | 22. August 2016







![*************m***]5**********`5**************l5**m5**n5**o5**p5**q5](http://s1.studylibde.com/store/data/000005519_1-2fb35a84f55fadf911e9aeb4075dcbae-300x300.png)