Bordetella-bronchiseptica-Infektionen
Werbung

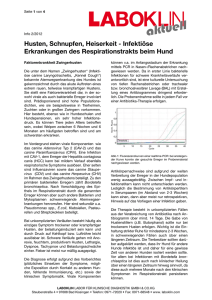
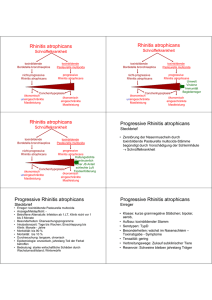
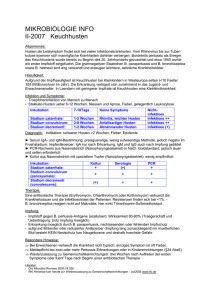
ATEMWEGSERKRANKUNGEN Atemwegserkrankungen beim Schwein (Teil 4) Bordetella-bronchiseptica-Infektionen Großtierpraxis 6:01, 35-40 (2005) von B. Iben Zu den Bordetellen werden sieben Arten gerechnet, von denen einige für Tier und Mensch pathogen sind. V on größter BedeuVon tung sind Bordetella pertussis (Erreger des Keuchhustens) und Bordetella bronchiseptica. B. bronchiseptica kommt häufig in Verbindung mit Atemwegserkrankungen des Schweines vor vor,, besonders häufig findet man den Krankheitserreger in V erbindung Verbindung mit Rhinitis atrophicans. Einleitung Die Infektion mit B. bronchiseptica stellt neben ihrer Beteiligung am Krankheitsgeschehen der Schnüffelkrankheit eine Gefahr für Saugferkel und Absatzferkel dar. Zu Beginn der Erkrankung findet sich seltsam heiser klingender Husten, der sehr schnell in Niesen und Dyspnoe übergeht. Da B. bronchiseptica ein Parasit des Flimmerepithels des Respirationstraktes ist, verwundern diese Symptome nicht, insbesondere, wenn man zusätzlich die Virulenzeigenschaften des Erregers betrachtet, welche zu Zi- liostase und Destruktion des Flimmerepithels führen. Als Resultat der Infektion ergibt sich eine Bronchopneumonie. Der Erreger Die Bordetellen gehören zur Familie Alcaligenaceae innerhalb der βGruppe der Proteobakterien. Abb. 1 zeigt schematisch einen auf den DNASequenzen der ribosomalen 16SRNA-Gene beruhenden phylogenetischen Stammbaum der Bordetellen und der eng benachbarten Gattungen Achromobacter und Alcaligenes. Bordetellen sind gramnegative, 0,5 – 1,0 mm große, kokkoide bis ovale, pleomorphe Stäbchen, die peritrich begeißelt sind. Der Keim wächst gut auf Blutagar. Nach 24 Std. Bebrütung zeigt sich der Erreger in kleinen, hellen Kolonien (Abb. 2). Der Erreger ist in der Lage verschiedene Virulenzfaktoren wie Toxine, Aggressine und Adhäsine zu bilden. Ein weiterer Virulenzfaktor ist ein Endotoxin mit den charakteristischen Eigenschaften der Lipopolysaccharide gramnegativer Bakterien. Inwieweit B. bronchiseptica weitere Virulenzfaktoren besitzt, ist nicht geklärt. Für B. pertussis sind weitere Faktoren und Toxine bekannt, die in Übersicht 1 aufgeführt sind. Möglicherweise gibt es bislang unerforschte Gemeinsamkeiten. So ist bislang nicht geklärt, welche Faktoren B. bronchiseptica das Anheften an die mit Zilien besetzten Epi- Zum Titelbild: Längsschnitt durch einen Schweinerüssel. Durch die bakteriellen Erreger ist es zur Eiteransammlung im Nasenmuschelbereich gekommen. (Quelle: Handbuch Gesunde Schweine, Kamlage Verlag, Osnabrück) GROSSTIERPRAXIS 1/2005 35 Abb. 1. Systematik der Bordetellen. Abb. 2. Bordetella bronchiseptica, Reinkultur auf Blutagar (Quelle: Farbatlas zur Diagnose bakterieller Infektionskrankheiten der Tiere; Verlag Paul Parey 1988). thelzellen des oberen Atmungstraktes ermöglichen. Diese Adhäsion ist der wichtigste Schritt, weil er den Bakterien die Kolonisierung des oberen Atmungstraktes ermöglicht. Der für B. pertussis wichtigste Adhäsionsfaktor ist das Filamentöse Hämagglutinin (FHA). Dieses verfügt über wenigstens drei unterschiedliche Adhäsionsaktivitäten. Die Bindung von Adhäsinen an Oberflächenproteine der Wirtszellen dient nicht nur der Anheftung der Bakterien, sondern kann auch bestimmte für die Bakterien vorteilhafte Reaktionen dieser Zellen auslösen (Fuchs und Gross 2001). Die Kolonisierung erfordert die Synthese einiger Zellgifte, zu denen bei B. pertussis das Pertussis-Toxin (für B. bronchiseptica ist ein Pendant bislang unbekannt) und für diesen sowie die übrigen Bordetella-Arten das Adenylazyklase-Toxin (CYA) und das Tracheale Zytotoxin (TCT) gehören. Ihre zellschädigende Wirkung dient nicht nur der Schwächung der Abwehrmechanismen, sondern kann beispielsweise auch Eisen freisetzen, das für die Vermehrung des Erregers wichtig ist. Das CYA-Toxin wirkt auf zweifache Weise: Es kann Blutzellen lysieren (Hämolyse) und in eukaryotischen Zellen die Umsetzung von ATP zu cAMP katalysieren. Das Tracheale Zytotoxin (TCT) entstammt der Mureinschicht der Bakterienzellwand und bewirkt zusammen mit den auf der Zellwand befindlichen Lipopolysacchariden die Produktion großer Mengen Stickoxide durch die Epithelzellen. Diese Stickoxide wirken als Zell- Übersicht 1: Virulenzfaktoren von B. pertussis (Fuchs und Gross 2001) Virulenzfaktor Pertussis-Toxin (PT) Adenylatzyklase-Toxin (CYA) Tracheales Zytotoxin (TCT) Filamentöses Hämagglutinin (FHA) Pertactin (PRN) Trachealer Kolonisierungsfaktor (TCF) Serumresistenzfaktor BrkA Lipopolysaccharid (LPS) 36 GROSSTIERPRAXIS 1/2005 Wirkung ADP-Ribosylierung von Gi-Proteinen; Steigerung des cAMP-Spiegels; Interferenz mit Effektorzellen des Immunsystems Hämolyse und Steigerung des cAMP-Spiegels; Interferenz mit Effektorzellen des Immunsystems Zerstörung von Zilien tragenden Epithelzellen durch Induktion der übermäßigen Produktion von Stickoxid (NO) Adhäsion an Epithelzellen und Phagozyten; Bindung an Zielzellen durch RGD-Motiv, Kohlenhydrat- und Heparin-Bindemotive Adhäsion und Kolonisierung Adhäsion und Kolonisierung Resistenz gegen bakterielle Mechanismen in Kombination mit TCT-Induktion der übermäßigen Produktion von Stickoxid (NO) ATEMWEGSERKRANKUNGEN gift und sind vermutlich die Ursache des Hustens, da durch den Verlust der Zilien die Atemwege nicht mehr von Schleim, Staub und Bakterien gesäubert werden können. Epidemiologie und Pathogenese B. bronchiseptica ist weltweit verbreitet. Der Erreger kommt nicht nur beim Schwein vor, empfänglich sind auch Hund, Katze, Pferd und Pute. Beim Hund ist B. bronchiseptica Auslöser nutzt. Auch von Menschen konnte der Erreger isoliert werden. Infizierte Menschen können für SPF-Zuchten gefährlich werden, der Erreger verbreitet sich in solchen Beständen innerhalb kürzester Zeit. Bordetellen werden im Schweinesektor durch den Viehhandel verbreitet. Es bestehen nur wenige Betriebe, die sich von dem Erreger freihalten konnten. Als prädisponierende Faktoren gelten: • früheres Auftreten von Rhinitis atrophicans im Bestand • schlechte Hygiene in den Abferkelställen Bordetellen werden durch den Viehhandel verbreitet. des Zwingerhustens (Tracheobronchitis), bei der Katze am Krankheitsbild Katzenschnupfen beteiligt (siehe Seite 20). Andere Tiere kommen als Träger in Frage (Ratte, Maus, Opossum, Wildvögel, Meerschweinchen, Kaninchen). Wiederkäuer werden von B. bronchiseptica gewöhnlich nicht als Wirt be- • ungünstige Umweltbedingungen in allen Bestandsabteilungen (mangelnde oder zu starke Belüftung, gesundheitsschädliche Gase, hohe Staubbelastung, zu hohe oder zu niedrige Luftfeuchtigkeit) • zu hohe Remontierung, die die Bildung einer Populationsimmunität verhindert (Kobisch und Tillon 1982). Die Infektion der Saugferkel erfolgt über die Muttertiere oder durch ältere Ferkel aus der Nachbarschaft. Durch Schniefen und Niesen werden im Stallraum massive Tröpfchenaerosole gebildet. Diese werden eingeatmet und es kommt zur Kolonisierung durch Adhäsion auf den Schleimhäuten der oberen Atemwege. Kurz darauf kommt es durch Bildung von Toxinen und Stoffwechselprodukte des Krankheitserregers zur Hemmung der Aktivität des Flimmerepithels bis zur vollständigen Zerstörung der Zilien sowie pathologischer Veränderung der darunter liegenden Gewebe. Das Tracheale Zytotoxin (TCT) verursacht Ziliostase und Destruktion des Flimmerepithels. Hinzu kommt das hitzestabile Toxin (HLT), auch als Dermonekrotisierendes Toxin (DNT) bezeichnet und das bivalente Toxin AdenylatzyklaseToxin (CYA), welches zytolytisch auf Immunzellen (Neutrophile, Monozyten, Makrophagen) wirkt. Im Allgemeinen bildet sich eine streifenförmige Bronchopneumonie in den kranialen Hälften der Lunge, die durch Zonen lädierten Parenchyms charakterisiert und von tiefen Rinnen Bindegewebe getrennt ist (Abb. 3; Pfeile), das bis zur Narbenbildung bestehen bleibt (Häni et al. 1976). Die veränderten Bezirke sind anfangs dunkelrot, dann graurot bis graugelb gefärbt und fest (Abb. 3). Fibrinöse bis fibröse Pleuritis tritt gewöhnlich nur über besonders heftig entzündeten Lungenbezirken auf. Schwellungen der Lymphknoten sind sehr unterschiedlich ausgeprägt. Nach Sieverding (2000) unterscheiden sich die Organbefunde bei der Sektion deutlich von den Veränderungen der progressiven RA und der Enzootischen Pneumonie. Abb. 3. Lungenveränderungen bei Bordetella-Bronchopneumonie (aus Smith et al., Wolfe Publishing, Ipswich, England 1990). 38 GROSSTIERPRAXIS 1/2005 Größere Knoten weisen auf der Schnittfläche öfter kleine, rote bis bräunliche Stellen auf, die von Blutungen und Nekrosen herrühren. Die Bronchien der betroffenen Lungenabschnitte enthalten meist schleimig-eitriges Exsudat. Übersicht 2: Möglichkeiten der biochemischen Differenzierung von Bordetellen Reaktion Urease (Harnstoffspaltung erfolgt bereits nach 4 – 6 Std. und stellt eine charakteristische Eigenschaft dar) Kohlenhydratspaltung (zu ihrer Feststellung reicht die Prüfung von Glukose, Laktose und Saccharose) Darüber hinaus können geprüft werden: Indol-Reaktion Voges-Proskauer-Reaktion Methylrot-Reaktion Schwefelwasserstoffbildung Gelatineverflüssigung Katalase Lackmusmilch (Alkalisierung) Ausfall + - + + (nach 2 Std.) Für die serologische Typisierung sind z.Zt. keine kommerziellen Typenseren erhältlich. Die Typisierung wichtiger Stämme ist jedoch nach vorheriger Absprache mit dem Bundesinstitut für gesundheitlichen Verbraucherschutz und Veterinärmedizin, Bereich Jena, möglich. Gleiches gilt für den Toxinund Antikörpernachweis. Differentialdiagnose Differentialdiagnostisch müssen Rhinitis atrophicans, Mykoplasmen, Pasteurellen, hämophile Keime und Chlamydien ausgeschlossen werden. Therapie Das histologische Bild entspricht dem makroskopischen. Neben unveränderten Läppchen finden sich Bezirke mit heftiger katarrhalischer bis eitriger und nekrotisierender Pneumonie oder großzellig-proliferativer Pneumonie. Durch die toxinbedingte Gefäßschädigung wird die Pneumonie von starken Flüssigkeitsaustritt und Blutungen aus den Kapillaren begleitet. Klinische Erscheinungen Die klinischen Erscheinungen sind wenig charakteristisch und unterscheiden sich kaum von denen anderer Erkrankungen, die etwa durch Mykoplasmen, Pasteurellen oder Chlamydien hervorgerufen werden. Nach Sieverding Diagnose Die klinischen Symptome lassen nur eine Verdachtsdiagnose zu. Am größten ist die Wahrscheinlichkeit der Isolierung von B. bronchiseptica bei Ferkeln im Alter von 10 Tagen bis 10 Wochen (Sieverding 2000). Am Ende einer Infektion kann wegen des Vorliegens einer Immunität bei den Tieren unter Umständen ein bakteriologisch negatives Ergebnis vorliegen (Kobisch und Tillon 1982). Zur Absicherung der klinischen Diagnose müssen entweder Trachealtupfer oder Lungenspülproben untersucht werden. Bei akuten Infektionen liegen die Erreger im pathologischen Material in großen Mengen vor und sind mittels Gramfärbung darstellbar. Klinische Erscheinungen sind wenig charakteristisch. (2000) ist anfänglich heiser klingender Husten zu hören, der sehr schnell in Niesen und Atemnot übergeht. In einigen Beständen wird das Niesen von Tränenfluss begleitet. Bei den Ferkeln sind deutlich sichtbare Tränenringe um die Augen erkennbar, d.h. eine sichere Diagnose kann nur im Labor erfolgen. Die Krankheitsanzeichen sind bei 10 Tage bis 10 Wochen alten Ferkeln zu beobachten und gehen unbehandelt etwa 2 Monate nach der Infektion zurück. Als Folge können sich Wachstumsdepressionen einstellen. 40 GROSSTIERPRAXIS 1/2005 Die kulturelle Untersuchung erfolgt auf Selektivnährböden (McConkeyAgar mit 100 µg Nitrofurantoin und 10 IE Penicillin/ml Nährboden). Die Bebrütung erfolgt über 24 bis 48 Std. bei 37 °C. Zur biochemischen Differenzierung werden die traditionellen Röhrchenverfahren und Mikromethoden in vorgefertigten Platten angewendet. Das biochemische Verhalten von B. bronchiseptica ist sehr einheitlich, so dass für die Routine die Prüfung einiger Reaktionen ausreicht (Übersicht 2). B. bronchiseptica zeigt geringgradige Resistenz bei Tetrazyklin, Neomycin, Gentamicin, Colistin und Florfenicol, mittelgradige Resistenz bei Enrofloxacin, relativ hochgradige Resistenz bei Amoxicillin, hochgradige bis höchstgradige Resistenz bei TMP/ S, Ampicillin und Penicillin (Weisser 2003). Doch Vorsicht: Dies sind Ergebnisse im Einzugsgebiet des CVUA Stuttgart aus den Jahren vor 2002. In anderen Gebieten sind abweichende Resistenzprobleme zu erwarten. Auch aus diesem Grund muss einer antibiotischen Therapie ein Resistenztest vorausgehen. Bei entsprechender Empfindlichkeit des Erregers können dann die Empfehlungen von Sieverding (2000) aufgegriffen werden. Danach soll die Einzeltierinjektion mit 10 – 20 mg/kg KG Amoxicillin, 2,5 mg/kg KG Enrofloxacin, 1,25 mg/kg KG Donafloxacin, 2 mg/kg KG Marbofloxacin oder 5 mg/kg KG Gentamicin erfolgen. Für die orale Behandlung werden 400 g Pulmotil/t Futter oder 500 – 1.000 g Trimethoprim-Sulfonamid/t Futter angegeben. Prophylaxe Prophylaktische Maßnahmen zielen auf die allgemeine Stärkung des Immunsystems sowie die Optimierung des Stallwetters und der Haltungsbedingungen. In Großraumställen enthält die Luft mehr schwebende Teilchen (die potentiell mit Krankheitserregern behaftet sind), die durch die Tiere aufgenommen werden können. Staub, gesundheitsschädliche Gase, Trockenheit und extrem niedrige oder hohe Luftfeuchtigkeit sowie inadäquate Temperaturen erhöhen die Empfindlichkeit der Schweine gegenüber Pneumonieerregern. Staubpartikel können als abiotische Vektoren Infektionserreger sowie Endotoxine beherbergen und gemeinsam mit anderen Luftverunreinigungen das Epithel des Atmungstraktes schädigen. Gesundheitsschädliche Gase, wie Ammoniak, Schwefelwasserstoffgas, Kohlendioxid und Kohlenmonoxid sollten zumindest in den Grenzen der gesetzli- chen Regelungen gehalten werden, wobei der Wert für NH3 in der Schweinehaltungshygieneverordnung mit 20 ppm als eindeutig zu hoch anzusehen ist. Die Stalltemperatur ist einmal von ihrem absoluten Wert her zu optimieren, zum anderen müssen extreme Schwankungen verhindert werden. Temperaturschwankungen von mehr als 12 °C innerhalb von 24 Stunden sind nicht selten. Derartige Schwankungen vermindern die natürliche Immunität und führen dadurch zu gehäuftem Auftreten von Pneumonien. Gleiches gilt für Schweine in Freilandhaltungen bei plötzlichem Temperaturabfall. Immunprophylaxe Eine Schutzimpfung gegen B. bronchiseptica kann mit Impfstoffen der Firmen IDT (Respiporc® bzw. Respiporc ATEMWEGSERKRANKUNGEN ART+EP®) sowie Intervet (Porcilis ART®) erfolgen. Die Impfung von Sauen führt zur passiven Immunisierung der Ferkel durch das Kolostrum. Man kann der Erkrankung auch mit stallspezifischen Impfstoffen Autovakzinen zu Leibe rücken. Anschrift des Verfassers: Dr. Dr. Bernd Iben Mündener Straße 5 37213 Witzenhausen Tel.: 05542 / 507 701 Fax: 05542 / 507 690 e-mail: [email protected] Zusammenfassung Atemwegserkrankungen beim Schwein (Teil 4) Bordetella bronchiseptica-Infektionen Schlüsselwörter: Schwein, Atemwegserkrankungen, B. bronchiseptica, Klinik, Diagnose, Therapie, Prophylaxe B. bronchiseptica ist nicht nur am Krankheitsgeschehen der progressiven Rhinitis atrophicans beteiligt, sondern kann auch als Einzelerreger eigenständige Infektionen hervorrufen, die Bordetella-brochinseptica-Infektion. Klinisch ist die Erkrankung nicht si- cher von anderen Erkrankungen des porzinen Atmungstraktes zu unterscheiden. Einfache labordiagnostische Untersuchungsmethoden stehen jedoch zur Verfügung Die Therapie erfolgt mit Antibiotika, die sich im Antibiogramm als wirksam erwiesen ha- ben. Prophylaktische Maßnahmen umfassen die Optimierung der Haltungsbedingungen. Zur Immunprophylaxe stehen verschiedene Impfstoffe zur Verfügung. Eine Immunprophylaxe kann auch mit Autovakzinen erfolgen Summary Diseases of the respiratory tract in pig (part 4) Infections caused by Bordetella bronchiseptica Keywords: pig, respiratory disease, B. bronchiseptica, clinic, diagnosis, therapy, prophylaxis B.bronchiseptica ist not only involved in the course of progressive Rhinitis atrophicans but is, being a single pathogen, able to cause independent infections as the Bordetella-bronchiseptica infection. Clinical there is no safe method to differ the disease from other porcine respiratory diseases. However simple methods for lab diagnosis are available. Antibiotics, which have been shown effective in antibiogram are used in therapy. Pre- cautionary measures include optimized keeping conditions. Various kind of vaccine to realize prophylactic immunization is available. Prophylactic immunisation can also be done by autovaccination. GROSSTIERPRAXIS 1/2005 41