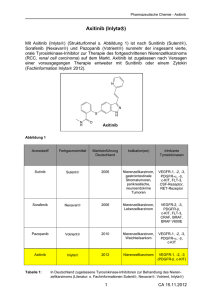
Aflibercept (Eylea®)
Werbung

Pharmazeutische Chemie - Aflibercept Aflibercept (Eylea ) Aflibercept (Eylea) ist ein neues rekombinantes Fusionsprotein („-cept“), das in Form einer intravitrealen Injektion zur Behandlung der neovaskulären (feuchten) altersabhängigen Makuladegeneration (AMD) angewendet wird. Dabei wird die Therapie mit drei Injektionen im monatlichen Abstand eingeleitet gefolgt von einer Injektion alle zwei Monate. Nach einem Jahr ist es möglich je nach Verlauf das Injektionsintervall zu verlängern (Fachinformation Eylea 2012). Die altersabhängige Makuladegeneration ist eine Hauptursache für Erblindung bei älteren Erwachsenen. Bei der feuchten Form bilden sich unter der Netzhaut zu Blutungen neigende Gefäße aus (choroidale Neovaskularisation). Zur Behandlung der neovaskulären Form der AMD werden heutzutage vorwiegend Arzneistoffe eingesetzt, die die Gefäßneubildung hemmen (Tabelle 1). Diese Arzneistoffe werden intravitreal in den Glaskörper injiziert und sind gegen die VEGF-Familie (vascular endothelial growth factor) oder deren Rezeptoren gerichtet. Ranibizumab (Lucentis) ist ein Fragment eines humanisierten rekombinanten monoklonalen Antikörpers, das gegen verschiedene Isoformen des VEGF-A gerichtet ist. Es bindet mit hoher Affinität u.a. an die VEGF-A-Isoform VEGF165, die für die AMD von besonderer Bedeutung zu sein scheint. Durch die Bindung von Ranibizumab an VEGF165 wird die Bindung an die VEGF-Rezeptoren 1 und 2 unterbunden, so dass das Signal zur Endothelzell-Proliferation und Neovaskularisation unterbleibt (Fachinformation Lucentis 2012). Das Aptamer Pegaptanib (Macugen) bindet hochspezifisch nur an die Isoform VEGF165 und unterbindet damit die Angiogenese (Fachinformation Macugen 2012). Während für Lucentis und Macugen eine Zulassung zur Behandlung der AMD vorliegt, erfolgt zudem eine Off-Label-Behandlung mit dem humanisierten rekombinaten monoklonalen Anti-VEGF-Antikörper Bevacizumab (Avastin), der eigentlich zur Therapie von Kolon-, Ovarial-, Bronchial- und Mammakarzinomen zugelassen ist (Krebs et al. 2009, Fachinformation Avastin 2012). Arzneistoff FAM Zulassung Arzneistoffart Target Bevacizumab Avastin 2005* Monoklonaler Antikörper alle VEGF-AIsoformen Pegaptanib Macugen 2006 Aptamer VEGF165-Isoform Ranibizumab Lucentis 2007 Monoklonaler Antikörper Aflibercept Eylea 2012 Fusionsprotein alle VEGF-AIsoformen alle VEGF-AIsoformen und PIGF *nicht für AMD zugelassen, Off-label-Anwendung Tabelle 1: Anti-VEGF-Arzneimittel zur Behandlung der neovaskulären AMD 1 CA 30.12.2012 Pharmazeutische Chemie - Aflibercept Neben Lucentis und Macugen ist Eylea nun das dritte Arzneimittel, das explizit zur Behandlung der neovaskulären AMD zugelassen ist. Die Familie der VEGF scheint für die Entstehung der neovaskulären AMD von entscheidender Bedeutung zu sein. Zu dieser Familie zählen die proangiogenen Wachstumsfaktor-Peptide VEGF-A, VEGF-B, VEGF-C, VEGF-D und PIGF (= Plazenta-Wachstumsfaktor). Von besonderer Wichtigkeit ist VEGF-A (vielfach auch einfach als VEGF bezeichnet), das sich nochmals in verschiedene Isoformen unterteilen lässt. Die wichtigsten Isoformen sind VEGF121, VEGF145, VEGF165, VEGF189 und VEGF206. VEGF165 ist hierbei die am häufigsten sezernierte und die physiologisch aktivste Isoform. VEGF-A steigert die Angiogenese, erhöht die vaskuläre Permeabilität und fördert die Freisetzung von Stammzellen aus dem Knochenmark (Takahashi 2011, Chang et al. 2012). Die VEGF binden an drei verschiedene Rezeptor-Tyrosinkinasen: VEGFR-1 (= Flt-1), VEGFR-2 (= KDR) und VEGFR-3, wobei VEGFR-3 auf lymphatische Endothelzellen beschränkt ist. Die VEGFs haben verschiedene Affinitäten für die drei RezeptorSubtypen. So bindet VEGF-A an VEGFR-1 und –2, wobei VEGFR-2 der für die Angiogenese wichtigere zu sein scheint. Die Bindung an VEGF-A induziert eine Dimerisierung mit nachfolgender Autophosphorilierung, die letztlich zu einem mitogenen und proliferativen Signal führt (Takahashi 2011, Chang et al. 2012). 2 2 3 3 1 1 2 2 3 3 4 4 5 5 6 6 7 7 Fc-Anteil IgG1 Aflibercept Abbildung 1: Kinase Kinase VEGFR-1 VEGFR-2 Aufbau des Aflibercepts nach Moroney et al. 2009 2 CA 30.12.2012 Pharmazeutische Chemie - Aflibercept Aflibercept ist ein rekombinantes Fusionsprotein (hergestellt in Ovarialzellen chinesischer Hamster (CHO), Typ K1), das als sogenannter Köderrezeptor („VEGFTrap“) aufgrund seiner hohen Affinität zu VEGF-A, diesen Wachstumsfaktor (und PIGF) abfängt, bevor er an VEGF-Rezeptoren binden kann. Zusammengesetzt ist Aflibercept aus extrazellulären Domänen der VEGF-Rezeptoren 1 und 2 sowie dem Fc-Fragment des Immunglobulins G1 (IgG1) (Stewart 2011, Fachinformation Eylea 2012). Ursprünglich enthielt das Aflibercept-Fusionsprotein die ersten drei Domänen des VEGFR-1 und die konstante Region des IgG1. Dieses Protein zeigte auch eine beeindruckende, picomolare Affinität zu VEGF-A sowie Antitumor-Aktivität, allerdings besaß es auch eine positive Ladung, die dazu führte, dass dieses „VorläuferAflibercept“ unspezifisch an negativ geladene, extrazelluläre Matrixproteine band. Dementsprechend schlecht waren auch die pharmakokinetischen Parameter dieser Substanz. Anschließende Modifikationen führten dann zum eigentlichen Aflibercept, das nun die Fc-Region des IgG1 kombiniert mit der zweiten Domäne von VEGFR-1 und der dritten Domäne von VEGFR-2 enthält (Abbildung 1). Diese Änderungen führten dazu, dass die hohe Affinität zu VEGF-A erhalten blieb, die Pharmakokinetik aber entscheidend verbessert wurde (Moroney et al. 2009). Aflibercept bildet mit VEGF-A einen 1:1-Komplex, der sehr stabil und für bis zu 14 Tage nach einer einmaligen subkutanen Gabe systemisch nachweisbar ist. Bindungsstudien, die mit der vorherrschenden VEGF-A-Isoform VEGF165 durchgeführt wurden, zeigten einen Kd-Wert von 1pM (Holash et al. 2002). Literatur: Chang, J.H. et al. Surv Ophthalmol 2012, 57, 415 Fachinformation Avastin 2012 Roche Registration Limited Fachinformation Eylea 2012 Bayer Pharma AG Fachinformation Lucentis 2012 Novartis Europharm Limited Fachinformation Macugen 2012 Pfizer Limited Holash, J. et al. Proc Natl Acad Sci USA 2002, 99, 11393 Krebs, I. et al. Acta Ophthalmol 2009, 87, 611 Moroney, J.W. et al. Future Oncol 2009, 5, 591 Stewart, M.W. Inflamm Allergy Drug Targets 2011, 10, 497 Takahashi, S. Biol Pharm Bull 2011, 34, 1785 3 CA 30.12.2012