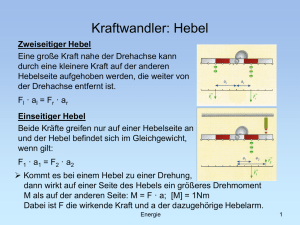
Voransicht
Werbung

4. Grundlagen der Quantenphysik 1 von 28 Schrödingers Atommodell – Grundlagen der Quantenphysik Dr. Johannes Günther, Karlstadt Foto: Süddeutsche Zeitung In der Zeit von 1920 bis 1930 veränderten die Arbeiten zweier Physiker die Vorstellungen der Physik grundlegend, Louis de Broglie und Erwin Schrödinger. In seiner Doktorarbeit1 stellte de Broglie 1924 die kühne These auf, dass der Welle-Teilchen-Dualismus der Photonen auch für massebehaftete Teilchen wie Elektronen oder Protonen gelten solle. Der Promotionsprüfungsausschuss der Pariser Universität Sorbonne war sich mit der Bewertung dieser Arbeit so unsicher, dass er ein Exemplar an Albert Einstein sandte, der wiederum Max Born, Max Planck und andere über de Broglies Ideen informierte. So machte de Broglies Postulat der Materiewellen unter den führenden Physikern der damaligen Zeit schnell die Runde. II/E Louis de Broglie (1892–1987) T H C I S N A R O V Foto: picture-alliance/dpa Bereits zwei Jahre später veröffentlichte Erwin Schrödinger seine berühmte Gleichung2, die das Verhalten der Materiewellen in einem gegebenen Potenzial beschreibt. 1929 wurde de Broglie und 1933 Schrödinger für seine Arbeit mit dem Nobelpreis ausgezeichnet. Zeigen Sie Ihren Schülern Schritt für Schritt diese faszinierende Entwicklung auf. Ihre Schüler bekommen so Einblick in die mathematische Welt der Quantenphysik. Sie erlangen dabei ein grundlegendes Verständnis für die Vorgehensweisen der theoretischen Physik. Wischer: Eine schrittweise Hinführung zur Schrödingergleichung! Erwin Schrödinger (1887–1961) Der Beitrag im Überblick Klasse: 12 (G8) Inhalt: Dauer: • Das Linienspektrum des H-Atoms 8–10 Stunden Ihr Plus: • Die De-Broglie-Wellenlänge üAnregung für Diskussionen über die Quantenphysik • Das Bohr’sche Atommodell • Quantisierung im Potenzialtopf • Schrödingergleichung 1 L. de Broglie: Recherches sur la théorie des quanta. Dissertation. Masson & Cie, Paris 1924; Ann. Phys. 3 (1925), 22−128. 2 E. Schrödinger: Quantisierung als Eigenwertproblem. Mitteilungsreihe in den Annalen der Physik: Ann. Phys. 79, 361 (1926); Ann. Phys. 79, 489 (1926); Ann. Phys. 80, 437 (1926); Ann. Phys. 81, 109 (1926). 26 RAAbits Physik Februar 2012 4. Grundlagen der Quantenphysik 2 von 28 Fachliche und didaktisch-methodische Hinweise Historischer Abriss: Die Spektrallinien – ein Fingerabdruck der Atome Als Joseph von Fraunhofer 1814 das Sonnenlicht mit seinem Spektroskop untersuchte, entdeckte er dunkle Linien im Spektrum der Sonne. Als Erster konnte er zeigen, dass diese Linien dem Sonnenlicht eigen sind und kein technisches Artefakt. Ein knappes halbes Jahrhundert später untersuchten Gustav Kirchhoff und Robert Bunsen spektroskopisch das Licht, das chemische Elemente in der Flamme eines Gasbrenners aussenden. Sie konnten zeigen, dass Fraunhofers dunkle Absorptionslinien hier als leuchtende Emissionslinien auftauchen, die man den jeweiligen chemischen Elementen zuordnen kann. Ebenfalls um 1850 wurde die Gasentladungsröhre erfunden. Auch hier zeigte sich, dass das Licht der verschiedenen Gase aus einzelnen typischen Linien zusammengesetzt ist und kein kontinuierliches Spektrum aufweist. 1885 fand Johann Jakob Balmer heraus, dass sich die Wellenlängen der Spektrallinien des Wasserstoffs durch die später nach ihm benannte Serienformel 1 1 1 = R − 2 4 λ n II/E mit n ≥ 3 T H C berechnen lassen. Die Rydberg-Konstante R ist hierbei eine von Balmer experimentell bestimmte Naturkonstante. Mithilfe des Bohr’schen Atommodells gelang es schließlich, die Serienformel theoretisch herzuleiten und die Rydberg-Konstante durch fundamentale Größen wie die Ladung und die Masse des Elektrons auszudrücken. I S N Balmer und Rydberg legten damit den Grundstein für die Quantenphysik. Der empirisch gefundene Serienindex n wurde von Bohr als Hauptquantenzahl der Atome gedeutet. Die Spektralserien waren damit der entscheidende experimentelle Ausgangspunkt für die Erklärung der quantenhaften, in diesem Sinne ganzzahlig abzählbaren Struktur der Atome. A R O Hinweise zur Gestaltung des Unterrichts V Ziel der Unterrichtseinheit ist es, Ihre Schüler an die mathematisch geprägte Denkweise der Quantenphysik heranzuführen. Das uns vertraute Bild eines Sonnensystems, das Bohr zu seinem Atommodell inspirierte, stellte sich als unbrauchbar und irreführend heraus: Man konnte die Bewegung von Quantenobjekten (Elektronen usw.)1 nicht beobachten. Vielmehr führten die Erkenntnisse in Zusammenhang mit dem Welle-Teilchen-Dualismus dazu, dass man die Vorstellung deterministischer Prozesse aufgeben musste. An ihre Stelle treten Aufenthaltswahrscheinlichkeiten, die den Zustand eines Quantensystems beschreiben. Die Unterrichtsmaterialien geben einen Einblick in die quantenphysikalischen Berechnungsmethoden, wenden sie auf das Elektron im Potenzialtopf an und ermöglichen einen Ausblick auf die Lösungen der Schrödingergleichung für das Wasserstoffatom. Zum Umgang mit den Materialien Die Arbeitsmaterialien sind so gedacht, dass sich die Schüler die Inhalte selbstständig erarbeiten können. Sie als Lehrer übernehmen die Rolle eines Moderators und Helfers. • Lassen Sie die Schüler die Arbeitsblätter am besten in Partnerarbeit bearbeiten. Motivieren Sie sie, möglichst viel miteinander zu diskutieren. • Tauschen Sie nach der Erarbeitungsphase die Partner. Ihre Schüller sollen ihre Lösungswege und Ergebnisse dem neuen Partner erklären. 1 Austauschteilchen werden in diesem Beitrag nicht betrachtet. 26 RAAbits Physik Februar 2012 4. Grundlagen der Quantenphysik 3 von 28 • Halten Sie die Lösungen für die Schüler zur Selbstkontrolle bereit. • Lassen Sie die Schüler ihre Ergebnisse artikulieren, verbessern Sie Fehler nicht gleich selbst, sondern fordern Sie die Mitschüler zur kritischen Stellungnahme auf. • Am Ende besprechen Sie die Ergebnisse gemeinsam. Kopieren Sie die Materialien dafür am besten auf Folie. Voraussetzungen, die Ihre Lerngruppe mitbringen sollte Die Unterrichtseinheit richtet sich an Schüler der 12. (oder 13.) Klasse. Sicher werden einige Ihrer Schüler Physik als Abiturfach belegt haben und ein technisches oder naturwissenschaftliches Studium anstreben. Insbesondere für diese Schüler ist das Material gedacht. – Ihre Schüler sollten ihre Vorstellungen über den Aufbau des Atoms aus der Mittelstufe wiederholen und an der Tafel darstellen. Fordern Sie sie auf, ein Atom zu zeichnen. Sie werden erstaunt sein, wie vielfältig die Vorstellungen der Schüler sind, die sie aus dem Chemie- und Physikunterricht mitbringen. Greifen Sie die verschiedenen Modellvorstellungen auf und diskutieren Sie vermeintliche und offensichtliche Fehlvorstellungen. – Für das einführende Experiment zum Wasserstoffspektrum müssen die Schüler mit den Grundlagen der Interferenz am Gitter vertraut sein. Licht als elektromagnetische Welle sollte bekannt sein. Die Schüler benötigen Kenntnisse darüber, wie man eine Welle im Ortsraum mathematisch darstellt. II/E T H C – Machen Sie den Schülern der Schrödingergleichung die Newton’sche vor der Behandlung Bewegungsgleichung ( F = m • a ) als Differenzialgleichung begreiflich. Die harmonische Schwingung und das Hooke’sche Kraftgesetz sollten Sie dazu auffrischen. Das Arbeitsblatt zur Newton’schen Bewegungsgleichung führt auch die potenzielle Energie und das Potenzialdiagramm ein. I S N A R O – Aus Sicht der Quantenphysik sollte der Charakter von Photonen als Teilchen mit Energie E = h • f = m • c², h = 6,626 • 10 −34 Js bekannt sein. Idealerweise wurde auch schon der Fotoeffekt als Beleg für die Existenz der Photonen besprochen. V – Ihre Schüler sollten sicher mit der Energieeinheit Elektronenvolt (eV) umgehen können und ihre Vorteile für die Berechnung der Energie von Elektronen erkannt haben. – Für den Umgang mit der Schrödingergleichung ist ein sicheres Anwenden der Ableitungsregeln für sin(x) und die e-Funktion notwendig. Zum Unterrichtsverlauf – vom Experiment zur Theorie Gehen Sie mit Ihren Schülern schrittweise den Weg vom Experiment zur Theorie. Beginnen Sie Ihren Unterricht mit der experimentellen Bestimmung der Wellenlängen der Spektrallinien des Wasserstoffatoms (M 1). Diskutieren Sie mit Ihren Schülern die Konsequenzen dieses Experimentes für unser Bild vom Atom. Nutzen Sie dieses Experiment, um die Modellvorstellungen der Schüler vom Atom aufzugreifen und zu diskutieren. Ihrer Lerngruppe sollte bewusst werden, dass aus der beobachtbaren Wechselwirkung von Licht mit dem Atom die energetische Quantisierung der Atomhülle zwangsläufig folgt. Zeigen Sie auf, wie es Bohr gelang, die Struktur der Serienformeln aus wenigen theoretischen Annahmen herzuleiten. Für Bohrs Annahmen ist die De-Broglie-Wellenlänge eine wichtige Grundlage. Lassen Sie Ihre Schüler de Broglies Gedankengänge mithilfe von M 2 nachvollziehen. Als Einstieg kann ein Schüler über das Leben und Wirken de Broglies referieren. Nach der Bearbeitung von M 2 gehen Sie auf die experimentelle Bestätigung von de Broglies Wellenlänge durch die Elektronenbeugungsversuche von Davisson und Germer ein. Führen Sie die Elektronenbeugungsröhre vor oder zeigen Sie diese als Realexperiment im Internet. In der Mediothek finden Sie entsprechende Hinweise. 26 RAAbits Physik Februar 2012 4. Grundlagen der Quantenphysik 6 von 28 Materialübersicht · V = Vorbereitungszeit SV = Schülerversuch Ab = Arbeitsblatt/Informationsblatt · D = Durchführungszeit LV = Lehrerversuch Fo = Folie M1 LV/SV · V: 10 min · D: 30 min M2 Ab Das Wasserstoffspektrum – die Balmerserie bestimmen rBalmerlampe rGitter mit 600–1000 Linien/mm rFarbkreide rMaßband oder Tafellineal Die De-Broglie-Wellenlänge – eine Revolution Ihre Schüler setzen sich mit den Gedankengängen de Broglies auseinander und leiten einen Ausdruck für die De-Broglie-Wellenlänge her. M3 Ab Das Bohr’sche Atommodell Ihre Schüler vollziehen in Eigenarbeit die Bohr’sche Quantenbedingung nach. Sie werden dazu angeleitet, mit den Annahmen Bohrs die energetische Quantisierung der Zustände im Wasserstoffatom nachzurechnen. II/E M4 Ab T H C Arbeiten mit dem Potenzialdiagramm I S N Anhand eines iktiven Potenzials erlernen Ihre Schüler die wichtigsten Grundlagen im Umgang mit dem Potenzialdiagramm. M5 Ab Das Potenzialdiagramm des Wasserstoffs Ihre Schüler erschließen sich das Potenzialdiagramm des Wasserstoffs und berechnen die Wellenlängen der Balmerserie aus den in M 3 berechneten Energien der Zustände. A R O M6 V M7 Ab Der unendlich tiefe Potenzialtopf Ihre Schüler lernen das Modell des linearen Potenzialtopfes kennen und lösen einige einfache Aufgaben selbstständig. Ab Die Differenzialgleichung des harmonischen Oszillators Anhand des harmonischen Oszillators erlernen Ihre Schüler selbstständig den Umgang mit einer einfachen Differenzialgleichung. M8 Ab Für Experten: Die Schrödingergleichung Ihre Schüler leiten aus einem anschaulichen Ansatz und unter Einbeziehung der Energieerhaltung eine einfache Form der Schrödingergleichung her. M9 Ab Der Tunneleffekt beim endlich tiefen Potenzialtopf Zum Abschluss der Lerneinheit wenden Ihre Schüler alle besprochenen Inhalte am Beispiel des endlich tiefen Potenzialtopfes an und vertiefen sie. M 10 Ab Das quantenmechanische Modell des Wasserstoffatoms M 11 Sw-Fo Experimentelle Erkenntnisse und Anwendungen M 12 Tippkarten Die Erläuterungen und Lösungen zu den Materialien finden Sie ab Seite 20. 26 RAAbits Physik Februar 2012 4. Grundlagen der Quantenphysik M1 7 von 28 Das Wasserstoffspektrum – die Balmerserie bestimmen Lehrerversuch/Schülerversuch · Vorbereitung: 10 min Durchführung: 30 min Materialien rBalmerlampe rMaßband oder Tafellineal rGitter mit 600–1000 Linien/mm rFarbkreide Ziel des Versuches Bestimmen Sie die Wellenlängen der Balmerserie des Wasserstoffatoms. Versuchsaufbau Balmerlampe und Gitter werden so auf dem Pult aufgebaut, dass die Gerade vom Gitter zur Lampe senkrecht zur Tafelebene steht. II/E T H C I S N A R O V Versuchsdurchführung Sie schauen durch das Gitter, um die Balmerlampe und das Spektrum der Lampe zu sehen. Gehen Sie mit dem Auge sehr nah heran. Anschließend arbeiten Sie zu zweit im Team. Während einer von Ihnen durch das Gitter schaut und die Lage der virtuellen Bilder der Lampe vor der Tafel beschreibt, macht der andere an der Tafel an den entsprechenden Stellen einen farbigen Strich. Achten Sie darauf, dass alle Tafelstriche genau über den virtuellen Bildern liegen. Bewegen Sie dazu den Kopf leicht hin und her. Ein dritter Schüler kann zur Kontrolle durch das Gitter schauen. Auswertung Zunächst ist der Gitterabstand d aus der Anzahl der Linien pro mm zu bestimmen. Messen Sie dann den Abstand b des Gitters zur Tafel und für jeden Strich einer Spektrallinie den jeweiligen Abstand a zum Bild der Lampe an der Tafel. Aus den Längen b und a wird der Beugungswinkel und die entsprechende Wellenlänge bestimmt. Dabei gilt: λ a sin(α) = und tan(α) = (siehe Graik) d b Stellen Sie die Ergebnisse für die verschiedenen Linien in einer Tabelle zusammen. 26 RAAbits Physik Februar 2012 4. Grundlagen der Quantenphysik 8 von 28 M2 Die De-Broglie-Wellenlänge – eine Revolution Heute, da wir viel über die Quantennatur der Elementarteilchen wissen, scheint es uns einfach, de Broglies Gedanken nachzuvollziehen. Damals war es ein revolutionärer Schritt. Foto: Süddeutsche Zeitung In seiner Doktorarbeit „Recherches sur la théorie des quanta“ (Untersuchungen zur Quantentheorie)1 veröffentlichte Louis de Broglie 1924 einen völlig neuen Gedankengang. Aufbauend auf Einsteins Arbeiten zur Relativitätstheorie – unter anderem der Forderung, dass Photonen den Charakter von Teilchen haben – postulierte er, dass der Welle-Teilchen-Dualismus auch für massebehaftete Elementarteilchen gelten solle. Schon 1927 gelang Davisson und Germer der experimentelle Nachweis der Wellennatur von Elektronen durch Beugungsversuche. 1929 erhielt de Broglie für seine Arbeit den Nobelpreis für Physik. Louis de Broglie II/E T H C Aufgaben: Arbeiten Sie de Broglies Gedankengang heraus! 1. Impuls eines Photons Zeigen Sie, dass sich aus der Einstein’schen Gleichung E = m • c und der Gleichung für die Energie eines Photons E = h • f der Photonenimpuls h pPhoton = m ⋅ c = (I) λ herleiten lässt. Nehmen Sie dafür an, dass Photonen Teilchen mit der Masse m und der Geschwindigkeit v = c sind, und verwenden Sie f = c/λ. I S N 2 A R O 2. De Broglies Wellenlänge für massebehaftete Teilchen V Annahme: Dieser Zusammenhang zwischen Impuls und Wellenlänge gilt auch für alle anderen Teilchen mit Masse m und Geschwindigkeit v. Begründen Sie, dass aus dieser Annahme die de Broglie’sche Wellenlänge h (II) λ= mv für Teilchen mit der Masse m und der Geschwindigkeit v folgt. 3. Stellen Sie die Quanteneigenschaften (Masse, Energie, Impuls, Wellenlänge, Frequenz) von Elektron und Photon in einer Tabelle vergleichend gegenüber. 4. Bestimmen Sie die De-Broglie-Wellenlänge eines Elektrons mit einer a) Geschwindigkeit v = 12 • 104 m/s. b) kinetischen Energie von 1,5 eV. Da diese Energie im Vergleich zur Ruheenergie sehr 1 gering ist, können Sie mit der Formel E = ⋅ m ⋅ v 2 rechnen. 2 5. Damit Elektronen an einem Doppelspalt mit Spaltabstand d = 1,0 µm merklich gebeugt werden, sollte ihre Wellenlänge eine vergleichbare Größenordnung haben. Mit welcher Spannung müssten Elektronen demnach beschleunigt werden, um eine Wellenlänge von 1,0 µm (µm = 10 –6 m) zu haben? 1 L. de Broglie: Recherches sur la théorie des quanta. Dissertation. Masson & Cie, Paris 1924; Ann. Phys. 3 (1925), 22−128. 26 RAAbits Physik Februar 2012 4. Grundlagen der Quantenphysik M3 9 von 28 Das Bohr’sche Atommodell Mit zwei vergleichsweise einfachen Annahmen gelang es Bohr, die Wellenlängen des Wasserstoffspektrums in sehr guter Näherung zu berechnen und so zu erklären. 1. Annahme: Wie bei einer eingespannten Saite passen nur ganzzahlige Vielfache (n-Fache) der De-Broglie-Wellenlänge des Elektrons auf die Kreisbahn um den Kern. Man indet daher nur bestimmte Wellenlängen λn. Auch der Impuls ist quantisiert in Werte pn. n λn = 2 π rn (I) mit λn = h h (II) = pn me vn II/E T H C 2. Annahme: Elektronen beschreiben eine Kreisbahn, die durch die Anziehungskraft zwischen Proton und Elektron, die Coulomb-Kraft, verursacht wird. Daher kann man die Zentripetalkraft gleich der Coulomb-Kraft setzen. I S N me vn2 e2 = (III) rn 4 π ε 0 rn2 A R O Damit ergeben sich drei Gleichungen mit den Unbekannten rn, vn und λn. V Aufgaben 1. Lösen Sie das Gleichungssystem nach rn auf, indem Sie vn und λn eliminieren. Bestimmen Sie die Radien der ersten vier Bahnen (me = 9,11 • 10 −31 kg; ε0 = 8,85 • 10 −12 As/Vm). 2. Bestimmen Sie einen von rn unabhängigen Term für die kinetische Energie des Elektrons auf der n-ten Bahn: 1 Ekin n = me vn2 = ? (IV) 2 3. Vergleichen Sie diesen Term mit der potenziellen Energie des Elektrons im Abstand rn von der Kernladung Q = e. 1 qQ 1 e2 (V) Epot = − =− 4 π ε 0 rn 4 π ε 0 rn Zum Vorzeichen: Einem Elektron muss man Energie zuführen, um es vom Kern zu lösen. Im feldfreien Raum weit weg vom Kern soll es eine potenzielle Energie von null haben. Daher muss die potenzielle Energie in der Nähe des Kerns negativ deiniert sein. 4. Bestimmen Sie nun die Gesamtenergie Eg = Ekin + Epot der Elektronen für die ersten vier Bahnen. Berechnen Sie die Energien in Elektronenvolt (eV) [1 eV = 1,602 • 10 −19 J]. 5. Überlegen Sie, welche Bedeutung diese immer noch negativen Energiewerte haben. 26 RAAbits Physik Februar 2012 4. Grundlagen der Quantenphysik 10 von 28 M4 Arbeiten mit dem Potenzialdiagramm Der Energieerhaltungssatz besagt, dass sich die Gesamtenergie eines energetisch abgeschlossenen Systems nicht ändert, die Gesamtenergie also eine charakteristische Größe eines physikalischen Systems ist. Sehr wohl ändern kann sich allerdings der Anteil der potenziellen und kinetischen Energie. Betrachten Sie hierzu ein Federpendel. Eine Kugel mit der Masse m schwinge entlang der x-Achse mit der Amplitude A. Die potenzielle Energie der Masse ist dabei vom Ort abhängig. Sie ist umso größer, je weiter die Feder ausgelenkt ist. Es gilt: 1 Epot (x) = D x2 2 Im nebenstehenden Potenzialdiagramm stellt sich dies folgendermaßen dar: II/E Der Abstand von der Ruhelage gibt die potenzielle Energie vor, die bis zur maximalen Auslenkung (Amplitude A) zunimmt und bei A der Gesamtenergie Eg entspricht. T H C Bei allen anderen Orten ergibt sich Ekin als Differenz zwischen Eg und Epot. Aufgaben I S N Ein Teilchen der Masse m beinde sich in dem iktiven Potenzial, das im nebenstehenden Potenzialdiagramm dargestellt ist. Es soll jeweils Gesamtenergien von 0 J, 20 J, 30 J oder 40 J haben. A R O 1. Bestimmen Sie für die gegebenen Gesamtenergien aus der Graik näherungsweise die potenzielle und die kinetische Energie für die gegebenen Orte zwischen 0 m und 4 m. Tragen Sie die Ergebnisse in den nachfolgenden Tabellen ein. V 2. In welchem Bereich kann sich das Teilchen mit der jeweiligen Gesamtenergie aufhalten? Eg = 0 J x [m] Eg = 20 J 0 1 2 4 x [m] Epot [J] Epot [J] Ekin [J] Ekin [J] Eg = 30 J Eg = 40 J x [m] 0 1 2 4 x [m] Epot [J] Epot [J] Ekin [J] Ekin [J] 26 RAAbits Physik Februar 2012 0 1 2 4 0 1 2 4 4. Grundlagen der Quantenphysik M5 11 von 28 Das Potenzialdiagramm des Wasserstoffs Die Gesamtenergie des Elektrons im Wasserstoffatom für einen bestimmten Bahnradius rn beträgt nach M 3: 1 e2 Eg = − 8 π ε 0 rn Ihr Verlauf ist im folgenden Diagramm dargestellt. II/E T H C I S N Aufgaben 1. Übernehmen Sie die Werte für die Radien rn und die entsprechenden Gesamtenergien aus M 3. Tragen Sie diese als vertikale bzw. horizontale Linien in das Diagramm ein. Die Linien repräsentieren die verschiedenen Energiezustände im Wasserstoffatom. A R O Im Grundzustand ist das Elektron im Mittel etwa 0,5 • 10 −10 m vom Atomkern entfernt. Je größer seine Energie ist, desto weiter kann es sich vom Kern fortbewegen. V Wechselt ein Elektron seine Bahn von größeren zu kleineren Energiewerten, so gibt es die überschüssige kinetische Energie in Form von Lichtquanten entsprechender Wellenlänge ab. Die Spektrallinien der Balmerserie des Wasserstoffspektrums kommen zustande, wenn Elektronen aus der 3., 4. … n-ten Bahn auf die 2. Bahn fallen und ihre Energie als Photon abgeben. Die Energien der Photonen können durch: EPh = En – E2 mit n > 2 bestimmt werden: 2. a) Tragen Sie die Übergänge der ersten drei Linien der Balmerserie als farbige Pfeile in das Potenzialdiagramm ein. Bestimmen Sie die Energien dieser Übergänge. E32 = E3 – E2 = eV; E42 = eV; E52 = eV E5 = –0,54 eV b) Mit E = h • f = h ⋅ λ32 = c können Sie schließlich die Wellenlängen der Photonen bestimmen. λ nm; λ 42 = nm; λ 52 = nm h = 6,626 • 10 –34 Js und 1 J = 0,6242 • 1019 eV ⇒ h = 4,14 • 10 –15 eVs und h • c = 1,24 • 10 –6 eVm 26 RAAbits Physik Februar 2012 4. Grundlagen der Quantenphysik M7 13 von 28 Die Differenzialgleichung des harmonischen Oszillators Erinnern Sie sich an das Gesetz von Hooke? Zieht an einer Feder eine Kraft, so wird die Feder gedehnt. Je größer die Kraft F ist, desto größer ist die Dehnung x. Wie gut sich eine Feder dehnen lässt, gibt die Richtgröße D der Feder in N/m an. Es gilt: F (x) = –D • x . Die Kraft ist hier also eine vom Ort x abhängige Größe. Sie ist der Dehnungsrichtung entgegengerichtet. Allgemein gilt für eine Kraft F = m • a . Jede Kraft, die auf eine Masse wirkt, ruft eine entsprechende Beschleunigung hervor. Hieraus folgt: Zusammenhang zwischen Kraft und Beschleunigung: m • a = –D • x (I) Die Beschleunigung a ist die momentane Änderung und damit die Ableitung der Geschwindigkeit nach der Zeit: ∆v v(t + ∆ t) − v(t) • a = lim = lim = v ∆ t→ 0 ∆ t ∆ t→ 0 ∆t ∆x x(t + ∆ t) − x(t) • Ebenso: v = lim = lim = x ∆ t→ 0 ∆ t ∆ t→ 0 ∆t II/E T H C I S N Beides zusammen ergibt, dass die Beschleunigung die Änderung der Änderung des Ortes . Dabei wird mit den Punkten über und damit zweite Ableitung nach der Zeit ist: a(t) = x(t) eine Schreibweise für die Ableitung nach t verwendet, die dem f ′(x) und f ′′(x) v und x für die Ableitungen nach dem Ort x entspricht. A R O Gleichung (I) lautet (, wenn man den vektoriellen Charakter der Größen vernachlässigt): D = − D x(t) bzw. mx(t) x(t) = − x(t) m V Diese Gleichung stellt einen Zusammenhang zwischen dem Ort x(t) und der 2. Ableitung her. Sie besagt, dass die Funktion x(t) von der Variablen t abhängt und mit der Funkx(t) tion x(t) bis auf das Vorzeichen und eine Konstante D/m identisch ist. Eine solche Gleichung, die einen Zusammenhang zwischen einer Funktion und ihrer Ableitung herstellt, nennt man Differenzialgleichung (DGL). Lösung einer DGL ist nicht ein Wert oder eine Wertemenge, sondern die Menge der Funktionen, die die Differenzialgleichung erfüllen. Funktionen, die beim zweimaligen Ableiten bis auf ein Minus (und eine Konstante) sich selbst ergeben, kennen Sie. Es sind die Sinus- und Kosinusfunktion. Aufgaben 1. Formulieren Sie die Zeit-Orts-Funktion x(t) als Sinusfunktion so, dass sie die obige DGL erfüllt. Modifizieren Sie die Sinusfunktion dafür so, dass durch zweimaliges Differenzieren die Konstante D/m vor der Funktion entsteht. Die Sinusfunktion einer Schwingung beschreibt man durch den Ausdruck 2π x(t) = A sin( t) mit der Amplitude A und der Periodendauer T. T 2. Stellen Sie einen Zusammenhang zwischen D, m und T her. Richtgröße und Masse legen so die Periodendauer und damit die Frequenz der Schwingung fest. 3. Begründen Sie, dass für alle Funktionen x(t), die die DGL erfüllen auch A • x(t) eine Lösung der DGL ist. 26 RAAbits Physik Februar 2012 4. Grundlagen der Quantenphysik 14 von 28 M8 Für Experten: Die Schrödingergleichung II/E In der Kopenhagener Deutung der Quantenmechanik einigten sich 1927 Niels Bohr und Werner Heisenberg darauf, dass man das Quadrat dieser Wellenfunktion als Aufenthaltswahrscheinlichkeit eines Quants interpretieren kann. Foto: picture-alliance/dpa 1926, schon zwei Jahre nach de Broglies Postulat der Materiewellen, gelang es Erwin Schrödinger, das Verhalten einer Materiewelle in einem gegebenen Potenzial mathematisch zu beschreiben und zu erklären. Schrödinger griff das revolutionäre Konzept der Materiewelle auf und wendete die Gesetzmäßigkeiten der mechanischen und elektromagnetischen Wellenphysik darauf an. Der Quantenzustand im Topf mit der de Broglie’schen Wellenlänge λ wird demnach durch eine Materiewelle der Form 2π Ψ(x) = A • sin ( • x) λ beschrieben. Erwin Schrödinger (1887–1961) T H C Bis heute wurde diese Annahme durch viele Messungen an den unterschiedlichsten Quantensystemen immer wieder belegt. Das Ergebnis von Schrödingers Arbeit war die heute nach ihm benannte Differenzialgleichung. Diese Gleichung ermöglicht es, sowohl die Energien als auch die Aufenthaltswahrscheinlichkeiten der Quantenzustände in einem bestimmten Potenzial zu berechnen. I S N Aufgaben 2π • x). λ Erstellen Sie damit eine Differenzialgleichung der Form Ψ’’(x) = –k² Ψ(x). 1. Bestimmen Sie die 2. Ableitung von Ψ(x) = A • sin ( A R O Welchen Wert hat der Faktor k? V 2. Eliminieren Sie nun mit Ekin = p2 2m und dem Impuls p = Differenzialgleichung. h die Wellenlänge aus der λ Zeigen Sie damit, dass gilt: Ψ ′′(x) = − 8 π2 m Ekin Ψ(x) h2 3. Zeigen Sie, dass man diese Gleichung mit dem Zusammenhang Ekin = Eg – Epot schreiben kann als: Eg Ψ(x) = − h2 Ψ ′′(x) + Epot Ψ(x) 8 π2 m Dies ist die (zeitunabhängige) Schrödingergleichung, die Grundgleichung der Quantenmechanik. Ihre Lösungen sind die stationären Eigenzustände Ψn(x). Deren Betragsquadrat beschreibt die Aufenthaltswahrscheinlichkeit eines massebehafteten Quantenobjektes am Ort x, das in dem gegebenen Potenzial gebunden ist. Sie gilt in dieser Form nicht für Photonen, die keine Ruhemasse m haben und beschreibt keine zeitliche Entwicklung des Systems. 26 RAAbits Physik Februar 2012 4. Grundlagen der Quantenphysik 19 von 28 M 12 Tippkarten M 3 Das Bohr’sche Atommodell Tipp 1 Zeigen Sie, dass vn = hn e2 und rn = me 2 π rn 4 π ε 0 me vn2 gilt. Setzen Sie dann vn in rn ein. Tipp 2 Setzen Sie vn in Ekin und rn in Epot ein. Vergleichen Sie die Terme nach dem Vereinfachen. M 6 Der unendlich tiefe Potenzialtopf Tipp 1 Bei einer stehenden Welle passen immer n halbe Wellenlängen zwischen die zwei festen Enden. Überlegen Sie, wie die Wellenlänge und die Topfbreite zusammenhängen müssen, damit diese Bedingung erfüllt ist. Tipp 2 Gehen Sie von der kinetischen Energie aus, erweitern Sie mit der Masse m. T H C Ersetzen Sie dann den Impuls nach de Broglie durch p = h / λ. I S N M 7 Die Differenzialgleichung des harmonischen Oszillators Tipp Leiten Sie die allgemeine Sinusfunktion x(t) = A • sin (k • t) zweimal ab. Vergleichen Sie beide Funktionen mit der Differenzialgleichung, um k zu bestimmen. A R O V Gleichen Sie dann Ihren Ausdruck für k mit der allgemeinen 2π Beschreibung einer Schwingung x(t) = A sin( t) ab. T M 8 Für Experten: Die Schrödingergleichung Tipp 1 Zeigen Sie, dass λ 2 = h2 gilt. 2mEkin Setzen Sie diesen Ausdruck in Ihr Ergebnis für k 2 in der DGL ein. Tipp 2 II/E Ersetzen Sie Ekin gemäß der Gleichung Eg = Ekin + Epot durch Eg – Epot und lösen Sie die Gleichung schrittweise nach Eg auf. M 9 Der Tunneleffekt beim endlich tiefen Potenzialtopf Tipp zu 5. Leiten Sie folgende Funktionen zweimal ab: Ψ ( x) = A cos (k x) ; Ψ ( x) = A ek x ; Ψ ( x) = A e−k x ; Ψ ( x) = A xk und vergleichen Sie mit der Differenzialgleichung Ψ ′′(x) = k 2 Ψ(x) . Begründen Sie, warum nur Ψ ( x) = A e−k x im äußeren Bereich eine sinnvolle Lösung ist. 26 RAAbits Physik Februar 2012 4. Grundlagen der Quantenphysik 20 von 28 Erläuterungen und Lösungen M1 Das Wasserstoffspektrum – die Balmerserie bestimmen Ziel des Experimentes ist es, die Wellenlängen der Linien der Balmerserie des Wasserstoffs zu bestimmen. Führen Sie diesen Versuch als Demonstrationsexperiment mit reger Schülerbeteiligung durch. Beachten Sie, dass einige feine optische Gitter eine Vorzugsrichtung haben, sodass das linke oder das rechte Interferenzbild deutlich stärker ausgeprägt sind. Schauen Sie in beiden Richtungen durch das Gitter und vergleichen Sie die Helligkeit. Bild der Spektrallinien an der Tafel II/E T H C I S N A R O V Sie stellen die Balmerlampe dazu auf dem Pult auf. Im Abstand von circa 1 m davor platzieren Sie ein Gitter in einem entsprechenden Halter so, dass die Gerade, auf der Gitter und Lampe liegen, senkrecht zur Tafel steht. Schauen Sie nun schräg durch das Gitter, so können Sie im Raum das Wasserstoffspektrum als mehrfaches virtuelles Bild der Gasentladungsröhre in den verschiedenen Farben beobachten. Guten Schülern können Sie mitteilen, dass es sich tatsächlich um das Spektrum des atomaren Wasserstoffs handelt. Denn in der Balmerlampe ist Wasserdampf, dessen Moleküle durch die elektrische Entladung in ein H+ und ein OH – -Ion aufgespalten werden. Das H+ leuchtet bei der Rekombination mit einem Elektron zu atomarem Wasserstoff. Rege Schülerbeteilung Zunächst lassen Sie alle Schüler durch das Gitter schauen. Als Lehrkraft stellen Sie sich am besten vor die Tafel an den Platz des Bildes, sodass die Schüler zu Ihnen in die richtige Richtung schauen. Die Schüler zeichnen einen Kreidestrich an der jeweiligen Position in der jeweiligen Farbe der Linie an die Tafel. Ein Schüler schaut dazu durch das Gitter und dirigiert, der andere zeichnet den Strich. Ein dritter Schüler kontrolliert die Richtigkeit des Striches. Sind alle Striche – das 0. Maximum und jeweils ein Strich für die drei oder vier Balmerlinien (n = 2) – gezeichnet, erfolgt die Ausmessung. Lassen Sie jeweils zwei Schüler mit einem Maßband den Abstand b und die verschiedenen Längen a messen und in eine Tabelle eintragen. 26 RAAbits Physik Februar 2012