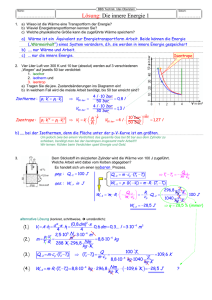
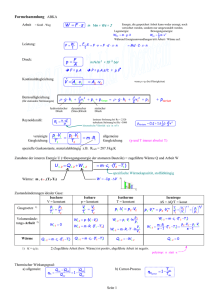
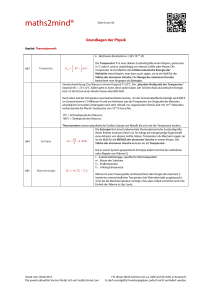
Folien vom 13.3.
Werbung

34 2. Hauptsatz der Thermodynamik 2. Hauptsatz der Thermodynamik Einem makroskopischen System im Gleichgewicht kann Ei k k i h S t i Gl i h i ht k die Zustandsfunktion Entropie S zugeordnet werden, für die gilt: 1. Die Entropie ist extensiv. 2. Bei reversibler Transformation ist die zugeführte Wä Wärme δQ δQ mit der Entropieänderung it d E t i ä d dS verknüpft k ü ft durch : „Integrierender Faktor“ : „Integrierender Faktor 3. Die Entropie eines isolierten Systems kann niemals abnehmen. Jeder reale Prozess läuft von selbst so lange ab, bis die Entropie ein Maximum erreicht. 35 Für die Energie E(S,V,N) folgt daraus bei reversibler Zustandsänderung: für reversible ü e e sbe Prozesse Mit 36 E l Gl i h Euler Gleichung Vergrößerung eines Systems um Faktor Vergrößerung eines Systems um Faktor Für extensive Variablen gilt: Die Energie ist eine homogene Funktion ersten Grades. Zum Vergleich: Fundamentalgleichung in differentieller Form Fundamentalgleichung 37 Kreisprozesse: idealisierte Wärmekraftmaschinen • Beispiel: Carnot Prozess für ideales Gas 1 → : isotherme Expansion 2 1 isotherm 2 adiabatisch di b i h Arbeit wird vom System geleistet 3 Wärme wird dem System zugeführt 2 → : adiabatische Expansion 3 1 2 3 38 Kreisprozesse: idealisierte Wärmekraftmaschinen • Beispiel: Carnot Prozess für ideales Gas 3 → : isotherme Kompression 4 1 Arbeit δW<0 isotherm adiabatisch 2 4 adiabatisch di b i h isotherm 4 → : adiabatische Kompression 1 3 Wärme δQ>0 Wärme δQ>0 1 2 4 3 39 Bilanzgleichungen: Insgesamt geleistete Arbeit: l i b i die beiden isothermen Prozesse Prozess 2→ 3 Prozess 4→ 1 Insgesamt zugeführte Wärme: Wirkungsgrad= geleistete Arbeit geleistete Arbeit zugeführte Wärme