4.2 Grundzüge des Kohlenhydratstoffwechsels
Werbung

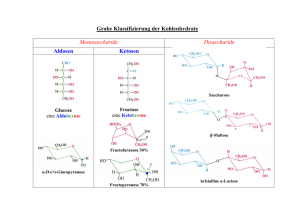
Grundzüge des Kohlenhydratstoffwechsels • 4.2 Grundzüge des Kohlenhydratstoffwechsels – 4.2.1 Mono-, Oligo- und Polysaccharide Funktionen der Kohlenhydrate • Kohlenhydrate erfüllen im Organismus zahlreiche wichtige Funktionen: – Brennstoff und Energiespeicher – Metabolite – Bausteine von DNA und RNA – Strukturbausteine – Teile von Funktionseinheiten der Zell-ZellKommunikation – Usw. Struktur der Kohlenhydrate • Bezeichnung Kohlenhydrate umfasste ursprünglich Verbindungen der Summenformel Cn(H2O)n • Es gibt allerdings auch Kohlenhydrate anderer Zusammensetzung (Bsp.:Desoxyribose) • Nomenklatur unterscheidet – Monosaccharide • 3-9 C-Atome – Disaccharide • 2 Monosaccharide – Oligosaccharide • 3-20 Monosaccharide – Polysaccharide • >20 Monosaccharide – Dabei sind die einzelnen Monosaccharide über sog. Glykosidische Bindungen verknüft Monosaccharide • Monosaccharide sind die Aldehyde bzw. Ketone von mehrwertigen Alkoholen – Aldosen – Ketosen • Abhängig von der Anzahl der Kohlenstoffatome (3-9) gibt es Triosen, Tetrosen, Pentosen, Hexosen, usw. Konfiguration und optische Drehung • Die Absolutkonfiguration erfolgt nach Emil Fischer anhand des Glycerinaldehyds, dessen Enantiomerenpaar als Referenz für alle anderen Zucker dient. • Das D-Glycerinaldehyd ist rechtsdrehend, das LGlycerinaldehyd linksdrehend. • Absolutkonfiguration und Drehsinn hängen nicht miteinander zusammen! Stereochemie der Monosaccharide • Monosaccharide mit 4, 5, 6 und 7 C-Atomen werden als Tetrosen, Pentosen, Hexosen und Heptosen bezeichnet • sie besitzen viele asymmetrische C-Atome, kommen als Diastereomere vor (Isomere, die nicht wie Enantiomere Bild und Spiegelbild zueinander sind) • Symbole D und L bezeichnen die absolute Konfiguration des asymmetrischen C-Atoms, das am weitesten von der Aldehyd-oder Ketogruppe entfernt ist • Epimere sind KH, die sich nur an einem asymmetrischen CAtom unterscheiden: z.B. D-Glucose/D-Mannose (C-2 Epimere) oder D-Glucose/D-Galaktose (C-4 Epimere) D-Aldosen D-Ketosen Beispiel: Enantiomere der Glucose Beispiel: Diastereomere der D-Glucose Die Diastereomere werden durch ihre Namen, die Enantiomerenpaare durch die Präfixe L-/D- unterschieden. Zyklisierung • Pentosen und Hexosen zyklisieren intramolekular unter Bildung eines Halbacetals bzw. eines Halbketals • Abhängig davon, welche Atome reagieren, bildet sich die Furanose- oder Pyranose-Form Pyranosen • Durch intramolekularen Ringschuluss zwischen C1 und C5 • C1 wird asymmetrisch Anomere (α-/β-Form): – α-Form: OH-Gruppe unterhalb der Ringebene – β-Form: OH-Gruppe überhalb der Ringebene • Einstellung eines Gleichgewichts zwischen den beiden Anomeren durch Mutarotation – α-D-Glucose in Lösung ergibt 36% α-D-Glucose und 64% β-D-Glucose Furanosen • Durch intramolekularen Ringschluss zwischen C2 und C5 • Anomerbildung und Mutarotation analog zu den Pyranosen • Sowohl Ketosen als auch Aldosen können Furanose- und Pyranoseformen eingehen. Meist ist allerdings eine Form stabiler. • Beispielsweise liegt Fructose ungebunden meist in Pyranoseform vor, gebunden jedoch als Furanose. Keto-Enol-Tautomerie der Fructose Redoxverhalten von Kohlenhydraten • Nachweisreaktion mit Fehlingscher Lösung (Cu2+-Tartratkomplex), Tollens Reagenz (Ag+) – Zucker mit freier CHO-Gruppe bezeichnet man als reduzierende Zucker – Modifiziere Zucker, die nicht in eine Form mit freier CHO-Gruppe umgewandelt werden können, bezeichnet man als nichtreduzierende Zucker Phosphorylierte Monosaccharide • Kinasen (Hexokinase I-III, Hexokinase IV = Glucokinase) übertragen Phosphoryl-Rest auf C6Atom der Glucose • Gründe: • Negative Ladung verhindert den Membranübergang • Aktivierung für weitere Metabolisierung Glycosidische Bindung • Sehr reaktive OH-Gruppe am Halbacetal/-ketal Di-, Oligo-, & Polysaccharide • entstehen durch glykosidische Verknüpfung mehrerer Monosaccharide. • Zur genauen Definition sind wichtig: – Monosaccharid-Bausteine? • Welches Monomer? • Anomerenform (α-/β-Form)? – Welche OH-Gruppe des jeweils folgenden Zuckers geht die glycosidische Bindung ein? – Verknüpft/Unverknüpft? – Eventuell noch andere Bausteine außer Zuckern? Disaccharide • Saccharose – α-1,2-glykosidisch verknüpft – Aus Zuckerrohr und Zuckerrüben – Nichtreduzierend • Lactose – β-1,4-glykosidisch verknüpft – Zucker der Milch – Reduzierend • Maltose – α-1,4-glykosidisch verknüpft – Abbauprodukt von Stärke – Reduzierend Polysaccharide • Gerüstpolysaccharide – Cellulose • Homopolymer (nur Glucose) • β-1,4 glykosidisch verknüpft lange, unverzweigte Ketten • Speicherpolysaccharide – Stärke • Speicherpolysaccharid der Pflanzen • Homopolymer (nur Glucose) • 2 Formen: – Amylose (α-1,4-glykosidisch verknüpft unverzweigt) – Amylopektin (neben α-1,4 auch ca. alle 30 Glucoseeinheiten α-1,6 verknüpft) Polysaccharide • Speicherpolysaccharide – Glykogen • Speicherpolysaccharid der Tiere • Homopolymer (nur Glucose) + Glykogenin (Protein) • Ähnlich dem Amylopektin neben α-1,4 auch ca. alle 10 Glucoseeinheiten α-1,6 verknüpft • Vorteil der Speicherform als Glykogen: – Osmotisch wirksame Monomere werden in osmotisch wenig wirksame Polymere umgewandelt – Verzweigungen erlauben im Fall von Energiemangel den gleichzeitigen Abbau von Glucose-Einheiten an mehreren Stellen des gleichen Glykogen-Moleküls. Oligo-/Polysaccharidaufbau • Ein für den Oligo-/Polysaccharidaufbau wichtiger aktivierter Stoff ist Glucose-1Phosphat. • Dieses entsteht unter Einwirkung von Glucose1,6-bisphosphatat als Cosubstrat aus Glucose6-Phosphat. • Das katalysierende Enzym ist Phosphoglucomutase (eine Transferase) • Aus Glucose-1-Phoshat leiten sich die Nukleosiddiphosphat-Zucker ab: – – ADPG (Adenosindiphosphoglucose) UDPG (Uridindiphosphoglucose) • • Cosubstrate sind jeweils ATP/UTP Die Reaktion verläuft unter Abspaltung von Pyrophosphat, welches hydrolytisch in zwei Phosphatreste gespalten wird, wodurch das Gleichgewicht zum ADPG/UDPG hin verschoben wird. • Ab hier unterscheiden sich die Synthesen von Stärke und Glykogen Saccharosesynthese • Charakteristisch für pflanzliche Organismen • Substrate sind UDPG und Fructose bzw. Fructose-6-Phosphat. • Mechanismus: – Glucoserest des UDPG wird auf Fructose bzw. Fructosephosphat übertragen. – Es entsteht Saccharose bzw. Saccharose-Phosphat. – Letzteres wird hydrolytisch zu Saccharose und Phosphat gespalten. Stärkesynthese • Ausgangsverbindung ist ADPG • Das Enzym Stärkesynthase überträgt den Glucose-Rest des ADPG auf ein Startermolekül, welches aus α-1,4verknüpften Glucosemolekülen besteht. • Die Verzweigungen des Amylopektins werden durch ein anderes Enzym eingebaut. • Die Stärkesynthese läuft in den Plastiden ab (Amyloplasten) Stärkeabbau • Durch Amylasen und R-Enzym Amylasen Bestandteile des Speichels sowie des Sekrets des Pankreas α-Amylasen sind Endoamylasen α-1,4-Bindungen Aus Amylopektin entstehen deshalb Isomaltose und sog. Grenzdextrine (werden vom R-Enzym abgebaut) β-Amylasen (rein pflanzlich) sind Exoamylasen α1,4-Bindungen werden unter Invertierung der αBindung gespalten sodass β-Maltose entsteht Glykogenstoffwechsel • Glycogen ist ein wichtiger Energiespeicher des tierischen Organismus. • Alle Körperzellen außer Erythrocyten enthalten Glycogen und können dieses auch selbst synthetisieren • Mengenmäßig am wichtigsten sind Skelettmuskulatur (ca. 1g/100g) und die Leber (ca. 10g/100g) • Insgesamt reicht die Speicherkapazität für 400g Glycogen, welches den Energieverbrauch für ca. 24h deckt. Glycogenbiosynthese • • • • Substrat für die Glycogenbiosynthese ist das UDPG Dabei wird der Glucose-Rest des UDPG unter Abspaltung von UDP auf das C4Atom des letzten Glucose-Monomers eines aus mindestens vier GlucoseEinheiten bestehenden Rest des „Starter“-Glycogens übertragen. Das verantwortliche Enzym ist die Glycogensynthase (UDPGlycogenTransglucosylase). Produkt ist unverzweigtes, 1,4-glycosidisch verknüpftes Glycogen (entspricht der Amylose) Glycogenbiosynthese • Für die Einführung von Verzweigungen wird ein aus 6-7 Glycosyl-Resten bestehendes Ende der Glycogenkette auf das C6-Atom eines anderen Glucose-Restes im Glycogenmolekül übertragen • Das Enzym ist die Amylo-1,4-1,6-Transglycolase (branching enzyme, Verzweigungsenzym) Glykogenbiosynthese • Da die Glycogensynthase immer bereits vorhandenes Glycogen benötigt, kann dieNeubildung eines Glycogenmoleküls durch diesen Mechanismus nicht erklärt werden. • Für die Neubildung ist Glycogenin nötig. • Dieses hat eine Glycosyltransferaseaktivität und kann sich selbst selbst mit UDPG an einem Tyrosyl-Rest glycosylieren. • Das glycosylierte Glycogenin ist dann Substrat für die Glycogensynthase. Glycogenabbau • Der Glycogenabbau erfolgt grob in drei Schritten: – Freisetzung von Glucose-1-Phosphat – Umstrukturierung des Glycogens für weiteren Abbau – Umwandlung von Glucose-1-Phopshat zu Glucose 6Phosphat • Glucose-6-Phosphat kann anschließend weiter metabolisiert werden: – Als Substrat für die Glycolyse – Als Substrat für den Pentosephosphat-Weg – Als freie Glucose ins Blut Glycogenabbau • Für den Glycogenabbau sind vier Enzymaktivitäten nötig: – Eine für die Abspaltung von Glucose-1-Phosphat – Zwei für den Umbau des Glycogens, damit es Substrat für den Abbau bleibt (Verzweigungen) – Eine für die Umwandlung von Glucose-1-Phosphat in Glucose-6-Phosphat • Meist läuft der Glycogenabbau nicht bis auf die Stufe des Glycogenins. Glycogenabbau • Glycogenphosphorylase • Glycogen wird phosphorolytisch und nicht hydrolytisch gespalten, um das ATP zu sparen, das zur Phosphorylierung der Glucose nötig wäre – Phosphorolyse ist die Spaltung einer Bindung unter Einfügung eines Orthophosphat-Restes • Phosphorylase ist Schlüsselenzym bei der Regulierung des Abbaus Glycogenabbau • Bei der phosphorolytischen Spaltung wird Pyridoxalphosphat als prosthetische Gruppe verwendet Glycogenabbau