Genetisches Praktikum 2010 (20160)
Werbung
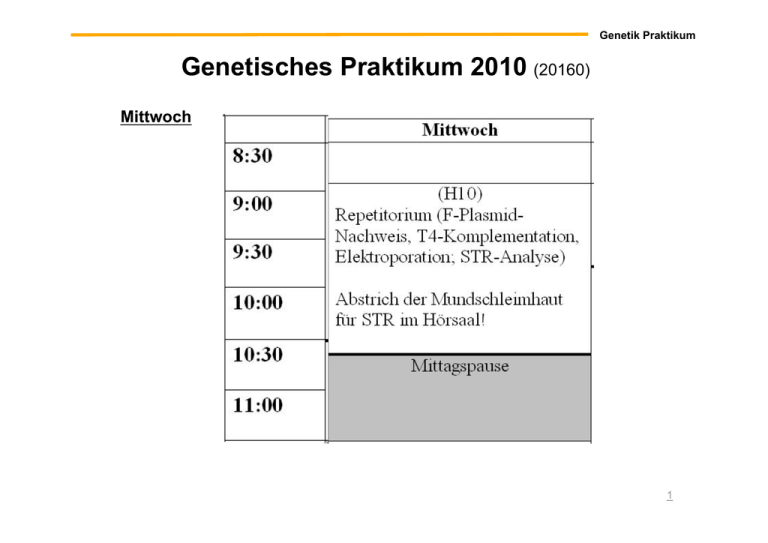
Genetik Praktikum Genetisches Praktikum 2010 (20160) Mittwoch 1 Genetik Praktikum Genetisches Praktikum 2010 (20160) Mittwoch 2 Genetik Praktikum Praktikumsversuche I. Allgemeines A. Plasmid-Curing B. F-Plasmid-Nachweis C. Komplementations-Test mit rII-Mutanten des Phagen T4 D. PCR-Fingerprint mittels STR-Analyse II. Methoden A. Titerbestimmung bei Bakterienkulturen B. !-Galaktosidase-Test III. Mutagenese und DNA-Reparatur A. Isolierung und Identifizierung von Auxotrophie-Mutanten B. Nachweis der Transposon-Mutagenese des Plasmids pTS115 C. Ames-Test IV. Projekt: Klonierung eines Genfragments A. PCR B. Gelelektrophorese C. Ligation D. Elektrotransformation E. Plasmid-Präparation 3 Phagengenetik Genetik der Bakteriophagen •! Bakteriophagen: ‚Bakterienviren‘, infizieren Bakterium und benutzen dessen Maschinerie zur eigenen Vermehrung; Genom in Form von DNA oder RNA (ssDNA, dsDNA linear, dsDNA zirkulär; lineare RNA) z.B. T4 Phage Graw ‚Genetik‘ 4. Aufl. 2006 4 Phagengenetik Lytischer Zyklus des T4-Bakteriophagen 5 Phagengenetik Lytischer Zyklus des T4-Bakteriophagen 6 Phagengenetik host cells ausgehend von einer infizierten Bakterienzelle führt wiederholte intrazelluläre Phagenvermehrung, Wirtszelllyse und Infektion benachbarter Bakterien zu Plaques (= klare Lyse-Höfe) in einem Rasen aus Bakterienzellen 7 Phagengenetik rII-Locus Phagengenetik Lyse S. Benzer (1957): cis-trans Test am rII -Locus von T4 (rIIA, rIIB) Lyse Cistron = genetische Einheit, in der keine Komplementation auftritt Komplementationsgruppe Doppelinfektion mit Phagen verschiedenen Genotyps: keine Lyse keine Lyse 12 Phagengenetik Rekombination in der rII Region von T4 ! durch Mischen mit Phagen bekannter Mutationen können unbekannte Mutationen kartiert werden 13 Phagengenetik virulente Phagen: lysieren die Wirtszelle innerhalb des lytischen Zyklus sofort (z.B. T4) temperente Phagen: können in der Wirtszelle verbleiben, ohne diese abzutöten (z.B. ") Prophage: Integration des Phagen ins Wirtschromosom " lysogenes Bakterium; kann durch Excision des Phagen in den lytischen Zyklus übergehen Bakteriophagen können bakterielle DNA übertragen: Transduktion Unspezifische (generelle) Transduktion: zufälliger Einbau der Wirts DNA in Phagenköpfe eines virulenten Phagen 14 Phagengenetik Unspezifische (allgemeine) Transduktion: zufälliger Einbau der Wirts DNA in Phagenköpfe eines virulenten Phagen kann benutzt werden, um den Abstand von Genen zu bestimmen: Kotransduktion je höher die Kotransduktionsfrequenz, desto geringer der Abstand 15 Phagengenetik Spezifische (spezielle) Transduktion: bei "Ausschneiden" von Prophagen Beispiel Phage ": Integration an bestimmter Stelle im E. coli Chromosom ungenaue Excision ergibt defekten Phagen, der gal oder bio transduziert 16 Phagengenetik 17 Kartierung mit molekularen Markern Kartierung mit molekularen Markern •! phänotypische Merkmale zur Kartierung sind begrenzt " Kartierung / Kopplungsanalyse mit molekularen Markern 1. SNPs: single nucleotide polymorphisms 2. SSLP: short sequence length polymorphisms Single Nucleotide Polymorphisms (SNPs) MboI 5‘ 3‘ . . . T G A C G A T C A A C A G C A T T . . . . . . A C T G C T A G T T G T C G T A A . . . 3‘! 5‘ ! SNP eng gekoppelt mit Erbkrankheit (z.B. cystische Fibrose) 5‘ 3‘ . . . T G A C G C T C A A C A G C A T T . . . . . . A C T G C G A G T T G T C G T A A . . . 3‘! 5‘ Nachweis solcher SNPs? 1. DNA-Sequenzierung 2. RFLP-Analyse wenn Restriktionsschnittstelle betroffen (Restriktionsfragment Längenpolymorphismus) 3. DNA-Chip ! 18 Kartierung mit molekularen Markern Kopplung von Krankheiten und SNPs beim Menschen 19 Kartierung mit molekularen Markern Kartierung von menschlichen Genen mittels SNPs Haplotyp: chromosomaler Abschnitt mit Anordnung von bestimmten SNP Allelen •!humane SNPs haben einen Abstand von ca. 1 kb 20 Kartierung mit molekularen Markern Restriktionsfragment Längenpolymorphismus 21 Kartierung mit molekularen Markern Bsp: RFLP gekoppelt mit einer Erbkrankheit bei Mäusen Ist das dominante Krankheitsallel D mit dem RFLP (Morph) M2 gekoppelt? Testkreuzung: rekombinant Erklärung: 22 Kartierung mit molekularen Markern Kartierung mit Sequenzlängen Polymorphismen •! die meisten eukaryontischen Genome besitzen großen Anteil repetitiver DNA Sequenzen •! repetitive DNA Sequenzen sind unterschiedlicher Natur Humangenom: > 50 % repetitive DNA 3 % Tandemwiederholungen (tandem repeats) Mikrosatelliten (2 – 14 bp) Minisatelliten (15 – 100 bp) 47 % verstreute Wiederholungen (interspersed elements) RNA Transposons 44 % DNA Transposons 3 % LINEs: long interspersed elements SINEs: short interspersed elements SSLPs: simple sequence length polymorphisms: Mikro-, Minisatelliten DNA = VNTRs: variable number of tandem repeats 23 Kartierung mit molekularen Markern Minisatelliten (15 – 100 bp): verstreute Einheiten von Wiederholungen im Genom Anzahl repetitiver Sequenz pro Einheit unterschiedlich Einheiten ergeben Gesamtlänge von 1 – 5 kb DNA fingerprint: •! Restriktion der genomischen DNA (Enzym schneidet nicht in Minisatelliten) •! Southern Blot •! Sonde zur Erkennung der Minisatelliten Sequenz •! DNA fingerprints sind individuell hochgradig verschieden (forensische Analysen) 24 I.D STR-Analyse Mikrosatelliten (2 – 14 bp): in der Regel 2 – 4 bp, die 10 – 100 mal wiederholt auftreten = STR (short tandem repeat) Detektion individueller Mikrosatelliten über PCR mit flankierenden primern bei Verwendung von mehreren Primerpärchen: ‚PCR fingerprint‘ » Anwendung z.B. bei Vaterschaftstests 25 I.D STR-Analyse Brief History of "The Genetic Fingerprint" •! 1980 - Ray White describes first polymorphic RFLP marker •! 1985 - Alec Jeffreys discovers multilocus VNTR probes •! 1985 - first paper on PCR •! 1991 - first STR paper •! 1998 - FBI launches CODIS database I.D STR-Analyse Human Identity Testing – What for? •! Forensic cases -- matching suspect with evidence •! Paternity testing -- identifying father •! Historical investigations •! Missing persons investigations •! Mass disasters -- putting pieces back together •! Convicted felon DNA databases I.D STR-Analyse Steps in DNA Sample Processing Biology DNA Quantitation DNA Extraction PCR Amplification of Multiple STR markers Technology Separation and Detection of PCR Products (STR Alleles) Sample Genotype Determination Genetics Comparison of Sample Genotype to Other Sample Results Generation of Case Report with Probability of Random Match If match occurs, comparison of DNA profile to population databases I.D STR-Analyse Sources of Biological Evidence •! •! •! •! •! •! •! •! Blood Semen Saliva Urine Hair Teeth Bone Tissue I.D STR-Analyse Multiplex PCR •! Over 10 Markers Can Be Copied at Once •! Different Fluorescent Dyes Used to Distinguish STR Alleles with Overlapping Size Ranges •! Commercially available Kits, e.g. PowerPlex™ 16 (Promega, since 2000): power of discrimination: 1 in 2 x 1017 » "Genetic fingerprint" I.D STR-Analyse !"#$%&'()#*&)+,&)-.-/-%0& '1!"#$%&')()'#$&%*'*+,-%!' •! .,%&'/01'2#$3#$4',%1#52'61#!%,'5$&'7$,028%&'65,%,' 9#-:'1%;%5-'0//%$&%1,' •! <%=7#1%,'>?'<@AB'!513%1,' 5$&C01'DE'601%'FG<'!513%1,' I.D STR-Analyse 13 CODIS Core STR Loci and their Chromosomal Positions TPOX TH01: STR auf Chr.11 versch. Allele PCR-Produkt: 146-190 bp D3S1358 D8S1179 D5S818 FGA CSF1PO TH01 VWA D7S820 AMEL D13S317 D16S539 D18S51 D21S11 Amelogenin: Geschlechtsmarker in PAR (pseudoautosomaler Region) X: 106 bp PCR-Produkt Y: 112 bp PCR-Produkt AMEL I.D STR-Analyse 33 I.D STR-Analyse http://www.cstl.nist.gov/strbase 34











