Interaktion mit Wirtszellen – individuell
Werbung

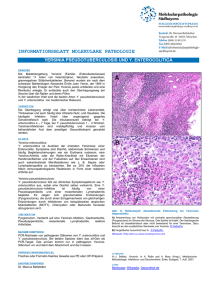
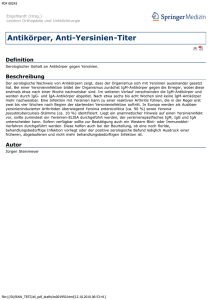
225_261_BIOsp_0307.qxd 25.04.2007 15:28 Uhr Seite 258 WISSENSCHAFT 258 Enteropathogene Yersinien Interaktion mit Wirtszellen – individuell TANJA HEISE UND PETRA DERSCH INSTITUT FÜR MIKROBIOLOGIE, TECHNISCHE UNIVERSITÄT BRAUNSCHWEIG Die enteropathogenen Vertreter der Gattung Yersinia, Y. pseudotuberculosis und Y. enterocolitica, lösen ein weites Spektrum darmassoziierter Krankheiten aus, die von akuter Gastroenteritis mit wässrigem Durchfall bis hin zu ernsten systemischen Infektionen und Folgeerkrankungen wie reaktiver Arthritis reichen. Sie sind weit verbreitet und werden im Boden, auf Nutzpflanzen und in Assoziation mit Insekten gefunden, von welchen sie auf Wild- und Haustiere gelangen. Auf den Menschen werden sie hauptsächlich über verunreinigte Nahrungsmittel übertragen. ó Der erste wichtige Schritt im Infektionsprozess ist die Einwanderung in M-Zellen der Darmepithelschicht. Nach der Durchwanderung dieser Zellen besiedeln die Yersinien die darunter liegenden Lymphfollikel und gelangen durch abfließende Lymphgefäße, oder auch direkt vom Darm, in die mesenterialen Lymphknoten, in die Organe und in wenigen Fällen auch in die Blutbahn[1, 2]. Um eine effiziente Besiedelung zu gewährleisten, besitzen enteropathogene Yersinien unterschiedlich strukturierte oberflächenexponierte Proteine, die eine starke Bindung an verschiedene Zellkomponenten vermitteln und oft auch die Einwanderung in menschliche Zellen ermöglichen. Bisher sind vier adhäsive Faktoren bekannt, die im direkten Zusammenhang mit der Assoziation von YerA sinien an menschliche Zellen stehen: (1) das pH6-Antigen, eine Fimbrien-ähnliche Struktur, (2) das integrale Außenmembranprotein Ail, (3) das Invasin, das die effizienteste Internalisation in Wirtszellen vermittelt und (4) das Yersinia-Adhäsin A (YadA), das neben zellädhäsiven Funktionen autoaggregative und Komplement-protektive Eigenschaften hat[3]. Gleiche Adhäsine – ganz verschieden Invasin und YadA gehören zu den bestuntersuchten bakteriellen Adhäsinen. Die Proteine sind in den enteropathogenen Yersinien konserviert und weisen hohe Sequenzhomologien auf. Doch neue funktionelle Analysen zeigen, dass sie sich in ihren Virulenzeigenschaften sehr unterscheiden. Wie ist das erklärbar? Der an der Oberfläche exponierte B Fn D5 D4 D5 D3 D4 D2 D3 Ko D1 D1 Außenmembran YadA pstb Invasin Y. pstb Y. ent YadA ent YadA Y. pstb Y. ent ˚ Abb. 1: Invasin und YadA-Proteine aus Y. enterocolitica und Y. pseudotuberculosis. A, Strukturelle Unterschiede zwischen den Invasin- und YadA-Molekülen. Die für die Invasion verantwortlichen Domänen sind rot, die Multimerisierungsdomäne im Invasin ist hellblau dargestellt. B, Köpfchendomäne der YadA-Moleküle aus Y. pseudotuberculosis (YadApstb), Y. enterocolitica (YadAent) und ihre Interaktion mit den extrazellulären Matrixproteinen Fibronektin (Fn) bzw. Kollagen (Ko). Anteil des Invasins aus Y. pseudotuberculosis bildet eine 18 nm lange Einheit aus fünf aufeinander folgenden Domänen D1–D5 aus[4] (Abb. 1A). Die Domänen D4/D5 stellen dabei die eigentliche Adhäsions- und Invasionseinheit dar und vermitteln eine hochaffine Bindung an αβ1-Integrinrezeptoren der Wirtszelle. Die Effizienz der Internalisation wird noch deutlich durch die Domäne D2 gesteigert, die eine Multimerisierung von Invasinmolekülen in der bakteriellen Außenmembran bewirkt und ein „Clustering“ von αβ1Integrinrezeptoren in der Wirtszellmembran induziert[5]. Sehr wahrscheinlich werden dadurch Signaltransduktionswege verstärkt, die zur Umlagerung des Zellzytoskeletts führen und den Invasionsvorgang einleiten. Das Invasin aus Y. enterocolitica ist dem aus Y. pseudotuberculosis sehr ähnlich, doch ist sein extrazellulärer Anteil deutlich kürzer (14 nm), da die Domäne D2 fehlt (Abb. 1A). Dies hat zur Folge, dass das Y. enterocolitica-Invasin zwar noch effizient an Wirtszellen bindet, doch weniger effizient invadieren kann[6]. Noch deutlichere funktionelle Unterschiede findet man zwischen den hoch-homologen YadA-Proteinen. Das YadA aus Y. enterocolitica bildet 23 nm lange homotrimere Oberflächenstrukturen, die eine lollipop-Struktur mit einer Stiel- und Köpfchendomäne ausbilden[7]. Das Y. pseudotuberculosis-YadA scheint ähnlich strukturiert zu sein. Es besitzt einen kürzeren Stiel und bildet ein etwas größeres Köpfchen aus. Beide YadA-Moleküle weisen allerdings fundamentale Unterschiede in ihrem Aggregationsverhalten und ihrer Spezifität für extrazelluläre Matrixproteine auf, und nur YadA von Y. pseudotuberculosis, nicht aber von Y. enterocolitica, kann die Internalisation in bestimmte humane Epithelzellen (z. B. HEp-2) auslösen[8]. Neue Untersuchungen haben gezeigt, dass diese drastischen Unterschiede durch eine kurze Aminosäureabfolge bestimmt werden, die im Köpfchenbereich von YadA aus Y. pseudotuberculosis vorhanden ist, dem YadA aus Y. enterocolitica aber fehlt (Abb. 1). Diese Domäne vermittelt eine starke Bindung an Fibronektin-gebundene α5β1-Integrine und ist essenziell für die Initiation des Aufnahmeprozesses. Wird dieses Motiv entfernt, so werden alle EigenBIOspektrum | 03.07 | 13. Jahrgang 225_261_BIOsp_0307.qxd 25.04.2007 15:28 Uhr Seite 259 259 schaften des YadA-Proteins aus Y. enterocolitica generiert. Das Molekül verliert seine starken Aggregationseigenschaften, seine Bindefähigkeit an Fibronektin und seine Invasivität. Dagegen kann es weitaus besser mit den extrazellulären Matrixproteinen Laminin und verschiedenen Typen von Kollagen interagieren, die an β1-Integrine mit einer anderen α-Kette gebunden sind[8] (Abb. 1B). Es ist unklar, was dazu geführt hat, dass Y. enterocolitica und Y. pseudotuberculosis zwei homologe Adhäsine besitzen, die sich in ihren adhäsiven und invasiven Eigenschaften so deutlich unterscheiden. Sicherlich haben diese Unterschiede Konsequenzen für den Verlauf der Infektion. In der Tat scheint Y. pseudotuberculosis das Wirtsgewebe schneller zu besiedeln, da ein besserer Durchtritt durch die Darmepithelschicht mittels der invasiveren Invasin- und YadA-Proteine möglich ist. Die unterschiedlichen Aggregations- und Zellbindeeigenschaften von YadA könnten auch dazu führen, dass verschiedene Orte im Gewebe durch Y. pseudotuberculosis und Y. enterocolitica besiedelt werden, und könnten Einfluss darauf nehmen, in welcher Form sich die Bakterien dort vermehren. Y. enterocolitica ist generell extrazellulär in tiefer liegenden Geweben zu finden, und die Besiedelung führt häufig zur Bildung von Abszessen, die eine große Anzahl von Bakterien beinhalten[9]. Bei Y. pseudotuberculosis-Infektionen hingegen findet man häufig nur kleine Mikrokolonien, die tief und gleichmäßig im Gewebe verteilt sind (Abb. 2A). Optimal abgestimmte Expression In Y. pseudotuberculosis wird zu Beginn der Infektion nur das Invasin-Protein produziert, das eine schnelle Durchwanderung des Darmtrakts ermöglicht. Bereits nach wenigen Stunden kann man jedoch kein Invasin mehr in den Bakterien im Darm und in tieferen Geweben der infizierten Mäuse nachweisen. Umgekehrt ist dann aber eine stark induzierte Synthese des YadA-Proteins zu beobachten (Abb. 2A). Wir haben in den letzten Jahren Komponenten identifiziert, die die Expression der Adhäsine kontrollieren und konnten zeigen, dass Invasin und YadA entgegengesetzt reguliert sind, und je nach Umwelteinfluss (z. B. Temperatur) entweder das eine oder das andere Adhäsin exprimiert wird[10]. Sowohl das Invasin- als auch das YadA-Gen unterliegen dabei der Kontrolle durch ein komplexes Netzwerk, das auf transkriptionaler und posttranskriptionaler Ebene fungiert und verschiedene Transkriptionsfaktoren BIOspektrum | 03.07 | 13. Jahrgang ˚ Abb. 2: Expression von YadA und Invasin in Y. pseudotuberculosis. A, Kolonisation von Y. pseudotuberculosis im Lebergewebe der Maus. Die YadA-Expression auf der Oberfläche der Bakterien wurde mit spezifischen und FITC-markierten Antikörpern sichtbar gemacht. B, Regulatorisches Netzwerk der miteinander gekoppelten Invasin- und YadA-Expression. (+) positiver, (-) negativer Einfluss; ncRNA: regulatorische RNA. (RovA, RovM), Nucleoid-assoziierte Proteine (H-NS, YmoA), kleine regulatorische RNAs und Proteasen (ClpP, Lon) beinhaltet[11, 12] (Abb. 2B). Dieses Regulationssystem scheint nicht nur die Expression früher und später Virulenzgene aufeinander abzustimmen, sondern auch mit der Expression bestimmter Stoffwechselwege, der Biofilm-Bildung und der Motilität zu koordinieren, um die bakterielle Fitness für die Initiation und Persistenz der Infektion zu optimieren. ó Literatur [1] Bottone, E. J. (1997): Yersinia enterocolitica: the charisma continues. Clin. Microbiol. Rev. 10: 257–276. [2] Barnes P., Bergman, M. A., Mecsas, J., Isberg, R. R. (2006): Yersinia pseudotuberculosis disseminates directly from a replicating bacterial pool in the intestine. J. Exp. Med. 203: 1591–1601. [3] Isberg, R. R. (1996): Uptake of enteropathogenic Yersinia by mammalian cells. Curr. Top. Microbiol. Immunol. 209: 1–24. [4] Hamburger, Z. A., Brown, M. S., Isberg, R. R., Bjorkman, P. J. (1999): Crystal structure of invasin: a bacterial integrinbinding protein. Science 286: 291–295. [5] Dersch, P., Isberg, R. (1999): A region of the Yersinia pseudotuberculosis invasin protein enhances integrin-mediated uptake into mammalian cells and promotes self-association. EMBO J. 18: 1199–1213. [6] Dersch, P., Isberg, R. (2000): An immunoglobin superfamily-like domain unique to the Yersinia pseudotuberculosis invasin protein is required for stimulation of bacterial uptake via integrin receptors. Infect. Immun. 68: 2930–2938. [7] Hoiczyk, E., Roggenkamp, A., Reichenbecher, M., Lupas, A., Heesemann, J. (2000): Structure and sequence analysis of Yersinia YadA and Moraxella UspAs reveal a novel class of adhesins. EMBO J. 19: 5989–5999. [8] Heise, T., Dersch, P. (2006): Identification of a domain in Yersinia virulence factor YadA that is crucial for extracellular matrix-specific cell adhesion and uptake. Proc. Natl. Acad. Sci. USA 103: 3375–3380. [9] Une, T. (1977): Studies on the pathogenicity of Yersinia enterocolitica. Experimental infection in rabbits. Microbiol Immunol. 21: 341–363. [10] Eitel, J., Dersch, P. (2001): The YadA protein of Yersinia pseudotuberculosis mediates high-efficiency uptake into human cells under environmental conditions in which invasin is repressed. Infect. Immun. 7: 63–77. [11] Heroven, A., Nagel, G., Tran, H. J., Parr, S., Dersch, P. (2004): RovA is autoregulated and antagonizes H-NS-mediated silencing of invasin and rovA expression in Yersinia pseudotuberculosis. Mol. Microbiol. 53: 871–888. [12] Heroven A., Dersch, P. (2006): RovM, a novel LysR-type regulator of the virulence activator gene rovA, controls cell invasion, virulence and motility of Yersinia pseudotuberculosis. Mol. Microbiol. 62: 1469–1483. Korrespondenzadresse: Prof. Dr. Petra Dersch Institut für Mikrobiologie Technische Universität Braunschweig Spielmannstr. 7 D-38106 Braunschweig Tel.: 0531-391-5803, Fax: 0531-391-5854 [email protected] www.tu-braunschweig.de/ifm/abt/dersch AUTORINNEN Petra Dersch Tanja Heise Jahrgang 1965, Biologiestudium in Ulm und Konstanz, 1995 Promotion bei Prof. Dr. Erhard Bremer an der Universität Konstanz und am Max-Planck-Institut für Terrestrische Mikrobiologie in Marburg. 1995–1998 Postdoktorandin an der Tufts University, Boston, USA bei Prof. Dr. Ralph Isberg. 1998–2002 Wissenschaftliche Assistentin an der Freien Universität Berlin. Von 2003–2005 Leiterin einer Nachwuchsgruppe am Robert-Koch-Institut in Berlin. Seit 2005 W2-Professorin am Lehrstuhl für Mikrobiologie der Technischen Universität Braunschweig. Jahrgang 1978; 1997–2002 Biologiestudium an der Freien Universität Berlin. Seit 2003 Doktorandin am Robert-KochInstitut in Berlin und an der Technischen Universität Braunschweig.