RPS INFLAMMADRY DETECTOR™ PACKUNGSBEILAGE
Werbung

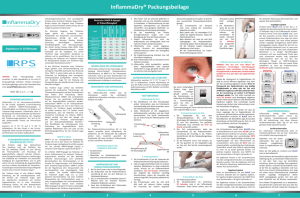
RPS INFLAMMADRY DETECTOR™ PACKUNGSBEILAGE ZUSAMMENFASSUNG UND ERKLÄRUNG DES TESTS HINWEIS: Die Packungsbeilage nicht verwerfen. In jeder Spenderbox ist nur eine Packungsbeilage enthalten. Weitere Kopien der Packungsbeilage können unter folgender Adresse heruntergeladen werden: http://www.RPSdetectors.com/downloads/ Ergebnisse in 10 Minuten Right Diagnosis Right Treatment Right Now™ VERWENDUNGSZWECK Der RPS InflammaDry Detector ist ein Immunoassay-Schnelltest für die visuelle, qualitative In-vitroErkennung eines erhöhten MMP-9Proteinspiegels in humanen Tränen zur Unterstützung der Diagnose von Patienten mit TrockenesAuge-Syndrom. Der Test ist für den professionellen Einsatz in einer Praxis, einer Klinik oder einem Krankenhaus in Verbindung mit anderen Methoden der klinischen Beurteilung vorgesehen. Zwischen 25 °C (77 °F) und 4 °C (39 °F) aufbewahren. Für den Einsatz in der In-vitro-Diagnostik. Nicht innerlich einnehmen. Außerhalb der Reichweite von Kindern aufbewahren. 1 Das Trockene Auge bzw. Dysfunctional Tear Syndrome, wie es vom Dry Eye Work Shop (DEWS) bezeichnet wird, ist eine Störung der Tränensekretion und Erkrankung der Augenoberfläche aufgrund mehrerer Faktoren, die zu Symptomen wie Beschwerden, Sehstörungen und Instabilität des Tränenfilms mit potenzieller Schädigung der Augenoberfläche führt. Begleitet wird es von einer erhöhten Osmolarität des Tränenfilms und einer Entzündung der Augenoberfläche [1]. Das Trockene Auge ist eine äußerst häufige Erkrankung, die oft unterdiagnostiziert wird. Die Schwere des Trockenen Auges kann von episodischen Symptomen wie Augenbeschwerden bis zu einer chronischen Erkrankung reichen, die eine therapeutische Intervention erfordert. Man nimmt an, dass Entzündungsmechanismen eine grundlegende Ursache eines chronisch Trockenen Auges sind. Derzeit basiert die Diagnose eines Trockenen Auges auf einer klinischen Untersuchung, die von einigen Zusatztests erhärtet wird. Die klinische Diagnose des Trockenen Auges umfasst auch die Auswertung einer Kombination von Symptomen und Anzeichen [1]. Typischerweise bittet der Arzt den Patienten, ihm über auftretendes Brennen, Stechen sowie über vorhandene Schmerzen, Lichtempfindlichkeit und Sehschwankungen zu berichten. Der Ocular Surface Disease Index (OSDI, Index zu Augenoberflächenerkrankungen) wurde entwickelt, um die häufigsten, mit einem Trockenen Auge verbundenen Symptome zu erfassen und zu quantifizieren. Dies ist das im Screening von Patienten mit Trockenen Augen für therapeutische Studien zum Trockenen Auge verwendete Standardinstrument [1]. Zu den klinischen Anzeichen eines Trockenen Auges gehören auch Hornhautverfärbung und verringerte TränenfilmAufrisszeit (Tear Break Up Time, TBUT). In vielen Fällen wird ein Schirmer-Tränentest zur Bestätigung einer verringerten Tränenproduktion durchgeführt [1]. Andere Tests zum Trockenen Auge für die Messung der Osmolarität bzw. des Lactoferrins der Tränen sind ebenfalls verfügbar; sie sind jedoch nicht empfindlich genug und werden nicht routinemäßig eingesetzt. Das Trockene Auge umfasst das Verhältnis zwischen der produzierten Tränenmenge, der Tränenverdunstungsrate und dem Vorhandensein oder Fehlen einer Entzündung ein. MatrixMetallproteinasen (MMP) sind proteolytische Enzyme, die von gestressten Epithelzellen auf der Augenoberfläche produziert werden. Insbesondere MMP-9 ist ein nichtspezifischer Entzündungsmarker, der sich in den Tränen von Patienten mit Trockenen Augen durchgehend als erhöht erwiesen hat [5-20]. In Studien wurde nachgewiesen, dass bei Patienten mit einer schwereren Erkrankung ein höherer MMP-9Spiegel vorliegt und dass der Spiegel mit den Befunden klinischer Untersuchungen korreliert [6]. Eine Identifikation des Vorhandenseins einer Entzündung der Augenoberfläche durch objektive Maßnahmen kann sich stark auf den Behandlungsalgorithmus für das Trockene Auge auswirken. MMP-9 in Tränen MMP-9 ist ein nichtspezifischer Entzündungsmarker, der sich in den Tränen von Patienten mit Trockenen Augen durchgehend als erhöht erwiesen hat. Der normale MMP-9-Spiegel (ng/ml) in humanen Tränen reicht von 3 ng/ml bis 40 ng/ml [5-10]. Ein erhöhter MMP-9-Spiegel bei Patienten mit einem mittelschweren bis schweren Trockenes-Auge-Syndrom korreliert mit den Befunden klinischer Untersuchungen. Eine veränderte Barrierefunktion des Hornhautepithels ist die Ursache für Augenreizungen und Sehstörungen beim Trockenes-Auge-Syndrom. MMP-9 scheint bei der Regulierung einer Desquamation des Hornhautepithels eine physiologische Rolle zu spielen. Die erhöhte MMP-9-Aktivität bei Trockenen Augen trägt u.U. zu einer gestörten Barrierefunktion und 2 einer erhöhten Desquamation des Hornhautepithels sowie zu einer Unregelmäßigkeit der Hornhautoberfläche bei [17]. Der RPS InflammaDry Detector erkennt einen erhöhten MMP-9Spiegel ≥ 40 ng/ml in Tränen und bestätigt so die Diagnose des Trockenes-Auge-Syndroms. Normaler MMP-9-Spiegel in Tränen Studie Normale Kontrollen DurchStandardschnittlicher abweichung MMP-9-Spiegel 1 2 3 4 5 6 18 16 17 10 20 28 23,61 ng/ml 8,39 ng/ml 7,2 ng/ml 10,5 ng/ml 6,9 ng/ml 22,7 ng/ml Gesamt/ Durchschn./ Bereich 109 13,2 ng/ml Oberer Bereich von MMP-9 17,4 ng/ml 4,70 ng/ml 2,1 ng/ml 0,2 ng/ml 1,4 ng/ml 14 ng/ml 41 ng/ml 13 ng/ml 9 ng/ml 11 ng/ml 8 ng/ml 37 ng/ml ~ 40 ng/ml GRUNDLAGEN DES VERFAHRENS Der RPS InflammaDry Detector arbeitet mit der Technologie „Direct Sampling Micro-Filtration“ (DirektentnahmeMikrofiltration). Ist MMP-9 in der Tränenprobe vorhanden, wird es von MMP-9-spezifischen monoklonalen und polyklonalen Antikörpern mit einer Konzentration von über 40 ng/ml umschlossen. REAGENZIEN UND MATERIAL Mitgelieferte Materialien Das RPS InflammaDry Detector-Kit enthält zwei Folienbeutel, welche die nachfolgend aufgeführten Materialien enthalten: Probenauffangvorrichtung (A) Testkassette (B) 8. Der RPS InflammaDry Detector muss visuell abgelesen werden. Das Testergebnis nicht auswerten, wenn die Farberkennung beeinträchtigt ist. 9. Die Ergebnisauswertung erfordert eine hell erleuchtete Umgebung. 10.Einen RPS InflammaDry Detector nur bei jeweils einem Patienten einsetzen. Den RPS InflammaDry Detector zwischen 25 °C (77 °F) und 4 °C (39 °F) aufbewahren. Sowohl der RPS InflammaDry Detector als auch der Puffer ist bis zu dem auf der jeweiligen Außenverpackung und dem Behälter aufgebrachten Ablaufdatum stabil. 1.Das Ablaufdatum auf der Verpackung prüfen. Sicherstellen, dass die Folienbeutel nicht beschädigt sind. Nicht verwenden, wenn die Folienbeutel beschädigt sind. 2. Jeden Folienbeutel Probenauffangan der angegebenen vorrichtung (A) Perforation (J) Perforationsstelle (J) aufreißen und den Inhalt herausnehmen. Das Entnahmevlies Perforation (J) (C) nur mit der Testkassette E n t n a h m e s t e l l e (B) (Bindehaut) und dem Perforation (J) Probentransferfenster (G) am Testkassettengehäuse (D) in Kontakt bringen. Perforation (J) Pufferampulle (I) Die Probenauffangvorrichtung (A) ist eine separat verpackte sterile Komponente, die problemlos auf das Testkassettengehäuse (D) aufgesetzt werden kann. Zusätzlich garantiert das Testkassettengehäuse (D) einen korrekten Probentransfer auf den Lateralfluss-Teststreifen. Nicht mitgelieferte Materialien • Zeitschaltuhr • Handschuhe • Materialien zur Qualitätskontrolle (siehe Abschnitt zu externen Kontrollvorrichtungen) WARNHINWEISE UND VORSICHTSMASSNAHMEN 1. Nur für den Einsatz in der In-vitro-Diagnostik. 2. Die Testkassette und die Probenauffangvorrichtung bis kurz vor dem Gebrauch im Folienbeutel belassen. 3. Das im Entnahmevlies verwendete Dacron-Material kann bei einigen Menschen allergische Reaktionen auslösen. 4.Den RPS InflammaDry Detector nicht nach dem Ablaufdatum verwenden. 5. Alle Proben sind als potenziell gefährlich zu betrachten und wie eine infektiöse Substanz zu handhaben. In Übereinstimmung mit den regionalen, überregionalen und nationalen Vorschriften sind geeignete Methoden zur Handhabung und Entsorgung festzulegen. 6. Bei der Handhabung der Proben Einweghandschuhe tragen und nach Beendigung des Tests die Hände waschen. 7. Sowohl der RPS InflammaDry Detector als auch die mitgelieferte Pufferampulle sind Einwegartikel. Nicht mit mehreren Proben wiederverwenden. 3 Die Ergebnisse des Tests werden mit zwei Linien angezeigt, Linie im Kontrollbereich. Die Kontrolllinie zeigt die korrekte (D) und der Schutzkappe (F) lokalisieren. Die geöffnete und Durchführung des Tests an und muss Absorbent Tip Anwendung (E) Testkassette muss binnen einer (1) Stunde verwendet with Protectiveerscheinen, Cap (F) damit der Test gültig ist. Test werden. Result Window (H) Cassette Body (D) Absorptionsspitze (E) Absorbent Tip (E) Sample Transfer NEGATIVES NEGATIVE withSchutzkappe Protective Cap (F) (G) mit (F) ERGEBNIS RESULT Window Test TestCassette kassettenBody (D)(D) gehäuse Probentransferfenster Sample Transfer Window (G) (G) POSITIVE Result Window (H) POSITIVES RESULT ERGEBNIS TESTVERFAHREN I. VORBEREITUNG DES TESTS Absorbent Tip (E) with Protective Cap (F) in einer hell erleuchteten Umgebung. Untersuchung die im Ergebnisfenster (H) erscheinen: die Ergebnislinie Sample Transfer 1.Die Testkassette (B) mit dem Testkassettengehäuse Window (G) und die Kontrolllinie. Die Kontrolllinie erscheint als BLAUE AUFBEWAHRUNG UND STABILITÄT Pufferampulle (I) Die Schutzkappe (F) schützt die Absorptionsspitze (E) vor versehentlicher physischer Beschädigung. Test III. ZUSAMMENSETZEN DES Cassette DETEKTORS Body (D) Result Window (H) Ergebnisfenster 2. Den Test zusammensetzen; dabei das Entnahmevlies (C) der Probenauffangvorrichtung (A) vorsichtig in das Probentransferfenster (G) des Testkassetten- gehäuses (D) einlegen. UNGÜLTIGES INVALID ERGEBNIS RESULT 3.An der Aufschrift „Press“ fest drücken, bis der Test gesichert ist. Ein Doppelklick zeigt an, dass der Test korrekt zusammengesetzt wurde. UNGÜLTIGES ERGEBNIS IV. DURCHFÜHREN DES TESTS 1.Die Pufferampulle (I) öffnen. Die Schutzkappe (F) vom Test abnehmen. Kein Teil des Tests außer der Absorptionsspitze (E) darf mit der Pufferampulle (I) in Berührung kommen. II. PROBENENTNAHME Sampling Fleece (C) SamplingEntnahmevlies Fleece (C) 1.Das (C) an der Unterseite der Probenauffangvorrichtung (A) lokalisieren. 2.Die Absorptionsspitze (E) mindestens 20 Sekunden lang in die Pufferampulle (I) eintauchen. Sampling Fleece (C) Entnahmevlies Erscheint keine BLAUE Linie, ist der Test u.U. ungültig. Die Absorptionsspitze (E) erneut für weitere 10 Sekunden in die Pufferampulle (I) tauchen. Erscheint immer noch keine BLAUE Linie, ist der Test zu verwerfen und der Patient muss durch eine erneute Probenentnahme vom Auge mit einem neuen RPS InflammaDry Detector-Kit noch einmal getestet werden. Ein ungültiges Testergebnis darf dem Patienten nicht mitgeteilt werden. Obwohl für den Test nur 10 μl Flüssigkeit gebraucht werden, ist, wenn eine zweite Probe benötigt wird, beim wiederholten Abtupfen u.U. weniger Augenflüssigkeit vorhanden und eine ausreichende Probe kann nicht entnommen werden. Jede zusätzliche Probenentnahme kann die auf den Test übertragene Menge an MMP-9-Antigenen verringern oder verändern. Ist eine zweite Probenentnahme nötig, kann sie eine Stunde später wiederholt werden. NEGATIVES ERGEBNIS 2. Ab mindestens 10 Minuten vor der Entnahme einer Probe darf kein Anästhetikum mehr in das Auge eingebracht werden. Das untere Augenlid des Patienten zur Freilegung der Augenlidbindehaut sanft nach unten ziehen. Das Entnahmevlies (C) 6-8-mal sanft auf mehrere Stellen entlang der Innenseite des unteren Augenlids (Augenlidbindehaut) tupfen; anschließend für weitere 5 Sekunden auf der Bindehaut ruhen lassen. Auf diese Weise wird das Entnahmevlies angefeuchtet. Bei der Probenentnahme keine Ziehbewegung machen. Bei Sättigung mit Tränenflüssigkeit glänzt das Vlies. Basierend auf dem Volumen und der Zusammensetzung der Tränen erscheint die Farbe des Vlieses weiß oder ungleichmäßig rosa. 4 3.Die Absorptionsspitze (E) aus der Pufferampulle (I) nehmen, die Schutzkappe (F) wieder aufsetzen und den Test waagerecht für 10 Minuten auf eine ebene Oberfläche legen. V. ABLESEN UND AUSWERTEN DER ERGEBNISSE HINWEIS: Den Test erst nach Ablauf der 10 Minuten Entwicklungszeit auswerten. Unter Umständen ist eine violette Flüssigkeitswelle zu beobachten, die während der Laufzeit des Tests quer über das Ergebnisfenster (H) läuft. Im Kontrollbereich erscheint nur eine BLAUE Linie. Ein negatives Ergebnis ist bezüglich des Vorhandenseins von MMP-9 < 40 ng/ml als negativ zu melden. POSITIVES ERGEBNIS Das Vorhandensein einer BLAUEN Linie im Kontrollbereich und einer ROTEN Linie im Ergebnisbereich weist auf ein positives Ergebnis hin. Eine ungleichmäßige oder unvollständige ROTE Linie ist auf eine ungleichmäßige Verteilung von Augenflüssigkeit auf dem Entnahmevlies (C) zurückzuführen. Auch wenn die ROTE Linie nur farblich schwach, unvollständig über die Breite des Teststreifens verteilt oder farblich ungleichmäßig ist, muss sie als positiv gewertet werden. Ein positives Ergebnis weist auf das Vorhandensein von MMP-9 > 40 ng/ml hin. Sobald der Hintergrund im Ergebnisfenster (H) weiß ist und 10 Minuten abgelaufen sind, kann der Test präzise abgelesen werden. Ist im Hintergrund nach 10 Minuten eine streifige Flüssigkeitswelle zu sehen, sollte die Laufzeit des Tests vor der Auswertung um weitere 5-10 Minuten verlängert werden. Der Test sollte innerhalb von 12 Stunden nach Beendigung abgelesen werden. Nach diesem Zeitraum sind abweichende Ergebnisse möglich. Eine präzise visuelle Auswertung erfordert eine 5 6 RPS INFLAMMADRY DETECTOR™ PACKUNGSBEILAGE QUALITÄTSKONTROLLE EINSCHRÄNKUNGEN Der RPS InflammaDry Detector verfügt über integrierte Verfahrenskontrollen (siehe unten). Für die tägliche Qualitätskontrolle empfiehlt RPS die Aufzeichnung, dass diese internen Verfahrenskontrollen jeden Tag für die erste getestete Probe überprüft wurden. 1.MMP-9 ist ein nichtspezifischer Indikator für das Vorhandensein einer Entzündung. Ein positives Testergebnis darf nicht als alleinige Grundlage für Therapien oder sonstige Behandlungsentscheidungen verwendet werden. 2. Patienten, die an einem Trockenes-Auge-Syndrom mit schwerem Tränenmangel leiden, produzieren u.U. nicht genug Tränen für die Probenentnahme, was zu einem falsch negativen Ergebnis führen könnte. 3. Der RPS InflammaDry Detector darf nicht innerhalb von 15 Minuten nach Durchführung eines Schirmer-Tränentests verwendet werden, da dies u.U. die Degranulierung von MMP-9 stimulieren und zu einem falsch positiven Ergebnis führen kann. 4. Eine kürzlich erfolgte Augenoperation oder Infektion kann zu einem erhöhten MMP-9-Spiegel und damit zu einem falsch positiven Ergebnis führen. 5. Bestimmte Medikamente, wie z.B. topische oder orale Steroide, Cyclosporin, Tetracyclin und topisches Azithromycin sind dafür bekannt, dass sie die Metallproteinase-Aktivität hemmen. Die Verwendung dieser Medikamente führt u.U. zu falsch negativen Ergebnissen. 6.Mit diesem Test erzielte Ergebnisse sollten in Verbindung mit anderen, dem Arzt zugänglichen klinischen Informationen genutzt werden, insbesondere bei schwach sichtbaren Testlinien, die schwer auszuwerten sind. Verfahrenskontrollen Die nicht verwendete Vorrichtung weist eine orangefarbene Linie im Kontrollbereich auf. Wenn der Test läuft und die Reagenzien wirken, wechselt diese orangefarbene Linie während des Testverfahrens stets zu einer blauen Linie. Damit wird die Funktionsfähigkeit des Tests angezeigt. Das Erscheinen der Kontrolllinie zeigt die korrekte Anwendung und Durchführung des Tests an. Die Kontrolllinie muss in allen gültigen Tests erscheinen. Erscheint die Kontrolllinie nicht, ist der Test als ungültig zu betrachten und muss durch eine erneute Probenentnahme vom Auge mit einem neuen RPS InflammaDry DetectorKit wiederholt werden. Während der Laufzeit des Tests ist eine violette Flüssigkeitswelle zu beobachten, die quer über das Ergebnisfenster (H) läuft. Sobald der Hintergrund im Ergebnisfenster (H) weiß ist und 10 Minuten abgelaufen sind, kann der Test präzise abgelesen werden. Ist im Hintergrund nach 10 Minuten eine streifige Flüssigkeitswelle zu sehen, sollte die Laufzeit des Tests vor der Auswertung um weitere 5-10 Minuten verlängert werden. Die Entfärbung der Hintergrundfarbe im Ablesefenster ist eine negative Hintergrundkontrolle. Externe Kontrollvorrichtungen Es wird empfohlen, zusätzlich zu den Standardverfahren für die Qualitätskontrolle Ihrer Einrichtung einmalig bei jeder neuen Chargennummer von RPS InflammaDry Detectors einen Test mit einer positiven externen Kontrollvorrichtung durchzuführen. Positive externe Kontrollvorrichtungen, die rekombinantes MMP-9-Protein an der unteren Erkennungsgrenze des RPS InflammaDry Detector enthalten, sind direkt bei RPS erhältlich. Zur Bestellung von externen Kontrollvorrichtungen bitte den Abschnitt mit Bestellinformationen dieser Packungsbeilage einsehen. Die Packungsbeilagen der Kontrollvorrichtungen für Anweisungen zur Durchführung der externen Kontrollen einsehen. Auf jeder Verpackung der externen Kontrollvorrichtungen ist ein individuelles Ablaufdatum aufgedruckt. Weitere Kontrollen können gemäß den Anforderungen der regionalen, überregionalen und nationalen Vorschriften bzw. von Akkreditierungsorganisationen durchgeführt werden. Für Richtlinien bezüglich ordnungsgemäßer QKTests siehe CLSI-Dokument EP12-A und 42 CFR 493.1202c. Werden keine korrekten Kontrollergebnisse erzielt, vor Patiententests die Testkontrolle wiederholen oder RPS unter der Nummer +1-941-556-1850 kontaktieren. Probleme mit der Vorrichtung sind RPS unter der Nummer +1-941-556-1850 bzw. per E-Mail unter [email protected] oder direkt der US-amerikanischen FDA unter www.fda.gov/medwatch zu melden. 7 ERWARTETE WERTE Das Trockene Auge tritt bei 5% bis 30% der Menschen im Alter von > 50 Jahren auf. In den USA sind schätzungsweise 21 Millionen Menschen vom Trockenen Auge betroffen [1-3]. Eine nationale Studie mit 2.003 Personen ergab, dass fast 40% der US-Amerikaner an Symptomen des Trockenen Auges leiden; diese können Trockenheit, Juckreiz, Reizung, verschwommenes Sehen, Lichtempfindlichkeit, Fremdkörpergefühl und übermäßiger Tränenfluss [1,4] umfassen. Die Prävalenz des Trockenen Auges steigt mit zunehmenden Alter an und ist bei Frauen weitaus häufiger. Zu den weiteren Risikofaktoren gehören die Verwendung bestimmter Medikamente, entzündliche Autoimmunerkrankungen, das Tragen von Kontaktlinsen, eine LASIK sowie ein refraktiver Eingriff und die Menopause [1]. LEISTUNGSCHARAKTERISTIKA Die Empfindlichkeit und Spezifität des RPS InflammaDry Detectors wurde mit klinischen Fakten verglichen, wie sie anhand von üblicherweise verwendeten Kriterien zur Diagnose von Trockenen Augen definiert wurden, bestehend aus einer Kombination notwendiger klinischer Krankengeschichten, dargestellt durch einen hohen Wert des Ocular Surface Disease Index (OSDI) von ≥ 13, einen positiven Wert zum verschwommenen Sehen und das Vorhandensein von mindestens zwei Anzeichen, wie z.B. einem Schirmer-Tränentest zur Bestätigung einer verringerten Tränenproduktion von < 10, einer verringerten TränenfilmAufrisszeit (TBUT) von < 10 und das Vorhandensein einer Hornhaut-Bindehaut-Verfärbung. Normale Gesundheitskontrollen ohne Anzeichen und Symptome eines Trockenen Auges wurden ebenfalls durchgeführt. Diese Patienten wiesen einen OSDI von < 1 und kein verschwommenes Sehen auf, der Schirmer-Tränentest ergab einen Wert von ≥ 10, die TBUT betrug ≥ 10 und es zeigte sich keine Hornhaut-Bindehaut-Verfärbung. In zwei klinischen Einrichtungen wurde der RPS InflammaDry Detector mit klinischen Fakten verglichen. 8 Die klinischen zusammengefasst: Ergebnisse sind nachfolgend RPS InflammaDry Detector Klinische Untersuchung + + 26 1 4 11 Patienten Referenz Empfindlichkeit Spezifität Trockene Augen (N=30) Normale Kontrollen (N=12) Gesamter N=42 Klinische Fakten Klinische Fakten 87% (26/30) - - 92% (11/12) Einschränkungen der Erkennung Der obere Grenzwert beim RPS InflammaDry Detector wurde anhand einer Reihe von Verdünnungen von humanem MMP-9 in humanen Tränen auf 40 ng/ml festgelegt. Kreuzreaktivität Im Labor wurden verschiedene infektiöse, in Zellkulturen erzeugte Augenpathogene und wichtige Augenenzyme zur Bestimmung potenzieller Kreuzreaktivitäten eingesetzt: • Staphylococcus aureus • Methicillin-resistenter Staphylococcus aureus (MRSA) • Moraxella catarrhalis • Haemophilus influenzae • Staphylococcus epidermis • Streptococcus pneumoniae • Pseudomonas aeroginosa • Influenza A • Influenza B (Lee) • Parainfluenza-Virus: 2, 3 und 4a • Rhinovirus Typ 1a • Herpes simplex 1, 2 • Coxsackie-Virus B1 • Echovirus: 6, 7, 9, 11 und 30 • Adenovirus: 1, 3, 4, 5, 7, 11, 14, 15 und 37 • Matrix-Metallproteinase: 1, 2 und 3 • Gewebehemmer von MMP: MMP-1, MMP-2 Alle Isolate wurden aus humanen Proben kultiviert. Die Konzentrationen der Suspensionen lagen zwischen 500.000 und 1.500.000 Mikroorganismen (Viren, Bakterien) pro ml Supernatant. Beim Test von 10 µl der Kultursuspension entwickelten sich keine positiven Testlinien und es traten keine Kreuzreaktivitäten gegenüber diesen Spezies auf. Kein Augenenzym löste eine Kreuzreaktivität aus. SUBSTANZEN MIT WECHSELWIRKUNG Folgende Augenmedikamente wurden auf Wechselwirkungen mit dem RPS InflammaDry Detector getestet. Zur Prüfung auf Spezifität wurde ein unverdünntes reines Medikament auf das Entnahmevlies aufgetragen. Die Empfindlichkeit wurde mit 1:1-Mischungen von rekombinantem MMP-9-Protein in humanen Tränen am oberen Grenzwert und dem entsprechenden Medikament geprüft. Alle getesteten Medikamente außer Trusopt zeigten keine falsch positiven oder falsch negativen Ergebnisse. Als Trusopt direkt auf den Teststreifen aufgetragen wurde, kam es zu einer verstärkten Bindung von MMP-9 sowie einem offenbar falsch positiven Ergebnis. 9 • Alcon, Alcaine • Alcon, Tobra Dex • Alcon, Econopred • Alcon, Vigamox • Alcon, Pataday • Alcon, Nevanac • Alcon, Travatan • Alcon, Systaine • Alcon, Azopt • Allergan, Refresh Liquigel • Allergan, Alphagan • Allergan, Zymar • Allergan, Refresh Tears • Allergan, Elastat • Allergan, Lumigan • Allergan, FML • Allergan, Optive • Allergan, Combigan • Allergan, Acular LS • Allergan, Pred Forte • Amo, Blink Tears • AVS, Thera Tears • Bausch & Lomb, Lotemax • Bausch & Lomb, Alrex • Bausch & Lomb, Zylet • Falcon, Polymyxin B Sulfate • Falcon, Timolol • Falcon, Gentamycin Sulfate • Inspire, AzaSite • Ista, Xibrom • Medpoint, Optivar • Merck, Trusopt • Novartis, GenTeal • Novartis, Voltaren • Novartis, Zaditor • Pfizer, Visine • Pharmacia, Xalatan • Sigma-Aldrich, Human IgA (1 mg/ml) • Sigma-Aldrich, Human Lactoferrin (1 mg/ml) • Sigma-Aldrich, Transferrin (1 mg/ml) • Vistakon, Betimol • Vistakon, Quixin • Vistakon, Iquix • Wilson, Proparacaine HINWEIS: Bestimmte Medikamente können fehlerhafte Ergebnisse auslösen, wenn sie direkt vor einer Probenentnahme verwendet werden. Es wird empfohlen, innerhalb von 30 Minuten vor einer Probenentnahme außer einem Augenanästhetikum keine topischen Medikamente zu verwenden. Ab mindestens 10 Minuten vor der Entnahme einer Probe darf kein Anästhetikum mehr in das Auge eingebracht werden. REFERENZEN [1] Definition and Classification of Dry Eye. Report of the Diagnosis and Classification Subcommittee of the Dry Eye Work Shop (DEWS). Ocular Surface 2007;5:75-92. [2] Market Scope. Report on the Global Dry Eye Market. St. Louis, Mo: Market Scope, July 2004. [3] Multi-sponsor surveys, Inc. Gallup study of dry eye sufferers. Princeton, NJ, 2006. [4] Schaumberg, DA, Buring JE, Sullivan DA, Dana MR. Hormone replacement therapy and dry eye syndrome. JAMA 2001;286:2114-2119. 10 [5] Acera A, Rocha G, Vecino E, Lema I, Durán JA. Inflammatory markers in the tears of patients with ocular surface disease. Ophthalmic Res. 2008 Oct; 40(6):315-21. [6] Chotikavanich S, de Paiva CS, Li de Q, Chen JJ, Bian F, Farley WJ, Pflugfelder SC. Production and activity of matrix metalloproteinase-9 on the ocular surface increase in dysfunctional tear syndrome. Invest Ophthalmol Vis Sci. 2009 Jul; 50(7):3203-9. [7] Solomon A, Dursun D, Liu Z, Xie Y, Macri A, Pflugfelder SC. Pro- and anti-inflammatory forms of interleukin-1 in the tear fluid and conjunctiva of patients with dry-eye disease. Invest Ophthalmol Vis Sci. 2001 Sep; 42(10):2283-92. [8] Leonardi A, Brun P, Abatangelo G, Plebani M, Secchi AG. Tear levels and activity of matrix metalloproteinase (MMP)-1 and MMP-9 in vernal keratoconjunctivitis. Invest Ophthalmol Vis Sci. 2003 Jul; 44(7):3052-8. [9] Lema I, Sobrino T, Durán JA, et al. Subclinical keratoconus and inflammatory molecules from tears. Br J Ophthalmol. 2009 Jun;93(6):820-4. [10] Honda N, Miyai T, Nejima R, et al. Effect of latanoprost on the expression of matrix metalloproteinases and tissue inhibitor of metalloproteinase 1 on the ocular surface. Arch Ophthalmol. 2010 Apr;128(4):466-71. [11] Hadassah J, Bhuvaneshwari N, Rao U, Sehgal PK. Evaluation of succinylated collagen bandage lenses in corneal healing by the expression of matrix metalloproteinases (MMP-2 and MMP-9) in tear fluid. Ophthalmic Res. 2009; 42(2):64-72. [12] Sobrin L, Liu Z, Monroy DC, Solomon A, Selzer MG, Lokeshwar BL, Pflugfelder SC. Regulation of MMP-9 activity in human tear fluid and corneal epithelial culture supernatant. Invest Ophthalmol Vis Sci. 2000 Jun; 41(7):1703-9. [13] Afonso AA, Sobrin L, Monroy DC, Selzer M, Lokeshwar B, Pflugfelder SC. Tear fluid gelatinase B activity correlates with IL-1alpha concentration and fluorescein clearance in ocular rosacea. Invest Ophthalmol Vis Sci. 1999 Oct; 40(11):2506-12. [14] Oh JY, In YS, Kim MK, Ko JH, Lee HJ, Shin KC, Lee SM, Wee WR, Lee JH, Park M. Protective effect of uridine on cornea in a rabbit dry eye model. Invest Ophthalmol Vis Sci. 2007 Mar; 48(3):1102-9. [15] Pflugfelder SC, de Paiva CS, Tong L, Luo L, Stern ME, Li DQ. Stress-activated protein kinase signaling pathways in dry eye and ocular surface disease. Ocul Surf. 2005 Oct; 3(4 Suppl):S154-7. [16] Luo L, Li DQ, Corrales RM, Pflugfelder SC. Hyperosmolar saline is a proinflammatory stress on the mouse ocular surface. Eye Contact Lens. 2005 Sep; 31(5):186-93. [17] De Paiva CS, Corrales RM, Villarreal AL, Farley WJ, Li DQ, Stern ME, Pflugfelder SC. Corticosteroid and doxycycline suppress MMP-9 and inflammatory cytokine expression, MAPK activation in the corneal epithelium in experimental dry eye. Exp Eye Res. 2006 Sep; 83(3):526-35. [18] Luo L, Li DQ, Doshi A, Farley W, Corrales RM, Pflugfelder SC. Experimental dry eye stimulates production of inflammatory cytokines and MMP-9 and activates MAPK signaling pathways on the ocular surface. Invest Ophthalmol Vis Sci. 2004. Dec; 45(12):4293-301. [19] Pflugfelder SC, Farley W, Luo L, Chen LZ, de Paiva CS, Olmos LC, Li DQ, Fini ME. Matrix metalloproteinase-9 knockout confers resistance to corneal epithelial barrier disruption in experimental dry eye. Am J Pathol. 2005 Jan; 166(1):61-71. [20] Li DQ, Chen Z, Song XJ, Luo L, Pflugfelder SC. Stimulation of matrix metalloproteinases by hyperosmolarity via a JNK pathway in human corneal epithelial cells. Invest Ophthalmol Vis Sci. 2004 Dec; 45(12):4302-11. 11 BESTELL- UND KONTAKTINFORMATIONEN Bestellinformationen RPS-DE – RPS InflammaDry Detector RPS-DESTD – RPS InflammaDry Detector Externe Kontrollvorrichtung Kontaktinformationen und technische Unterstützung Rapid Pathogen Screening, Inc. 7227 Delainey Court • Sarasota, FL 34240 USA t 1-941-556-1850 • f 1-941-556-1851 [email protected] RPSdetectors.com Hersteller Rapid Pathogen Screening, Inc. 7227 Delainey Court • Sarasota, FL 34240 USA t 1-941-556-1850 • f 1-941-556-1851 [email protected] RPSdetectors.com Vertreter in der EU MT Promedt Consulting GmbH, Altenhofstr. 80 D-66386 St. Ingbert, Germany t 49-6894-58 10 20 • f 49-6894-58 10 21 www.mt-procons.com US-Patente 6,514,773 und 7,723,124 sowie andere Patente anhängig. Spec 375 Rev 0. 01/2011 12