Rezidivierende, stärkste Oberbauchschmerzen bei einem 45
Werbung

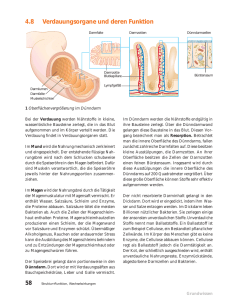
Kasuistiken Internist 2006 · 47:1068–1072 DOI 10.1007/s00108-006-1692-x Online publiziert: 9. August 2006 © Springer Medizin Verlag 2006 E. Biecker1 · H.-P. Fischer2 · G. Lutterbey3 · U. Pütz4 · T. Sauerbruch1 · F. Lammert1 1 Medizinische Klinik und Poliklinik I, Universitätsklinikum Bonn 2 Pathologisches Institut, Universitätsklinikum Bonn 3 Radiologische Klinik, Universitätsklinikum Bonn 4 Klinik und Poliklinik für Chirurgie, Universitätsklinikum Bonn Rubrikherausgeber K. Werdan, Halle /Saale Fallbericht Anamnese Der 45-jährige Patient stellte sich in unserer Abteilung notfallmäßig mit stärksten, kolikartigen Oberbauchschmerzen vor. Er berichtete über rezidivierende epigastrische Schmerzattacken. Die Schmerzen träten etwa 30 min nach dem Essen auf und seien von einer vermehrten Darmaktivität begleitet. Nach etwa einer bis zwei Stunden ließen die Schmerzen dann spontan nach. Zur ersten Schmerzepisode sei es vor etwa neun Monaten gekommen. Zu die- Wie hätten Sie es gemacht? Wir behandeln Kranke, nicht Krankheiten. Deshalb finden sich bei jeder unserer vorgestellten Kasuistiken individuelle Besonderheiten des Krankheitsverlaufs. Hätten Sie bei der Betreuung des Patienten einen anderen Weg gewählt? Schreiben Sie uns. Gerne regen wir einen Gedankenaustausch mit den Autoren an und bringen diesen ggf. zur Veröffentlichung. Senden Sie Ihre Anregungen oder Kasuistiken an: Prof. Dr. K. Werdan Klinikum Kröllwitz Innere Medizin III Martin-Luther-Universität Halle-Wittenberg Ernst-Grube-Str. 40 D-06097 Halle/Saale Fax 0345/5572422 [email protected] 1068 | Der Internist 10 · 2006 Rezidivierende, stärkste Oberbauchschmerzen bei einem 45-jährigen Patienten sem Zeitpunkt war der Berufssoldat in Afghanistan stationiert. Damals wurde die Diagnose einer akuten Gastroenteritis gestellt. Nach der Rückkehr nach Deutschland kam es jedoch zu weiteren Schmerzepisoden. In der Folge stellte sich der Patient mit akuten Oberbauchschmerzen immer wieder notfallmäßig in verschiedenen Krankenhäusern vor. Die dort durchgeführten umfangreichen diagnostischen Maßnahmen (Labor, Sonografie, Röntgen-Abdomenübersicht, Ösophago-Gastro-Duodenoskopie, Koloskopie, MR-Abdomen, MRCP) hatten durchweg unauffällige Befunde gezeigt. Wesentliche Vorerkrankungen waren nicht bekannt. Befunde Klinischer Untersuchungsbefund Der Patient (178 cm, 85 kg) befand sich in gutem Allgemeinzustand und wirkte Abb. 1 7 CT-Abdomen: ausgeprägte Dilatation einer Dünndarmschlinge mit Spiegelbildung (großer Pfeil) sowie eine Gewebsvermehrung im Bereich der Mesenterialwurzel (kleiner Pfeil) deutlich schmerzgeplagt. Das Abdomen war weich, es bestand keine Abwehrspannung. Resistenzen waren nicht zu tasten, die Darmgeräusche waren spärlich. Die Untersuchung der restlichen Organsysteme erbrachte bis auf einen grenzwertigen arteriellen Hypertonus keinen pathologischen Befund. Klinisch-chemische Befunde Das Aufnahmelabor war lediglich auffällig für ein marginal erhöhtes Gesamtbilirubin (1,44 mg/dl, Referenzbereich: 0,1– 1,2 mg/dl), eine leicht erhöhte CK (205 U/ l, Referenzbereich: <171 U/l) sowie ein erhöhtes Laktat (5,4 mmol/l, Referenzbereich: 0,4–2,2 mmol/l). Alle anderen Laborparameter (insbesondere Blutbild, CRP, Lipase, LDH, Troponin) waren im Referenzbereich. Zusammenfassung · Abstract Diagnose und Therapie Die bei Aufnahme durchgeführte Röntgenaufnahme des Thorax zeigte einen altersentsprechenden Normalbefund. Die etwa drei Stunden nach Aufnahme durchgeführte Sonografie des Abdomens ergab eine unauffällige Darstellung der Oberbauchorgane. Im Verlauf von etwa 90 min nach der Aufnahme kam es zu einer völligen Rückbildung der Beschwerdesymptomatik. Der Patient wurde zunächst auf Station weiter beobachtet. Nach einem Tag wurde ein Kostaufbau begonnen, der initial gut toleriert wurde. Am zweiten Tag nach der stationären Aufnahme kam es erneut zu stärksten, krampfartigen Oberbauchschmerzen mit einer vegetativen Begleitsymptomatik und Erbrechen. Auffällig waren hochgestellte Darmgeräusche. Zur Diagnostik führten wir im akuten Anfall sofort eine Computertomografie des Abdomens durch (. Abb. 1). Es zeigte sich eine ausgeprägte Dilatation einer proximalen Dünndarmschlinge mit Spiegelbildung und der Verdacht auf eine pathologische Gewebsvermehrung im Bereich der Mesenterialwurzel, die nicht genauer zugeordnet werden konnte. Eine Darmwandverdickung, eine Invagination oder ein Tumor kamen nicht zur Darstellung. Die Perfusion der abdominalen Gefäße war regelrecht. Die dilatierte Darmschlinge ließ in Zusammenschau mit der Klinik an einen (Sub-)Ileus denken. Zur weiteren Diagnostik wurde im Verlauf noch eine Dünndarmuntersuchung in Doppelkontrasttechnik nach Sellink (. Abb. 2) durchgeführt. Es stellte sich im Bereich des mittleren Ileums eine 40 cm lange, deutlich dilatierte Darmschlinge dar, die unter Palpation nicht verschieblich war. In diesem Bereich floss das Kontrastmittel erst mit einiger Verzögerung und starken Schmerzen ab. Eine sichere Aussage über das zu Grunde liegende Hindernis konnte aber auch in dieser Untersuchung nicht erbracht werden. Da sich die Mesenterialwurzel im CT-Abdomen auffällig dargestellt hatte, erfolgte zum Ausschluss eines ischämischen Geschehens noch eine Mesentericografie, die eine regelrechte Perfusion der unpaaren Aortenabgänge zeigte. Wir besprachen die Befunde des Patienten in der interdisziplinären inter- Internist 2006 · 47:1068–1072 DOI 10.1007/s00108-006-1692-x © Springer Medizin Verlag 2006 E. Biecker · H.-P. Fischer · G. Lutterbey · U. Pütz · T. Sauerbruch · F. Lammert Rezidivierende, stärkste Oberbauchschmerzen bei einem 45-jährigen Patienten Zusammenfassung Ein 45-jähriger Patient stellte sich mit rezidivierenden abdominalen Beschwerden unklarer Genese vor. Die weitere Diagnostik zeigte eine verdichtete Mesenterialwurzel im CT-Abdomen sowie einen segmentalen Ileus im Bereich des Jejunums. Intraoperativ kam als Ursache ein neuroendokriner Tumor des Dünndarms zur Darstellung. Neuroendokrine Tumoren des Dünndarms können seltene Ursachen für rezidivierende abdominale Beschwerden sein. Insbesondere bei einem auffälligen CT-Befund der Mesenterialwurzel („desmoplastische Reaktion“), evtl. in Kom- bination mit einem segmentalen Ileus, sollte differenzialdiagnostisch an einen neuroendokrinen Tumor gedacht werden. Therapie der Wahl ist die Operation, gefolgt von systemischer Therapie mit Somatostatinanaloga oder Chemotherapie bei hormonaktiven Tumoren und Vorliegen von Metastasen. Schlüsselwörter Neuroendokriner Tumor · Ileus · Desmoplastische Reaktion · Rezidivierende abdominale Beschwerden · Mesenterialwurzel Recurring, severe upper abdominal pain in a 45 year old patient Abstract A 45-year-old patient presented with a history of recurrent abdominal pain of unknown origin. The CT scan of the abdomen demonstrated a thickened mesenteric root and a segmental ileus of the jejunum. Laparotomy revealed a neuroendocrine tumour of the small bowel. Such tumours are rare causes of recurrent abdominal pain. Especially when the CT scan of the abdomen reveals mesenteric abnormalities (desmoplastic reaction) and/or a segmental ileus, a neuroendocrine tumour of the small bowel should be considered. The therapy of choice is resection of the tumour followed by systemic therapy including somatostain analogues and chemotherapy in the case of a hormone secreting tumour or metastases. Keywords Neuroendocrine tumour · Ileus · Desmoplastic reaction · Recurrent abdominal pain · Mesenteric root Der Internist 10 · 2006 | 1069 Kasuistiken Abb. 2 9 Dünndarmdarstellung nach Sellink in Doppelkontrasttechnik: deutlich dilatierte, ca. 40 cm lange Darmschlinge im Bereich des mittleren Ileums, die unter Palpation nicht verschieblich war; in diesem Bereich floss das Kontrastmittel erst mit einiger Verzögerung und starken Schmerzen ab Abb. 3 9 Die Histologie zeigt aus isomorphen Zellen aufgebautes, gering proliferationsaktives Tumorgewebe eines Neuroendokrinen Karzinoms (HE-Färbung) nistisch-chirurgischen Konferenz. Zur definitiven Diagnosestellung und ggf. Therapie wurde der Patient zur Laparotomie in die chirurgische Klinik verlegt. Intraoperativ zeigte sich ein Dünndarmkonglomerat mit einem ausgedehnten Tumor im Mesenterium auf Höhe des terminalen Ileums mit tastbaren Lymphknotenvergrößerungen entlang des Dünndarms. Es wurde daraufhin die Jejunumsegmentresektion auf einer Gesamtlänge von 40 cm unter En-bloc-Mitnahme des mesenterialen Tumors, welcher bis in die tiefe Mesenterialwurzel hineinragte, durchgeführt. Die histopathologische Aufarbeitung (. Abb. 3) ergab ein neuroendokrines Karzinom, welches alle Darmwandschichten bis auf die peritoneale Oberfläche infiltrierte. Die Absetzungsränder waren tumorfrei. Das Tumorstadium wurde entsprechend mit pT4, R0, L0, V1, pN0 (0/14) M1 festgelegt. 1070 | Der Internist 10 · 2006 Der weitere postoperative Verlauf gestaltete sich problemlos. Zur Metastasenlokalisation wurde (bei immunhistochemischem Nachweis von Somatostatinrezeptoren) noch eine Octreotidszintigrafie durchgeführt, die keinen Anhalt für eine pathologische Anreicherung erbrachte. Auf eine adjuvante Chemotherapie wurde daher verzichtet. Diagnose E Neuroendokrines Karzinom des Jejunums Diskussion Epidemiologie und Klinik Neuroendokrine Tumoren (NET) des Gastrointestinaltraktes sind seltene Erkrankungen. Die Prävalenz von NET des Dünndarms beträgt 0,5 Fälle auf 100.000 Einwohner/Jahr. Bei 13 bis 34 aller Dünndarmneoplasien handelt es sich um NET. Der Großteil der NET findet sich im Ileum (ca. 80); die restlichen 20 verteilen sich zu gleichen Teilen auf das Duodenum und das Jejunum [9, 16]. Neuroendokrine Tumoren präsentieren sich in der Mehrzahl der Patienten als hormoninaktiv. Die hormonaktiven neuroendokrinen Tumoren (z. B. Insulinom, Gastrinom, VIPom) werden häufig durch die durch den Tumor freigesetzten Hormone klinisch auffällig. Bei hormonaktiven NET des Dünndarms tritt das „Karzinoidsyndrom“ in der Regel nur auf, wenn die Abbaufähigkeit der Leber für Serotonin überschritten wird oder sich in der Leber Metastasen finden. Dementsprechend entwickeln nur 3 bis 5 aller Patienten mit NET ein Karzinoidsyndrom [13]. Die malignen neuroendokrinen Tumoren des Pankreas und des Dickdarms sowie des Rektums fallen in der Regel erst durch lokale Symptome auf, welche durch Fernmetastasen bedingt sind. Jedoch können auch maligne und funktionell inaktive Tumoren des unteren Dünndarms rezidivierende Abdominalschmerzen verursachen [13]. Diesen Schmerzen liegt häufig keine direkte mechanische Dünndarmobstruktion zu Grunde. Vielmehr wird davon ausgegangen, dass autokrin freigesetzte Tumorprodukte zu einer Raffung des Mesenteriums („desmoplastische Reaktion“) führen [2, 6, 7]. Diese „Raffung“ bedingt eine Kompression oder ein Abknicken von Mesenterialgefäßen, die dann in Kombination mit Hormoneffekten und ggf. einer Kompression durch Lymphknotenmetastasen zu einer Ischämie in den betroffenen Darmwandanteilen führen können, welche für die Beschwerden verantwortlich sind. Diagnostik Nur selten werden NET des Dünndarms präoperativ sicher diagnostiziert und lokalisiert. Sollte die Bildgebung vor der Operation einen Tumor nachgewiesen haben, so handelt es sich hierbei oft um Lymphknotenmetastasen und nicht um den NET selbst. Die betroffenen Patienten werden häufig unter dem Bild eines mechanischen Ileus oder einer Ischämie operiert [19]. Auch im vorliegenden Fall wurde die Diagnose erst durch die Operation gesichert. Da eine unspezifische abdominale Beschwerdesymptomatik vorlag und karzinoidtypische Symptome fehlten, wurde ein NET von uns nicht in die Differenzialdiagnose einbezogen. Auch die im CT diagnostizierte diskrete Gewebsvermehrung im Bereich des Mesenteriums wurde zunächst nicht als eine mögliche „desmoplastische Reaktion“ bei NET des Dünndarms gedeutet. Bei somatostatinrezeptorpositiven NET kann mittels Octreotidszintigrafie eine Metastasensuche und -lokalisation durchgeführt werden. Im Verlauf kann dann auch das Ansprechen auf eine Therapie dokumentiert werden [14, 18]. Neben den genannten Verfahren kann der Einsatz einer Positronenemissionstomografie (PET), kombiniert mit einer CT (sog. PET-CT), die diagnostische Treffsicherheit erhöhen [1]. Ein neues diagnostisches Verfahren stellt die PET mit Somatostatinanaloga markierten Positronenemittern wie z. B. 68Ga-DOTA-TOC dar. Bei diesem Verfahren werden die Vorteile der Szintigrafie mit den Vorteilen der PET kombiniert [12]. Therapie und Prognose Die Prognose wird wesentlich vom Ausmaß der Metastasierung (Lymphknotenbefall und Lebermetastasierung) bestimmt. Bei alleinigem lokalem Befall liegt die Fünfjahresüberlebensrate bei etwa 75, bei Lymphknotenbefall sinkt die Rate auf 60 und beträgt bei Lebermetastasen nur noch 20 bis 25 [16]. Die Therapie der Wahl von NET des Dünndarms ist die Resektion. Aufgrund der deutlich schlechteren Prognose bei Metastasierung sollte eine ausgedehnte Operation mit Segmentresektion und regionaler Lymphadenektomie durchgeführt werden. Intraoperativ muss der gesamte Intestinaltrakt sorgfältig untersucht werden, um mögliche Zweit-NET (in 20– 40 der Fälle) zu entdecken [16]. Auch wenn schon Leber- und Lymphknotenmetastasen oder eine peritoneale Beteiligung vorliegen, sollte die Operation angestrebt werden. Zum einen werden hierdurch, wie im vorliegenden Fall, die lokalen Symptome behandelt, zum ande- ren werden die Aussichten einer medikamentösen Therapie verbessert [15]. Zum Zeitpunkt der Diagnose ist die Prognose im Einzelfall oftmals nur schlecht abzuschätzen, da die Geschwindigkeit des Tumorwachstums nicht bekannt ist. Karzinoide des Jejunums metastasieren früh (<2 cm Größe) in die regionalen Lymphknoten und später in die Leber. Bei 10 bis 20 der Patienten mit NET des Mitteldarms tritt das Karzinoidsyndrom auf. Somatostatinanaloga ermöglichen bei den meisten Patienten eine effektive Beeinflussung der Symptomatik. Der antiproliferative Effekt der Somatostatinanaloga ist geringer ausgeprägt als die symptomatische Wirksamkeit. Komplette Remissionen sind sehr selten; bei weniger als 5 der Patienten kommt es zu einer partiellen Remission. Ein „stable disease“ lässt sich bei 40 bis 50 der Patienten nachweisen. Bei der verbleibenden Hälfte der Patienten kommt es trotz guter Symptomkontrolle zu einer Tumorprogression [3, 4]. Neben Somatostatinanaloga kommt auch Interferon-α zum Einsatz. Auch für Interferon-α ist eine Symptomkontrolle und eine Kontrolle der Tumorprogression beschrieben. Die Ansprechraten scheinen insgesamt aber unter denen der Somatostatinanaloga zu liegen, die Nebenwirkungsrate ist allerdings deutlich höher. Eine Kombinationstherapie der beiden Substanzen bringt gegenüber den Einzelsubstanzen keinen Vorteil [8]. Die Chemotherapiesensitivität von gut differenzierten NET ist relativ gering; Streptozotocin, Doxorubicin, Melphalan und 5-Fluorouracil (5-FU) sind die wirksamsten Substanzen. Unter Abwägung der Wirkung und Toxizität wird in der Regel 5-FU oder Doxorubicin der Vorzug vor Streptozotocin gegeben [11]. Bei niedrig differenzierten und metastasierten NET gilt dagegen die systemische Chemotherapie mit Etoposid und Cisplatin als Therapie der Wahl [17]. Die Kombination von anderen Substanzen wie Paclitaxel/Carboplatin/Etoposid [10] oder Capecitabin/Oxaliplatin wird ebenfalls angewandt, scheint aber keinen Überlebensvorteil zu bringen [11]. Insgesamt ist die Prognose mit einem Zweijahresüberleben von unter 20 bei gering differenzierten NET auch unter einer systemischen Chemotherapie schlecht. Ein viel versprechendes neues Therapieverfahren – besonders bei Patienten mit einer hohen Somatostatinrezeptorexpression des Tumors oder der Metastasen und langsam wachsenden Tumoren – stellt die Kopplung von Somatostatinanaloga (es handelt sich hierbei um kleine spezifische Peptide) mit radioaktiven Strahlern dar. Zum Einsatz kommen u. a. die Kombinationen aus DOTA-TOC (Octreotid) oder DOTA-LAN (Lanreotid) mit dem β-Strahler 90Yttrium oder aus DOTA-TATE (Octreotate) und 177Lutetium. Diese Substanzen binden selektiv an Somatostatinrezeptoren exprimierende Tumoren und Metastasen und bestrahlen diese gezielt von „innen“. In mehreren klinischen Studien konnte gezeigt werden, dass 27 bis 39 der so behandelten Patienten eine zumindest partielle Remission erreichten [5]. Die Therapie ist prinzipiell gut verträglich, kann aber im Einzelfall zur Myelosuppression und besonders zur Nephrotoxizität führen. Fazit für die Praxis Bei Patienten mit rezidivierenden Oberbauchschmerzen unklarer Genese sollte auch bei Fehlen einer typischen Karzinoidsymptomatik differenzialdiagnostisch ein neuroendokriner Tumor des Dünndarms in die Überlegungen einbezogen werden. Dies gilt insbesondere bei auffälliger Darstellung der Mesenterialwurzel im CT-Abdomen und dem Verdacht auf einen segmentalen Ileus ohne Nachweis eines Tumors in der Bildgebung. Korrespondierender Autor Dr. Dr. E. Biecker Medizinische Klinik und Poliklinik I, Universitätsklinikum Bonn Sigmund-Freud-Str. 25, 53105 Bonn [email protected] Interessenkonflikt. Es besteht kein Interessenkonflikt. Der korrespondierende Autor versichert, dass keine Verbindungen mit einer Firma, deren Produkt in dem Artikel genannt ist, oder einer Firma, die ein Konkurrenzprodukt vertreibt, bestehen. Die Präsentation des Themas ist unabhängig und die Darstellung der Inhalte produktneutral. Der Internist 10 · 2006 | 1071