Allgemeine Anatomie des Abwehrsystems
Werbung

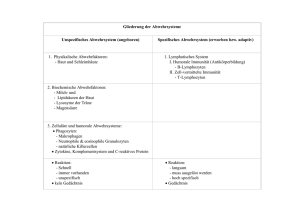
Allgemeine Anatomie des Abwehrsystems: Angeborene, unspezifische Abwehr: Komplementsystem (MHC III) Granulozyten Makrophagen Non-T, Non-B-Lymphozyten (Natürliche Killerzellen) Erworbene, spezifische Abwehr: B-Lymphozyten T-Lymphozyten Major histocompatibility Complex (MHC) I und II Die Zellen der Immunreaktion sind überwiegend Mesenchymderivate und sind z.T. in Geweben und Organen zusammengefaßt, die reich an Lymphozyten sind. Primäre (zentrale) lymphatische Organe: Knochenmark B-Lymphozyten fetale Leber B-Lymphozyten Thymus T-Lymphozyten Funktion: Proliferation und Differenzierung lymphatischer Stammzellen zu reifen Lymphozyten (Erwerb der Immunkompetenz; Ausstattung mit spezifischen Antigenrezeptoren) durch somatische Rekombination. Sekundäre (periphere) lymphatische Organe: Lymphknoten mit Lymphgefäßen Waldeyer-Rachenring (Tonsilla palatina, pharyngea, lingualis) Milz Peyer-Plaques Mukosaassoziierte solitäre Lymphfollikel des Magen-Darm-Traktes Funktion: Speicherorgane für reife, immunkompetente Zellen. Bei entsprechendem funktionellen Reiz können die verschiedenen Lymphozyten hier proliferieren (klonale Selektion), bevor die Freisetzung in die Blut- und Lymphbahn erfolgt (Lymphozytenrezirkulation). Differenzierung der Zellen des Immunsystems: Alle Zellen stammen von pluripotenten Stammzellen des Knochenmarks ab. a) Myeloische Differenzierung: Polymorphkernige Granulozyten: basophile (1%) neutrophile (60%) eosinophile (3%) Mononukleäre Granulozyten: Cave: In der Regel Proliferation im Knochenmark, dann über Blutbahn in Peripherie. Monozyten (6%) Makrophagen wahrscheinlich auch antigenpräsentierende Zellen wie die sich aus den Langerhanszellen entwickelnden interdigitierenden dendritischen Zellen (IDC) ( Antigenpräsentation an T-Lymphozyten) und follikuläre dendritische Zellen (FDC) ( Antigenpräsentation an BLymphozyten) Hilfszellen: Mastzellen weitere antigenpräsentierende Zellen Thrombozyten b) lymphatische Differenzierung: Nach Erwerb der Immunkompetenz im Thymus Ansiedelung in peripheren lymphatischen Organen, die sie häufig wechseln. Dort bei funktioneller Stimulation Proliferation. - B-Lymphozyten T-Lymphozyten Non-T, Non-B-Zellen (10% der L. im Diff-BB) (70% der L. im Diff-BB) (20% der L. im Diff-BB) Reihenfolge des Einsetzens bei Entzündungsreaktionen: Unspezifische Entzündungsreaktion: Basophile Granulozyten und Mastzellen: Ausschüttung folgender Entzündungsmediatoren Leukotriene, Prostaglandine, Histamin: Durchblutungsförderung durch Vasodilatation Erhöhung der Kapillarpermeabilität (Histamin), dadurch Austritt von Blutplasma und Leukozyten in das Interstitium Heparin: Verhinderung der lokalen Blutgerinnung sowie Bindung von Histamin Chemotaktische Faktoren: Anlockung von Leukozyten Einschub: Auch Makrophagen sind zum Sezernieren von Leukotrienen, Prostaglandinen und chemotaktischen Faktoren befähigt, wodurch diese ebenfalls die Entzündungsreaktion einleiten können. Neutrophile Granulozyten: Diapedese (s.o.) des Endothels, durchwandern amöboid das entzündete Gewebe In das Gewebe eingedrungene Bakterien werden durch von den Neutrophilen abgegebene Produkte im Wachstum behindert, abgetötet und schließlich phagozitiert. Anschließend gehen letztere zugrunde und setzen proteolytische Enzyme frei (Schaffung eines Einschmelzungsherdes / Eiter) Eosinophile Granulozyten: Diapedese Freisetzung von Major Basic Protein (Abtötung von Fremdzellen und Parasiten) Spezifische Entzündungsreaktion: Bindung von Antigen-Antikörper-Komplexen, die anschließend durch Neutrophile und Makrophagen phagozitiert werden Mononukleäre Phagozyten (Monozyten): Monozyten verlassen Blutbahn auch ohne akuten Anlaß, um das Bindegewebe mit Sicherheitsreserve von Makrophagen zu versorgen. Bei Entzündung vermehrte Anlockung durch chemotaktische Faktoren der aktivierten Komplementkaskade und Mastzellen. Phagozytose: Mikroorganismen und Tumorzellen (Rezeptor für Fc-Region von Antikörpern und Komplementproteinen, daher bessere Phagozytose bei entsprechend opsonierten Antigenen) Degenerierte körpereigene Zellen / Gewebetrümmer Anorganische Partikel Sekretion: Leukotriene, Prostaglandine (s. Basophile) Wachstumsfaktoren Kapillarisierung, Bindegewebsbildung (Wund- und Entzündungsheilung!) Antigenpräsentation (Brücke zur spezifischen Abwehr): Bindung von Fragmenten der Fremdproteine (8-24 AS) an MHC II – Proteine an der Makrophagenoberfläche, die T-Helferzellen präsentiert werden Hilfszellen Mastzellen (s. Basophile) Antigenpräsentierende Zellen (durch Zytokine über Ausbildung von MHC II – Proteinen dazu befähigt werden können z.B. Endothelzellen, Astroglia oder B-Lymphozyten) Thrombozyten Freisetzung von vasoaktiven und kapillarpermeabilitätssteigernden Substanzen sowie chemotaktischen Faktoren Spezifische Entzündungsreaktion: Einschub: Immuninkompetente Lymphozyten Ausbildung der Immunkompetenz durch somatische Rekombination in - fetale Leber / Knochenmark B-Lymphozyten - Thymus T-Lymphozyten Beide Arten entsprechen den kleinen Lymphozyten. Große Lymphozyten stellen Non-T, Non-B-Zellen (natürliche Killerzellen) dar. B-Lymphozyten / Humorale Immunität: Lokalisation im Knochenmark und B-Arealen der peripheren lymphatischen Organe Gegen Fremdproteine gerichtete Rezeptoren an der Zelloberfläche; nach Kontakt mit Antigen Umwandlung in Plasmazellen (Antikörperbildung) und B-Gedächtniszellen Erneuter Antigenkontakt: Zentroblasten Zentrozyten Plasmazellen (in der Regel nicht in der Blutbahn, Antikörperproduktion und Abgabe derselben in die Blutbahn; dort Bindung an gelöste und zellgebundene Antigene T-Lymphozyten / Zelluläre Immunität (Cave: Nur Erkennung zellgebundener Antigene): T-Gedächtniszellen: Lokalisation in der parakortikalen Zone bei Antigenpräsentation Bildung von T-Lymphoblasten ( Helferzellen, Supressorzellen, Killerzellen) T-Helferzellen Erkennung von MHC II – gebundenen Antigenen an antigenpräsentierenden Zellen Aktivierung von B-Lymphozyten und T-Killerzellen T-Supressorzellen negative Rückkopplung zur Vermeidung einer Endlosstimulation T-Killerzellen Abgabe in Blut- und Lymphbahn Erkennung von - körpereigenen MHC I /Fremdpeptid-Komplexen - allogenen (körperfremden) MHC I / Peptid-Komplexen Vernichtung der entsprechenden Zelle durch Proteasen und zytotoxische Substanzen Non-T, Non-B-Zellen: Unspezifische zytotoxische Aktivität gegen Tumorzellen und virusinfizierte Zellen Sekretion von Zytokinen Proteine des Major histocompatibility complex: MHC I: An der Oberfläche aller Körperzellen, innerhalb eines Individuums identisch Bindung einer Sequenz intrazellulär synthetisierter Proteine MHC II: Exprimierung an der Oberfläche antigenpräsentierender Zellen MHC III: Komponenten des Komplementsystems Erwerb der Immunkompetenz (primäre lymphatische Organe): Lymphatische Stammzellen weisen einen homogenen DNA-Bestand auf. Im Laufe des Erwerbs der Immunkompetenz werden die Gene zur Expression der Antikörper bei jeder Teilung neu kombiniert (somatische Rekombination). Spezifizierung auf Antigene (sekundäre lymphatische Organe): Bei einem erste Antigenkontakt proliferieren diejenigen Klone, deren Antikörper am besten zum präsentierten Fremdprotein passen. Dabei treten Mutationen in der antikörperspezifizierenden DNA auf. Tochterzellen, deren Rezeptoren dem Antigen entsprechen, proliferieren weiter und werden zahlenmäßig verstärkt. (klonale Selektion). Bei wiederholter Konfrontation mit demselben Antigen erfolgt dann eine direkte Vervielfältigung der entsprechenden Funktionszellen. Für neu auftretende Antigene stehen noch genügend „jungfräuliche“ Lymphozyten zur weiteren klonalen Selektion zur Verfügung.