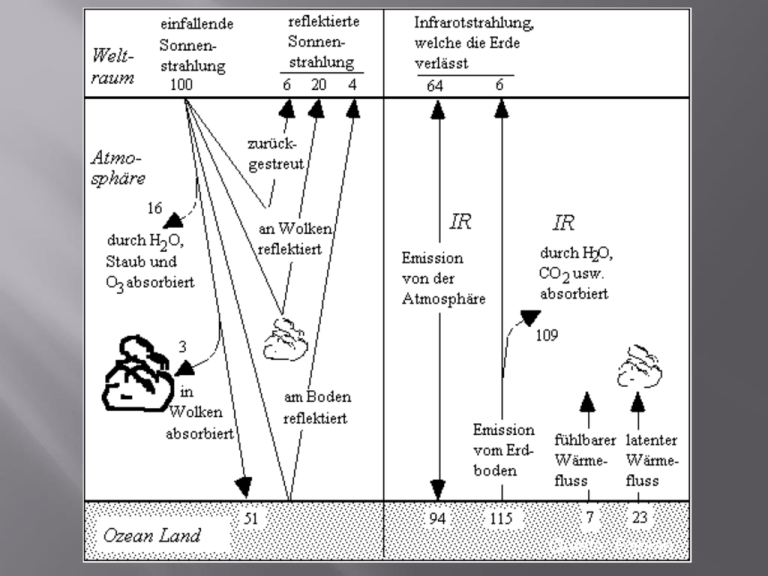
Quelle: Fabian
1 kg Wasser zu verdampfen braucht 2,256∙106 J
1 kg Eis zu schmelzen braucht 3,338∙105 J
Spezifische Wärme von flüssigem Wasser: 4180 J kg-1 K-1
Mit der Energie, die notwendig ist, um 1 kg 0°C Eis zu
schmelzen, kann 1 kg 0°C Wasser auf ? °C aufgeheizt werden?
Quelle: Alpine Naturschau
Grossglockner Hochalpenstrasse
Wien (178 m)
65 Frosttage
840 mm Niederschlag
Quelle: Alpine Naturschau
Grossglockner Hochalpenstrasse
Quelle: Alpine Naturschau
Grossglockner Hochalpenstrasse
Die untere Troposphäre ist eine ziemlich
reaktionsträge Gasmischung.
Je höher wir in der Atmosphäre hinaufsteigen, desto
mehr spielen photochemische Reaktionen eine Rolle.
In über 90 km Höhe.
Ein auf Hochtouren laufender
chemischer Reaktor!
Die intensive UV-Strahlung
hat Energien in der
Größenordnung der Energien
von chemischen Bindungen,
produziert eine komplizierte
Mischung von Atomen, Ionen
und Molekülfragmenten.
Sonnenaufgang über
der Thermosphäre
aufgenommen am 28.
Nov. 1983 vom Space
Shuttle Columbia NASA
Night Airglow (Ursache: UV-Strahlung der
Sonne)
Entdeckt 1868 von Anders Ångström
Manche der Photodissoziationsprozesse
führen zu Atomen und Ionen in angeregten
Elektronenzuständen, welche die
überschüssige Energie als sichtbares Licht
emittieren.
Die Rückkehr in den Grundzustand kann
sehr verzögert sein, sodass noch Stunden
nach Sonnenuntergang ein nächtlichen
Leuchten des Himmels zu beobachten ist, das
mindestens ebensoviel Licht produziert wie die
Sterne.
Ebenso wie das Nordlicht (Aurora) hat der
night airglow bei bestimmten Wellenlängen
starke Emissionen. Grünes Licht bei 557,7 nm,
rotes Licht bei 630 nm (beides SauerstoffEmissionen).
NASA 15. September 2011
Night airglow over Brisbane,
Australia
Aurora (Ursache: Sonnenwind)
Aurora Borealis Seen From Space by
NASA
Ein energiereicher Strom aus Elektronen und
Protonen und Alfa-Teilchen (Plasma) aus der
Sonnencorona, der ständig auf die
Magnetosphäre der Erde prallt. Benötigt 2-4 Tage
von der Sonne bis zur Erde.
Wird durch das Magnetfeld der Erde so
abgelenkt, dass er die Erde umfließt.
Nur in den Polargebieten, wo die Feldlinien des
Erdmagnetfeldes nahezu senkrecht zur
Oberfläche verlaufen, können die geladenen
Teilchen in die Erdatmosphäre eindringen und
erzeugen die Polarlichter (Aurora) simultan an
beiden Polen.
In Zeiten intensiver Sonnenfleckenaktivität kann
der Sonnenwind auch niedrigere Breiten erreichen
und bis auf 150 km herunterkommen (=
Geomagnetischer Sturm = Abschwächung des
Erdmagnetfelds ausgelöst von
Schockwellenfronten des Sonnenwindes).
Plasma-Ausbruch aus
der Sonnencorona
Bild: U.S. National
Oceanic and
Atmospheric
Administration
Beginnt in der oberen Mesosphäre in 60 km Höhe und endet in der
unteren Hälfte der Thermosphäre in 600 km Höhe.
Die Ionosphäre entsteht durch Absorption solarer UV und
Gammastrahlung.
Auch die kosmische Höhenstrahlung und Meteoriten, die in der
Erdatmosphäre verglühen, sind beteiligt
Es entstehen positive Ionen und freie Elektronen und somit ein
elektrisch leitender Bereich der Atmosphäre.
Die Schichtung der Elektronendichte wird mit den Buchstaben D, E, F1
und F2 gekennzeichnet. F2 bleibt auch in der Nacht bestehen, die
anderen verschwinden durch Rekombination
Die rund-um-die-Welt Radiokommunikation beruht auf der sukzessiven
Reflexion von Radiowellen zwischen bestimmten Schichten der
Ionosphäre und der Erdoberfläche.
Ob Reflexion oder Absorption der Radiowellen stattfindet, hängt von
der Konzentration an geladenen Partikeln und von der Wellenlänge der
elektromagnetischen Strahlung ab.
Die Stratosphäre (geschichtete Sphäre) ist im Gegensatz zur
Troposphäre stabil geschichtet, da sie von oben erwärmt
wird (durch exotherme chemische Reaktionen, vor allem die
Ozonbildung).
Am Boden der Thermosphäre (90 km Höhe) ist praktisch
alle Strahlung unterhalb 170 nm verschwunden.
Es gibt aber eine sehr wichtige Ausnahme: Ein starker Peak
der Sonnenemission, die Lyman-α-WasserstoffEmissionslinie bei 121,57 nm ist imstande, in die obere
Stratosphäre durchzudringen.
Diese Wellenlänge wird sehr stark von O2 absorbiert, was
zur Dissoziation führt.
Quelle:
Fabian
Die Stratosphäre ist im Gegensatz zur
Thermosphäre eine für diese Reaktion
ausreichend dichte Atmosphärenregion, auch
die Temperatur ist niedrig genug.
O2 + O + M (=Stoßpartner)
Exotherme Reaktion!
O3 + M
ΔH=-105 kJ/mol
Ozon ist ein wenig stabiles Molekül.
Absorption von Licht in jeder Region des Spektrums, angefangen
von IR<1200 nm bis hin zum kurzwelligen UV spaltet Ozon:
O3
O2 + O
Die erste starke Absorptionsbande tritt im Hartley-Kontinuum
auf, das bei 320 nm beginnt und sich zu kürzeren Wellenlängen
fortsetzt.
Es ist diese Absorption,die das Leben auf der Erde vor der
kurzwelligen UV-B Strahlung schützt.
UV-B: 280<λ<320 nm
UV-A: 320<λ<400 nm
Ozon ist die zentrale Spezies der stratosphärischen
Chemie.
In der Ozonschicht (10 – 80 km Höhe, Peak bei 25 km)
gibt es nirgends mehr als 10 Ozonmoleküle pro 1 Million
Luftmoleküle.
90% des gesamten Ozons befinden sich in der
Stratosphäre, 10% in der Troposphäre.
Die konstante Konzentration an Ozon wird durch ein
Fließgleichgewicht zwischen Ozonaufbau und
Ozonabbau erreicht.
The unit is named after G.M.B. Dobson, one of the first scientists to investigate
atmospheric ozone (~1920 - 1960). He designed the 'Dobson Spectrometer' - the
standard instrument used to measure ozone from the ground. The Dobson
spectrometer measures the intensity of solar UV radiation at four wavelengths, two
of which are absorbed by ozone and two of which are not.
Centre for Atmospheric Science, University of Cambridge
1)
2)
Photodissoziation bei Wellenlängen bis zu 1200 nm
Ozonzerstörungsreaktion durch Sauerstoffatome:
O3 O O2 O2
Ist wie die Ozonbildungsreaktion exotherm und trägt
daher zur Erwärmung der Stratosphäre bei.
310 nm
Der bei der Photolyse gebildete
atomare Sauerstoff befindet sich im
Grundzustand (Triplett-P oder 3P)
310 nm
Der bei der Photolyse gebildete
atomare Sauerstoff befindet sich im
angeregten Zustand (Singulett-D
oder 1D)
O
O*
O
O*
2px 2py 2pz
2px 2py 2pz
2s
2s
1s
1s
AO
triplett,
paramagnetisch
AO
singulett,
diamagnetisch
Die hierdurch gebildeten Substanzen sind äußerst
reaktive Radikale.
Bewirken katalytische Reaktionen, durch die die
Ozonschicht erheblich modifiziert wird.
Quelle: Mikrobielle
Nitrifikation und
Denitrifikation in Böden und
Sedimenten
Reagiert in der Stratosphäre
mit dem angeregten
Sauerstoffatom
NO zerstört Ozon
Dies führt dazu, dass die
Ozonschicht ca. 25% weniger
Ozon enthält, als es ohne
diesen Prozess der Fall wäre.
N2O O NO NO
NO O3 NO2 O2
UV-Strahlung mit Wellenlängen <310 nm
dringt, wenn auch geschwächt, bis in die
Troposphäre.
Dort gibt es zwar wesentlich weniger
Ozon als in der Stratosphäre, doch wird
genug O* gebildet, um aus dem
allgegenwärtigen Wasserdampf das
Hydroxylradikal zu erzeugen.
Das OH Radikal ist sehr reaktiv und löst in
der Troposphäre äußerst wichtige
Reaktionsketten aus.
In der Stratosphäre entsteht das OH
Radikal trotz des viel geringeren
Wasserdampfgehaltes nach dem gleichen
Mechanismus. Kann auch dort von
grundlegender chemischer Bedeutung
sein!
H 2O O OH OH
*
UV-Strahlung mit λ<242 nm kann das O2
Molekül photolysieren. Dabei entsteht
atomarer Sauerstoff O.
Das geschieht nur, während die Sonne
einstrahlt.
Es bilden sich „ungerade“ SauerstoffKomponenten: O, O* und O3.
Nach Beendigung der Einstrahlung (in der
Nacht oder Polarnacht) bleibt davon nur
das Ozon erhalten, denn O und O* wird
durch Stoßreaktionen in O2 oder O3
übergeführt.
Die globale Ozon-Verteilung ist durch die allgemeine Zirkulation
der Atmosphäre wesentlich mitgeprägt.
Quelle:
Forkel
Für den sonnenbeschienenen Teil der Atmosphäre kann man
die Einstellzeit des photochemischen Gleichgewichts
zwischen den Sauerstoff-Spezies (O2, O, O*, O3) berechnen
(=Relaxationszeit tR).
Hängt ab von der O2 Konzentration und der UV Strahlung
und damit von der Höhe.
tR = ca. 10 sec. in 80 km Höhe
tR = ca. 1 Jahr in 20 km Höhe.
In der Mesosphäre und oberen Stratosphäre herrscht
immer photochemisches Gleichgewicht.
Die Ozonkonzentration als Funktion der Höhe lässt sich
also theoretisch berechnen.
In der unteren Stratosphäre wird der Einfluss der
atmosphärischen Dynamik bedeutend, Abweichungen vom
Modell!!
Konzentrationsmaximum in 25 km Höhe
Ozon-Konzentration fällt in allen
Höhenbereichen von niederen zu höheren
Breiten hin ab,
weil die solare UV Strahlung mit wachsender
Breite immer schräger und damit ineffektiver
einfällt.
Quelle:
Fabian
2,5 mm am Äquator
4,5 – 5,5 mm (je nach Jahreszeit) in hohen nördlichen
Breiten, Maximum auf dem Nordpol!
Auf der Südhalbkugel nimmt die Ozon-Schichtdicke
nur bis zu einem Maximum bei 55° S-Breite zu, von da
zum Südpol wieder etwas ab.
Ursache: Aufgrund der unterschiedlichen Land-SeeVerteilung verläuft die Allgemeine Zirkulation beider
Hemisphären nicht völlig symmetrisch.
Erfolgt heute von Satelliten aus.
Dabei misst man die atmosphärische IR-Emission bei
9600 nm (= Peak des O3 im „infraroten Fenster“ der
Atmosphäre),
oder die von der Erdoberfläche zurück gestreute UVStrahlung.
Die IR-Technik liefert auch Messdaten auf der
Nachtseite der Erde.
Berechnet man die Ozonschichtdicke nach den
reinen Sauerstoff-Reaktionen, so erhält man
einen Wert, der um 30% höher ist als der
gemessene Wert.
Dies ist auf katalytische Ozon zerstörende
Prozesse durch Spurengase zurückzuführen!
Die atmosphärischen Katalysatoren sind freie
Radikale.
X O3 XO O2
O3 h O O2
O XO X O2
Als Nettobilanz dieses katalytischen
Reaktionszyklus werden zwei Ozonmoleküle in
drei Sauerstoffmoleküle umgewandelt.
Ein Lichtquant wird benötigt:
2 O3 h 3 O2
NO
OH
Cl
bewirkt 25% Reduktion
bewirken gemeinsam 5%
Reduktion
______________________________
Insgesamt 30% Ozon-Reduktion gegenüber
den reinen Sauerstoff-Reaktionen
Die atmosphärischen Katalysatoren entstehen durch den
Abbau von Quellgasen in der Stratosphäre.
Quellgase sind - in der Troposphäre – sehr langlebige
Spurengase, die von der Erdoberfläche abgegeben werden,
und nicht oder wenig wasserlöslich sind (z.B. N2O, FCKW).
Gelangen durch troposphärisch-stratosphärische
Mischungsprozesse in die Stratosphäre.
Auch Gase, die durch Vulkanausbrüche in die Stratosphäre
geschleudert werden (H2, HCl, CO, H2O, CH4, H2S)
Die Quellgase werden in der Stratosphäre durch UVStrahlung sowie durch Reaktionen mit O* und OH
abgebaut.
Die Volumenanteile der Quellgase nehmen von einem
etwa höhenkonstanten troposphärischen Wert in der
Stratosphäre nach oben hin ab.
Die Vertikalprofile entsprechen einem stationären
Gleichgewicht zwischen den Abbauprozessen und der
Nachlieferung von unten aufgrund der
atmosphärischen Dynamik.
Als einziges Quellgas zeigt CO oberhalb 20 km einen
erneuten Anstieg der Konzentration, der auf eine
weitere CO Quelle in größerer Höhe hindeutet!
In der oberen Stratosphäre und in der Mesosphäre
wird CO durch Photolyse von CO2 gebildet, sowie
durch Oxidation von CH4.
H2S, CS2, COS, (CH3)2S, NO, N2O, NH3, CH3Cl, CH3Br, CH3I, CH4,
H2
Anthropogene Quellgase
•FCKW
•CF4 stammt aus der Aluminiumherstellung, wird
erst oberhalb 50 km abgebaut.
•Anthropogener Anstieg von N2O aufgrund der
künstlichen Stickstoff-Fixierung und Düngung
•Wasserstoff-Technologie würde zu einem
Ansteigen des H2 führen.
Quelle: Fabian
Hängt von der Höhe ab!
Der ClOx – Zyklus ist besonders im Höhenbereich zwischen 35 und
45 km wirksam.
Erst dort ist die Photolyse, die Cl aus den Quellgasen freisetzt,
ausreichend intensiv.
Auch ist erst in dieser Höhe genug atomarer Sauerstoff für die
Rückreaktion vorhanden:
ClO O Cl O2
Der ClOx Zyklus spielt also in der eigentlichen Ozonschicht
gewöhnlich keine Rolle.
Die HOx – Zyklen dominieren in oberen
Bereich der Stratosphäre und in der
Mesosphäre.
Hier entstehen HOx Radikale durch Photolyse
von H2O.
Wichtiger für die Ozonschicht ist die Zunahme
der Ozon-Abbauraten durch HOx in der
unteren Stratosphäre, die auf den HOx-Zyklus
IIa zurückzuführen ist.
Hier könnte die Wasserzufuhr durch den
Flugverkehr die Ozonschicht beeinträchtigen.
Quelle: Fabian
Es gibt auch einen BrOx – Zyklus, denn auch Br und
BrO Radikale zerstören Ozon.
Brom wurde vor allem in Halonen = FBKW (Pestizide
und Feuerlöschmittel) verwendet. (Die Produktion von
Halonen ist weltweit seit 1994 verboten).
Brom zerstört Ozon ca. 40 mal effektiver als Chlor, weil
die inaktiven „Reservoirgase“ HBr und BrONO2
weniger stabil sind und sich nur in geringen Mengen
bilden.
Atmosphärische Lebensdauer von Chlor- und
Bromatomen in der Stratosphäre: ca. 30 Jahre!
Modellrechnungen ergeben für zukünftige Jahrzehnte noch eine
3,5% ige Abnahme der Gesamtschichtdicke.
In 40 km Höhe Abnahme um 25% zu erwarten!
Die Absorption solarer Strahlung durch Ozon spielt eine wichtige
Rolle für die thermische Bilanz der oberen Stratosphäre.
Ozonabnahme führt zu starker Abkühlung in der oberen
Stratosphäre.
Stärkste Auswirkung in der Höhe des Temperaturmaximums in
50 km Höhe.
Die Ozonschicht der Arktis reagiert sehr stark auf die Abkühlung
der Stratosphäre.
Zusätzliche Ozonverluste an den Polen!!
(Forschungsstelle Potsdam des Alfred-Wegener-Instituts für
Polar- und Meeresforschung)
Natürliche Zufuhr von Chlor:
Vulkanausbrüche (HCl), Transport von
Methylchlorid (von Meeresalgen und aus
terrestrischen Ökosystemen z.B. von
immergrünen Laubbäumen abgegeben) aus der
Troposphäre.
Natürlicher Chlorgehalt der Stratosphäre: 0,6
ppbv.
Derzeitige Konzentration: ca. 3 ppbv.
2 Cl O3 ClO O2
ClO ClO M Cl2O2 M
Cl2O2 h 400nm 2 Cl O2
Nur bei sehr tiefen Temperaturen wirksam, weil
nur da Cl2O2 beständig ist.
Daher nur über der Antarktis.
Keine O Atome benötigt!
HO NO2 M HNO3 M
ClO NO2 M ClONO2 M
HNO3 und Chlornitrat sind
Reservoirsubstanzen, die Ozon nicht
angreifen.
Auf diese Weise neutralisieren sich zwei
„Ozonkiller“ gegenseitig und es entstehen
Reservoirs für reaktive Radikale.
HNO3 h 330nm HO NO2
ClONO2 h 450nm ClO NO2
•Da diese Prozesse nur im sonnenbeschienenen Teil
der Atmosphäre ablaufen, wächst tagsüber die
Konzentration der Radikale auf Kosten der
Reservoirsubstanzen.
•Nachts ist das Umgekehrte der Fall!
= ein Regelsystem: Am Tag wird Ozon sehr lebhaft
gebildet und abgebaut, nachts wo es nicht gebildet
wird, wird es auch nicht abgebaut.
Der Einfall energiereicher geladener Teilchen führt in
der Atmosphäre zur Bildung von NOx und HOx
Radikalen.
Sowohl die kosmische Höhenstrahlung (= galaktische
kosmische Strahlung) als auch der Sonnenwind spielen
eine Rolle.
Mesosphäre: HOx Radikale (durch Spaltung von H2O)
Stratosphäre: NOx Radikale (O2 reagiert mit N2)
Intensive solare Protonenausbrüche
abrupte
Verminderung der Ozonschichtdicke!
Hochenergetische γ-Strahlung erzeugt
in der Stratosphäre NO2
Ozonschicht über NOx Mechanismus
erheblich reduziert
Globale Abkühlung durch Absorption
sichtbarer Sonnenstrahlung in hohen
Atmosphärenschichten







