Skript Woche 07
Werbung
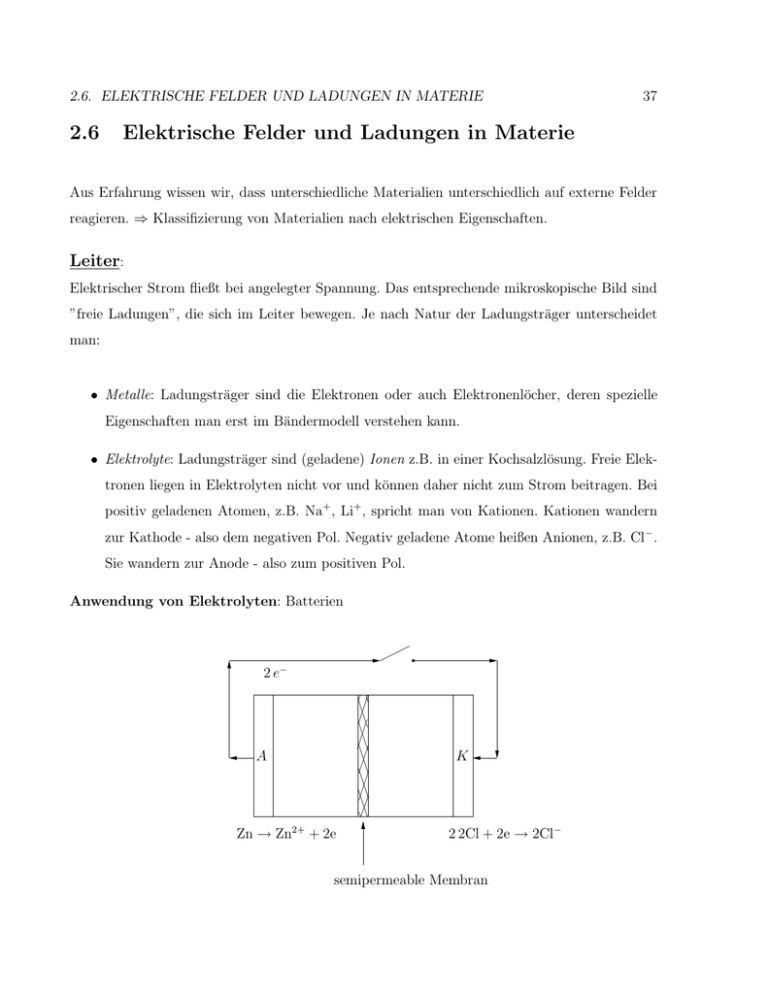
2.6. ELEKTRISCHE FELDER UND LADUNGEN IN MATERIE 2.6 37 Elektrische Felder und Ladungen in Materie Aus Erfahrung wissen wir, dass unterschiedliche Materialien unterschiedlich auf externe Felder reagieren. ⇒ Klassifizierung von Materialien nach elektrischen Eigenschaften. Leiter: Elektrischer Strom fließt bei angelegter Spannung. Das entsprechende mikroskopische Bild sind ”freie Ladungen”, die sich im Leiter bewegen. Je nach Natur der Ladungsträger unterscheidet man: • Metalle: Ladungsträger sind die Elektronen oder auch Elektronenlöcher, deren spezielle Eigenschaften man erst im Bändermodell verstehen kann. • Elektrolyte: Ladungsträger sind (geladene) Ionen z.B. in einer Kochsalzlösung. Freie Elektronen liegen in Elektrolyten nicht vor und können daher nicht zum Strom beitragen. Bei positiv geladenen Atomen, z.B. Na+ , Li+ , spricht man von Kationen. Kationen wandern zur Kathode - also dem negativen Pol. Negativ geladene Atome heißen Anionen, z.B. Cl− . Sie wandern zur Anode - also zum positiven Pol. Anwendung von Elektrolyten: Batterien PSfrag replacements +Q 2 e− −Q d A K Zn → Zn2+ + 2e 2 2Cl + 2e → 2Cl− semipermeable Membran 38 KAPITEL 2. ELEKTROSTATIK Der metallische Draht leitet die Elektronen. Die beiden Zellen werden durch eine semipermeable Membran voneinander getrennt, die nur Ionen aufgrund ihrer geringen Größe passieren lässt, jedoch undurchlässig für das Lösungsmittel der Ionen ist. Freie Elektronen gibt es praktisch nicht im Elektrolyt. K bezeichnet die Kathode in der Abbildung, die ihren Namen trägt, da die Kationen dorthin wandern. Entsprechend bezeichnet A die Anode. Durch die Elektronen, die über die externe Leitung kommen, können sich die Cl negativ aufladen und in Lösung gehen. (Die wirklichen chemischen Reaktionen sind sehr viel komplizierter, aber diese Schritte sind quasi die Essenz.) Dort lagern sie sich an die positiv geladenen Zink Kationen an. Die Energie, die durch den Energieübertrag der Elektronen vom Zink an die Chloratome gewonnen werden kann, ist so nicht einfach verpufft, sondern im Schaltkreis genutzt worden. Spannung : Energiegewinn 2 Elektronen ∆U = ∆Q 2 Elektronen Beachte: Selbst wenn der Draht ideal leitet, folgt kein unendlich großer Stromfluss, da die gezeigten Prozesse schließlich nicht unendlich schnell ablaufen können. Diesen Prozessen kann PSfrag replacements man genüge +Q tragen, indem man der Batterie einen inneren Widerstand zuordnet. −Q real ideal d Ri ≈ Stromkreis Stromkreis permeable Membran Berechnung von Leitfähigkeiten und Widerstäanden Ausgangspunkt sind ”freie” Ladungen qn . Auf Ladungen wirken ”Zufallskräfte” (Stöße) deren summierter Effekt eine Reibungskraft bewirkt. In guter Näherung gilt: FReibung = −γ · v (2.38) 2.6. ELEKTRISCHE FELDER UND LADUNGEN IN MATERIE 39 ähnlich wie in Wasser sedimentierende Teilchen. ⇒ Bewegungsgleichung m·a+γ·v =q·E Im statischen Grenzfall: a = 0; (2.39) E = const ⇒ PSfrag replacements v= q E γ (2.40) +Q E −Q d dA2 dA1 ∆l ∆l um von der Oberfläche A2 zu A1 zu gelangen. Die |v| Anzahl der Ladungen, die durch A1 in dieser Zeit treten (mit der Materialkonstannte ρ als Eine Ladung benötigt eine Zeit ∆t = (Zahlen)Dichte der freien Ladungsträger). Nq = ρ · (A1 · ∆l) ⇒ q · Nq ist die Ladung, die in der Zeit ∆t durch die Fläche A1 treten: ∆Q q · Nq q · Nq = = · |v| (2.41) ∆t ∆l/ |v| ∆l !"#$ Strom: I % 2 & q A = ·ρ · · ∆l (2.42) ! "#· E$ γ ∆l !"#$ ! "# $ Spannung: V Leitfähigkeit: σ geometr. Eigenschaft ! "# $ inverser Widerstand: 1/R ⇒ Ohm’sche Gesetz: V = R · I (2.43) 40 KAPITEL 2. ELEKTROSTATIK oder wenn das gängige Symbol U für die Spannung verwendet wird: U =R·I [R] = 1 Ω = 1C 1V "" Ohm"" Die Leitfähigkeit ist eine Materialeigenschaft. Symbol: σ. 1 l · σ A 1 l ⇒σ = · R A (2.44) R = [σ] = 1 S = 1 Ω·m "" Siemens"" Die inverse Leitfähigkeit heißt spezifischer Widerstand. Sie hat das Symbol ρ aber keine eigene S.I. Einheit. Werte für Leitfähigkeiten in S (bei Zimmertemperatur) Material Leitfähigkeit ·1 S Klasse Kohlenwasserstoffe 10−14 Nichtleiter/Isolator Diamant 10−4 Nichtleiter 2, 5 · 10−4 Nichtleiter ≈ 10−4 ≤ σ ≤≈ 104 Halbleiter undotiertes Si dotiertes Si Tellur 5 · 10−3 Leitungswasser 0, 05 Meerwasser ≈5 Aluminium, Kupfer, Gold YBa2 Cu3 O7−x ≈ 3, 5 · 107 Elektrolyt Metalle (σ stark T-abhängig) ≈ 1 bei T = 300 K (schlechter Leiter) → ∞ bei T = 30 K Supraleiter (keinen elektr. Widerstand) Wir sehen, dass die Leitfähigkeit - selbst ohne Supraleiter - extrem viele Größenordnungen abdeckt. Fast alle anderen Eigenschaften der genannten Materialien wie z.B. Dichte oder Elastizitätsmodul, variieren bedeutend weniger. Die große Bandbreite an Leitfähigkeiten kann wieder über das Bändermodell verstanden werden: Die Anzahl der freien Elektronen kann je nach Ma- 2.6. ELEKTRISCHE FELDER UND LADUNGEN IN MATERIE 41 terial und thermodynamischen Größen wir Druck und Temperatur um viele Dekaden variieren. Echte Stromspannungscharakteristik der meisten Materialien: I I g replacements PSfrag replacements +Q +Q −Q −Q U d U d Extremfall → Die Unterscheidung “leitet” bzw. “leitet nicht” ist also eher willkürlich. Bei extrem großer Spannung kann es zu einem “Durchschlag” kommen. In Luft macht sich ein Durchschlag durch einen Blitz bemerkbar. Strom-Spannungs-Charakteristika haben automatisch dann die Eigenschaft I(V ) = −I(−V ), wenn das Material entlang der Richtung des Stromlflusses spiegelsymmetrisch sind - ansonsten kann man (wie Sie später bei der Diode sehen werden) auch einen PSfrag replacements nicht-symmetrischen Verlauf haben. Siehe auch die Diskussion in der Besprechung der Aufgabe +Q Piezoelektrizität. −Q PSfrag replacements Elektrotechnisches Symbol für einen Widerstand:d +Q Serienschaltung: −Q d I I R1 = ' U = U 1 + U2 R2 R1 + R 2 ⇒ U = (R1 + R2 ) · I 42 KAPITEL 2. ELEKTROSTATIK ⇒ In Serie geschaltete Widerstände addieren sich. RSerie = R1 + R2 siehe auch 2.44 (2.45) PSfrag replacements ⇒ +Q R = −Q Parallelschaltung: d 1 1 · · (d1 + d2 ) σ A I1 I1 + I 2 I2 I1 I1 + I 2 Iges. V U = R %1 & 1 1 = + ·U R1 R2 1 = ·U Rges. Rparallel = % 1 1 + R1 R2 &−1 (2.46) Fließt durch einen Nichtleiter Ladung hindurch, entsteht dabei Wärme. Diese berechnet sich wie folgt: ∆U = V · ∆Q ( mit ∆Q = I · ∆t) → = V · I∆t ∆U ⇒ verlorene Energie pro Zeiteinheit (Leistung): = V · I = R · I 2 = V 2 /R.(2.47) ∆t Nichtleiter: Es liegen keine - oder genauer gesagt vernachlässig bar wenige - freie Ladungsträger vor. Ein externes elektrisches Feld bewirkt lediglich eine Polarisierung der Materie, z.B. durch Induzierung elektrischer Dipole (Verschiebung von Elektronenhülle gegen den Atomkern) oder die Ausrichtung vorher bereits bestehender aber stochastisch verteilter Dipole - wie z.B. in Wasser. 2.6. ELEKTRISCHE FELDER UND LADUNGEN IN MATERIE 43 ohne E-Feld PSfrag replacements PSfrag replacements isotropes Atom/Molekül +Q +Q H mit E-Feld −Q −Q d O H zufällige Orientierung d induzierter Dipol im Mittel ausgerichtet Die Polarisation berechnet sich in guter Näherung meist zu: p=α·E Für zufällig orientierte Dipole ist 'p( = 0, dagegen ist bei im Mittel ausgerichteten Dipolen 'p( = α · E. Hier steht das Symbol '...( für einen Mittelwert, also den Mittelwert über viele Atome und Moleküle. Momentan ist für uns jedoch lediglich relevant: Die Induzierung von Dipolen/Orientierung von Dipolen bewirkt eine Erhöhung der elektrostatischen Feldenergie Energiedichte = 1 ε0 εr E2 2 (2.48) εr ist die Dielektrizitätszahl und stellt eine materialspezifische Größe dar. Man kann nun bereits ahnen, dass Materialien, in denen die chemischen Bindungen einen starken ionischen Anteil haben, hohe & Werte haben, weil sich resultierende Dipole nur im externen Feld ausrichten müssen aber nicht erst induziert werden müssen. Weil Kohlenstoff und Wasserstoff praktisch dieselbe Elektronegativität haben sind die Partialladungen auf diesen Atomen quasi null. Daher 44 KAPITEL 2. ELEKTROSTATIK würden wir eine kleine Dielektrizitätskonstante für diese Materialien erwarten. Wassermoleküle hingegen haben einen großen Dipol, werden also eine große Dielektrizitätskonstante haben. In SiO2 liegen zwar große Partialladungen vor, aber das Material ist auch sehr steif, weshalb sich die Ladungen nicht gerne verschieben lassen (zudem ist die Bandlücke sehr groß) und wird daher keinen extrem großen & Wert haben. Einige Werte sind: Medium εr Vakuum 1 Polymere ≈2 Glas (SiO2 ) ≈8 Gummi ≈ 16 Methanol (CH3 OH) ≈ 30 Wasser ≈ 80 Metalle ∞ Verwendung: Dielektrika werden zur Kapazitätssteigerung von Kondensatoren, der Verhinderung elektrostatischer Entladungen oder auch als gate-Material in elektronischen Schaltkreisen eingesetzt. Dielektrika haben weitere Klassifizierungen, z.B. gibt es neben den gewöhnlichen Dielektrika: • Piezoelektrische Materialien: Verformen sich in guter Näherung linear mit einem extern anliegenden Feld, sodass die relative Längenänderung ∆l/l wie folgt vom externen E-Feld abhängt: ∆l =d·E l d ist die piezoelektrische Konstante - siehe auch die Zusatzaufgabe diese Woche. • Ferroelektrika: haben einen permanenten elektrischen Dipol und oft extrem groß Werte für εr (zum Teil > 1000).






![Elektrische Spannung U [V]](http://s1.studylibde.com/store/data/002479720_1-141ad09aa3ab46fc5af48362f775ec08-300x300.png)



