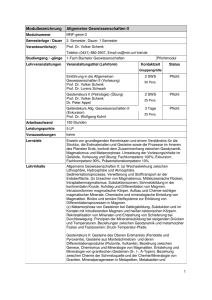
Mineralogie
Werbung

Mineralogie
LV 620.074
3 ECTS
4. Semester
Bakkalaureatsstudium Angewandte Geowissenschaften
Ronald J. Bakker
Johann Raith
SS 2007
Einleitung
1
Mineralklassen (Systematik nach H. STRUNZ)
Klasse 1. Elemente
Gediegene Metalle, Semimetalle, Nichtmetalle
Klasse 2. Sulfide
(inklusive Selenide, Telluride, Arsenide, Antimonide, Bismutide)
0.15 % der Erdkruste
Klasse 3. Halogenide
(F, Cl, Br, J)
Klasse 4. Oxide und Hydroxide
inkl. SiO2 etwa 17 % der Erdkruste
Klasse 5. Karbonate, Nitrate, Borate
Kation in Dreierkoordination: [CO3]2-, [NO3]-, [BO3]3-
Klasse 6. Sulfate, Chromate, Molybdate, Wolframate
6-wertiges Kation in Viererkoordination: [SO4]2-, [CrO4]2- etc.
Klasse 7. Phosphate, Arsenate, Vanadate
mengenmäßig untergeordnet
5-wertiges Kation in Viererkoordination: [PO4]3- etc.
Klasse 8. Silikate
etwa 80 % der Erdkruste; technisch und wirtschaftlich wichtig
[SiO4]4-, [Si2O7]6-, [Si2O6]4-, uzw.
Klasse 9. Organische Minerale
Mineralogie LV 620.074
Bakker, Raith
2
Einleitung
Webseiten
http://www.mindat.org/
Mindat.org is the largest mineral database and mineralogical reference website
on the internet. This site contains worldwide data on minerals, mineral
collecting, mineral localities and other mineralogical information.
This site is growing every day, with new mineral information,
localities and photographs added by members - whether you are interested in
mineral collecting, a student or a professional mineralogist why not join so
you can keep the site updated with information on areas you are familiar with.
http://www.mineralienatlas.de/
Mineralienatlas ist ein nicht kommerzielles Projekt von und für Besucher. Der
Schwerpunkt liegt auf Mineralogie, Paläobiologie, Geologie, Bergbau sowie
Lagerstätten (Fundstellen). Bei uns kann und soll jeder mitmachen! Es haben
sich schon 2229 Benutzer registriert. Unsere stetig wachsende Enzyklopädie
mit derzeit 23061 Seiten wird Ihnen ebenso, wie unser gut besuchtes Forum
bei der Informationssuche helfen.
http://rruff.geo.arizona.edu/rruff/
Welcome to the Rruff Project website containing an integrated database of
Raman spectra, X-ray diffraction and chemistry data for minerals.
http://de.wikipedia.org/wiki/Portal:Geowissenschaften
Die Geowissenschaften beschäftigen sich mit der Erforschung der Erde und
gehören damit zu den Naturwissenschaften. Dieses Portal bietet einen Einstieg
in den Themenkomplex der Geowissenschaften … Viel Spaß!
Lehrbücher
Klein C. (2002) Mineral Science. John Wiley & Sons, USA, pp. 641.
Matthes S. (1993) Mineralogie. Springer-Lehrbuch, 4.Auflage, Berlin-Heidelberg. pp. 461.
Offerman E. (2004) Kristalle und ihre Formen. Band 1 und 2, KristalloGraphik Verlag,
Achberg (Germany).
Putnis A. (1995) Introduction to Mineral Sciences. Cambridge University Press, BAS Printer
Ltd., Over Wallop, Hempshire, pp. 457.
Wenk H.-R., Bulakh A. (2004) Minerals, their constitution and origin. Cambridge University
Press, UK, pp. 646.
Mineralogie LV 620.074
Bakker, Raith
Einleitung
3
Verteilung der Elemente in der Erdkruste
Die chemischen Elemente sind in der Erdkruste sehr ungleichmäßig verteilt; nur 8, nämlich
Si, Al, Mg, Fe, Ca, Na, K und O sind mit mehr als 1% vertreten und bauen, vorwiegend in
silikatischer Form, zu über 98 mass% die Erdkruste auf. Zwölf weitere sind mit 0.1 bis 1%
vertreten. Die Konzentrationen aller ander Elemente sind nicht höher als 0.1% und liegen
meisten weit darunter.
Daraus wird deutlich, dass alle wirtschaftlich interessanten Elemente in irgendeiner
Weise durch geologische Vorgänge in der Kruste angereichert werden müssen, um
ökonomisch genutzt werden zu können.
In der Erdkruste
•
Ultramafische Gesteine: Cr mit Duniten und Harzburgiten in Ophiolith-Komplexen
und einigen tholeiitischen Intrusionen. Daneben Pt und andere PlatingruppenElemente (PGE), seltene Erden, Nb, Ta, Zr, P in Carbonatiten. Diamant in
Kimberliten.
•
Basische Gesteine (Gabbros, Norite, Anorthosite). Separation sulfidischer und/oder
oxidischer Schmelzen (silikatischen). Damit Anreicherung von Nickel-Kupfer + PGE
(sulfidisch) und Cr, Fe-Ti-V (oxidisch). Gravitative Absaigerung von dichteren
Kristallen aus einer weniger dichten Schmelze (z.B. Chromit in tholeiitischen
Intrusionen). Anreicherung in fluider (H2O-reicher) Restphase.
•
Granitische Gesteine i.w.S.: Hydrothermale Gänge mit Au-Ag (Ontario; Australien),
mit Pb-Zn (Harz), mit disseminiertem Cu-Mo (Butte, Montana), mit Sn-Cu (Cornwall;
Indonesien); mit Pegmatiten (H2O-reiche Differentiate der Granite): Sn, W, Nb-Ta,
Edelsteine. Dazu kommen alle Anreicherungen in Verbindung mit syenitischen
Gesteinen: Korund, Zr, Apatit (Phosphat).
•
metamorph: Meist keine echte, durch Metamorphose hervorgerufene Anreicherung,
sondern Veredelung durch Umkristallisation ursprünglich anders gearteter Lagerstätte,
z.B. Korund aus Bauxit- und Laterit (Izmir; Naxos), Siderite → Magnetit, Veredelung
von Braunkohle und Torf zu Anthrazit usw., hydrothermale Gold Ablagerungen.
An der Erdoberfläche
In diese Katagorie fallen alle sedimentären Lagerstätten. Diverse Mechanismen sind bekannt:
Chemische Anreicherung:
• vulkano-sedimentäres Milieu; submarin-exhalative Vorgänge z.B. an konstruktiven
Plattenrändern (z.B. im Roten Meer). Abhängig von der großtektonischen Situation.
Bildung von stratiformen (dh. schichtgebundenen) Lagerstätten verschiedener
Metallinhalte. Wichtigste Buntmetalllagerstätten (Pb-Zn-Cu±Ag±Au) fallen in diese
Kategorie.
•
sedimentär (ohne hydrothermale Aktivität); z.B. Kupferschiefer (Merallgehalte in
Schwarzschiefer), oolitische Eisenerze, Manganknollen; Evaporite (Salzlagerstüatten,
durch Eindampfung von Meerwasser entstanden), Nitratlagerstätten (terresrischer
Entstehung, Atacama, Chili), Phosphat (± U und V).
Mineralogie LV 620.074
Bakker, Raith
Einleitung
4
Mechanische Anreicherung:
• Seifenlagerstätten; Au, U (z.B. Witwatersrand, Südafrika), Pt-Seifen, Fe-Ti
(Ilmenitsande), Zr-Monazit Sande (Sri Lanka), Diamantseifen (Namibia): Entstehung
fluviatil (Ablagerung aus fließenden Gewässern) oder marin (als Strandseifen).
Äolisch (durch Windeinwirkung). Anreicherung aufgrund großer Dichte und
besonderer
mechanischer
wie
chemischer
Widerstandskraft
gegenüber
Transportmilieu.
Anreicherung durch Verwitterung:
• Wichtig sind Kaolinvorkommen (Keramikindustrie) durch Verwitterung granitischer
Gesteine i.w.S., Bauxite (Aluminiumerz), Garnierite (Nickel-Laterite auf
ultramafischen Gesteinen in New Caledonia), einige Mn-Erze. Schon bestehende Erze
können durch Verwitterung weiter angereichert werden → Eisener Hut.
Mineralogie LV 620.074
Bakker, Raith
Elemente
1
Elemente
Überblick Chemie
Mineralogie LV 620.074
Bakker, Raith
2
Elemente
Natürliche Elemente in die Geowissenschaften
Etwa 20 chemische Elemente kommen in der Natur in metallischer (dh. gediegener) Form
vor. Sie werden zweckmäßigerweise eingeteilt in Metalle, Halbmetalle (Metalloide) und
Nichtmetalle, je nachdem, wie die Atome gebunden sind.
Metalle
Name
Formel
Struktur
Gold-Gruppe
Gold
Silber
Kupfer
Au
Ag
Cu
kub. flächenzentriert
kub. flächenzentriert
kub. flächenzentriert
Platin-Gruppe
Platin
Pt
kub. flächenzentriert
Eisen-Gruppe
Eisen
α-Fe
kub. innenzentriert
Quecksilber-Gruppe
Quecksilber
Amalgam
Hg
Hg,Ag
flüssig!
Wismut
Bi
hexagonal
Name
Formel
Struktur
Arsen
As
hexagonal
Antimon
Sb
hexagonal
Metalloide
Nichtmetalle
Mineralogie LV 620.074
Name
Formel
Struktur
Schwefel
S
orthorhombisch
Diamant
C
kubisch
Graphit
C
hexagonal,
orthorhombisch
Bakker, Raith
3
Elemente
Metalle
Allgemeine Eigenschaften von Metallen
•
sehr dichte "Packung" der Atome: alle Bausteine (Atome) haben die gleiche Größe.
kubisch dichteste Kugelpackung
Tetraeder- und Oktaederlücken in kubisch dichteste Kugelpackung
Tetraeder- und Oktaederlücken in hexagonal dichteste Kugelpackung
Mineralogie LV 620.074
Bakker, Raith
4
Elemente
Allgemeine Eigenschaften von Metallen
•
hohe Koordinationszahl: jedes Atom ist von 12 gleichartigen Nachbarn im gleichen
Abstand umgeben, z. B. Au[12] in kubisch flächenzentrierten Gittern.
•
Struktur: kubisch flächenzentriert, kubisch innenzentriert, hexagonal flächenzentriert
flächenzentriert
innenzentriert
•
hohe Dichte
•
metallische Bindung
•
exzellente elektrische und thermische Leitfähigkeit
•
Deformierbarkeit und geringe Härte
•
Legierbarkeit
•
Dendritische Wachstumsformen
Mineralogie LV 620.074
Bakker, Raith
5
Elemente
Gold, Au
Chemismus
Au (100%), und natürliche Legierung mit Ag (30-45%) in Elektrum
Structur:
kubisch flächenzentriertes Gitter (m3m)
Ausbildung
gediegenes Gold (native gold), meist drahtförmig, dendritisch-skelettförmige Aggregate
Goldmuseum Brad (Rumänien)
Mineralogie LV 620.074
Bakker, Raith
6
Elemente
Gedingen Gold. a. Oktaeder mit typisch gekrümter Oberfläche, b. mit dendritischem Wachstum.
Eigenschaften
Härte:
Dichte:
Farbe:
Glanz:
Schmelzpunkt:
2.5 - 3
15 - 19.3 g·cm-3
goldgelb
metallisch
1064.18 ˚C
Strich: goldgelb
Vorkommen:
• primär: Berggold vor allem in hydrothermalen Ganglagerstätten mit Quarz ± Karbonat
(Tauern, Kalifornien, West-Australien); mechanische Beimengung (2%) in Arsenkies
(FeAsS) und Pyrit (FeS2), aber nicht ins Gitter eingebaut; disseminiert mit Chalcopyrit
in sogenannten "porphyry copper" Lagerstätten (0.5 - 5 g/t), Nebenprodukt der CuGewinnung.
• sekundär: Anreicherung in Seifen (rezent und fossil), Seifengold, Waschgold
(nuggets), aufgrund hoher Dichte und Widerstandsfähigkeit. Flußläufe und
Meeressande (Rheingold, Yukon, Indonesien). Fossil in der größten Goldlagerstätte
der Welt: Witwatersrand (S.-Afrika).
Gewinnungsproblematik:
• geringe Konzentration der Erze → große Abraummengen
• Zyanidlaugung (KCN-, NaCN-Laugen)
• Amalgamierung (Fällung mit Quecksilber)
Verwendung: Währungsmetall; Elektronikindustrie; Chemie; Zahntechnik; Schmuckindustrie
Kupfer, Cu
Struktur: kubisch flächenzentriert (m3m)
Eigenschaften
Härte:
Dichte:
Farbe:
Glanz:
Schmelzpunkt:
2.5 - 3
8.95 g·cm-3
kupferrot, braun, schwarz
metallisch
1085 ˚C
Strich: kupferrot
Ausbildung: meist dentritische und formlose Aggregate, Oxidationshaut
Mineralogie LV 620.074
Bakker, Raith
7
Elemente
Silber, Ag
Struktur: kubisch flächenzentriert (m3m)
Eigenschaften
Härte:
Dichte:
Farbe:
Glanz:
Schmelzpunkt:
2.5 - 3
10.1 - 11.1 g·cm-3
silberweiß
Strich: silberweiß bis gelblich
metallisch, mattschwarzen Anlauffarben
961.78 ˚C
Ausbildung: Kristallisiert in draht-, haar- oder moosförmigen bis dendritischen Aggregaten
oder in einer feinkristallinen Masse
Platin, Pt
Chemismus
Bis zu 21% Fe in Gitter eingebaut, daneben treten gewöhnlich wechselnde Gehalte an anderen
Platingruppenelementen (PGE) auf (Palladium, Osmium, Iridium, Ruthenium, Rhodium)
Struktur: kubisch flächenzentriert (m3m)
Eigenschaften
Härte:
Dichte:
Farbe:
Glanz:
Schmelzpunkt:
4 - 4.5
14 - 21.45 g·cm-3
grauweiß
metallisch
1768 ˚C
Strich: grauweiß
Vorkommen
• Ultrabasische Gesteine mit Chromit (FeCr2O4) (Ural)
• Abpressungen basischer (gabbroider) Gesteine (Bushveld-Komplex, S.-Afrika;
Stillwater-Komplex, USA) und Pentlandit-Magnetkies-Anreicherungen
• Diskordante, ultramafische Pegmatit-Pipes (Bushveld)
• Chromit Horizonte (Bushveld)
• In Fluß-Seifen (Ural, Alaska)
Eisen, Fe
Chemismus
Beschränkt mischbar mit Ni
Vorkommen
Elementares Eisen hat in irdischen Vorkommen nur ganz geringe Bedeutung, ist aber in
Eisenmeteoriten (Kamacit) und lunaren Basalten häufig. Selten: näturlicher
Hochoffenprozess, z.B. wenn der FeO-Gehalt basischer Magmen beim Durchtritt durch
Kohlenflöze reduziert wird (Grönland). Der Erdkern besteht wahrscheinlich aus Ni-reichem
Eisen (Taenit).
Mineralogie LV 620.074
Bakker, Raith
8
Elemente
Struktur: kubisch innenzentriert (α-Fe), Polymorphie bei höheren Temperaturen und Drucken.
bcc = body-centred cubic
(innenzentriert)
fcc = face-centred cubic
(flächenzentriert)
hcp = hexagonal closest
packed
ortho = orthorhombic
(also double hexagonal
closest packed)
Eigenschaften
Härte:
Dichte:
Farbe:
Glanz:
Schmelzpunkt:
Mineralogie LV 620.074
4-5
7.3 - 7.9 g·cm-3
grauweiß
metallisch
1535 ˚C
Strich: grau
Bakker, Raith
9
Elemente
Nichtmetalle
Kohlenstoff, C
Polymorphie:
Graphit
Diamant
hexagonal (bzw. orthorhombisch) (6/mmm)
kubisch (m3m)
Vergleich der Struktur von Diamant und Graphit
Stabilitätsbedingungen der Kohlenstoff-Modifikationen
Diamant-Struktur, vergleich mit kubisch dichteste
Kugelpackung (Allgemeine Eigenschaften von
Metallen).
Mineralogie LV 620.074
Bakker, Raith
10
Elemente
Vergleich Diamant - Graphit
Chemismus
Kristallsystem
Härte nach Mohs
Dichte
Lichtbrechung
Glanz
Farbe
Spalbarkeit
Therm. Leitfähigkeit
Elek. Leitfähigkeit
Diamant
C[4]
kubisch
10! extrem hart
3.51 g·cm-3
n = 2.417; hohe Dispersion!
Diamantglanz
farblos, gelb, blau, etc.
deutlich nach (111)
exzellent
Isolator bis Halbleiter
Graphit
C[3]
hexagonal/orthorohombisch
1-2! weich, blättrig
2.09 - 2.23 g·cm-3
Metallglanz, matt
schwarz, grau
volkommen (0001)
guter Leiter
Bedeutung von Graphit
• Schmelztiegel; Graphitelektroden; Bleistiftminen; Kohlestäbe
• Schmier- und Poliermittel
• Stahl- und Gießereigraphit
• Elektrographit: Reaktortechnik, Abbremsen von Neutronen
• Kunststoffindustrie
Ein Großteil des Graphitbedarfs wird heute künstlich gewonnen (verkoken von Braunkohle,
Steinkohle, Erdöl und Peche, aber auch Kunststoffe)
Vorkommen von Graphit:
Häufig in metamorphen Gesteinen durch Reduktion von primärer organischer Substanz (z.B.
Kohle) durch Temperatur (Sunk, Kaisersberg). Daneben in magmatischen Gesteine (nur bei
niederigen Sauerstoff-Partialdrucken) und in Meteoriten. Wichtig sind mit Graniten
assoziierte Graphitgänge (Sri Lanka, Madagaskar, USA), die durch Oxidation von Methan
enstanden sind.
Wachstumformen Diamant:
Mineralogie LV 620.074
Bakker, Raith
11
Elemente
Wie und wo entsteht Diamant?
Diamant ist die HochdruckModifikation von Kohlenstoff;
an alte Kratone gebunden
kontinentale Kollisionszonen
mit UHP Metamorphose (z.B.
China). Muttergesteine und
Alter der Diamanten:
•
•
•
Kimberlite und
Lamproite: 50 - 1600
Ma; Diamanten sind
meist älter!
Harzburgite: ca. 3.3 Ga
Eklogite: ca. 1 bis 3 Ga
Sekundäre Anreicherungen in
Seifen (fluviatil und marin).
Große Vorkommen an der
Küste von Namibia, Zaire und
Angola (Abbau aus 2000 m
Tiefe). Seifendiamanten sind
meist kleiner als solche in
Primärlagerstätten, aber oft
von besseren Qualität und
Haltbarkeit.
Bedeutung von Diamant:
•
•
•
•
Edelstein, Wertanlage: Brillantschliff, Schmuckstein
Schneiden, Schleifen, Bohren (auch synthetisch erzeugt = Industriediamanten)
Elektronikindustrie
Wissenschaft: Einschlüsse in Diamant als einzige Zeugen für Prozesse im tieferen
Erdmantel
Bewertungskriterien (die 3C)
•
•
•
Carat - Gewicht in Karat (1 Karat = 0.2 Gramm)
Clarity - Reinheit, Feuer
Colour - Farbe (N → gelb; B → blau)
Der größte bisher gefundene Diamant ist der "Cullinan" (British Crown Jewel, 1905) mit
3106 ct (621.2 Gramm). Der "Cullinan 1" (oder "Great Star of Africa") ist ein 530 Karat
schwerer Diamant, welcher aus dem "Cullinan" herausgeschnitten wurde.
Carat size
0.5 carat
1.0 carat
1.5 carats
2.0 carats
Mineralogie LV 620.074
Cost per carat (US$), 2007
3,000
6,500
8,500
13,000
Total cost (US$), 2007
1,500
6,500
12,750
26,000
Bakker, Raith
Elemente
12
Schwefel, S
Struktur
S8-Ring (Moleküle) mit van-der-Waals Bindungen zwischen ihnen.
Polymorphie:
• α-Schwefel : orthorhombisch (<95.5 ˚C) (mmm)
• β-Schwefel: monoklin (95.5 - 115 ˚C) (2/m)
Mineralogie LV 620.074
Bakker, Raith
13
Elemente
Ausbilding:
Orthorombische Kristalle (oft Kombination von Bipyramiden, Prisma); häufig feinkristalline
Kristallrasen, derbe Aggregate
Eigenschaften
Härte:
Dichte:
Farbe:
Glanz:
Schmelzpunkt:
1.5 - 2
2 - 2.1 g·cm-3
schwefelgelb
Harzglanz
115.21 ˚C
Strich: weiß
Vorkommen:
vulkanische Exhalationen (Reduktion SO2
und Oxidation von H2S); sedimentär durch
bakterielle Sulfatreduktion. Oxidation von
Pyrit unter bestimmten SauerstoffPartialdrucken. Hauptproduktion aus
USA; Sizilien, Japan, Indonesien
(Thermen-Absätze).
Verwendung:
Herstellung von Schwefelsäure;
Vulkanisieren von Kautschuk;
Zellstoffindustrie; Schädlingsbekämpfung;
Pyrotechnik
Solfataren auf Vulcano (Eolische Inseln, Italien)
(Exkursion, 2006)
Mineralogie LV 620.074
Bakker, Raith
1
Sulfide
Klasse 2: Sulfide und Arsenide
Sulfide sind die Salze von H2S; bei Arseniden Austausch von As für S, auch Verbindungen
von Metallen mit Sb, Se und Te zählen zu dieser Mineralklasse.
Allgemeine Merkmale
•
Wichtigste Gruppe der Erzminerale; Quelle für Übergangselemente (Cu, Pb, Zn, Ni, Co,
Hg, Mo, Sb), S und As
•
Metall-Schwefel-Verbindungen können Ionen-, Kovalent- und Metallbindungen sein;
einige Sulfide mit Schichtstruktur (z.B. Molybdänit) zeigen auch van der Waalsche
Bindungen zwischen den Schichten; der teilweise metallische Charakter der Bindungen
resultiert in niedriger bis mittlerer Härte, mittleres bis hohes Reflexionsvermögen;
elektrische Halbleiter
•
Sulfide sind meist opak (undurchsichtig) und zeigen oft metallischen Glanz; seltener
halbmetallischer Diamant- bis Fettglanz (z.B. Sphalerit)
•
Neben der Härte sind die Farbe im Handstück und vor allem die Strichfarbe wichtige
Merkmale für die erste makroskopische Bestimmung
•
Genauere Bestimmung im Auflichtmikroskop bzw. Elektronen-Mikrosonde (EMS)
Klassifikation
Unterteilung in Gruppen mit abnehmendem Metall/Nichtmetall-Verhältnis (nach Strunz).
Bisher ist es nicht möglich, für diese Mineralgruppe eine allgemeine gültige und anwendbare
Klassifikation aufgrund der Kristallstruktur aufzustellen, wie etwa bei Silikaten. Der alten, auf
rein makroskopischen Merkmalen beruhende Einteilung in Kiese, Glanze, Blenden und Fahle
wird in der Deutschen Nahmensgebung zum Teil noch Rechnung getragen.
Mineralogie LV 620.074
Bakker, Raith
2
Sulfide
•
Sulfide mit Metall/Schwefel Verhältnis > 1
In diese Gruppe fallen einige wirtschaftlich sehr bedeutende Minerale der Metalle
Cu, Ag, Ni mit den Nichtmetallen S (und Se). Das Verhältnis Metall/Nichtmetall ist
meist 2; häufig sind mehrere Modifikationen bei gleicher Stöchiometrie, was die
vollkommene Aufklärung der Strukturen bisher erfolgreich behindert hat.
•
Pentlandit
(Ni, Fe)9 S8
kub.
Chalkosin (Kupferglanz)
Cu2S
hex/orthorhomb
Akanthit (Silberglanz)
Ag2S
kub/mkl
Sulfide (und Arsenide) mit Metall/Schwefel Verhältnis = 1
Diese Gruppe enthält eine Reihe wirtschaftlich äußerst wichtiger Sulfide. Man
unterscheidet nach der Koordination der Kationen:
1. in tetraedrischer Koordination, Ableitung vom Diamant-Struktur: Zinkblende
Gitter und Wurtzit-Gitter
2. in oktaedrischer Koordination, Ableitungen durch Verzerrung der NaClStruktur (Bleiglanz-Reihe)
3. in Koordination trigonaler Prismen: Ableitung vom NiAs-Typus
4. Koordinationen zu Schichtgittern: Covellin
Die Kristallstrukturen sind meist relativ einfach und aus der kubisch- oder
hexagonal-dichtesten Kugelpackung abzuleiten. Der Bindungscharakter ist
einerseits kovalent (Blenden) oder betont metallisch (Glanze).
Sphalerit (Zinkblende)
ZnS
kub.
(siehe Einf. Min. Pet.!)
Chalcopyrit (Kupferkies)
CuFeS2
tetr.
(siehe Einf. Min. Pet.!)
Galenit (Bleiglanz)
PbS
kub.
(siehe Einf. Min. Pet.!)
Cinnabarit (Zinnober)
HgS
trig.
Nickelin (Rotnickelkies)
NiAs
hex.
Pyrrhotin (Magnetkies)
FeS – Fe1-xS hex.
Covellin (Kupferindig)
CuS
Mineralogie LV 620.074
hex.
Bakker, Raith
3
Sulfide
•
Sulfide (und Arsenide) mit Metall/Schwefel Verhältnis < 1
Eine große Gruppe von Sulfiden, zu der einige sehr weit verbreitete Minerale
gehören (z.B. Pyrit, Markasit). Die Kristallstrukturen sind meist einfach: Abgeleitet
von NaCl-Struktur (z.B. Pyrit); oder Schichtgittern (z.B. Molybdänit)
•
Stibnit (Antimonit)
Sb2S3
orh.
Pyrit (Schwefelkies)
FeS2
kub.
Markasit
FeS2
orthorhomb.
Arsenopyrit (Arsenkies)
FeAsS
orh.
Molybdänit (Molybdänglanz)
MoS2
hex.
(siehe Einf. Min. Pet.!)
Komplexe Sulfide (Sulfosalze)
Fahlerzreihe: Tetraedrit - Tennantit
AxBySn (A=Metalle, B=Halbmetalle)
Sulfide mit Metall/Schwefel Verhältnis > 1
Pentlandit, (Ni, Fe)9 S8
Struktur:
Isometrisch, kubisch dichteste Kugelpackung der S-Atome: Elementarzelle enthalt 32
Schwefel atome, 32 Metallatome in tetraedrischen und 4 in oktaedrische Lücken (abgeleitet
von Spinell-Struktur). Ni und Fe sind statistisch verteilt.
Spinel structure
cubic close-packed array of oxygen atoms with the A
and B cations occupying one eight of the tetrahedral
sites and one half of the octahedral sites. Therefore,
there are 32 oxygen atoms in the spinel unit cell.
Chemismus:
Fe/Ni Verhältnis ≈ 1 (15-45% Ni, 25-42% Fe), geringe Menge an Co. Pentlandit ist unterhalb
610 ˚C stabil, darüber weitgehende Mischbarkeit im System Fe-Ni-S. Die reinen Entglieder
Fe9S8 und Ni9S8 sind nicht stabil.
Ausbildung:
meist derb, körnige Aggregate; Kristalle selten: Oktaeder {111}, Kombination von Würfel
{100} und Oktaeder {111}
Mineralogie LV 620.074
Bakker, Raith
Sulfide
4
Eigenschaften:
• Spaltbarkeit: deutlich nach Oktaeder; spröder Bruch
• Härte:
3.5 - 4
• Dichte:
4.6 - 5 g/cm3
• Farbe:
bronzegelb
Strich: hell bronze-braun
• Glanz:
Metallglanz
• im Unterschied zu Pyrrhotin nicht magnetisch
Vorkommen:
Mineral
der
"liquidmagmatischen"
Vererzung:
Entmischung einer Sulfidschmelze
mit
Kupferkies
(CuFeS2),
Magnetkies (FeS) und PGM
(platinum-group
minerals).
Wichtigste Ni-Co Lagerstätte:
Sudbury Complex (Canada)
Schüsselformig Intrusionen (40 x
60 km) von mafischen gabbroiden
Gesteinen mit einer "Sublayer"
(sulfidreicher Norit mit massiven
Sulfiden), Augit-Norit, QuarzGabbro
und
Granophyr
(granitisch). Sulfidvererzungen nur
am
Kontakt
und
"Offset"
Vererzungen. Die innere Gesteine
haben genetisch mit der Intrusion
nichts zu tun.
Mineralogie LV 620.074
Bakker, Raith
5
Sulfide
Bedeutung:
Wichtigstes Ni-Erz, auch wichtig für Co und Pd-Gewinnung. Zu 80% Verwendung als
Legiermetall mit anderen Metallen (Stahlveredler). Ni-Cr Stähle, Galvanotechnik,
Münzmetall.
Chalkosin (Kupferglanz), Cu2S
Struktur:
Polymorphie: T<103 ˚C orthorhombisch, T>103 ˚C hexagonal
Eigenschaften:
• Spaltbarkeit:
• Härte:
• Dichte:
• Farbe:
• Strich:
• Glanz:
undeutlich; muscheliger Bruch
2.5 - 3
5.5 - 5.8 g/cm3
bleigrau auf frischen Bruchflächen; schwarz anlaufend
grauschwarz
Metallglanz
Ausbildung:
derbe Massen, selten Kristalle
Vorkommen:
Mit Covellin (CuS) zusammen in den Zementationszonen primär armer Kupferlagerstätten
(hydrothermal), die oft nur aufgrund der sekundären Anreicherung dieser Mineralien
wirtschaftlich sind.
Bedeutung:
wichtiges Cu-Mineral
Mineralogie LV 620.074
Bakker, Raith
6
Sulfide
Akanthit (Silberglanz), Ag2S
Struktur:
Polymorphie: T<179 ˚C monoklin, T> 179 ˚C isometrisch (= "Argentit") kubisch
flächenzentriert
Eigenschaften:
• Spaltbarkeit:
• Härte:
• Dichte:
• Farbe:
• Glanz:
fehlt; duktil, schneidbar, prägbar, pulverig zerfallend
2 - 2.5
7.3 g/cm3
schwarz anlaufend
Strich: dunklegrau
bleigrauer Metallglanz auf frischen Schnittflächen
Ausbildung:
Meist derb oder pulvrig, selten spießige Kristalle bei monoklinene Akanthit, kubische
Kristalle bei isometrischem Akanthit.
Vorkommen:
Wichtiger Silberträger in Galenit (PbS); in primärer Verwachsungen und Entmischungen.
Bedeutung:
wichtiges Silbermineral, Aufbereitung mit Hilfe der Zinkentsilberung: in die Bleischmelze
wird Zn gegeben → Bildung von Zn-Ag-Legierungen, die auf der Bleischmelze schwimmen.
Trennung von Zn und Ag durch Destillation. Bei niedrig gradigen Erzen Graden
Cyanidlaugerei und Gewinnung des Ag durch Elektrolyse.
Sulfide (und Arsenide) mit Metall/Schwefel Verhältnis = 1
1. Kationen in tetraedrischer Koordination
Sphalerit, ZnS
Struktur:
Isometrisch, ableitbar von Diamant-Struktur
Mineralogie LV 620.074
Bakker, Raith
7
Sulfide
Chemismus:
kann Fe und seltene Elemente (Mn, Cd, Ga, In, Tl, Hg, Ge) im Gitter einbauen (wichtiger
Lieferant dieser Sondermetalle!)
Eigenschaften:
• Härte:
• Dichte:
• Farbe
• Strich:
• Glanz
• Spaltbarkeit:
3.5 - 4
3.9 - 4.1 g/cm3
gelb, honigfarben, braun bis schwarz
gelblich bis dunkelbraun
starker Diamantglanz
volkommen in 4 Richtungen
Ausbildung:
Vorkommen:
mit Galenit in Pb-Zn Lagerstätten; sedimentär-exhalativ; hydrothermale Gänge; Verdrängung
von Karbonatgesteinen (z.B. Bleiberg, Kärnten)
Bedeutung:
wichtigstes Zn-Mineral; andere Elemente als Nebenprodukt. Verzinken, Legierungen
(Messing), Galvanik, Farben. Technische Problematik: toxisches Schwermetall; v.a. in
Assoziation mit Cd Tl.
Chalcopyrit, CuFeS2
Struktur:
Tetragonal, Ableitbar von ZnS: Zn[4]S[4] → Cu[4]Fe[4]S2[4]
Eigenschaften:
• Spaltbarkeit
• Härte:
• Dichte:
• Farbe:
•
•
Strich:
Glanz:
Mineralogie LV 620.074
fehlt
3.5 - 4
4.1 - 4.3 g/cm3
messingfarbig, grünlich gelb bis
dunkelgelb
schwarz bis grünschwarz
Metallglanz
Bakker, Raith
Sulfide
8
Ausbildung:
derbe bis feinkörnige Massen, selten Kristalle: tetragonales Bisphenoid, Skalenoeder.
Zwillungsverwachsungen.
Vorkommen:
verbreitetes Cu-Mineral; sedimentär-exhalativ (Kupferschiefer); liquid-magmatisch; bei
Verwitterung entstehen die Kupferkarbonate Malachit (grün) und Azurit (blau); disseminiert
in porphyrischen Kupferlagerstätten ("porphyry copper"):
Chalkopyrit liegt in dioritisch-monzonitischen subvulkanischen Gesteine vor. Porhyry
coppers bilden den Übergang vom plutonischen zum subvulkanischen Milieu. Mineralisation
erfolgt mit Hilfe hydrothermaler Lösungen, die für die Exploration hilfreiche, sehr typische
Alterationshöfe erzeugten. Meist 0.4 bis 1% Cu neben Mo, Au und Nb. Bis zu 1000 Millionen
t. Erz in einer Lagerstätte (niederiggradig, sehr hohe Reserven), z.B. Chuquicamata, Chili.
Bedeutung:
das wirtschaftlich wichtigste Cu-Erzmineral
Mineralogie LV 620.074
Bakker, Raith
9
Sulfide
2. Kationen in oktaedrischer Koordination
Galenit, PbS
Struktur:
Isometrisch, isotyp mit Steinsalz (NaCl-Struktur); Pb[6]S[6]
Eigenschaften:
• Spaltbarkeit:
• Härte:
• Dichte:
• Farbe
• Glanz:
vollkommen in 3 Richtungen (nach dem Würfel)
2.5 - 3
7.4 - 7.6 g/cm3
bleigrau
Strich: grauschwarz
starker Metallglanz
Ausbildung:
Würfel!, Oktaeder und Kombinationen
Vorkommen:
mit Sphalerit in Pb-Zn Lagerstätten; sedimentär-exhalativ; hydrothermale Gänge (in die Nähe
eines Granites); Verdrängung von Karbonatgesteinen
Bedeutung:
wichtigstes Pb-Mineral; wichtigste Silberträger (oft feine Einschlüsse von Fahlerz und
Akanthit), nur 0.1% in Gitter. Die Silberproduktion aus Pb-Erz kann nicht beliebig
ausgeweitet werden, Pb müsste dann auf Halde produziert werden, was sich nachteilig auf den
Bleipreis auswirken würde. Metallisches Blei für Akkus, Bleiplatten, Legierungsmetall;
Strahlenschutz; früher als Antiklopfmittel in Benzin; toxisches Schwermetall
Mineralogie LV 620.074
Bakker, Raith
10
Sulfide
Cinnabarit (Zinnober), HgS
Struktur:
Trigonal; deformierte NaCl-Struktur; pseudooktaedrische Koordination
Eigenschaften:
• Spaltbarkeit:
• Härte:
• Dichte:
• Farbe:
• Glanz:
ziemlich vollkommen; muschelig spröder Bruch
2 - 2.5
8.1 g/cm3
rot (!)
Strich: rotbraun
Diamantglanz
Ausbildung:
meist derb körnig, dichte erdige Aggregate. Selten tiefrote rhomdoedrische bis tafelige
Kristalle
Vorkommen:
hydrothermale Imprägnationen (Zusammenhang mit andesitisch-dacitischen Magmatiten),
sedimentär-exhalativ (Teil der Antimon-Wolfram-Quecksilber Formation).
Bedeutung:
wichtiges Hg-Erzmineral, Amalgame (Zahntechnik, Goldgewinnung); Umweltproblematik
von metallischen Hg.
3. Kationen in Koordination trigonaler Prismen
Nickelin (Rotnickelkies), NiAs
Struktur:
hexagonal dichteste
Kugelpackung, Ni[6]As[6]
Mineralogie LV 620.074
Bakker, Raith
11
Sulfide
Eigenschaften:
• Härte
• Dichte
• Farbe
• Glanz
5 - 5.5
7.8 g/cm3
hell kupferrot, dunkler anlaufend
starker Metallglanz
Strich: bräunlichschwarz
Ausbildung:
gewöhnlich in derben, körnigen Massen, nur sehr selten Kristalle
Vorkommen:
In hydrothermalen Ganglagerstätten (z.B. Ontario, Thüringer Wald)
Pyrrhotin (Magnetkies), FeS - Fe1-xS
Struktur:
"NiAs-Struktur"; hexagonal; Leerstellen im Gitter (nicht ganz stöchiometrisch).
Eigenschaften:
• Spaltbarkeit: deutlich nach Basisflächen; muschelig spröder Bruch
• Härte
4
• Dichte
4.6 - 4.7 g/cm3
• Farbe
hell bronzefarben (!) mattbraun anlaufend Strich: grauschwarz
• Glanz
Metallglanz
• meist magnetisch!
Ausbildung:
meistens derb und eingesprengt, körnig bis blättrig, selten Kristalle.
Vorkommen:
vorherrschender Bestandteil liquid-magmatischer Sulfidlagerstätten; weiteste Verbreitung
akzessorisch in sauren und basischen magmatischen Gesteinen; Troilit (FeS) koexistiert mit
elementären Fe nur in Eisenmeteoriten
Bedeutung:
Pentlandit-führender Pyrrhotin ist ein Ni-Erz (kein Eisenerzmineral!)
4. Kationen Koordinationen zu Schichtgittern
Covellin (Kupferindig), CuS
Struktur:
hexagonal, Schichtgitter: Schichten von CuS3-Dreiecken zwischen einer Doppelschicht von
CuS4-Tetraedern, kovalente S-S Bindung zwischen den Schichten.
Mineralogie LV 620.074
Bakker, Raith
12
Sulfide
Eigenschaften:
• Spaltbarkeit:
• Bruch:
• Härte:
• Dichte:
• Farbe
•
•
Strich:
Glanz:
vollkommen nach (0001)
muschelig spröde
1.5 - 2 (weich!)
4.6 - 4.8 g/cm3
blauschwarz bis indigoblau (!),
dunkler anlaufend
bläulich schwarz
halbmetallischer Glanz
Ausbildung:
meist derb, feinkörnig oder spätig; selten tafelige
Kristalle
Vorkommen:
typisches Mineral der Zementationszone über
sulfidischen Kupferlagerstätten (Grenze Zementations/
Oxidationszone): sekundäres Erzmineral
Sulfide (und Arsenide) mit Metall/Schwefel Verhältnis < 1
Stibnit (Antimonit), Sb2S3
Struktur:
Orthorhombisch, Sb2S3-Moleküle in Doppelketten angeordnet, die sich parallel der c-Achse
erstrecken. Zwischen den Ketten nur schwache Bindungen (dadurch gute Spaltbarkeit!)
Eigenschaften:
• Spaltbarkeit:
• Härte:
• Dichte:
• Farbe
• Strich:
• Glanz:
Mineralogie LV 620.074
vollkommen nach {010}
2 - 2.5
4.5 - 4.6 g/cm3
bleigrau, metallschwärzlich bis bläulich anlaufend
dunkelbleigrau
starker Metallglanz
Bakker, Raith
13
Sulfide
Ausbildung:
spieß- und nadelförmig, bisweilen büschelig oder wirr-strahlig
aggregiert.
Vorkommen:
Schichtgebunden als Teil der Antimon-Wolfram-QuecksilberFormation, z.B. Schlaining im Burgenland; Rabant, Kärnten
(Schwarzschiefer). Verwittert zu gelben Oxiden: Sb2O4 (Cervantit) und
Sb2O3 (Valentinit).
Bedeutung:
wichtigste Sb-Erzmineral. Legiermetall (für Pb, Cu, Sn).
Halbleiterindustrie.
Pyrit, FeS2
Struktur:
Isometrisch, ableitbar von NaCl-Struktur: Na[6]Cl[6] → Fe[6]S2[6] (S2-Hanteln)
Eigenschaften:
• Spaltbarkeit
• Härte:
• Dichte:
• Farbe
• Glanz:
undeutlich
6-6.5 (hart!)
5 g/cm3
gold
Strich: grünschwarz
licht messingfarbener Metallglanz
Chemismus:
kann bis 14% Co und 17% Ni im Gitter einbauen, daneben geringe Gehalte an As (für S).
Gehalte an Au, Ag, Zn, Cu gehen immer auf mechanische Beimengungen zurück.
Mineralogie LV 620.074
Bakker, Raith
Sulfide
14
Ausbildung:
Kristalle: Würfel, Pentagondodekaeder, Oktaeder.
Vorkommen:
häufigstes Sulfid in vielen Gesteinen und Lagerstätten. Bei Verwitterung entstehen
Eisenhydroxide ("Limonit")
Bedeutung:
Gewinnung von Schwefelsäure: unter Sauerstoffeinfluß verbrennt Pyrit bei 600 ˚C zu Hämatit
(Fe2O3) und SO2, das mit H2O zu Schwefelsäure reagiert (H2SO4). Anwendung von
Schwefelsäure: Düngemittel (über Salpetersäure), Katalysator, Trockenmittel, Autobatterien,
Ätzen, Trinkwasseraufbereitung, Aufschließen andere Erze, etc. Goldträger in AuLagerstätten.
Markasit, FeS2
Struktur:
Orthorhombisch, polymorph mit Pyrit, kubisch innenzentrierte Anordnung von Fe
Mineralogie LV 620.074
Bakker, Raith
15
Sulfide
Eigenschaften:
• Spaltbarkeit:
• Härte:
• Dichte:
• Farbe
• Strich:
• Glanz
unvollkommen
6 - 6.5 (hart!)
4.8 - 4.9 g/cm3
im Vergleich zu Pyrit mehr grünlichgelb, grünlich anlaufend gold
grünschwarz
Metallglanz
Ausbildung:
Einzelkristalle meist tafelig; häufig verzwillingt hahnenkammförmige Gruppen; strahlige
Aggregate.
Vorkommen:
nicht so häufig wie Pyrit; eher bei niedrigen Temperaturen stabil, hydrothermal, besonders
sedimentär (Konkretionen in Sedimenten mit hohem organischen Anteil).
Arsenopyrit (Arsenkies), FeSAs
Struktur:
Monoklin, ableitbar von Markasit: anstatt S2 hier AsS und dadurch Verdoppelung der
Abstände a und b im Gitter (Erniedrigung der Symmetrie).
Eigenschaften:
• Härte:
• Dichte:
• Farbe
• Glanz
Mineralogie LV 620.074
5.5 - 6
5.9 - 6.1 g/cm3
zinnweiß, dunkel oder bunt anlaufend
Metallglanz
Strich: schwarz
Bakker, Raith
16
Sulfide
Ausbildung:
primatische Kristalle, häufig säulige Aggregate, massig und körnig. Oft 6-seitige Drillinge
Vorkommen:
Weitverbreitet in hochtemperierten Gold-Quarz Gängen (hydrothermal). Goldträger (wie
Pyrit).
Bedeutung:
Gewinnung von Arsen; historisch: Produktion von Arsenik
Mineralogie LV 620.074
Bakker, Raith
17
Sulfide
Molybdänit (Molybdänglanz), MoS2
Struktur:
hexagonal, Schichtgitter. Zwischen 2 S-Schichten 1 Metallschicht, Mo[6]S2[3]. Innerhalb der
Schichten kovalente Bindungen, zwischen den Schichten ganz schwache Van-der-Waals
Bindungen (ähnlich Graphit!).
Eigenschaften:
• Spaltbarkeit:
• Bruch:
• Härte:
• Dichte:
• Farbe:
• Glanz:
sehr vollkommen nach (0001)
biegsam, unelastisch
1 - 1.5, sehr weich!
4.7 - 4.8 g/cm3
stahlgrau
Strich: blaugrau
Metallglanz
Ausbildung:
häufig massig und verfältelt, manchmal sechseitige Blättchen
Vorkommen:
hoch temperierte hydrothermale Lagerstätten und Pegmatite. In Sn-W Mineralisationen
(Erzgebirge). Am wichtigsten sind heute die Porphyry Molybdän Lagerstätten (Climax,
Colorado).
Bedeutung:
wichtigstes Mo-Erzmineral, Stahlveredler, Schmiermittel
Mineralogie LV 620.074
Bakker, Raith
Sulfide
18
Komplexe Sulfide (Sulfosalze)
Strukturell sehr komplex zusammengesetzte Sulfide, auf deren Systematik hier nicht näher
eingegangen werden soll. Sie unterscheiden sich von den bisher besprochenen Sulfiden und
Arseniden dadurch, daß As und Sb innerhalb ihrer jeweiligen Kristallstruktur mehr oder
weniger die Rolle eines Metall einnehmen.
Fahlerze
Chemismus:
Tetraedrit (Cu12Sb4S13) - Tennantit (Cu12As4S13), As und Sb sind vollständig austauschbar
und können auch durch Bi ersetzt werden; bis 18% Ag-Gehalt (Freibergit); bis 17% HgGehalt (Schwazit); Cu kann durch Fe, Zn, Ag oder Hg ersetzt werden;
Struktur:
Isometrisch, abgeleitet von Sphalerit-Struktur
Ausbildung:
kubische Kristalle, meist Tetraeder; Durchkreuzungszwillinge; derb und körnig.
Vorkommen:
hydrothermale Gänge. Häufiges Begleitmineral in Pb-Zn Lagerstätten, dort wichtiger
Silberträger im Galenit.
Mineralogie LV 620.074
Bakker, Raith